Результат интеллектуальной деятельности: СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ МЯГКИХ ТКАНЕЙ И СЛИЗИСТЫХ ОБОЛОЧЕК
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно к средствам, обладающим антимикробным, сорбционным и ранозаживляющим действием на местные гнойно-воспалительные процессы мягких тканей и слизистых оболочек, используемым в хирургии, дерматологии, акушерстве и гинекологии, оториноларингологии.
Проблема лечения гнойных ран до сих пор является актуальной в современной медицинской практике. По данным некоторых авторов от всех хирургических заболеваний гнойные осложнения составляют 30-35%, а летальность от них достигает 25%.
Без сомнения, для достижения положительного результата современные препараты должны обладать разнонаправленным действием и сочетать в себе такие свойства, как широкая антимикробная активность, высокая дегидратирующая способность, стимуляция регенерации тканей.
На сегодняшний день для воздействия на многообразие микроорганизмов, которые вызывают гнойно-воспалительный процесс в мягких тканях, используются препараты местного применения с антибиотиками. Однако следует отметить, что массовое, а в некоторых случаях бесконтрольное их применение приводит к преобладанию в ране малочувствительной или нечувствительной к ним микрофлоры. В связи с этим в хирургической практике при лечении местных гнойно-воспалительных процессов все больше возрастает интерес к антисептикам и химиопрепаратам.
С целью абсорбции гнойного экссудата и дренированию раневой поверхности в лекарственных препаратах (мази, гели и др.) для наружного применения в настоящее время широко используют полиэтиленоксиды (ПЭО), углеродные сорбенты, производные целлюлозы и др.
Прототипом нашего изобретения рассматривается лекарственный препарат, в состав которого входит (в массовых долях) антибиотик эритромицина эстолат (1,0), антисептики - экстракт ромашки (2,0) и раствор метиленового синего (0,004), а в качестве основы - сплав ПЭО-400 (79,2) и ПЭО-1500 (19,8), вода очищенная (2,0) («Экспериментальное обоснование применения новых многокомпонентных мазей эритромицина эстолата и виброакустического воздействия в лечении гнойных ран». Бирюков В.И. Диссертация канд. мед. н-к, 14.00.27-хирургия, Курск, 2006 г.)
Однако, несмотря на то что антибиотик эритромицин до сих пор используется в клинической практике, применение его ограничено, так как к нему быстро развивается устойчивость микроорганизмов, он имеет относительно узкий спектр антимикробной активности, нестабильность всасывания, короткую продолжительность действия. В свою очередь антисептики экстракт ромашки и метиленовый синий обладают недостаточно широким спектром антимикробного действия.
Техническим результатом изобретения является создание эффективного лекарственного средства, обладающего противомикробной, сорбционной и ранозаживляющей активностью.
Технический результат достигается тем, что средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек содержит в качестве основы сплав полиэтиленоксидов с молекулярной массой 400 и 1500, отличается тем, что в качестве лечебных компонентов содержит комбинацию антисептика бензалкония хлорида и метронидазол в следующих массовых долях:
|
Характеристика объектов:
Бензалкония хлорид (Bensalkonium chlorid). Оказывает микробостатическое и микробоцидное действие на грамположительные, в больших дозах - на грамотрицательные бактерии и грибы рода Candida. Он известен и как консервант, который используют для предотвращения микробной контаминации при длительном хранении лекарственных форм, в частности мазей, гелей и др. Кроме антисептического, обладает дезодорирующим действием. Помимо этого, бензалкония хлорид является катионным поверхностно-активным веществом, который способен влиять на степень измельчения лекарственных веществ, тем самым повышая их биодоступность и эффективность.
Метронидазол. Антибактериальный химиотерапевтический препарат, производное 5-нитроимидазола, обладает высокой активностью в отношении широкого спектра бактерий и простейших. Доказано, что анаэробы сохранили к нему 100% чувствительность. Механизм действия заключается в биохимическом восстановлении 5-нитрогруппы метронидазола внутриклеточными транспортными протеинами анаэробных микроорганизмов и простейших. Восстановленная 5-нитрогруппа метронидазола взаимодействует с ДНК клетки микроорганизмов, ингибируя синтез их нуклеиновых кислот, что ведет к гибели бактерий.
Полиэтиленоксиды обладают дегидратирующим действием, причем в гнойной ране оно распространяется не только на ее ткани, но и на содержащиеся в ней микробные клетки. ПЭО-основа обезвоживает микробную клетку, резко снижает ее биологическую активность и ослабляет сопротивляемость к различным лекарственным средствам, в результате чего существенно возрастает антимикробная активность многих антибиотиков, сульфаниламидов и антисептиков. Благодаря способности ПЭО абсорбировать экссудат, а вместе с ним и микробные токсины продукты распада тканей, биологически активные вещества - лизосомальные ферменты и другие медиаторы воспалительного процесса, «обрывая» тем самым его прогрессирующее течение, они обуславливают потенцирующее влияние на лечебный эффект лекарственного препарата в целом.
СПОСОБ ОСУЩЕСТВЛЯЕТСЯ СЛЕДУЮЩИМ ОБРАЗОМ.
Изготовление лекарственного средства включает три стадии:
Первая стадия: рассчитанное количество полиэтиленоксида М.м. 1500 (ПЭО М.м. 1500) расплавляют на водяной бане, после чего в него добавляют рассчитанное количество полиэтиленоксида М.м. 400 (ПЭО М.м. 400), перемешивают до получения однородной массы, полученный сплав охлаждают.
Вторая стадия: рассчитанное количество навески метронидазола измельчают в присутствии рассчитанного количества бензалкония хлорида. Третья стадия: к измельченной смеси метронидазола и бензалкония хлорида по частям добавляют сплав ПЭО М.м. 1500 и ПЭО М.м. 400 и гомогенизируют до получения однородной массы.
ПРИМЕР 1 (ПО СПОСОБУ ПОЛУЧЕНИЯ)
20,0 массовых долей ПЭО М.м. 1500 плавят на водяной бане, после чего добавляют по частям 80,0 массовых долей ПЭО М.м. 400 и перемешивают до получения однородной массы, полученный сплав оставляют остывать. Затем измельчают навеску 1,0 массовой доли метронидазола в присутствии 0,02 массовых долей бензалкония хлорида. После чего к полученной смеси метронидазола и бензалкония хлорида по частям добавляют сплав полиэтиленоксидов (ПЭО М.м. 400 и ПЭО М.м. 1500) и гомогенизируют до получения однородной массы.
ПРИМЕР 2 (ПО СПОСОБУ ПОЛУЧЕНИЯ)
30,0 массовых долей ПЭО М.м. 1500 плавят на водяной бане, после чего добавляют по частям 90,0 массовых долей ПЭО М.м. 400 и перемешивают до получения однородной массы, полученный сплав оставляют остывать. Затем измельчают навеску 2,0 массовой доли метронидазола в присутствии 0,04 массовых долей бензалкония хлорида. После чего к полученной смеси метронидазола и бензалкония хлорида по частям добавляют сплав полиэтиленоксидов (ПЭО М.м. 400 и ПЭО М.м. 1500) и гомогенизируют до получения однородной массы.
ОПРЕДЕЛЕНИЕ МИКРОБИОЛОГИЧЕСКОЙ АКТИВНОСТИ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ МЯГКИХ ТКАНЕЙ И СЛИЗИСТЫХ ОБОЛОЧЕК
Антимикробное действие средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек изучалось методом диффузии в агар (ГФ XII, 2007) в отношении тест-штаммов St. aureus АТСС 6538-Р, Вас. cereus АТСС 10702, E.coli ATCC 25922, Proteus vulgaris и Pseudomonas aeruginosa АТСС 9027, Candida albicans АТСС 885-653. Результаты определения представлены в табл.1.
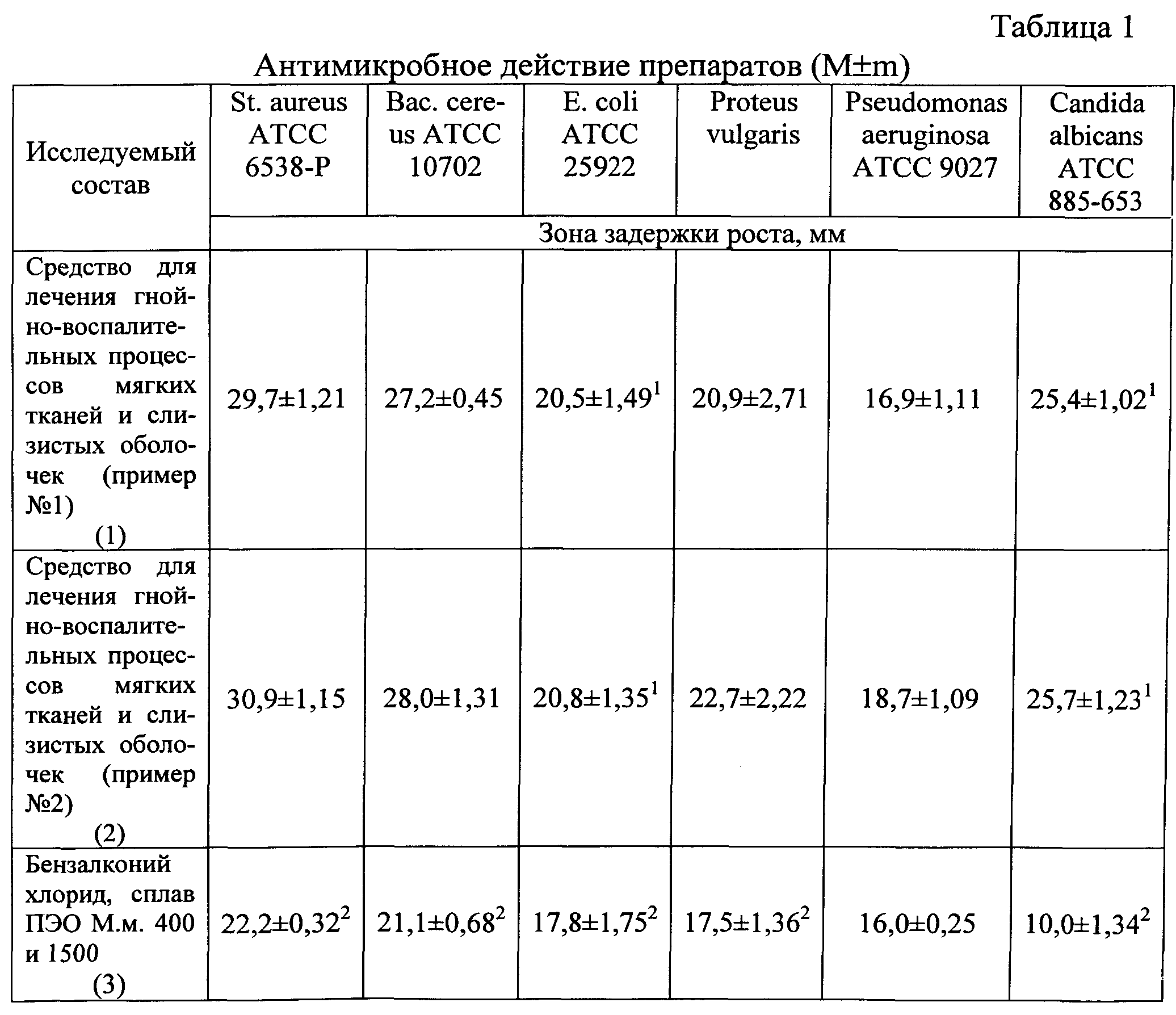

Из данных, представленных в табл.1, следует, что средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1 и №2) обладает достаточно сильным биоцидным действием в отношении всех исследуемых тест-штаммов. Зона ингибирования роста при изучении спектра антимикробной активности наиболее выражена в отношении тест-штаммов St. aureus ATCC 653 8-Р, Вас. cereus ATCC 10702, Candida albicans ATCC 885-653, E. coli ATCC 25922, Proteus vulgaris, что не уступает, а по ряду показателей даже превосходит зоны задержки роста при исследовании прототипа (эритромицина эстолат, экстракт ромашки, раствор метиленового синего сплав ПЭО М.м. 400 и 1500).
ПРИМЕР 3 (ЭКСПЕРИМЕНТАЛЬНОЕ ПРИМЕНЕНИЕ)
Изучение ранозаживляющей активности средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1 и №2) проводили в эксперименте на крысах-самцах породы «Вистар» массой 180-200 г, у которых моделировалась гнойная рана по методике П.И. Толстых (1976). Экспериментальные животные были разделены на три серии по 36 животных в каждой:
В 1-й серии (модель) лечение не проводилось.
Во 2-й серии (контроль) использовали для лечения мазь эритромицина эстолат, экстракт ромашки, раствор метиленового синего, сплав ПЭО М.м. 400 и 1500 (прототип).
В 3-й серии проводили лечение средством для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №1).
В 4-й серии проводили лечение средством для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример №2).
Течение раневого процесса у экспериментальных животных оценивали планиметрическим (метод Л.И. Поповой), микробиологическим, гистологическим методами. Результаты исследований обработаны статистически (рассчитаны средние величины, критерий достоверности).
Животные выводились из эксперимента путем передозировки эфирного наркоза на 1, 3, 5, 8, 10, 15 сутки.
После моделирования на 1-е сутки во всех сериях отмечалась гиперемия краев раны, отек окружающих тканей, дно ран было покрыто налетом фибрина с участками некроза, наблюдалось гнойное отделяемое.
В процессе лечения происходило очищение поверхности раны от гнойно-некротических масс, купировался отек, появлялись грануляции и краевая эпителизация.
Данные планиметрического исследования свидетельствуют о более быстром уменьшении площади ран в 3-й и 4-й серии по сравнению с моделью и контролем (исходная площадь ран была 250 мм2), с 3-х суток площади ран имели статистически значимые различия. Процесс заживления протекал быстрее в 3-й и 4-й серии по сравнению с контрольной и моделью. Результаты планиметрического исследования представлены в табл.2.
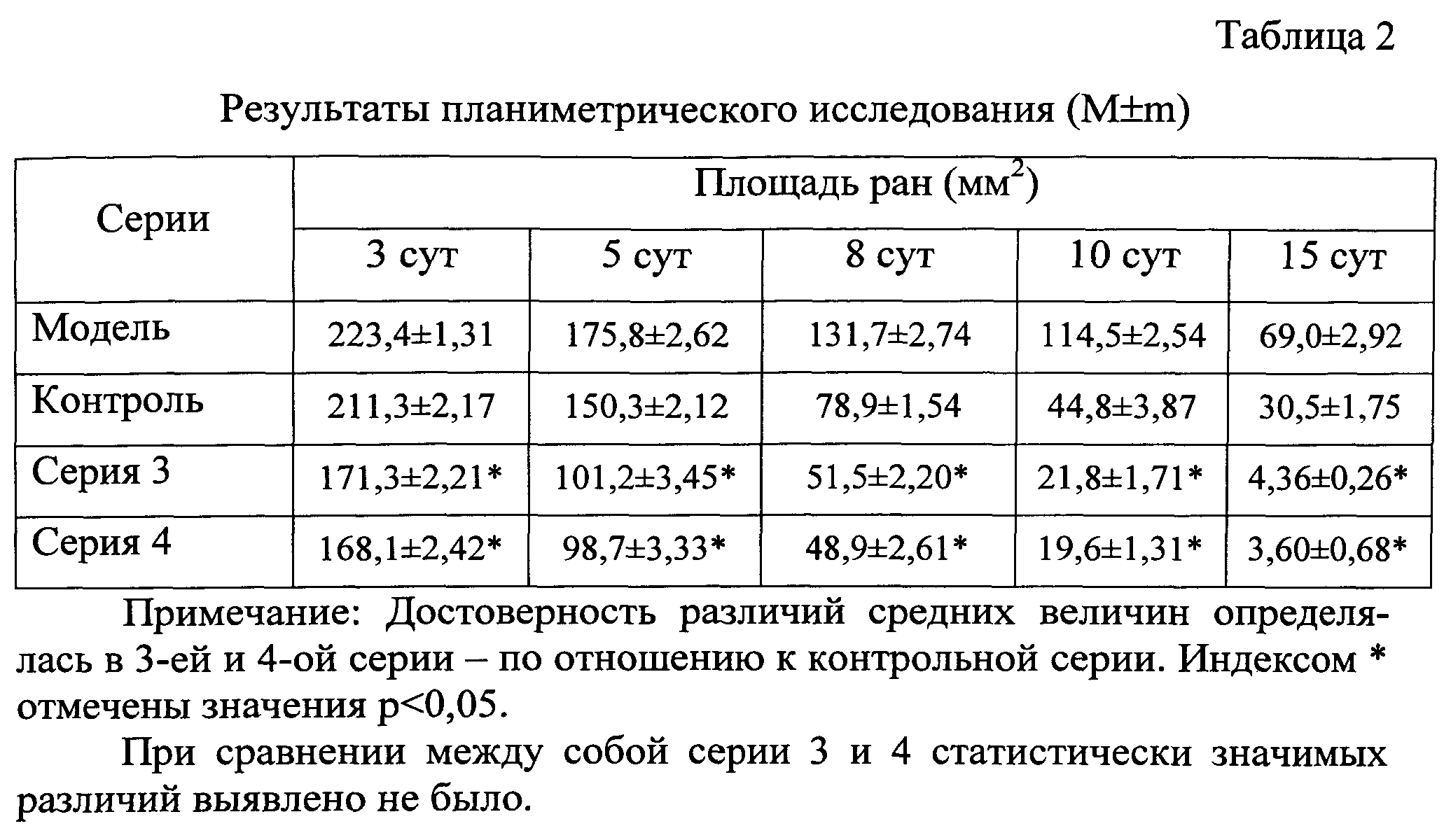
Таким образом, полученные данные планиметрического исследования подтверждают высокую эффективность средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (примеры 1 и 2) в лечении гнойных ран. К 15-м суткам площадь ран в 3-й и 4-й серии сократилась на 98,3%, что было выше скорости заживления ран в среднем в 2,8 раза, по сравнению с контрольной серией.
Данные микробиологического исследования показали, что в 3-й и 4-й серии микробная обсемененность ран достоверно меньше, чем в контрольной серии, начиная с 5-х суток и на протяжении всего срока наблюдения. В 3-й и 4-й серии на 5-е сутки микробная обсемененность ран в 2,2 раза меньше, чем в контрольной серии (64,1×2,82×105, 57,3±3,17×105 и 1,4±0,21×107 КОЕ/г соответственно), на 10-е сутки - в 4,1 раза меньше, чем в контрольной серии (18,9±1,54×103, 16,1±2,21×103 и 7,6±0,93×104 КОЕ/г соответственно). Таким образом установлено, что средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (примеры 1 и 2) в 2,2-4,1 раза сокращает микробную обсемененность ран по сравнению с прототипом - мазью, содержащей эритромицина эстолат, экстракт ромашки, раствор метиленового синего, сплав ПЭО М.м. 400 и 1500.
Для полной оценки состояния раны в динамике был использован гистологический метод исследования раневых биоптатов, дающий возможность объективно оценить динамику течения раневого процесса.
На 1-е сутки после моделирования микроскопическая картина во всех сериях выглядит следующим образом. Поверхность раны покрыта толстым фибринозно-лейкоцитарный слоем. Лейкоциты - в состоянии распада. Соединительная ткань под лейкоцитарным струпом отечна, инфильтрирована единичными макрофагами и сегментоядерными лейкоцитами. Соединительнотканная клетчатка разрыхлена, фибробласты имеют базофильную цитоплазму и набухшие разрыхленные ядра. Встречаются очаги геморрагии диапедезного характера. Эпителий дистрофичен, край его уплощен.
На 3-и сутки в группе животных в контрольной серии на поверхности раны - широкий фибринозно-лейкоцитарный струп, под которым наблюдается активный рост грануляционной ткани. Грануляционная ткань обильно инфильтрирована лейкоцитами. Фибробласты набухшие с базофильной цитоплазмой располагаются тяжами. Межклеточное вещество отечно, разрыхлено. На 10-е сутки лейкоцитарно-некротический струп полностью отделен от поверхности раны. В поверхностном слое раны определяются фибробласты и многочисленные макрофаги. Инфильтрация выражена слабее, чем на предыдущие сутки наблюдения. По поверхности грануляций продолжается рост эпителия. На 15-е сутки рана на значительной поверхности эпителизирована. Под эпителием располагается соединительная ткань слоистого строения, содержащая коллагеновые волокна и инфильтрированная лейкоцитами и макрофагами. Отечное межклеточное вещество.
На 3-и сутки при использовании средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (примеры 1 и 2) отмечается слабая инфильтрация свежих грануляций лейкоцитами. На 10-е сутки происходит восстановление кожи (наползание эпителиального вала с краев раны). На 15-е сутки рана эпителизирована, наблюдалось практически полное восстановление кожи за исключением ее производных.
Таким образом, в 3-й и 4-й серии отмечается более быстрое очищение поверхности раны от лейкоцитарно-некротических масс, активный рост грануляций. К 10-м суткам значительная часть раны или вся ее поверхность эпителизированы.
Применение средства для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек (пример 1 и 2) в I и II фазах раневого процесса повышает скорость заживления ран в 2,8 раза, в 2,2 -4,1 раза сокращает микробную обсемененность ран, ускоряет формирование и созревание грануляционной ткани, способствует ранней и быстрой эпителизации раневой поверхности по сравнению с лечением мазью, содержащей эритромицина эстолат, экстракт ромашки, раствор метиленового синего, сплав ПЭО М.м. 400 и 1500 (прототип изобретения).
Средство для лечения гнойно-воспалительных процессов мягких тканей и слизистых оболочек, содержащее в качестве основы сплав полиэтиленоксидов с молекулярной массой 400 и 1500 и включающее в качестве лечебных компонентов комбинацию антисептика бензалкония хлорида и метронидазол в следующих массовых долях:
