Результат интеллектуальной деятельности: ОКСИНТОМОДУЛИН ЧЕЛОВЕКА, ЕГО ПРИМЕНЕНИЕ, ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ЕГО ОСНОВЕ И СПОСОБ ПРИМЕНЕНИЯ ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГИПЕРГЛИКЕМИИ
Вид РИД
Изобретение
Область изобретения
Изобретение относится к медицине и конкретно к препаратам, нормализующим уровень глюкозы в крови при лечении сахарного диабета 2 типа.
Уровень техники
При изучении секреции глюкагоно-подобного пептида-1 (ГЛП-1) у больных сахарным диабетом 2 типа были выявлены существенные нарушения его секреции, что явилось предпосылкой для разработки препаратов-агонистов рецептора ГЛП-1 для лечения сахарного диабета 2 типа. Предполагалось, что терапевтические эффекты агонистов рецептора ГЛП-1 позволят существенно повысить качество лекарственной помощи больным сахарным диабетом 2 типа за счет усиления синтеза и секреции инсулина, подавления апоптоза бета-клеток и стимуляции их регенерации, подавления секреции глюкагона и ангиотропного эффекта (Аметов А.С., 2006)
Эксенатид представляет собой олигопептид, содержащий 39 аминокислот, являющийся агонистом рецепторов глюкагоно-подобного пептида 1. Аминокислотная последовательность эксенатида частично соответствует последовательности человеческого ГПП-1, в результате чего он связывается и активирует рецепторы GLP-1 у человека, что приводит к усилению глюкозо-зависимого синтеза и секреции инсулина в бета-клетах поджелудочной железы Эксенатид стимулирует высвобождение инсулина из бета-клеток в присутствии повышенных концентраций глюкозы. Лечебная эффективность препарата связана с его способностью усиливать глюкозозависимую секрецию инсулина из бета-клеток поджелудочной железы при гипергликемических состояниях. При этом секреция инсулина прекращается по мере снижения концентраций глюкозы в крови и приближения ее к норме, тем самым уменьшается потенциальный риск гипогликемии. Секреция инсулина в течение первых 10 минут, известная как "первая фаза инсулинового ответа", специфично отсутствует у пациентов с сахарным диабетом типа 2. Кроме того, утрата первой фазы инсулинового ответа является ранним нарушением функции бета-клеток при сахарном диабете типа 2. Введение эксенатида восстанавливает или значительно усиливает как первую, так и вторую фазу инсулинового ответа у пациентов с сахарным диабетом типа 2. Вследствие этого раннее применение эксенатида позволяет значительно снизить инвалидизацию и смертность, связанную с сосудистыми осложнениями сахарного диабета 2 типа.
Оксинтомодулин представляет собой естественный человеческий 37 членный олигопептид содержащий 29 аминокислот идентичных последовательности аминокислот фрагмента глюкагона человека и уникальную С-концевую последовательность из 8 аминокислот. Структура оксинтомодулина и его способность повышать уровень цАМФ в культуре париетальных клеток желудка крыс были впервые описаны в 1981 году и приведена на рисунке 1 (Bataille D., 1981).
Ряд исследований продемонстрировал способность оксинтомодулина подавлять индуцированную приемом пищи секрецию желудочного сока у грызунов. Эффект при этом был сравним с действием глюкагоно-подобного пептида-1 и глюкагоно-подобного пептида-2. Оксинтомодулин является слабым агонистом рецептора глюкагона и имитирует эффекты глюкагона в печени и поджелудочной железе. Оксинтомодулин подавляет аппетит при внутримозговом введении грызунам. Аноректогенный эффект оксинтомодулина подавляется эксенатидом. Специфический рецептор оксинтомодулина в настоящее время не идентифицирован. Показано, что многие эффекты оксинтомодулина реализуются путем взаимодействия последнего с рецепторами ГПП-1 и ГПП-2. Парентеральное введение оксинтомодулина подавляет аппетит, но в отличие от ГПП-1 при этом отсутствует эффект подавления эвакуаторной функции желудка. Оксинтомодулин также имитирует действие ГПП-1 на бета клетки поджелудочной железы, включая стимуляцию глюкозо-зависимой секреции инсулина и подавление апоптоза бета-клеток (Jarrousse С., 1986; Schjoldager В., 1988; Dakin С., 2004; А. Maida, 2008).
Известно применение оксинтомодулина для лечения ожирения (RU 2351359). Оксинтомодулин, в отличие от эксенатида, не подавляет моторную функцию желудка. Все это вместе делает оксинтомодулин перспективным кандидатом для создания лекарственного средства - миметика инкретина. К сожалению, при исследовании на людях оксинтомодулин не оказывал достоверного гипогликемического эффекта (Wynne K., 2005) и был в 500 раз менее активен, чем эксенатид в гипогликемическом тесте у мышей (A. Maida, 2008).
Краткое описание изобретения
Задачей изобретения является создание химически модифицированной формы оксинтомодулина с высокой гипогликемической активностью для лечения сахарного диабета 2 типа. Эта задача решается тем, что в качестве химической модификации молекулы природного оксинтомодулина используется ковалентное присоединение гомополимерного полисахарида, содержащего 50 звеньев альфа-2,8 сиаловой кислоты.
Полисиаловые кислоты (PSA) представляют собой природные неразветвленные полимеры сиаловой кислоты, вырабатываемые определенными штаммами бактерий и в определенных клетках у млекопитающих (Roth., 1993). Их можно получать с различной степенью полимеризации, от n = примерно 80 или более остатков сиаловой кислоты до n=2 путем кислотного гидролиза или расщеплением нейраминидазами, или фракционированием природных вырабатываемых бактериями видов полимера. Состав различных полисиаловых кислот также изменяется таким образом, что существуют гомополимерные формы, такие как, например альфа-2,8-связанная полисиаловая кислота, включающая капсульный полисахарид штамма К1 Е. coli и В-группы менингококков, который также обнаруживают в эмбриональной форме молекулы клеточной адгезии нейрона (N-CAM). Также существуют гетерополимерные формы, такие как чередующаяся альфа-2,8 альфа-2,9 полисиаловая кислота штамма К92 Е. coli и полисахариды C группы N. meningitidis. Сиаловую кислоту также можно обнаружить в чередующихся сополимерах с мономерами, отличающимися от сиаловой кислоты, таких как группа W135 или группа Y N. meningitidis.
Полисиаловые кислоты обладают важным биологическим действием, включая уклонения патогенных бактерий от иммунной системы и системы комплемента. Альфа-2,8-связанная полисиаловая кислота штамма К1 Е. coli также известна как «коломиновая кислота» и ее формы различной длины используют в настоящем изобретении.
Среди бактериальных полисахаридов альфа-2,8 связанная форма полисиаловой кислоты представляет собой единственную неиммуногенную (не вызывающую ни ответа Т-клеток, ни образования антител у млекопитающих, даже при конъюгации с иммуногенными носителями белками). Более короткие формы полимера (до n=4) обнаруживают в ганглиозидах клеточной поверхности, которые широко распространены в организме и считаются эффективными для сообщения и поддержания иммунологической толерантности по отношению к полисиаловой кислоте.
В последние годы биологические свойства полисиаловых кислот, в особенности биологические свойства альфа-2,8 связанной гомополимерной полисиаловой кислоты, были использованы для модификации фармакокинетических свойств белковых или низкомолекулярных молекул лекарственных веществ [Gregoriadis, 2001; Jain et al., 2003; US-A-5846951, WO-A-0187922].
Альфа-2,8-связанная полисиаловая кислота (PSA) предлагает привлекательную альтернативу для модификации белков, представляя собой иммунологически невидимый биологически разрушаемый полимер, являющийся естественной частью человеческого организма, и который разрушается тканевыми нейраминидазами до сиаловой кислоты, нетоксичного сахарида
Выбор авторов настоящего изобретения основан на результатах исследования, проведенного авторами настоящего изобретения, которые обнаружили, что ковалентное присоединение гомополимерного полисахарида, содержащего 50 звеньев альфа-2,8 сиаловой кислоты к молекуле природного оксинтомодулина существенно воздействует на биологическую активность последнего, а именно существенно усиливает его гипогликемическую активность. Именно это свойство оксинтомодулина человека, ковалентно связанного с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты, позволило решить поставленную задачу.
Настоящее изобретение предлагает оксинтомодулин человека, ковалентно связанный с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты.
Далее, согласно настоящему изобретению предлагается лекарственный препарат для лечения или профилактики гипрегликемии у пациента страдающего диабетом 2 го типа, содержащий в качестве активного вещества оксинтомодулин человека, ковалентно связанный с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты и в качестве неактивных компонентов стабилизирующие добавки и наполнители, смешанные с апирогенной водой или другими фармацевтически приемлимыми носителями.
Далее, согласно настоящему изобретению предложен способ лечения и профилактики гипергликемии у пациента с сахарным диабетом 2 типа, который нуждается в указанном лечении или профилактике, включающий подкожное введение указанному пациенту лекарственного препарата, содержащего в качестве активного вещества оксинтомодулин человека, ковалентно связанный с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты.
Далее согласно настоящему изобретению предлагается применение оксинтомодулина человека, ковалентно связанного с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты в качестве активного вещества лекарственного препарата для лечения гипергликемии при сахарном диабете 2 типа.
Подробное описание изобретения и примеры его реализации
Сущность изобретения поясняется двумя примерами получения заявляемого соединения и заявляемого лекарственного средства и таблицей и рисунками, где дано:
В таблице 1 результаты оценки гипогликемической активности конъюгата человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты массой 14 кДа
На фиг.1 аминокислотная последовательность оксинтомодулина человека.
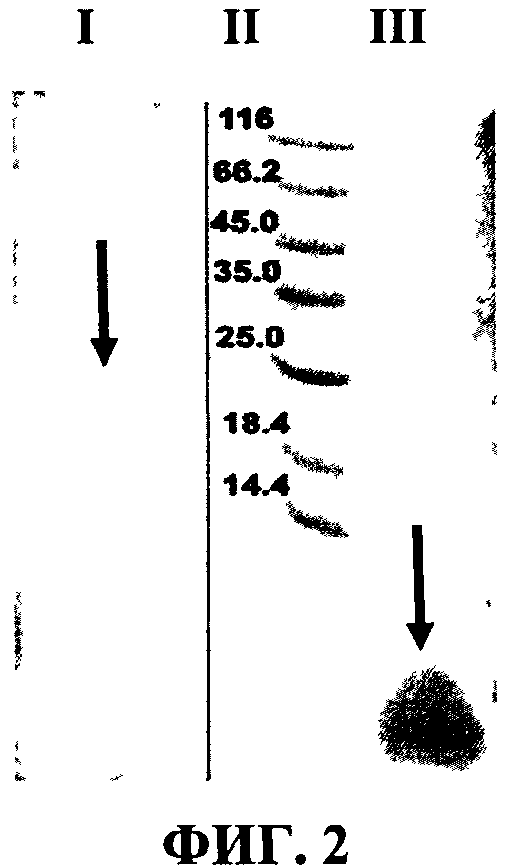
На фиг.2 результаты хроматографического анализа ковалентного конъюгата человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты массой 14 кДа, содержащим 50 звеньев сиаловой кислоты.
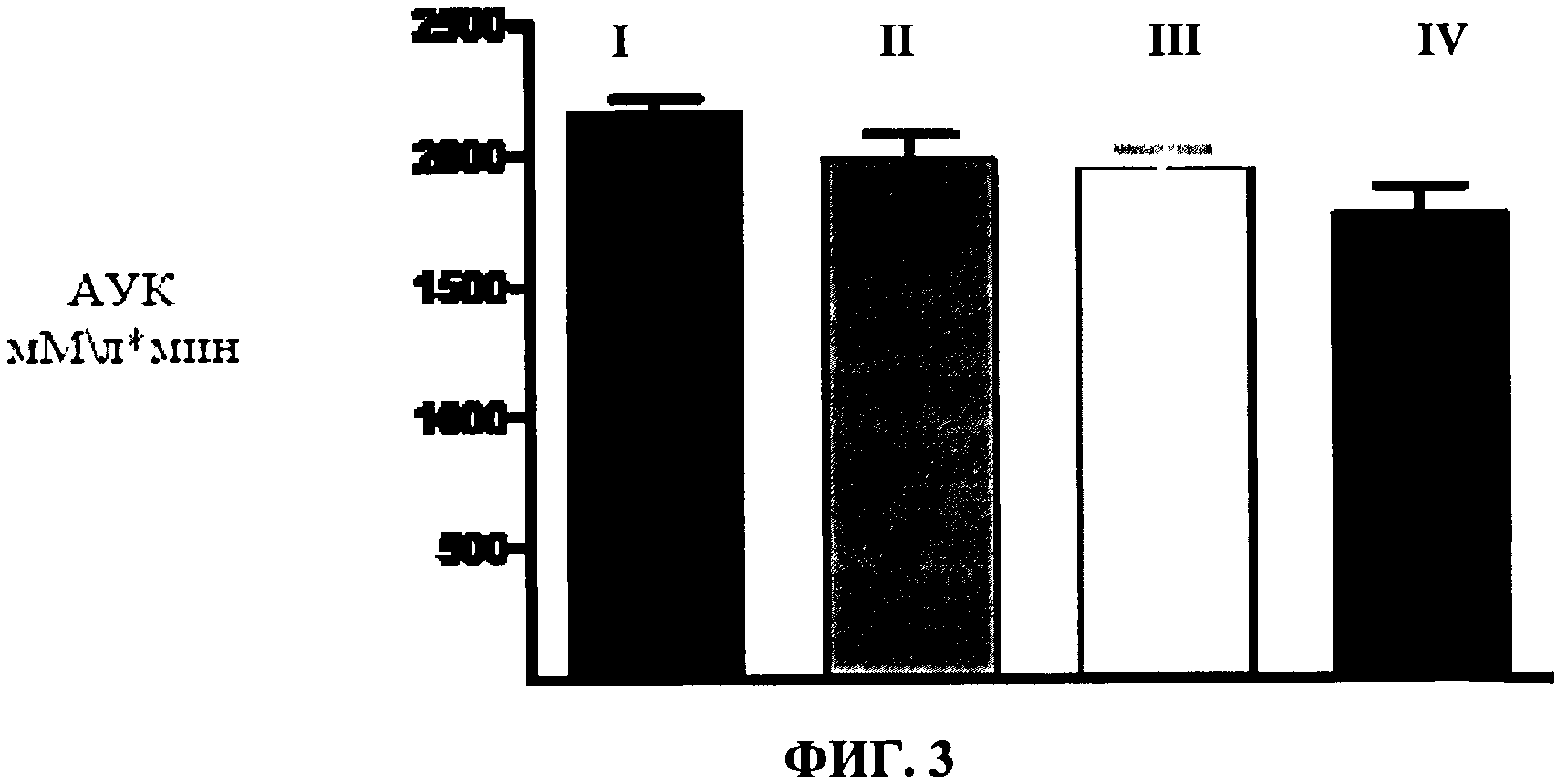
На фиг.3 результаты оценки гипогликемической активности конъюгата человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты массой 14 кДа в сравнении с эксенатидом в тесте нагрузки глюкозой
Заявленное лекарственное средство получают, например, следующим образом.
Пример 1. Получение рекомбинантного оксинтомодулина, ковалентно связанного с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты
Для конструирования экспрессионной плазмиды ген оксинтомодулина и интеина Ssp dnaB из Synechocestis sp синтезировали из перекрывающихся олигонуклеотидов и клонировали в экспрессионную плазмиду pTWIN1 с последующей трансформацией штамма Е. coli ER2566. В результате был создан штамм-продуцент Е. coli ER2566/pER-Oxm в котором при индукции образуется гибридный белок (Int-Oxm), содержащий на N-конце модифицированный интеин DnaB, включающий хитин-связывающий домен, а на С-конце - последовательность оксинтомодулина. Продуцент Е. coli ER2566/pEROxm культивировали при 37°C до оптической плотности культуры 0.6-0.7, затем индуцировали ИПТГ и выращивали 4 ч. при 37°C. После выделения и солюбилизации телец включения индуцировали автокаталитическое расщепление белка на хитиновом сорбенте (V.N. Stepanenko et al., 2007). После завершения реакции расщепления выпавший в осадок ГБ отделяли центрифугированием; очистку оксинтомодулина от остаточного пептида и ГБ, не выпавшего в осадок, производили с помощью установки для тангенциальной ультрафильтрации на мембране VivaFlow 50 10000 MWCO RC для отсечения от нерасщепленного гибридного белка и интеина Оксинтомодулин (молекулярная масса 3 кДа) оставался в фильтрате с максимальной концентрацией 0,05 мг/мл. Фильтрат, содержащий оксинтомодулин, наносили на колонку SP Sepharose High Performance, уравновешенную в аммонийно-ацетатном буфере при pH 4,0. Оксинтомодулин элюировали буфером К (20 мМ Tris pH 10 8 М мочевина 1.7 М NaCl. При этом происходило концентрирование оксинтомодулина в 500 раз по сравнению с объемом нанесения. Окончательную очистку оксинтомодулина проводили с помощью ВЭЖХ на полупрепаративной колонке (250×16) Диасорб-130-С16Т 7 мкм в градиенте 25-65% ацетонитрила с 0,1% ТФУ со скоростью 2,5 мл/мин. Конъюгацию целевого белка проводят при мольном соотношении 14 kDa ПСА (альфа-2,8 полисиаловая кислота) - целевой пептид 2:1 с последовательным поэтапным добавлением ПСА и концентрации NaCNBH3 2,5 мг/мл при 37±2°C при pH 6 и присутствии ацетонитрила в течение 4 ч. Очистку конъюгата осуществляли обращено-фазовой ВЭЖХ на колонке Диасорб-130-С16Т с последующей гель-фильтрацией. Очищенный ковалентный конъюгат человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты содержащим 50 звеньев сиаловой кислоты анализировали с помощью градиентного ПААГ.
Пример 2. Получение рекомбинантного оксинтомодулина, ковалентно связанного с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты
На первой стадии тиольные группы вводили в последовательность человеческого рекомбинантного оксинтомодулина тиолированием амина лизина. Полученный, как описано в примере 1, человеческий рекомбинантный оксинтомодулин, 4 мг, растворяли в 0,25 мл PBS+10 мМ ЭДТА и добавляли 0,498 мг 2-иминотиолана (2-IT или реактива Траута 50 моль-эквивалентов 3,6×10-6 моль) в 0,25 мл того же буфера. Пробирку закрывали фольгой и оставляли для инкубации при перемешивании гибкой мешалкой в течение 1 ч при 3°C. Тиолированный человеческий рекомбинантный оксинтомодулин очищали от свободного 2-IT (реактив Траута) гель-фильтрацией (PD-10) и 0,5 мл фракции анализировали на присутствие белка (ВСА анализ) или тиола (анализ Элмана). Окисленную полисиаловую кислоту с молекулярной массой 25 кДа вводили в реакцию с 5 молярными эквивалентами гидразида N-[в-малеимидпропионовой кислоты] в 0,1 М ацетате натрия в течение 2 часов при 37°C. Полученный гидразон (САМ) осаждали в этаноле, повторно суспендировали в ацетате натрия и повторно осаждали в этаноле, повторно растворяли в воде и подвергали сухой заморозке. К тиолированному человеческому рекомбинантному оксинтомодулину (3,6 мг) в 2 мл PBS/ЭДТА добавляли 22,5 мг САМ (9×10-7 моль, 15 моль-эквивалентов). Пробирку запечатывали и оставляли для инкубации при 37°C в течение 1 ч при мягком перемешивании. Полученный конъюгат затем выделяли последовательно ионообменной и обращено-фазовой хроматографией. Очищенный ковалентный конъюгат человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты содержащим 50 звеньев сиаловой кислоты растворяли в фосфатном буфере (pH 7,0), разливали во флаконы объемом 2 мл, содержащие гликопептид в концентрации 100 мкг/мл и использовали для анализа гипогликемической активности.
В таблице 1 приведены результаты оценки гипогликемической активности конъюгата человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты массой 14 кДа, свидетельствующие о выраженной гипогликемической активности конъюгата.
|
Эксперименты выполнялись на крысах Спрег-Доули массой 230-250 г, мужского пола Для изучения гипогликемического действия препарат вводили крысам натощак однократно подкожно в забуференном физиологическом растворе (pH 7,4) в дозах 5 и 25 мкг/кг. В качестве негативного контроля использовали забуференный физиологический раствор (pH 7,4) (растворитель). В каждой группе использовали 6 животных. Кровь для анализа отбирали из орбитального синуса и определяли уровень глюкозы в сыворотке ортотолуидиновым методом
На фиг.1 представлена аминокислотная последовательность оксинтомодулина человека.
На фиг.2 приведены результаты хроматографического анализа ковалентного конъюгата человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты массой 14 кДа, содержащим 50 звеньев сиаловой кислоты, свидетельствующие об образовании истинного конъюгата.
I - ковалентный конъюгат человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты содержащим 50 звеньев сиаловой кислоты
II - стандарты молекулярных масс (кДа),
III - рекомбинантный оксинтомодулин человека
На фиг.3 приведены результаты оценки гипогликемической активности конъюгата человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты массой 14 кДа в сравнении с эксенатидом в тесте нагрузки глюкозой, свидетельствующие о том, что специфическая гипогликемическая активность конъюгата не уступает таковой эксенатида. При расчете площади под кривой (АУК) полученной из результирующей картины концентраций глюкозы в плазме крови (площадь выше уровня 0 мМ/л глюкозы плазмы крови) выявлено достоверное (P<0,05) снижение АУК в группе животных получавших конъюгат человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты содержащим 50 звеньев сиаловой кислоты дозе 25 мкг/мл (ВСА-метод). В тоже время в группе животных получавших эксенатид в дозе 25 мкг/кг по сравнению с животными контрольной группы не было выявлено достоверных отличий.
Эксперименты выполнялись на 32 крысах Спрег-Доули массой 230-250 г, мужского пола. Натощак крысам подкожно вводились испытуемые вещества - ковалентный конъюгат человеческого рекомбинантного оксинтомодулина с гомополимером альфа-2,8 сиаловой кислоты содержащим 50 звеньев сиаловой кислоты (ИБХ-1) и эксенатид, а через час после этого перорально вводилась глюкоза в дозе 3 г/кг (раствор в дистиллированной воде 500 мг/мл). Препараты вводились следующим образом:
Группа 1 - Физиологический раствор
Группа 2 - ИБХ-1; 5 мкг/кг
Группа 3 - Эксенатид; 25 мкг/кг
Группа 4 - ИБХ-1; 25 мкг/кг
Уровни глюкозы в крови определяли каждые 30 мин на протяжении 3 часов. Каждая группа состояла из 8 животных (n=8).
Таким образом, приведенные выше материалы позволяют утверждать, что заявляемый конъюгат и лекарственное средство на его основе для лечения гипергликемии является новым. Из опубликованных источников информации заявителям не известно применение оксинтомодулина человека, ковалентно связанного с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты для лечения гипергликемии при сахарном диабете 2 типа.
Заявляемый лекарственный препарат промышленно применим, что подтверждено примерами его изготовления и применения, показавшими, что он имеет выраженный гипогликемический эффект, не уступающий таковому эксенатида.
Заявляемое применение является неочевидным. Гипогликемическая активность оксинтомодулина человека, ковалентно связанного с гомополимерным полисахаридом, содержащим 50 звеньев альфа-2,8 сиаловой кислоты существенно отличается от таковой природного человеческого оксинтомодулина. Механизмы указанного феномена в настоящий момент исследуются авторами.
Из вышеизложенного следует, что заявленное применение ново, неочевидно и промышленно применимо, т.е. соответствует всем требованиям, предъявляемым к изобретению.
Пример 3. Состав и описание лекарственного препарата, содержащего конъюгат оксинтомодулина и полисиаловой кислоты, согласно изобретению.
Одним из примеров лекарственных препаратов, содержащих конъюгат оксинтомодулина и полисиаловой кислоты, согласно изобретению является лекарственный препарат «Окситолонг» (ОАО «Фармсинтез»).
Указанный препарат содержит конъюгат оксинтомодулина человека и полисиаловой кислоты, характеризующийся следующей структурной формулой:
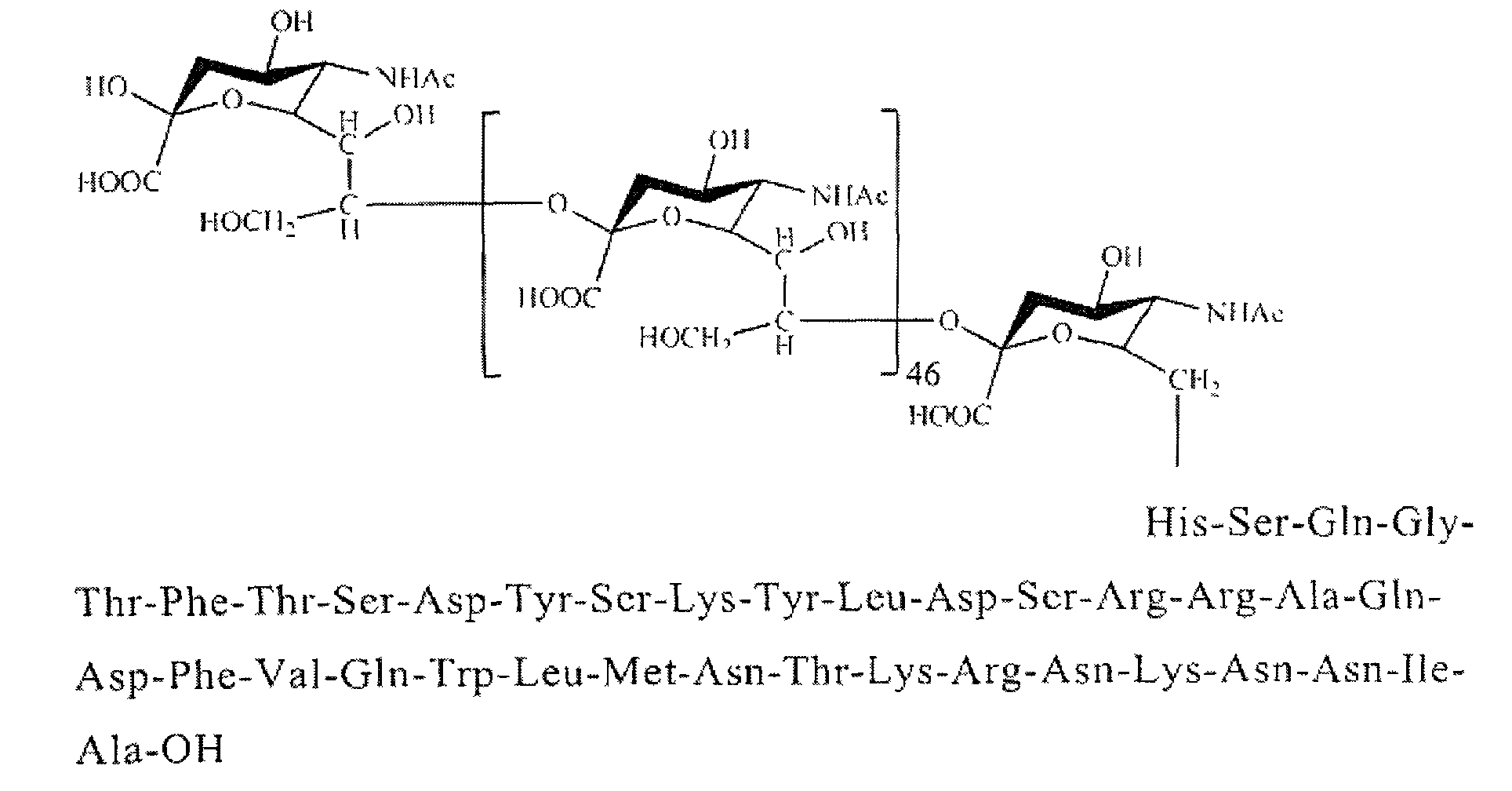
Состав препарата «Окситолонг»:
Активное вещество:
|
Вспомогательные вещества:
|
Аметов А.С. Регуляция секреции инсулина в норме и при сахарном диабете 2 типа: роль инкретинов. Русский медицинский журнал. 14.12.2006, том 14, №26.
Bataille D. et al., Peptides, 1981, V.2, Suppl. 2, P.41-44.
Jarrousse C, Niel H, Audousset-Puech MP, Martinez J, Bataille D., Oxyntomodulin and its C-terminal octapeptide inhibit liquid meal-stimulated acid secretion., Peptides. 1986; 7 Suppl 1:253-6.
Schjoldager ВТ, Baldissera FG, Mortensen PE, Holst JJ, Christiansen J. Oxyntomodulin: a potential hormone from the distal gut. Pharmacokinetics and effects on gastric acid and insulin secretion in man Eur J Clin Invest. 1988 Oct; 18(5):499-503.
Dakin CL, Small CJ, Batterham RL, Neary NM, Cohen MA, Patterson M, Ghatei MA, Bloom SR., Peripheral Oxyntomodulin reduces food intake and body weight gain in rats. Endocrinology, 2004 Jun; 145(6):2687-95. Epub 2004 Mar 4.
Wynne K, Park AJ, Small CJ, Meeran K, Ghatei MA, Frost GS, Bloom SR Oxyntomodulin increases energy expenditure in addition to decreasing energy intake in overweight and obese humans: a randomized controlled trial hit J Obes (Lond). 2006 Dec; 30(12): 1729-36. Epub 2006 Apr
Adriano Maida, Julie A. Lovshin, Laurie L. Baggio, and Daniel J. Drucker, The glucagon-like peptide-1 receptor agonist oxyntomodulin enhances b-cell function but does not inhibit gastric emptying in mice, Endocrinology July 31, 2008.
V.N. Stepanenko, et a., Recombinant Oxyntomodulin, Russian Journal of Bioorganic Chemistry, 2007, Vol.33, No. 2, pp.227-232.
Roth, J., Rutishauser, U., Troy, F.A. (Eds.), Polysialic acid: from microbes to man, Birkhauser Verlag, Basel, Advances in Life Sciences, 1993.
Gregoriadis, G., Drug and vaccine delivery systems, in: PharmaTech, World Markets Research Centre Limited, London (2001) 172-176.
Jain, S., Hirst, D.H., Laing, P., Gregoriadis, G., Polysialylation: The natural way to improve the stability and pharmacokinetics of protein and peptide drugs, Drug Delivery Systems and Sciences, 4(2) (2004) 3-9