Результат интеллектуальной деятельности: СПОСОБ ПРИГОТОВЛЕНИЯ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОГО ПРЕПАРАТА ИЗ ЖИВЫХ ШТАММОВ МИКРООРГАНИЗМОВ ЛАКТОБАЦИЛЛ И БИФИДОБАКТЕРИЙ "LB-КОМПЛЕКС ПЛЮС"
Вид РИД
Изобретение
Изобретение относится к медицинской и пищевой биотехнологии и может быть использовано для приготовления лечебно-профилактических препаратов, биологически активных добавок и продуктов питания с использованием в качестве стартерных культур живых пробиотических штаммов микроорганизмов.
В настоящее время разработаны и широко применяются бактерийные препараты и биологически активные добавки к пище (БАД) из живых штаммов лакто- и бифидобактерий как в сухой (порошки, таблетки и пр.), так и в жидкой формах.
К преимуществам сухих сублимированных форм можно отнести длительный срок хранения (до нескольких лет), удобство применения и реализации. Но при сублимационной сушке нарушается структура поверхностных белков-адгезинов, что снижает колонизационную способность бактерий, а также разрушается большая часть ценных метаболитов, положительно влияющих на процесс восстановления микрофлоры. В жидких формах пробиотиков клетки находятся в физиологически активном состоянии и способны активно колонизировать кишечник уже через 2 часа после попадания в организм, структура адгезинов не нарушена, в питательной основе сохраняются ценные бактериальные метаболиты, в частности органические кислоты: уксусная, молочная, витамины В, С, К, которые, попадая в кишечник, изменяют в нем свойства среды, что благотворно влияет на развитие собственной микрофлоры и угнетает патогенные и условно-патогенные микроорганизмы (Бондаренко В.М., Шапошникова Л.И. Клинический эффект жидких пробиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл, 2007)
Известны жидкие препараты-пробиотики как на основе цельного коровьего молока, так и на основе гидролизатов, в качестве стартерных культур которых использованы композиции штаммов лакто- и бифидобактерий. См., например, способ приготовления лечебно-профилактического препарата на основе гидролизата обезжиренного молока (обрата) из живых штаммов микроорганизмов «LB-комплекс» (патент РФ №2192269, А61К 35/74, А23С 9/127, С12N 1/20, С12R 1:07, 1:225, 1:25, опубликован 10.11.2002).
Способ включает раздельное культивирование штаммов бифидо- и лактобактерий и смешивание их в соотношении 1:1 по окончании культивирования. Культивирование проводят на гидролизатно-молочной среде (ГМС). В качестве основы ГМС используют гидролизат обезжиренного молока и дополнительно вводят аскорбиновую кислоту в количестве 230-250 мг на 1000 мл гидролизата. Готовый препарат расфасовывают во флаконы с учетом необходимой суточной дозы. Способ позволяет получить готовый к употреблению препарат, воздействующий на бифидо- и лактокомпоненты микрофлоры человека, с длительным сроком годности.
Используют ГМС следующего состава:
|
рН 8,5-8,6
Но, во-первых, использующееся по данному способу исходное сырье для приготовления гидролизата - обрат молока (обезжиренное молоко), - по количественному содержанию белка казеина нестабильный продукт, и проведение гидролиза по указанному способу не обеспечивает полное расщепление казеина, в связи с этим получаемый полупродукт (основа среды) имеет низкий уровень аминного азота (150-160 мг%), что обуславливает применение неразведенного гидролизата обезжиренного молока по данному способу.
Во-вторых, использование в рецептуре среды лактозы в количестве 10 г на литр делает невозможным применение препарата, приготовленного по данному способу, у людей с лактазной недостаточностью.
Лактазная недостаточность является наиболее часто встречающимся вариантом синдрома мальабсорбции у детей. По данным российских исследователей, она ответственна за 70% длительных диарей у детей грудного возраста. Под лактазной недостаточностью понимают сниженную активность кишечной лактазы - фермента пристеночного пищеварения, расщепляющего дисахарид лактозу до моносахаров - глюкозы и галактозы. Фермент синтезируют зрелые энтероциты, расположенные на вершине кишечных ворсинок. Дефицит лактазы у детей в России встречается в 10-75% случаев в зависимости от национальности популяции (Самаль Т.Н., Украинцев С.Е. БГМУ. Опубликовано в журнале ″Медицинская панорама″, №2 за 2004).
В качестве прототипа принят способ приготовления лечебно-профилактического препарата на основе живых штаммов микроорганизмов лакто- и бифидобактерий «LB-комплекс Л» (патент РФ №2441907, C12N 1/20, А61К 35/74, А23С 9/127, опубл. 10.02. 2012).
Способ включает культивирование смеси штаммов микроорганизмов на питательной среде, содержащей питательную основу - казеин, гидролизованный поджелудочной железой крупного рогатого скота, и дистиллированную воду для разведения ферментированного гидролизата до заданного содержания аминного азота, в качестве углеводной составляющей, содержащей лактозу и раффинозу в соотношении 1:1, причем раффиноза является как углеводным компонентом, так и пребиотической составляющей. Смесь штаммов добавляют к сорбирующему компоненту, предварительно расфасованному из расчета 1/2 - 1/4 часть общего объема созданной комплексной системы. Процесс иммобилизации на сорбенте-носителе БАД к пище «Литовит М» происходит при температуре +6°±2°С в течение 18-24 ч. В качестве штаммов-продуцентов используют L.plantarum 8 RA-3, L.fermentum 39, L.fermentum 90 ТС-4, B.bifidum 1, B.bifidum 791, B.longum 379. Способ позволяет получить иммобилизованный препарат - синбиотик с высоким содержанием живых микробных клеток нескольких штаммов лактобацилл и бифидобактерий, обладающий повышенным защитным лечебным действием.
Недостатком данного способа является использование лактозы в качестве углеводной составляющей в количестве 5 г на литр и длительный трехэтапный технологический процесс для масштабирования биомассы штаммов-продуцентов с высокой концентрацией живых микробных клеток 1010-1012КОЕ/мл, занимающий в общей сложности 84 часа.
Этот недостаток устраняется предлагаемым решением.
Решаемая задача - совершенствование способа приготовления гипоаллергенного безлактозного многокомпонентного пробиотика. Технический результат - получение препарата синбиотика для детей с ферментопатиями (лактазная недостаточность как вариант синдрома мальабсорбции) за счет замены углеводной составляющей лактозы на натуральный плодовый сахар фруктозу (синонимы: левулеза, b-D-фруктофураноза), при сокращении времени технологического процесса.
Этот результат достигается тем, что в способе приготовления лечебно-профилактического препарата из живых штаммов микроорганизмов лактобацилл и бифидобактерий путем их культивирования при температуре 37±1°С на питательной среде, содержащей питательную основу - гидролизат казеина, разведенный дистиллированной водой, хлористый натрий, углеводную составляющую, агар-агар, кислую составляющую, в качестве штаммов-продуцентов используют L.plantarum 8 RA-3, L.fermentum 39, L.fermentum 90 ТС-4, B.bifidum 791, B.longum 379, B.bifidum 1, расфасовку жидкого препарата с учетом необходимой для пациентов суточной дозы, для культивирования лактобацилл и бифидобактерий используют две различные среды: одна среда для лактобацилл с содержанием аминного азота 160-170 мг%, другая - для бифидобактерий - 180-200 мг%, различным содержанием агар-агара - 750±10 мг/л и 1000±10 мг/л, различной рН готовой среды 7,8 - 8,0 и 8,5 - 8,6 соответственно, в качестве углеводной составляющей в обеих средах используют фруктозу, разведенные в среде для лактобацилл штаммы L. plantarum 8 RA-3 и L. fermentum 39 соединяют в соотношении 1:1 и совместно культивируют 24±1 ч, полученную биомассу первой генерации смешивают со свежей питательной средой в соотношении 1:1000 и продолжают культивирование в течение 24±1 ч, а штамм L. fermentum 90 ТС-4 культивируют по тому же способу отдельно, штаммы В. bifidum 791 и В. longum 379, разведенные в среде для бифидобактерий, соединяют в соотношении 1:1 и совместно культивируют 24±1 ч, полученную биомассу первой генерации смешивают со свежей питательной средой в соотношении 1:1000 и продолжают культивирование в течение 48±1 ч, а штамм В. bifidum 1 культивируют по тому же способу отдельно, по окончании культивирования биомассы штаммов, выращенных на различных средах, смешивают в соотношении 2:1: 2:1
Таким образом, предложен оптимальный комплекс, позволяющий при сокращении времени технологического процесса до 72 часов (т.е. в 1,2 раза) получить гипоаллергенный безлактозный многокомпонентный пробиотик в форме бактериального концентрата с высоким содержанием живых микробных клеток всех 6-ти стартерных культур в единице объема с длительным сроком хранения.
Способ осуществляется следующим образом:
1. Готовят единый полупродукт - основу питательной среды по следующей схеме: разводят казеин в теплой питьевой воде, добавляют молотую поджелудочную железу крупного рогатого скота, доводят температуру до 48±1°С, устанавливают рН 10-20% раствором NaOH, перемешивают, добавляют хлороформ и помещают в термостат на 72 часа, первый час постоянно перемешивают, затем фильтруют через бумажный фильтр. В готовом гидролизате контролируют аминный азот.
2. Далее для приготовления гидролизатно-казеиновой среды ГКС-Л разводят полупродукт, приготовленный по п.1., дистиллированной водой до аминного азота 160- 170 мг%, добавляют агар-агар 750±10 мг/л, хлористый натрий, пептон, фруктозу, аскорбиновую кислоту, устанавливают рН 10-20% раствором NaOH и стерилизуют, рН готовой ГКС-Л должен составлять 7,8-8,0.
3. Для приготовления гидролизатно-казеиновой среды ГКС-Б разводят полупродукт, приготовленный по п.1., дистиллированной водой до аминного азота 180-200 мг%, добавляют агар-агар 1000±10 мг/л, хлористый натрий, пептон, фруктозу, аскорбиновую кислоту, устанавливают рН 10-20% раствором NaOH и стерилизуют, рН готовой среды ГКС-Б должен составлять 8,5-8,6.
Культивирование штаммов-продуцентов лактобацилл и бифидобактерий проводят на разных средах по единому способу - два штамма вместе, один отдельно в два этапа таким образом, что время, затраченное на наращивание биомассы лактобацилл, составляет 48±1 ч, а бифидобактерий - 72±1 ч, таким образом, весь процесс занимает 72 часа. По окончании культивирования биомассы штаммов смешивают в соотношении 2:1:2:1 и расфасовывают во флаконы. Затем флаконы маркируют, фасуют в коробки по 25 штук (минимальный курс лечения).
Пример осуществления способа
На первом этапе готовят впрок полупродукт - гидролизат казеина следующим образом: питьевую воду (ГОСТ 2874-82) нагревают до 48±1°С, засыпают казеин (казеин пищевой кислотный по ОСТ 4960-74) в количестве 60-70 г на литр, размешивают, доводят рН до 7,8-8,2 ЕД 20% раствором NaOH, ставят в термостат при 48±1°С на два часа для набухания, затем добавляют промолотую поджелудочную железу крупного рогатого скота (ГОСТ 11285-93) в количестве 60-70 г/л и хлороформ в количестве 10±0,5 мл/л, доводят рН до 7,9-8,0 10-20% раствором NaOH и ставят в термостат при температуре 48±1°С. В течение первого часа содержимое несколько раз перемешивают (пробку после встряхивания прокалывают для удаления паров хлороформа) и оставляют для осуществления процесса гидролиза на 72 часа, после выдержки в термостате сливают надосадочную жидкость через бумажный фильтр. Готовый гидролизат должен содержать 450-500 мг/% аминного азота. Хранят гидролизат впрок под хлороформом 1% к объему при температуре 4±10°С.
Из полученного полупродукта готовят две питательные среды ГКС-Л и ГКС-Б по следующим рецептурам (таб.1.).
Для приготовления ГКС-Л разводят цельный гидролизат дистиллированной водой до показателя аминного азота 160-170 мг/%. В разведенный гидролизат добавляют из расчета на 1 л 5 г хлористого натрия, 2 г пептона, 10 г фруктозы, аскорбиновой кислоты 0,24±0,1 г и 0,75±0,1 г предварительно стандартно приготовленного агар-агара. Добавляют NaOH 20% раствор для установления рН 7,8-8,0.
Для приготовления ГКС-Б разводят цельный гидролизат дистиллированной водой до показателя аминного азота 180-200 мг/%. В разведенный гидролизат добавляют из расчета на 1 л 5 г хлористого натрия, 2 г пептона, 10 г фруктозы, аскорбиновой кислоты 0,24±0,1 г и 1,0±0,1 г предварительно стандартно приготовленного агар-агара. Добавляют NaOH 20% раствор для установления рН 8,5-8,6.
Готовые среды ГКС-Л и ГКС-Б стерилизуют по единому способу при 0,5 атм. 30 минут.
Использование для приготовления гидролизата стандартного продукта - кислотного казеина, обеспечивает высокий уровень аминного азота получаемого полупродукта - 450-500 мг%, что позволяет разводить полупродукт до требуемого уровня аминного азота в питательных средах, обеспечивающего высокий выход биомассы препарата.
Аскорбиновая кислота используется как стимулятор роста для бифидобактерий и лактобацилл.
Пептон представляет собой смесь поли- и олигопептидов, аминокислот, солей и микроэлементов, соответственно, является источником питательных веществ.
Агар увеличивает вязкость среды, что приводит к равномерному росту микроорганизмов по всей толще среды и равномерному потреблению факторов роста и питательных веществ.
Фруктоза - углевод - энергетический субстрат и источник углерода.
Хлорид натрия поддерживает оптимальное осмотическое давление клеток.
В качестве штаммов-продуцентов используют L.plantarum 8RA-3, и L.fermentum 90-ТС-4 и L.fermentum 39, B.bifidum 791, B.bifidum 1, B.longum 379.
Культивирование штаммов-продуцентов лактобацилл и бифидобактерий производится по следующему способу:
I генерация: лактобацилл - в ампулы с сухими штаммами лактобацилл L.plantarum 8RA-3 и L.fermentum 39 добавляют по 1 мл ГКС-Л, далее содержимое обеих ампул смешивают во флаконе с 18 мл ГКС-Л; сухой штамм L.fermentum 90ТС-4 разводят 1 мл ГКС-Л, далее содержимое ампулы переносят во флакон с 9 мл ГКС-Л.
Штаммы бифидобактерий готовятся по тому же способу на среде ГКС-Б, штаммы B.bifidum 791 и B.longum 379 смешивают во флаконе, B.bifidum 1 разводят отдельно. Затем штаммы-продуценты культивируют в течение 24+1 ч при температуре 37±1°С (табл. 2).
II генерация - полученные биомассы I генерации каждую отдельно смешивают со свежей питательной средой (ГКС-Л для лактобацилл и ГКС-Б для бифидобактерий) в соотношении 1:1000 (т.е. 10 мл I генерации вносят в 9,99 л среды и получают 10 л II генерации) и продолжают культивировать лактобациллы в течение 24±1 ч при температуре 37±1°С, бифидобактерий в течение 48±1 ч при 37±1°С (табл.2).
По окончании культивирования полученные биомассы смешивают в соотношении 2:1:2:1.
Разливают смесь биомассы стартерных культур лактобацилл и бифидобактерий в стерильные флаконы по 2,0, 2,5, 5,0 мл с учетом суточной дозы пробиотика.
Герметично закрывают резиновой пробкой и алюминиевым колпачком. Затем флаконы маркируют, фасуют в коробки по 25 штук (минимальный курс лечения). Хранится препарат при температуре +6±2°С до 60 суток с сохранностью живых микробных клеток в 1 мл жидкого препарата 1010-1012 КОЕ/мл (табл. 3).
Препарат может быть получен реакторным методом.
Препарат может использоваться перорально в 1 или 2 приема по 1 флакону в день перед едой с водой, компотом, морсом, соком и т.п. с температурой не выше 30°С. Перед употреблением флакон с препаратом тщательно встряхивают.
Для детей первых месяцев жизни «LB-КОМПЛЕКС плюс» вводится в любые адаптированные искусственные смеси в количестве 2-2,5 мл в сутки (дробно на 3 кормления).
Показания к применению:
- в качестве пробиотической составляющей диетотерапии при любых заболеваниях, осложненных дисбактериозом кишечника, в качестве средств, нормализующих микрофлору: при длительном лечении антибиотиками, химио- и гормональными препаратами; при аллергических заболеваниях (аллергодерматозы, экземы и т.п.); при хронических заболеваниях ЖКТ, острых кишечных инфекциях бактериальной и вирусной этиологии (дезинтерия, коли-энтерит, сальмонеллез, ОКИ невыясненной этиологии, рота-и энтеровирусная инфекция и др.), пищевых токсикоинфекциях; и др.
Может применяться при лактазной недостаточности и сахарном диабете, а также на фоне антибактериальной терапии с учетом фармакокинетики и фармакодинамики антибиотика/химиопрепарата.
Клиническая апробация пробиотика, приготовленного по способу, представленному в заявке, была проведена в следующих лечебно-профилактических учреждениях города Н. Новгорода: МЛПУ Детская Городская клиническая больница №27 «Айболит», МЛПУ «Детская поликлиника №49» Приокского Райздравотдела, Государственное казенное учреждение здравоохранения Нижегородской области «Нижегородский специализированный дом ребенка».
Указанные результаты подтвердились. Полученный предлагаемым способом препарат условно назван «LB-КОМПЛЕКС плюс». 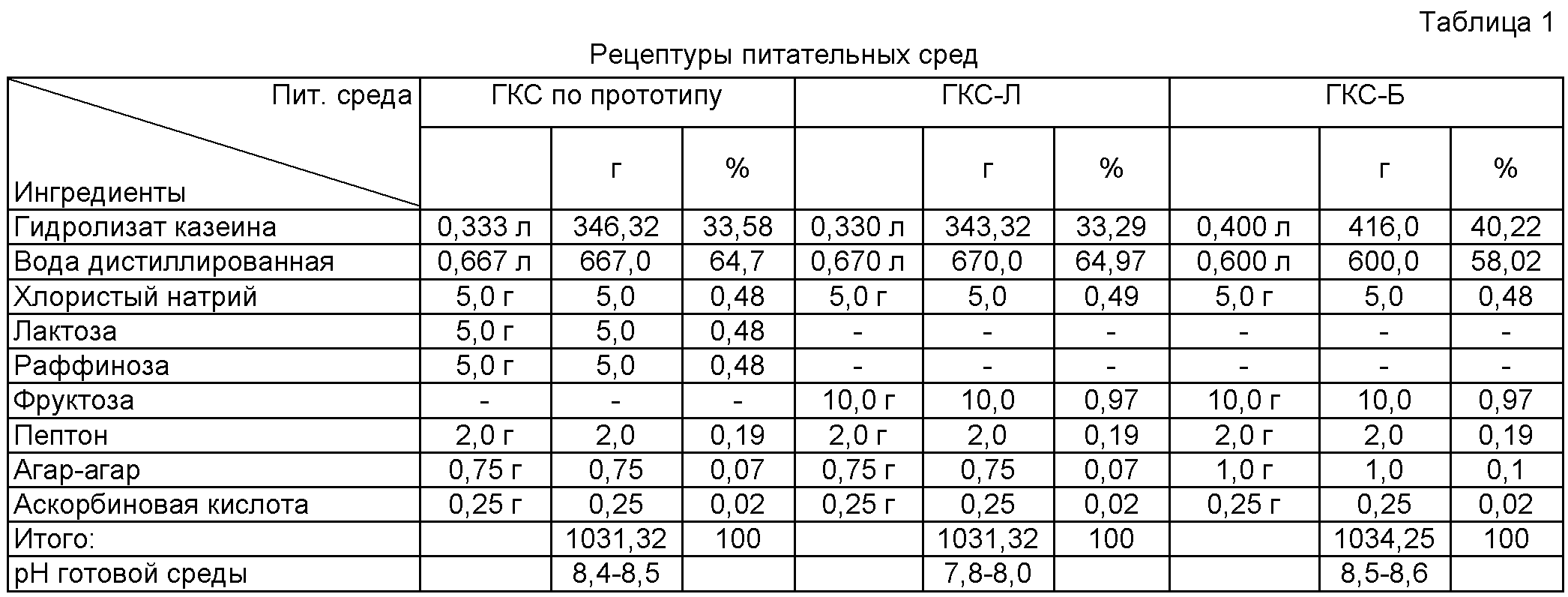
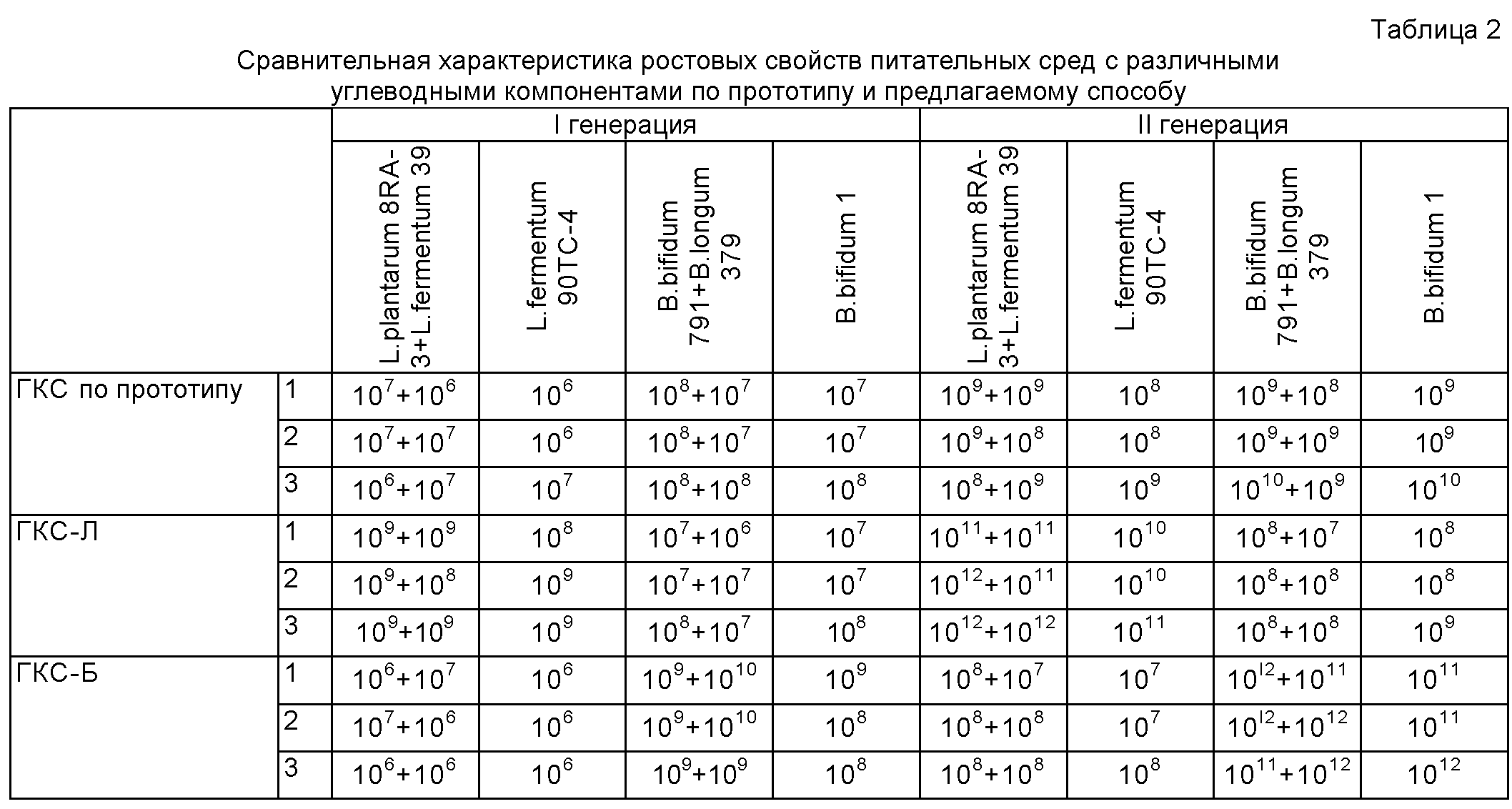
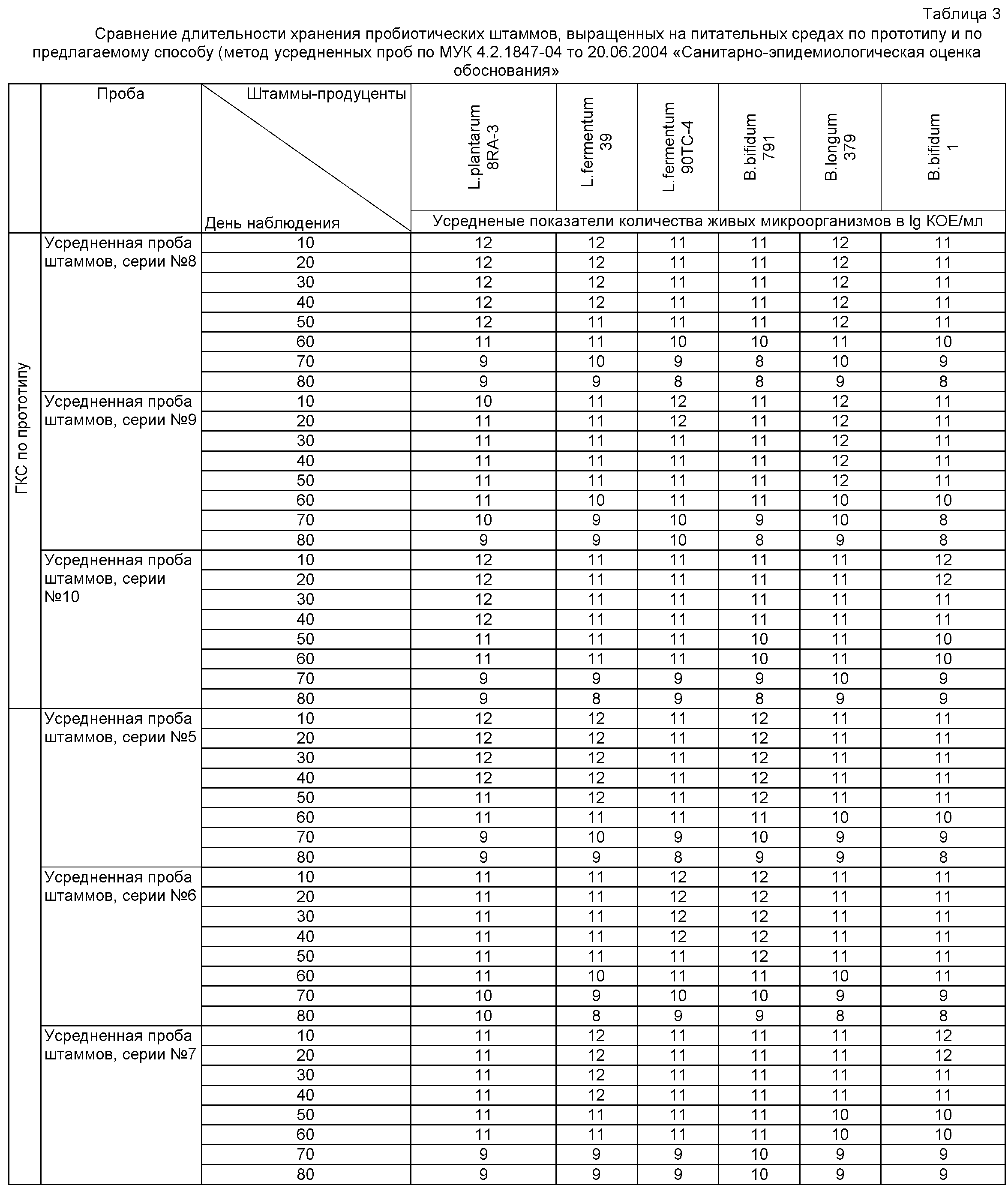
Из таблиц видно, что замена углеводной составляющей не повлияла на количество живых микробных клеток в единице объема готового пробиотика и на сохранность препарата.
Способ приготовления лечебно-профилактического препарата из живых штаммов микроорганизмов лактобацилл и бифидобактерий путем их культивирования при температуре 37±1°С на питательной среде, содержащей питательную основу: гидролизат казеина, разведенный дистиллированной водой, хлористый натрий, углеводную составляющую, пептон, агар-агар, кислую составляющую - аскорбиновую кислоту, дистиллированную воду, в качестве штаммов-продуцентов используют Lactobacillus plantarum 8 RA-3, Lactobacillus fermentum 39, Lactobacillus fermentum 90 ТС-4, Bifidobacterium bifidum 791, Bifidobacterium longum 379, Bifidobacterium bifidum 1, расфасовку жидкого препарата с учетом необходимой для пациентов суточной дозы, при этом в качестве углеводной составляющей питательных сред используют фруктозу при следующем соотношении компонентов: для культивирования лактобацилл и бифидобактерий готовят, соответственно, среду с содержанием агар-агара 0.75 и 1,0 г/л, аминного азота в разведенном дистиллированной водой гидролизате казеина 160-170 и 180-200 мг% и рН готовой среды 7.8-8.0 и 8.5-8.6, разведенные в среде для лактобацилл штаммы Lactobacillus plantarum 8 RA-3 и Lactobacillus fermentum 39 соединяют в соотношении 1:1 и совместно культивируют 24±1 ч, полученную биомассу первой генерации смешивают со свежей питательной средой в соотношении 1:1000 и продолжают культивирование в течение 24±1 ч, а штамм Lactobacillus fermentum 90 ТС-4 культивируют по тому же способу отдельно, штаммы Bifidobacterium bifidum 791 и Bifidobacterium longum 379, разведенные в питательной среде для бифидобактерий, соединяют в соотношении 1:1 и совместно культивируют 24±1 ч, полученную биомассу первой генерации смешивают со свежей питательной средой в соотношении 1:1000 и продолжают культивирование в течение 48±1 ч, а штамм Bifidobacterium bifidum 1 культивируют по тому же способу отдельно, по окончании культивирования биомассы штаммов, выращенных на различных средах, смешивают в соотношении 2:1:2:1.
