Результат интеллектуальной деятельности: СПОСОБ ЛЕЧЕНИЯ ЗАМЕДЛЕННОЙ ЭЛИМИНАЦИИ МЕТОТРЕКСАТА ПОСЛЕ ЕГО ВЫСОКОДОЗНОЙ ИНФУЗИИ ПРИ ОПУХОЛЯХ ГОЛОВНОГО МОЗГА У ДЕТЕЙ
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к онкологии и онкопедиатрии, и может быть использовано для ускорения замедленной элиминации метотрексата при лечении опухолей головного мозга у детей после его высокодозной инфузии.
Препарат с антифолатной активностью - метотрексат (MTX - methotrexate) - нарушает метаболизм фолиевой кислоты посредством конкурентного ингибирования дигидрофолатредуктазы и других ферментов. В стандартных дозах это лекарство широко используется в лечении как онкологических, так и неонкологических заболеваний (псориаза, ревматоидного артрита, системной красной волчанки, болезни Крона). Спектр опухолей, в режимах терапии которых используются различные дозы метотрексата, велик, и к ним на сегодняшний день, помимо гемобластозов, относятся такие солидные новообразования, как остеогенная саркома и опухоли головного мозга. При последних используется дозная интенсификация режимов полихимиотерапии метотрексатом.
Замедленная элиминация метотрексата из плазмы крови - редкая патология, встречающаяся в единичных случаях. Период полувыведения метотрексата составляет 6-7 часов с девиацией от 3 до 17 часов. Значительно удлиняется период выведения у пациентов с полисерозитами (плевритом, асцитом). Выведение препарата осуществляется через почки путем клубочковой фильтрации и секреции в проксимальных канальцах. Около 5-20% метотрексата и 1-5% 7-гидроксиметотрексата элиминируется через желчевыводящие пути.
Среди осложнений лечения высокодозным метотрексатом выделяют нефро-, гепато-, гастроинтестино- и миелотоксичность. Применение MTX приводит к смерти в 6% случаев, при этом 80% из них обусловлены тяжелой миелосупрессией и как следствие, сепсисом и геморрагическим синдромом, оставшиеся 20% - почечной недостаточностью. Тяжесть осложнений связана с возрастом больного: чем моложе пациент, тем переносимее токсичность, в то время как у больных старшего возраста осложнения протекают в тяжелой степени и нередко сопряжены со смертельным исходом.
Инфузия высоких доз метотрексата стала возможной после внедрения в онкологичекую практику антагониста антифолатов лейковорина (кальция фолината). В большинство лечебных программ с использованием высоких доз метотрексата включен кальция фолинат как препарат, снижающий токсичность последнего. В механизме превращения лейковорина в тетрагидрофолаты дигидрофолатредуктаза, инактивированная метотрексатом и его метаболитом, участия не принимает, поэтому процессы репарации и репликации ДНК и РНК с применением кальция фолината достаточно быстро восстанавливаются.
Дозы лейковорина варьируют от 10 мг/м2 каждые 6 ч до 1000 мг/м2 каждые 3 ч. Единого мнения о режимах введения кальция фолината нет.
Известен способ ускорения замедленной элиминации метотрексата при лечении опухолей головного мозга у детей после его высокодозной инфузии, включающий использование номограммы доз лейковорина, назначаемых после высоких доз метотрексата. (Dombrowsky E., Jayaraman В., Narayan M. and Barrett J.S. Evaluating performance of the decision support system to improve methotrexate pharmacotherapy in children and yang adults with cancer // Ther. Drug Monit. - 2011. - №1. - P. 99-107).
Данная номограмма сложна в использовании: на оси абсцисс и ординат проецируются время после инфузии (20, 40, 60 ч и т.д.) и концентрация препарата в сыворотке (10-8, 10-7, 10-6 моль) соответственно, значения которых не удобны в клинической практике. Кроме того, она не учитывает конкретный режим введения метотрексата (дозу и длительность) и морфологический вариант опухоли. Разные режимы введения препарата (доза от 0,5 г/м2 при неходжкинских лимфомах до 12 г/м2 при остеогенной саркоме, длительность от 4 ч при остеогенной саркоме до 24 ч при опухолях головного мозга и гемобластозах), а также генез и локализация опухоли уже предопределяют индивидуальный клиренс метотрексата и его метаболитов.
Техническим результатом предлагаемого изобретения является оптимизация индивидуальных доз лейковорина у детей с опухолями головного мозга, в лечении которых применяется 24-часовая инфузия метотрексата в дозе 5 г/м2 с целью уменьшения токсического воздействия на организм и предупреждения или снижения глубины и длительности различных осложнений лечения.
Указанный технический результат достигается тем, что в известном способе ускорения замедленной элиминации метотрексата при лечении опухолей головного мозга у детей после его высокодозной инфузии путем введения лейковорина, согласно изобретению, дозу лейковорина определяют через 24 часа после начала 24-часовой инфузии метотрексата и далее через каждые 6 часов в зависимости от концентрации метотрексата в сыворотке крови и времени, прошедшего от начала 24-часовой инфузии метотрексата в дозе 5 г/м2, следующим образом:
при концентрации метотрексата в сыворотке крови ≥151 µмоль/л через 24 часа после начала инфузии доза введения лейковорина составляет 100 мг/м2, через 30-42 часа - 200 мг/м2, через 48 часов и более - 2000 мг/м2;
при концентрации метотрексата 101-150 µмоль/л через 24 часа после начала инфузии лейковорин не вводят, через 30-54 часов после начала инфузии доза лейковорина составляет 200 мг/м2, через 60 часов и более - 2000 мг/м2;
при концентрации метотрексата 21-100 µмоль/л через 24 часа после начала инфузии лейковорин не вводят, через 30 часов после начала инфузии доза лейковорина составляет 15 мг/м2, через 36-66 часов - 30 мг/м2; через 72 часа и более - 200 мг/м2;
при концентрации метотрексата 4-20 µмоль/л через 24-30 часов после начала инфузии лейковорин не вводят, через 36-66 часов после начала инфузии доза лейковорина составляет 15 мг/м2, через 72 часа и более - 30 мг/м2;
при концентрации метотрексата 0,2-3,9 µмоль/л через 24-42 часа после начала инфузии лейковорин не вводят, через 48 часов и более после начала инфузии доза лейковорина составляет 15 мг/м2,
причем лейковорин вводят до тех пор, пока концентрация метотрексата в сыворотке крови не составит менее 0,2 µмоль/л.
В результате проведенных исследований были определены оптимальные дозы лейковорина, вводимые каждые 6 часов, в зависимости от концентрации метотрексата после его 24-часовой инфузии в дозе 5 г/м (см. табл.1).
|
* - после 120 ч наблюдения при замедленной элиминации метотрексата дозы лейковорина соответствуют табличным для 120 ч, препарат вводится до тех пор, пока концентрация MTX в сыворотке не составит <0,2 µмоль/л.
Материалом для составления таблицы послужили сведения о концентрации метотрексата в сыворотке крови, полученные после проведения 34 циклов химиотерапии метотрексатом высокими дозами (от 5 до 12 г/м2) у 13 больных.
Зная время, прошедшее после начала инфузии высокодозного метотрексата, и концентрацию его в сыворотке крови на данный час, можно с помощью табл.1 определить дозу лейковорина, необходимую для инактивации препарата.
Использование предлагаемого способа позволяет ускорить выведение токсических метаболитов метотрексата и самого препарата, тем самым предотвращая их побочное влияние на организм ребенка, сокращая сроки госпитализации и уменьшая риск инвалидизации больных. Сопоставительный анализ с прототипом показывает, что использование индивидуальных доз лейковорина, основанных на индивидуальных значениях «концентрация метотрексата - время», более практично в использовании и применимо у детей с опухолями головного мозга, в терапии которых использована 24-часовая инфузия метотрексата в дозе 5 г/м2.
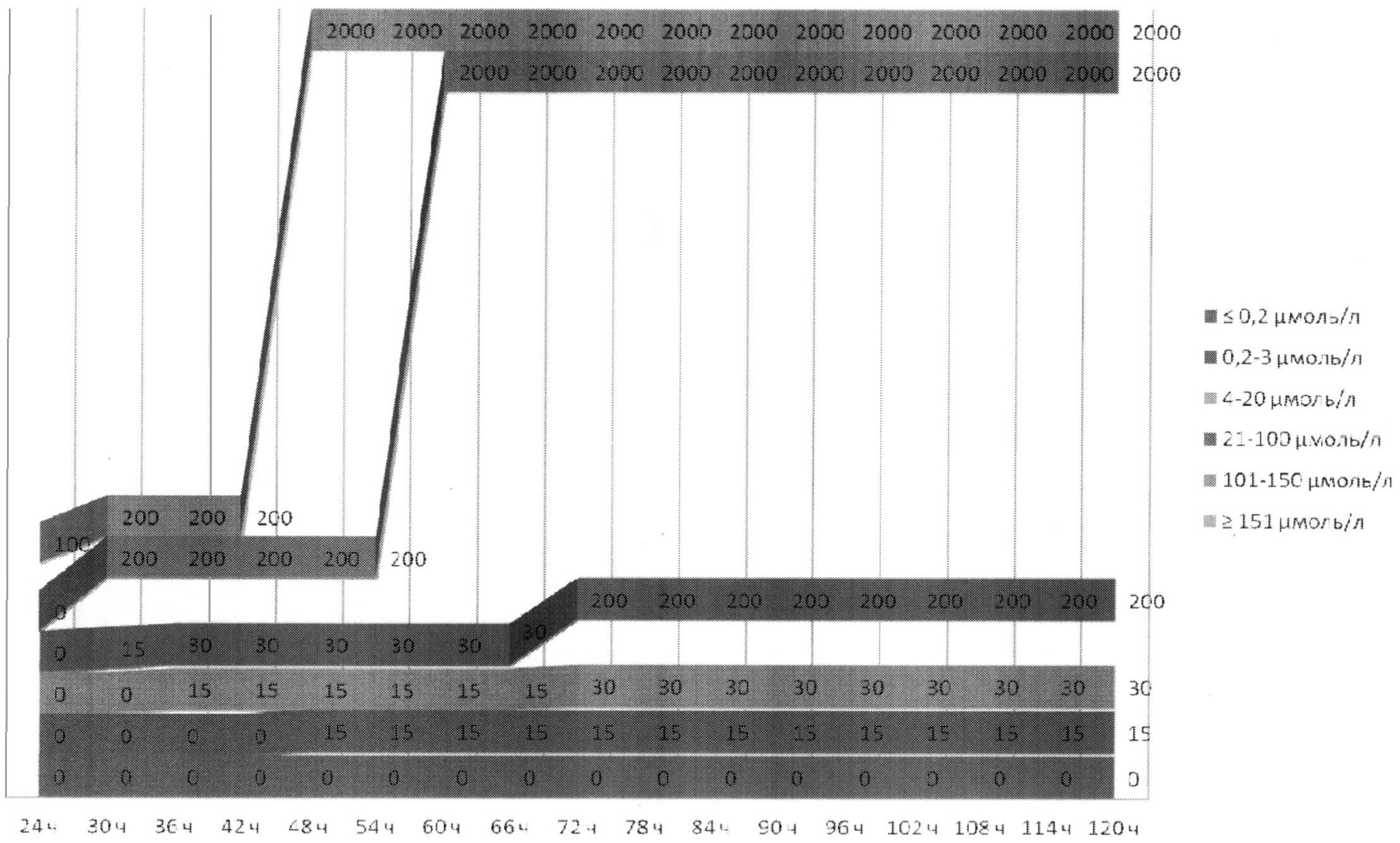
Сущность изобретения поясняется изображением на фиг., где представлена диаграмма доз лейковорина (мг/м2) при замедленной элиминации метотрексата после его 24-часовой инфузии в дозе 5 г/м2 при опухолях головного мозга, основанная на индивидуальном профиле «концентрация метотрексата - время», построенная в соответствии с табл.1, со стандартной (положительной) прямоугольной системой координат на плоскости, на которой по оси абсцисс в соответствии с выбранным масштабом проецируется время, прошедшее после начала инфузии метотрексата, начиная с 24 ч с промежутками в 6 ч; объемные горизонтальные прямоугольники представляют собой диапазоны возможных значений концентрации метотрексата в сыворотке крови больного; на ось ординат проецируется необходимая индивидуальная доза лейковорина, рассчитанная на площадь поверхности тела, вводимая каждые 6 часов.
Способ осуществляют следующим образом.
Через 24 часа после начала 24-часовой инфузии метотрексата в дозе 5 г/м2 и далее через каждые 6 часов определяют концентрацию метотрексата в сыворотке крови. По начальной концентрации метотрексата в сыворотке и времени, прошедшему от начала инфузии, в соответствии с табл.1, или по диаграмме (фиг.) определяют индивидуальные дозы лейковорина, вводимые каждые 6 или 3 часа.
Например, если через 30 ч после начала инфузии метотрексата в дозе 5 г/м2 концентрация последнего в сыворотке крови составила 105 µмоль/л, доза лейковорина по табл.1 должна быть 100 мг/м2 каждые 3 часа или 200 мг/м2, вводимая каждые 6 часов. Препарат вводят до тех пор, пока концентрация MTX в сыворотке не составит менее 0,2 µмоль/л. Если время лечения замедленной элиминации метотрексата составит более 120 часов, то дозы лейковорина соответствуют значениям для 120 часов.
Сущность изобретения иллюстрируется следующим клиническим примером.
Пример. Больной, 6 мес., получал лечение по поводу морфологически верифицированной примитивной нейроэктодермальной опухоли хиазмально-селлярной области головного мозга. После перенесенного ОРЗ мать отметила ухудшение аппетита, левосторонний птоз. По рекомендации невропатолога и окулиста выполнено МРТ головного мозга, при которой выявлено объемное образование хиазмально-селлярной области с супра-параселлярным ростом, размерами 17×21×25 мм, накапливающее контрастное вещество.
Было выполнено микрохирургическое вмешательство с использованием операционного микроскопа, интраоперационной навигации и нейрофизиологического исследования при внутримозговых новообразованиях головного мозга, остеопластическая краниотомия в левой лобной области с заходом за среднюю линию, субфронтальная ревизия основания передней и средней черепной ямки, парциальное удаление опухоли. Иммуногистохимическое исследование: Chromogranin+, CD99+, S100+, NB слабо фокально+, Synaptophysin отдельные клетки+, NSE-, GFAP-, Ki67 экспрессируют около 45% клеток.
При МРТ головного мозга сохранялась остаточная опухоль размерами 20×25 мм, МРТ шейного, грудного и пояснично-крестцового отделов позвоночника показала диффузное накопление контраста в области оболочек спинного мозга.
Уровень креатинина в сыворотке и его клиренс были в пределах референтных значений. Специфическая лекарственная терапия начата по жизненным показаниям по программе HIT-2000 (ветка MET-HIT 2000-BIS4 для примитивной нейроэктодермальной опухоли) с редукцией доз препаратов. Цикл состоял из винкристина (0,005 мг/кг) и карбоплатина (25 мг/кг) в 1-й день, вепезида (2 мг/кг) и циклофосфамида (65 мг/кг) во 2-3 дни, метотрексата (5 г/м2) в 5-й день. Расчетная доза метотрексата составила 1,8 г. Накануне, перед и во время введения МТХ проводилась инфузионная терапия глюкозо-солевыми препаратами, а также ощелачивание организма с использованием 5% раствора соды (NaHCO4). Инфузия, согласно протоколу, продолжалась 24 часа. Водный баланс был адекватным, почасовой диурез составлял 1,6-2,0 мл/кг/ч без диуретиков. При контрольном анализе через 24 ч отмечена высокая концентрация МТХ в сыворотке крови (522 µмоль/л), доза лейковорина рассчитывалась по табл.1.
В табл.2 представлены индивидуальные значения доз лейковорина для данного больного в зависимости от концентраций метотрексата в сыворотке крови и времени от начала инфузии метотрексата.
|
Мониторинг сывороточного метотрексата проводился до его значений менее 0,5 µмоль/л. При достижении данного уровня лейковорин вводился еще 11 раз каждые 6 ч в дозе 15 мг/м2.
При использовании предлагаемого способа, основанного на индивидуальных значениях «концентрация метотрексата-время», был осуществлен подбор доз лейковорина для конкретного пациента с опухолью головного мозга, удалось полностью элиминировать метотрексат и его продукты метаболизма.
Предлагаемый способ ускорения замедленной элиминации метотрексата при лечении опухолей головного мозга у детей после его высокодозной инфузии был использован после 11 циклов химиотерапии с 24-часовой инфузией метотрексата в дозе 5 г/м2 у 4 больных с опухолями головного мозга.
Изобретение позволяет выбрать оптимальные индивидуальные дозы лейковорина у детей с опухолями головного мозга, в лечении которых применяется 24-часовая инфузия метотрексата в дозе 5 г/м2, тем самым уменьшая токсическое воздействие на организм, предупреждая и снижая различные осложнения лечения.
Способ ускорения замедленной элиминации метотрексата при лечении опухолей головного мозга у детей после его высокодозной инфузии путем введения лейковорина, отличающийся тем, что дозу лейковорина определяют через 24 часа после начала 24-часовой инфузии метотрексата и далее через каждые 6 часов в зависимости от концентрации метотрексата в сыворотке крови и времени, прошедшего от начала 24-часовой инфузии метотрексата в дозе 5 г/м, следующим образом:при концентрации метотрексата в сыворотке крови ≥151 µмоль/л через 24 часа после начала инфузии доза введения лейковорина составляет 100 мг/м, через 30-42 часа - 200 мг/м, через 48 часов и более - 2000 мг/м;при концентрации метотрексата 101-150 µмоль/л через 24 часа после начала инфузии лейковорин не вводят, через 30-54 часов после начала инфузии доза лейковорина составляет 200 мг/м, через 60 часов и более - 2000 мг/м;при концентрации метотрексата 21-100 µмоль/л через 24 часа после начала инфузии лейковорин не вводят, через 30 часов после начала инфузии доза лейковорина составляет 15 мг/м, через 36-66 часов - 30 мг/м; через 72 часа и более - 200 мг/м;при концентрации метотрексата 4-20 µмоль/л через 24-30 часов после начала инфузии лейковорин не вводят, через 36-66 часов после начала инфузии доза лейковорина составляет 15 мг/м, через 72 часа и более - 30 мг/м;при концентрации метотрексата 0,2-3,9 µмоль/л через 24-42 часа после начала инфузии лейковорин не вводят, через 48 часов и более после начала инфузии доза лейковорина составляет 15 мг/м,причем лейковорин вводят до тех пор, пока концентрация метотрексата в сыворотке крови не составит менее 0,2 µмоль/л.