Результат интеллектуальной деятельности: СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА РАЗВИТИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к кардиологии, в частности к способам прогнозирования развития наджелудочковых нарушений сердечного ритма (НСР), а именно фибрилляции предсердий (ФП).
Аналогом предлагаемого решения является способ прогнозирования развития пароксизмов ФП, заключающийся в определении ширины и амплитуды зубца Р электрокардиограммы (ЭКГ), причем при выявлении зубца Р более 0,12 с и (или) амплитудой более 2,5 мм прогнозируется развитие пароксизмов этих аритмий в течение нескольких лет после первого обследования (Кушаковский М.С. Аритмии сердца: руководство для врачей / М.С.Кушаковский. - 3-е изд., испр. и доп.- СПб.: Фолиант, 2004. - 672 с.).
По наиболее близкой технической сущности в качестве прототипа выбран способ определения риска развития пароксизмов ФП, заключающийся в определении размера или объема правого и или левого предсердий, причем при дилатации предсердий более 4,0 см определяется риск развития этой аритмии в течение 1-3 лет и более после первого обследования (Кушаковский М.С. Аритмии сердца: руководство для врачей / М.С.Кушаковский. - 3-е изд., испр. и доп. - СПб.: Фолиант, 2004. - 672 с.).
Недостатком аналога и прототипа является недостаточная точность определения риска развития ФП.
Техническим результатом изобретения является повышение точности определения риска развития ФП после первого обследования.
Технический результат изобретения достигается тем, что больному проводят ЭКГ исследование, регистрацию сигнал-усредненной ЭКГ и чреспищеводную электрокардиостимуляцию (ЧПЭКС), затем определяют продолжительность фильтрованной волны «Р» (FiP-P) сигнал-усредненной ЭКГ, дисперсию зубца «Р» (Pd), частотный порог индуцирования аритмии (ЧПИА) и ее продолжительность с помощью ЧПЭКС и риск развития ФП определяют по формуле: РРФП=(FiP-P/Pd)×(ЧПИА/А), где РРФП - риск развития ФП, FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ в мс, Pd - дисперсия зубца «Р» в мс, определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирования аритмии, определяемый как произведение количества стимулов при проведении ЧПЭКС на длительность стимуляции в минутах, А - продолжительность индуцированной аритмии в минутах, причем при значениях РРФП до 0,5 определяют высокий (в течение 1-3 месяцев), от 0,5 до 1,5 - средний (от 3 месяцев до 1 года), более 1,5 - низкий (более 1 года) риск развития ФП после первого обследования пациента.
Способ осуществляется следующим образом.
Больному проводят ЭКГ исследование, регистрацию сигнал-усредненной ЭКГ и ЧПЭКС. Затем определяют Pd по стандартной ЭКГ, зарегистрированной в 12 отведениях, продолжительность фильтрованной волны «Р» (FiP-P) сигнал-усредненной ЭКГ, ЧПИА и продолжительность аритмии с помощью ЧПЭКС. Затем риск развития ФП определяют по формуле:
РРФП=(FiP-P/Pd)×(ЧПИА/А), где РРФП - риск развития ФП, FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс), Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирования аритмии, определяемый как произведение количества стимулов при проведении ЧПЭКС на длительность стимуляции (в минутах), А - продолжительность индуцированной аритмии (в минутах), причем при значениях РРФП до 0,5 определяют высокий (в течение 1-3 месяцев), от 0,5 до 1,5 - средний (от 3 месяцев до 1 года), более 1,5 - низкий (более 1 года) риск развития ФП после первого обследования пациента.
Существенные отличительные признаки заявляемого способа и причинно-следственная связь между ними и достигаемым результатом:
- определяют продолжительность фильтрованной волны «Р» (FiP-P) сигнал-усредненной ЭКГ, дисперсию зубца «Р» (Pd), частотный порог индуцирования аритмии (ЧПИА) и ее продолжительность с помощью ЧПЭКС;
- риск развития фибрилляции предсердий (РРФП) определяют по формуле: РРФП=(FiP-P/Pd)×(ЧПИА/А), где РРФП - риск развития ФП, FiP-P -продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ в мс, Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирования аритмии, определяемый как произведения количества стимулов при проведении ЧПЭКС на длительность стимуляции (в минутах), А - продолжительность индуцированной аритмии (в минутах);
- при значениях РРФП до 0,5 прогнозируют высокий (в течение 1-3 месяцев), от 0,5 до 1,5 - средний (от 3 месяцев до 1 года), более 1,5 - низкий (более 1 года) риск развития ФП после первого обследования пациента.
В настоящее время известно, что при регистрации возбуждения по миокарду предсердий или желудочков проведение возбуждения (ПВ) подчиняется закону “стока” от одного кардиомиоцита к другому (Физиология и патофизиология сердца: Т. 1.: пер. с англ. - Под. ред. Н.Сперелаксиса. - М.: Медицина, 1990., Olshansky В., Okumura К., Hess P.O., Waldo A.L. Demonstration of the area of slow conduction in human atrial flytter. // J. Amer. Coll. Cardiol. -1991. - Vol.16, N. 6. - P. 1639 - 1648., Shimisu A., Nosaki A., Rudy Y., Waldo A.L. Multiplexing studies of effects of rapid atrial pacing on the area of slow conduction during atrial flutter in canine pericarditis model. // Circulation. - 1991. -Vol.83, N. 3. - P.983-994.). Поэтому путем прямого наложения электродов на миокард регистрируют характер и направление проведения возбуждения по сердечной мышце. Кроме того, миокард предсердий является тканью с быстрым ответом, т.е. для мембранного потенциала сократительных волокон предсердий характерны быстрая деполяризация (Физиология и патофизиология сердца: Т. 1.: пер. с англ. - Под. ред. Н.Сперелаксиса. - М.: Медицина, 1990).
Наличие наджелудочковых аритмий, обусловлено тем, что отмечается замедление и неравномерное проведение возбуждения в верхних и средних отделах предсердий, что отражает дисперсию возбудимости миокарда предсердий (Бокерия Л.А. Лекции по кардиологии / Л.А.Бокерия, Е.З.Голухова. - М., 2002. - 296 с., Braunwald's Heart Disease: a textbook of cardiovascular medicine / Ed. by P.Libby et al. - Phyladelfhia, W.B. Saunders Company, 2007. -2183р.), причем у этих больных нарушение предсердной проводимости отмечается задолго до увеличения предсердий и других предикторов развития ФП (Шабров А.В., Олесин А.И., Голуб Я.В., Голуб В.И. Клиническая оценка использования неинвазивного метода определения внутри- и межпредсердной проводимости у больных ишемической болезнью сердца. // Тер. архив.-1999.-№1. - С.34-39). Одним из методов, выявляющих наличие дисперсии возбудимости миокарда предсердий, является регистрация сигнал-усредненной ЭКГ и Pd, а также индуцирование ФП с помощью ЧПЭКС (Олесин А.И., Шабров А.В., Разумова Т.В., Александров B.C. Использование различных режимов кардиостимуляции для выбора противорецидивной терапии пароксизмов мерцания и трепетания предсердий у больных ишемической болезнью. // Тер. архив. - 2000. - №11. - С.39-43, Braunwald's Heart Disease: a textbook of cardiovascular medicine / Ed. by P.Libby et al. - Phyladelfhia, W.B. Saunders Company, 2007. - 2183р.).
В предлагаемом способе предполагается, что наличие дисперсии проведения возбуждения, выявляемой по данным сигнал-усредненной ЭКГ и Pd, свидетельствует о возможном развитии циркуляции возбуждения (reentry) в миокарде предсердий или вокруг анатомического препятствия, например, при движении волны вокруг полых или легочных вен. Индуцирование ФП с помощью ЧПЭКС отражает возможность развития этой аритмии за счет различных тригерных механизмов (Braunwald's Heart Disease: a textbook of cardiovascular medicine / Ed. by P.Libby et al. - Phyladelfhia, W.B. Saunders Company, 2007. - 2183р.) Следует отметить, что после формирования фронта волны возбуждения она фракционируется, разделяется на дочерние волны, каждая из которых становится независимой, причем при разделении более крупной волны в локальном участке блокированного проведения либо при активном движении по направлению к другому предсердию может формироваться критическое число блуждающих волн, необходимых для формирования ФП, причем формирование этих волн является случайным или «хаотическим» процессом (Allessie M.A., Rensma P.L., Brugada J. et al. Pathophysiology ofatrial fibrillation.// Cardiac electrophysiology. From cell to bedside. - Eds. Zipes D.P., Jalife J. - Philadelphia: W.B. Saunders, 1990. - P.548-559, Allessie M.A., Konings K., Kirchhof C. Mapping of atrial fibrillation. In: Ollson S.B., Allesie M.A., Campbel R.W.F., eds. Atrial fibrillation: mechanism and therapeutic strategies. Armonk NY: Futura Publishing Company, 1994. - P.37-49). Кроме того, для формирования пароксизма ФП необходимо наличие 3 и более волн рециркуляции, а если число движущихся волн понижается менее 3 - аритмия прекращается, чем и определяется продолжительность, в том числе индуцированной, этой аритмии (Allessie M.A., Konings К., Kirchhof С.Mapping of atrial fibrillation. In: Ollson S.B., Allesie M.A., Campbel R.W.F., eds. Atrial fibrillation: mechanism and therapeutic strategies. Armonk NY: Futura Publishing Company, 1994. - P.37-49). Поэтому РРФП является независимым предиктором развития ФП, определяемого путем комплексной оценки предикторов развития ФП, в том числе определение возможности ее индуцирования.
Совокупность отличительных существенных признаков является новой и позволяет повысить точность определения риска развития фибрилляции предсердий.
Для иллюстрации заявляемого способа приводим примеры из клинической практики.
Пример 1.
ИБ №1258. Больной А., 69 лет, поступил в дневной стационар 12.07.2011 г. по направлению участкового врача по поводу ИБС: стенокардии, периодических приступов сердцебиения. Из анамнеза известно, что больной страдает ИБС: стенокардией II функционального класса в течение последних 4-5 лет. Постоянно принимает предуктал MB, аспирин в дозе 300-400 мг в сутки, метопролол в дозе 25-50 мг в сутки. В последние 3-4 месяца стал отмечать появление перебоев в работе сердца. При суточном мониторировании ЭКГ, выполненном амбулаторно 10.12.2004 г., была выявлена одиночная желудочковая экстрасистолия с частотой до 2 экстрасистол в час.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: стабильная стенокардия напряжения II функционального класса, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была продолжена терапия предукталом MB, аспирином в дозе 300 мг в сутки, эналоприлом (эднит) в дозе 5 мг в сутки.
На второй день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях, сигнал-усредненная ЭКГ на протяжении 5 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г.Иванове). Затем после компьютерной обработки была определена FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс) и Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ. У больного А., 69 лет FiP-P и Pd составили 135 мс и 65 мс соответственно. Больному была индуцирована ФП методом залповой сверхчастой стимуляции с помощью ЧПЭКС, причем ЧПИА составил 3 имп/мин (была проведена стимуляция 30 стимулами продолжительностью 6 сек (0,1 мин), причем ЧПИА был рассчитан как произведение 30 стимулов на 0,1 мин, что составило 3 имп/мин). Аритмия купировалась самостоятельно через 23 минуты. Следует отметить, что при ЧПЭКС показатели, отражающие функцию синусового узла, такие как время восстановления функции синусового узла, корригированное время восстановления функции синусового узла, время синоатриального проведения, определенные по общепринятой методике (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993), не выходили за пределы колебаний нормальных величин. Затем был рассчитан РРФП, определяемый по формуле: РРФП=(FiP-P/Pd)×(ЧПИА/А),
где РРФП - риск развития ФП, FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс), Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирования аритмии, определяемый как произведение количества стимулов при проведении ЧПЭКС на длительность стимуляции (в минутах), А - продолжительность индуцированной аритмии (в минутах),
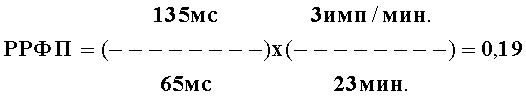
В последующем больному была проведена терапия предукталом, аспирином, ренитеком (эналаприлом) в дозах, указанных выше. Противоаритмические препараты не назначались. Спонтанные приступы ФП длительностью от 20 секунд до 35 минут были выявлены при суточном мониторировании ЭКГ, проведенным через день после вышеуказанного обследования.
Данный пример иллюстрирует, что при выявлении значений РРФП 0,19 определяют высокий риск развития ФП, то есть в течение 2 суток после первого обследования.
Пример 2.
ИБ №1244. Больной С., 56 лет поступил в стационар 21.09.2010 г.по направлению врача скорой помощи по поводу ИБС: прогрессирующей стенокардии. Из анамнеза известно, что больной страдает ИБС: стенокардией II функционального класса в течение последних 3 лет. Постоянно принимает нитросорбид, антиагреганты. За два дня до госпитализации у больного усилились ангинозные боли по частоте, длительности, интенсивности, а также изменился характер болевого синдрома. Госпитализация в стационар.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: прогрессирующая стенокардия, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была продолжена терапия нитросорбидом в дозе 30 мг в сутки, аспирином в дозе 300 мг в сутки, ренитеком в дозе 5 мг в сутки, поляризующей смесью с нитроглицерином.
На третий день пребывания больного в стационаре характер ангинозных болей стабилизировался.
На третий день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 40 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г.Иваново). Затем после компьютерной обработки была определена FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс) и Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ. У больного С., 56 лет FiP-P и Pd составили 132 мс и 53 мс соответственно.
У больного С., 56 лет прогнозировалось развитие ФП. Больному было индуцировано ФП методом залповой сверхчастой стимуляции с помощью ЧПЭКС, причем ЧПИА составил 4 имп/мин. Аритмия купировалась самостоятельно через 15 минут. Следует отметить, что при ЧПЭКС показатели, отражающие функцию синусового узла, такие как время восстановления функции синусового узла, корригированное время восстановления функции синусового узла, время синоатриального проведения, определенные по общепринятой методике (Кушаковский М.С. Аритмии сердца. - Л.: Медицина,1993), не выходили за пределы колебаний нормальных величин. Затем был рассчитан РРФП, определяемый по формуле:
РРФП=(FiP-P/Pd)×(ЧПИА/А),
где РРФП - риск развития ФП, FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс), Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирования аритмии, определяемый как произведение количества стимулов при проведении ЧПЭКС на длительность стимуляции (в минутах), А - продолжительность индуцированной аритмии (в минутах),
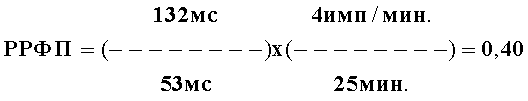
В последующем больному была проведена терапия нитратами, аспирином в дозах, указанных выше. Противоаритмические препараты не назначались.
Спонтанные приступы ФП длительностью от 15 секунд до 10-25 минут были выявлены при суточном мониторировании ЭКГ через 1,5 месяца после вышеуказанного обследования, причем при проведении ЧПЭКС в этот же период (через 3 недели после первой стимуляции) ЧПИА составил 2,6 имп/мин.
Данный пример иллюстрирует, что при выявлении значений РРФП 0,40 определяют высокий риск развития ФП, то есть в течение 1,5 месяцев после первого обследования.
Пример 3.
ИБ №269. Больной О., 60 лет поступил в стационар 21.01.2010 г. по направлению врача поликлиники по поводу ИБС: впервые возникшей стенокардии. Из анамнеза известно, что больной ранее считал себя практически здоровым.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: впервые возникшая стенокардия, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была начата терапия оликардом в дозе 40 мг в сутки, аспирином в дозе 300 мг в сутки, зоокором 20 мг в сутки, поляризующей смесью с нитроглицерином.
На третий день пребывания больного в стационаре характер ангинозные боли купировались и в дальнейшем не рецидивировали.
На третий день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 35 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г.Иваново). Затем после компьютерной обработки была определена FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс) и Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ. У больного С., 56 лет FiP-P и Pd составили 122 мс и 61 мс соответственно.
У больного О., 68 лет прогнозировалось развитие ФП. Больному было индуцировано ФП методом залповой сверхчастой стимуляции с помощью ЧПЭКС, причем ЧПИА составил 6 имп/мин. Аритмия купировалась самостоятельно через 10 минут. Следует отметить, что при ЧПЭКС показатели, отражающие функцию синусового узла, такие как время восстановления функции синусового узла, корригированное время восстановления функции синусового узла, время синоатриального проведения, определенные по общепринятой методике (Кушаковский М.С. Аритмии сердца. - Л.: Медицина,1993), не выходили за пределы колебаний нормальных величин.
Затем был рассчитан РРФП, определяемый по формуле:
РРФП=(FiP-P/Pd×(ЧПИА/А),
где РРФП - риск развития ФП, FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс), Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирована аритмии, определяемый как произведение количества стимулов при проведении ЧПЭКС на длительность стимуляции (в минутах), А - продолжительность индуцированной аритмии (в минутах),
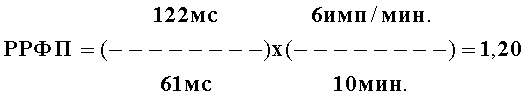
В последующем больному была проведена терапия нитратами, аспирином, зоокором в дозах, указанных выше. Противоаритмические препараты не назначались.
При последующем наблюдении в течение года, включающего проведения суточного мониторирования ЭКГ один раз в 3 месяца, неустойчивые пароксизмы ФП длительностью от 15 секунд до 5 минут были выявлены в течение 7 месяца после первого обследования.
Данный пример иллюстрирует, что при выявлении значений РРФП 1,20 определяют средний риск развития ФП, то есть в течение 7 месяцев после первого обследования.
Пример 4.
ИБ №97. Больной К., 68 лет, поступил в стационар 11.01.2010 г.по направлению участкового врача по поводу ИБС: стенокардии, периодических приступов сердцебиения. Из анамнеза известно, что больной страдает ИБС: стенокардией II функционального класса в течение последних 6 лет. Постоянно принимает моночинкве в дозе 50 мг в сутки, аспирин в дозе 300-400 мг в сутки, эналаприл (ренитек) в дозе 20 мг в сутки. В последние 3-4 месяца стал отмечать появление перебоев в работе сердца. При суточном мониторировании ЭКГ, выполненном амбулаторно 10.12.2009 г., была выявлена одиночная ПЭ с частотой до 1 экстрасистолы в час.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: стабильная стенокардия напряжения II функционального класса, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была продолжена терапия моночинкве в дозе 50 мг в сутки, аспирином в дозе 300-400 мг в сутки, эналаприлом (ренитек) в дозе 20 мг в сутки.
На второй день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 25 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г.Иваново). Затем после компьютерной обработки была определена FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс) и Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ. У больного С., 56 лет FiP-P и Pd составили 121 мс и 43 мс соответственно.
Больному было индуцировано ФП методом залповой сверхчастой стимуляции с помощью ЧПЭКС, причем ЧПИА составил 17,5 имп/мин. Аритмия купировалась самостоятельно через 12 минут. Следует отметить, что при ЧПЭКС показатели, отражающие функцию синусового узла, такие как время восстановления функции синусового узла, корригированное время восстановления функции синусового узла, время синоатриального проведения, определенные по общепринятой методике (Кушаковский М.С. Аритмии сердца. - Л.: Медицина,1993), не выходили за пределы колебаний нормальных величин.
Затем был рассчитан РРФП, определяемый по формуле:
РРФП=(FiP-P/Pd)×(ЧПИА/А),
где РРФП - риск развития ФП, FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ (в мс), Pd - дисперсия зубца «Р» (в мс), определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирования аритмии, определяемый как произведение количества стимулов при проведении ЧПЭКС на длительность стимуляции (в минутах), А - продолжительность индуцированной аритмии (в минутах),
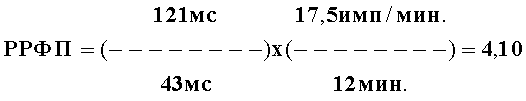
В последующем больному была проведена терапия нитратами, аспирином, ренитеком (эналоприлом) в дозах, указанных выше. Противоаритмические препараты не назначались. Спонтанный приступ ФП развился через 1,5 года после обследования, купированный сублингвальным приемом метопролола в дозе 50 мг. В качестве противорецидивной терапии пароксизмов ФП больному дополнительно к проводимой терапии был назначен метопролол в дозе 100 мг в сутки. Аритмия не рецидивировала на протяжении 2 лет.
Данный пример иллюстрирует, что при выявлении значений РРФП 4,10 определяют низкий риск развития ФП, то есть в течение 1,5 лет после первого обследования.
Наблюдалось 212 больных ИБС. Всем больным проводилась терапия нитратами пролонгированного действия, антиагрегантами, ингибиторами ангиотензинпревращающего фермента (ренитек, эналоприл, энап). Антиаритмические препараты не назначались. У всех больных определение РРФП проводилось по предлагаемому способу и согласно прототипу.
Статистический анализ полученных результатов проведен на ЭВМ. Сопоставление точности прогнозирования развития ФП у обследованных больных, определенному по предлагаемому способу в зависимости от значений РРФП и согласно прототипу представлено в таблице 1.
|
У 50 (23,58%) больных по заявляемому способу значения РРФП составили <0,5 (в среднем 0,2±0,06) (у этих больных прогнозировалось развитие ФП в течение 1-3 месяцев после первого обследования) (I группа), у 90 (42,45%) - от 0,5 до 1,5 (в среднем 0,8±0,01) (у этих больных прогнозировалось развитие ФП в течение от 3 месяцев до 1 года после первого обследования) (II группа), а у остальных 72 больных (33,96%) >1,5 (в среднем 3,2±0,2) (у этих больных прогнозировалось развитие ФП в течение более чем 1 года после первого обследования) (III группа).
Развитие ФП наблюдалось у 45 из 50 (90,00%) больных I группы в течение 1-3 месяцев после первого обследования, у 80 из 90 (88,89%) больных II группы в течение от 3 месяцев до 1 года после первого обследования и у 25 из 72 (34,72%) больных III группы более чем 1 год после первого обследования.
У 115 (54,25%) из всех обследованных пациентов, то есть из 212, согласно прототипу определялся РРФП в течение 1-3 лет после обследования. У 5 (2,36%), 45 (21,23%) и 65 (30,66%) больных согласно прототипу определялся РРФП у пациентов I, II и III группы соответственно.
Развитие ФП при использовании прототипа не наблюдалось ни у одного больного из 5 I группы - в течение 1-3 месяцев после первого обследования, точность определения РРФП составляет 0,00%; у 5 больных из 45 II группы - в течение от 3 месяцев до 1 года после первого обследования, точность определения РРФП - 11,11% и у 15 из 65 больных III группы - более чем 1 год после первого обследования, точность определения РРФП - 23,08%.
Сравнительные данные по заявляемому способу и способу прототипу представлены в таблицах 2-5.
|
|
|
|
Примечание: А - прогнозируемый, Б - реальный результат развития ФП, ΔM - точность определения РРФП в сравнении с прототипом.
Точность способа определения РРФП по заявляемому способу по сравнению с прототипом в течение 1-3 месяцев после первого обследования повышается практически на 100,00% в течение от 3 месяцев до 1 года - на 1600,00% и более чем 1 года - на 66,47%, что обеспечит своевременное назначение адекватной терапии.
Способ определения риска развития фибрилляции предсердий (ФП) путем проведения электрокардиографического (ЭКГ) исследования, сигнал-усредненной ЭКГ и чреспищеводной электрокардиостимуляции (ЧПЭКС), отличающийся тем, что определяют продолжительность фильтрованной волны «Р» (FiP-P) сигнал-усредненной ЭКГ, дисперсию зубца «Р» (Pd), частотный порог индуцирования аритмии (ЧПИА) и ее продолжительность с помощью ЧПЭКС и риск развития ФП определяют по формуле:РРФП=(FiP-P/Pd)×(ЧПИА/А),где РРФП - риск развития ФП, FiP-P - продолжительность фильтрованной волны «Р» сигнал-усредненной ЭКГ в мс, Pd - дисперсия зубца «Р» в мс, определяемая как разница между максимальными и минимальными значениями продолжительности зубца «Р» при регистрации 12 отведений стандартной ЭКГ, ЧПИА - частотный порог индуцирования аритмии, определяемый как произведения количества стимулов при проведении ЧПЭКС на длительность стимуляции в минутах, А - продолжительность индуцированной аритмии в минутах,и при значениях РРФП до 0,5 определяют высокий РРФП, в течение 1-3 месяцев, от 0,5 до 1,5 - средний, от 3 месяцев до 1 года, более 1,5 - низкий, более 1 года, после первого обследования пациента.
