Результат интеллектуальной деятельности: КОРМОВАЯ БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА ДЛЯ МОЛОДНЯКА СВИНЕЙ
Вид РИД
Изобретение
Изобретение относится к кормопроизводству, в частности получению кормовых добавок, нормализующих обмен веществ и повышающих неспецифическую резистентность организма у животных.
Известна кормовая добавка «Витапептид» для животных (Телишевская Л.Я., Демидова С.С., Богаутдинов З.Ф. Патент на изобретение РФ №2133097, 1999 г.), для получения которой используется коллагенсодержащее сырье мясоперерабатывающих предприятий (свиная шкурка, говяжья жилка, мясные зачистки и мясная крошка). Однако технологический процесс приготовления данной кормовой добавки сложный и дорогостоящий, так как включает такие этапы, как измельчение исходного сырья до размера частиц 0,8-2,0 см, суспендирование сырья деминерализованной водой в определенном режиме, ферментативный гидролиз с необходимой рН, кипячение продуктов гидролиза, отделение жира и примесей, концентрирование смеси до содержания в ней сухих веществ 25-35%, сушку.
Известна кормовая добавка для животных (Лисицын А.Б., Сницарь А.И., Стекольников Л.И., Евстафьев В.В. Патент на изобретение РФ №2115330, 1998 г.), которая состоит из отходов пивоваренного производства в виде пивной дробины и отходов мясоперерабатывающей промышленности в виде мясокостной или костной муки и крови убойных животных. Однако включение в состав данной добавки таких дорогостоящих компонентов, как мясокостная и костная мука, значительно повышают ее стоимость. При этом скармливание этой кормовой добавки не оказывает стимулирующего влияния на неспецифические факторы защиты организма животных.
Существует кормовая добавка (Терехов В.И., Тельнов С.Н., Марков А.Н. Патент на изобретение №2186497, 2002 г.), которая включает кислотный гидролизат, полученный из крови убойных животных, молочную и бензойную кислоты при следующем соотношении компонентов (масс.%): молочная кислота 0,3-0,4; бензойная кислота 0,04-0,05; кислотный гидролизат крови - остальное. Недостатком этой кормовой добавки являются большие затраты, необходимые на использование специального оборудования и квалифицированного обеспечения при получении кислотного гидролизата.
В качестве прототипа выбрана кормовая биологически активная добавка для поросят (Снегирев Ф.Ф. Ученые записки Таврического национального университета им. В.В.Вернадского. Серия «Биология, химия», - Т.19 (58), 2006, - №3, - С.71-75). Данная кормовая биологически активная добавка представляет собой отходы биологической промышленности, которые получают после культивирования клеток при производстве вакцин в технических условиях биофабрик. Она содержит комплекс аминокислот, минеральных и витаминных компонентов, а также биологические продукты жизнедеятельности культивируемых клеток, которые выполняют роль естественных биостимуляторов.
Несмотря на безусловную эффективность кормовой биологически активной добавки, взятой за прототип, ее недостатком является то, что она имеет слабо выраженные иммуностимулирующие и антиоксидантные свойства.
Технической задачей изобретения является получение новой комплексной кормовой биологически активной добавки для молодняка свиней, обладающей метаболизирующим, иммуностимулирующим и антиоксидантными свойствами.
Решение технической задачи достигается тем, что для получения кормовой биологически активной добавки используются отходы культурального производства, полученные после культивирования клеток, в которые вносят янтарную кислоту, нуклеинат натрия и органический селен в форме препарата Сел-Плекс. При следующем соотношении компонентов, масс.%: янтарная кислота - 18.0-20.0; нуклеинат натрия - 25,0-30,0; препарат Сел-Плекс - 0,25-0,30; отходы культурального производства остальное. Все указанные компоненты безвредные и физиологически совместимые.
Отходы культурального производства получают после культивирования клеток млекопитающих в дисперсионной (питательной) среде содержащей комплекс аминокислот, минеральных веществ, углеводов, витаминов. В качестве дисперсионных сред применяют среды Игла, Эрла, Хэнкса, Тироде, Дюльбекко, среду 199. Данные среды используют отдельно или в виде их смесей в различных сочетаниях. После культивирования клеток в отходах все компоненты сред остаются практически в том же количестве и соотношениях. При этом в процессе культивирования клетки млекопитающих выделяют в окружающую среду продукты своей жизнедеятельности, многие из которых являются естественными биостимуляторами и при введении в организм животных оказывают положительное действие на обмен веществ и неспецифические факторы защиты организма. Например, на Курской биофабрике культуральные отходы получают при производстве вакцины Марека. При этом в качестве дисперсионной среды используется смесь сред Игла и 199, с добавлением сыворотки крови крупного рогатого скота.
Биохимический анализ компонентов, входящих в состав отходов, полученных после культивирования клеток при производстве вакцины Марека, показал, что в их состав входят: альбумины - 52,0%, альфа-глобулины - 20,0%, бета-глобулины - 18,0%, гамма-глобулины - 10,0%, лизин-13 5,7 мг/л, гистидин - 67,8 мг/л, аргинин - 158,4 мг/л, аспарагиновая кислота - 73,4 мг/л, треонин - 111,8 мг/л, серин - 63,7 мг/л, глютаминовая кислота - 144,8 мг/л, пролин - 53,2 мг/л, глицин - 88,5 мг/л, аланин - 74,7 мг/л, валин - 98,8 мг/л, метионин - 63,3 мг/л, изолейцин - 105, 6 мг/л, лейцин - 208,7 мг/л, тирозин - 103,0 мг/л, фенилаланин - 107,7 мг/л, кальций - 388,4 мг/л, фосфор - 225,6 мг/л, магний - 199,4 мг/л, хлориды - 955,7 мг/л, калий - 108,3 мг/л, натрий - 211,8 мг/л, глюкоза - 1988,0 мг/л, пиридоксин - 1,47 мг/л, ретинол - 0,48 мг/л, тиамин - 0,12 мг/л, кальциферол - 2,05 мг/л, аскорбиновая кислота - 1,88 мг/л, рибофлавин - 0,97 мг/л, пантотеновая кислота - 1,17 мг/л.
Отходы культурального производства в дальнейшем технологическом процессе не используются и, например, на Курской биофабрике утилизируются.
Включение в состав предложенной кормовой биологически активной добавки янтарной кислоты способствует усилению клеточного дыхания, усвоению кислорода клетками. Янтарная кислота является катализатором биоэнергетических процессов, обладает антиоксидантными свойствами, обезвреживает свободные радикалы, предотвращает разрушение эритроцитов, укрепляет иммунитет, участвует в нейтрализации токсинов, активизирует ряд важнейших ферментов.
Добавление в состав кормовой добавки нуклеината натрия значительно повышает ее иммуностимулирующие свойства. Нуклеинат натрия индуцирует лейкоцитарную реакцию, стимулирует деятельность костного мозга, внутриклеточный метаболизм и нуклеиновый обмен. Он обладает активностью поликлонального иммуномодулятора, регулирует миграцию Т-лимфоцитов и процессы кооперации Т- и В-лимфоцитов, стимулирует фагоцитарную активность макрофагов и продукцию факторов неспецифической защиты организма, особенно при иммунодефицитах.
Включение в состав предложенной кормовой добавки органического селена в форме препарата Сел-Плекс способствует поступлению селена в организм животных, который повышает интенсивность метаболизма, регулирует скорость окислительно-восстановительных реакций, воздействует на активность фосфатаз и синтез АТФ, влияет на процессы тканевого дыхания и иммунобиологическую активность организма. Микроэлемент селен входит в состав фермента глутатионпероксидазы, являющейся важной составляющей антиоксидантной системы защиты организма. В природе селен существует в неорганической и органической формах. При этом органический селен представлен селенметионином и селенцистеином, которые более доступны для организма животных по сравнению с неорганической формой селена.
Получают кормовую биологически активную добавку для молодняка свиней путем механического смешивания компонентов. Для получения 1 л кормовой добавки в стеклянную емкость последовательно вносят 500 мл отходов культурального производства, в которых последовательно растворяют 18-20 г янтарной кислоты, 25-30 г нуклеината натрия, 0,25-0,30 г препарата Сел-Плекс и затем доводят объем до 1000 мл добавлением отходов культурального производства.
Выбранные количества янтарной кислоты и нуклеината натрия, входящих в предлагаемую кормовую добавку, было определено экспериментальным путем и обосновано тем, что при уменьшении янтарной кислоты (менее 18 г) снижается стимулирующее действие кормовой добавки на обмен веществ. При уменьшении нуклеината натрия (менее 25 г) значительно снижается иммуностимулирующее действие кормовой добавки. Увеличение янтарной кислоты (более 20 г) и нуклеината натрия (более 30 г) не оказывает существенных изменений свойств кормовой добавки, сопровождается расходом компонентов и дополнительными затратами. Уменьшение количества органического селена (менее 0,25 г) приводит к снижению антиоксидантных свойств предлагаемой кормовой добавки, а повышение (более 0,30 г) - вызывает у молодняка свиней снижение аппетита и уменьшение среднесуточных привесов.
Полученная кормовая биологически активная добавка представляет собой прозрачную жидкость светло-желтого цвета, без запаха, с рН 6,0-6,5.
Токсическое действие изготовленной кормовой добавки проверяли на морских свинках, содержащихся в виварии Курской государственной сельскохозяйственной академии им. И.И.Иванова. С этой целью биодобавку использовали в различных дозировках. Опыты проводили на 4 группах морских свинок-аналогов (по 10 голов в каждой). Скармливали кормовую добавку путем индивидуального выпаивания с использованием шприца с резиновой насадкой.
Морским свинкам 1 группы добавку скармливали (вводили) в дозе 5 мл/гол. один раз в сутки. Свинкам 2 группы добавку скармливали в дозе 10 мл/гол, в два приема по 5 мл. Свинкам 3 группы добавку скармливали в дозе 15 мл/гол, в три приема по 5 мл. Свинки 4 группы являлись контрольными, они кормовую добавку не получали.
Продолжительность эксперимента составляла 10 суток. В этот период за подопытными животными проводили наблюдение, учитывали у них общее состояние и поведенческие реакции. По окончании эксперимента у морских свинок брали кровь из сердца, а затем убивали. После убоя проводили осмотр внутренних органов и извлекали печень для гистологического анализа. В крови исследовали скорость оседания эритроцитов (СОЭ), гематокрит, содержание эритроцитов и гемоглобина с использованием общепринятых методов (Клиническая лабораторная диагностика в ветеринарии - М.: Агропромиздат, 1985). Содержание общего белка исследовали рефрактометрически, белковые фракции определяли с использованием электрофореза на пластинах из ацетата целлюлозы. Ферментативную активность аминотрансфераз (ACT, АЛТ), щелочной фосфатазы (ЩФ), содержание билирубина установили с применением наборов реактивов «Био-Ла-Тест» фирмы «Лахема».
Наблюдение за морскими свинками, получавшими кормовую добавку в течение 10 дней, показало, что их состояние и поведенческие реакции не отличались от контрольных животных. Они были активными, на внешние раздражители реагировали адекватно, аппетит был хороший.
При вскрытии внутренние органы патологических изменений не имели. Размеры печени, ее цвет, структура на разрезе не отличались от таковых у свинок контрольной группы. Гистологические исследования печени не выявили патологических изменений в морфологии органа.
Исследования крови показали, что у свинок, получавших кормовую биологически активную добавку, содержание общего белка в плазме крови было достоверно (Р<0,05) больше, чем у контрольных животных (таблица 1). В свою очередь у морских свинок 3 группы содержание белка в крови было выше, чем у свинок 1 и 2 групп. Электрофоретический анализ показал, что увеличение общего белка у животных, получавших кормовую биологически активную добавку, происходило за счет фракции альбуминов, содержание которых в их крови колебалось в пределах 45,0±2,17 - 49,4±2,05%. У морских свинок опытных групп в крови отмечалось относительно высокое содержание гамма-глобулинов по сравнению с контрольными животными.
Анализ содержания билирубина, ферментативной активности АЛТ, ACT и ЩФ показал, что данные биохимические показатели крови подопытных животных находились в пределах физиологических норм. Это указывает на то, что кормовая добавка в исследуемых дозах не вызывала повышенной «нагрузки» на печень морских свинок.
Таким образом, проведенные исследования свидетельствуют, что предлагаемая кормовая биологически активная добавка не оказывает отрицательного влияния на организм животных.
Пример 1. Изучение влияния разных доз предложенной кормовой добавки на привесы и биохимический статус поросят проводили в учебно-опытном хозяйстве «Знаменское» Курской государственной сельскохозяйственной академии имени профессора И.И.Иванова.
Было отобрано три группы поросят-аналогов крупной белой породы 2-месячного возраста, которые содержались в одном помещении и получали одинаковый рацион.
Поросятам 1 группы дополнительно к рациону скармливали 50 мл/гол. предложенной кормовой добавки (суточная норма), поросятам 2 группы скармливали 100 мл/гол. добавки, поросята 3 группы являлись контрольными и получали только основной рацион. Скармливали кормовую добавку в течение 10 дней с комбикормом в виде влажной мешанки групповым способом. При этом суточную норму делили на две равные части.
До начала эксперимента и после его окончания у 7 поросят из каждой группы брали кровь, в которой определяли СОЭ, гематокрит, содержание эритроцитов, лейкоцитов, гемоглобина общепринятыми методами. Содержание общего белка устанавливали биуретовым методом, содержание глюкозы, общих липидов, общего кальция, неорганического фосфора, общего магния, витаминов А и С, ферментативную активность ACT и АЛТ исследовали с использованием наборов «Био-Ла-Тест» фирмы «Лахема» и наборов «Клини-Тест».
Результаты исследований показали, что предложенная кормовая добавка не оказывала отрицательного влияния на организм подопытных животных. Поросята всех групп в период эксперимента были активными, аппетит сохранен, поведенческие реакции не отличались от контрольных животных.
Определение массы тела у поросят через 30 дней после начала эксперимента показало, что у поросят, получавших кормовую добавку, она была выше по сравнению с контрольными животными (таблица 2). При этом среднесуточные привесы у поросят опытных групп были неодинаковыми. Так, у животных, получавших 50 мл/гол. добавки, среднесуточные привесы составляли 326,7±7,5 г, получавших 100 мл/гол. - 333,3±7,9 г. Динамика абсолютного прироста живой массы тела у поросят была аналогичной среднесуточным привесам. Наиболее высоким данный показатель отмечался у поросят 2 группы (10,0±0,2 кг), которые получали 100 мл/гол. кормовой добавки. У поросят контрольной группы абсолютный прирост массы тела был меньше и составлял 9,0±0,2 кг. При этом затраты кормов и эффективность их использования находились в прямой зависимости от нормы скармливания биологически активной добавки. На каждый килограмм прироста живой массы поросят 1 и 2 групп затрачивалось кормовых единиц и переваримого протеина рациона меньше по сравнению с контролем.
Лабораторный анализ крови показал (таблица 3), что общие гематологические показатели у поросят всех групп находились в пределах физиологических норм. СОЭ составляла 1,2±0,05 - 1,5±0,05 мм/час, гематокритная величина - 38,0±5,1 - 39,5±4,7%, содержание эритроцитов 6,0±0,14 - 6,7±0,10 - 109/л, гемоглобина - 95,8±4,7 - 100,5±6,8 г/л. Однако у поросят, получавших кормовую биологически активную добавку, «дыхательная» функция крови была выше по сравнению с контролем. При этом наиболее высокое содержание эритроцитов и гемоглобина было у поросят 2 опытной группы (6,7±0,10·1012/л; 100,5±6,8 г/л).
В свою очередь исследование биохимических компонентов крови у подопытных животных показало, что у поросят, получавших предложенную биологическую добавку, обменные процессы протекали на более интенсивном уровне по сравнению с животными контрольной группы.
Так, содержание общего белка, глюкозы, общего кальция неорганического фосфора, витаминов А и С у поросят 1 и 2 групп было достоверно (Р<0,05) больше, чем у контрольных животных.
Ферментативная активность ACT и АЛТ у поросят, получавших кормовую добавку существенно не отличалась от таковой у контрольных животных, что свидетельствует о нормальном функциональном состоянии печени.
Результаты данного эксперимента показали, что предложенная кормовая биологически активная добавка оказывает стимулирующее влияние на обмен веществ поросят, что сопровождается достоверным увеличением у них среднесуточных привесов.
Пример 2. Сравнительные исследования иммуностимулирующего действия предложенной кормовой добавки и кормовой добавки-прототипа проводили в свиноводческом комплексе ПТ «Надежда» Большесолдатского района Курской области.
Было отобрано три группы поросят 3-месячного возраста (по 10 голов в каждой) с клиническими признаками гипотрофии: у поросят масса тела не соответствовала возрасту, волосяной покров был матовым и взъерошенным, аппетит плохой. При этом общие клинические показатели (температура тела, частота пульса, частота дыхательных движений) находились в пределах физиологических норм.
Поросятам 1 группы скармливали дополнительно к рациону предложенную кормовую добавку в дозе 2 мл/кг один раз в сутки в течение 14 суток. Поросятам 2 группы скармливали кормовую добавку-прототип в том же режиме, что и поросятам 1 группы. Поросята 3 группы были контрольными, они получали основной рацион без кормовых добавок. Содержались поросята всех групп в одном помещении и получали одинаковый рацион.
Продолжительность эксперименты составляла 30 суток. До начала и в конце эксперимента у всех подопытных животных определяли массу тела и брали кровь, в которой исследовали общее содержание лейкоцитов на электронном счетчике «Пикоскель», уровень общих иммуноглобулинов устанавливали цинксульфатным методом, бактерицидную активность (БАСК) и лизоцимную активность (ЛАСК) крови определяли с использованием культуры клеток Micrococcus lysodeicticus и Staphylococcus aureus, фагоцитарную активность лейкоцитов (ФАЛ) оценивали по реакции фагоцитоза с латексом, количество В- и Т-лимфоцитов определяли методом разеткообразования, содержание малонового диальдегида (МДА) устанавливали по реакции с тио-барбитуровой кислотой, содержание церулоплазмина определяли экспресс-методом по 3. Тену (1981).
В ходе проведенных исследований было установлено, что у большинства поросят 1 и 2 групп через 5-7 суток после скармливания биодобавок повысился аппетит, поведение их стало более активным. На 15-20 сутки у поросят исчезла взъерошенность волосяного покрова, щетина приобрела блеск. Абсолютная масса тела у поросят, получавших предложенную биодобавку, в конце эксперимента была больше в среднем на 0,9 кг по сравнению с поросятами 2 группы и на 1,2 кг больше по сравнению с поросятами контрольной группы. При этом у 80% животных 1 группы масса тела соответствовала их возрастному периоду, а среди поросят 2 группы таких животных было 71%.
Состояние поросят контрольной группы практически не изменилось. Аппетит у них был плохой, общее состояние угнетенное, среднесуточные привесы низкие. У 5 поросят контрольной группы отмечались клинические признаки дисфункции желудочно-кишечного тракта. Эти животные были выведены из эксперимента в связи с назначением лечения, однако впоследствии все они пали. Среди поросят 1 и 2 групп заболевания не регистрировались.
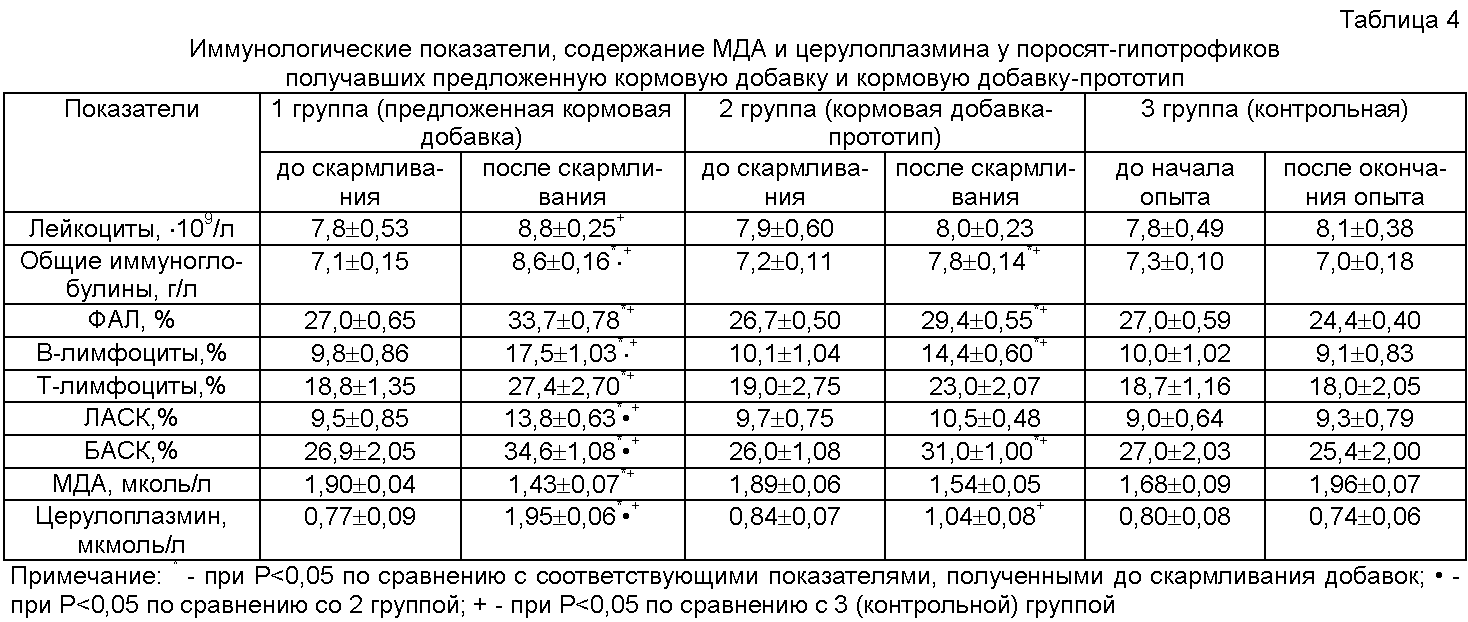
Анализ крови показал, что у поросят, получавших кормовые добавки, неспецифические факторы защиты были выше по сравнению с контрольными животными, о чем свидетельствуют данные, представленные в таблице 4. При этом у поросят, получавших предложенную кормовую добавку, все изучаемые показатели неспецифической резистентности, за исключением содержания Т-лимфоцитов были достоверно (Р<0,05) выше, чем у поросят получавших кормовую добавку-прототип.
В то же время выявленное уменьшение содержания МДА и повышение церулоплазмина в крови поросят, получавших предложенную кормовую добавку, указывает на то, что она обладает выраженными антиоксидантными свойствами.
Пример 3. Для выяснения влияния предложенной кормовой биологически активной добавки на белково-аминокислотный обмен у молодняка свиней, был проведен научно-производственный эксперимент в АО им. Тельмана Октябрьского района Курской области. На свиноводческой ферме хозяйства было сформировано две группы подсвинков на доращивании 4-месячного возраста по 10 голов в каждой.
Подсвинкам 1 (опытной) группы дополнительно к рациону скармливали предложенную кормовую добавку в дозе 2,0 мл/кг через день в течение 20 дней. Подсвинки 2 (контрольной) группы получали только основной рацион.
В конце эксперимента из каждой группы было убито по 5 подсвинков. При контрольном убое у животных отбирали кровь, пробы печени, длиннейшей мышцы спины и участки тонкого отдела кишечника.
Белковый азот в крови и тканях отобранных органов исследовали по методу Кьельдаля, содержание свободных аминокислот определяли на автоматическом анализаторе KLA - 3В фирмы «Chitaci».
В ходе исследований было установлено, что у подсвинков, которым скармливали предложенную кормовую добавку, в крови, тканях печени, длиннейшей мышцы спины и стенке тонкого отдела кишечника содержание общего азота было больше по сравнению с контрольными животными (таблица 5). Так, в крови подсвинков опытной группы его содержание превышало в среднем на 0,35 г %, в тканях печени - на 0,26 г %, в тканях длиннейшей мышцы спины - на 0,28 г %, в тканях стенки тонкого отдела кишечника - на 0,08 г %. При этом данное увеличение во всех случаях, за исключением содержания белкового азота в стенке тонкого отдела кишечника, было достоверным (Р<0,01).
Анализ идентифицированных свободных аминокислот (таблица 6) свидетельствует о том, что в конце эксперимента в тканях длиннейшей мышцы подсвинков, получавших кормовую добавку, суммарное содержание аминокислот было достоверно (Р<0,01) больше, чем у контрольных животных. В среднем выявленная разница составляла 167,7 мкмоль/л.
Увеличение содержания аминокислот у подсвинков, получавших кормовую добавку, происходило как за счет незаменимых, так и заменимых аминокислот. При этом повышение уровня незаменимых аминокислот было более выраженным (на 129,3 мкмоль/л; Р<0,001) по сравнению с заменимыми аминокислотами (на 38,4 мкмоль/л; Р<0,05). Отмечено, что содержание лизина, серина, глицина, аланина, валина, метионина, лейцина, фенилаланина в тканях длиннейшей мышцы спины у подсвинков опытной группы было в 1,2-1,5 раза больше, чем в контроле. Отклонение от контроля в сторону повышения содержания таких аминокислот, как гистидин, аргинин, изолейцин, тирозин в тканях длиннейшей мышцы спины у подсвинков опытной группы было несущественным (Р>0,05). В то же время содержание треонина, пролина, аспарагиновой и глютаминовой кислот в тканях длиннейшей мышцы спины подсвинков контрольной группы было больше, чем у животных, получавших кормовую добавку.
Таким образом, результаты проведенного эксперимента свидетельствуют о том, что скармливание кормовой биологически активной добавки изменяет аминокислотный состав у подсвинков тканей мышц в сторону повышения их товарного качества.
Результаты проведенных сравнительных испытаний свидетельствуют о том, что предложенная кормовая добавка по сравнению с прототипом оказывает более выраженное стимулирующее влияние на метаболизм и неспецифические факторы защиты организма, а также обладает антиоксидантными свойствами. В этой связи ее можно использовать при выращивании молодняка свиней.
|
|
|
|
|
|
|

