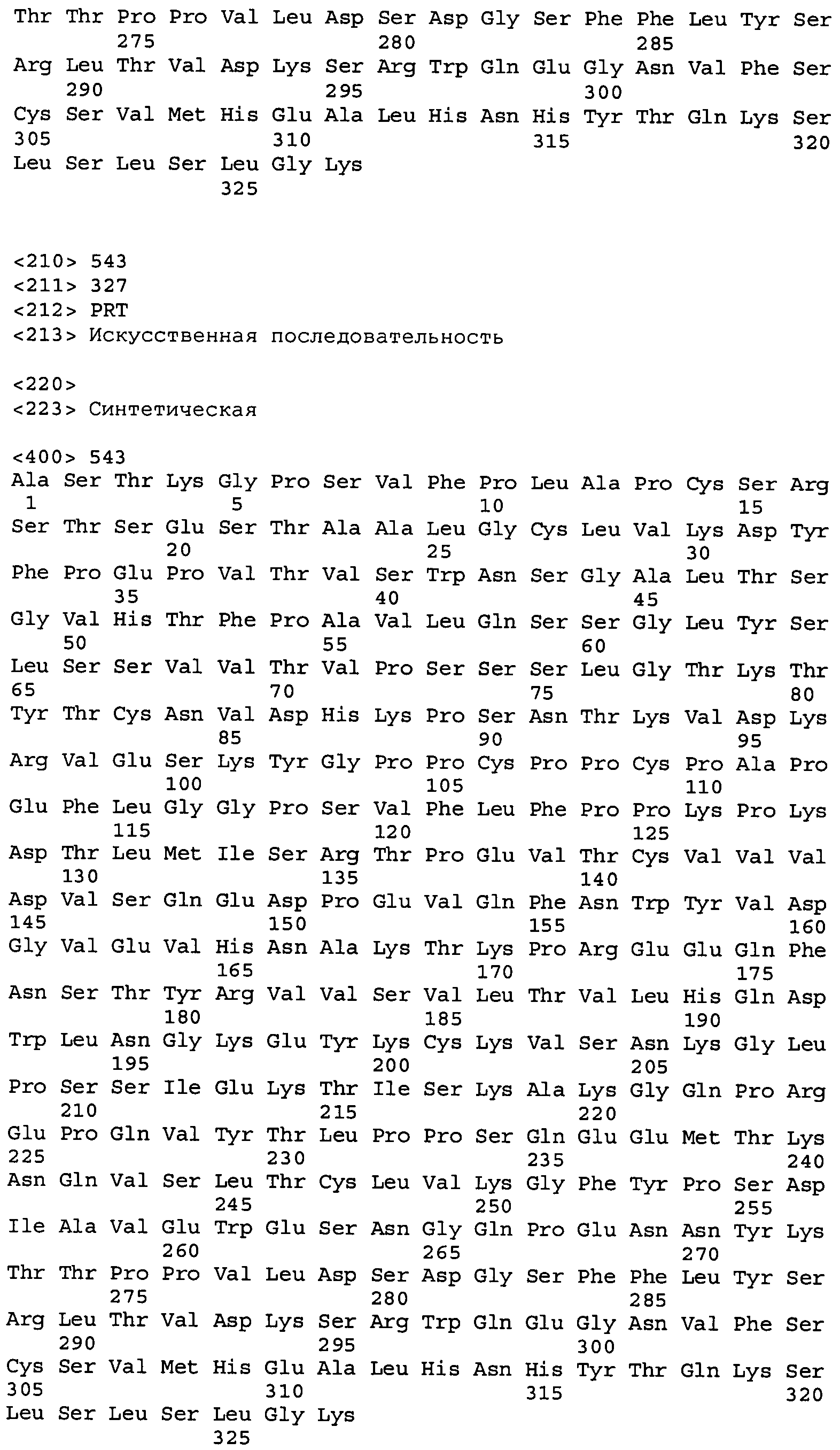Результат интеллектуальной деятельности: АНТИТЕЛА ЧЕЛОВЕКА С ВЫСОКОЙ АФФИННОСТЬЮ К ФАКТОРУ РОСТА НЕРВОВ ЧЕЛОВЕКА
Вид РИД
Изобретение
Область изобретения
Настоящее изобретение относится к антителам человека и антиген-связывающим фрагментам антител человека, которые специфическим образом связывают фактор роста нервов (NGF) человека, и к терапевтическим способам применения указанных антител.
Материалы, использованные при подготовке заявки
Фактор роста нервов (NGF) был первым из обнаруженных нейротрофинов, и его роль в развитии и выживании как периферических нейронов, так и нейронов центральной нервной системы, была хорошо описана. Было показано, что NGF является важнейшим фактором выживания и сохранения функций при развитии периферических симпатических и эмбриональных сенсорных нейронов и базальных холинергических нейронов переднего мозга (Smeyne et al. (1994) Nature 368:246-249; Crowley et al. (1994) Cell 76:1001-1011). NGF активизирует экспрессию нейропептидов в сенсорных нейронах (Lindsay et al. (1989) Nature 337:362-364), и его активность опосредована двумя различными интегрированными в мембрану рецепторами, рецептором TrkA и общим рецептором нейротрофинов p75.
Уровень NGF повышен в синовиальной жидкости пациентов, страдающих ревматоидным артритом и другими формами артрита. Было показано, что антагонисты NGF предупреждают гиперальгезию и аллодинию на моделях нейропатической и хронической воспалительной боли у животных.
Антитела против-NGF описаны, например, в WO 01/78698, WO 02/096458, WO 2004/032870, в публикациях патентов США 2005/0074821, 2004/0237124 и 2004/0219144.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В первом аспекте настоящее изобретение относится к полноразмерным антителам человека и их антиген-связывающим фрагментам, которые специфическим образом связывают фактор роста нервов (NGF) человека с KD порядка 5 пМ или менее и не вступают в перекрестную реакцию с нейротрофином-3 (NT-3). В предпочтительном варианте осуществления антитело против-NGF или его фрагмент связывает NGF человека с KD порядка 1,0 пМ или менее. Для данных антител характерно связывание с NGF с высокой аффинностью, высокой специфичностью и способность нейтрализовать активность NGF. В предпочтительных вариантах осуществления антитело или его фрагмент связывает NGF человека приблизительно в 2-10 раз выше, чем NGF крысы и/или NGF мыши.
Антитела могут быть полноразмерными (например, антитела IgG1 или IgG4) или включать только антиген-связывающую часть (например, фрагмент Fab, F(ab')2 или scFv) и могут быть модифицированы с целью воздействовать на функциональность, например удалять остаточные эффекторные функции (Glu, удаляющий остаточные эффекторные функции (Reddy et al. (2000) J. Immunol. 164:1925-1933).
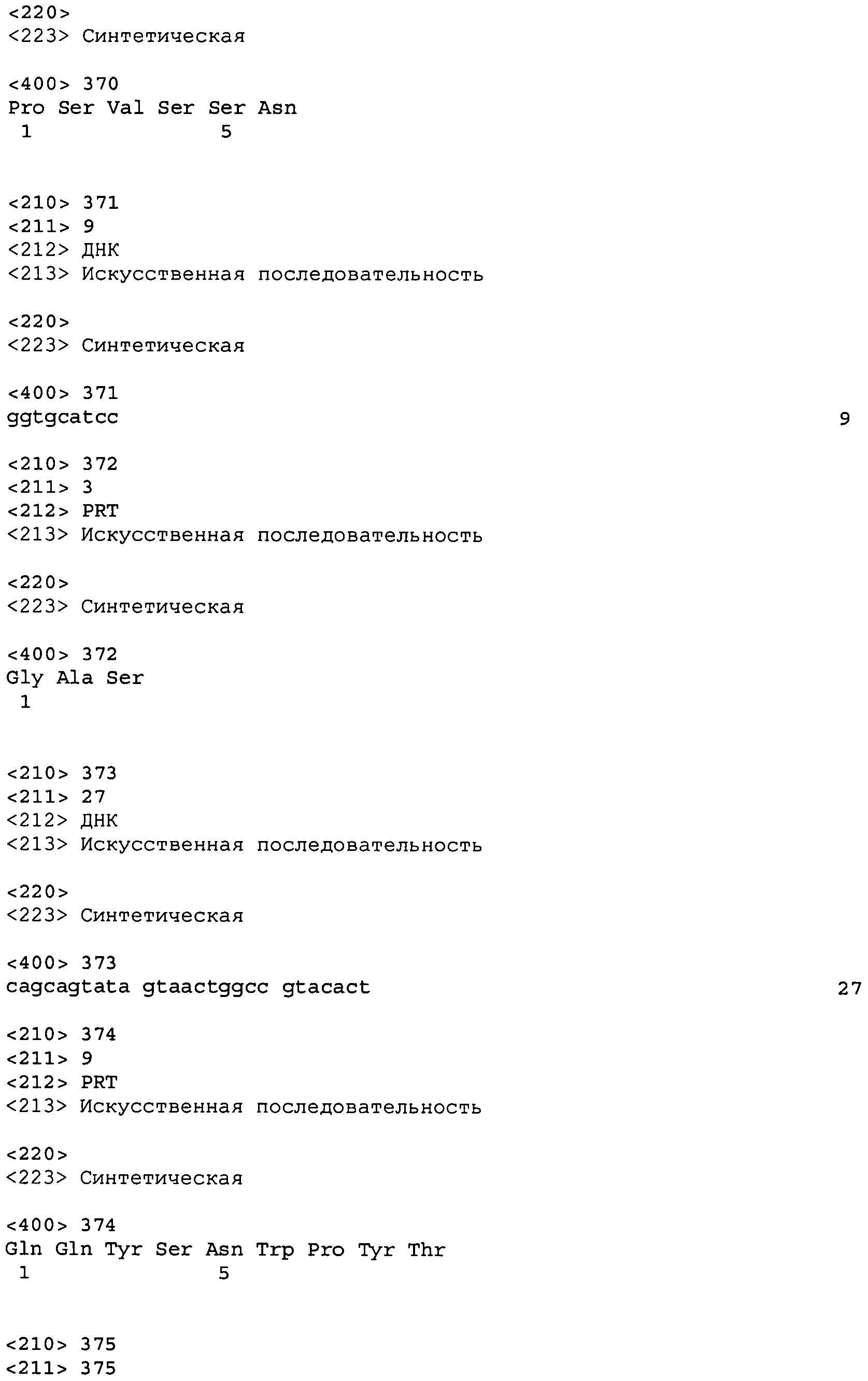
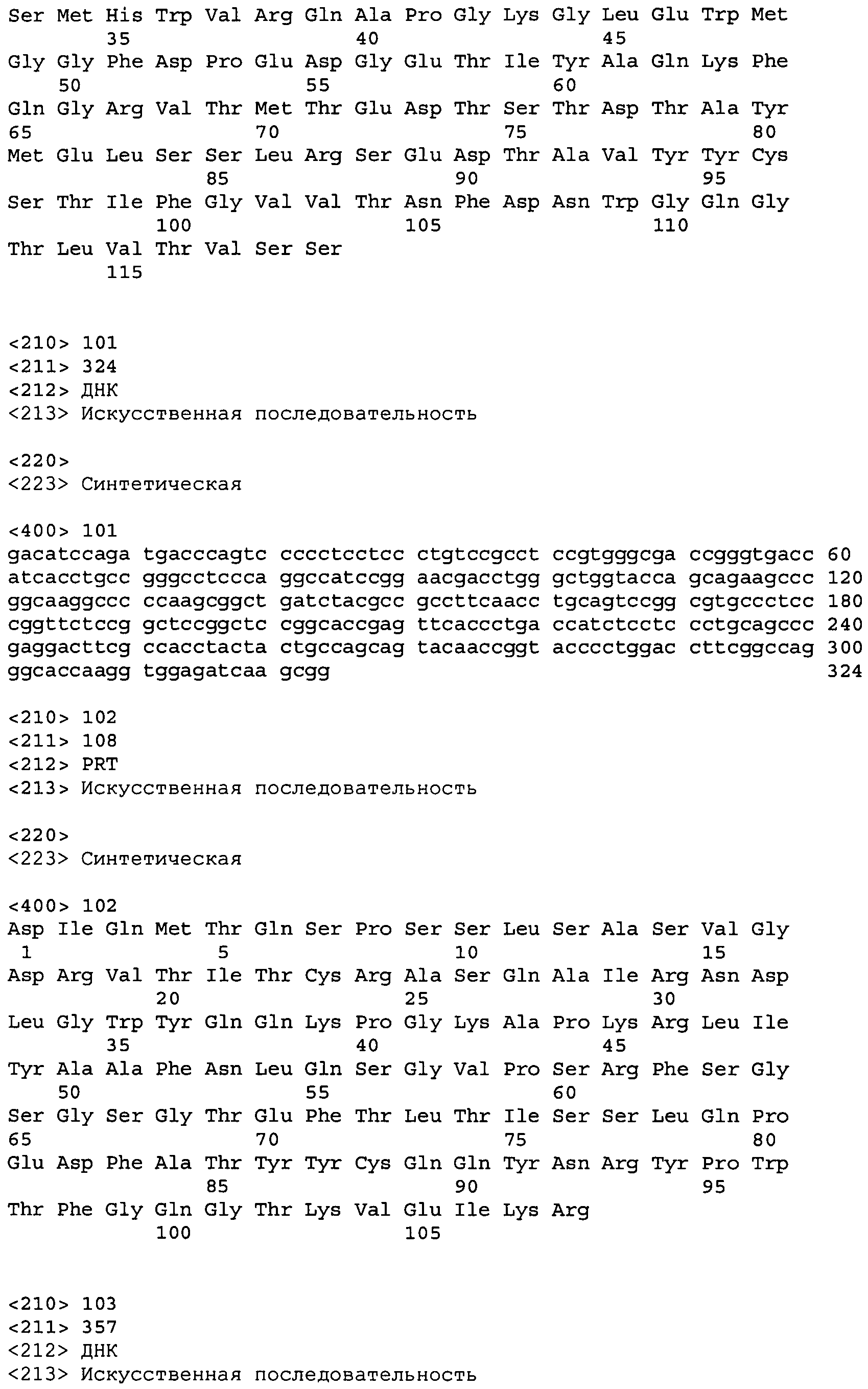
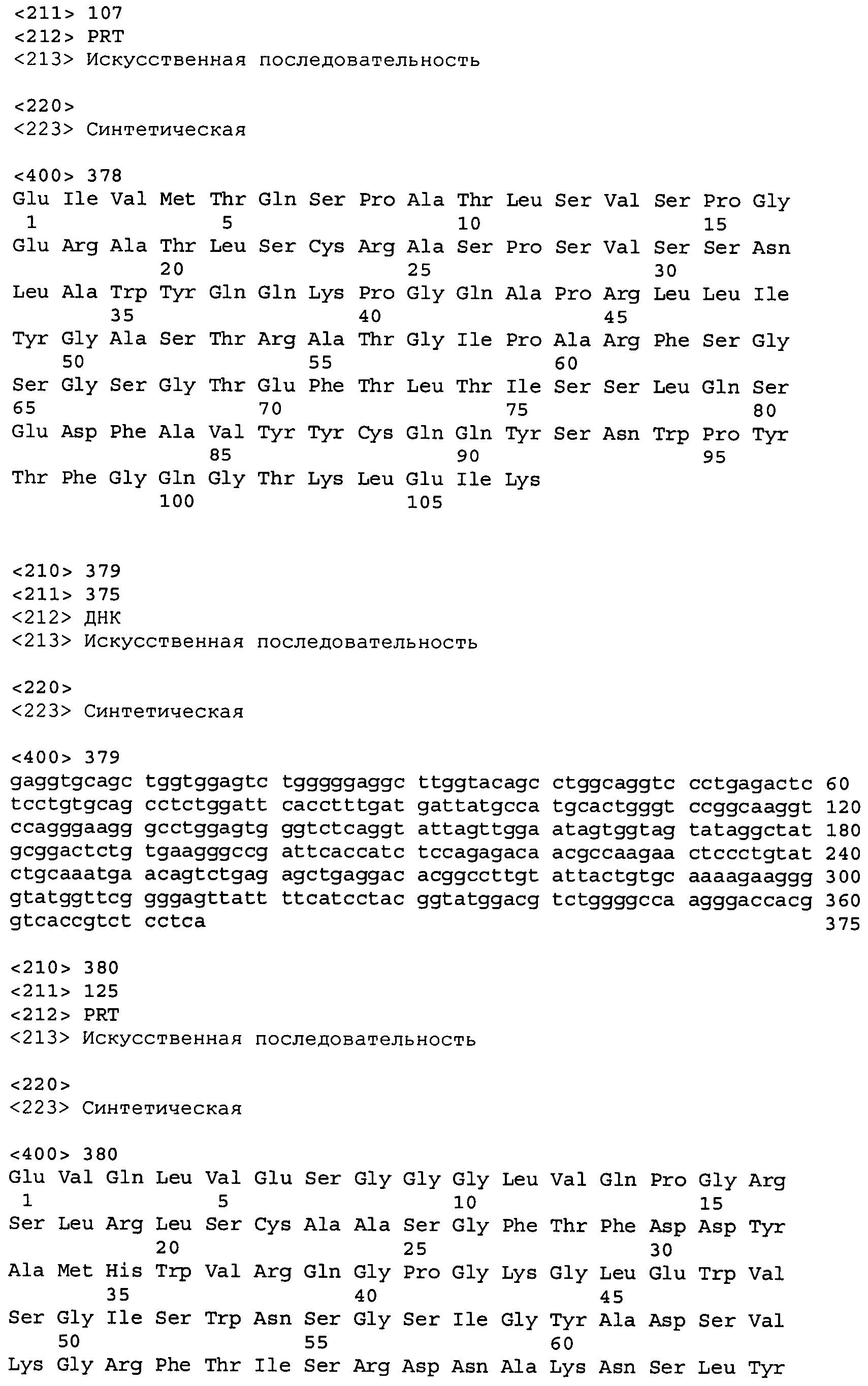
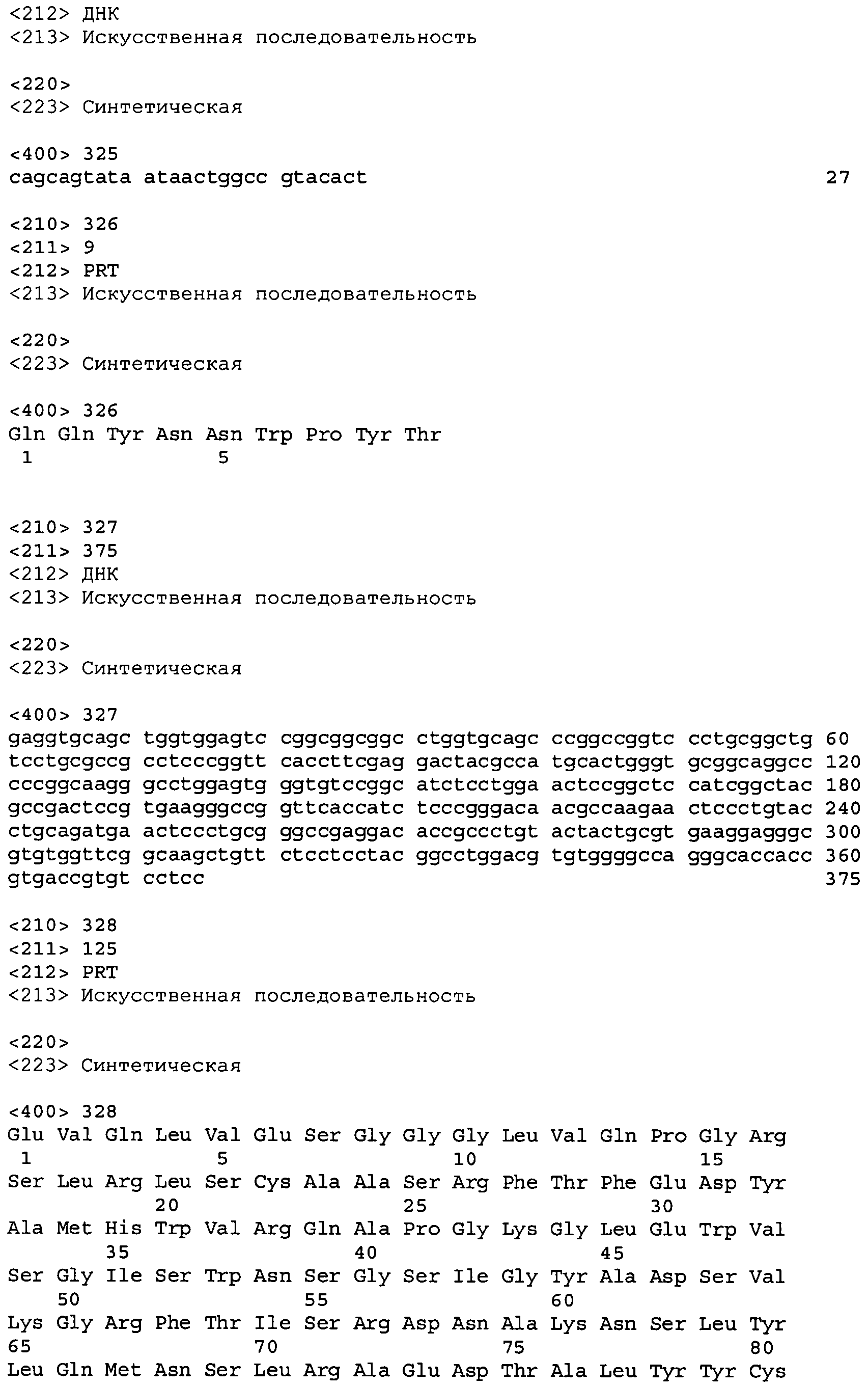
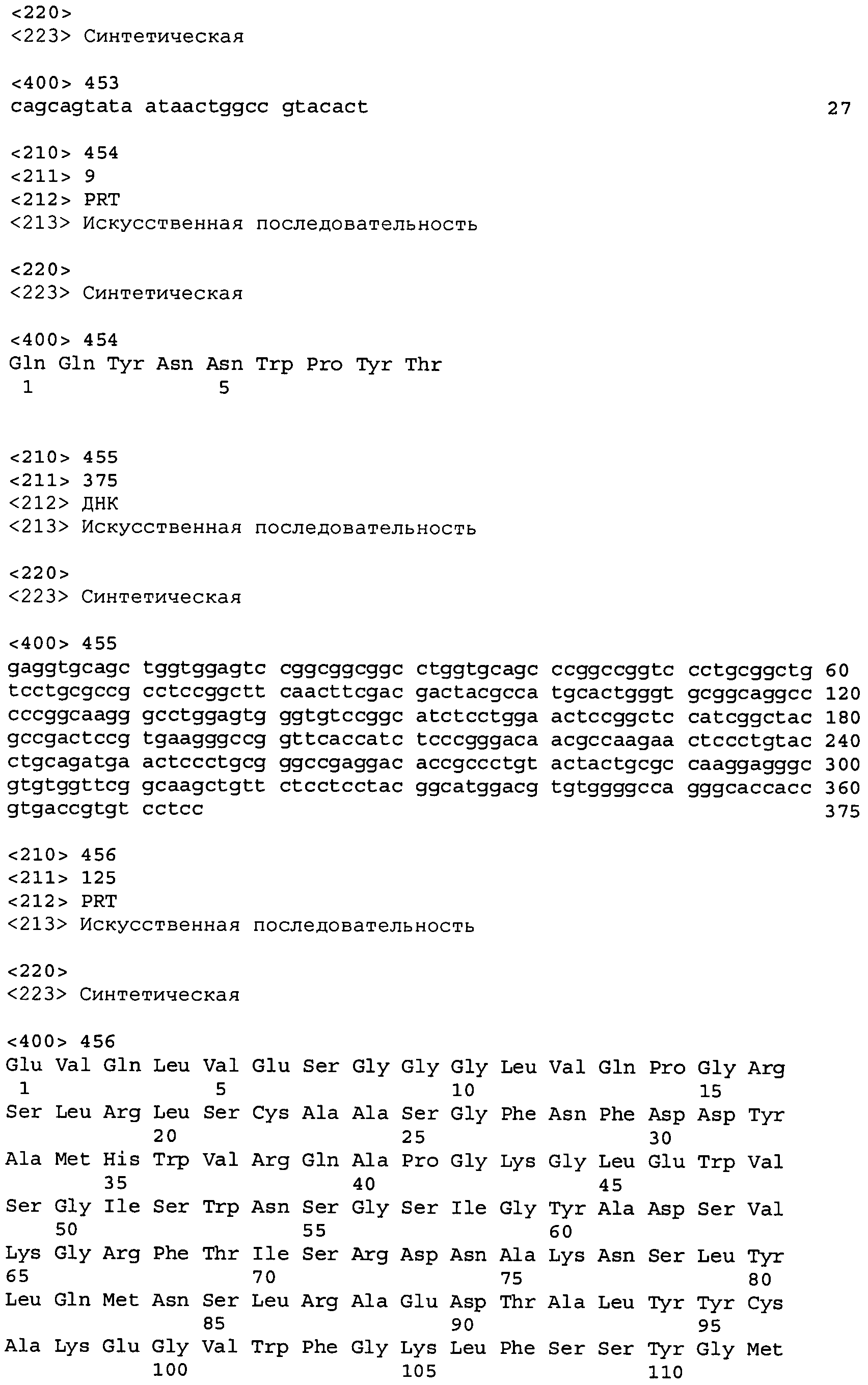
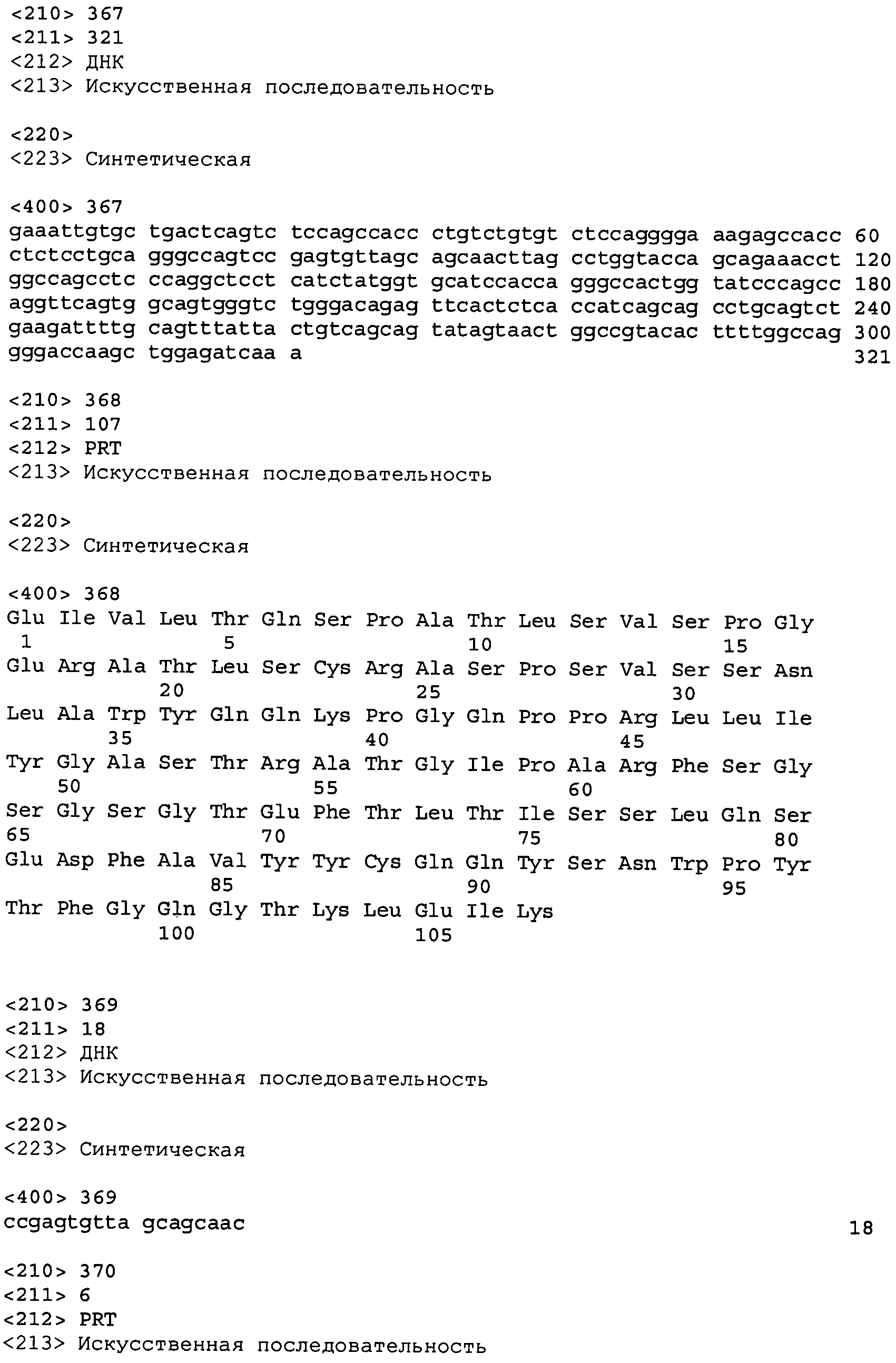
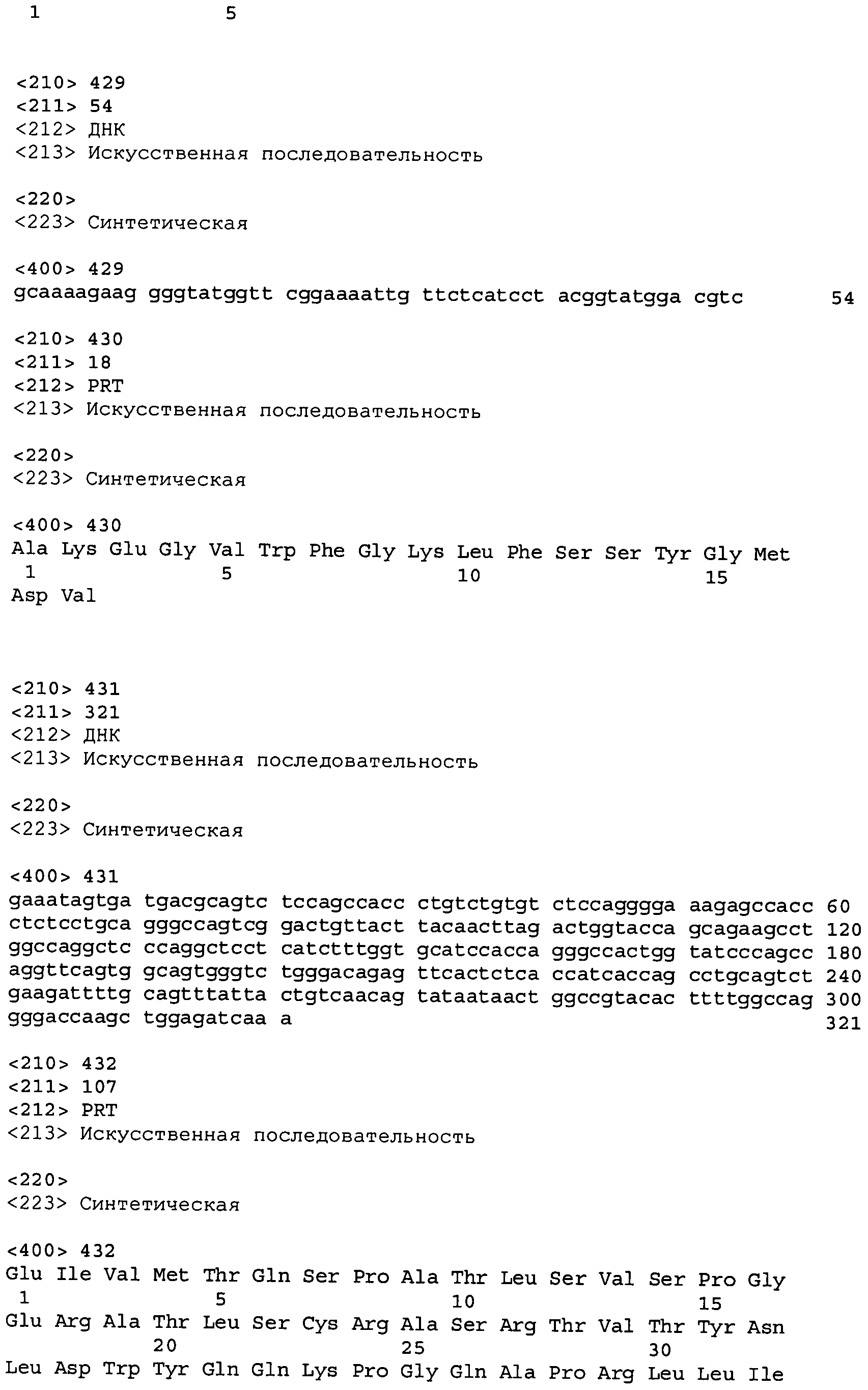
В одном из вариантов осуществления настоящее изобретение относится к антителу или антиген-связывающему фрагменту антитела, содержащему вариабельную область тяжелой цепи (HCVR), выбранную из группы SEQ ID No: 4, 20, 36, 52, 68, 84, 100, 104, 108, 112, 116, 132, 136, 140, 156, 160, 176, 180, 184, 200, 204, 208, 224, 228, 232, 236, 240, 256, 260, 264, 280, 284, 288, 304, 308, 312, 328, 332, 336, 352, 356, 360, 376, 380, 384, 400, 404, 420, 424, 440, 456, 460, 464, 480, 484, 488, 504, 508, 512, 528 и 532, или ее, по существу, аналогичную последовательность, которая идентична указанной последовательности на не менее 90%, не менее 95%, не менее 98% или не менее 99%; более предпочтительно, антитело или его фрагмент содержит HCVR, представленную как SEQ ID No: 108, 100 или 84; и еще более предпочтительно, HCVR является аминокислотной последовательностью, представленной как SEQ ID No: 108.
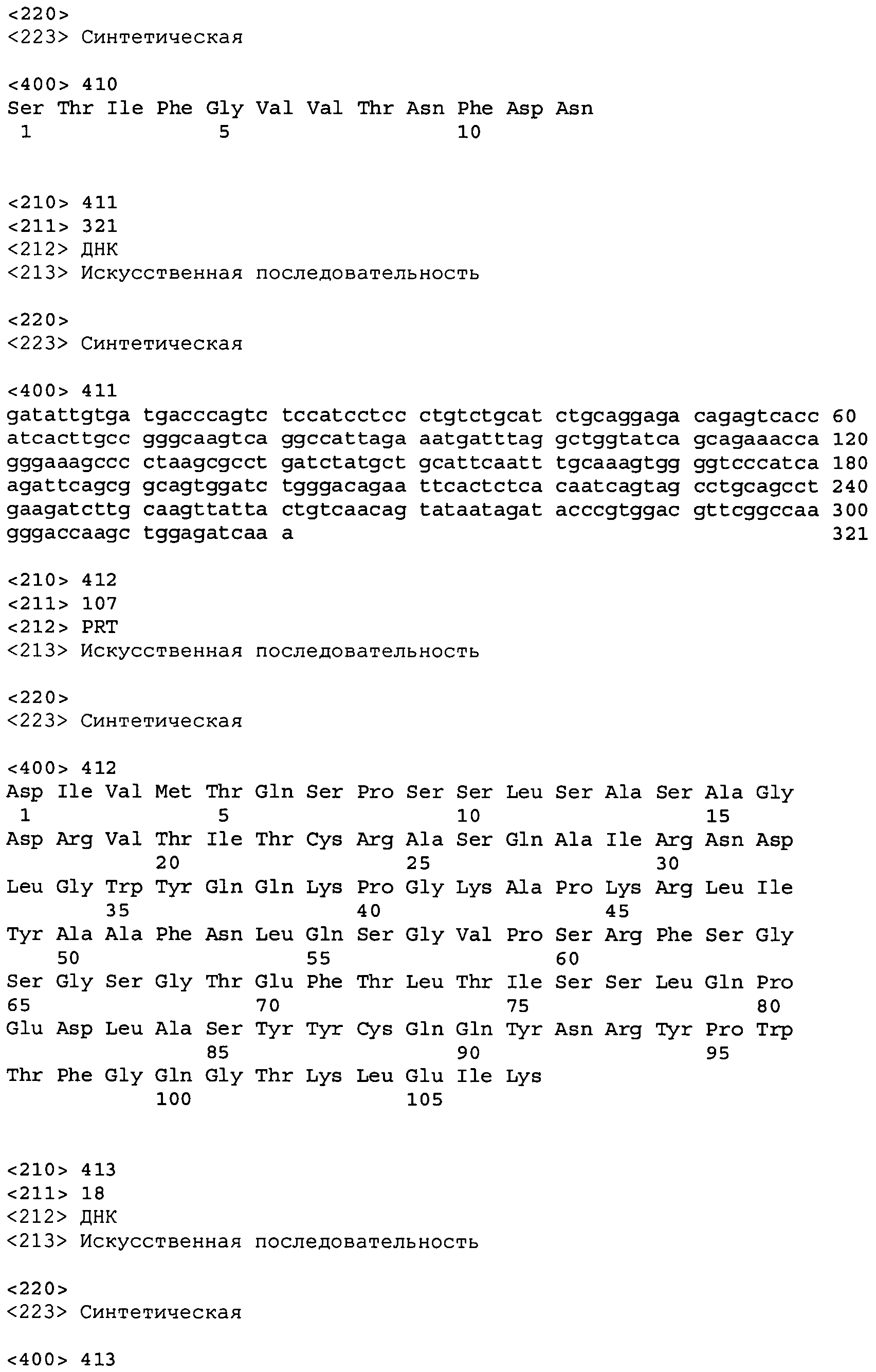
В одном из вариантов осуществления антитело или его фрагмент, кроме того, содержит вариабельную область легкой цепи (LCVR), выбранную из группы SEQ ID No: 12, 28, 44, 60, 76, 92, 102, 106, 110, 114, 124, 134, 138, 148, 158, 168, 178, 182, 192, 202, 206, 216, 226, 230, 234, 238, 248, 258, 262, 272, 282, 286, 296, 306, 310, 320, 330, 334, 344, 354, 358, 368, 378, 382, 392, 402, 412, 422, 432, 448, 458, 462, 472, 482, 486, 496, 506, 510, 520, 530 и 534, или ее существенно аналогичную последовательность, которая идентична указанной последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%. В предпочтительном осуществлении LCVR является SEQ ID No: 110, 102 или 92; еще более предпочтительно, LCVR является аминокислотной последовательностью, представленной в SEQ ID No: 110.
В конкретных осуществлениях антитело или его фрагмент содержит пару последовательностей HCVR и LCVR (HCVR/LCVR), выбранную из группы SEQ ID No: 4/12, 20/28, 36/44, 52/60, 68/76, 84/92, 100/102, 104/106, 108/110, 112/114, 116/124, 132/134, 136/138, 140/148, 156/158, 160/168, 176/178, 180/182, 184/192, 200/202, 204/206, 208/216, 224/226, 228/230, 232/234, 236/238, 240/248, 256/258, 260/262, 264/272, 280/282, 284/286, 288/296, 304/306, 308/310, 312/320, 328/330, 332/334, 336/344, 352/354, 356/358, 360/368, 376/378, 380/382, 384/392, 400/402, 404/412, 420/422, 424/432, 440/448, 456/458, 460/462, 464/472, 480/482, 484/486, 488/496, 504/506, 508/510, 512/520, 528/530 и 532/534. В предпочтительном осуществлении парой HCVR/LCVR является SEQ ID No: 108/110, 100/102 или 84/92; более предпочтительно, SEQ ID No: 108/110.
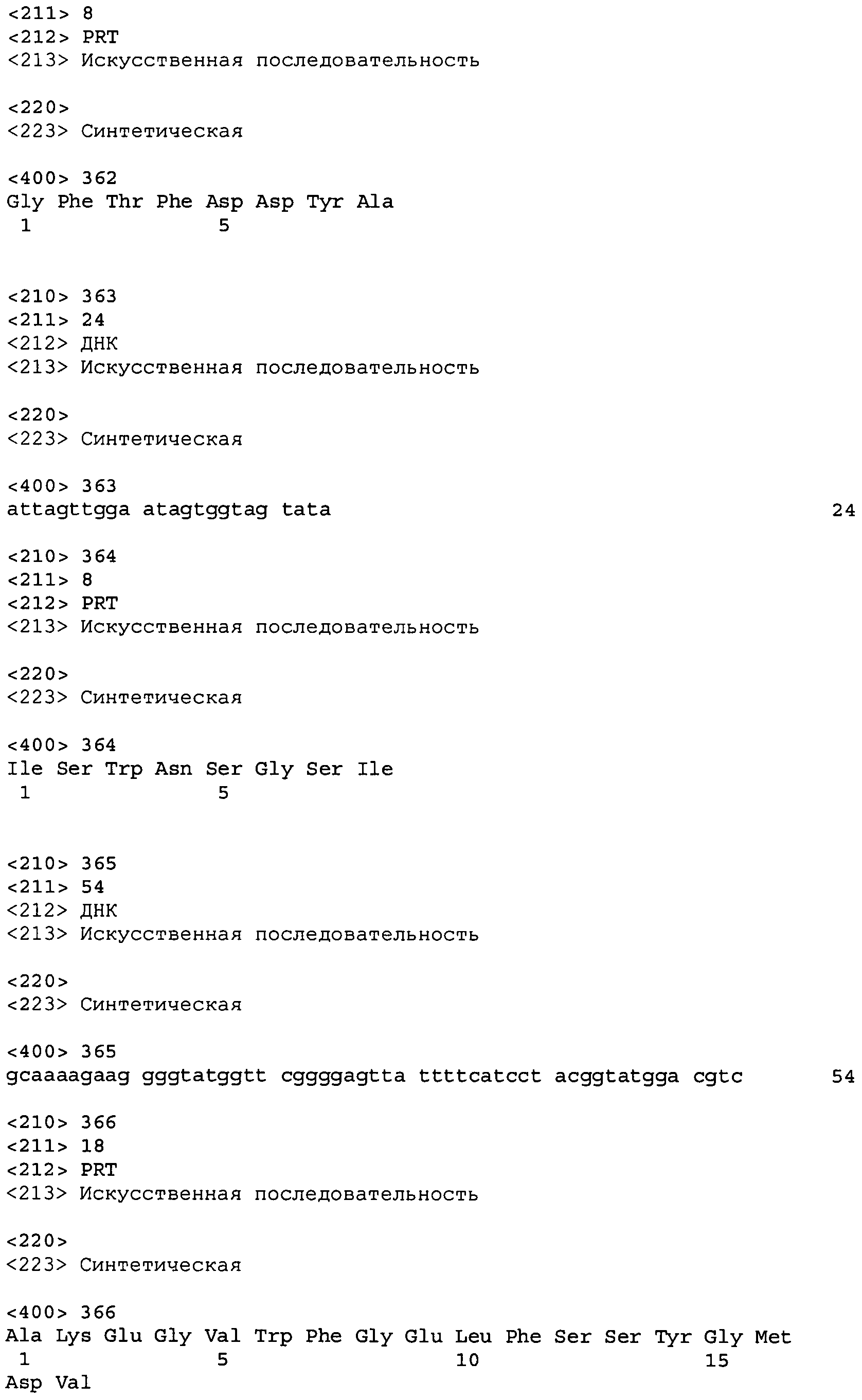
Во втором аспекте настоящее изобретение относится к антителу или антиген-связывающему фрагменту антитела, содержащему домен CDR3 (HCDR3) тяжелой цепи, выбранный из SEQ ID No: 10, 26, 42, 58, 74, 90, 122, 146, 166, 190, 214, 246, 270, 294, 318, 342, 366, 390, 410, 430, 446, 470, 494 и 518, или его существенно аналогичную последовательность, которая идентична указанной последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; и домен CDR3 (LCDR3) легкой цепи, выбранный из 18, 34, 50, 66, 82, 98, 130, 154, 174, 198, 222, 254, 278, 302, 326, 350, 374, 398, 418, 438, 454, 478, 502 и 526, или его существенно аналогичную последовательность, которая идентична указанной последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%. В предпочтительном осуществлении парой HCDR3/LCDR3 является SEQ ID No: 90 и 98, 214 и 222; 410 и 418; 430 и 438; или 446 и 454; более предпочтительно, SEQ ID No: 90 и 98.
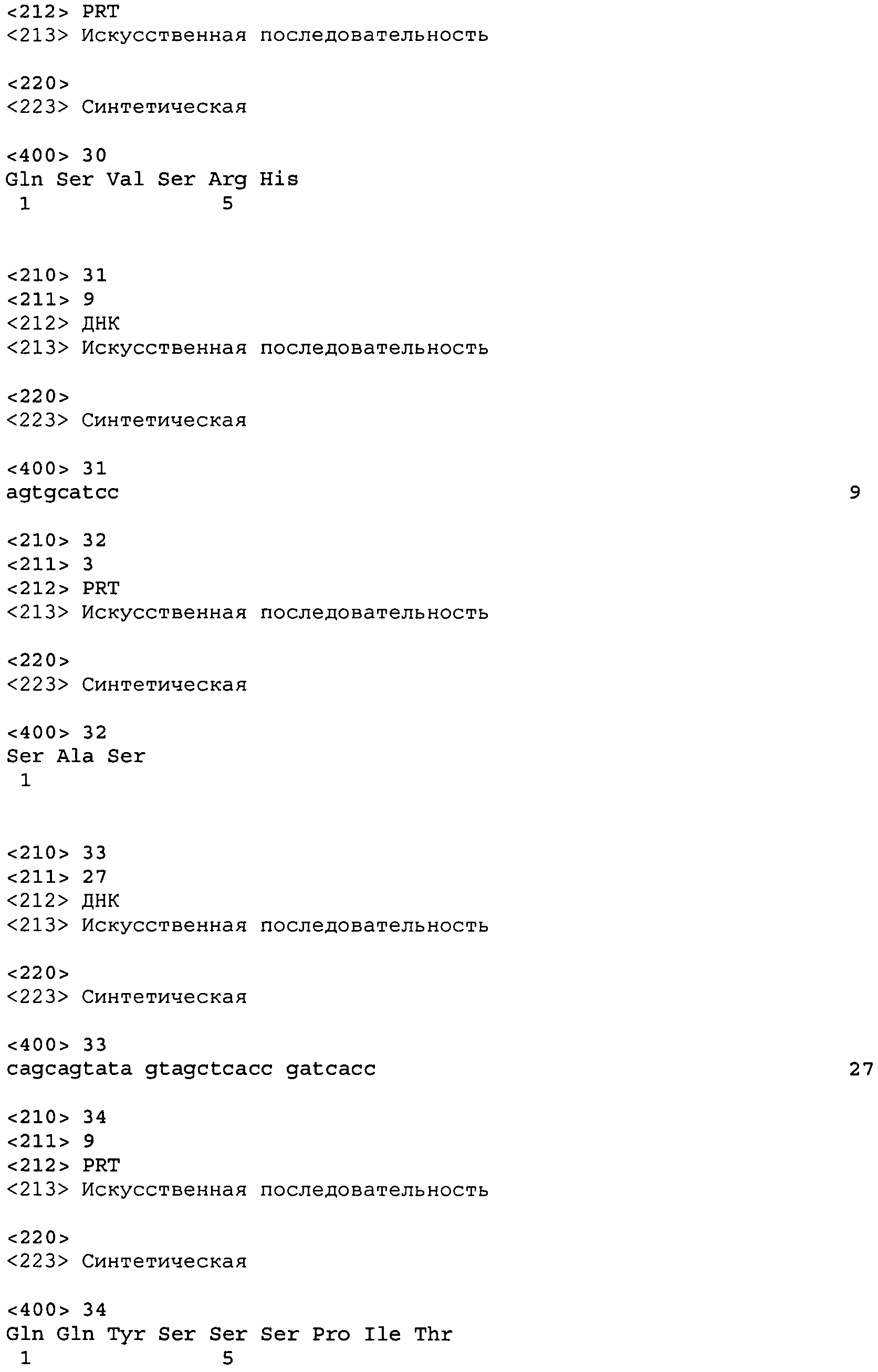
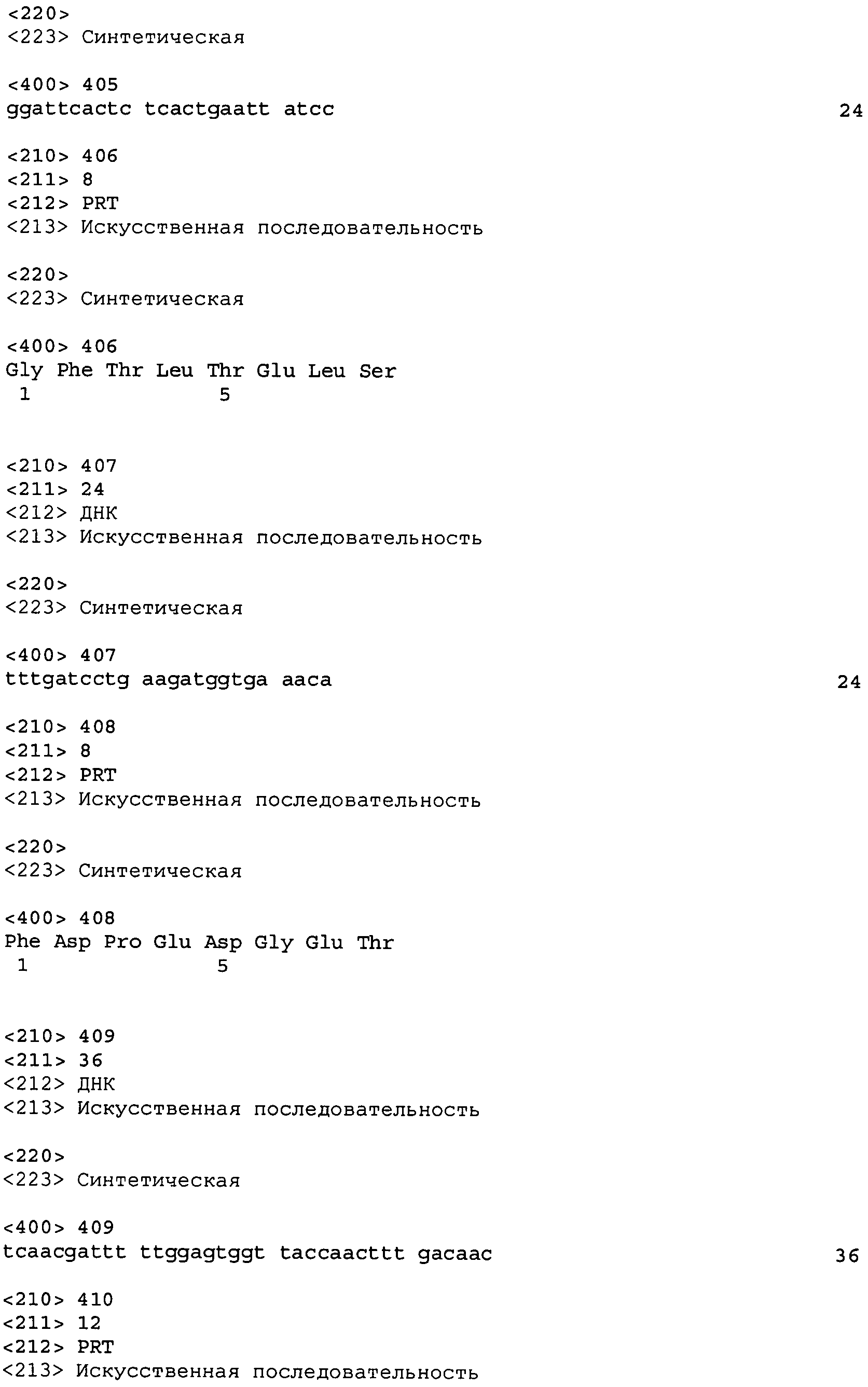
В дальнейшем варианте осуществления настоящего изобретения приводится антитело или его фрагмент, дополнительно содержащий домен CDR1 (HCDR1) тяжелой цепи, выбранный из SEQ ID No: 6, 22, 38, 54, 70, 86, 118, 142, 162, 186, 210, 242, 266, 290, 314, 338, 362, 386, 406, 426, 442, 466, 490 и 514, или его существенно аналогичную последовательность, которая идентична указанной последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен CDR2 (HCDR2) тяжелой цепи, выбранный из SEQ ID No: 8, 24, 40, 56, 72, 88, 120, 144, 164, 188, 212, 244, 268, 292, 316, 340, 364, 388, 408, 428, 444, 468, 492 и 516, или его существенно аналогичную последовательность, которая идентична указанной последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен CDR1 (LCDR1) легкой цепи, выбранный из SEQ ID No: 14, 30, 46, 62, 78, 94, 126, 150, 170, 194, 218, 250, 274, 298, 322, 346, 370, 394, 414, 434, 450, 474, 498 и 522, или его существенно аналогичную последовательность, которая идентична указанной последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%; и домен CDR2 (LCDR2) легкой цепи, выбранный из SEQ ID No: 16, 32, 48, 64, 80, 96, 128, 152, 172, 196, 220, 252, 276, 300, 324, 348, 372, 396, 416, 436, 452, 476, 500 и 524, или его существенно аналогичную последовательность, которая идентична указанной последовательности не менее 90%, не менее 95%, не менее 98% или не менее 99%. В предпочтительном осуществлении последовательностями CDR тяжелой и легкой цепей являются SEQ ID No: 86, 88, 90, 94, 96 и 98; 210, 212, 214, 218, 220 и 222; 406, 408, 410, 414, 416 и 418; 442, 444, 446, 450, 452 и 454; и 426, 428, 430, 434, 436 и 438; еще более предпочтительно, последовательностями CDR являются SEQ ID No: 86, 88, 90, 94, 96 и 98.
В третьем аспекте настоящего изобретения приводятся молекулы нуклеиновой кислоты, кодирующие антитела против-NGF или их фрагменты. Настоящее изобретение также охватывает рекомбинантные векторы экспрессии, несущие нуклеиновые кислоты настоящего изобретения, и клетки-хозяева, в которые включаются такие векторы, а также способы приготовления антител путем культивирования клеток-хозяев в условиях, допускающих производство антител и получение произведенных таким образом антител.
В одном варианте осуществления настоящего изобретения приводится антитело или его фрагмент, содержащий HCVR, кодируемую последовательностью нуклеиновой кислоты, выбранной из SEQ ID No: 3, 19, 35, 51, 67, 83, 99, 103, 107, 111, 115, 131, 135, 139, 155, 159, 175, 179, 183, 199, 203, 207, 223, 227, 231, 235, 239, 255, 259, 263, 279, 283, 287, 303, 307, 311, 327, 331, 335, 351, 355, 359, 375, 379, 383, 399, 403, 419, 423, 439, 455, 459, 463, 479, 483, 487, 503, 507, 511, 527 и 531, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; более предпочтительно, HCVR кодируется последовательностью SEQ ID No: 107 или 99.
В одном варианте осуществления антитело или его фрагмент дополнительно содержит LCVR, кодируемую последовательностью нуклеиновой кислоты, выбранной из SEQ ID No: 11, 27, 43, 59, 75, 91, 101, 105, 109, 113, 123, 133, 137, 147, 157, 167, 177, 181, 191, 201, 205, 215, 225, 229, 233, 237, 247, 257, 261, 271, 281, 285, 295, 305, 309, 319, 329, 333, 343, 353, 357, 367, 377, 381, 391, 401, 411, 421, 431, 447, 457, 461, 471, 481, 485, 495, 505, 509, 519, 529 и 533, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; предпочтительно, LCVR кодируется последовательностью SEQ ID No: 109 или 101.
В одном варианте осуществления настоящего изобретения приводится антитело или антиген-связывающий фрагмент антитела, содержащий домен HCDR3, кодируемый нуклеотидной последовательностью, выбранной из SEQ ID No: 9, 25, 41, 57, 73, 89, 121, 145, 165, 189, 213, 245, 269, 293, 317, 341, 365, 389, 409, 429, 445, 469, 493 и 517, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; и домен LCDR3, кодируемый нуклеотидной последовательностью, выбранной из SEQ ID No: 17, 33, 49, 65, 81, 97, 129, 153, 173, 197, 221, 253, 277, 301, 325, 349, 373, 397, 417, 437, 453, 477, 501 и 525, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%. В предпочтительном осуществлении последовательности HCDR3 и LCDR3 кодируются SEQ ID No: 89 или 97 соответственно.
В дополнительном варианте осуществления антитело или его фрагмент дополнительно содержит домен HCDR1, кодируемый нуклеотидной последовательностью, выбранной из SEQ ID No: 5, 21, 37, 53, 69, 85, 117, 141, 161, 185, 209, 241, 265, 289, 313, 337, 361, 385, 405, 425, 441, 465, 489 и 513, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен HCDR2, кодируемый нуклеотидной последовательностью, выбранной из SEQ ID No: 7, 23, 39, 55, 71, 87, 119, 143, 163, 187, 211, 243, 267, 291, 315, 339, 363, 387, 407, 427, 443, 467, 491 и 515, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; домен LCDR1, кодируемый нуклеотидной последовательностью, выбранной из SEQ ID No: 13, 29, 45, 61, 77, 93, 125, 149, 169, 193, 217, 249, 273, 297, 321, 345, 369, 393, 413, 433, 449, 473, 497 и 521, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%; и домен LCDR2, кодируемый нуклеотидной последовательностью, выбранной из SEQ ID No: 15, 31, 47, 63, 79, 95, 127, 151, 171, 195, 219, 251, 275, 299, 323, 347, 371, 395, 415, 435, 451, 475, 499 и 523, или ее существенно аналогичную последовательность с гомологией не менее 90%, не менее 95%, не менее 98% или не менее 99%. В предпочтительном осуществлении антитело или его фрагмент содержит последовательности CDR тяжелой цепи, кодируемые SEQ ID No: 85, 87 и 89; и последовательности CDR легкой цепи, кодируемые SEQ ID No: 93, 95 и 97.
В четвертом аспекте настоящего изобретения приводится изолированное антитело или антиген-связывающий фрагмент антитела, который специфическим образом связывает NGF человека, содержащий HCDR3 и LCDR3, где HCDR3 содержит аминокислотную последовательность формулы X1 - X2 - X3 - X4 - X5 - X6 - X7 - X8 - X9 - X10 - X11 - X12 - X13 - X14 - X15 - X16 - X17 - X18 (SEQ ID No: 537), где X1 - Ala или Ser, X2 - Thr или Lys, X3 - Glu или Ile, X4 - Phe или Gly, X5 - Val или Gly, X6 - Val или Trp, X7 - Val или Phe, X8 - Thr или Gly, X9 - Asn или Lys, X10 - Phe или Leu, X11 - Asp или Phe, X12 - Asn или Ser, X13 - Ser или отсутствует, X14 - Tyr или отсутствует, X15 - Gly или отсутствует, X16 - Met или отсутствует, X17 - Asp или отсутствует и X18 - Val или отсутствует; и LCDR3 содержит аминокислотную последовательность формулы X1 - X2 - X3 - X4 - X5 - X6 - X7 - X8 - X9 (SEQ ID No: 540), где X1 - Gln, X2 - Gln, X3 - Tyr, X4 - Asn, X5 - Arg или Asn, X6 - Tyr или Trp, X7 - Pro, X8 - Tyr или Trp и X9 - Thr.
В более конкретном варианте осуществления антитело или его фрагмент дополнительно содержит последовательность HCDR1 формулы X1 - X2 - X3 - X4 - X5 - X6 - X7 - X8 (SEQ ID No: 535), где X1 - Gly, X2 - Phe, X3 - Thr или Asn, X4 - Phe или Leu, X5 - Thr или Asp, X6 - Asp или Glu, X7 - Tyr или Leu и X8 - Ser или Ala; последовательность HCDR2 формулы X1 - X2 - X3 - X4 - X5 - X6 - X7 - X8 (SEQ ID No: 536), где X1 - Ile или Phe, X2 - Asp или Ser, X3 - Pro или Trp, X4 - Glu или Asn, X5 - Asp или Ser, X6 - Gly, X7 - Thr, Glu или Ser, X8 - Thr или Ile; HCDR3 содержит аминокислотную последовательность формулы X1 - X2 - X3 - X4 - X5 - X6 - X7 - X8 - X9 - X10 - X11 - X12 - X13 - X14 - X15 - X16 - X17 - X18 (SEQ ID No: 537), где X1 - Ala или Ser, X2 - Thr или Lys, X3 - Glu или Ile, X4 - Phe или Gly, X5 - Val или Gly, X6 - Val или Trp, X7 - Val или Phe, X8 - Thr или Gly, X9 - Asn или Lys, X10 - Phe или Leu, X11 - Asp или Phe, X12 - Asn или Ser, X13 - Ser или отсутствует, X14 - Tyr или отсутствует, X15 - Gly или отсутствует, X16 - Met или отсутствует, X17 - Asp или отсутствует и X18 - Val или отсутствует; последовательность LCDR1 формулы X1 - X2 - X3 - X4 - X5 - X6 (SEQ ID No: 538), где X1 - Gln или Arg, X2 - Ala, Ser или Thr, X3 - Val или Ile, X4 - Arg или Thr, X5 - Asn, Phe или Tyr и X6 - Asp или Asn; последовательность LCDR2 формулы X1 - X2 - X3 (SEQ ID No: 539) где X1 - Gly или Ala, X2 - Ala и X3 - Ser или Phe; и LCDR3 содержит аминокислотную последовательность формулы X1 - X2 - X3 - X4 - X5 - X6 - X7 - X8 - X9 (SEQ ID No: 540), где X1 - Gln, X2 - Gln, X3 - Tyr, X4 - Asn, X5 - Arg или Asn, X6 - Tyr или Trp, X7 - Pro, X8 - Tyr или Trp и X9 - Thr.
В пятом аспекте настоящего изобретения приводится полностью человеческое антитело или фрагмент антитела, который блокирует активность NGF с IC50 менее 10 нМ, согласно результатам измерения in vitro при помощи PC12-клеточного анализа (описано ниже). В предпочтительном осуществлении антитело изобретения демонстрирует IC50 порядка 500 пМ или менее; еще более предпочтительно, IC50 порядка 100 пМ или менее, порядка 50 пМ или менее, или порядка 25 пМ или менее.
В одном варианте осуществления настоящее изобретение описывает изолированное антитело человека или его антиген-связывающую область, которое связывает NGF с константой аффинности (KD) менее чем приблизительно 500 пМ, предпочтительнее, менее чем приблизительно 300 пМ, еще предпочтительнее, менее чем приблизительно 100 пМ, менее чем приблизительно 50 пМ, менее чем приблизительно 20 пМ, менее чем приблизительно 10 пМ, менее чем приблизительно 5 пМ или менее чем приблизительно 1 пМ, по данным поверхностного плазмонного резонанса (BIACORE™). В предпочтительном осуществлении антитело против-NGF человека или фрагмент антитела настоящего изобретения связывает NGF человека с KD порядка 0,5 пМ или менее. В предпочтительных осуществлениях антитело или его фрагмент связывает NGF человека при более высокой аффинности - приблизительно в 1,5 раза, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз или 10 раз выше чем NGF крысы, и приблизительно в 1,5 раза, 2 раза, 2,5 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз или 10 раз выше чем NGF мыши.
В предпочтительном варианте осуществления антитело или его фрагмент обладает высокой специфичностью в отношении NGF человека, например, не вступает в перекрестную реакцию с близко родственным нейротрофином-3 (NT-3). Так, в предпочтительном осуществлении антитело или его фрагмент с высокой аффинностью и высокой селективностью демонстрирует KD для NGF человека на уровне 1,0 пМ или менее, ингибирует связывание NGF с рецепторами TrkA и p75 и не вступает в перекрестную реакцию с NT-3 человека, по данным поверхностного плазмонного резонанса. NT-3 играет решающую роль в таких физиологических процессах как, например, мышечная координация при помощи мотонейронов, и, таким образом, антитела или фрагменты антител, не вступающие в перекрестную реакцию с NT-3, обеспечивают неожиданное клиническое и терапевтическое преимущество по сравнению с уже известными антителами. Было показано, что NT-3 предотвращает развитие термальной гипералгезии на модели невропатической боли по типу хронической компрессии (см., например, Wilson-Gerwing et al. (2005) J Neuroscience 25:758-767). В последнее время было продемонстрировано, что NT-3 существенно снижает экспрессию натриевых каналов, предположительно провоцирующих невропатическую боль (Wilson-Gerwing & Verge (2006) Neuroscience 141:2075-2085). Эти данные указывают на благотворную роль NT-3 в подавлении нейропатической боли.
Настоящее изобретение относится к антителам против-NGF с модифицированной структурой гликозилирования. В некоторых приложениях может оказаться полезным удалить нежелательные сайты гликозилирования или использовать антитело без фукозного фрагмента в олигосахаридной цепи, например для усиления функции антителозависимой клеточной цитотоксичности (ADCC) (см. Shield et al. (2002) JBC 277:26733). В других приложениях может осуществляться модификация галактозилирования с тем, чтобы изменить комплементзависимую цитотоксичность (CDC).
В шестом аспекте настоящего изобретения относится к составу, включающему рекомбинантное антитело человека или его фрагмент, которое специфически связывает NGF, и приемлемый носитель. В аналогичном аспекте настоящего изобретения приводится состав, представляющий собой сочетание ингибитора NGF и второго терапевтического средства. В одном варианте осуществления ингибитор NGF является антителом или его фрагментом. В предпочтительном осуществлении вторым терапевтическим средством является любое подходящее терапевтическое средство, которое оптимальным образом сочетается с ингибитором NGF.
В седьмом аспекте настоящее изобретение относится к способам ингибирования NGF человека с помощью антитела против-NGF или антиген-связывающей области антитела настоящего изобретения. Подлежащим лечению нарушением является любое заболевание или патологическое состояние, которое улучшается, облегчается, подавляется или предупреждается за счет устранения, ингибирования или снижения активности NGF. Более конкретно, в изобретении предлагается способ лечения патологических состояний или заболеваний, опосредованных NGF, например воспалительной боли, послеоперационной боли шва, комплексного регионарного болевого синдрома, боли при первичном или метастатическом раке кости, нейропатической боли, боли при переломах, боли при остеопорозных переломах, боли, вызванной ожогами, остеопорозом, суставной боли при подагре, боли, связанной с обострениями при серповидноклеточной анемии, других ноцицептивных болей, а также гепатоклеточной карциномы, рака молочной железы и цирроза печени путем введения ингибитора NGF, например антител настоящего изобретения или их фрагментов как при монотерапии, так и в качестве второго терапевтического средства. В предпочтительных вариантах нейропатической боли предпочтительна терапия реперкуссионной невралгии тройничного нерва, постгерпетической невралгии, фантомной боли в ампутированных конечностях, фибромиалгии, симпатической рефлекторной дистрофии и нейрогенных болях. Вторым терапевтическим средством может быть ингибитор интерлейкина-1 (IL-1), например слитой белок, подобный описанному в патенте США US6927044; или же антиэпилептическое средство, например габапентаин, прегабалин, топирамат или же трициклический антидепрессант, например амитриптиллин; целекоксиб; антагонист цитокинов, например белок-антагонист или антитело против IL-1, IL-6, IL-6R, IL-18 или IL-18R. В одном варианте осуществления вторым терапевтическим средством является другой нейротрофин, например NT-3.
В восьмом аспекте настоящее изобретение относится к применению описанного выше антитела или антиген-связывающего фрагмента для смягчения или ингибирования заболевания или патологического состояния в организме человека, опосредованного NGF. Опосредованное NGF патологическое состояние или болезнь подавляются без заметного ухудшения моторной координации, и к таким состояниям относятся воспалительная боль, послеоперационная боль шва, нейропатическая боль, боль при переломах, суставная боль при подагре, постгерпетическая невралгия, боль, вызванная ожогами, боль при раке, боль при остеоартрите или ревматоидном артрите, ишиасе, боль, связанная с обострениями при серповидноклеточной анемии или постгерпетическая невралгия.
В связанном аспекте настоящее изобретение также предусматривает использование описанного выше антитела или антиген-связывающего фрагмента антитела при производстве лекарственного препарата, применяемого для смягчения или ингибирования заболевания или патологического состояния в организме человека, опосредованного NGF.
Другие цели и преимущества станут очевидными при ознакомлении с приведенным ниже подробным описанием.
ПОЛНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Прежде чем приступить к описанию представляемого способа, необходимо отметить, что настоящее изобретение не ограничивается конкретными способами и изложенными экспериментальными условиями, поскольку такие способы и условия можно менять. Следует также понимать, что используемая в настоящем документе терминология предназначена исключительно для описания конкретных осуществлений и не носит ограничительного характера, поскольку охват настоящего изобретения ограничивается только прилагаемой формулой изобретения.
Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют такое же значение, которое общеизвестно рядовым специалистам в области, к которой относится настоящее изобретение. Хотя на практике или при проверке настоящего изобретения могут использоваться любые методы и материалы, аналогичные или идентичные описанным в настоящем документе, ниже приводится описание предпочтительных методов и материалов.
Определения
Термин «фактор роста нервов человека» или «NGF», используемый в настоящем документе, означает NGF человека с последовательностью нуклеиновой кислоты, представленной в SEQ ID No: 1, и аминокислотную последовательность SEQ ID No: 2, или его биологически активный фрагмент.
Используемый в настоящем документе термин «антитело» предназначен для обозначения молекул иммуноглобулина, составленных из четырех полипептидных цепей, при этом две тяжелые (Н) цепи и две легкие (L) цепи связываются друг с другом дисульфидными связями. Каждая тяжелая цепь содержит вариабельную область тяжелой цепи (сокращенно называемую в настоящем документе HCVR или VH) и константную область тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов: CH1, CH2 и CH3. Каждая легкая цепь содержит вариабельную область легкой цепи (сокращенно называемую в настоящем документе LCVR или VL) и константную область легкой цепи. Константная область легкой цепи состоит из одного домена: CL. Области VH и VL могут далее подразделяться на области гипервариабельности, которые называются определяющими комплементарность областями (CDR), перемежаемые областями с более высоким уровнем консервативности, называемыми остовными областями (FR). Каждая область VH и VL образована тремя CDR и четырьмя FR, расположенными от амино-терминального конца к карбокси-терминальному концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4.
Используемый в настоящем документе термин «антиген-связывающая область» антитела (или просто «часть антитела» или «фрагмент антитела») обозначает один или несколько фрагментов антитела, которые сохраняют способность к специфическому связыванию с антигеном (например, NGF). Было показано, что антиген-связывающая функция антитела может осуществляться фрагментами всей последовательности антитела. К примерам связывающих фрагментов, включенных в термин «антиген-связывающая область» антитела, относятся (i) фрагмент Fab, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) фрагмент F(ab')2, бивалентный фрагмент, состоящий из двух фрагментов Fab, связанных дисульфидным мостиком в шарнирной области; (iii) фрагмент Fd, состоящий из доменов VH и CH1; (iv) фрагмент Fv, состоящий из доменов VL и VH отдельной области антитела; (v) фрагмент dAb (Ward et al. (1989) Nature 241:544-546), состоящий из домена VH; и (vi) отдельная определяющая комплементарность область (CDR). Более того, несмотря на то что два домена в фрагменте Fv, VL и VH кодируются различными генами, их можно объединить, используя рекомбинантные технологии, посредством синтетического линкера, который позволяет построить из них единую белковую цепочку, в которой области VL и VH связываются с образованием моновалентных молекул (известных как одиночная цепь Fv (scFv); см., например, Bird et al. (1988) Science 242:423-426; и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Такие одноцепочечные антитела также включаются в сферу охвата термина «антиген-связывающая область» антитела. Сюда же входят и другие формы одноцепочечных антител, например диатела. Диатела представляют собой бивалентные биспецифичные антитела, в которых домены VH и VL экспрессируются на одной полипептидной цепи, но длина соединяющего их линкера слишком мала для связывания двух доменов на одной и той же цепи, что заставляет домены одной цепи связываться с комплементарными доменами другой цепи, создавая тем самым два сайта связывания антигена (см., например, Holliger et al. (1993) Proc. Natl. Acad Sci. USA 90:6444-6448; Poljak et al. (1994) Structure 2:1121-1123).
Далее, антитело или его антиген-связывающая область могут быть частью более крупных иммуноассоциированных молекул, образованных ковалентной или нековалентной ассоциацией антитела или части антитела и одной или более белковой молекулы или пептида. Примеры таких иммуноадгезивных молекул включают использование области ядра стрептавидина для получения тетрамерной молекулы scFv (Kipriyanov et al. (1995) Human Antibodies and Hybridomas 6:93-101) и использование остатка цистеина, маркера-пептида и C-терминального полигистидинового маркера для получения бивалентных и биотинилированных молекул scFv (Kipriyanov et al. (1994) Mol. Immunol. 31:1047-1058). Части антител, такие как фрагменты Fab и F(ab')2, могут быть получены из цельных антител с помощью стандартных методик, таких как папаиновое и пепсиновое расщепление цельных антител соответственно. Кроме того, антитела, части антител и иммуноассоциированные молекулы могут быть получены с использованием стандартных технологий рекомбинантной ДНК, как описано в настоящем документе.
Используемый в настоящем документе термин «антитело человека» предназначен для обозначения антител с вариабельной и константной областями, полученных из иммуноглобулиновых последовательностей зародышевых линий человека. Описываемые в настоящем изобретении антитела человека могут включать аминокислотные остатки, не кодируемые иммуноглобулиновыми последовательностями зародышевых линий человека (например, мутации, вызванные случайным или сайт-специфичным мутагенезом in vitro или соматическими мутациями in vivo), например в областях CDR, особенно в области CDR3. Однако используемый в настоящем документе термин «антитело человека» не подразумевает включения антител, в которых в каркасные области последовательности человека вставлены CDR последовательности, полученные из зародышевых линий другого вида млекопитающих, например мыши.
Используемый в настоящем документе термин «рекомбинантное антитело человека» подразумевает включение всех типов антител человека, которые получают, экспрессируют, создают или выделяют с использованием рекомбинантных технологий, в том числе антител, экспрессируемых с использованием рекомбинантного вектора экспрессии, трансфектированного в клетку-хозяина (как описано ниже), антител, выделеннных из рекомбинантной комбинаторной библиотеки антител человека (как описано ниже), антител, выделенных из животного (например, мыши), трансгенного по отношению к генам иммуноглобулина человека (см., например, Taylor et al. (1992) Nucl. Acids Res. 20:6287-6295), а также антител, полученных, экспрессированных, созданных или выделенных с использованием любых других методов, использующих сплайсинг последовательностей гена иммуноглобулина человека на другие последовательности ДНК. Такие рекомбинантные антитела человека имеют вариабельную и константную области, полученные из иммуноглобулиновых последовательностей зародышевых линий человека. В ряде осуществлений, однако, такие рекомбинантные антитела человека подвергаются мутагенезу in vitro (либо при использовании животных, трансгенных по иммуноглобулину человека, соматическому мутагенезу in vivo), и, таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител оказываются последовательностями, которые, хотя и получены из последовательностей VH и VL областей зародышевых линий человека и связаны с этими последовательностями, могут отсутствовать в естественно существующем in vivo наборе последовательностей зародышевых линий человека.
Используемый в настоящем документе термин «изолированное антитело» предназначен для обозначения антитела, существенно свободного от других антител, обладающих иной антигенной специфичностью (например, изолированное антитело, которое специфично связывает NGF, существенно свободно от антител, которые специфично связывают антигены, отличные от NGF). Изолированное антитело, которое специфично связывает NGF, тем не менее, может иметь перекрестную реактивность к другим антигенам, например молекулам NGF из других видов. Более того, изолированное антитело может быть существенно свободно от иных клеточных материалов и/или химических реагентов.
Используемый в настоящем документе термин «нейтрализующее антитело» (или «антитело, нейтрализующее активность NGF») предназначен для обозначения антитела, связывание которого с NGF приводит к ингибированию биологической активности NGF. Такое ингибирование биологической активности NGF может оцениваться посредством измерения одного или нескольких показателей биологической активности NGF, таких как клеточная активация, индуцированная NGF, и связывание NGF с рецептором NGF. Данные показатели биологической активности NGF могут оцениваться при помощи одного или нескольких методов анализа in vitro или in vivo, известных специалистам (см. примеры ниже).
«CDR» или определяющая комплементарность область представляет собой область гипервариабельности, перемежаемую областями с более высоким уровнем консервативности, называемыми «остовными областями». Группу областей CDR можно определить как согласованную последовательность аминокислот.
Используемый в настоящем документе термин «поверхностный плазмонный резонанс» относится к оптическому явлению, которое позволяет проводить анализ биоспецифических взаимодействий в реальном времени за счет детектирования изменений концентраций белка в биосенсорной матрице, например с помощью системы BIACORE™ (Pharmacia Biosensor AB, Uppsala, Sweden and Piscataway, N.J.).
Используемый в настоящем документе термин «KD» предназначен для обозначения равновесной константы диссоциации конкретного взаимодействия антитело-антиген.
Используемый в настоящем документе термин «изолированная молекула нуклеиновой кислоты» применительно к нуклеиновым кислотам, кодирующим антитела или части антител (например, VH, VL, CDR3), которые связывают NGF, предназначен для обозначения молекулы нуклеиновой кислоты, в которой нуклеотидные последовательности, кодирующие антитела или части антител, свободны от других нуклеотидных последовательностей, кодирующих антитела или части антител, которые связывают антигены, отличные от NGF, и такие другие последовательности могут естественным образом располагаться по обоим концам этой нуклеиновой кислоты в геномной ДНК человека. Так, например, изолированная нуклеиновая кислота настоящего изобретения, кодирующая область VH антитела против-NGF, не содержит никаких других последовательностей, кодирующих другие области VH, которые связывают антигены, отличные от NGF человека.
Используемый в настоящем документе термин «эпитоп» включает любой детерминант, предпочтительно полипептидный детерминант, способный к специфичному связыванию с иммуноглобулином или рецептором Т-клетки. В ряде осуществлений эпитопные детерминанты включают сгруппированные на поверхности химически активные молекулы, такие как аминокислоты, боковые цепи сахаров, фосфорильные группы или сульфонильные группы, и в ряде осуществлений могут иметь специфические трехмерные структурные характеристики и/или специфические зарядовые характеристики. Эпитоп представляет собой область антигена, которая связывается с антителом. В некоторых осуществлениях считается, что антитело специфично связывается с антигеном, если оно предпочтительно опознает свой антиген-мишень в сложной смеси белков и (или) макромолекул. В предпочтительных осуществлениях считается, что антитело специфично связывается с антигеном, если равновесная константа диссоциации не превышает 10-8 М, более предпочтительно, если равновесная константа диссоциации не превышает 10-9 М, и наиболее предпочтительно, если равновесная константа диссоциации не превышает 10-10 М.
Термин «существенная идентичность» или «по существу идентичны» в отношении нуклеиновой кислоты или ее фрагмента означает, что при оптимальном сопоставлении с другой нуклеиновой кислотой (или ее комплементарной цепью) с соответствующими добавлениями или делециями наблюдается идентичность нуклеотидной последовательности не менее примерно 90% и, более предпочтительно, не менее 95%, 96%, 97%, 98% или 99% оснований нуклеотидов, что измеряется с помощью любого известного алгоритма идентичности последовательностей, например FASTA, BLAST или GAP, которые обсуждаются ниже.
Применяемый в отношении полипептидов термин «существенное сходство» или «по существу подобные» означает, что две пептидные последовательности при их оптимальном сопоставлении, например, с помощью программ GAP или BESTFIT с учетом веса гэпов по умолчанию демонстрируют идентичность последовательностей не менее 90%, и еще более предпочтительно, не менее 95%, 98% или 99%. Предпочтительно положение неидентичных остатков отличается консервативным замещением аминокислот. «Консервативное замещение аминокислот» - это такое замещение, при котором один аминокислотный остаток замещается другим аминокислотным остатком, имеющим боковую цепь (группу R) с аналогичными химическими свойствами (например, заряд или гидрофобность). В общем случае консервативное замещение аминокислот не будет приводить к существенным изменениям функциональных свойств белка. В случае если две или более аминокислотные последовательности отличаются друг от друга консервативными замещениями, процент или степень аналогичности может корректироваться в сторону увеличения, с тем чтобы учесть консервативный характер замещения. Способы такой корректировки хорошо известны специалистам в данной области. См., например, Pearson (1994) Methods Mol. Biol. 24: 307-331. К примерам групп аминокислот, имеющих боковые цепи с аналогичными химическими свойствами, относятся 1) алифатические боковые цепи: глицин, аланин, валин, лейцин и изолейцин; 2) алифатические гидроксилированные боковые цепи: серин и треонин; 3) боковые цепи с амидной группой: аспарагин и глутамин; 4) ароматические боковые цепи: фенилаланин, тирозин и триптофан; 5) боковые цепи со свойствами основания: лизин, аргинин и гистидин; 6) боковые цепи со свойствами кислоты: аспартат и глутамат; и 7) серосодержащие боковые цепи: цистеин и метионин. Предпочтительными группами для консервативного замещения аминокислот являются: валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин. В альтернативном варианте консервативное замещение представляет собой любое изменение, приводящее к положительному значению в логарифмической матрице вероятностей PAM250, описанной в работе Gonnet et al. (1992) Science 256: 1443 45. «Умеренно консервативным» замещением называется любое изменение, приводящее к неотрицательному значению в логарифмической матрице правдоподопия PAM250.
Подобие последовательностей полипептидов обычно определяют с помощью программного обеспечения для анализа последовательности. Программа для анализа белков сопоставляет подобные последовательности с использованием показателей аналогичности, задаваемых для различных замещений, делеций и других модификаций, в том числе для консервативного замещения аминокислот. Например, программное обеспечение GCG содержит такие программы, как GAP и BESTFIT, которые могут использоваться с параметрами по умолчанию для определения гомологии или идентичности последовательности между близкородственными полипептидами, например гомологичными полипептидами различных видов организмов или между исходным белком и его мутантом. См., например, GCG Версия 6.1. Полипептидные последовательности можно также сопоставлять с помощью FASTA - программы, включенной в GCG Версия 6.1, - с использованием параметров по умолчанию или рекомендуемых параметров. FASTA (например, FASTA2 и FASTA3) обеспечивает сопоставление и определяет процент идентичности последовательностей в областях с наибольшим перекрыванием между заданной и исследуемой последовательностями (см. выше Pearson (2000)). Другим предпочтительным алгоритмом сопоставления последовательности настоящего изобретения с базой данных, содержащей большое число последовательностей различных организмов, является компьютерная программа BLAST, особенно BLASTP или TBLASTN, которая использует параметры по умолчанию. См., например, Altschul et al. (1990) J. Mol. Biol. 215: 403 410 и Altschul et al. (1997) Nucleic Acids Res. 25:3389 402.
Получение антител человека
К методам получения антител человека относятся, например, VELOCIMMUNE™, технология XENOMOUSE™ (Green et al. (1994) Nature Genetics 7:13-21), «минилокусный» метод и фаговый дисплей. Технология VELOCIMMUNE™ (US 6596541, Regeneron Pharmaceuticals) включает метод получения полностью человеческих антител с высокой специфичностью по отношению к выбранному антигену. Данная технология предполагает получение трансгенных мышей с геномом, содержащим вариабельные области тяжелой и легкой цепи человека, которые функционально связаны с эндогенными локусами константной области мыши, так что в ответ на антигенную стимуляцию мышь продуцирует антитело, содержащее вариабельную область человека и константную область мыши. ДНК, кодирующая вариабельные области тяжелой и легкой цепи антитела, выделяют и функционально связывают с ДНК, кодирующей константные тяжелые и легкие цепи человека. Затем ДНК экспрессируется в клетке, которая в состоянии экспрессировать полное антитело человека. В конкретном осуществлении такой клеткой является клетка СНО.
Антитела могут использоваться в терапевтических целях для блокирования лиганд-рецепторного взаимодействия или ингибирования взаимодействия рецепторной компоненты вместо уничтожения клеток путем фиксации комплемента и участия в комплементзависимой цитотоксичности (CDC) или уничтожения клеток за счет антителозависимой клеточно-обусловленной цитотоксичности (ADCC). Константная область антитела, таким образом, важна для обеспечения способности антитела фиксировать комплемент и опосредовать клеточно-обусловленную цитотоксичность. Поэтому изотип антитела можно выбирать в зависимости от того, насколько желательно, чтобы антитело опосредовало цитотоксичность.
Иммуноглобулины человека могут существовать в двух формах, что связано с гетерогенностью шарнирной области. В одной из форм молекула иммуноглобулина содержит стабильную четырехцепочечную конструкцию с весом примерно 150-160 кДа, в которой димеры удерживаются связывающим тяжелые цепи дисульфидным мостиком. Во второй форме димеры не связаны межцепочечными дисульфидными связями, и образуется молекула с приблизительным весом 75-80 кДа, включающая ковалентно сочлененные легкую и тяжелые цепи (половина антитела). Эти формы было исключительно сложно разделить, даже после аффинной очистки.
Частота проявлений второй формы в различных изотипах интактного IgG вызвана, кроме прочего, структурными различиями, связанными с изотипом шарнирной области антитела. Замена одной аминокислоты в шарнирной области человеческого IgG4 может существенно снизить долю второй формы (Angal et al., 1993, Molecular Immunology 30:105) до уровней, обычно характерных при использовании шарнирной области человеческого IgG1. В сферу охвата настоящего изобретения входят антитела, имеющие одну или несколько мутаций в шарнирной области, областях CH2 или CH3, которые могут быть желательны, например, при продуцировании антител для повышения выхода нужной формы антитела.
Антитела настоящего изобретения предпочтительно получаются с использованием технологии VELOCIMMUNE™. Трансгенные мыши, у которых вариабельные области тяжелой и легкой цепей эндогенного иммуноглобулина заменяются соответствующими вариабельными областями человека, стимулируются представляющим интерес антигеном, и у мыши, экспрессирующей антитела, берутся лимфатические клетки (например, В-клетки). Лимфатические клетки могут сливаться с линией клеток миеломы для получения иммортализованных линий клеток гибридомы, и такие линии клеток гибридомы проходят скрининг и селекцию для идентификации тех линий клеток гибридомы, которые продуцируют антитела к представляющему интерес антигену. ДНК, кодирующая вариабельные области тяжелой и легкой цепи антитела, можно выделить и связать с нужными изотипическими константными областями тяжелой и легкой цепей. Такой белок антитела может продуцироваться в клетке, например в клетке СНО. В альтернативном варианте ДНК, кодирующая антигенспецифические химерные антитела или вариабельные домены легкой и тяжелой цепей, можно выделить непосредственно из антигенспецифических лимфоцитов.
В общем случае антитела настоящего изобретения обладают очень высокой аффинностью, как правило имея KD от примерно 10-9 до примерно 10-12 M или выше, например, не менее примерно 10-9 M, не менее 10-10 M, не менее 10-11 M или не менее 10-12 M, если измерять по связыванию с антигеном, иммобилизованным на твердой подложке или анализируемым в растворе.
Первоначально выделают химерные антитела с высокой аффинностью, имеющие вариабельную область человека и константную область мыши. Как описано ниже, антитела характеризуют и выбирают по нужным свойствам, в том числе по аффинности, селективности, эпитопу и т.п. Константные области мыши заменяют желаемыми константными областями человека, с тем чтобы получить полностью человеческие антитела, описанные в настоящем изобретении, например исходный или модифицированный IgG1 или IgG4 (например, SEQ ID No: 541, 542 или 543). Выбранная константная область может меняться в зависимости от конкретного осуществления, а свойства высокой аффинности антиген-связывания и необходимая специфичность определяются вариабельной областью.
Эпитопное картирование и связанные с ним технологии
Для скрининга антител, которые связываются с конкретным эпитопом (например, блокирующих связывание IgE с соответствующим рецептором, обладающим высокой аффинностью), можно проводить стандартный кросс-блокинг, подобно описанному в Harlow and Lane (1990) выше. К другим методам относятся мутанты сканирования аланина, пептидный блоттинг (Reineke (2004) Methods Mol Biol 248:443-63), и анализ расщепления пептидов. Кроме того, могут использоваться такие методы, как вырезание эпитопа, экстракция эпитопа и химическая модификация антигенов (Tomer (2000) Protein Science: 487-496).
Используемый в настоящем документе термин «эпитоп» относится к сайту антигена, на который реагируют B и/или T-клетки. Эпитопы B-клеток могут быть образованы как непрерывной последовательностью аминокислот, так и разрозненными аминокислотами, оказавшимися в требуемом взаимном положении в результате фолдинга белка в третичную структуру. Эпитопы, образованные непрерывной последовательностью аминокислот, как правило, сохраняются при воздействии денатурирующих растворителей, тогда как эпитопы, возникшие в результате фолдинга белка в третичную структуру, разрушаются при обработке денатурирующими растворителями. Эпитоп, как правило, формируется по крайней мере 3, а обычно по крайней мере 5 или 8-10 аминокислотами во вполне конкретной пространственной конформации.
Определение профиля с помощью модификации (MAP), также известное как определение профиля антител на основе структуры антигена (ASAP), представляет собой метод классификации большого числа моноклональных антител (mAbs) к одному и тому же антигену в соответствии со сходствами профиля связывания каждого антитела с химически или энзиматически модифицированными антигенными поверхностями (US 2004/0101920). Каждая категория может отражать уникальный эпитоп, который либо четко отличается от эпитопа, представленного в любой другой категории, либо частично перекрывается с ним. Подобная технология позволяет быстро отделять генетически идентичные антитела, так что их идентификация может быть сконцентрирована на генетически отличающихся антителах. В случае применения для скрининга гибридомы, MAP может способствовать идентификации редких клонов гибридомы, производящих mAbs с нужными характеристиками. MAP может использоваться для сортировки антител против-NGF настоящего изобретения в группы антител, связывающих различные эпитопы.
Иммуноконъюгаты
В область настоящего изобретения входит анти-NGF моноклональное антитело человека, конъюгированное с терапевтическим средством («иммуноконъюгат»), например цитотоксином, химиотерапевтическим препаратом, иммунодепрессантом или радиоактивным изотопом. К цитотоксическим средствам относятся любые вещества, которые оказывают разрушительное воздействие на клетки. Примеры пригодных для применения цитотоксических средств и химиотерапевтических средств для образования иммуноконъюгатов известны специалистам в области, см., например, WO 05/103081.
Биспецифичность
Антитела настоящего изобретения могут быть моноспецифическими, биспецифическими или мультиспецифическими. Мультиспецифические антитела могут быть специфичны по отношению к различным эпитопам одного целевого полипептида или могут содержать антиген-связывающие домены, специфичные по отношению к нескольким целевым полипептидам. См., например, Tutt et al. (1991) J. Immunol. 147:60-69. Анти-NGF антитела человека могут быть связаны с другими функциональными молекулами или же экспрессироваться одновременно с ними, например с другим пептидом или белком. Например, антитело или его фрагмент могут быть функционально связаны (например, химической связью, генетическим слиянием, нековалентной ассоциацией или иным образом) с одной или несколькими молекулярными структурами, например с другим антителом или фрагментом антитела, с образованием биспецифичного или мультиспецифичного антитела с дополнительной специфичностью связывания.
Терапевтическое применение и составы препаратов
В изобретении приводятся терапевтические препараты, включающие антитела против-NGF или их антиген-связывающие фрагменты, входящие в сферу охвата настоящего изобретения. Введение терапевтических препаратов в соответствии с настоящим изобретением будет осуществляться в подходящих носителях, наполнителях и прочих веществах, которые включаются в состав препаратов, чтобы обеспечить более эффективное распространение, доставку, переносимость и пр. Множество подходящих составов можно найти в формулярах, известных всем специалистам в области фармацевтической химии: Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, PA. К таким препаратам относятся, например, порошки, пасты, мази, желе, воски, масла, липиды, липид-содержащие (катионные или анионные) везикулы (например, LIPOFECTIN™), конъюгаты ДНК, безводные абсорбционные пасты, эмульсии масла в воде и воды в масле, эмульсии Carbowax (полиэтиленгликоли различного молекулярного веса), полутвердые гели и полутвердые смеси, содержащие Carbowax. См. также Powell et al. "Compendium of excipients for parenteral formulations" PDA (1998) J. Pharm. Sci. Technol. 52:238-311.
Дозу можно менять в зависимости от возраста, веса и роста пациента, получающего лечение, заболевания или патологических состояний пациента, способа введения и пр. При использовании антитела настоящего изобретения для лечения различных патологических состояний и заболеваний, связанных с NGF, в том числе воспалительной боли, нейропатической и/или ноцицептивной боли, гепатоклеточной карциномы, рака молочной железы, цирроза печени и пр., для взрослых пациентов предпочтительно вводить внутривенно антитела настоящего изобретения, как правило, в разовой дозе примерно от 0,01 до 20 мг на кг веса тела, более предпочтительно примерно от 0,02 до 7 мг, примерно от 0,03 до 5 мг, или примерно от 0,05 до 3 мг на кг веса тела, предпочтительно примерно от 0,1 до 10 мг на кг веса тела, и еще более предпочтительно примерно от 0,1 до 5 мг на кг веса тела. В зависимости от тяжести состояния можно корректировать частоту и продолжительность лечения.
Известны различные системы доставки, и они могут использоваться для введения лекарственного препарата настоящего изобретения, например инкапсуляция в липосомы, микрочастицы, микрокапсулы, рекомбинантные клетки, способные экспрессировать мутантные вирусы, опосредованный рецепторами эндоцитоз (см., например, Wu et al. (1987) J. Biol. Chem. 262:4429-4432). К методам введения, среди прочих, относятся чрескожный, внутримышечный, внутрибрюшинный, внутривенный, подкожный, интраназальный, эпидуральный и пероральный. Препарат может вводиться любым подходящим способом, например вливанием или болюсной инъекцией, абсорбцией через эпиталиальные или кожно-слизистые оболочки (например, слизистую ротовой полости, слизистую прямой кишки и кишечника и пр.) и может применяться совместно с другими биологически активными средствами. Введение может быть системным или местным.
Фармацевтический препарат может также доставляться в везикуле, в частности в липосоме (см. Langer (1990) Science 249:1527-1533; Treat et al. (1989) в Liposomes in the Therapy of Infectious Disease and Cancer, Lopez Berestein and Fidler (eds.), Liss, New York, сс. 353-365; Lopez-Berestein, ibid., сс. 317-327; см. в целом там же.
В определенных ситуациях лекарственный препарат может доставляться в системе контролируемого высвобождения. В одном из осуществлений может использоваться насос (см. Langer; Sefton (1987) CRC Crit. Ref. Biomed. Eng. 14:201). В другом осуществлении могут использоваться полимерные материалы (см. Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Florida (1974). В еще одном варианте осуществления систему контролируемого высвобождения можно установить в непосредственной близости от цели препарата, а потому потребуется лишь малая доля от системной дозы (см., например, Goodson, in Medical Applications of Controlled Release, vol. 2, pp. 115-138, 1984). Другие системы контролируемого высвобождения обсуждаются в обзоре Langer (1990) Science 249:1527-1533.
К инъекционным препаратам могут относиться лекарственные формы для внутривенных, подкожных, чрескожных и внутримышечных инъекций, капельных вливаний и пр. Такие инъекционные препараты можно приготовить с помощью известных методов. Например, инъекционные препараты можно приготовить, в частности, посредством растворения, суспендирования или эмульгирования описанного выше антитела или его соли в стерильной водной среде или в масляной среде, которые обычно применяются для инъекций. В качестве водной среды для инъекций предлагаются, например, физиологический раствор, изотонический раствор, содержащий глюкозу и другие вспомогательные вещества и пр., которые могут использоваться в сочетании с соответствующим солюбилизирующим средством, например спиртом (в частности, этанолом), многоосновным спиртом (например, пропиленгликолем, полиэтиленгликолем), неионогенным поверхностно-активным веществом [например, полисорбатом 80, НСО-50 (аддуктом полиоксиэтилена (50 моль) и гидрогенизированного касторового масла] и пр. В качестве масляной среды используются, например, кунжутное масло, соевое масло и пр., которые могут применяться в сочетании с солюбилизирующим средством, например бензилбензоатом, бензиловым спиртом и пр. Приготовленный таким образом препарат для инъекций предпочтительно фасовать в соответствующие ампулы.
Фармацевтические препараты для перорального или парентерального введения, описанные выше, предпочтительно готовить в лекарственных формах с разовой дозой, подбираемой в соответствии с дозировкой активных ингредиентов. К таким лекарственным формам с разовой дозой относятся, например, таблетки, пилюли, капсулы, инъекции (ампулы), суппозитории и пр. Количество содержащегося в разовой дозе антитела обычно составляет от 5 до 500 мг на лекарственную форму; в форме инъекции предпочтительно, чтобы количество содержащегося антитела составляло примерно от 5 до 100 мг и примерно от 10 до 250 мг в случае других лекарственных форм.
Монотерапия и комбинационная терапия. В изобретении предлагаются терапевтические методы, в рамках которых антитело или фрагмент антитела настоящего изобретения применяется для лечения боли, связанной с самыми различными патологическими состояниями с участием NGF. Антитела против-NGF или их фрагменты, описанные в настоящем изобретении, особенно эффективны для лечения боли, вызванной любым патологическим состоянием, которое связано с нейрогенной, нейропатической или ноцицептической болью. В предпочтительных осуществлениях для нейропатической боли предпочтительна терапия при реперкуссионной невралгии тройничного нерва, постгерпетической невралгии, фантомной боли в ампутированных конечностях, фибромиалгии, симпатической рефлекторной дистрофии и нейрогенных болях. В других предпочтительных осуществлениях предпочтительно проводить лечение боли при раке, в особенности боли при раке кости, боли при остеоартрите или ревматоидном артрите, боли в нижнем отделе спины, боли послеоперационного шва, боли при переломах, боли при остеопорозных переломах, остеопорозе, суставной боли при подагре, диабетической нейропатии, ишиасе, боли, связанной с обострениями при серповидноклеточной анемии, мигрени и другими нейропатическими и/или ноцицептивными болями.
К другим показаниям относится, например, лечение рака молочной железы (Adriaenssens et al. (2008) Cancer Res 68:346-51). В конкретных осуществлениях терапевтических методов настоящего изобретения пациент, страдающий от боли в суставах, связанной с подагрой, проходил терапию комбинацией антитела или фрагмента антитела настоящего изобретения, в некоторых случаях со вторым терапевтическим средством. В одном из осуществлений в качестве второго терапевтического средства предпочтительно применяли антагонист интерлейкина-1 (IL-1), например рилонасепт («ловушка IL-1», Regeneron). В качестве подходящих вторых терапевтических средств может выступать один или несколько средств, выбранных из группы, в которую входят рилонасепт, анакинра (KINERET®, Amgen), рекомбинантная негликозилированная форма антагонистов рецепторов IL-1 человека (IL1Ra), препарат анти-IL-18, например IL-18BP или его производное, ловушка IL-18, или антитело, например анти-IL-18, анти-IL-18R1, анти-IL-18Racp, анти-IL-6 и/или антитело анти-IL6Ra. К другим формам совместной терапии, которые можно сочетать с антителом NGF или его антиген-связывающим фрагментом в качестве монотерапии или в сочетании с антагонистом IL-1, относятся колхицин в малых дозах, аспирин или другие NSAID, стероиды, например преднизолон, метотрексат, циклоспорин А в малых дозах, ингибиторы TNF, например ENBREL® или HUMIRA®, другие ингибиторы воспаления, например ингибиторы каспазы-1, p38, IKK1/2, CTLA-4Ig, и пр., и/или совместной терапии, в частности с использованием ингибиторов синтеза мочевой кислоты для подавления накопления мочевой кислоты в организме, например, аллопуринол, стимуляторы выведения мочевой кислоты для ускорения быстрого выведения мочевой кислоты, накопленной в организме, такие как пробенецид, сульфинпиразон и/или бензбромарон, являются стимуляторами выведения мочевой кислоты; кортикостероиды; нестероидные противовоспалительные препараты (NSAID), противоэпилептические препараты, например топирамат, габапентин, прегабаблин; целекоксиб; или же другой нейротрофин, например NT-3.
ПРИМЕРЫ
Приведенные ниже примеры предназначены для того, чтобы дать специалистам в области полную информацию и описание того, как следует получать и использовать способы и препараты настоящего изобретения, и не призваны ограничивать сферу охвата того, что изобретатели рассматривают как предмет своего изобретения. Предпринимались попытки добиться точности в отношении используемых показателей (например, количеств, температуры и пр.), но необходимо учитывать некоторые погрешности и отклонения эксперименов. Если не указано иначе, под частями понимаются весовые части, молекулярным весом называют усредненный молекулярный вес, температура приводится в градусах Цельсия, а давление находится на уровне атмосферного или близко к этому уровню. Статистический анализ проводили в соответствии со смешанным факториальным анализом ANOVA с применением апостериорных критериев Бонферрони или достоверной значимой разности Тьюки.
Пример 1. Иммунизация и получение антител
Грызуны могут быть иммунизированы с помощью любого метода, известного специалистам в области (см., например, Harlow and Lane, Antibodies: A Laboratory Manual: Cold Spring Harbor Press, New York; Malik and Lillehoj, Antibody techniques: Academic Press, САН ДИЕГО). В предпочтительном осуществлении белок NGF человека вводят непосредственно мышам с локусами ДНК, кодирующими вариабельную область тяжелой цепи человеческого Ig и вариабельную область легкой цепи каппа (VELOCIMMUNE™, Regeneron; US 6,596,541), в адъюванте для стимулирования иммунного ответа. Такой адъювант включает полный и неполный адъювант Фрейнда, систему адъюванта MPL+TDM (Sigma) или RIBI (мурамил-дипептид) (см. O'Hagan, Vaccine Adjuvant, Human Press, 2000, Totawa, NJ). Такой адъювант может препятствовать быстрому разбавлению полипептида, удерживая антиген в локальном депо, и может содержать факторы, которые способны стимулировать иммунный ответ хозяина. В одном варианте осуществления NGF вводят косвенным образом в виде ДНК-плазмида, который содержит ген NGF и экспрессирует NGF при помощи механизма экспрессии клеточного белка хозяина для получения полипептида антигена in vivo. При обоих подходах для получения оптимальных анти-антигенных ответов мышам вводят бустер-инъекции каждые 3~4 недели, и через 10 дней после каждой инъекции отбирают пробы сыворотки. Иммунный ответ антител контролируют с использованием стандартных методов прямого антиген-связывания ELISA. Пробы сыворотки после стимуляции, разбавленные в ходе 3-кратных последовательных разбавлений, наносят на планшеты, покрытые NGF. Титр сыворотки определяется как разбавление пробы сыворотки, которая давала при анализе двукратный по сравнению с фоном сигнал. Животные с оптимальной ответной реакций за 3-4 дня до эвтаназии получают последнюю бустер-инъекцию внутривенно и внутрибрюшинно без адъюванта. Собранные спленоциты обрабатывают, как описано ниже, с тем чтобы получить антиген-специфичные моноклональные антитела.
Пример 2. Выделение моноклональных антител
В одном варианте осуществления В-клетки, экспрессирующие антитело, сливают с клетками миеломы мыши, чтобы образовались клетки гибридомы. Гибридные клетки высевают в 96-луночные планшеты с селекцией НАТ и позволяют расти от 10 до 20 дней. Проводят скрининг кондиционированной среды с растущими клетками гибридомы для проверки связывания антигена и активности блокирования рецептора, как описано ниже. Клетки гибридомы, экспрессирующие представляющие интерес антитела, субклонированы из монокультуры с использованием проточной цитометрии, и из клональных клеток гибридомы были клонированы и секвенированы гены VH и VL. Из культур антиген-специфичных гибридом также выделяли белки антител с использованием обедненной IgG среды (Invitrogen), и их характеристики устанавливали в соответствии с описанной ниже процедурой.
В другом осуществлении антиген-специфические антитела выделяют непосредственно из антиген-положительных B-клеток без иммортализации с специфическими клетками миеломы, с получением клетки-хозяина СНО, производящей стабильное рекомбинантное антитело, как описано в USSN 11/809482 (публикация патента США No 2007/0280945).
Пример 3. Первичное антиген-связывание и скрининг блокирования рецептора
Для идентификации гибридом, продуцирующих антиген-специфичные антитела, кондиционированную среду отбирали из 96-луночных планшетов с клеточными культурами через 10-20 дней после слияния, и антиген-связывающую специфичность определяли с помощью высокопроизводительного метода прямого связывания ELISA. Кратко можно сказать, что кондиционированная среда в разбавлении 1:10 и 1:100 связывалась с рекомбинантным NGF белком, нанесенным на планшеты MAXISORB™ (Nunc) в концентрации 100 нг/лунку. Связанные на планшете антитела определяли с помощью специфического, конъюгированного с пероксидазой хрена поликлонального антитела козьего антимышиного IgG Fcγ (Jackson Immuno Lab). Планшеты проявляли с помощью субстратов, содержащих тетраметилбензидин (BD Pharmigen), и регистрировала оптическую плотность на уровне OD450nm. Параллельно пробы с таким же разбавлением наносили на обработанные стрептавидином и меченные биотином планшеты NGF, и детектировали связанные с планшетом антитела. Лунки, демонстрирующие активность связывания для любого из планшетов, отбирали для экспансии клеточной культуры и сохраняли при замораживании, а содержащие антитела супернатанты использовали для дальнейшего анализа с целью получения характеристик специфичности, аффинности и функциональности.
Кроме скрининга прямого связывания антигена, использовали также функциональный скрининг, с тем чтобы определить клоны, продуцирующие антитела с желаемыми свойствами. Планшеты Maxisorb выдерживали в течение ночи при 4oC для покрытия рекомбинантным TrkA-hFc человека в концентрации 100 нг/лунка. Кондиционированную среду при разбавлении 1:2 и 1:10 связывали с раствором 2 нг/мл биотин-NGF в течение 1 часа до переноса на покрытые TrkA-hFc планшеты для измерения связанного с планшетом биотина-NGF. Связанные на планшете биотин-NGF определяли с помощью конъюгированного с пероксидазой хрена стрептавидина (Pierce) и проявляли с помощью субстратов, содержащих тетраметилбензидин (BD Pharmigen), при регистрации оптической плотности. Гибридомы, в которых культуральная среда препятствовала связыванию биотина-NGF с TrkA-hFc, относили к потенциальным блокаторам и исследовали дополнительно.
Аналогичные процедуры скрининга in vitro проводили с 96-луночной кондиционированной средой клеток CHO, трансфектированных полностью человеческим IgG, содержащим V-гены, полученным непосредственно из антиген-положительных В-клеток. Кроме того, проводили скрининг образцов для выявления активности связывания NGF с использованием покрытых антигеном гранул LUMINEX™, антиген-специфическое антитело к которым детектировали с помощью Fcγ-специфичных поликлональных антител козы античеловеческого IgG. Для антиген-связывающих антител проводили измерения аффинности с использованием BIACORE™. Вкратце можно сказать, что антитела из супернатантов неочищенной культуры фиксировали на поверхности аминосвязанного специфического поликлонального антитела hFc. Отслеживали связывание антигена при фиксированной концентрации. Для подгонки сенсограммы связывания использовали модель бимолекулярного взаимодействия 1:1, с тем, чтобы определить антиген-связывающую аффинность (KD) с помощью кинетических констант скоростей ka и kd для взаимодействия каждого из антител при идентичных условиях. В частности, Fcγ-специфичные поликлональные антитела козы античеловеческого IgG ковалентно фиксировали на поверхности чипа CM-5, и содержащие антитела супернатанты CHO вводили со скоростью 1 мкл/мин в течение 5 минут, после чего проводили промывку буфером. NGF человека (25 нМ) вводили в течение 3 минут, чтобы обеспечить связывание NGF с поверхностью иммобилизированных человеческих антител. Сразу же после введения NGF на поверхность наносили буфер со скоростью 100 мкл/мин в течение примерно 10 минут и регистрировали спад сигнала RU. Поверхность регенерировали для удаления связанных антител и NGF и повторяли цикл со следующим образцом супернатанта СНО.
Пример 4. Определение антиген-связывающей аффинности
Антиген-связывающие аффинности антител для NGF человека определяли из поверхностной кинетики методом поверхностного плазмонного резонанса биосенсора в реальном времени (BIACORE™). Антитела удерживали на поверхности поликлонального антитела козьего, античеловеческого или антимышиного IgG, образованной посредством прямого аминного связывания удержанного антитела с чипом BIACORE™. На поверхности захваченных антител вводили различные концентрации NGF человека, и связывание антигена с антителом и диссоциацию связанного комплекса контролировали в реальном времени. Расчет равновесной константы диссоциации (KD) и константы скорости диссоциации осуществляли при помощи кинетического анализа, причем константу скорости диссоциации использовали для расчета полупериода диссоциации комплекса антиген/антитело (t1/2) (таблица 1). Гуманизированное античеловеческое моноклональное антитело NGF E3 (“RN624”) (танезумаб; CAS Registry No. 880266-57-9; публикация патента США 2004/0237124) использовали в качестве контрольного антитела.
|
Антиген-связывающие аффинности некоторых очищенных антител для NGF также определяли из поверхностной кинетики методом поверхностного плазмонного резонанса биосенсора в реальном времени (BIACORE™), как описано выше. Для удобства пользования антитело 301272-3H10-A10 переименовали в «REGN261» (HCVR/LCVR SEQ ID No: 84/92 и hIgG1 SEQ ID No: 541); 301272-6E07-D10 переименовали в «REGN263» (HCVR/LCVR SEQ ID No: 208/216 и hIgG1 SEQ ID No: 541). Протестированные производные антитела включали REGN472 (HCVR/LCVR SEQ ID No: 100/102 и hIgG1 SEQ ID No: 541), REGN474 (HCVR/LCVR SEQ ID No: 100/102 и мутант hIgG4 SEQ ID No: 543), REGN475 (HCVR/LCVR SEQ ID No: 108/110 и мутант hIgG4 SEQ ID No: 543), REGN476 (HCVR/LCVR SEQ ID No: 224/226 и мутант hIgG4 SEQ ID No: 543), и REGN477 (HCVR/LCVR SEQ ID No: 232/234 и мутант hIgG4 SEQ ID No: 543).
|
Пример 5. Перекрестная реакционная способность нейротрофина-3 (NT-3)
NGF и NT-3 принадлежат к семейству факторов роста нервов и относятся к основным небольшим секреторным белкам, которые обеспечивают выживание конкретных популяций нейронов. Несмотря на определенные аминокислотные сходства этих двух нейротрофинов, их биологические функции могут различаться (Barde et al. 1990 Prog Growth Factor Res 2(4):237-48).
Изучали перекрестную реакционную способность связывания антител против-NGF и человеческого NT-3. Вкратце можно сказать, что поликлональное антитело козы античеловеческого IgG химически связывалось с чипом CM5. Моноклональные антитела против-NGF вводили таким образом, чтобы образовалась поверхность с примерно от 50 до 900 RU иммобилизированных антител посредством взаимодействия со связанными с чипом поликлональными антителами. На поверхность наносили белок NGF или NT-3 в концентрации 20 нМ с последующей промывкой буфером, чтобы дать возможность диссоциировать связанным лигандам. Контролировали фазу ассоциации и диссоциации и проводили анализ данных. Результаты приведены в таблице 3 (NB = активность связывания не наблюдалась). В отличие от контрольного антитела (RN624), все тестируемые антитела не проявляли поддающегося измерению связывания с NT-3, что указывает на более высокую степень антиген-специфичности по отношению к контрольному антителу.
|
Конкурентный анализ в растворе на основе OCTETTM также использовали для измерения способности REGN475 и RN624 конкурировать в растворе за связывание с NT-3, NGF или с нейротрофическим фактором из мозга человека (hBDNF). Вкратце можно сказать, что образцы антитело-антиген готовили преинкубированием контрольного антитела RN624 (2,5 мкг/мл) или REGN475 (2,5 мкг/мл) с различными концентрациями NT-3 (от 0 до 4 мкМ), hBDNF (от 0 до 4 мкМ) или NGF (от 0 до 0,2 мкМ) в течение 1 часа при 30°C. Стрептавидиновые сенсоры FA с высоким уровнем связывания (HBS, ForteBio, Inc., Калифорния) инкубировали с биотином-NGF при 2 мкг/мл в течение 10 минут при 30°C. Связанные с биотин-NGF сенсоры затем инкубировали с преинкубированными образцами антитело-антиген в течение 10 минут при 30°C. Изменение вязкости биологического слоя измерялось после инкубации. Величину связывания нормировали в процентах от связывания относительно связывания антитела в отсутствие конкурента. Как показано в таблице 4, связывание между NGF и RN624 блокировалось NT-3 зависимым от дозы образом, тогда как связывание между REGN475 и NGF не блокировалось NT-3. Присутствие hBDNF не препятствовало связыванию как RN624, так и REGN475 с NGF, тогда как присутствие растворимого NGF практически полностью блокировало связывание и RN624, и REGN475 с иммобилизированным NGF.
|
Связывание между выборочными очищенными человеческими анти-NGF антителами REGN472, REGN474, REGN475, REGN476, REGN477 или контрольным антителом RN624 и NT-3 также оценивали с использованием анализа BIACORETM с концентрациями NT-3 в диапазоне от 1,25 нМ до 40 нМ. В то время как контрольное антитело (RN624) связывалось с NT-3 с KD 1,1 нМ, ни одно из испытываемых антител не проявляло поддающейся измерению аффинности к NT-3.
Пример 6. Перекрестная реакционная способность по отношению к NGF мышей и крыс
NGF человека (NGF) имеет высокую гомологичность по аминокислотной последовательности NGF мыши (mNGF) и NGF крысы (rNGF) с уровнем идентичности примерно 90%. Аффинность связывания антител с mNGF и rNGF определяли по описанной выше методике. Все антитела демонстрировали перекрестную реакционную способность к mNGF и rNGF. Одна группа антител прочно связывала NGF всех видов со значением KD меньше 10 пМ; вторая группа предпочтительно связывала NGF и демонстрировала KDs > ~ 100 пМ для mNGF и rNGF (контроль = RN624) (таблица 5).
|
Также определяли аффинность связывания некоторых очищенных антител против-NGF с mNGF и rNGF (таблица 6).
|
Пример 7. Ингибирование связывания NGF с рецепторами TrkA/hFc и p75/hFc
Для идентификации блокирующих антител разрабатывали метод анализа блокирования рецепторов с помощью прибора BIACORE™ 3000. Рекомбинантные человеческие белки TrkA-hFc и p75-hFc фиксировали аминной связью на чипе CM5 до плотности примерно 5000-6000 RU. NGF человека (от 10 нМ до 25 нМ) связывали с поверхностью TrkA и p75 для определения максимального значения RU для связывания NGF. Затем проводили регенерацию поверхности, и NGF в концентрации от 10 нМ до 25 нМ смешивали с избыточными молярными концентрациями индивидуальных антител или растворимых белков рецепторов, а раствор наносили на поверхность регенерированного чипа, чтобы зафиксировать связывающие сигналы остаточного свободного NGF. В таблице 7 приводится процентная доля свободного NGF, закрепленного на TrkA и p75, в присутствии антитела или белка рецептора. Максимальной величине RU для связывания человеческого NGF в отсутствие антитела присваивали значение 100%. В качестве положительного контроля использовали RN624, TrkA-hFc и p75-hFc в растворе, а в качестве отрицательного контроля связывания использовали контроль IgG1 (AVASTIN®; Genentech, Калифорния).
|
Способность некоторых испытываемых антител REGN472, REGN474, REGN475, REGN476 и REGN477, а также контрольного антитела RN624 блокировать связывание человеческого NGF с рецепторами человека TrkA и p75 также количественно измеряли с помощью конкурентного сэндвичевого анализа ELISA, в ходе которого присутствие антитела с фиксированной концентрацией NGF в растворе не позволяло NGF связываться с TrkA-hFc или p75-hFc, нанесенными на планшет для микротитрования. NGF человека, использованный в ходе анализа, представлял собой рекомбинантный белок, продуцируемый в E. coli, а человеческие белки TrkA-hFc и p75-hFc были димерными слитыми белками, состоящими из двух внеклеточных доменов соответствующих рецепторов, слитых последовательно с Fc-частью человеческого IgG1. Меченный биотином белок NGF с фиксированной концентрацией 50 пМ титровали различными количествами антитела с концентрацией от 1,5 пМ до 1,5 нМ в растворе в течение одного часа при комнатной температуре. Количество несвязанного свободного биотина-NGF в смесях растворов затем определяли посредством фиксации биотина-NGF на планшетах для микротитрования, покрытых hTrkA-hFc или hp75-hFc, после чего связанный с планшетом биотинилированный NGF детектировали с помощью системы стрептавидин-пероксидаза из хрена. В частности, планшеты для микротитрования готовили посредством нанесения на них растворов 0,5 мкг/мл hTrkA-hFc или 1 мкг/мл hp75-hFc в PBS-буфере в течение ночи при 4°C с последующим блокированием планшетов 0,5% BSA перед использованием. Для измерения несвязанного биотин-NGF преинкубированное антитело и растворы биотин-NGF переносили на покрытые рецептором планшеты с последующей инкубацией в течение 1 часа при комнатной температуре. Связанный с планшетом биотин-NGF определяли с помощью конъюгированного с пероксидазой хрена стрептавидина и проявляли с помощью колориметрического субстрата ТМВ с регистрацией OD450 нм. Зависимость значений OD450 нм от концентраций REGN475 в растворах перед связыванием анализировали на основе сигмоидной модели ответа на дозу, поставляемой PRISMTM (Graph Pad, Калифорния). Прогнозируемое значение IC50, которое определяется как концентрация антитела, необходимая для блокирования 50% связывания 50 пМ биотинилированного NGF с покрытыми рецептором планшетами, использовали в качестве индикатора способности антитела блокировать связывание NGF с hTrkA-hFc или hp75-hFc. В таблице 8 приводятся значения IC50 каждого антитела, проходившего тестирование по отношению к hTrkA-hFc и hp75-hFc. Контроль mAb = RN624.
|
Пример 8. Ингибирование связывания NT-3 с рецепторами TrkA-, TrkB-, TrkC- и p75/hFc
Также тестировали связывание 20 нМ человеческого NT-3 с поверхностью TrkA-, TrkB-, TrkC- и p75-hFc человека, соответственно, в присутствии 500 нМ REGN475, RN624 и AVASTIN® (контроль IgG1). TrkA-hFc человека (9300 RU), TrkB-hFc(6000 RU) человека, TrkC-hFc (9100 RU) человека и p75-hFc (7500 RU) человека ковалентно связывали с поверхностью чипа BIACORE® CM5 посредством аминного сочетания. 20 нМ человеческого NT-3 смешивали с 500 нМ контроля (контроль IgG1 AVASTIN®), REGN475, RN624, hTrkA-hFc, TrkB-hFc, TrkC-hFc или p75-hFc в растворе. Смесь для связывания сначала инкубировали при комнатной температуре до равновесного состояния (примерно 1 час), а затем вводили на поверхности TrkA-hFc, TrkB-hFc, TrkC-hFc и p75-hFc. Измеряли уровень связывания человеческого NT-3 в каждом образце. RU связывания в каждом образце нормировали в соответствии с величиной RU для отрицательного контрольного образца (то есть 20 нМ человеческого NT-3 с 500 нМ AVASTIN®) и выражали в % связывания с поверхностями Trk (таблица 9). REGN475 не демонстрировал практически никакой конкуренции со связыванием NT-3 с рецепторами, тогда как остальные образцы в значительной степени блокировали связывание NT-3 с рецепторами.
|
Пример 9. Нейтрализация биологического эффекта NGF in vitro
Способность антител NGF блокировать активность роста клеток, зависимая от NGF и опосредованная рецептором TrkA, оценивали с использованием клеток MG87, стабильно трансфектируемых плазмидой, которая кодирует человеческий рецептор TrkA. Вкратце говоря, трансфектированные клетки обрабатывали трипсином и ресуспендировали в концентрации примерно 2,5×105 клеток в мл, а затем высевали по 5000 клеток на лунку в 96-луночный планшет для культур тканей. Очищенные белки антител подвергали последовательному разбавлению в указанной среде плюс 0,1% BSA и добавляли к клеткам на планшете в концентрациях от 0 до 500 нМ. NGF человека добавляли в лунки до конечной концентрации 373 пМ. Ответ измеряли после инкубации клеток в течение 3 дней при 37°C во влажном инкубаторе с 5% CO2. Активность роста клеток определяли с помощью набора CCK8 (Dojindo) и регистрировали OD450нм. Зависимость сигналов от концентраций антитела анализировали с указанием значений IC50 (таблица 10, столбец 2).
Способность антител NGF блокировать сигнал NGF для активности, опосредованной рецепторами p75 и TrkA, также измеряли in vitro с использованием линии хромаффинных клеток крыс PC12, которые обеспечивают эндогенную экспрессию обоих рецепторов (Urdiales et al. 1998 J. Neuroscience 18(17):6767-6775). Вкратце можно сказать, что PC12 клетки стабильно трансфектировались репортерной плазмидой, содержащей элемент ответа сыворотки (SRE), связанный с геном люциферазы. Трансфектированные клетки ресуспендировали в концентрации примерно 2,5×105 клеток в мл, а затем высевали по 50000 клеток на лунку в 96-луночный планшет для культур тканей, выдерживая в среде Opti-MEM в течение ночи. Очищенные белки антител подвергали последовательному разбавлению в среде (DMEM плюс 0,1% BSA) и добавляли к клеткам на планшете в концентрациях от 0 до 100 нМ. NGF человека добавляли в лунки до конечной концентрации 12,5 пМ. Активность люциферазы измеряли после инкубации клеток в течение 6 часов при 37°C во влажном инкубаторе с 7,5% CO2 с использованием системы анализа люциферазы BRIGHT GLOW™ (Promega). Значения IC50 определяли согласно описанию выше и указывали в столбце 3 таблицы 10. Контроль mAb = RN624.
|
Способность некоторых очищенных антител против-NGF, REGN472, REGN474 и REGN475, а также контроля mAb RN624 блокировать сигналы NGF через опосредованную рецепторами p75 и TrkA активность в линии клеток PC12 также оценивали с помощью описанного выше люциферазного метода анализа (таблица 11).
|
Способность антител против-NGF, REGN475 и контрольного антитела блокировать сигналы NT-3 через опосредованную рецепторами p75 и TrkA активность в линии клеток PC12 оценивали с помощью описанного выше люциферазного метода анализа, модифицированного за счет замены 12,5 пМ NGF на 75 нМ NT-3. Результаты показали, что контроль mAb RN624 блокировал сигналы NT-3 с IC50 примерно 104,8 нМ, тогда как в данных экспериментальных условиях REGN475 не влияло на сигнал NT-3.
Кроме того, был разработан метод биологической пробы для определения способности антител против-NGF, REGN475 и RN624 нейтрализовать опосредованную NT-3 клеточную функцию за счет TrkC in vitro. Генно-инженерную линию клеток HEK293, экспрессирующих TrkC, трансфектировали репортерной плазмидой SRE-люциферазы. NT-3 регулирует экспрессию люциферазы в 6-часовой пробе. Способность REGN475 и RN624 блокировать сигнал NT-3 за счет активности, опосредованной рецептором TrkC в этой генно-инженерной клеточной линии, оценивали по люциферазному методу анализа. Генно-инженерную линию клеток HEK293 высеивали на 96-луночные планшеты в концентрации 1×104 клеток/лунку в бессывороточной среде и инкубировали в течение ночи при 37°С, 5% CO2. REGN475 и RN624 в концентрациях от 1,6 мкМ до 28 пМ преинкубировали с 15 пМ NT-3 в течение 1 часа, и смесь добавляли к клеткам. Клетки затем инкубировали при температуре 37°C в атмосфере 5% CO2 в течение 6 часов. Активность люциферазы определяли при добавлении в соответствующих объему лунки количеств BRIGHT GLOW™ (Promega). Результаты показали, что RN624 ингибировал опосредованную NT-3 активность люциферазы с IC50 примерно 150-200 нМ в присутствии постоянной концентрации 15 пМ NGF, тогда как REGN475 не ингибировал опосредованную NT-3 активность люциферазы.
Пример 10. Нейтрализация биологической активности NGF in vivo
Тест на воспалительную боль с полным адъювантом Фрейнда (ПАФ). Для того чтобы установить, в состоянии ли антитела против-NGF купировать боль в модели хронической периферической воспалительной боли мышей, полный адъювант Фрейнда (ПАФ) вводили подкожно (п/к) в заднюю лапу самцов мышей линии C57BL/6, вызывая термическую гиперальгезию, которую оценивали по тесту Харгрейвса (Torres et al. (2007) Pain 130:267-278). Контрольные мыши получали чистый носитель (то есть PBS). После адаптации мышей в аппарате Харгрейвса (модель 336, IITC Life Science) в течение 2-3 часов в день в течение 3 дней они проходили тестирование в аппарате при активных установках интенсивности, равных 17%. Во избежание повреждения тканей использовали время отсечки 25 с. Для каждой из мышей отсчет показаний производили трижды в течение периода 30 минут ежедневно, и для анализа использовали медианную латентность. После получения базисных значений в аппарате Харгрейвса за 1 час до введения 50% раствора ПАФ (10 мг/20 мкл) в подошву задней лапы в дозе 10 мг/кг или 25 мг/кг п/к вводили тестируемые антитела против-NGF, 301272-7E05-F6 (REGN268) и 301272-7G09-E4 (REGN270), а также гуманизированное антитело против-NGF (RN624) в качестве положительного контроля. Тест Харгрейвса повторяли ежедневно в течение до 4 дней после инъекции ПАФ и рассчитывали % снижения по сравнению с базисными показателями латентности отдергивания лапы (таблицы 12 и 13, средний % изменения ± СОС). Значительное уменьшение термической гиперальгезии наблюдалось по крайней мере в один из дней анализа для каждого из тестируемых антител по сравнению с контрольными мышами, которые получали только носитель (p < 0,001-0,05). Не регистрировалось статистического различия между тестируемыми антителами и контрольным антителом. Таблица 12: n=7 для каждой группы; все группы 10 мг/кг. Таблица 13: носитель: n=5; контроль RN624: n=5, 10 мг/кг; оба REGN269: n=9.
|
|
Модель боли послеоперационного шва. Модель боли послеоперационного шва у грызунов, при которой разрез подошвы задней лапы вызывает повышенную чувствительность к прикосновениям, защитное поведение и термическую гиперальгезию, использовали для изучения эффективности терапии антителами против-NGF. При операции по рассечению подошвы у мышей C57BL/6 под изофлураном проводили разрез через кожу, фасцию, после чего изолировали нижележащую мышцу сгибателя, которую рассекали вертикально. После наложения шва и заживления, мышей в течение 5 дней проверяли на термическую анальгезию в ходе теста Харгрейвса и на защитное поведение в тесте нагрузки на лапу (модель 600, IITC Life Science). Разовую п/к инъекцию носителя (n=7), mAb REGN268 (n=7) или контроля mAb RN624 (n=7) в дозе 10 мг/кг проводили за 1 час до рассечения (таблица 14, среднее процентное изменение от базисного значения Харгрейвса ± СОС). В таблице 15 приводятся результаты теста нагрузки на лапу (средний процент распределения веса на поврежденную конечность ± СОС) (n=7 для каждой группы, контроль RN624 и REGN268, по 10 мг/кг каждый). В обоих тестах предварительная обработка испытываемыми антителами или контрольным антителом значительно снижала послеоперационную боль по сравнению с контрольными мышами, которые получали только носитель (p < 0,001-0,05).
Таблица 14
|
|
Для того чтобы установить, могут ли антитела против-NGF снижать установившуюся боль в модели боли послеоперационного шва, REGN475 (25 мг/кг, n=7), RN624 (25 мг/кг, n=7) и контрольное антитело IgG1 (25 мг/кг, n=7) вводили внутрибрюшинно (в/б) в день 1 послеоперационного периода после проведения поведенческих исследований. Термическую гиперальгезию исследовали в ходе теста Харгрейвса, а механическую аллодинию изучали в тесте фон Фрея. В последнем тесте испытания на мышах проходили после их акклиматизации в течение 2-3 часов в течение 4 дней в аппарате с проволочной сеткой вместо пола. Тест проводили посредством прикладывания в порядке нарастания последовательности нитей фон Фрея через проволочную сетку к поверхности подошвы задней лапы со швом. Ответ считали положительным, если в ответ на прикосновение нити лапу отрывали от платформы. Начиная с самой тонкой нити, каждую нить фон Фрея прикладывали до пяти раз, до тех пор пока не наблюдался ответ. Результаты теста Харгрейвса (таблица 16) показали, что введение антитела REGN475 приводило к заметному возврату термической гиперальгезии к исходным показателям по прошествии 72 часов после операции (p < 0,001-0,01). Такой возврат к исходному уровню не наблюдался в группе мышей, получавших RN624, которые вели себя так же, как и группа, получавшая контрольный IgG. В тесте фон Фрея (порог отдергивания лапы) (g) (таблица 17) оба антитела против-NGF вызывали аналогичное купирование механической аллодинии (p < 0,001-0,05) (IgG1 контроль=AVASTIN®, 25 мг/кг, n=7; RN624, 25 мг/кг, n=7; REGN475, 25 мг/кг, n=7).
|
|
По состоянию на день 4 после завершения тестов поведения в рамках модели боли послеоперационного шва сыворотку мышей собирали и анализировали для определения циркулирующих уровней нейтрофина-3 (NT-3) с применением сэндвичевого метода ELISA. Для выяснения ответа концентрационной кривой уровень детектирования (~40 пг/мл) устанавливали равным двум стандартным отклонениям (2σ) от фона, определяемого минимум по пяти стандартам NT-3. Уровни NT-3 у мышей, получавших RN624 (среднее ± ст. откл. пг/мл, таблица 18), демонстрировали значительный рост (172 ± 114 пг/мл, n=7) по сравнению с получавшими REGN475 (не обнаружен = ND, n=7) или контроль IgG (AVASTIN®; ND, n=7).
|
Для сравнения, интактные мыши C57BL/6 под изофлураном получали разовую п/к инъекцию (50 мг/кг) REGN475, RN624 или контроля IgG1 mAb (AVASTIN®), и их сыворотку анализировали через 1, 7 и 14 дней после введения для определения уровней NT-3 с использованием сэндвичевого метода ELISA. Для выяснения ответа концентрационной кривой уровень детектирования (~40 пг/мл) устанавливали равным двум стандартным отклонениям (2σ) от фона, определяемого минимум по пяти стандартам NT-3. Уровни NT-3 (таблица 19) у мышей, получавших RN624 (131-199 пк/мл, n=6), повышались по сравнению с REGN475 (ND, n=6) или контролем IgG (ND, n=6), как было показано с помощью описанной выше модели боли послеоперационного шва.
|
Модель острой суставной боли при подагре. Модель суставной боли у мышей, вызванной инъекцией кристаллов мононатрия урата (MSU) в голеностоп, использовали для исследования эффективности антител настоящего изобретения для лечения суставной боли при подагре. Свободные от эндотоксинов кристаллы MSU (0,5 мг/20 мкл) вводили внутрисуставно в голеностоп мышей C57BL/6, после чего их тестировали на наличие пяточной термической боли в ходе теста Харгрейвса в течение до 3 дней после инъекции кристаллов MSU. Параметры адаптации и характеристики аппарата для теста Харгрейвса описаны выше. Испытываемые mAb 7E05-F6 (REGN268; n=7), 6E07-D10 (REGN263; n=7), контрольные гуманизированные mAb (RN624; n=7) или носитель (n=7) вводили п/к в дозе 10 мг/кг за 1 час до инъекции кристаллов MSU в голеностоп. Как видно из таблиц 20 и 21, испытываемые антитела значительно снижали суставную боль по сравнению с контрольными мышами, которые получали только носитель (p < 0,001-0,05).
|
|
Способность антител против-NGF снижать установившуюся боль в модели острой подагры более подробно изучали на мышах, получавших инъекцию антагониста IL-1 (ловушка IL-1 (rinolacept), Economides et al. (2003) Nature 9:47-52) или колхицина. Через день после инъекции кристаллов MSU в голеностоп мышам вводили ловушку mIL-1 (35 мг/кг; n=7), колхицин (1 мг/кг; n=7), контроль mAb RN624 (10 мг/кг; n=7) или носитель (n=7) и проверяли наличие термической гиперальгезии в соответствии с описанной выше процедурой. Кроме того, другая группа мышей (n=3) получала комбинированное лечение с ловушкой mIL-1 и контролем RN624. Комбинационная терапия антителами против-NGF и антагонистом IL-1 на день 2 после лечения в значительной мере купировала установившуюся термическую гиперальгезию по сравнению с лечением одним носителем (p < 0,001-0,05), монотерапией антителом против-NGF (p < 0,001) или монотерапией антагонистом IL-1 (p < 0,001) (таблица 22).
|
Нейропатическая боль. Модель Зельтцера нейропатической боли у мышей (Malmberg et al. (1998) Pain 76:215-222) использовали для самцов мышей C57BL/6, у которых формировалось частичное повреждение нерва за счет наложения жесткой лигатуры шелковой шовной нитью 7-0 вокруг примерно от 1/3 до 1/2 диаметра седалищного нерва на одном из бедер у каждой мыши. После операции мышам дали восстановиться в течение по крайней мере двух дней, а затем их изучали несколько недель после вмешательства для выявления термической гиперальгезии в тесте Харгрейвса. В качестве контроля использовали мышей со симулируемой операцией, в ходе которой открывался доступ к седалищному нерву, но его перевязку не проводили. После операции мыши проходили испытания в день 4 и день 7 после вмешательства для подтверждения развития термической гиперальгезии. В день 7 после хирургии мышам вводили п/к mAb REGN268 (100 мг/кг), контроль IgG1 (AVASTIN® 100 мг/кг) и носитель. REGN268 в значительно мере купировали установившуюся термическую гиперальгезию в рамках данной модели повреждения нерва (таблица 23; p < 0,05). Такое купирование боли не отмечалось у мышей со симулированной операцией. Результаты представлены в форме среднего процентного изменения по сравнению с исходным уровнем Харгрейвса ± СОС (симуляция-носитель, n=3; симуляция-100 мг/кг контроля IgG1 (AVASTIN®), n=4; симуляция-100 мг/кг REGN268, n=5; Зельтцер-носитель, n=5; Зельтцер-100 мг/кг контроль IgG1 (AVASTIN®), n=5; Зельтцер-100 мг/кг REGN268, n=8).
|
Во втором эксперименте, для того чтобы установить, может ли введение анти-NGF купировать термическую гиперальгезию через 7 дней после операции, анти-NGF REGN268 (100 мг/кг) вводили п/к в день 7, 14 или 21 после вмешательства. Заметное купирование боли регистрировалось для всех трех точек по времени по сравнению с контролем IgG1 (AVASTIN® 100 мг/кг; p < 0,05) (таблица 24, среднее процентное изменение по сравнению с исходным уровнем Харгрейвса ± СОС; 100 мг/кг контроль IgG1, n=6; 100 мг/кг REGN268, n=7).
|
В третьем эксперименте на модели Зельтцера испытывали характеристики другого антитела против-NGF REGN475. После операции по Зельтцеру мыши проходили испытания в день 5 и день 7 после вмешательства для подтверждения развития термической гиперальгезии. Затем в день 7 после хирургии мышам вводили п/к или в/б REGN475 (50 мг/кг), контроль mAb RN624 (50 мг/кг) или контроль IgG1 (AVASTIN® 50 мг/кг). Заметное купирование боли наблюдалось для обоих антител против-NGF в обеих группах мышей, как после п/к (таблица 25), так и после в/б (таблица 26) введения, тогда как контроль IgG1 не демонстрировал никаких эффектов (p<0,001-0,05) (среднее процентное изменение по сравнению с исходным уровнем Харгрейвса ± СОС; 50 мг/кг контроль IgG1, n=7; 50 мг/кг RN624, n=7; 50 мг/кг REGN475, n=7).
|
|
Для установления способности антител нейтрализовать активность человеческого NGF in vivo приготовили трансгенных мышей, у которых эндогенный локус NGF мыши заменили на ген NGF человека. Этих мышей использовали в модели нейропатической боли Зельтцера для тестирования REGN268 и контрольного mAbs. После операции по Зельтцеру мыши проходили испытания в день 4 и день 8 после вмешательства для подтверждения развития термической гиперальгезии. Затем в день 8 после хирургии мышам вводили п/к 50 мг/кг mAb REGN268 (n=7), 50 мг/кг контроля RN624 (n=8) или 50 мг/кг контроля IgG1 (AVASTIN®) (n=6). Результаты (таблица 27) показывают, что введение REGN268 было столь же эффективным, что и введение гуманизированного антитела против-NGF(RN624) при купировании нейропатической боли у гуманизированных NGF-мышей, тогда как контроль IgG1 не оказывал никакого воздействия (p < 0,05).
|
Пример 11. Эффект воздействия анти-NGF на двигательные функции животных
Для того чтобы установить, может ли терапия анти-NGF изменить двигательную функцию, оценивали моторную координацию в ходе теста с вращающимся стержнем на интактных самцах мышей C57BL/6. Сначала животных приучали находиться на стержне (Columbus Instruments, 3,5 см в диаметре, 9 см шириной), который вращался с нарастающей скоростью (максимальная скорость 1 об/мин). Тренировку мышей продолжали при 10 об/мин до тех пор, пока они не привыкали непрерывно двигаться в течение 60 с, или до тех пор, пока они не двигались в целом 2 мин на вращающемся стержне при 10 об/мин ежедневно в течение трех дней подряд. После тренировки каждую мышь помещали на вращающийся стержень при 10 об/мин три раза подряд (с коротким перерывом между попытками) и регистрировали латентность падения со стержня. Если животные не падали, через 1 минуту их снимали и фиксировали результат 60 с. Для анализа использовали средний результат 3 попыток для каждой мыши. После получения исходного уровня отсчета на вращающемся стержне mAbs REGN475, RN624 или отрицательный контроль IgG вводили п/к в дозах 50 мг/кг или 100 мг/кг. Затем мышей тестировали в течение до 20 дней после введения антител. Результаты (таблица 28, выраженные как латентность падения в секундах) (среднее ± сос) показывают, что мыши, получавшие RN624 без REGN475, демонстрировали заметно худшую моторную координацию (p < 0,001-0,05). Интересно, что по имеющимся данным, у мышей с нокаутом генов NT-3 и TrkC отмечались аномальные движения и позиции, а также потеря проприоцепции (Ernfors et al. (1994) Cell 77:503-512; и Klein et al. (1994) Nature 368:249-251). Кроме теста с вращающимся стержнем, также проводились испытания по Харгрейвсу и фон Фрею с интактными мышами, получавшими инъекции антител против-NGF. В течение 20 дней после введения антител не отмечалось никаких статистически значимых различий для любой группы мышей в тестах Харгрейвса и фон Фрея (n=6 для каждой группы).
|
Пример 12. Лечение пациента, страдающего постгерпетической невралгией
Пациенту, у которого развилась хроническая боль в месте высыпания опоясывающего герпеса, поставили диагноз постгерпетической невралгии. Пациент получал лечение в форме введения терапевтически эффективного количества фармацевтически приемлемого препарата, включающего анти-NGF mAb настоящего изобретения. Терапия могла проводиться посредством подкожной или внутривенной инъекции в концентрациях антитела против-NGF предпочтительно в интервале от 0,1 до 10 мг/кг веса тела. Введение могло осуществляться каждые 1-12 недель или по мере необходимости. В течение нескольких дней после введения препарата антител против-NGF острота боли у пациента существенно снизилась. Повторное введение препарата анти-NGF mAb стабилизирует купирование такой боли.
Пример 13. Лечение пациента, страдающего болью при остеоартрите
Пациент, страдающий умеренной или острой болью, вызванной остеоартритом любого сустава, получал лечение в форме введения терапевтически эффективного количества фармацевтически приемлемого препарата, включающего анти-NGF mAb настоящего изобретения. Состав мог вводиться внутривенно в концентрациях антитела против-NGF в интервале от 10 мкг/кг массы тела до 10 мг/кг массы тела. Введение могло осуществляться каждые 1-12 недель или по мере необходимости. В течение нескольких дней после введения препарата антител против-NGF острота боли у пациента существенно снизилась и восстановилась подвижность пораженного сустава. Терапию можно повторять по мере необходимости.