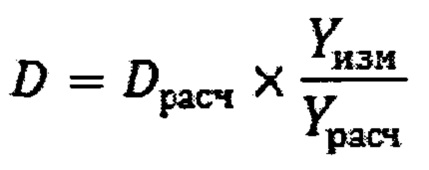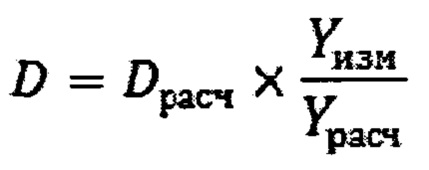Результат интеллектуальной деятельности: Способ определения поглощенной дозы от тепловых нейтронов при бор-нейтронозахватной терапии злокачественных опухолей
Вид РИД
Изобретение
Изобретение относится к ядерной медицине, в частности к нейроонкологии, и может быть применено при проведении бор-нейтронозахватной терапии (БНЗТ) злокачественных опухолей для определения поглощенной дозы.
Концепция нейтронозахватной терапии в онкологии была предложена в 1936 году, спустя четыре года после открытия нейтрона. Ее физический принцип заключается в следующем. Раствор, содержащий стабильный изотоп бор-10, вводится в кровь человека, и через некоторое время бор сорбируется преимущественно в клетках опухоли. Затем опухоль облучается потоком эпитепловых (с энергией от 0,5 эВ до 10 кэВ) нейтронов. В результате поглощения нейтрона стабильным изотопом 10В происходит ядерная реакция, и образующиеся энергетичные α-частица и ион 7Li быстро тормозятся на длине размера клетки и выделяют энергию ~2,3 МэВ в пределах именно той клетки, которая содержала ядро бора, что приводит к ее поражению. Т.о., бор-нейтронозахватная терапия (БНЗТ) позволяет осуществить избирательное поражение клеток злокачественных опухолей.
Целесообразность развития технологии нейтронозахватной терапии обусловлена ее ориентацией на лечение таких видов злокачественных опухолей, которые практически не поддаются никаким другим методам, - глиобластомы мозга и метастазы меланомы.
В начале 1950-х годов доктором Свитом было впервые продемонстрировано, что определенные соединения бора позволяют получить более высокую концентрацию бора в клетках раковой опухоли по сравнению со здоровыми [W. Sweet. The uses of nuclear disintegration in the diagnosis and treatment of brain tumor. N. Engl. J. Med. 245 (1951) 875-878; W. Sweet, M. Javid. The possible use of slow neutrons plus boron-10 in the therapy of intracranial tumors. Trans. Am. Neurol. Assoc. 76 (1951) 60-63]. С середины 1950-х годов методику с переменным успехом отрабатывали на ядерных ректорах в ряде стран. Основные достижения были связаны с именем японского нейрохирурга Хироши Хатанака. Хатанака стал применять внутриартериальное введение обогащенного изотопом 10В боркаптата натрия (BSH, Na210B12H11SH), синтезированного доктором Соловэй [A. Soloway, Н. Hatanaka, М. Davis. Penetration of brain and brain tumor. VII. Tumor binding sulfhydryl boron compounds. J. Med. Chem. 10 (1967) 714-717], проводить открытое облучение опухоли после хирургического лечения и добился впечатляющих результатов - 5-летняя выживаемость составила 58% для группы пациентов со злокачественными глиомами 3 и 4 степени злокачественности [Hatanaka Н. Clinical results of boron neutron capture therapy. Basic Life Sci. 54 (1990) 15-21]. В 1987 г. Мишима осуществил лечение поверхностной злокачественной меланомы, применив обогащенный изотопом 10В борфенилаланин в оптически изомерной форме L (BPA, (HO)210B-C6H4-CH2CH(NH2)-CO2H) [Y. Mishima, et al. Selective thermal neutron capture therapy and diagnosis of malignant melanoma: from basic studies to first clinical treatment. Basic Life Sci. 50-(1989) 251-260]. Применение этих фармпрепаратов позволяет создавать концентрацию изотопа 10В в опухолевой ткани до 40 мкг/г, что в 3,5 раза больше, чем в здоровой ткани. Такая концентрация и контраст позволяют сделать вклад фонового облучения приемлемо малым и действительно обеспечить возможность избирательного поражения клеток опухоли.
Одной из основных проблем, требующих решения для внедрения бор-нейтронозахватной терапии в клиническую практику, является определение или измерение поглощенной дозы, причем как дозы, получаемой опухолевыми клетками, так и здоровыми. В отличие от γ-терапии, протонной или ионной, в БНЗТ, помимо определения характеристик ионизирующего излучения, необходимо знать пространственное распределение бора в организме пациента.
Вклад в поглощенную дозу дают следующие процессы.
Во-первых, процесс поглощения нейтронов бором, в результате которого выделяется энергия 2,79 МэВ - в 6,1% случаев энергия распределяется только между ядрами лития и α-частицей, в 93,9% случаев ядро лития вылетает в возбужденном состоянии и испускает γ-квант энергией 0,48 МэВ. Эту компоненту дозы называют борной дозой.
Во-вторых, захват нейтронов ядрами водорода, приводящий к образованию дейтерия и к испусканию γ-кванта энергией 2,2 МэВ, захват нейтронов ядрами азота, приводящий к образованию ядра 14С и протона отдачи с выделением энергии 580 кэВ, захват нейтронов ядрами хлора, приводящий к испусканию γ-квантов с энергией до 8,85 МэВ. Эту компоненту дозы называют дозой от тепловых нейтронов.
В-третьих, появление ядер отдачи при упругом рассеянии нейтронов, преимущественно быстрых, от ядер вещества, преимущественно водорода. Эту компоненту дозы называют дозой от быстрых нейтронов.
В-четвертых, поток γ-квантов от мишенного узла, включая мишень и систему формирования пучка нейтронов. Эту компоненту дозы называют доза от γ-квантов. Достаточно часто под дозой от γ-квантов понимают не только дозу от внешнего источника (мишенный узел), но и от внутреннего (облучаемый объект), когда образуются γ-кванты в результате поглощения нейтрона водородом или хлором. В данном случае под дозой от γ-квантов понимается только доза от внешнего источника γ-излучения, а доза, выделяемая γ-квантами из-за поглощения нейтрона водородом и хлором, относится к дозе от тепловых нейтронов.
При проведении терапии каждая из этих компонент дает свой вклад в поглощенную дозу, некоторые из них - определяющий вклад. Так, борная доза является определяющей дозой при облучении опухолевых клеток, в которых накоплен бор, например, глиобластомы. Доза от быстрых нейтронов значительна для кожи, через поверхность которой направляется поток нейтронов к опухоли. Доза от тепловых нейтронов определяющая в дозе, получаемой клетками здоровых органов, например, клетками мозга при лечении глиобластомы.
Измерение компонент доз является важной задачей при проведении БНЗТ.
В настоящее время большинство способов измерения поглощенной дозы в опухолевых тканях связано с определением концентрации бора в опухоли и близлежащих тканях и с последующим проведением численных расчетов переноса нейтронов и γ-излучения в фантоме с заданным пространственным распределением концентрации бора. Для измерения концентрации бора используют, как правило, забор клеток опухоли. Концентрацию бора в образцах можно определить с помощью нескольких методик: атомной эмиссионной спектроскопией [A. Wittig, et al. Boron analysis and boron imaging in biological materials for boron neutron capture therapy (BNCT). Crit. Rev. Oncol. Hematol. 68(1) (2008) 66-90]; высокоразрешающей альфа-авторадиографией [W.S. Kiger III, et al. Boron microquantification in oral muscosa and skin following administration of a neutron capture therapy agent. Radiat. Prot. Dosimetry 99(1-4) (2002) 409-412]; нейтронозахватной рентгенографией [R. Pugliesi, M. Pereira. Study of the neutron radiography characteristics for the solid state nuclear track detector makrofol-de. NIM A 484 (2002) 613-618]; лазерной вторичной нейтронной масс-спектрометрией [P. Binns, et al. An international dosimetry exchange for boron neutron capture therapy, part 1: absorbed dose measurements. Med. Phys. 32 (2005) 3729-3736]; электронной микроскопией [Y. Zhu, R. Egerton, M. Malac. Concentration limits for the measurement of boron by electron energy loss spectroscopy and electron-spectroscopic imaging. Ultramicroscopy 87 (2001) 135-145]; с помощью флюоресцентного окрашивания содержимого туморотропных носителей; магнитно-резонансной томографией; позитрон-эмиссионной томографией [K. Ishiwata, et al. A unique in vivo assessment of 4-[10B]borono-L-phenylalanine in tumour tissues for boron neutron capture therapy of malignant melanomas using positron emission tomography and 4-borono-2-[18F] fluoro-L-phenylalanine. Melanoma Res. 2 (1992) 171-179].
Все перечисленные выше методы позволяют определить только распределение бора. Для определения поглощенной дозы требуется проведение расчета переноса нейтронов и γ-излучения, которое осуществляется программой MCNP, разработанной в национальной лаборатории Лос-Аламос (США) [Х-5 Monte Carlo Team (2003) MCNP - a general Monte Carlo N-particle transport Code, Version 5. Los Alamos National Laboratory, LA-UR-03-1987], или программой ПРИЗМА, разработанной в Федеральном ядерном центре Снежинск (Россия) [М. Arnautova, et al. Monte-Carlo simulation in nuclear geophysics: Comparison of the PRIZMA Monte Carlo program and benchmark experiments. Nuclear Geophysics 7 (1993) 407-418], с использованием базы данных сечений ENDF/B разных версий и константы справочника [С.Н. Абрамович и др. Ядерно-физические константы термоядерного синтеза. Москва, ЦНИИатоминформ, 1989]. Такая процедура широко используется в БНЗТ. При определении поглощенной дозы вычисляют все четыре компоненты дозы: борную дозу, дозу от тепловых нейтронов, дозу от быстрых нейтронов и дозу от γ-квантов.
Методом, который напрямую позволяет измерить борную дозу в опухоли, является γ-спектроскопия, основанная на регистрации γ-кванта энергией 478 кэВ, испускаемого при мгновенном распаде ядра бора после поглощения им нейтрона [Т. Kobayashi, K. Kanda. Microanalysis system of ppm order B-10 concentrations in tissue for neutron capture therapy by prompt gamma-ray spectrometry. Nucl. Instrum. Methods Phys. Res. 204 (1983) 525-531].
Однако применение этого метода для БНЗТ представляется маловероятным. Причин несколько. Во-первых, вся аппаратура регистрации γ-квантов по большому числу каналов должна находиться и работать вблизи пациента в процессе его облучения потоком нейтронов. Во-вторых, система формирования пучка нейтронов, состоящая из замедлителя, отражателя и поглотителя, вплотную приближена к пациенту и не позволит разместить регистрирующую аппаратуру как минимум в половине пространства. В-третьих, детекторы будут регистрировать не только полезные сигналы от распада ядер бора, но и паразитные сигналы от γ-квантов и нейтронов.
Вторым методом, который напрямую позволяет измерить борную дозу в опухоли, является метод, защищенный патентом [С.Ю. Таскаев, А.А. Заборонок. Способ измерения поглощенной дозы при бор-нейтронозахватной терапии злокачественных опухолей. Патент на изобретение №2606337 от 10.01.2017]. Он реализуется следующим образом. Перед проведением облучения, в соответствии с процедурой БНЗТ, пациенту вводят препарат адресной доставки бора, дополнительно маркированный стабильным атомным ядром, характеризующимся большим сечением радиационного захвата нейтронов, лучше всего ядром золота, можно индия или серебра. В процессе облучения эпитепловыми нейтронами помимо процесса поглощения нейтронов бором, приводящим к мгновенному распаду возбужденного ядра бора и выделению энергии (накоплению поглощенной дозы), будет происходить процесс радиационного захвата нейтронов маркированными атомными ядрами, приводящий к появлению и накоплению радиоактивных ядер. Если период полураспада образующихся радиоактивных ядер больше или сравним с характерным временем облучения нейтронами (порядка 1 часа), то измерение наведенной активности можно осуществить γ-спектрометром, расположенным вне облучательного помещения и в отсутствие генерации нейтронов.
Таким образом, измерение соотношения концентраций бора и ядер-мишеней для радиационного захвата нейтронов и измерение после облучения наведенной активности позволяют восстановить пространственное распределение поглощенной дозы.
Дозу в здоровой ткани определяют аналогично: путем проведения численных расчетов переноса нейтронов и γ-излучения в фантоме с заданным пространственным распределением концентрации бора. Поскольку основной вклад в дозу в здоровых тканях, за исключением кожи, вносит захват нейтронов ядрами водорода, азота и хлора, то неопределенность с концентрацией бора не так значительна, как в случае с дозой в опухоли. Другими словами, результаты расчета дозы в здоровых тканях более достоверны, чем опухоли, в том числе и потому, что накоплен большой опыт терапии рентгеновским и γ-излучением. Вместе с тем, прямой метод измерения дозы в здоровых тканях или компонент доз является крайне актуальным.
При проведении БНЗТ на ядерных реакторах используется метод, косвенно дающий представление о дозе в здоровых тканях. Так, на реакторе KURRI в Институте интегрированных радиационных и ядерных наук (ранее до 01.03.2018 г.: Институте реакторных исследований) Университета Киото (Япония) используется рентгеновская пленка. К вертикальному каналу пучка нейтронов пациента подкатывают на тележке, на которой установлен коллиматор. Во время облучения коллиматор размещен между реактором и пациентом. После облучения тележка с пациентом и коллиматором отъезжает от реактора и, пока пациент находится в том же положении, как и во время облучения, к коллиматору со стороны реактора приставляют рентгеновскую пленку, которая засвечивается излучением ядер веществ, активированных нейтронами. Степень засветки рентгеновской пленки дает информацию о степени активации ткани, подвергнутой облучению нейтронами, и качественно - о дозе, знание которой считается полезной при анализе терапии.
Недостатком метода является то, что он не позволяет определить пространственное распределение дозы от тепловых нейтронов и установить величину максимальной дозы, полученной здоровой тканью, что критически важно при планировании терапии.
Наиболее близким к предлагаемому способу можно считать способ измерения поглощенной дозы в опухоли, защищенный патентом на изобретение [С.Ю. Таскаев, А.А. Заборонок. Способ измерения поглощенной дозы при бор-нейтронозахватной терапии злокачественных опухолей. Патент на изобретение №2606337 от 10.01.2017].
Этот способ измерения поглощенной дозы в опухоли реализуется следующим образом. Перед проведением облучения, в соответствии с процедурой БНЗТ, пациенту вводят препарат адресной доставки бора, маркированный стабильным атомным ядром, характеризующимся большим сечением радиационного захвата нейтронов - ядром золота или индия. В процессе облучения эпитепловыми нейтронами помимо процесса поглощения нейтронов бором, приводящим к мгновенному распаду возбужденного ядра бора и выделению энергии (накоплению поглощенной дозы), будет происходить процесс радиационного захвата нейтронов маркированными атомными ядрами, приводящий к появлению и накоплению радиоактивных ядер. После проведения БНЗТ с помощью γ-спектрометра, расположенного в отдельном помещении, измеряют пространственное распределение интенсивности излучения γ-квантов с энергией 411 кэВ (в случае применения золота) и с учетом полученного расчетным путем соотношения интенсивности активации золота к интенсивности поглощения нейтронов бором восстанавливают пространственное распределение поглощенной дозы.
Недостатком данного способа можно считать, то что он позволяет измерить борную дозу, а не дозу от тепловых нейтронов.
Предлагаемое изобретение направлено на создание способа, позволяющего определить поглощенную дозу от тепловых нейтронов при проведении БНЗТ. Эта компонента дозы от тепловых нейтронов вносит определяющий вклад в полную поглощенную дозу, получаемую здоровой тканью.
Техническим результатом предлагаемого изобретения является определение поглощенной дозы от тепловых нейтронов при проведении БНЗТ.
Сущность предлагаемого способа определения поглощенной дозы от тепловых нейтронов при проведении БНЗТ состоит в следующем:
Перед проведением БНЗТ пациенту вводят препарат адресной доставки бора с тем, чтобы в опухоли накопить бор в достаточной концентрации. Проведение БНЗТ состоит в облучении пациента потоком эпитепловых нейтронов при том, что в опухоли содержится бор в концентрации, достаточной для терапевтического эффекта.
В процессе облучения эпитепловыми нейтронами происходит захват нейтронов ядрами водорода, приводящий к образованию дейтерия и к испусканию γ-кванта энергией 2,2 МэВ, захват нейтронов ядрами азота, приводящий к образованию ядра 14С и протона отдачи с выделением энергии 580 кэВ, захват нейтронов ядрами хлора, приводящий к испусканию γ-квантов с энергией до 8,85 МэВ. Методом численного моделирования переноса нейтронов и γ-излучения с применением программ MCNP или ПРИЗМА рассчитывают величину поглощенной дозы от тепловых нейтронов; обозначим эту величину Dрасч.
В процессе облучения эпитепловыми нейтронами помимо поглощения нейтронов ядрами водорода, азота и хлора с выделением энергии будет происходить радиационный захват нейтронов стабильными атомными ядрами, приводящий к появлению и накоплению радиоактивных ядер. Методом численного моделирования переноса нейтронов и γ-излучения с применением программ MCNP или ПРИЗМА рассчитывают интенсивность излучения γ-квантов атомных ядер, активированных эпитепловыми нейтронами; обозначим эту величину Yрасч.
После проведения терапии (облучения эпитепловыми нейтронами) с помощью γ-спектрометра, расположенного в отдельном помещении и в отсутствие генерации нейтронов, измеряют интенсивность излучения γ-квантов атомных ядер, активированных эпитепловыми нейтронами; обозначим эту величину Yизм.
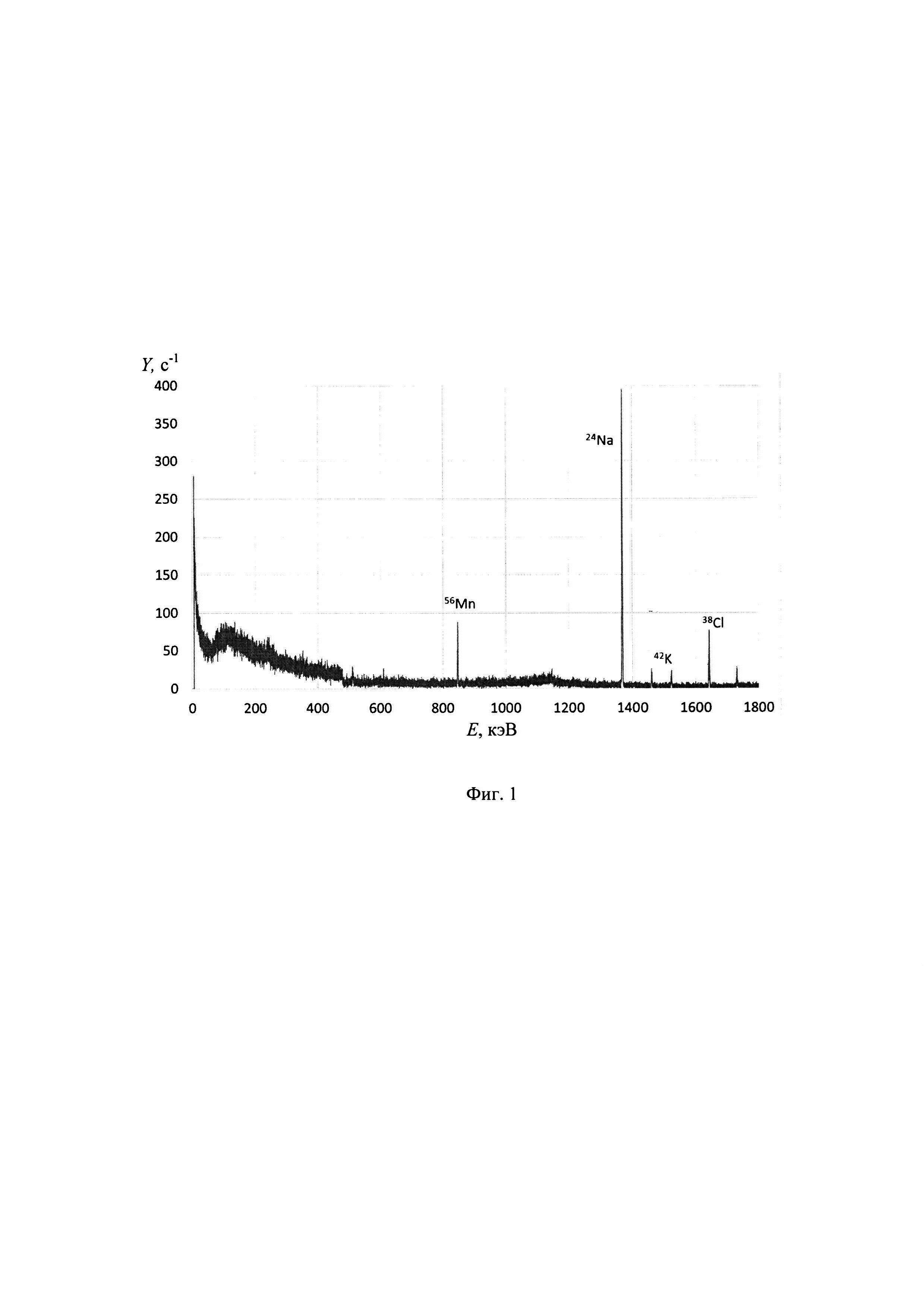
Поглощенную дозу от тепловых нейтронов определяют из соотношения
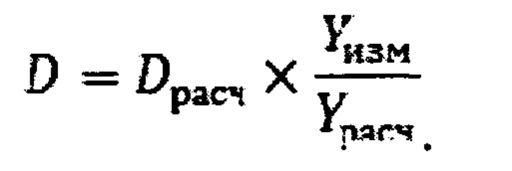
Стабильными ядрами-мишенями для радиационного захвата нейтронов в организме человека являются такие, как ядра, натрия, хлора, калия и марганца. В таблице приведены характеристики этих стабильных ядер и радиоактивных ядер, образующихся при поглощении нейтронов.
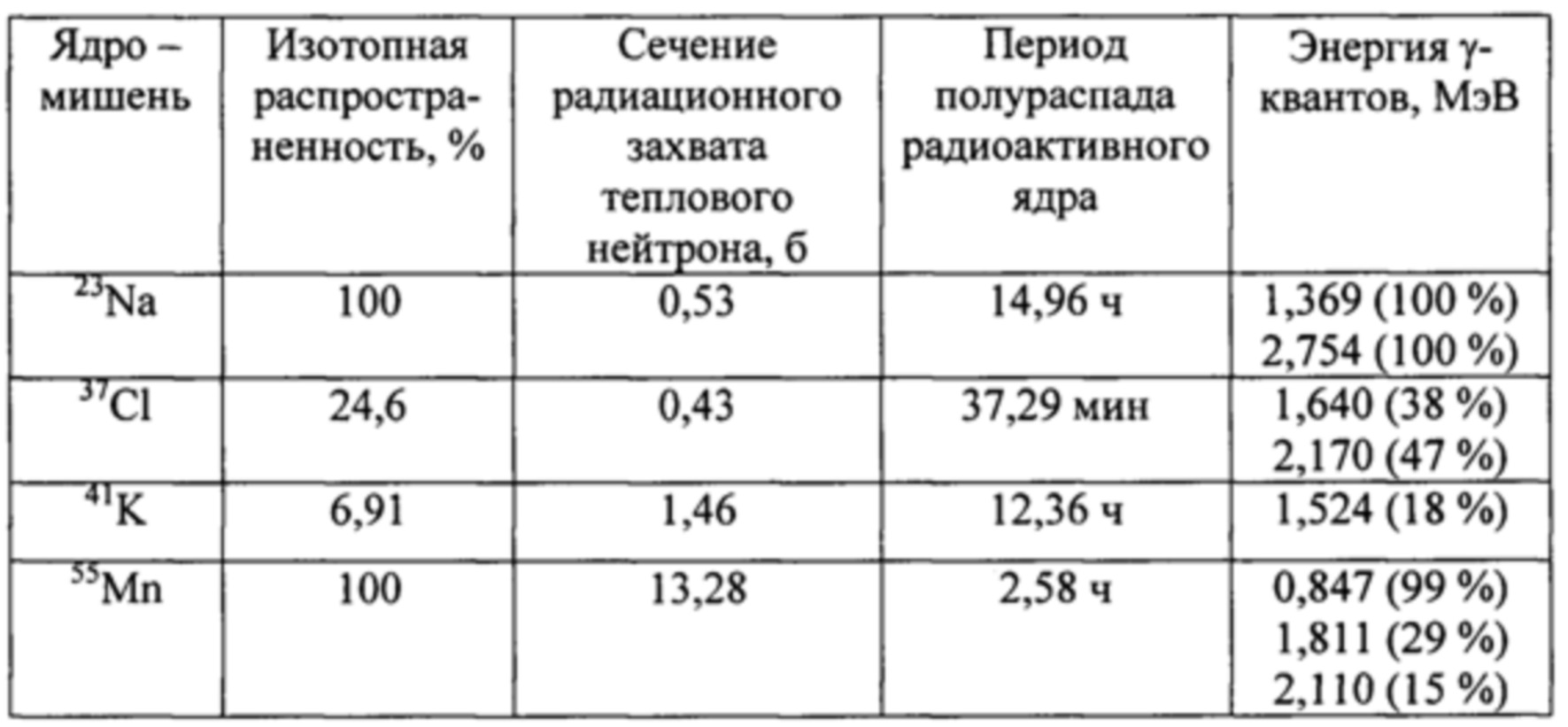
Сечение радиационного захвата нейтронов ядрами натрия, хлора, калия и марганца невелико, но вследствие большого содержания этих элементов в организме человека интенсивность излучения γ-квантов атомных ядер, активированных эпитепловыми нейтронами, достаточна для измерения γ-спектрометром. Период полураспада радиоактивных ядер от получаса до 15 ч приемлем для точного измерения интенсивности излучения γ-квантов. Атомные ядра натрия, хлора, калия и марганца, активированные эпитепловыми нейтронами, испускают γ-кванты с энергией 0,847, 1,369, 1,524 и 1,640 МэВ.
Таким образом, предложенный способ определения поглощенной дозы от тепловых нейтронов при проведении БНЗТ может быть реализован на практике следующим образом. Пациенту вводят препарат адресной доставки бора, облучают потоком эпитепловых нейтронов, рассчитывают поглощенную дозу от тепловых нейтронов (Dрасч), рассчитывают интенсивность излучения γ-квантов атомных ядер (Yрасч), активированных эпитепловыми нейтронами, затем, после облучения γ-спектрометром, измеряют интенсивность излучения γ-квантов атомных ядер натрия, хлора, калия и марганца, (Yизм), активированных эпитепловыми нейтронами, и определяют поглощенную дозу от тепловых нейтронов из соотношения
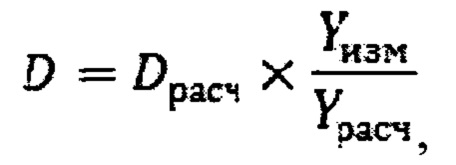
при этом γ-спектрометром измеряют интенсивность излучения γ-квантов с энергией 0,847, 1,369, 1,524 и 1,640 МэВ., излучаемых 24Na, 54Mn, 38Cl и 42K,
Реализуемость предлагаемого способа измерения дозы иллюстрируется Фиг. 1. На Фиг. 1 приведена зависимость интенсивности излучения Y лабораторной мыши после ее облучения эпитепловыми нейтронами от энергии γ-квантов Е. Спектр излучения измерен γ-спектрометром СЕГ-1КП-ИФТП на основе полупроводникового детектора, выполненного из особо чистого германия. На спектре отчетливо видны линии излучения 24Na, 54Mn, 38Cl и 42K, обусловленные захватом нейтронов ядрами натрия, хлора, калия и марганца, присутствующих в организме животного.