Результат интеллектуальной деятельности: Способ идентификации видовой принадлежности баранины и говядины в продовольственном сырье, кормах и пищевых продуктах
Вид РИД
Изобретение
Изобретение относится к ветеринарной микробиологии, в частности к методам определения видовой принадлежности мяса с помощью полимеразной цепной реакции.
Известно определение видовой принадлежности мяса для этого используют концентрированные экстракты различных групп мышц, например грудной, бедренной, голени и др. одной особи, предварительно определяют свежесть мяса по рН, затем подвергают фотометрированию, измеряют их оптическую плотность при длине волны 310-320 нм, составляют сравнительную таблицу, по которой определяют видовую принадлежность исследуемого мяса. Способ позволяет сократить сроки и повысить точность определения видовой принадлежности мяса птиц, однако - не высокая точность (патент РФ №2178169, кл. G01N 33/12. 2002).
Также известен способ идентификации видовой принадлежности баранины и говядины в продовольственном сырье, кормах и пищевых продуктах, включающий выделение ДНК из баранины (Ovis) и говядины (Boss) сорбционным методом, постановку одноэтапной полимеразной цепной реакции, проведение 45 циклов амплификации с детекцией в реальном времени с использованием специфичных для участка генома ДНК баранины (Ovis) и говядины (Bos) олигонуклеотидных праймеров, зондов, красителей, внутреннего контрольного образца в виде суспензии бактериофага и положительных контрольных образцов - содержащих фрагменты геномов ДНК баранины (Ovis) и говядины (Bos), измерение специфических сигналов и сигнала контролей и интерпретацию результатов (Сорокина М.Ю. Автореферат диссертации по ветеринарии на тему Разработка тест-системы для определения видовой принадлежности мясных ингредиентов в кормах методом полимеразной цепной реакции, Москва, 2004 - прототип).
Однако в известном способе нуклеотидная последовательность непосредственно читается по электрофореграмме. Длина фрагмента, который может быть расшифрован этим методом, ограничивается разрешающей способностью метода гель-электрофореза, что влияет на точность диагностирования видовой принадлежности говядины или баранины в кормах. Кроме того, отсутствует возможность идентификации видовой принадлежности баранины и говядины в продовольственном сырье и пищевых продуктах.
Техническим результатом является повышение точности идентификации видовой принадлежности говядины или баранины и расширение функциональных возможностей.
Технический результат достигается тем, что в способе идентификации видовой принадлежности баранины и говядины в продовольственном сырье, кормах и пищевых продуктах, включающем выделение ДНК из баранины (Ovis) и говядины (Bos) сорбционным методом, постановку одноэтапной полимеразной цепной реакции, проведение 45 циклов амплификации с детекцией в реальном времени с использованием специфичных для участка генома ДНК баранины (Ovis) и говядины (Bos) олигонуклеотидных праймеров, зондов, красителей, внутреннего контрольного образца в виде суспензии бактериофага и положительных контрольных образцов - содержащих фрагменты геномов ДНК баранины (Ovis) и говядины (Bos), измерение специфических сигналов и сигнала контролей и интерпретацию результатов, согласно изобретению дополнительно исследуют продовольственное сырье и пищевые продукты, содержащие ДНК баранины (Ovis) и говядины (Bos), проводят полимеразную цепную реакцию с флуоресцентной детекцией с применением термоциклера типа Rotor-Gene Q и измеряют накопление флуоресцентных сигналов по каналам соответствующих флуоресцентных красителей: JOE/Yellow для специфического сигнала для баранины (Ovis); ROX/Orange - для говядины (Bos) и Cy5/Red - для внутреннего контрольного образца, интерпретацию результатов проводят на основании наличия или отсутствия пересечения кривой флуоресценции с пороговой линией, если кривые накопления флуоресцентного сигнала выходят до 35 цикла, то результат реакции считается положительным, а если кривые не пересекают пороговую линию или пересекают ее после 35 цикла, то результат реакции - отрицательный, при этом для внутреннего контрольного образца используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл, а для положительного контрольного образца - смесь содержащую фрагменты геномов баранины (Ovis), говядины (Bos) и бактериофага Т4 взятых в соотношении 1:1:1 со следующими нуклеотидными последовательностями:

Новизна заявляемого способа состоит в идентификации видовой принадлежности баранины и говядины с помощью полимеразной цепной реакции (ПЦР) с флуоресцентной детекцией в режиме реального времени, что в свою очередь позволяет с высокой точностью определить наличие их ингредиентов в продовольственном сырье, кормах и пищевых продуктах.
Признаки, отличающие заявляемое техническое решение от прототипа, направлены на достижение технического результата и не выявлены при изучении данной и смежной областей науки и техники и, следовательно, соответствуют критерию «изобретательский уровень».
Заявляемый способ рекомендовано использовать в специализированных ветеринарных, санитарно-эпидемиологических, животноводческих, сельскохозяйственных предприятиях, что соответствует критерию «промышленная применимость».
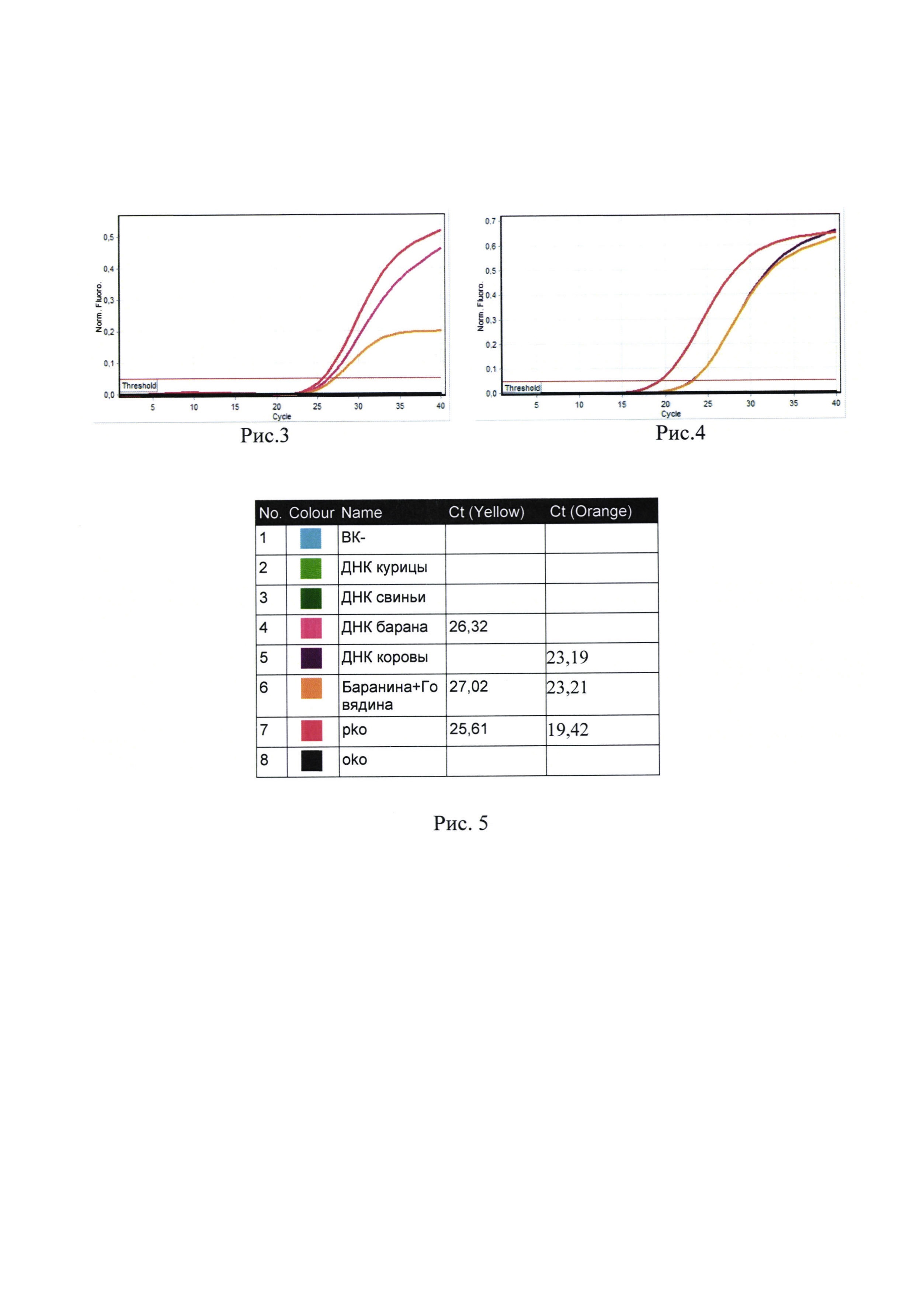
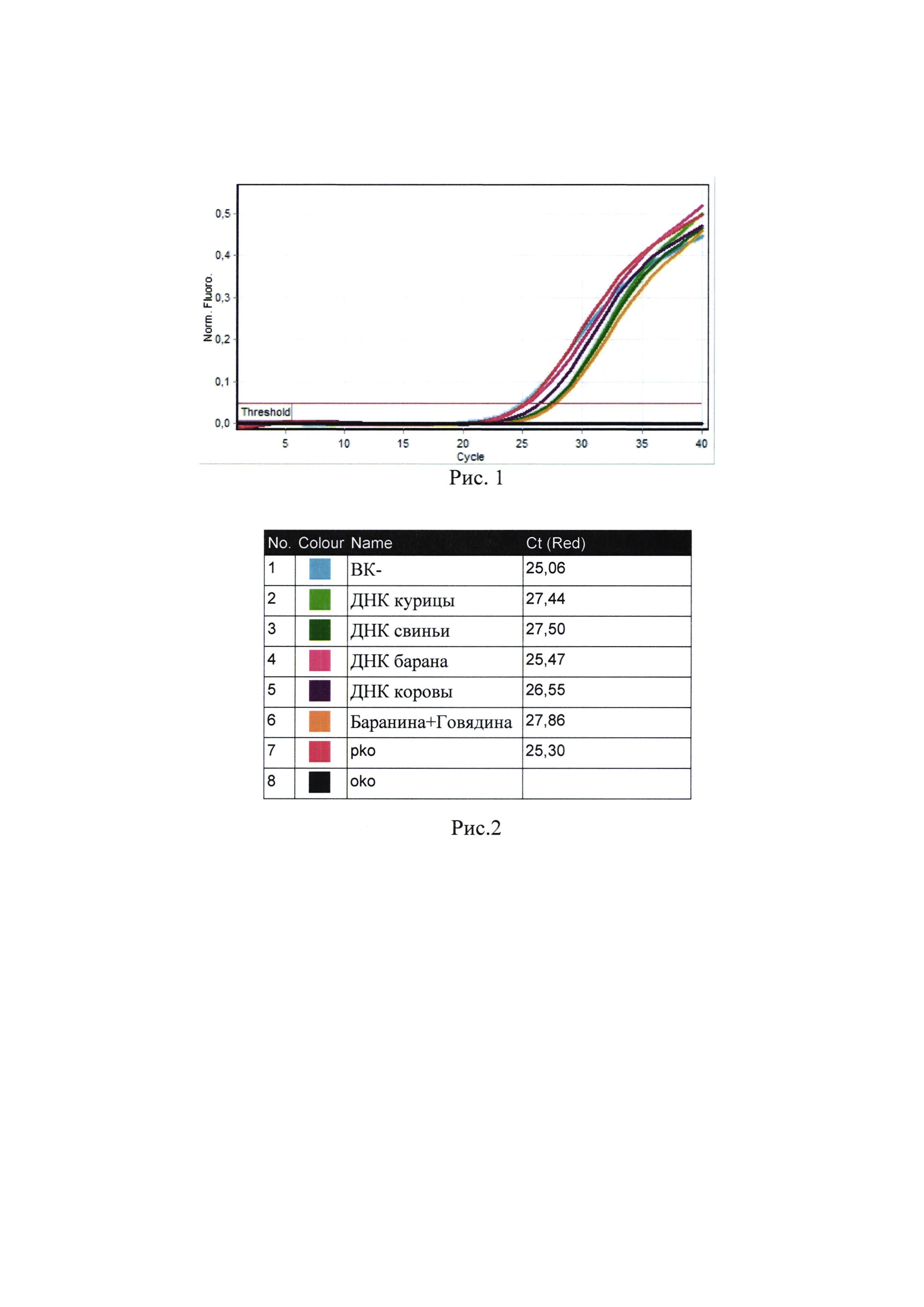
Сущность изобретения поясняется чертежом, где на рисунках 1-6 представлены скриншоты с дисплея прибора Rotor-Gene Q: рис. 1 - представлен график канала Су5 для внутреннего контрольного образца (ВКО); рис. 2 - таблица количественных данных для Cycling A.Red (ВКО); рис. 3 - представлен график канала JOE/Yellow для специфического сигнала баранины (Ovis); рис. 4 - представлен график канала ROX/Orange - для говядины (Bos); рис. 5 - таблица количественных данных для Cycling A.Yellow (Ovis) и A.Orange (Bos.).
Способ идентификации видовой принадлежности баранины и говядины в продовольственном сырье, кормах и пищевых продуктах осуществляется следующим образом.
Для исследования кормов, продовольственного сырья и пищевых продуктов на содержание ДНК баранины (Ovis) и говядины (Bos) проводят полимеразную цепную реакцию с флуоресцентной детекцией с применением термоциклера типа Rotor-Gene Q при соответствующих температурно-временных режимах амплификации и измеряют накопление флуоресцентных сигналов по каналам соответствующих флуоресцентных красителей: JOE/Yellow для специфического сигнала для баранины (Ovis); ROX/Orange - для говядины (Bos) и Cy5/Red - для внутреннего контрольного образца. Интерпретацию результатов проводят на основании наличия или отсутствия пересечения кривой флуоресценции с пороговой линией, если кривые накопления флуоресцентного сигнала выходят до 35 цикла, то результат реакции считается положительным, а если кривые не пересекают пороговую линию или пересекают ее после 35 цикла, то результат реакции - отрицательный. Для повышения точности идентификации мяса для внутреннего контрольного образца используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл, если концентрация копий нуклеотидных последовательностей отклоняется в большую или меньшую сторону, то наблюдаются повторности сомнительных образцов. Для положительного контрольного образца используют смесь содержащую фрагменты геномов баранины (Ovis), говядины (Bos) и бактериофага Т4 взятых в соотношении 1:1:1 со следующими нуклеотидными последовательностями:

Использование для разных видов контроля различные формы материала бактериофага Т4: суспензии и фрагмента генома со специфическими к нему праймерами и зондом обусловлено тем, что это позволяет контролировать корректное прохождение реакции в каждой пробирки, а также контролируется этап выделения ДНК из образцов.
При конструировании праймеров и зонда основными требованиями были: степень гомологии (комплементарность) с выбранным участком гена; отсутствие самокоплементарных участков внутри олигонуклеотидов и комплементарности друг другу, чтобы не допускать возникновения устойчивых вторичных структур (димеров); близость значений температуры отжига праймеров.
Конструирование специфических праймеров и зонда осуществляли с помощью компьютерных программ на основании анализа нуклеотидных последовательностей референтных штаммов и изолятов, опубликованных на ресурсе GenBank и подбора условий для проведения ПЦР в реальном времени с применением разработанных праймеров и зонда, несущего флуорофор и тушитель, и комплементарного части амплифицируемого со специфическими праймерами фрагмента.
Праймеры, специфичные для барана (Ovis aries) и быка (говядины) (Bos taurus) были отобраны на основе митохондриальных последовательностей ДНК геномов барана (Ovis aries isolate SH21 ATP synthase F0 subunit 6 (ATP6) gene, partial cds; mitochondrial, код доступа KY453456.1 complete genome, участок между 122 и 353) и быка (Bos taurus mitochondrion, complete genome, код доступа MF925711, участок между 4724 и 4957). Праймеры спроектированы с использованием Primer Express Software v3.0 (Applied Biosystems) и исследованы с использованием BLAST, чтобы подтвердить их специфичность. Для детекции продуктов амплификации подобраны олигонуклеотидные флуоресцентно-меченные зонды Ovis Р (комплементарный участку нуклеотидной последовательности, ограниченной позициями отжига праймеров Ovis F и Ovis R) и BosP (комплементарный участку нуклеотидной последовательности, ограниченной позициями отжига праймеров BosF и Bos R). Зонды были помечены красителями FAM и HEX. Используя программу "Oligo 6.0" описаны основные свойства рассчитанных олигонуклеотидов, определившие возможность их использования в ПЦР. Ни одна из выбранных последовательностей не обнаружена в геноме любых видов растений и животных, которые потенциально встречаются вблизи тех, которые определены в кормах и пищевых продуктах.
В качестве внутреннего контроля использовался бактериофаг Т4, имеющий геномную ДНК порядка 169 тысяч пар нуклеотидов (Enterobacteria phage Т4Т, complete genome GenBank: HM137666.1). В результате анализа был выбран участок между 400 и 500 нуклеотидами, содержащий уникальные нуклеотидные последовательности, рассчитаны первичные структуры олигонуклеотидных праймеров, фланкирующих выбранный участок генома. Праймеры были спроектированы с использованием Primer Express Software v3.0 (Applied Biosystems) и исследованы с использованием BLAST, чтобы подтвердить их специфичность.
Для детекции продуктов амплификации подобран олигонуклеотидный флуоресцентно-меченный зонд Т4Р, комплементарный участку нуклеотидной последовательности, ограниченной позициями отжига праймеров T4F и T4R. Зонд был помечен красителем Су5. Используя программу "Oligo 6.0" описаны основные свойства рассчитанных олигонуклеотидов, определившие возможность их использования в ПЦР.
Пример конкретного осуществления способа идентификации видовой принадлежности баранины и говядины в продовольственном сырье, кормах и пищевых продуктах.
Для подтверждения эффективности способа были использованы сухие корма в виде рыбной и мясной муки; сырые и термически обработанные мясные продукты, т.е. мясные полуфабрикаты.
От пробы плотной консистенции отбирают на исследование общую пробу весом 10-50 г. Гранулированную или консервированную продукцию перед исследованием (10-20 г) растирают в ступке до гомогенного состояния.
Лабораторные пробы (20-40 мг) отбирают на исследование в одноразовые микропробирки вместимостью 1,5 мл в двух повторах. Отобранные лабораторные пробы направляют на выделения ДНК.
Исследование проводят с помощью набора реагентов «ПЦР-БАРАНИНА-ГОВЯДИНА-ФАКТОР». Набор состоит из комплекта реагентов для проведения мультиплексной ПЦР (комплект №1) и комплекта контрольных образцов (комплект №2). Набор выпускается в двух вариантах: 1) Для анализа 55 образцов (включая контрольные образцы)
2) Для анализа 110 образцов (включая контрольные образцы).
Наборы используют в соответствии с инструкцией по применению набора реагентов «ПЦР-БАРАНИНА-ГОВЯДИНА-ФАКТОР» для определения видовой принадлежности тканей жвачных животных видов Ovis aries (бараны) и Bos taurus (быки) методом полимеразной цепной реакции (ПЦР) с флуоресцентной детекцией в режиме реального времени ТУ21.10.60-152-51062356-2018, http.7/www.vetfaktor.ru/.
Состав набора приведен в Таблицах 1 и 2.
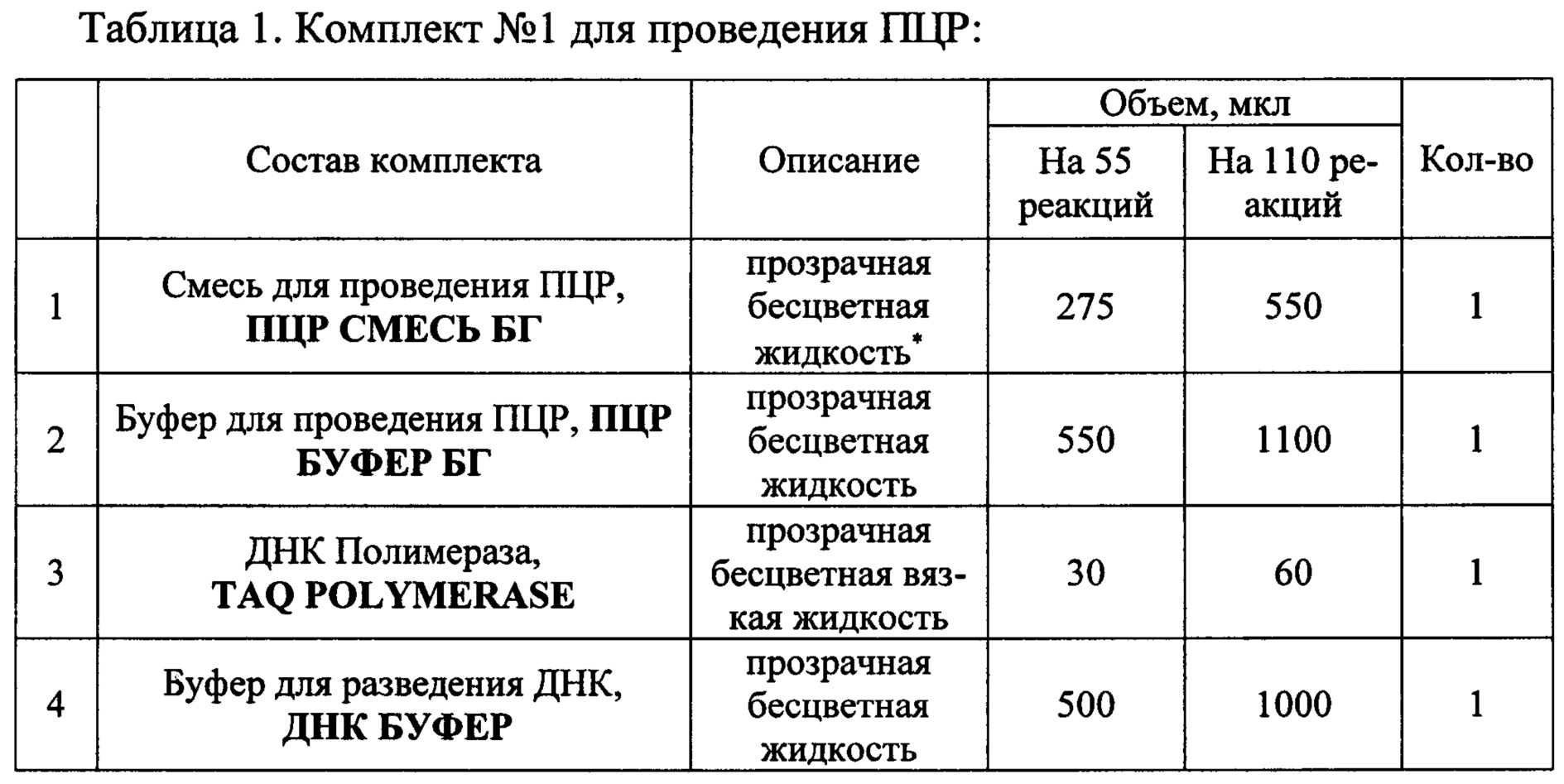
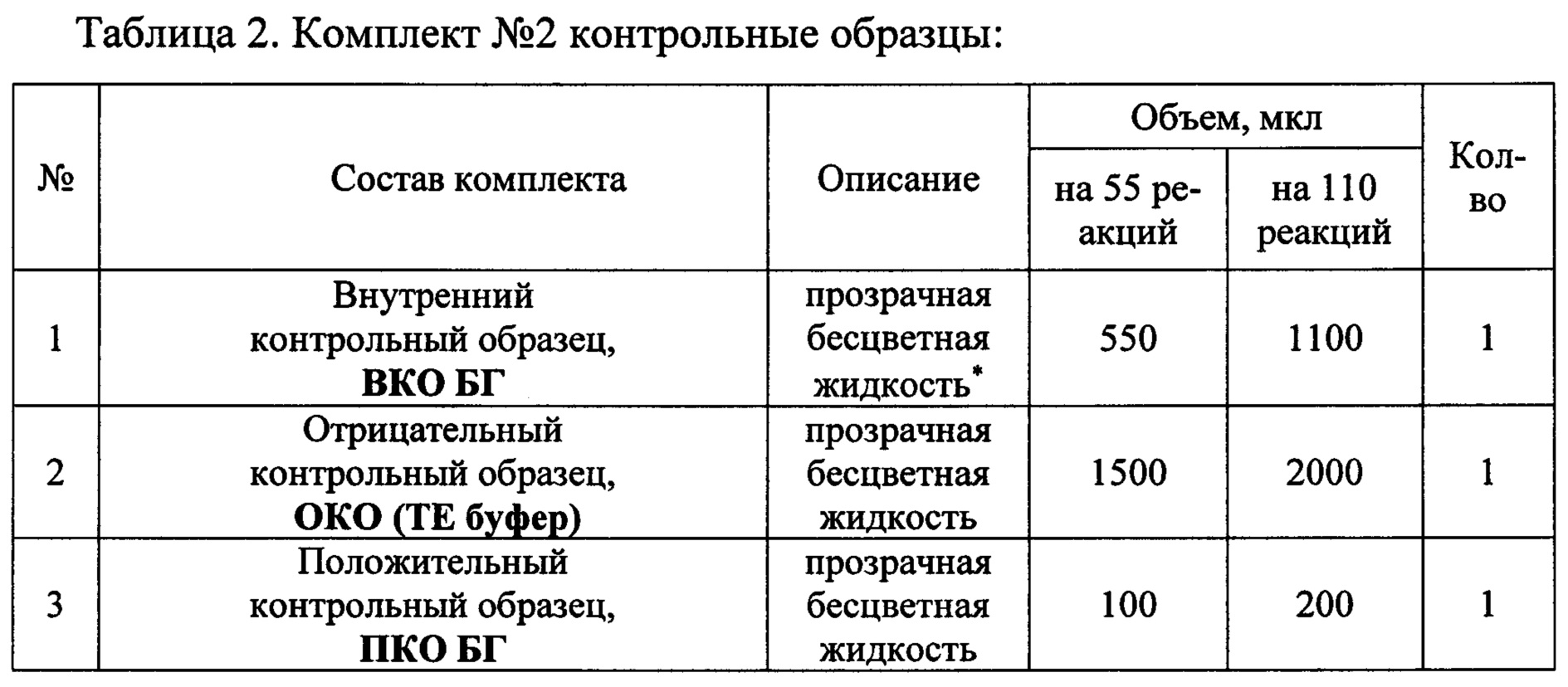
Исследования состоит из трех этапов:
- экстракция нуклеиновая кислота (НК);
- проведение реакции ПЦР РВ;
- учет результатов анализа.
* Возможна легкая опалесценция
Для экстракции (выделение) НК из исследуемых проб отбирают необходимое количество одноразовых пробирок объемом 1,5 мл, включая отрицательный контроль выделения. Во все пробирки с исследуемыми образцами, включая пробирку для отрицательный контрольный образец (ОКО), вносят по 10 мкл внутренний контрольный образец (ВКО) для баранины и говядины (БГ) в качестве которого используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл.
Следующий этап это подготовка образцов к проведению ПЦР.
Общий объем реакционной смеси - 25 мкл, объем ДНК-пробы - 10 мкл.
Успешное прохождение реакции контролируют использованием положительный контрольный образец (ПКО) БГ, ВКО БГ и ДНК буфера. В качестве ПКО используют смесь содержащую фрагменты геномов баранины (Ovis), говядины (Bos) и бактериофага Т4 взятых в соотношении 1:1:1.
В отдельной пробирке смешать компоненты набора из расчета на каждую реакцию:
5 мкл ПЦР СМЕСЬ БГ;
10 мкл ПЦР БУФЕР БГ;
0,5 мкл TAQ POLYMERASE
Перемешивают смесь на вортексе и сбросывают капли кратковременным центрифугированием.
Отбирают необходимое количество пробирок для амплификации ДНК исследуемых и контрольных проб. Вносят по 15 мкл приготовленной реакционной смеси.
Помещают подготовленные для проведения ПЦР пробирки в ячейки амплификатора и используют программное обеспечение прибора. Далее проводят ПЦР РВ с флуоресцентной детекцией.
Параметры температурно-временного режима амплификации на приборе «Rotor-Gene Q» представлены в таблице 3.

Интерпретация результатов анализа.
Полученные данные - кривые накопления флуоресцентного сигнала анализируются с помощью программного обеспечения используемого прибора для проведения ПЦР в соответствии с инструкцией производителя к прибору.
Учет результатов ПЦР РВ проводится по наличию или отсутствию пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией (что соответствует наличию или отсутствию значения порогового цикла «Ct» для исследуемого образца).
Результат считается достоверным в случае корректного прохождения положительных и отрицательных контролей амплификации и экстракции ДНК в соответствии с таблицей 4.
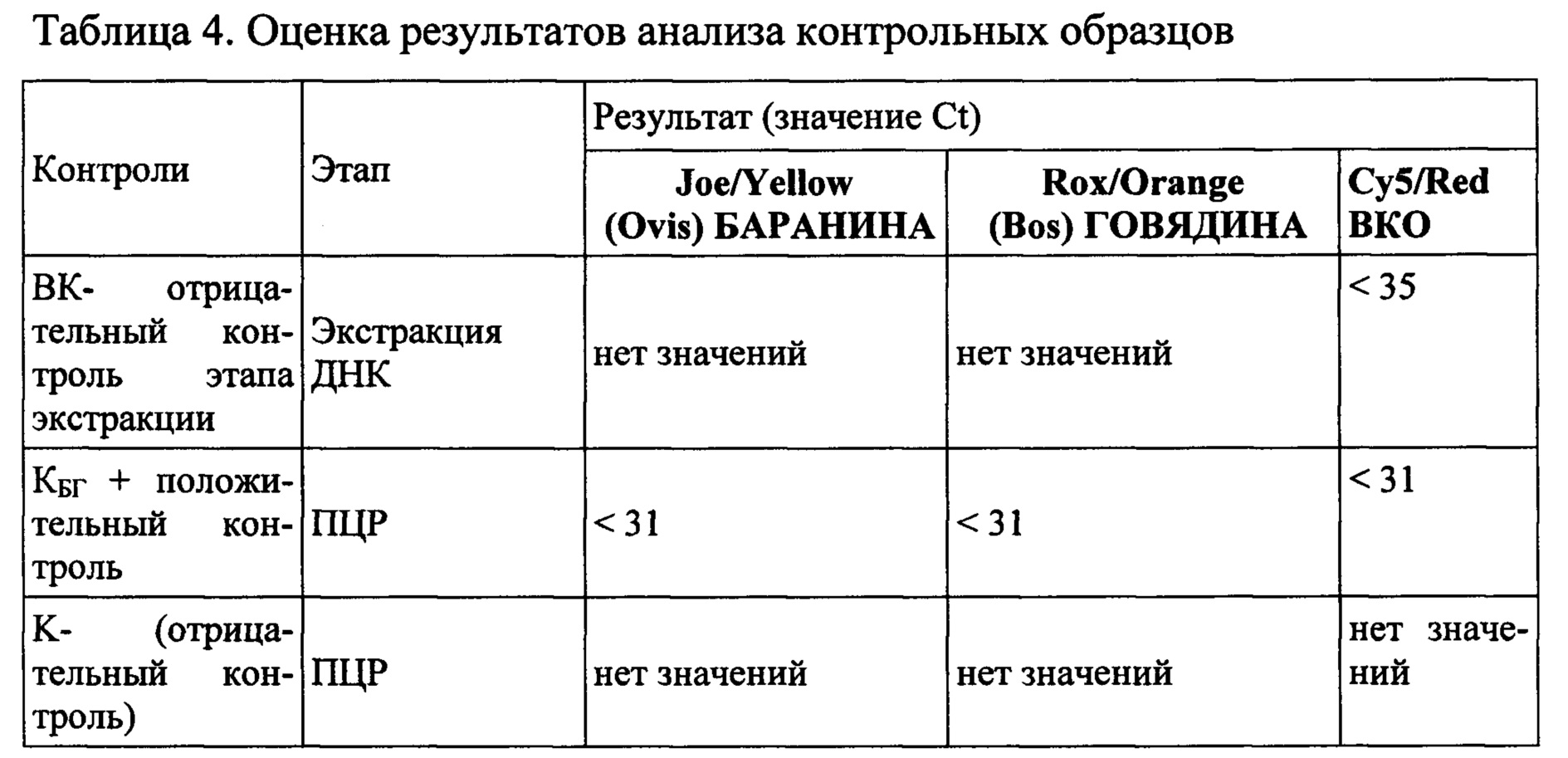
Появление любого значения Ct в таблице 4 результатов для отрицательного контроля этапа экстракции ВК- на каналах ROX/Orange и JOE/Yellow и для отрицательного контроля этапа ПЦР К- на любом из каналов свидетельствует о наличии контаминации реактивов или образцов (рис 1, 2). В этом случае результаты анализа для всех проб считаются недействительными. Требуется повторить анализ всех проб, а также предпринять меры по выявлению и ликвидации источника контаминации.
Образцы, для которых значение Ct по каналу Cy5/Red отсутствует или превышает 35 цикл (и при этом не получен положительный результат на каналах JOE/Yellow и/или ROX/Orange) требуют повторного проведения исследования с этапа экстракции ДНК. Задержка в значениях пороговых циклов для исследуемых образцов указывает на присутствие ингибиторов в пробе(ах) или на ошибки при экстракции ДНК или при постановке реакции ПЦР РВ.
В образце обнаружена ДНК Ovis aries баранины, если наблюдается экспоненциальный рост сигнала на канале JOE/Yellow, при этом значения Ct контрольных образцов находятся в пределах нормы (Табл. 4, рис. 3, 5).
В образце обнаружена ДНК Bos taurus говядины, если наблюдается экспоненциальный рост сигнала на канале Rox/Orange, при этом значения Ct контрольных образцов находятся в пределах нормы (Табл. 4, рис. 4, 5).
Если для исследуемого образца по каналам JOE/Yellow и/или ROX/Orange значение Ct определяется позднее 37 цикла при корректном прохождении положительных и отрицательных контролей, образец исследуется повторно с этапа экстракция ДНК. Если при повторной постановке Ct более 37 результат считается отрицательным (содержание целевой ДНК ниже предела обнаружения метода).
Образец считается отрицательным (ДНК Ovis aries и/или Bos taurus не обнаружена) если не определяется значение Ct (не наблюдается рост специфического сигнала) на канале Rox/Orange и/или JOE/Yellow при этом значения Ct контрольных образцов находятся в пределах нормы (Табл. 4, рис 3, 4, 5), а значение Ct по каналу Cy5/Red менее 35.
Для исследуемых образцов (сухой корм и мясные полуфабрикаты) предел точности содержания баранины и говядины представлен в таблице 5.
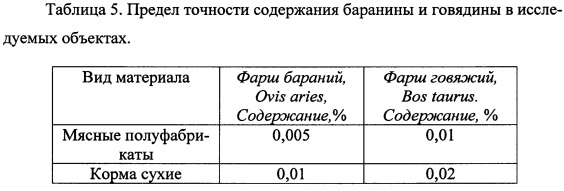
Для доказательства эффективности использования ПЦР с флуоресцентной детекцией в режиме реального времени проводился сравнительный анализ чувствительности заявляемого с прототипом, в котором использовался метод ПЦР с электрофоретической детекцией. Оказалось чувствительность ПЦР с флуоресцентной детекцией при обнаружении примеси тканей баранины и говядины в кормах в 10 раз выше, чем ПЦР с электрофоретической детекцией.