Результат интеллектуальной деятельности: Биосенсор на основе клеток Escherichia coli, продуцирующих флуоресцентный белок Katushka2S, для проведения ультравысокопроизводительного скрининга
Вид РИД
Изобретение
Изобретение относится к биотехнологии, а именно: к технологии получения живых флуоресцентных микроорганизмов и может быть использовано в биотехнологии для поиска антимикробных препаратов, обладающих бактериостатическим или бактерицидным действием по отношению к различным штаммам бактерии Escherichia coli.
Общая схема поиска микроорганизмов способных подавлять рост или элиминировать патогенные бактерии заключается в следующем:
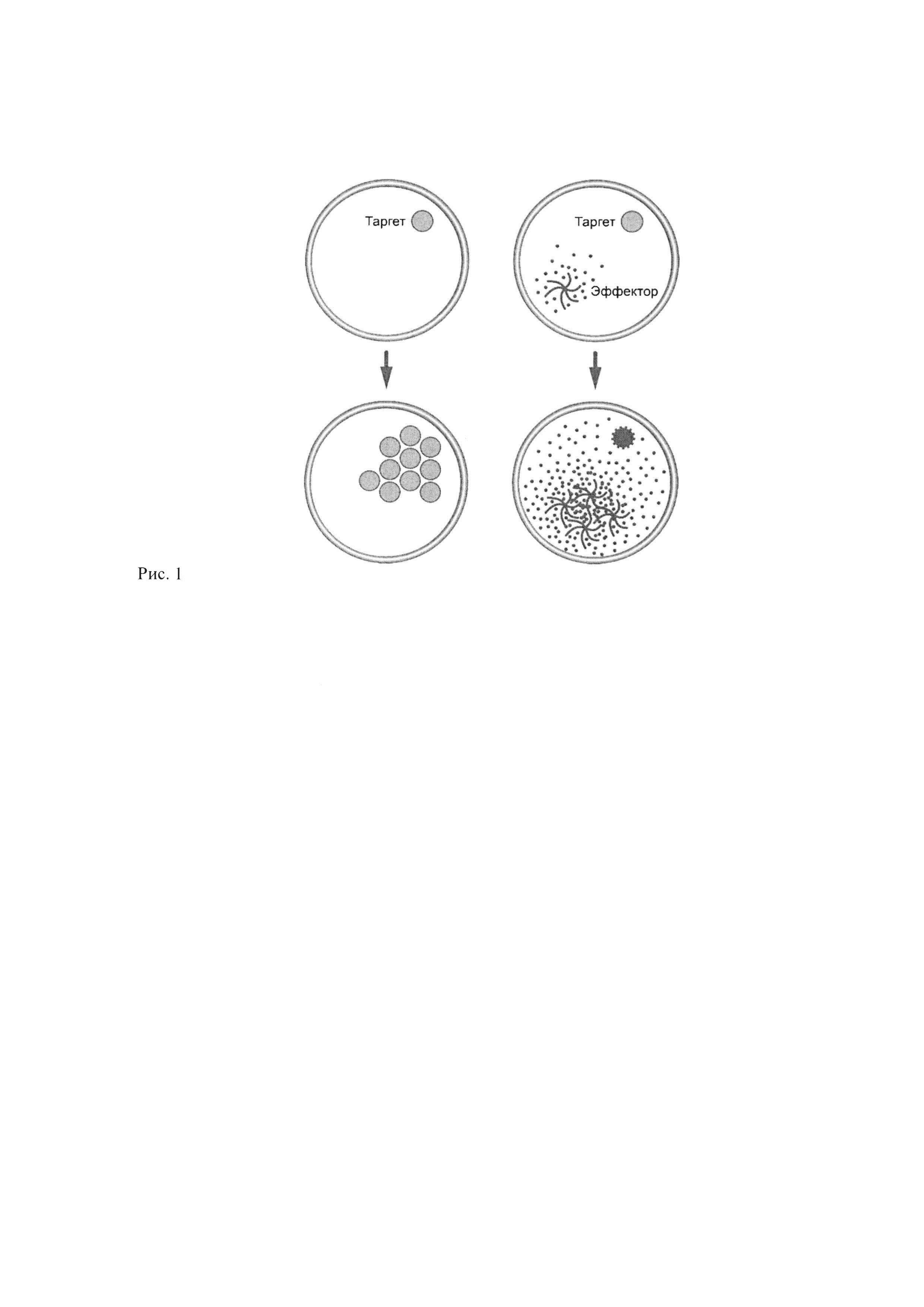
1) На начальном этапе имеется бактерия-патоген - «таргет», для которой поставлена задача поиска штамма микроорганизма - «эффектор», способного продуцировать вещества (антимикробные пептиды, низкомолекулярные вещества) обладающие антимикробными свойствами.
2) Далее, с использованием технологии микрофлюидики и оригинальных микрофлюидных чипов собственного производства, проводится инкапсулирование пары «таргет»-«эффектор». Для регистрации антимикробной активности вводятся специальные флуоресцентные маркеры: (i) внутриклеточный флуоресцентный белок - для наблюдения за бактерией «таргетом», (ii) - флуоресцентный краситель - для идентификации живых клеток микроорганизмов и (iii) - флуоресцентный краситель для определения количества клеток бактерии «таргета» «на входе».
3) После инкубации при выбранных условиях проводится отбор «позитивных» инкапсулированных пар с использованием стандартного клеточного сортера (FACS AriaIII или аналог) и подобранных условиях сортинга.
4) Полученные в результате отбора инкапсулированные пары анализируются методами NGS-секвенирования и масс-спектрометрии в режимах без и после культивации в стандартных условиях. Проводится биоинформатический анализ и определяются штаммы микроорганизмов и веществ, обладающих антимикробным действием.
Основным аналитическим сигналом, позволяющим дискриминировать инкапсулированные пары и провести их отбор с использованием клеточного цитофлуориметра-сортера (FACS), является флуоресценция. Следовательно, необходимо обеспечить флуоресцентный маркер, который с одной стороны позволит определить наличие бактерии в капле, с другой стороны будет коррелировать с количеством бактериальных клеток в капле, что позволит оценить их размножение. Наиболее простым решением этой задачи является введение ДНК-кодируемого флуоресцентного маркера. В качестве такого маркера нами был выбран дальне-красный флуоресцентный белок -
Katushka-2S. Отобранные рекомбинантные штаммы бактерий-патогенов будут выступать в качестве биосенсора антибиотической активности в каждой конкретной капле. При этом, если в каплю микрофлюидной двойной эмульсии попадает бактерия-эффектор, ингибирующая рост таргета своими метаболитами, таргет погибает и капля будет обладать низким уровнем флуоресценции Katushka-2S.
В качестве таргетных микроорганизмов выбран Е. coli.
Е. coli также является удобным объектом для данного исследования. Несмотря на то, что Е. coli, в основном, является частью нормальной микрофлоры кишечника, некоторые штаммы Е. coli (O157:Н7, О104:Н4) проявляют чрезвычайно высокую энтеропатогенность ввиду продукции шига- и шигаподобных токсинов. Продукция токсинов может приводить к возникновению геморрагической диареи и острой почечной недостаточности. Терапия антибиотиками в свою очередь не приводит к улучшению состояния, более того может развиваться гемолитико-уремический синдром. Поиск альтернативных вариантов терапии отравления энтеропатогенными штаммами Е. coli представляет высокую значимость.
Для создания биосенсора были использованы штаммы Escherichia coli DH5α экспрессионная векторная плазмида pKatushka2S-B. Экспрессия происходит под индуцибельным lac-промотером. Это позволяет добиться более высокого уровня трансформации, но требует индукции добавлением изопропил-β-D-1-тиогалактопиранозида (ИПТГ) в ростовую среду.
Поставленная задача решается за счет создания штамма-продуцента на основе штамма Escherichia coli DH5α, трансформированного экспрессионной векторной плазмидой pKatushka2S-B, содержащей нуклеотидные последовательности индуцибельного промотера Т5 в составе lac-оперона, гена дальне-красного флуоресцентного белка Katushka-2S, гена blat устойчивости к ампициллину, обеспечивающей внутриклеточную продукцию дальне-красного флуоресцентного белка Katushka2S.
Изобретение иллюстрируют следующими графическими материалами:
Рис. 1. Использование бактериальных биосенсоров на основе штаммов клеток - бактерий-патогенов (таргетов). Таргеты, экспрессирующие GFP обозначены зеленым, эффекторы - серым, метаболиты эффекторов и мертвые таргеты - красным.
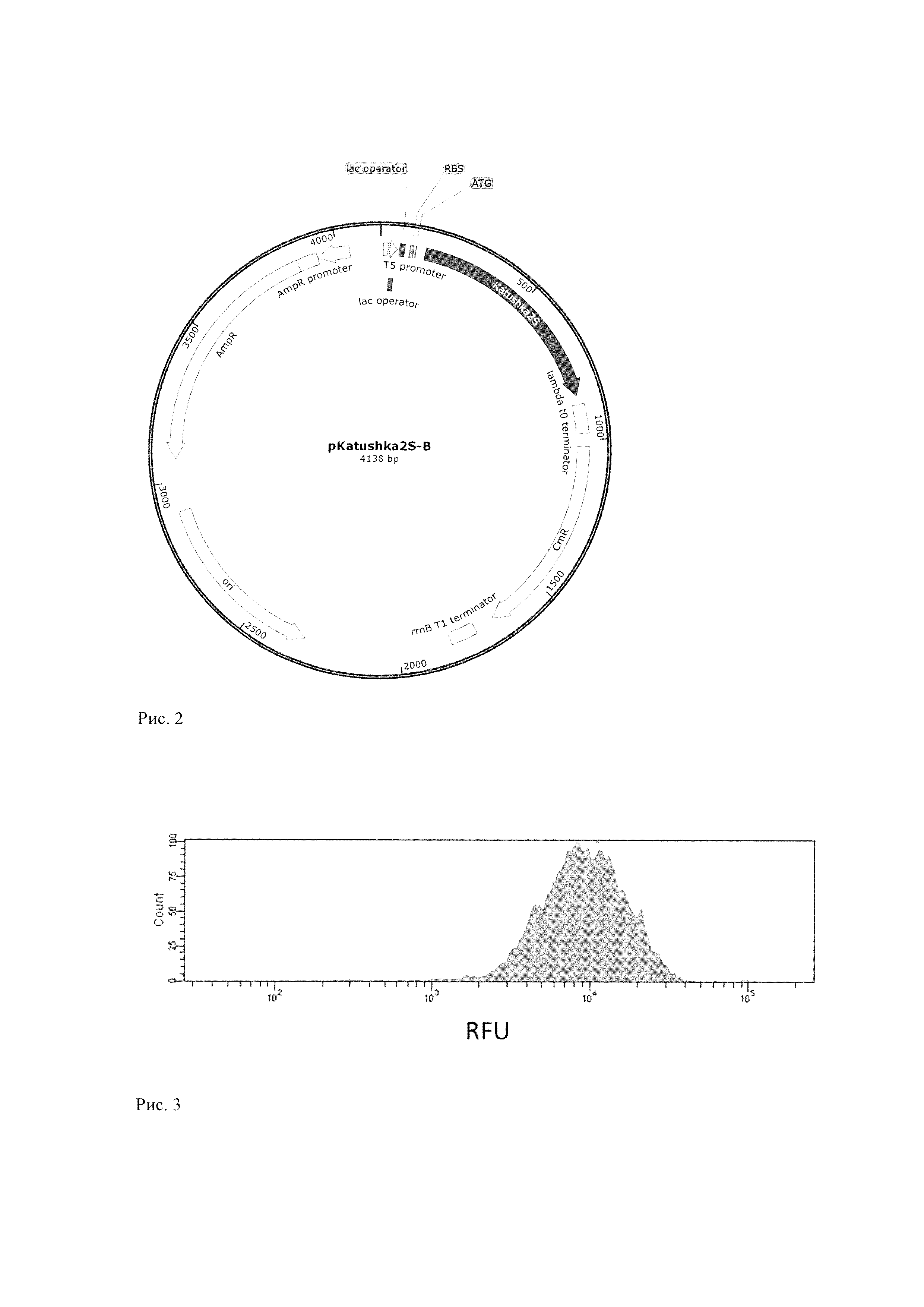
Рис. 2. Схема генетической конструкции pKatushka2S-B.
Рис. 3. Анализ флуоресценции капель двойной эмульсии, содержащих биосенсор.
Изобретение иллюстрируют следующими примерами.
ПРИМЕР 1
Создание биосенсора на основе клеток Escherichia coli.
Трансформацию проводят стандартным методом электропорации. Для этого 1 мкг плазмидной ДНК смешивают со 100 мкл электрокомпетентных клеток Escherichia coli DH5a и проводят электропорацию при напряжении 2.1 кВ/см, сопротивлении 100 Ом, емкость 25 мкФ. Полученную смесь инкубируют в 1 мл свежей среды SOB с 50 мМ глюкозы в течение 30 минут при 37°C и высевают на две чашки Петри со 100 мкг/мл ампициллина и 40 мкг/мл ИПТГ в количестве 100 и 900 мкл. Через 10-16 часов при инкубации в термостате при 37°C обнаружили появление единичных колоний красного цвета ввиду внутриклеточной продукции Katushka2S. Эффективность трансформации составила 5.0×107 колоний/мкг для Escherichia coli DH5α.
ПРИМЕР 2
Анализ флуоресценции биосенсора.
Клетки E.coli культивируют в среде 2YT с 50 мкг/мл ампицилина. Культивацию проводят в колбе при 37°C при 250 об/мин. достижения логарифмической фазы роста (4-6 часов). Полученные суспензии клеток промывают 3 раза средой для кокультивации (0.16% триптона, 0.1%) дрожжевого экстракта, 0.05% NaCl, 0.5% глицерина, 0.67% YNB и 1 мМ ИПТГ), после чего подвергают фильтрации с использованием клеточных сит с размером пор 40 мкм (Greiner Bio-One, Германия) и разводят до 0.1 ОЕ600 (λ=10). Клетки подвергают инкапсуляции с использованием 60 мкм чипов. Полученную эмульсию инкубируют в течение 48 часов при 25°C. Капли были отобраны с использованием клеточного сортера FACSAria III (BD, США). Выбор популяции капель двойной эмульсии осуществлялся с использованием светорассеяния и фоновой флуоресценции субстрата или ростовой среды.
Штамм-продуцент флуоресцентного белка Katushka2S на основе штамма Escherichia coli DH5α, трансформированного экспрессионной векторной плазмидой pKatushka2S-B, содержащей нуклеотидные последовательности индуцибельного промотера Т5 в составе lac-оперона, гена дальне-красного флуоресцентного белка Katushka2S, гена blat устойчивости к ампициллину, обеспечивающей внутриклеточную продукцию дальне-красного флуоресцентного белка Katushka2S, для проведения ультравысокопроизводительного скрининга.