Результат интеллектуальной деятельности: КОМПОЗИЦИЯ СО СТАБИЛИЗИРОВАННЫМ СУБТИЛИЗИНОМ
Вид РИД
Изобретение
Ссылка на перечень последовательностей
Данная заявка содержит перечень последовательностей в читаемой на компьютере форме.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к композиции, содержащей субтилизин, который стабилизирован с помощью производного пептида, содержащего альдегидную группу. Оно также относится к способу получения композиции и к соединению для применения в композиции.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
WO 98/13458, WO 94/04651, WO 98/13460, WO 95/25791 и WO 2009/118375 раскрывают жидкие моющие средства с субтилизинподобной протеазой, стабилизированной пептидом, содержащим альдегидную группу. WO 2011/036153 раскрывает, что добавление пептида, содержащего альдегидную группу, к субтилизинсодержащему моющему средству в форме частиц может улучшить моющую способность.
Общеизвестно, что альдегиды могут образовывать с NaHSO3 растворимые аддукты (бисульфитные или гидросульфитные аддукты) и эти пептиды, содержащие альдегидную группу, как правило, являются умеренно водорастворимыми.
WO 98/47523 и US 6500802 раскрывают пептидил-2-амино-1-гидроксиалкенсульфоновые кислоты и их использование в качестве ингибиторов протеазы. US 5436229 раскрывает бисульфитные аддукты производные L-аргинина, содержащих альдегидную группу, и их применение в качестве ингибиторов тромбина.
US 4703036, US 4478745 и US 5578574 раскрывают способы получения пептидов, содержащих альдегидную группу, в сухом виде.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В крупномасштабном производстве композиций со стабилизированным субтилизином из соображений безопасности и осуществления способа настоятельно рекомендуют использовать жидкие исходные материалы. Пептиды, содержащие альдегидную группу, как правило, являются умеренно водорастворимыми, что делает получение концентрированных водных растворов затрудненным или невозможным и требует использования либо сухого продукта, либо очень разбавленных водных растворов, когда получают растворы стабилизированного субтилизина для использования в жидких составах или для грануляции, для получения гранулированных композиций.
Превращение пептида, содержащего альдегидную группу, в гидросульфитный аддукт может быть использовано для увеличения растворяемости в воде при очистке пептидов, содержащих альдегидную группу. Предпочтительно, было обнаружено что данный гидросульфитный аддукт сам по себе является эффективным в качестве ингибитора и стабилизатора субтилизина, и что он также может стабилизировать второй (не субтилизин) фермент, если он присутствует. Было обнаружено, что гидросульфитный аддукт будет эффективным в качестве ингибитора субтилизина, и было обнаружено, что он сохраняет свои ингибирующий и стабилизирующий эффекты в жидком моющем средстве при хранении. Таким образом, путем применения гидросульфитного аддукта можно избежать затрат средств и времени на превращение его обратно в пептид, содержащий альдегидную группу, и можно сэкономить на последующем высушивании пептида, содержащего альдегидную группу, и с помощью этого можно избежать неудобства использования пептида, содержащего альдегидную группу, в виде порошка или в виде очень разбавленного водного раствор. Кроме того, добавление бисульфитного аддукта пептида, содержащего альдегидную группу, может также улучшить моющую способность (моющую характеристику) субтилизинсодержащего моющего средства.
Соответственно, настоящее изобретение обеспечивает композицию, содержащую субтилизин и гидросульфитный аддукт пептида, содержащего альдегидную группу, который имеет формулу X-B1-NH-CHR-CHOH-SO3M. Группы в формуле имеют следующее значение:
a) М является Н (водородом) или щелочным металлом, предпочтительно Na или K;
b) R является такой группой, чтобы NH-CHR-CO являлся L- или D-аминокислотным остатком (в дальнейшем обозначен В0);
c) В1 является одним аминокислотным остатком; и
d) X состоит из одного или нескольких аминокислотных остатков (предпочтительно одного или двух), которые необязательно содержат N-концевую защитную группу.
Настоящее изобретение также обеспечивает способ получения композиции, причем способ включает смешивание субтилизина, водного раствора, содержащего гидросульфитный аддукт пептида, содержащего альдегидную группу, который имеет формулу X-B1-NH-CHR-CHOH-SO3M (где М, R, В1 и Х определены выше), и необязательно поверхностно-активного вещества.
Дополнительно, настоящее изобретение обеспечивает соединение для использования в композиции, которая включает гидросульфитный аддукт пептида, содержащего альдегидную группу, который имеет формулу X-B1-NH-CHR-CHOH-SO3M. R может быть п-гидрокси-бензолом, и М, В1 и Х определены выше.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Композиция со стабилизированным субтилизином
Композиция по настоящему изобретению содержит субтилизин и гидросульфитный аддукт пептида, содержащего альдегидную группу, и может необязательно содержать второй фермент. Композиция может быть в жидкой или гранулированной форме. Это может быть моющий состав, который дополнительно содержит поверхностно-активное вещество.
В композиции, такой как жидкое или гранулированное моющее средства, количество каждого фермента (субтилизина и второго дополнительного фермента) обычно будет составлять 0,04-80 мкмоль (или мкмоль/кг), в частности 0,2-30 мкмоль, главным образом 0,4-20 мкмоль (в основном 1-2000 мг/л или мг/кг, в частности 5-750 мг/л, главным образом 10-500 мг/л) в пересчете на чистый белок-фермент. В композиции, такой как концентрат ферментного препарата, количество каждого фермента обычно будет составлять 0,01-20 ммоль, в частности 0,04-10 ммоль, главным образом 0,1-5 ммоль (в основном 0,3-500 г/л, в частности 1-300 г/л, главным образом 3-150 г/л) в пересчете на чистый белок-фермент.
Молярное соотношение стабилизатора или ингибитора фермента к субтилизину в соответствии с настоящим изобретением составляет по меньшей мере 1:1 или 1,5:1, и это составляет менее 1000:1, более предпочтительно менее 500:1, еще более предпочтительно от 100:1 до 2:1 или от 20:1 до 2:1, или более предпочтительно молярное соотношение составляет от 10:1 до 3:1.
Пептид, содержащий альдегидную группу
Бисульфитный аддукт, применяемый в способе, может быть получен из пептида, содержащего альдегидную группу, с формулой Х-В1-В0-H, где группы определены выше, при этом В0 является отдельным аминокислотным остатком с L- или D-конфигурацией с формулой: NH-CHR-CO.
NH-CHR-CO (В0) является L- или D-аминокислотным остатком, где R может быть алифатической или ароматической боковой цепью, например, аралкилом, таким как бензол, где R может быть необязательно замещенным. Более конкретно, остаток В0 может быть объемным, нейтральным, полярным, гидрофобным и/или ароматическим, необязательно замещенным. Примерами являются D- или L-формы Tyr (п-тирозина), м-тирозина, 3,4-дигидроксифенилаланина, Phe, Val, Met, норвалина (Nva), Leu, Ile или норлейцина (Nle); в частности Tyr, м-тирозина, 3,4-дигидроксифенилаланина, Phe, Val, Met, Nva или Nle.
В приведенной выше формуле, Х-В1-В0-Н, остаток В1 в частности может быть небольшим, алифатическим, гидрофобным и/или нейтральным. Примерами являются аланин (Ala), цистеин (Cys), глицин (Gly), пролин (Pro), серии (Ser), треонин (Thr), валин (Val), норвалин (Nva) и норлейцин (Nle); в частности Ala, Cys, Gly, Ser, Thr, Val, Nva и Nle.
X в частности может быть одним или двумя аминокислотными остатками с дополнительной N-концевой защитной группой (например, соединение является три- или тетрапептидом, содержащим альдегидную группу, с или без защитной группой). Таким образом, Х может быть В2, В3-В2, Z-B2, Z-B3-B2 где каждый В3 и В2 представляют собой один аминокислотный остаток, и Z является N-концевой защитной группой.
Остаток В2 может быть в частности небольшим, алифатическим и/или нейтральным, например, Ala, Gly, Thr, Arg, Leu, Phe или Val; в частности Gly, Thr или Val.
Остаток В3 может быть в частности большим, гидрофобным, нейтральным и/или ароматическим, необязательно замещенным, например, Phe, Tyr, Trp, фенилглицин, Leu, Val, Nva, Nle или Ile.
N-концевая защитная группа Z (если присутствует) может быть выбрана из формильной, ацетильной (Ас), бензоильной, трифторацетильной, фторметоксикарбонильной, метоксисукцинильной, ароматической и алифатической уретановой защитной группы, бензилоксикарбонильной (Cbz), т-бутилоксикарбонильной, адамантилоксикарбонильной, п-метоксибензильной карбонильной (MOZ), бензильной (Bn), п-метоксибензильной (РМВ) или п-метоксифенильной (РМР), метоксикарбонильной (Moc); метоксиацетильной (Mac); метилкарбаматной или метиламинокарбонильной/метилмочевинной группы. В случае тетрапептида, содержащего альдегидную группу, с защитной группой (например Х=Z-В3-В2), Z предпочтительно является небольшой алифатической группой, например, формильной, ацетильной, фторметоксикарбонильной, т-бутилоксикарбонильной, метоксикарбонильной (Moc); метоксиацетильной (Mac); метилкарбаматной или метиламинокарбонильной/метилметилмочевинной группой. В случае трипептида, содержащего альдегидную группу, с защитной группой (например Х=Z-B2), Z предпочтительно является большой ароматической группой, такой как бензоильная, бензилоксикарбонильная, п-метоксибензилкарбонильная (MOZ), бензильная (Bn), п-метоксибензильная (РМВ) или п-метоксифенильная (РМР).
Пригодные пептиды, содержащие альдегидную группу, описаны в WO 94/04651, WO 95/25791, WO 98/13458, WO 98/13459, WO 98/13460, WO 98/13461, WO 98/13461, WO 98/13462, WO 2007/141736, WO 2007/145963, WO 2009/118375, WO 2010/055052 и WO 2011/036153, Более конкретно, пептид, содержащий альдегидную группу, может быть Z-
 Здесь, Z является бензилоксикарбонилом, Me является метилом, Et является этилом, Ас является ацетилом, Н является водородом и другие буквы представляют аминокислотные остатки, обозначенные с помощью стандартного однобуквенного обозначения (например, F=Phe, Y=Туr, L=Leu).
Здесь, Z является бензилоксикарбонилом, Me является метилом, Et является этилом, Ас является ацетилом, Н является водородом и другие буквы представляют аминокислотные остатки, обозначенные с помощью стандартного однобуквенного обозначения (например, F=Phe, Y=Туr, L=Leu).
Альтернативно, пептид, содержащий альдегидную группу, может иметь такую формулу, как раскрыто в WO 2010/055052:
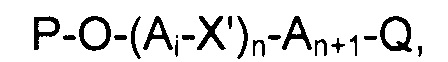
где Q является водородом, СН3, СХ3, СНХ2 или СН2Х, где Х является атомом галогена;
где один X' является "двойной N-блокирующей группой" СО, СО-СО, CS, CS-CS или CS-CO, наиболее предпочтительно уридо (СО), и другие X' отсутствуют,
где n=1-10, предпочтительно 2-5, наиболее предпочтительно 2,
где каждый из Ai и An+1 является аминокислотным остатком, который имеет структуру:
-NH-CR-CO- для остатка справа от Х=-СО- или
-CO-CR-NH- для остатка слева от Х=-СО-,
где R является Н- или необязательно замещенной алкильной или алкиларильной группой, которая может необязательно включать гетероатом и может необязательно быть связанной с атомом N, и
где Р является водородом или любой С-концевой защитной группой. Примеры подобных пептидов, содержащих альдегидную группу, включают α-MAPI, β-MAPI, F-мочевина-RVY-Н, F-мочевина-GGY-Н, F-мочевина-GAP-Н, F-мочевина-GAY-H, F-мочевина-GAL-H, F-мочевина-GA-Nva-H, F-мочевина-GA-Nle-H, Y-мочевина-RVY-Н, Y-мочевина-GAY-H, F-CS-RVF-H, F-CS-RVY-H, F-CS-GAY-H, антипаин, GE20372A, GE20372B, химостатин А, химостатин В и химостатин С.
Также примеры пептидов, содержащих альдегидную группу, раскрытые в WO 2010/055052 и WO 2009/118375, WO 94/04651, WO 98/13459, WO 98/13461, WO 98/13462, WO 2007/145963, (P&G) включены в данный документ посредством ссылки.
Гидросульфитный аддукт пептида, содержащего альдегидную группу
Гидросульфитный аддукт пептида, содержащего альдегидную группу, может быть получен из пептидов, содержащих альдегидную группу, которые описаны выше.

Субтилизин
Субтилизины являются подгруппой серин-протеаз. Серин-протеаза является ферментом, который катализирует гидролиз пептидных связей, и в активном сайте которых присутствует обязательный остаток серина (White, Handler и Smith, 1973 "Principles of Biochemistry," Fifth Edition, McGraw-Hill Book Company, NY, pp.271-272). Субтилизины включают, предпочтительно состоят из, подгрупп I-81 и I-S2, как определено Siezen et al., Protein Engng. 4 (1991) 719-737; и Siezen et al., Protein Science 6 (1997) 501-523. Исходя из высоко консервативной структуры активного сайта серин-протеаз, субтилизин в соответствии с настоящим изобретением может быть функционально эквивалентным предлагаемой подгруппе подробно определенной Siezen et al. (ранее).
Субтилизин может быть животного, растительного или микробного происхождения, включая химически или генетически модифицированных мутантов (варианты белковой инженерии). Примерами субтилизинов являются полученные из Bacillus, например, субтилизин Novo, субтилизин Carlsberg, субтилизин BPN', субтилизин 309, субтилизин 147 и субтилизин 168 (описанный в WO 89/06279) и протеаза PD138 (WO 93/18140). Примеры описаны в WO 98/020115, WO 01/44452, WO 01/58275, WO 01/58276, WO 03/006602 и WO 04/099401. Другие примеры являются вариантами, которые описаны в WO 92/19729, WO 98/20115, WO 98/20116, WO 98/34946, WO 2011/036263 и смеси протеаз.
Примеры коммерчески доступных субтилизинов включают Kannase™, Everlase™, Relase™, Esperase™, Alcalase™, Durazym™, Savinase™, Ovozyme™, Liquanase™, Coronase™, Polarzyme™, Pyrase™, Pancreatic Trypsin NOVO (PTN), Bio-Feed™ Pro и Clear-Lens™ Pro; Blaze (все доступны от Novozymes A/S, Багсвард, Дания). Другие коммерчески доступные субтилизины включают Ronozyme™ Pro, Maxatase™, Maxacal™, Maxapem™, Opticlean™, Properase™, Purafast™, Purafect™, PurafectOx™, Purafact Prime™, Excellase™, FN2™, FN3™ и FN4™ (доступны от Genencor International Inc., Gist-Brocades, BASF или DSM). Другими примерами являются Primase™ и Duralase™. Blap R, Blap S и Blap X, доступные от Henkel.
Второй фермент
В дополнение к субтилизину, моющий состав может необязательно содержать второй фермент, такой как липаза, кутиназа, амилаза, карбогидраза, целлюлаза, пектиназа, пектат-лиаза, маннаназа, арабиназа, галактаназа, ксиланаза, оксидаза, лакказа, и/или пероксидаза. Композиция может содержать один, два или более несубтилизиновых ферментов.
Липаза и кутиназа
Пригодные липазы и кутиназы включают таковые бактериального или грибкового происхождения. Включают химически модифицированные или мутанты белковой инженерии. Примеры включают липазу из Thermomyces, например, из Т.lanuginosus (которую ранее называли Humicola lanuginosa), как описано в ЕР 258068 и ЕР 305216, кутиназа из Humicola, например Н.insolens, как описано в WO 96/13580, Pseudomonas липаза, например, из Р.alcaligenes или Р.pseudoalcaligenes (ЕР 218272), Р.cepacia (ЕР 331376), Р.stutzeri (GB 1372034), Р.fluorescens, Pseudomonas sp. штамм SD 705 (WO 95/06720 и WO 96/27002), P.wisconsinensis (WO 96/12012), липаза Bacillus, например, из В.subtilis (Dartois et al., 1993, Biochemica et Biophysica Acta, 1131: 253-360), В.stearothermophilus (JP 64/744992) или В.pumilus (WO 91/16422).
Другие примеры являются вариантами липаз, таких как описанные в WO 92/05249, WO 94/01541, ЕР 407225, ЕР 260105, WO 95/35381, WO 96/00292, WO 95/30744, WO 94/25578, WO 95/14783, WO 95/22615, WO 97/04079, WO 97/07202, WO 00/060063, WO 2007/087508 и WO 2009/109500.
Предпочтительные коммерчески доступные ферменты-липазы включают Lipolase™, Lipolase Ultra™ и Lipex™; Lecitase™, Lipolex™; Lipoclean™, Lipoprime™ (Novozymes A/S). Другие коммерчески доступные липазы включают Lumafast (Genencor Int Inc); Lipomax (Gist-Brocades/Genencor Int Inc) и липазу Bacillus sp от Solvay.
Амилаза
Пригодные амилазы (α и/или β) включают таковые бактериального или грибкового происхождения. Включают химически модифицированные или мутанты белковой инженерии. Амилазы включают, например, α-амилазы полученные из Bacillus, например, специальный штамм Bacillus licheniformis, описанный более детально в GB 1296839.
Примерами полезных амилаз являются варианты, описанные в WO 94/02597, WO 94/18314, WO 96/23873 и WO 97/43424, особенно варианты с заменами одной или нескольких следующих позиций: 15, 23, 105, 106, 124, 128, 133, 154, 156, 181, 188, 190, 197, 202, 208, 209, 243, 264, 304, 305, 391, 408 и 444.
Коммерчески доступными амилазами являются Stainzyme; Stainzyme Plus; Duramyl™, Termamyl™, Termamyl Ultra; Natalase, Fungamyl™ и BAN™ (Novozymes A/S), Rapidase™ и Purastar™ (от Genencor International Inc.).
Лиазы
Пектат-лиаза может быть ферментом дикого типа, полученной из Bacillus, в частности В.licherniformis или B.agaradhaerens, или вариантом, полученным от любого из этих, например, как описано в US 6124127, WO 1999/027083, WO 1999/027084, WO 2002/006442, WO 2002/092741, WO 2003/095638. Коммерчески доступной пектат-лиазой является XPect; Pectawash и Pectaway (Novozymes A/S).
Маннаназа
Маннаназа может быть щелочной маннаназой семейства 5 или 26. Она может быть дикого типа из Bacillus или Humicola, в частности 6. agaradhaerens, В.licheniformis, В.halodurans, В.clausii или Н.insolens. Подходящие маннаназы описаны в WO 1999/064619. Коммерчески доступной маннаназой является Mannaway (Novozymes A/S).
Целлюлаза
Пригодные целлюлазы включают таковые бактериального или грибкового происхождения. Включают химически модифицированные или мутанты белковой инженерии. Пригодные целлюлазы включают целлюлазы из рода Bacillus, Pseudomonas, Humicola, Fusahum, Thielavia, Acremonium, например, грибковые целлюлазы, полученные от Humicola insolens, Myceliophthora thermophila и Fusahum oxysporum, раскрытые в US 4435307, US 5648263, US 5691178, US 5776757 и WO 89/09259.
Особенно пригодными целлюлазами являются щелочные или нейтральные целлюлазы, имеющие преимущества сохранения цвета. Примерами таких целлюлаз являются целлюлазы, описанные в ЕР 0495257, ЕР 0531372, WO 96/11262, WO 96/29397, WO 98/08940. Другими примерами являются такие варианты целлюлаз, как описанные в WO 94/07998, ЕР 0531315, US 5457046, US 5686593, US 5763254, WO 95/24471, WO 98/12307 и WO 99/01544.
Коммерчески доступными целлюлазами являются Celluzyme, Celluclean; Endloase; Carezyme; Renozyme; whitezyme (Novozymes A/S).
Приготовление пептида, содержащего альдегидную группу, и гидросульфитного/бисульфитного аддукта
Пептид, содержащий альдегидную группу, может быть преобразован в водорастворимый гидросульфитный аддукт с помощью реакции с бисульфитом натрия, как описано в учебниках, например March, J. Advanced Organic Chemistry, fourth edition, Wiley-lnterscience, US 1992, p 895.
Преобразование в гидросульфитный аддукт является обратимым (Ex J. Am. Chem. Soc. 1978, 100, 1228). Таким образом, аддукт может частично или полностью восстанавливаться для высвобождения пептида, содержащего альдегидную группу, в жидкое моющее средство, в жидкий состав с субтилизином или в промывочную воду.
Обсуждаемый пептид, содержащий альдегидную группу, может быть получен известными способами, например, как описано в US 4703036, US 4478745 или US 5578574 с помощью исключения заключительного этапа досушивания, или может быть получен любыми способами, рассмотренными в J. Pept. Sci. 2007; 13; 1-15, или как представлено в Synthesis 1983, 676. Пептид, содержащий альдегидную группу, может быть сырым или очищенным, выделенным в виде твердого вещества или оставаться в растворе с помощью органического растворителя.
Водный раствор бисульфитного аддукта может быть получен благодаря реакции соответствующего пептида, содержащего альдегидную группу, с водным раствором бисульфита натрия (гидросульфита натрия, NaHSO3); бисульфита калия (KHSO3) известными способами, например, как описано в WO 98/47523; US 6500802; US 5436229; J. Am. Chem. Soc. 1978, 100, 1228; Org. Synth., Coll. Vol.7: 361.
Моющий состав
Моющее средство может быть гранулированным или жидким моющим средством. Жидкое моющее средство находится в физической форме, которая не является твердым веществом (или газом); это может быть текучая жидкость, текучий гель или нетекучий гель. Он может быть либо изотропный или структурированный, предпочтительно изотропной. Он включает составы, пригодные для стирки в автоматических стиральных машинах или для ручной стирки. Моющее средство содержит по меньшей мере одно поверхностно-активное вещество. Моющее средство может также включать наполнитель.
Твердый моющий состав может быть гранулированным или порошкообразным, или порошкообразным/гранулированным спрессованным в таблетку, брикет. Композиция может быть в форме таблетки, брикета или пакета, включая многокамерные пакеты. Композиция может быть в форме порошка, например свободнотекучего порошка, такого как агломерат, порошок, полученный распылительной сушкой, инкапсуоированный, экструдат, игольчатый, лентообразный, в виде хлопьев или любой их комбинации.
Ингредиенты моющего средства могут быть отделены физически один от другого с помощью камер в водорастворимых пакетах или в различных слоях таблеток (смотри одноразовую дозу ниже). Таким образом можно избежать отрицательного взаимодействия между компонентами при хранении. Различные профили растворимости каждой из камер могут также давать задержку растворяемости выбранных компоненты в моющем растворе.
Пакеты могут быть любой формы, вида и материала, который является пригодным для удерживания композиции, например, без возможности высвобождения композиции из пакета до контакта с водой. Пакет сделан из водорастворимой пленки, которая охватывает внутренний объем. Указанный внутренний объем может быть разделен на камеры пакета. Предпочитаемыми пленками являются полимерные материалы, предпочтительно полимеры, которые сформированы в пленку или слой. Предпочтительные полимеры, сополимеры или их производные выбраны из полиакрилатов и водорастворимых сополимеров акрилата, метилцеллюлозы, карбоксиметилцеллюлозы, декстрина натрия, этилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, мальтодекстрина, полиметакрилатов, наиболее предпочтительно сополимеры поливинилового спирта и гидроксипропилметилцеллюлоза (НРМС). Предпочтительно, уровень полимера в пленке, например, PVA, составляет по меньшей мере около 60%. Предпочтительный средний молекулярный вес обычно составляет от около 20000 до около 150000. Пленки могут также представлять собой смесь композиций, которая содержит гидролитическиразлагаемые и водорастворимые полимерные смеси, такие как полилактид и поливиниловый спирт (известный под торговым названием М8630, продаваемые Chris Craft In. Prod. Of Gary, Индиана, США) а также пластификаторы, такие как глицерин, этилен глицерин, пропиленгликоль, сорбитол и их смеси. Пакеты могут содержать твердую чистящую композицию для стирки или часть компонентов и/или жидкую чистящую композицию или часть компонентов разделенных водорастворимой пленкой. Камера для жидких компонентов может быть отличной по составу от камер, содержащих твердые вещества (смотри, например, US 2009/0011970).
Выбор компонентов моющего средства может включать, для ухода за тканью, рассмотрение типа ткани, которую необходимо очистить, тип и/или степень загрязнения, температуру при которой осуществляется чистка и состав продукта моющего средства. Хотя компоненты, упомянутые ниже, относят к категории с общим названием, в соответствии с конкретной функциональной возможностью, это не должно быть истолковано как ограничение, так как компонент может содержать дополнительные функциональные возможности, что будет понятно специалисту в данной области.
В одном варианте осуществления композиция со стабилизированным субтилизином по настоящему изобретению может быть добавлена к моющему составу в количестве, соответствующем 0,001-100 мг белка, таком как 0,01-100 мг белка, предпочтительно 0,005-50 мг белка, более предпочтительно 0,01-25 мг белка, еще более предпочтительно 0,05-10 мг белка, наиболее предпочтительно 0,05-5 мг белка и еще наиболее предпочтительно 0,01-1 мг белка на литр моющего раствора.
Одноразовая доза
Продукт одноразовой дозы представляет собой упаковку однократной дозы в одноразовом контейнере. Его все шире применяют в моющих средствах для стирки и мытья посуды. Продукт одноразовой дозы моющего средства представляет собой упаковку (например, в пакет сделанный из водорастворимой пленки) количества моющего средства, применяемого для одного мытья.
В одном аспекте моющий состав представлен в форме одноразовой дозы. Продукты моющего средства в форме одноразовой дозы включают таблетки, капсулы, саше, пакеты и т.д. В одном аспекте, для использования в данном документе, таблетки упакованы в водорастворимую пленку и водорастворимые пакеты. Вес моющего состава по настоящему изобретению составляет от около 10 до около 25 грамм, от около 12 до около 24 грамм или даже от 14 до 22 грамм. Данные количества веса являются очень удобными для того, чтобы продукт моющего средства подходил для дозирующего устройства автоматической посудомоечной машины. В случаях продуктов одноразовой дозы, которые имеют водорастворимый материал, упаковывающий моющий состав, водорастворимый материал не рассматривается как часть композиции. В одном аспекте, формой одноразовой дозы является водорастворимый пакет (например, водорастворимая пленка, упаковывающая моющий состав), в одном аспекте, многокамерный пакет, который включает множество пленок, образующих множество камер. Данная конфигурация способствует гибкости и оптимизации композиции. Это делает возможным разделение и контролируемое высвобождение различных ингредиенты. В одном аспекте, одна камера содержит моющий состав в твердой форме, а другая камера содержит моющий состав в жидкой форме.
В одном аспекте варианты осуществления многокамерного пакета две различные камеры могут содержать два различных чистящих средства. В одном аспекте пленки этих двух камер имеют различные профили растворимости, позволяющие высвободить одинаковые или различные средства в различное время. Например, средство из одной камеры (первой камеры) может быть доставлено в начале процесса мойки, чтобы помочь с удалением грязи и второе средство из другой камеры (второй камеры) может быть доставлено по меньшей мере на две минуты или еще по меньшей мере на пять минут позже, чем средство из первой камеры.
В одном аспекте раскрывается многокамерный пакет, содержащий две камеры, расположенные бок о бок, лежащие на другой камере, где по меньшей мере две различные камеры содержат два различных моющих состава.
Многокамерная упаковка образована из множества водорастворимых упаковывающих материалов, которые образовывают множество камер, одна из камер может содержать некоторые или все ингредиенты моющего состава, другая камера может содержать жидкую композицию, жидкая композиция может быть водной (например, содержит более 10 процентов воды по весу жидкой композиции) и камера может быть сделана из растворимого в теплой воде материала. В одном вариант осуществления одна камера сделана из растворимого в холодной воде материала. Это делает возможным разделение и контролируемое высвобождение различных ингредиенты. В других вариантах осуществления все камеры сделаны из растворимого в теплой воде материала.
Пригодные упаковки содержат по меньшей мере две камеры, расположенные бок о бок, лежащие (например, размещенные выше) на другой камере, особенно пригодными являются пакеты. Данное расположение способствует компактности, прочности и крепости упаковки, оно дополнительно минимизирует количество требуемого водорастворимого материала. Оно требует только три части материала, чтобы образовывать три камеры. Прочность упаковки позволяет также использовать очень тонкие пленки без ущерба для механической прочности упаковки. Упаковку также очень легко использовать, так как камеры не надо складывать для использования в машинных дозирующих устройствах с фиксированной конфигурацией. По меньшей мере две камеры упаковки содержат два различных моющих состава. Под "различными композициями" в данном документе понимают моющие составы, которые отличаются по меньшей мере одним ингредиентом.
В одном аспекте по меньшей мере одна из камер содержит твердый моющий состав, а другая камера водный жидкий моющий состав, обычно весовое соотношение твердой композиции к жидкой составляет от около 20:1 до около 1:20, от около 18:1 до около 2:1 или от около 15:1 до около 5:1. Данный тип упаковки является очень изменчивым, потому что он может адаптироваться под композиции, которые имеют широкий спектр значений соотношения твердого вещества : жидкости. Пакеты имеют высокое соотношение твердого вещества : жидкости, потому, что много ингредиентов моющего средства являются особенно пригодными для использования в твердой форме, в одном аспекте в виде порошка. Соотношение твердое вещество : жидкость, определенное в данном документе, относится к отношению между весом всей твердой композиции и весом всей жидкой композиции в упаковке.
Пригодные весовые соотношения твердого вещества : жидкости составляют от около 2:1 до около 18:1 или от около 5:1 до около 15:1. Данные весовые соотношения являются пригодными в случаях, в которых большинство ингредиентов моющего средства находятся в жидкой форме.
В одном аспекте, две камеры, расположенные бок о бок, содержат жидкие моющие составы, которые могут быть одинаковыми или различными, и другая камера содержит твердый моющий состав, например, в виде порошка, в одном аспекте, прессованного порошка. Твердая композиция способствует крепости и прочности упаковки.
Для того, чтобы подходить для дозирующего устройства, главным образом в автоматической посудомоечной машине, продукты формы одноразовой дозы в данном документе имеют квадратное или прямоугольное основание и высоту от около 1 до около 5 см или от около 1 до около 4 см. В одном аспекте вес твердой композиции составляет от около 5 до около 20 грамм или от около 10 до около 15 грамм и вес жидкой композиции составляет от около 0,5 до около 4 грамм или от около 0,8 до около 3 грамм. В одном аспекте по меньшей мере две пленки, которые образовали различные камеры, имеют различные растворимости при одинаковых условиях. Это позволяет высвобождать композиции, которые они частично или полностью упаковывают, в разное время.
Контролируемое высвобождение ингредиентов многокамерного пакета может быть достигнуто с помощью изменения толщины пленки и/или растворимости пленочного материала. Растворимость пленочного материала может быть задержана путем, например, сшивания пленки, как описано в WO 2002/102955. Другие водорастворимые пленки созданы для высвобождения при промывке, как описано в US 4765916 и US 4972017. Восковидное покрытие (смотри US 5453216) пленок может помочь с высвобождением при промывке. Средства для рН-контролируемого высвобождения описаны в US 5453216, в частности, аминоацетилированный полисахарид с избирательной степенью ацетилирования.
О других средствах для отсроченного высвобождения, которое достигается с помощью многокамерных пакетов с различными камерами, где камеры сделаны из пленок с различной степенью растворимости, сообщается в US 6727215.
Поверхностно-активные вещества
Моющий состав может содержать одно или несколько поверхностно-активных веществ, которые могут быть анионными, и/или катионными, и/или неионными, и/или полуполярными, и/или цвиттер-ионными или их смесью. В конкретном варианте осуществления моющий состав включает смесь одного или нескольких неионных поверхностно-активных веществ и одного или нескольких анионных поверхностно-активных веществ, но можно также использовать отдельно.
Поверхностно-активное(ые) вещество(а) обычно присутствует(ют) в количестве от около 0,1% до 60% по весу, таком как от около 1% до около 40%, или от около 3% до около 20%, или от около 3% до около 10%. Поверхностно-активное(ые) вещество(а) выбирают основываясь на целевом применении для очистки, и включает любое(ые) обычное(ые) поверхностно-активное(ые) вещество(а), известное(ые) в данной области техники. Для применения в моющих средствах, можно использовать любое поверхностно-активное вещество, известное в данной области техники.
Неограничивающие примеры анионных поверхностно-активных веществ включают сульфаты и сульфонаты, в частности, линейные алкилбензолсульфонаты (LAS), изомеры LAS, разветвленные алкилбензолсульфонаты (BABS), фенилалкенсульфонаты, альфа-олефинсульфонаты (AOS), олефинсульфонаты, алкенсульфонаты, алкен-2,3-диилбис(сульфаты), гидроксиалкенсульфонаты и дисульфонаты, алкилсульфаты (AS), такие как додецилсульфат натрия (SDS), сульфаты жирных спиртов (FAS), сульфаты первичных спиртов (PAS), эфирсульфаты спиртов (AES, или AEOS, или FES, также известные как этоксисульфаты спиртов или эфирсульфаты жирных спиртов, включая лаурилэфирсульфат натрия (SLES), мыла или жирные кислоты; вторичные алкенсульфонаты (SAS), сульфонаты парафина (PS), сульфонаты сложных эфиров, сложные эфиры глицерина и сульфонированных жирных кислот, метиловые сложные эфиры альфа-сульфожирных кислот (альфа-SFMe или SES), включая сульфонат сложного метилового эфира (MES), алкил- или алкенилянтарную кислоту, додецил/тетрадеценил янтарную кислоту (DTSA), жирнокислотные производные аминокислот, сложные диэфиры и моноэфиры сульфоянтарной кислоты или мыло и их комбинации.
Тогда как моющее средство, включенное в данный документ, будет обычно содержать от около 1% до около 40% по весу, как например от около 5% до около 30%, включая от около 5% до около 15% или от около 20% до около 25% анионного поверхностно-активного вещества.
Неограничивающие примеры неионных поверхностно-активных веществ включают этоксилаты спиртов (АЕ или АЕО), пропоксилаты спиртов, пропоксилированные жирные спирты (PFA), алкиловые сложные эфиры алкоксилированных жирных кислот, такие как алкиловые сложные эфиры этоксилированных и/или пропоксилированных жирных кислот, алкилфенолэтоксилаты (АРЕ), оксиэтилированные алкилфенолы (NPE), алкилполигликозиды (APG), алкоксилированные амины, моноэтаноламиды жирных кислот (FAM), диэтаноламиды жирных кислот (FADA), моноэтаноламиды этоксилированных жирных кислот (EFAM), моноэтаноламид пропоксилированной жирной кислоты (PFAM), амиды полигидроксиалкильных жирных кислот или N-ацил-N-алкильные производные глюкозамина (глюкамиды, GA, или глюкамид жирной кислоты, FAGA), a также продукты доступные под торговой маркой SPAN и TWEEN и их комбинации.
Тогда как моющее средство, включенное в данный документ, будет обычно содержать от около 0,2% до около 40% по весу неионного поверхностно-активного вещества, например от около 0,5% до около 30%, в частности от около 1% до около 20%, от около 3% до около 10%, такой как от около 3% до около 5% или от около 8% до около 12%.
Наполнители
Моющий состав может содержать по весу около 0-65% наполнителя моющего средства или сонаполнителя или их смесь. В моющем средстве для мытья посуды, уровень наполнителя составляет обычно 40-65%, в частности 50-65%. Наполнитель и/или сонаполнитель может быть, в частности, хелатирующим агентом, который образует водорастворимые комплексы с Са и Mg. Любые наполнитель и/или сонаполнитель, известные в данной области техники, могут быть использованы в моющих средствах для стирки. Неограничивающие примеры наполнителей включают цеолиты, дифосфаты (пирофосфаты), трифосфаты, такие как трифосфат натрия (STP или STPP), нитрилтрехуксусную кислоту, этилендиаминтетрауксусную кислоту (EDTA), диэтилентриаминпентауксусную кислоту, алкил- или алкенилянтарную кислоту, карбонаты, такие как карбонат натрия, растворимые силикаты, такие как метасиликат натрия, слоистые силикаты (например, SKS-6 от Hoechst), этаноламины, такие как 2-аминоэтан-1-ол (МЕА), иминодиэтанол (DEA) и 2,2',2''-нитрилотриэтанол (TEA), и карбоксиметилинулин (CMI) и их комбинации.
Наполнитель может быть сильным наполнителем, таким как метилглициндиацетилуксусная кислота ("MGDA") или тетранатриевая соль N,N-дикарбоксиметилглутаминовой кислоты (GLDA); он может быть средним наполнителем, таким как триполифосфат натрия (STPP), или он может быть слабым наполнителем, таким как цитрат натрия.
Отбеливающая система
Моющий состав может содержать по весу 0-50% отбеливающей системы. Может быть использована любая отбеливающая система, известная в данном уровне техники для применения в стиральных порошках. Компоненты пригодной отбеливающей системы включают катализаторы отбеливания, фотоотбеливатели, активаторы отбеливания, источники перекиси водорода, такие как перкарбонат натрия и пербораты натрия, заранее сформированные перкислоты и их смеси. Пригодные заранее сформированные перкислоты включают, но без ограничения, пероксикарбоновые кислоты и соли, перугольные кислоты и соли, перимидиновые кислоты и соли, пероксимоносерные кислоты и соли, например, оксон (R), и их смеси. Неограничивающие примеры отбеливающих систем включают отбеливающие системы на основе перекиси, которые могут содержать, например, неорганическую соль, в том числе соли щелочных металлов, такие как натриевые соли пербората (обычно моно- или тетрагидраты), перкарбонаты, персульфаты, перфосфаты, персиликатные соли, в комбинации с активатором отбеливания, образующим перкислоту. В данном документе активатор отбеливания означает соединение, которое реагирует с пероксидным отбеливателем, таким как перекись водорода с образованием перкислоты. Перкислота, полученная таким образом, представляет собой активированный отбеливатель. Пригодные активаторы отбеливания, которые будут использоваться в данном изобретении, включают те, которые принадлежат к классу сложноэфирных амидов, имидов или ангидридов. Подходящими примерами являются тетраацетилэтилендиамин (TAED), 3,5,5-триметилгексаноилоксибензолсульфонат натрия, дипероксидодекановая кислота, 4-(додеканоилокси)бензолсульфонат (LOBS), 4-(деканоилокси)бензолсульфонат, 4-(деканоилокси)бензоат (DOBS), 4-(3,5,5-триметилгексаноилокси)бензолсульфонат (ISONOBS), тетраацетилэтилендиамин (TAED) и 4-(нонаноилокси)бензолсульфонат (NOBS) и/или те, которые раскрыты в W098/17767. Конкретное семейство активаторов отбеливания, которое представляет интерес, раскрыто в ЕР624154 и наиболее предпочтительным в этом семействе является ацетилтриэтилцитрат (АТС). АТС или короткоцепочечный триглицерид, такой как триацин, имеет такое преимущество, что является экологически безопасным, так как в конце концов разрушается до лимонной кислоты и спирта. Кроме того, ацетилтриэтилцитрат и триацетин имеют хорошую гидролитическую стабильность в продукте при хранении и являются эффективным активатором отбеливания. Наконец, АТС обеспечивает хорошую вместимость наполнителя в добавке для стирки. Альтернативно, отбеливающая система может содержать пероксикислоты, например, амидного, имидного или сульфонового типа. Отбеливающая система может дополнительно содержать перкислоты, такие как 6-(фталоиламино)перкапроновая кислота (РАР). Отбеливающая система может дополнительно включать катализатор отбеливания.
Другие ингредиенты моющего состава, которые хорошо известны в данной области техники, включают гидротропы, тканевые окрашивающие средства, пеногасители, грязеудаляющие полимеры, средства против повторного осаждения и т.д.
Способы и композиции
В одном аспекте настоящее изобретение обеспечивает композицию, которая содержит субтилизин и гидросульфитный аддукт пептида, содержащего альдегидную группу, который имеет формулу X-B1-NH-CHR-CHOH-SO3M, где:
a) М является Н (водородом) или щелочным металлом;
b) R является такой группой, чтобы NH-CHR-CO являлся L или D-аминокислотным остатком;
c) В1 является одним аминокислотным остатком; и
d) X состоит из одного или нескольких аминокислотных остатков, которые необязательно содержат N-концевую защитную группу.
В одном варианте осуществления R является такой группой, чтобы NH-CHR-CO являлся L- или D-аминокислотным остатком Tyr, м-тирозина, 3,4-дигидроксифенилаланина, Phe, Val, Met, Nva, Leu, Ile или Nle.
В одном варианте осуществления В1 является остатком Ala, Cys, Gly, Pro, Ser, Thr, Val, Nva или Nle.
В одном варианте осуществления, X является В2, В3-В2, Z-B2 или Z-B3-B2, где каждый В2 и В3 представляет собой один аминокислотный остаток, и Z является N-концевой защитной группой. Предпочтительно, В2 является остатком Val, Gly, Ala, Arg, Leu, Phe или Thr. Предпочтительно, В3 является остатком Phe, Tyr, Trp, фенилглицина, Leu, Val, Nva, Nle или Ile.
В одном варианте осуществления Z является бензилоксикарбонилом (Cbz), п-метоксибензилкарбонилом (MOZ), бензилом (Bn), бензоилом (Bz), п-метоксибензилом (РМВ), п-метоксифенилом (РМР), формилом, ацетилом (Ас), метилокси или метилоксикарбонилом.
В одном варианте осуществления композиция находится в жидкой или гранулированной форме. Предпочтительно, композиция является моющим средством, которое дополнительно содержит поверхностно-активное вещество.
В одном варианте осуществления композиция дополнительно содержит второй фермент, в частности, липазу, кутиназу, амилазу, карбогидразу, целлюлазу, пектиназу, пектат-лиазу, маннаназу, арабиназу, галактаназу, ксиланазу, оксидазу, лакказу или пероксидазу.
В другом аспекте, настоящее изобретение обеспечивает способ получения композиции настоящего изобретения, как описано выше, способ, который включает смешивание субтилизина, водного раствора, который содержит гидросульфитный аддукт пептида, содержащего альдегидную группу с формулой X-B1-NH-CHR-CHOH-SO3M, как описано выше, и, необязательно, поверхностно-активное вещество.
В еще одном аспекте настоящее изобретение обеспечивает соединение для использования в композиции по настоящему изобретению, соединение, которое представляет собой гидросульфитный аддукт пептида, содержащего альдегидную группу с формулой X-B1-NH-CHR-CHOH-SO3M, где М и Х определены как описано выше, В1 является аминокислотным остатком, который является отличным от пролина (Pro), и R является такой группой, чтобы NH-CHR-CO являлся L- или D-аминокислотным остатком Tyr, м-тирозина, 3,4-дигидроксифенилаланина, Phe, Val, Met, Nva или Nle.
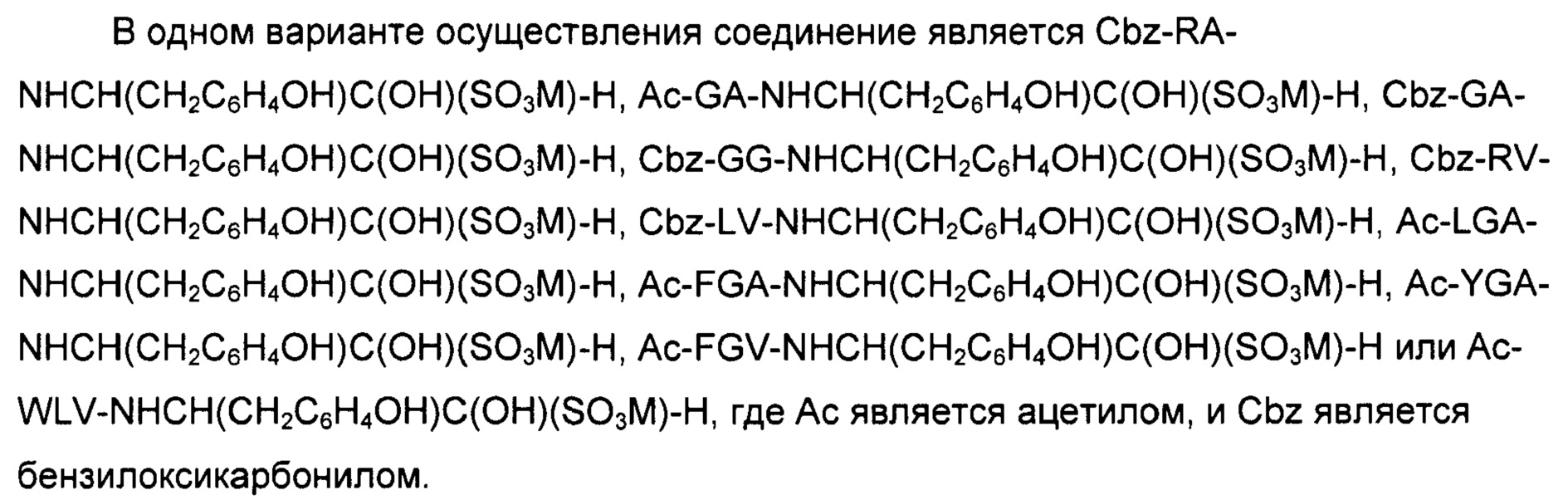
В еще одном аспекте, настоящее изобретение обеспечивает соединение для использования в композиции по настоящему изобретению, причем соединение является гидросульфитным аддуктом пептида, содержащего альдегидную группу, с формулой X-B1-NH-CHR-CHOH-SO3M, где М, R и Х определены как описано выше, и где В1 является аминокислотным остатком аланина (Ala), цистеина (Cys), глицина (Gly), серина (Ser), треонина (Thr), валина (Val), норвалина (Nva) и норлейцина (Nle).
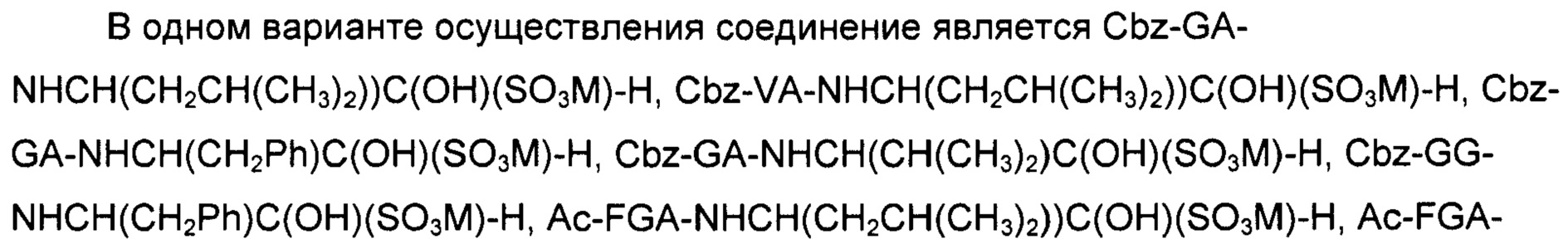
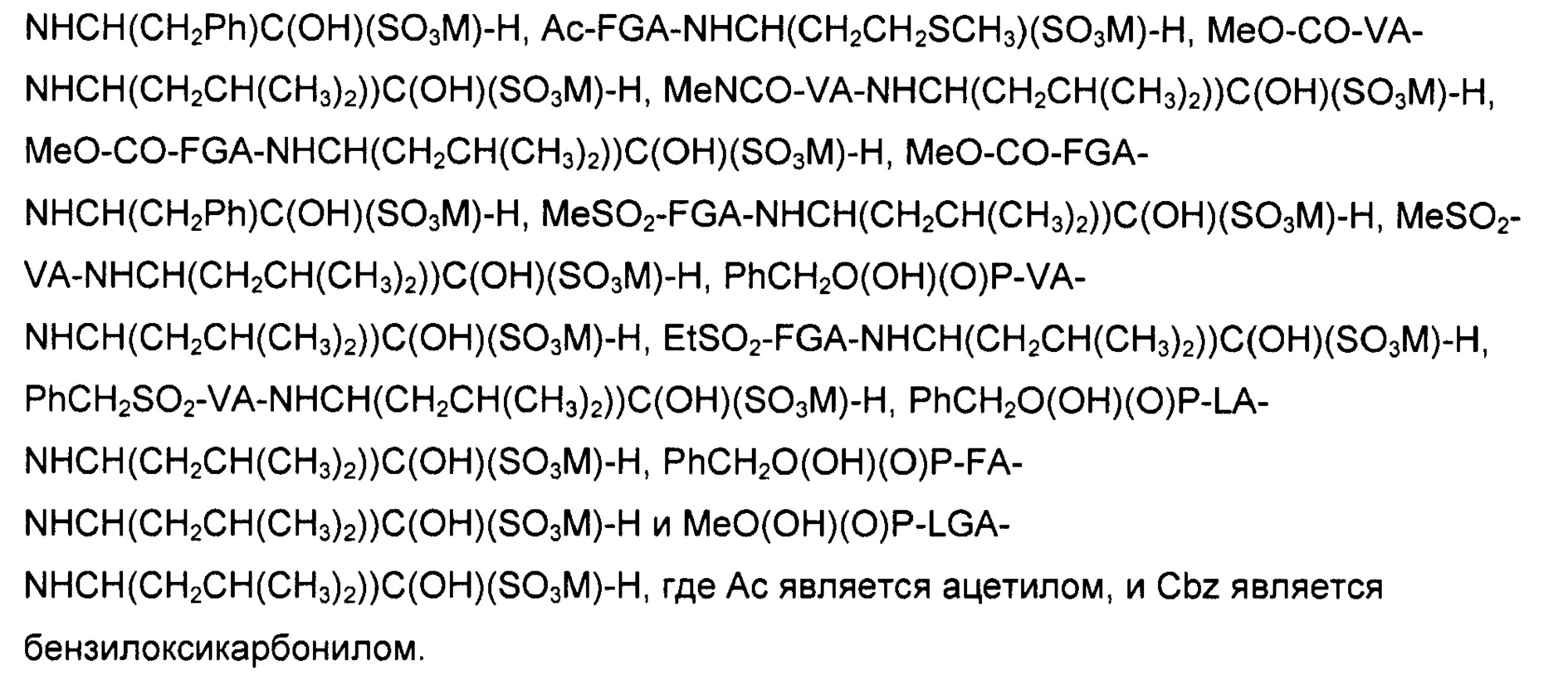
В еще одном аспекте настоящее изобретение обеспечивает соединение для использования в композиция по настоящему изобретению, причем соединение является гидросульфитным аддуктом пептида, содержащего альдегидную группу, с формулой X-B1-NH-CHR-CHOH-SO3M; где R и М определены как описано выше; В1 представляет собой один аминокислотный остаток, который отличен от пролина (Pro); X является В2, В3-В2, Z-B2, Z-В3-В2, где каждый из В3 и В2 является одним аминокислотным остатком, и Z является N-концевой защитной группой; и где В2 является Gly, Thr или Val.
В еще одном аспекте настоящее изобретение обеспечивает соединение для использования в композиция по настоящему изобретению, причем соединение является гидросульфитным аддуктом пептида, содержащего альдегидную группу, с формулой X-B1-NH-CHR-CHOH-SO3M; где R и М определены как описано выше; В1 представляет собой один аминокислотный остаток, который отличен от пролина (Pro); Х является В3-В2, Z-B3-B2, где каждый из В3 и В2 является одним аминокислотным остатком, и Z является N-концевой защитной группой; и где В3 является Phe, Tyr, Trp, фенилглицином, Leu, Val, Nva, Nle или Ile.
ПРИМЕРЫ
Химические вещества, применяемые в качестве буферов и субстратов, были коммерческими продуктами по меньшей мере со степенью чистоты выше технической.
ПРИМЕР 1
Получение гидросульфитного аддукта пептида, содержащего альдегидную группу
Пептид, содержащий альдегидную группу, с формулой Х-В1-В0-Н, как описано выше, превращают в соответствующий бисульфитный аддукт. К перемешиваемой суспензии 1 ммоль Х-В1-В0-Н в 8 мл этилацетата при комнатной температуре добавляют по каплям 1,06 ммоль бисульфита натрия (114 мг) в 6 мл воды и затем реакционную смесь перемешивают в течение 2 часов. Выделяют водную фазу и органический слой промывают 2×2 мл воды. Объединенные водные фазы, высушивают сублимацией с получением X-B1-NH-CHR-CHOH-SO3Na (предполагаемый выход 66%) в виде белого порошка.
ПРИМЕР 2
Получение жидкого состава гидросульфитного аддукта пептида, содержащего альдегидную группу.
4 ммоль твердого X-B1-NH-CHR-CHOH-SO3Na растворяют в 6 г деминерализованной воды и перемешивают в течение 30 мин при 35°С и впоследствии охлаждают с получением 25% водного раствора X-B1-NH-CHR-CHOH-SO3Na. Альтернативно, водную фазу вышеприведенного синтеза могут использовать для стабилизации фермента в следующем этапе и этот раствор имеет прибл. 3% (вес/вес).
ПРИМЕР 3
Получение состава со стабилизированным субтилизином, который содержит субтилизин и гидросульфитный аддукт пептида, содержащего альдегидную группу.
К коммерчески доступной Savinase 16L™ (Novozymes A/S, Багсвард, Дания) 0,9% X-B1-NH-CHR-CHOH-SO3Na добавляют с использованием 3,6% до около 25% водного раствора.
ПРИМЕР 4
Стабилизация субтилизина с помощью гидросульфитного аддукта
Общие детали эксперимента: Моющие средства с субтилизином (Savinase 16L) и липазой (Lipex 100L) с или без X-B1-NH-CHR-CHOH-SO3Na (гидросульфитный аддукт пептида, содержащего альдегидную группу, можно добавлять отдельно к моющему средству, содержащему субтилизин) помещают в закрытые стаканы при -18°С; 35°С и 40°С. Остаточные активности протеазы и липазы измеряют после различных отрезков времени с использованием стандартных аналитических способов (протеазы с помощью гидролиза N,N-диметилказеина при 40°С, рН 8,3 и липазы с помощью гидролиза pNp-валерата при 40°С, рН 7,7). Подобные испытания можно осуществить с помощью добавления субтилизина к моющему средству, которое уже содержит подходящие количества гидросульфитного аддукта пептида, содержащего альдегидную группу. Подобные результаты можно получить со всеми бисульфитными аддуктами пептида, содержащего альдегидную группу.
В качестве примера моющего состава с составом с стабилизированным субтилизином была получена композиция, описанная в таблице 1.
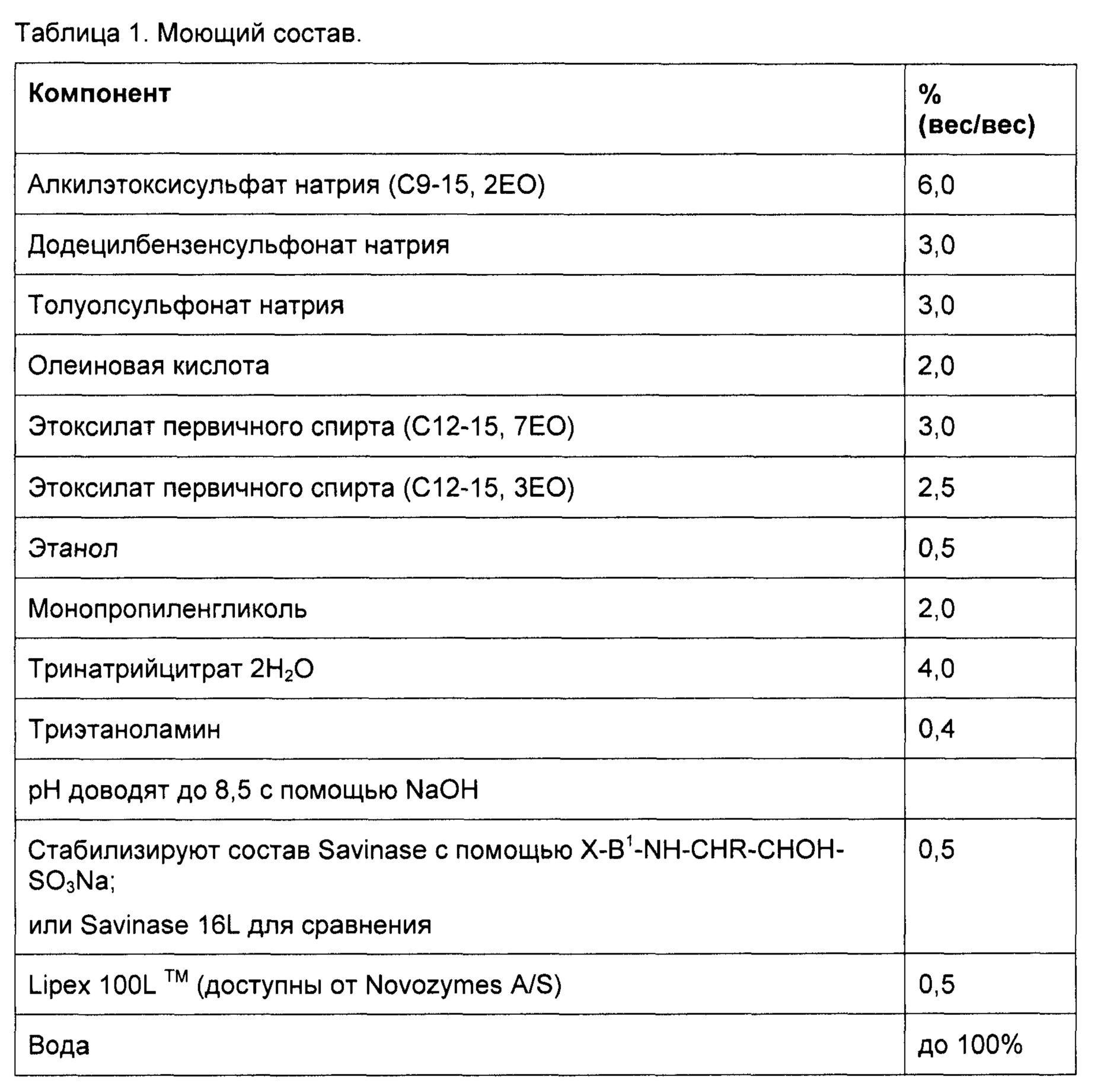
В таблице 2 показаны результаты, полученные с Х=Cbz-Gly; B1=Ala; R=-CH2-р(С6Н4)-ОН; стабильность измеряют после одной недели инкубации при 40°С в моющем средстве, описанном в таблице 1.

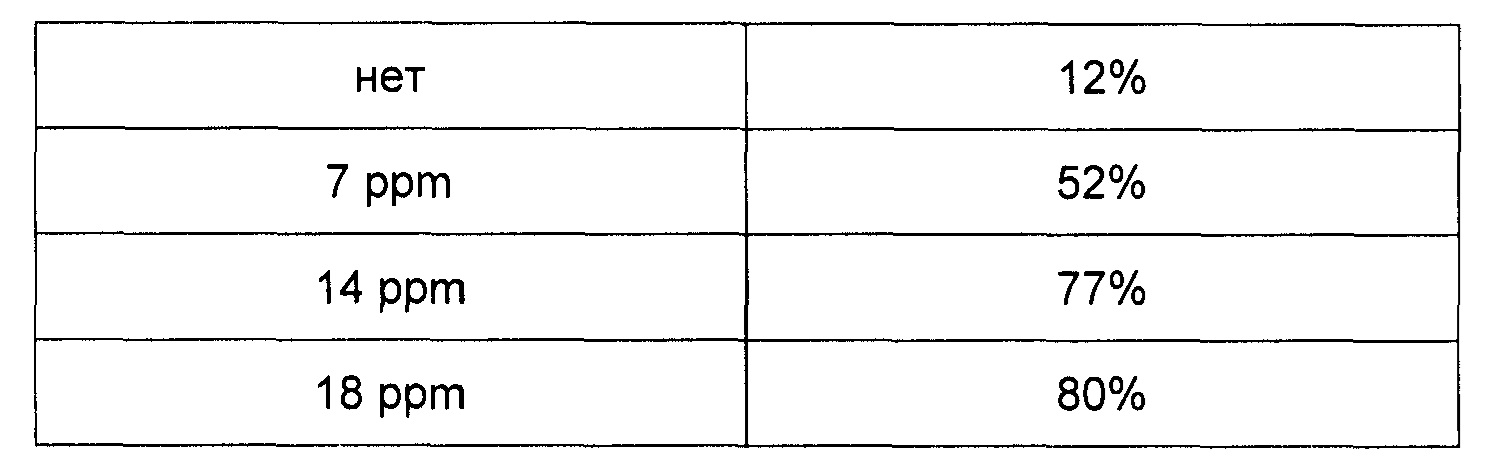
Результаты показывают стабилизацию субтилизина с помощью добавления гидросульфитного аддукта пептида, содержащего альдегидную группу.
ПРИМЕР 5
Стабилизация субтилизина и липазы
В качестве примера моющего состава с составом с стабилизированным субтилизином была получена композиция, описанная в таблице 3.
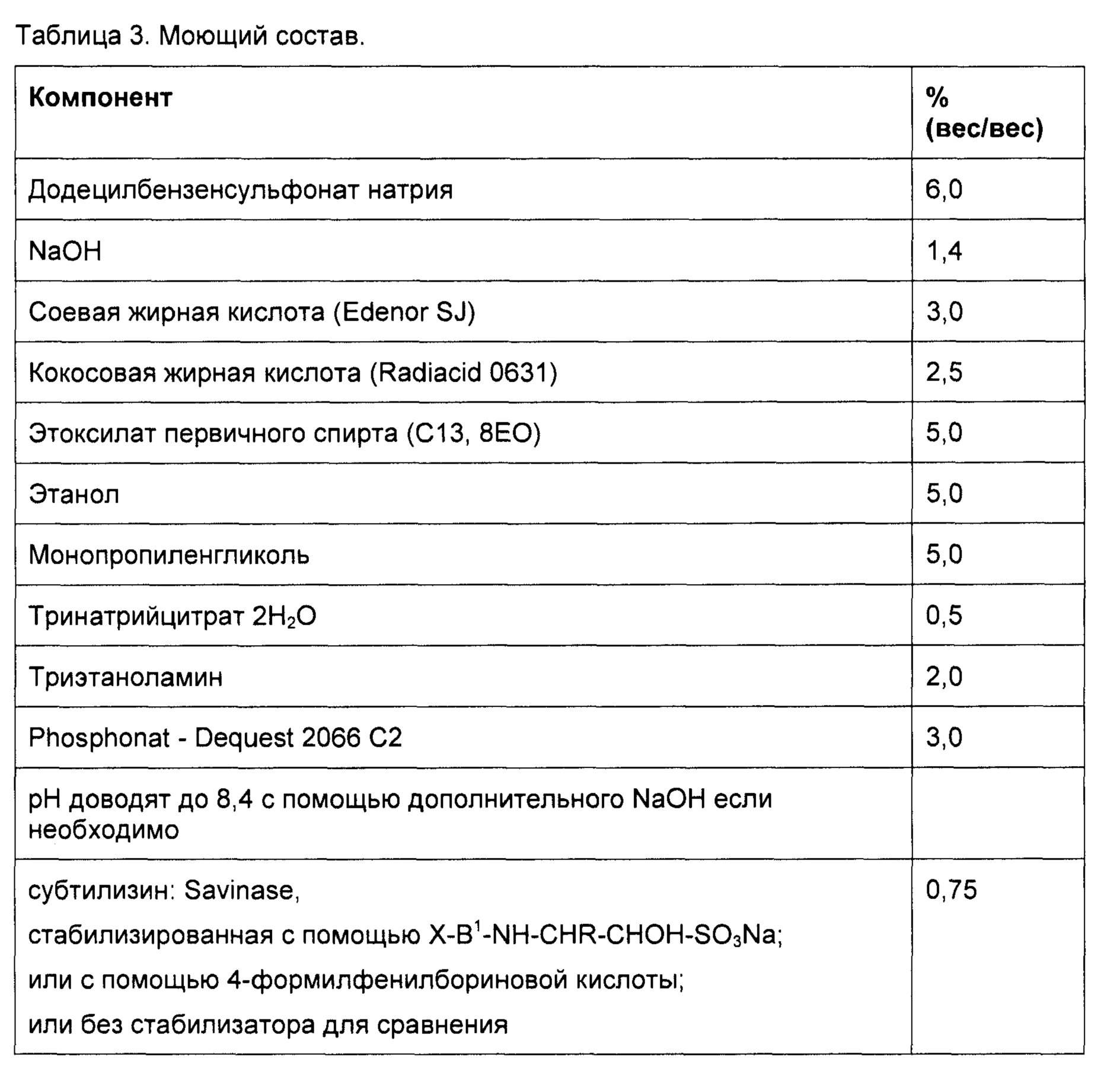

В таблице 4 показаны результаты, измеренные после двух недель инкубации при 35°С в моющем средстве, описанном в таблице 3.

Результаты показывают, что добавление гидросульфитного аддукта пептида, содержащего альдегидную группу, может стабилизировать субтилизин и второй фермент (липазу), и что это намного эффективней, чем стабилизатор из известного уровня техники.
ПРИМЕР 6
Стабилизация субтилизина и липазы
В качестве еще другого примера моющего средства с составом с стабилизированным субтилизином, была получена композиция, описанная в таблице 5.

В таблице 6 показаны результаты, измеренные после 4 недель инкубации при 37°С и после 8 недель инкубации при 30°С в моющем средстве, описанном в таблице 5.
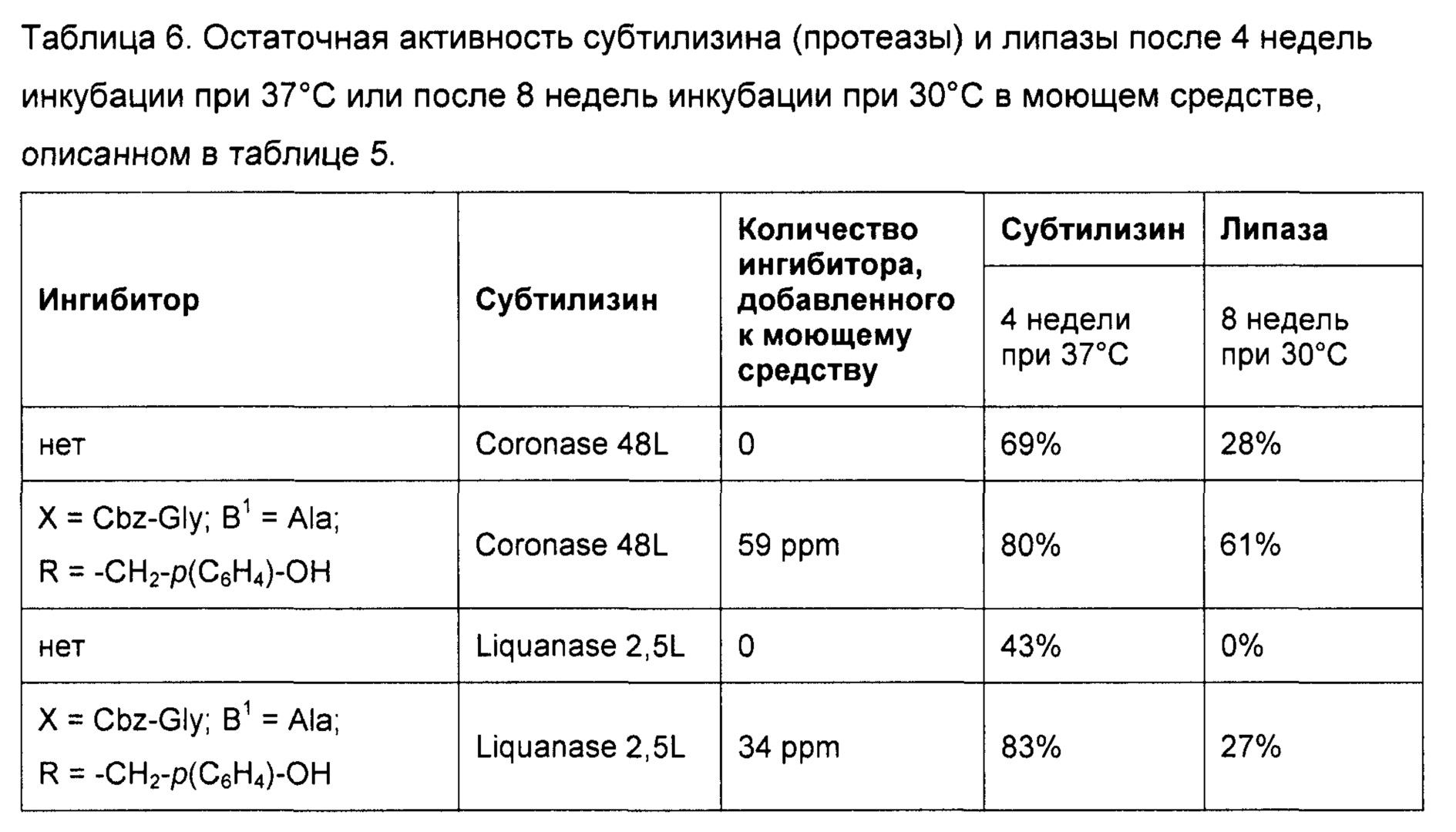
Результаты подтверждают, что добавление гидросульфитного аддукта пептида, содержащего альдегидную группу, может стабилизировать субтилизин и второй фермент (липазу) для различных субтилизинов.




