Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ 7,16,25-ТРИАРИЛ-7,8,16,17,25,26-ГЕКСАГИДРО-6Н,15Н,24Н-ТРИБЕНЗО[f,m,t][1,5,8,12,15,19]ГЕКСАОКСА[3,10,17]ТРИАЗАЦИКЛОХЕНИКОЗИНОВ
Вид РИД
Изобретение
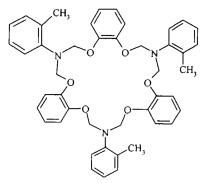
Предлагаемое изобретение относится к области органической химии, конкретно к способу получения 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6Н,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозинов общей формулы (1):
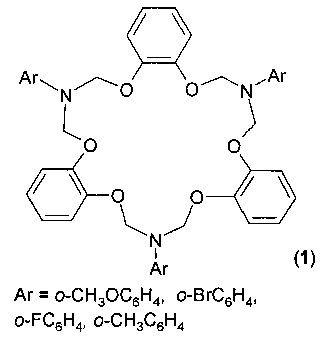
Циклические азот- и кислородсодержащие макроциклы перспективны в качестве селективных лигандов (Eds. Y. Inoue, G.W. Gokel. Cation Binding by Macrocycles. Marcel Dekker. New York. 1990. R.M. Izatt, K. Pawlak, J.S. Bradshaw, R.L. Bruening. Chem. Rev., 1991, 91, 1721 p), для экстракции и разделения катионов металлов (А.Т. Yordanov, D.M. Roundhill. Coord. Chem. Rev. 1998. 170, 93 p. K. Gloe, H. Graubaum, M. Wust, T. Rambusch, W. Seichter. Coord. Chem. Rev. 2001. 222. 103 p), для транспорта ионов через мембраны (Р. Bushlmann, Е. Pretsch, Е. Bakker. Chem. Rev. 1998, 98, 1593 р), в фоточувствительных системах (В. Valeur, I. Leray. Coord. Chem. Rev. 2000. 205. 3 p), выступают в роли межфазных катализаторов, моделирующих ферментативную активность (М.С. Feiters. In comprehensive Supramolecular Chemistry. Pergamon Press. Oxford. 1996, 9. 267 p).
Известен способ (K.L. Charbonniere, R.F. Ziessel. Cyclic di[(o-polyethyleneglycoxy)phenyl]amine: new members in the crown ether family. Tetrahedron Lett., 2000, 41, 2373-2376) получения дибензомоноазакраунэфира (2) взаимодействием бисфенола с производными олигоэтиленгликолей под действием оснований с выходом 22-68%
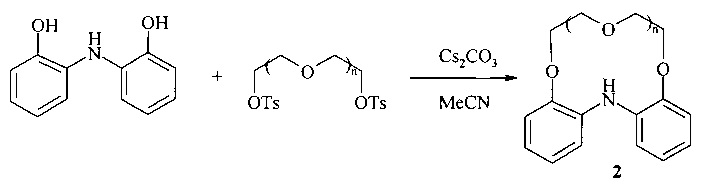
Известным способом не могут быть получены 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозины формулы (1).
Известен способ (M. Kamali, A. Shockravi, R. Mohtasham, S.P. Moghanlo. Synthesis of new aza- and thia-crown ethers and their metal ion templates synthesis as model case study. Arkivoc, 2014, 6, 242-251) получения 26-членного азакраун эфира (3) взаимодействием дитозилата гликоля с 2,6-бис(3-гидроксифенил)-4-фенилпиридином в присутствии K2CO3 при кипячении в ацетонитриле с выходом 70%
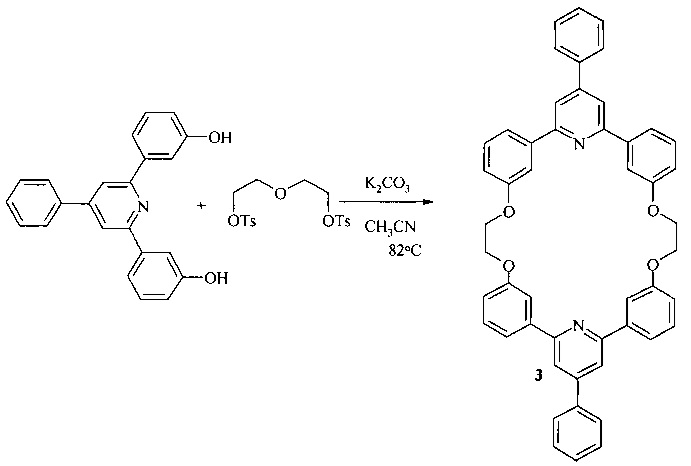
Известным способом не могут быть получены 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозины формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозинов формулы (1).
Предлагается новый способ получения 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозинов общей формулы (1).
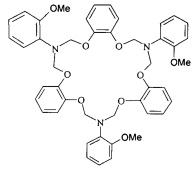
Сущность способа заключается во взаимодействии N,N-бис(метоксиметил)-N-арил(о-метоксифенил, о-метилфенил, о-бромфенил, о-фторфенил)амина с пирокатехином в присутствии катализатора азотнокислого самария, взятыми в мольном соотношении N,N-бис(метоксиметил)-N-ариламин : пирокатехин: Sm(NO3)3*6H2O = 1:1:(0.03-0.07), предпочтительно 1:1:0.05, при комнатной (~20°С) температуре и атмосферном давлении в этиловом эфире уксусной кислоты в качестве растворителя в течение 6-8 ч, предпочтительно 7 ч. Выход соответствующих 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6H,15Н,24Н-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозинов общей формулы (1) составляет 70-88%. Реакция протекает по схеме
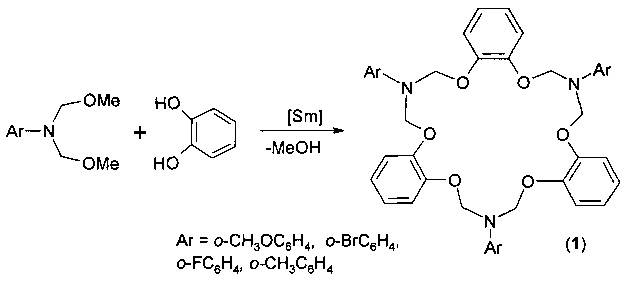
7,16,25-Триарил-7,8,16,17,25,26-гексагидро-6H,15Н,24Н-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозины общей формулы (1) образуются только лишь с участием N,N-бис(метоксиметил)-N-ариламинов и пирокатехина, взятых в стехиометрических количествах. При другом соотношении исходных реагентов снижается выход целевых продуктов (1). Без катализатора реакция не идет.
Проведение указанной реакции в присутствии катализатора Sm(NO3)3*6H2O больше 7 мол. % в расчете на исходный N,N-бис(метоксиметил)-N-ариламин не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Sm(NO3)3*6H2O менее 3 мол. % снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°С. При температуре выше 20°С (например, 60°С) увеличиваются энергозатраты, а при температуре ниже 20°С (например, 0°С) снижается скорость реакции. Опыты проводили в этиловом эфире уксусной кислоты, т.к. в нем хорошо растворяются исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа
В предлагаемом способе в реакцию с N,N-бис(метоксиметил)-N-ариламинами вовлекается пирокатехин в присутствии каталитических количеств Sm(NO3)3*6H2O. Реакция идет с селективным образованием 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозинов формулы (1).
В известном способе макроцикл формулы (3) получают конденсацией дитозилата гликоля с 2,6-бис(3-гидроксифенил)-4-фенилпиридином в присутствии стехиометрических количеств K2CO3.
Предлагаемый способ обладает следующими преимуществами. Способ позволяет получать с высокой селективностью и выходами 7,16,25-триарил-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозины формулы (1).
Способ поясняется следующими примерами.
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, помещают 0.19 г (1 ммоль) N,N-бис(метоксиметил)-N-(о-метилфенил)амина и 0.10 г (1 ммоль) пирокатехина, 5 мл этилового эфира уксусной кислоты, 0.02 г [5 мол. % в расчете на N,N-бис(метоксиметил)-N-(о-метилфениламин)] Sm(NO3)3*6H2O, перемешивают при комнатной (~20°С) температуре 7 ч, выделяют 7,16,25-три(о-метилфенил)-7,8,16,17,25,26-гексагидро-6Н,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозин (1) с выходом 72%.
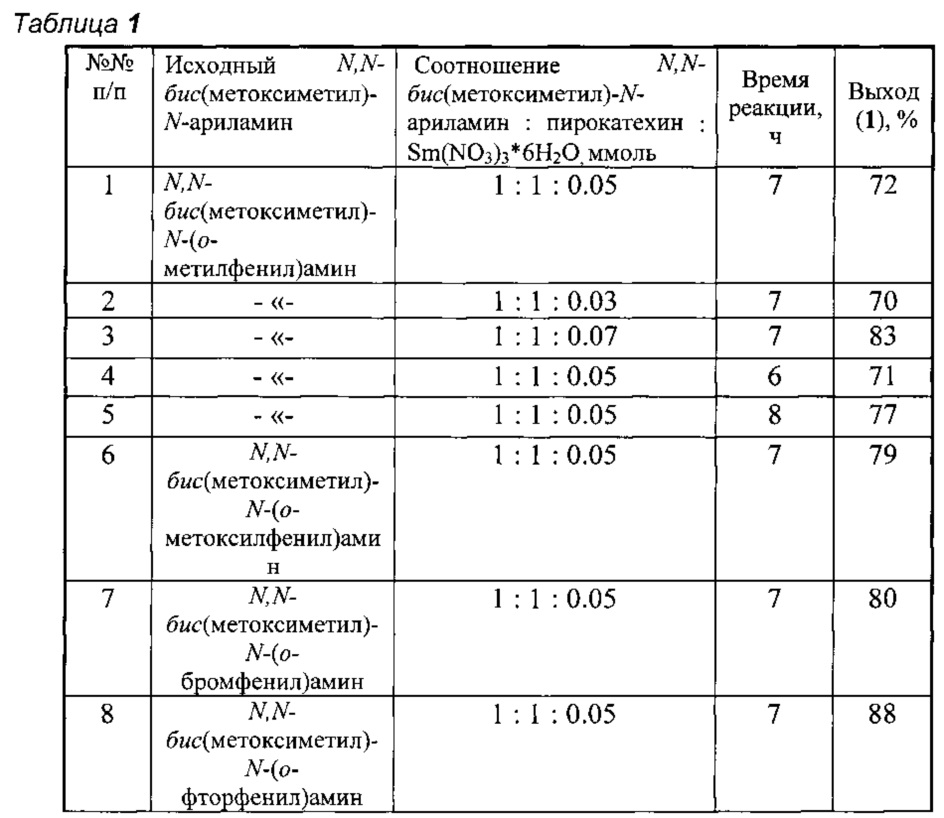
Другие примеры, подтверждающие способ, приведены в табл. 1.
Спектральные характеристики 7,16,25-три(о-метилфенил)-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозина:
|
Спектральные характеристики 7,16,25-три(о-метоксифенил)-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозина:
|
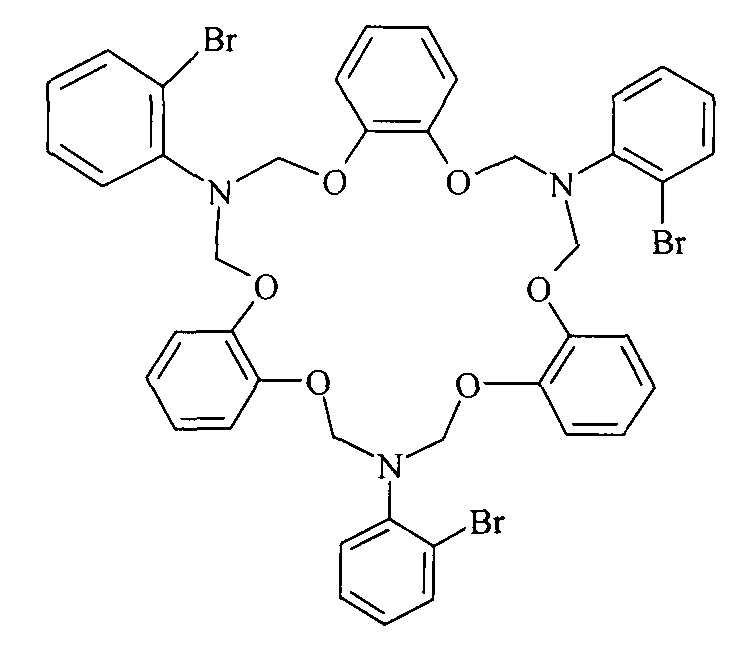
Спектральные характеристики 7,16,25-три(о-бромфенил)-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозина:
|
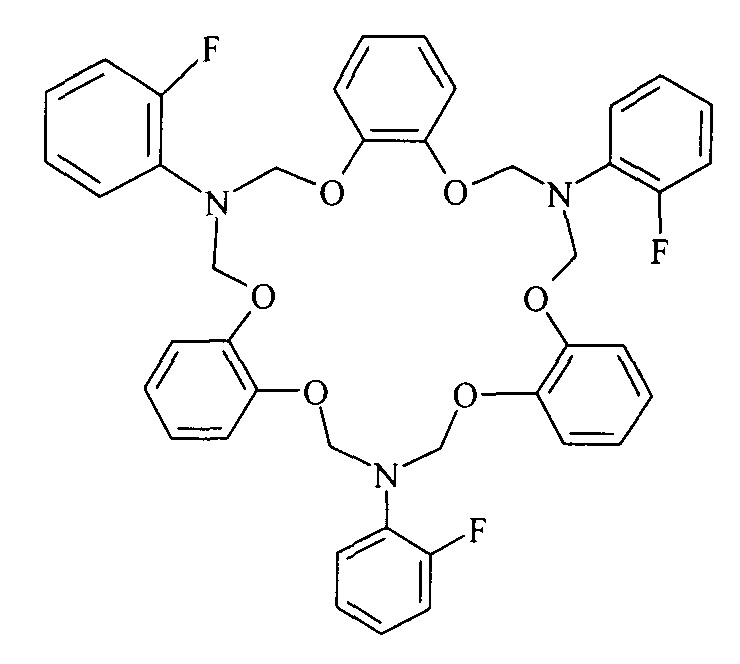
Спектральные характеристики 7,16,25-три(о-фторфенил)-7,8,16,17,25,26-гексагидро-6H,15H,24H-трибензо[ƒ,m,t][1,5,8,12,15,19]гексаокса[3,10,17]триазациклохеникозина:
|
![СПОСОБ ПОЛУЧЕНИЯ 7,16,25-ТРИАРИЛ-7,8,16,17,25,26-ГЕКСАГИДРО-6Н,15Н,24Н-ТРИБЕНЗО[f,m,t][1,5,8,12,15,19]ГЕКСАОКСА[3,10,17]ТРИАЗАЦИКЛОХЕНИКОЗИНОВ](https://fips.edrid.ru/images/rid/b5/eb/fb/af14bb5875fa7b3214edb92ac6d7fd89.jpg)
![СПОСОБ ПОЛУЧЕНИЯ 7,16,25-ТРИАРИЛ-7,8,16,17,25,26-ГЕКСАГИДРО-6Н,15Н,24Н-ТРИБЕНЗО[f,m,t][1,5,8,12,15,19]ГЕКСАОКСА[3,10,17]ТРИАЗАЦИКЛОХЕНИКОЗИНОВ](https://fips.edrid.ru/images/rid/b5/eb/fb/c69d66b2f5c8a8faf87051cfc1f51f5a.jpg)