Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ 1,7-ДИТИА-3,5-ДИАЗАЦИКЛОАЛКАН-4-ОНОВ
Вид РИД
Изобретение
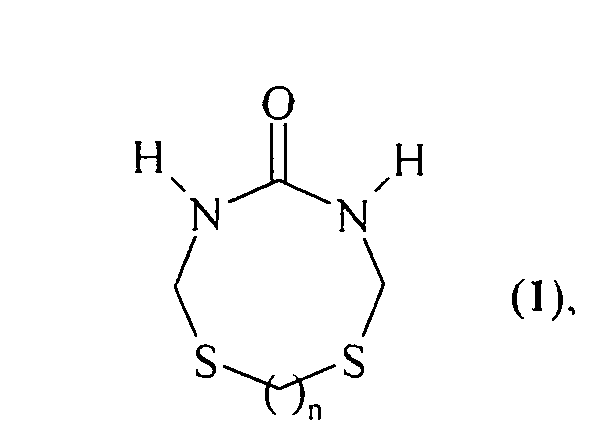
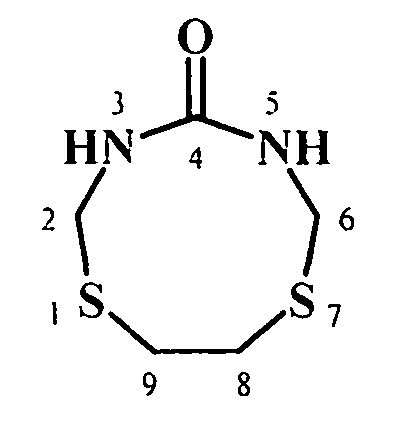
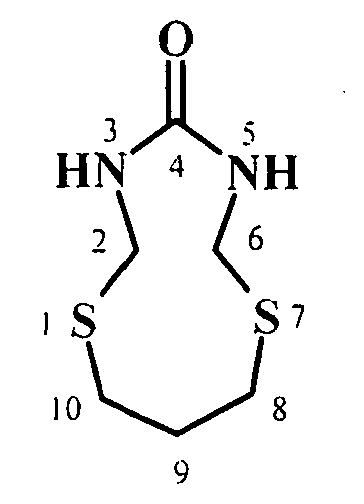
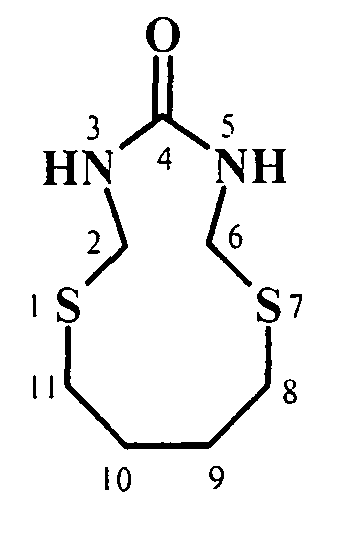
Изобретение относится к области органической химии, конкретно к способу получения 1,7-дитиа-3,5-диазациклоалкан-4-онов общей формулы (1)
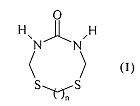
где n=2-4.
Азот и серусодержащие гетероциклы перспективны в качестве селективных сорбентов, экстрагентов благородных и драгоценных металлов [Муринов Ю.И., Майстренко В.Н., Афзалетдинова Н.Г. Экстракция металлов S,N-органическими соединениями. М.: Наука, 1993, с.192].
Известен способ [Arya V.P., Shenoy Mrs. J. Synthesis of new heterocycles: Part XV. Synthesis of novel cyclic and acyclic sulfamides. Indian J. Chem., 1976, 14B (10), p. 766] получения 1,2,9-тиадиазонин-1,1-диоксида (2) взаимодействием сульфамида с 1,6-пентандиамином с выходом 55%.
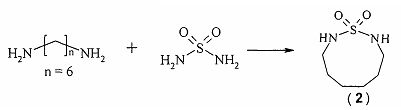
Известным способом не могут быть получены 1,7-дитиа-3,5-диазациклоалкан-4-оны общей формулы (1).
Известен способ [Regainia Z. et al. General synthesis of n-membered cyclic sulfamides. Tetrahedron, 2003, 59(32), p. 6051] получения 1,2,9-тиадиазонана (3) внутримолекулярной циклизацией галогенсодержащего сульфамида с выходом 60%.
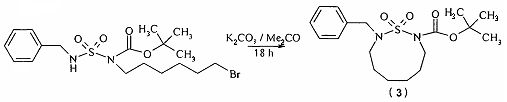
Известный способ не позволяет получать 1,7-дитиа-3,5-диазациклоалкан-4-оны общей формулы (1).
Известен способ [V.R. Akhmetova, R.R. Khairullina, I.S. Bushmarinov, T.V. Tyumkina, V.M. Janibin. Multicomponent reactions of urea and its derivatives with СН2О and H2S in the synthesis of 1,3,5-thiadiazinane-4-(thi)ones and macroheterocycles. ARKIVOC, 2011, 8, p. 149] получения 1,3,5-тиадиазинан-4-(ти)онов (4) конденсацией (тио)карбамида с СН2О и H2S в присутствии четырехмольного избытка н-BuONa с выходами ~60%.
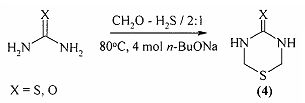
Известным способом не могут быть получены 1,7-дитиа-3,5-диазациклоалкан-4-оны общей формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении 1,7-дитиа-3,5-диазациклоалкан-4-онов общей формулы (1).
Предлагается новый способ селективного получения 1,7-дитиа-3,5-диазациклоалкан-4-онов общей формулы (1).
Сущность способа заключается во взаимодействии N,N′-бис(метоксиметил)мочевины с α,ω-алкандитиолом общей формулы HS(СН2)nSH (где n=2-4) в присутствии в качестве катализатора Cs2CO3, нанесенного на силикагель, взятыми в мольном соотношении N,N′-бис(метоксиметил)мочевина:HS(CH2)nSH=10:10, при содержании катализатора Cs2CO3/SiO2 в реакционной массе 30-50 мас.%, предпочтительно 40 мас.%, в расчете на N,N′-бис(метоксиметил)мочевину в этиловом спирте в качестве растворителя при температуре 50-70°С, предпочтительно 60°С, и атмосферном давлении в течение 5-7 ч. Выход 1,7-дитиа-3,5-диазациклоалкан-4-онов (1) составляет 44-70%. Реакция протекает по схеме
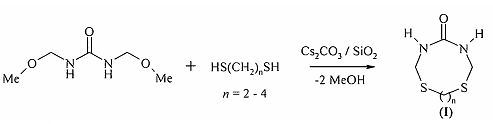
1,7-Дитиа-3,5-диазациклоалкан-4-оны (1) образуются только лишь с участием N,N′-бис(метоксиметил)мочевины и α,ω-алкандитиолов, взятых в стехиометрическом соотношении. При другом соотношении исходных реагентов снижается выход целевого продукта (1).
Проведение указанной реакции в присутствии катализатора Cs2CO3/SiO2 больше 50 мас.% не приводит к существенному увеличению выхода целевого продукта (1). Применение менее 30 мас.% Cs2CO3/SiO2 снижает выход целевого продукта (1). В отсутствие Cs2CO3/SiO2 реакция не проходит.
Реакции проводили при температуре 50-70°C. При меньшей температуре (например, 25°С) снижается скорость реакции.
Существенные отличия предлагаемого способа.
В известном способе в качестве исходных реагентов применяются (тио)карбамид, СН2О и H2S. Известным способом не могут быть получены 1,7-дитиа-3,5-диазациклоалкан-4-оны (1).
В предлагаемом способе используются в качестве исходных реагентов N,N′-бис(метоксиметил)мочевина и α,ω-алкандитиолы, в качестве катализатора Cs2CO3/SiO2, который может быть использован многократно без регенерации. Предлагаемый способ позволяет получать 1,7-дитиа-3,5-диазациклоалкан-4-оны общей формулы (1).
Катализатор Cs2CO3/SiO2 готовят в соответствии с известными общими принципами приготовления нанесенных катализаторов [И.А. Пахомов. Научные основы приготовления катализаторов: введение в теорию и практику. Новосибирск: Издательство СО РАН, 2011, с. 262] путем пропитки носителя SiO2 спиртовым раствором карбоната цезия с последующей стадией термообработки при 110°С в течение 5 ч. Катализатор содержит 6.3 мас.% Cs2CO3 и 93.7 мас.% SiO2.
Способ поясняется примерами.
Пример 1. В стеклянный реактор, установленный на магнитной мешалке, помещают 0.148 г (10 ммоль) N,N′-бис(метоксиметил)мочевины и 0.056 г (40 мас.% по отношению к N,N′-бис(метоксиметил)мочевине) Cs2CO3/SiO2 в 5 мл EtOH, перемешивают 10 мин при комнатной температуре (~20°С). Затем в реактор добавляют 0.094 г (10 ммоль) 1,2-этандитиола и перемешивают реакционную смесь 6 ч при температуре 60°С. Из реакционной массы выделяют 1,7-дитиа-3,5-диазонан-4-он с выходом 65%. Другие примеры, подтверждающие способ, приведены в табл.1.
|
Все опыты проводили с участием 10 ммоль N,N′-бис(метоксиметил)мочевины и 10 ммоль α,ω-алкандитиола в EtOH в качестве растворителя.
|