Результат интеллектуальной деятельности: ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ ЭШЕРИХИОЗА, СТРЕПТОКОККОЗА И СТАФИЛОКОККОЗА КРУПНОГО РОГАТОГО СКОТА
Вид РИД
Изобретение
Изобретение относится к ветеринарной медицине, в частности к вакцинам, и может быть использовано в учреждениях, занимающихся конструированием биологических препаратов, а также на предприятиях биологической промышленности.
Известна ассоциированная вакцина против диареи телят (патент на изобретение РФ №2035916 от 17.06.93, МКИ А61 39/125, 39/135), содержащая инактивированные этанолом клетки штаммов Proteus vulgaris ГИСК N198, Proteus mirabilis ГИСК N199, Klebsiella pneumoniae ГИСК N201, Klebsiella pneumoniae ГИСК N202, из антигенов эшерихий и сальмонелл, инактивированные этанолом клетки штаммов Escherichia coli 09 К99, Escherichia coli 0138 К88, Escherichia coli ГИСК N200, Salmonella typhimurium ГИСК N195, Salmonella Dublin ГИСК N196, Salmonella enteritidis ГИСК N197, фенол и изотонический раствор хлорида натрия, а в качестве адъюванта - гидроокись алюминия. Данная вакцина предназначена для профилактики инфекционных заболеваний у телят, вызываемых эшерихиями, сальмонеллами, протеями и клебсиеллами.
Известна инактивированная эмульсин-вакцина против сальмонеллеза телят (патент РФ на изобретение №2154495 от 15.10.97, МКИ А61К 39/112, C12N 1/20, А61К 39/39). Данная вакцина содержит в качестве антигенов смесь инактивированных формалином вирулентных штаммов рода Salmonella (S. dublin №1449, S. typhimurium №159) в качестве иммуномодулятора - взвесь клеток Rodococcus equi №2 в маслоланолиновой смеси, при этом компоненты, входящие в состав вакцины, берут в следующем соотношении из расчета на литр: антигены на физиологическом растворе с добавлением 0,4-0,5% формалина и концентрацией микробных клеток в 1 мл - 90 млрд (S. dublin №1449) 285-315 мл, антиген S. typhimurium №159 95-105 мл, взвесь клеток Rodococcus equi №2 на физиологическом растворе, содержащая 200 млрд микробных клеток; адъювант - маслоланолиновая смесь в соотношении 83-87:17-13 остальное. Принимаем указанную вакцину за прототип.
Технология изготовления указанной вакцины сложная. Данная вакцина применяется для профилактики сальмонеллеза телят. Использование масло-ланолиновой смеси в вакцине может вызывать у привитых животных различные поствакцинальные осложнения (воспалительные процессы, абсцессы на месте введения, хромоту и др.).
Техническим результатом изобретения является повышение специфичности, безвредности, эффективности вакцины для профилактики эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота путем введения новых чистых культур возбудителей, компонентов, исключив отрицательное и побочное влияние.
Технический результат достигается тем, что в вакцине ассоциированной против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота, содержащей суспензию инактивированных формалином антигенов, адъювант, согласно изобретению в качестве антигенов содержится суспензия клеток чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus в равных соотношениях, полученных путем отбора патологического материала от больного и павшего крупного рогатого скота из местного эпизоотического очага, а также формалин и гидроокись алюминия при следующем соотношении компонентов, мас. %:
|
Новизна заявляемого технического решения обусловлена тем, что в отличие от известных вакцин для получения сырья проводят отбор патологического материала от больного и павшего крупного рогатого скота из местного эпизоотического очага, приготовление суспензии, посев на дифференциально-диагностические среды, выделение чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus, выращивание чистых культур возбудителей проводят раздельно на мясо-пептонном бульоне, что позволяет повысить специфичность и иммуногенность вакцины.
Раздельное культивирование чистых культур возбудителей и добавление в питательную среду глюкозы до 0,2%-ной концентрации позволяет получать концентрацию микробных клеток не менее 4 млрд в 1 см в течение 14-24 часов инкубирования. Инактивирование культур возбудителей формалином в 0,4-0,5%-ной конечной концентрации при температуре 37°С в течение 72-96 часов позволяет подавить патогенность возбудителей и сохранить их иммуногенные свойства в течение 12 месяцев. Смешивание инактивированных антигенов эшерихий, стрептококков и стафилококков в равных соотношениях, внесение гидроокиси алюминия и тщательное перемешивание позволяет получить вакцину, которая не вызывает у привитых животных поствакцинальных осложнений, позволяет обеспечить формирование напряженного иммунитета у привитых животных (через 12-15 суток после внутримышечно или подкожно двукратного введения с интервалом 7-14 дней в дозе коровам по 5,0 см3, телятам в возрасте 1,0-1,5 месяца - в дозе 1,5-2,0 см3). Использование клеток чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus, выделенных из местного эпизоотического очага от больных и павших животных, позволяет значительно повысить специфичность вакцины, обеспечивает защиту животных сразу от трех опасных инфекционных болезней: эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота продолжительностью не менее 9 месяцев (срок наблюдения).
По данным патентной и научно-технической литературы не обнаружена аналогичная совокупность признаков, компонентов, что позволяет судить об изобретательском уровне заявленного технического решения.
Что касается критерия «промышленная применимость», то компоненты, входящие в состав вакцины, известны и широко применяются в ветеринарной практике при изготовлении инактивированных вакцин: ассоциированная вакцина против сальмонеллеза, пастереллеза и энтерококковой инфекции поросят ТУ 10.09-62-90, утверждено 01.08.90 г., инструкция по изготовлению и контролю данной вакцины утверждена Главным управлением ветеринарии 16.07.90 г.; вакцина против энтерококковой инфекции телят, ягнят и поросят ТУ 10.09-91-90, утверждено 15.12.90 г.
Методы выделения чистой культуры возбудителя колибактериоза и характеристика описаны в «Методических указаниях по бактериологической диагностике колибактериоза (эшерихиоза) животных», утвержденных 27.07.2000 г., №13-7-2/2117, Департаментом ветеринарии МСХ РФ, описана характеристика эшерихий в справочнике «Определитель зоопатогенных микроорганизмов» под редакцией профессора Сидорова М.А., М.: Колос, 1995, стр. 196-201, а также в «Практикуме по ветеринарной микробиологии и иммунологии» авторы: Костенко Т.С., Родионова В.Б., Скородумов Д.И., М.: «Колос», 2001, на стр. 219-222.
Методы выделения и характеристика стрептококков и стафилококков описаны в справочнике «Определитель зоопатогенных микроорганизмов» под редакцией профессора Сидорова М.А., М.: Колос, 1995, стр. 90-95; в «Практикуме по ветеринарной микробиологии и иммунологии» авторы: Костенко Т.С., Родионова В.Б., Скородумов Д.И., М.: «Колос», 2001, на стр. 165 - 171; в справочнике «Микробиологическая диагностика бактериальных болезней животных» авторы: Скородумов Д.И., Субботин В.В., Сидоров М.А., Костенко Т.С., М.: «ИзограФъ», 2005, на стр. 246-257; в «Методических указаниях по лабораторной диагностике стрептококкоза животных», утвержденных 25.09.1990 г. Главным управлением ветеринарии с государственной инспекцией при Государственной комиссии СМ СССР по продовольствию и закупкам.
Предложенная вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота проста в исполнении, доступна и является промышленно применимой.
Вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скотасодержит инактивированные формалином чистые культуры возбудителей Е. coli, Str. pneumoniae и Staph, aureus, адсорбированные на гидрате окиси алюминия. По внешнему виду вакцина представляет собой жидкость светло-желтого цвета с рыхлым осадком, который при встряхивании легко разбивается в гомогенную взвесь. Срок хранения в сухом, темном месте при температуре от 2 до 10°С 1 год. Вакцина предназначена для профилактики опасных инфекционных заболеваний крупного рогатого скота против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота. Она вызывает образование специфического иммунитета против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота. Вакцина безвредна и ареактогенна. Вакцину применяют в неблагополучных и угрожаемых по эшерихиозу, стрептококкозу и стафилококкозу крупного рогатого скота хозяйствах. Продукты убоя вакцинированных животных используют без ограничений, независимо от сроков вакцинации.
К факторам, обуславливающим получение вакцины заданного свойства, относятся последовательность изготовления и процентное соотношение между компонентами, входящими в препарат.
Приведено пять примеров, содержащих компоненты в различных соотношениях на 100 мл вакцины.
Пример 1
Берут патологический материал от больного и павшего крупного рогатого скота из местного эпизоотического очага, из которых приготавливают суспензию, далее делают посев на дифференциально-диагностические среды, после чего выделяют клетки чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus и отдельно выращивают в мясо-пептонном бульоне с добавлением глюкозы с титром 4-5 млрд в 1 см3, после чего раздельно инактивируют клетки возбудителей болезней внесением формалина до 0,4%-ной конечной концентрации при температуре 37°С в течение 72 часов и периодическом перемешивании, потом смешивают клетки чистых культур в равных соотношениях, затем в смесь инактивированных культур вносят адъювант - гидроокись алюминия, тщательно смешивают и получают вакцину при следующем соотношении компонентов, мас. %:
|
При данном соотношении компонентов вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота обладает слабой иммуногенной активностью.
Пример 2
Берут патологический материал от больного и павшего крупного рогатого скота из местного эпизоотического очага, из которого приготавливают суспензию, и далее делают посев на дифференциально-диагностические среды, после чего выделяют клетки чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus и отдельно выращивают в мясо-пептонном бульоне с добавлением глюкозы с титром 4-5 млрд микробных клеток в 1 см3, после этого раздельно инактивируют клетки чистых культур возбудителей болезней внесением формалина до 0,4%-ной конечной концентрации при температуре 37°С в течение 72 часов и периодическом перемешивании, потом смешивают клетки чистых культур в равных соотношениях, затем в смесь инактивированных культур вносят адъювант - гидроокись алюминия, тщательно смешивают и получают вакцину при следующем соотношении компонентов, мас. %:
|
При данном соотношении компонентов вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота обладает достаточной иммуногенной активностью.
Пример 3
Берут патологический материал от больного и павшего крупного рогатого скота из местного эпизоотического очага, из которого приготавливают суспензию, и далее делают посев на дифференциально-диагностические среды, после чего выделяют клетки чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus и отдельно выращивают в мясо-пептонном бульоне с добавлением глюкозы с титром 4-5 млрд микробных клеток в 1 см3, после этого раздельно инактивируют клетки чистых культур возбудителей болезней внесением формалина до 0,4%-ной конечной концентрации при температуре 37°С в течение 72 часов и периодическом перемешивании, потом смешивают клетки чистых культур в равных соотношениях, затем в смесь инактивированных культур вносят адъювант - гидроокись алюминия, тщательно смешивают и получают при следующем соотношении компонентов, мас. %:
|
При данном соотношении компонентов вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота обладает незначительной иммуногенной эффективностью.
Пример 4
Берут патологический материал от больного и павшего крупного рогатого скота из местного эпизоотического очага, из которого приготавливают суспензию, и далее делают посев на дифференциально-диагностические среды, после чего выделяют клетки чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus, и отдельно выращивают в мясо-пептонном бульоне с добавлением глюкозы с титром 4-5 млрд микробных клеток в 1 см3, после этого раздельно инактивируют клетки чистых культур возбудителей болезней внесением формалина до 0,4%-ной конечной концентрации при температуре 37°С в течение 72 часов и периодическом перемешивании, потом смешивают клетки чистых культур в равных соотношениях, затем в смесь инактивированных культур вносят адъювант - гидроокись алюминия, тщательно смешивают и получают при следующем соотношении компонентов, мас. %:
|
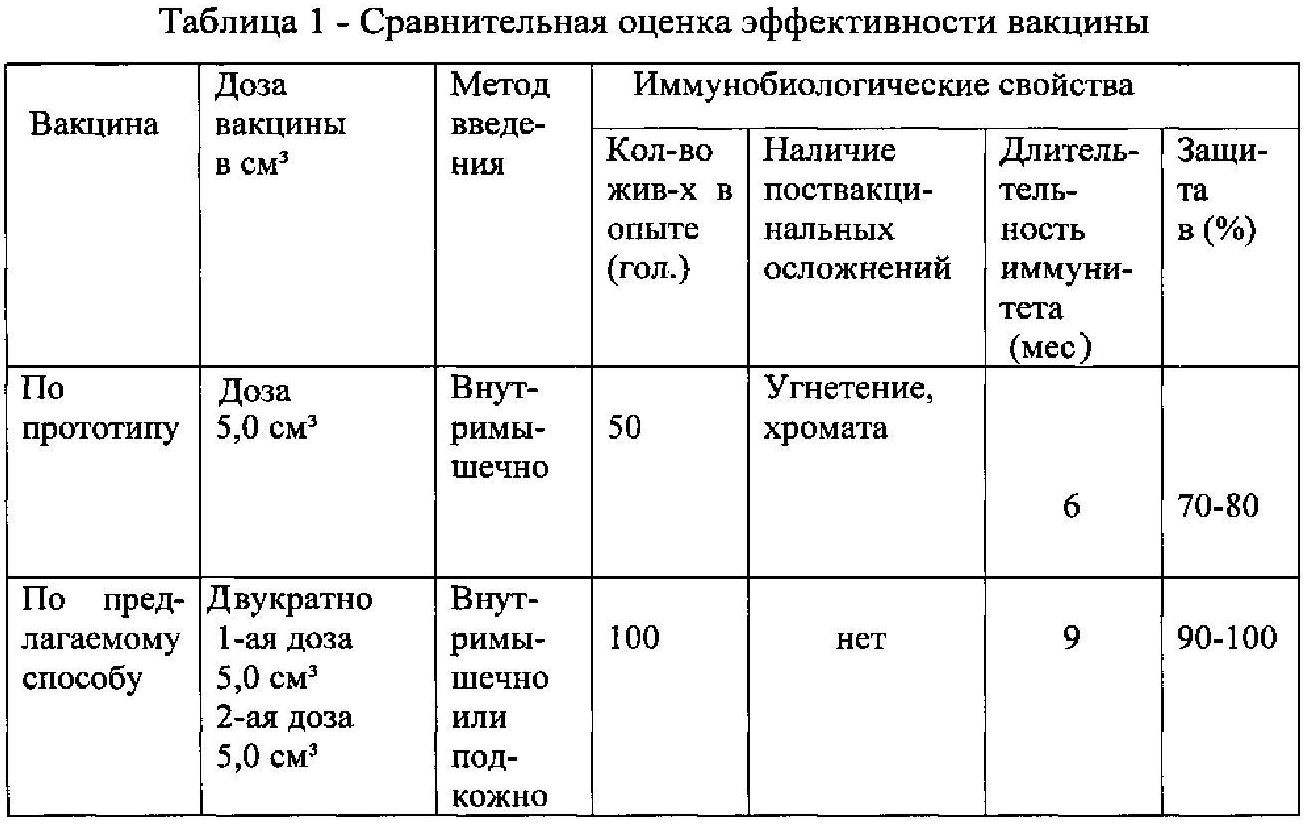
При данном соотношении компонентов вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота обладает высокой иммуногенной активностью, формирует после вакцинации выраженный напряженный иммунитет, не вызывает поствакцинальных осложнений, стабильна при хранении в течение 12 месяцев (таблица 1).
Пример 5
Берут патологический материал от больного и павшего крупного рогатого скота из местного эпизоотического очага, из которого приготавливают суспензию, и далее делают посев на дифференциально-диагностические среды, после чего выделяют клетки чистых культур возбудителей эшерихиоза Escherichia coli, стрептококкоза Streptococcus pneumoniae и стафилококкоза Staphylococcus aureus и отдельно выращивают в мясо-пептонном бульоне с добавлением глюкозы с титром 4-5 млрд микробных клеток в 1 см3, после этого раздельно инактивируют клетки чистых культур возбудителей болезней внесением формалина до 0,4%-ной конечной концентрации при температуре 37°С в течение 72 часов и периодическом перемешивании, потом смешивают клетки чистых культур в равных соотношениях, затем в смесь инактивированных культур вносят адъювант - гидроокись алюминия, тщательно смешивают и получают при следующем соотношении компонентов, мас. %:
|
При данном соотношении компонентов вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота обладает иммуногенной активностью, у отдельных животных на месте введение препарата вызывает слабое раздражение.
Из данных таблицы 1 видно, что предлагаемая вакцина ассоциированная против эшерихиоза, стрептококкоза и стафилококкоза крупного рогатого скота имеет значительные преимущества в сравнении с вакциной по прототипу.