Результат интеллектуальной деятельности: ЗАМЕЩЕННЫЕ ФЕНОКСИУКСУСНЫЕ КИСЛОТЫ, ИХ ЭФИРЫ И АМИДЫ, ВКЛЮЧАЮЩИЕ 2,6-ДИОКСО-2,3,6,7-ТЕТРАГИДРО-1Н-ПУРИН-8-ИЛОВЫЙ ФРАГМЕНТ, - АНТАГОНИСТЫ АДЕНОЗИНОВОГО A РЕЦЕПТОРА И ИХ ПРИМЕНЕНИЕ
Вид РИД
Изобретение
Данное изобретение относится к новым соединениям - замещенным феноксиуксусным кислотам и их эфирам и аминам, включающим 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, проявляющим антагонистическую активность по отношению к аденозиновым A2A рецепторам, и к их применению в качестве лекарственного начала и средства (адъюванта) для фармацевтических композиций, лекарственных средств, и к способам лечения заболеваний центральной нервной системы, онкологических, вирусных и бактериальных заболеваний.
А2А рецепторы являются одним из 4-х подтипов (A1, A2A, A2B и А3) аденозиновых рецепторов. A1 рецептор ингибирует аденилатциклазу, а также активирует или ингибирует (в зависимости от типа клеток) фосфоинозитидный обмен. Кроме того, при участии G-белков этот рецептор активирует К-каналы и ингибирует Са-каналы. A2 рецептор стимулирует аденилатциклазу. Оба типа рецептора имеют семь трансмембранных доменов и гомологичны другим мембранным рецепторам, сопряженным с G-белками. Аденозин связывается также с внутриклеточным участком на каталитической субъединице аденилатциклазы, вызывая ее ингибирование. Аденозиновые рецепторы локализованы в разных типах тканей и участвуют в регуляции целого ряда биологических процессов. Активация A1 и А3 рецепторов вызывает снижение уровня цАМФ [Jockers R., Linder M.E., Hoehnegger M. J. Biol. Chem. 1994, 269, 32077. Palmer T.M., Gettys T.W., Stiles G.L. J. Biol. Chem. 1995, 270, 16895.], а активация A2A и A2B рецепторов приводит к его увеличению уровня цАМФ [Kull В., Svenningsson P., Fredholm B.B. Mol. Pharmacol. 2000б 58, 771. Bruns R.F., Lu G.H., Pugsley T.A. Mol. Pharmacol. 1986, 29, 331.]. Кроме того, стимулирование A1 рецепторов вызывает активацию калиевых и дезактивацию кальциевых каналов [Iredale P.A., Alexander S.P.H., Hill S.J. Br. J. Pharmacol. 1994, 111, 1252. Bunemann M., Pott L.J. Physiol. 1995, 482, 81.], а стимулирование A2A рецепторов приводит к ингибированию функциональной активности D2 дофаминовых рецепторов, что имеет важное значение в развитии неврологических и психических заболеваний [Fuxe К., Ferre S., Zoli M., Agnati L.F. Brain Res. Rev. 1998, 26, 258. Franco R., Ferre S., Agnati L., Torvinen M., Gines S., Hillion J. Neuropsychoparmacol, 2000, 23, S50.].
Лиганды аденозиновых рецепторов находят широкое применение в фармакологии и медицине. Большое количество научных работ и патентов посвящено исследованиям по использованию антагонистов A2A рецепторов в качестве лекарственных кандидатов для лечения заболеваний центральной нервной системы (ЦНС), в частности болезни Паркинсона [Pinna A. Novel investigational adenosine A2A receptor antagonists for Parkinson's disease. Expert Opinion on Investigational Drugs, 2009, 18(11), 1619-1631.];
различного рода депрессий [E1 Yacoubi M, Costentin J, Vaugeois JM (December 2003). "Adenosine A2A receptors and depression". Neurology 61 (11 Suppl 6): S82-7. PMID 14663017. http://www.neurology.org/cgi/pmidlookup?view=long&pmid=14663017; Kaster MP, Rosa АО, Rosso MM, Goulart EC, Santos AR, Rodrigues AL (January 2004). "Adenosine administration produces an antidepressant-like effect in mice: evidence for the involvement of A1 and A2A receptors". Neuroscience Letters 355 (1-2):21-4. doi:10.1016/j.neulet.2003.10.040. PMID 14729225. http://linkinghub.elsevier.com/retrieve/pii/S0304394003012345; Lobato KR, Binfare RW, Budni J, Rosa АО, Santos AR, Rodrigues AL (May 2008). "Involvement of the adenosine A1 and A2A receptors in the antidepressant-like effect of zinc in the forced swimming test". Progress in Neuro-psychopharmacology & Biological Psychiatry 32 (4): 994-9. doi:10.1016/j.pnpbp.2008.01.012. PMID 18289757.],
когнитивных расстройств [Takahashi RN, Pamplona FA, Prediger RD (2008). "Adenosine receptor antagonists for cognitive dysfunction: a review of animal studies". Frontiers in Bioscience: a Journal and Virtual Library 13 (13):2614-32. doi:10.2741/2870. PMID 17981738. http://www.bioscience.org/2008/v13/af2870/fulltext.htm.]
и воспалительных процессов [Sullivan GW (November 2003). "Adenosine A2A receptor agonists as anti-inflammatory agents". Current Opinion in Investigational Drugs (London, England: 2000) 4 (11):1313-9. PMID 14758770; Lappas CM, Sullivan GW, Linden J (July 2005). "Adenosine A2A agonists in development for the treatment of inflammation". Expert Opinion on Investigational Drugs 14 (7): 797-806. doi:10.1517/13543784.14.7.797. PMID 16022569.].
Сравнительно недавно было показано, что аденозин, который накапливается вблизи опухолевой ткани [Blay J., White Т.D., Oskin D.W. The Extracellular Fluid of Solid Carcinomas Contains immunosuppressive Concentrations of Adenosine. Cancer Research, (1997) 57, 2602-2605.], существенно подавляет способность активированных Т-лимфоцитов и натуральных клеток-киллеров связываться с опухолевыми клетками и убивать их [Hoskin D. W, Reynolds Т., Blay J. 2-Chloroadenosine inhibits the MHC unrestricted cytolytic activity of anti-CD3-activated killer cells: evidence for the involvement of a non-A1/A2 cell-surface adenosine receptor. Cell Immunol. (1994) 159:85-93. Hoskin D.W., Reynolds Т., Blay, J. Adenosine as a possible inhibitor of killer T-cell activation in the microenvironment of solid tumours. Int. J.Cancer, (1994) 59:854-855.]. Было показано, что гипоксия, развивающаяся в условиях твердых опухолей, инициирует образование повышенных концентраций аденозина вблизи опухолевой ткани. Аденозин, связываясь с аденозиновыми рецепторами типа А2А, находящимися на клеточной мембране лимфоцитов, передает аденозиновый сигнал внутрь клеток путем активации внутриклеточной аккумуляции циклического аденозинмонофосфата (цАМФ), который, в свою очередь, и снижает способность лимфоцитов атаковать опухолевую ткань [Sitkovsky M.V, Kjaergaard J, Lukashev D, Ohta A. Hypoxia-Adenosinergic Immunosuppression:Tumor Protection by Т Regulatory Cells and Cancerous Tissue Hypoxia. Clin Cancer Res (2008) 14(19), 5947-5952.]. На основании этих наблюдений [Ohta A., Gorelik E., Simon J., Prasad S.J, Ronchese F., Lukashev D., Wong M. K.K., Huang X., Caldwell S., Liu K., Patrick Smith P., Chen J.-F., Jackson E. K, Apasov S., Abrams S., Sitkovsky M. A2A adenosine receptor protects tumors from antitumor Т cells. Proc Natl Acad Sci, USA (2006), 103, 13132-13137. Lukashev D., Sitkovsky M., Ohta A.. From "Hellstrom Paradox" to anti-adenosinergic cancer immunotherapy. Purinergic Signalling (2007) 3, 129-134] предложен инновационный подход к усилению эффективности противоканцерных вакцин с помощью адъюванта, являющегося ингибитором A2A аденозинового рецептора [Ohta A., Sitkovsky M. METHODS AND COMPOSITIONS FOR IMPROVING IMMUNE RESPONSES, WO 2008/147482 04.12.2008].
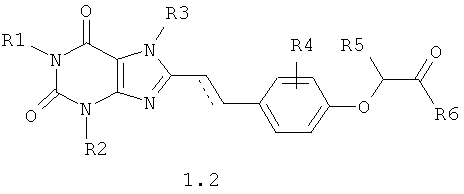
Описано и запатентовано большое количество антагонистов А2А рецепторов, в том числе клинические кандидаты:
- SCH58261: 2-(2-furanyl)-7-(2-phenylethyl)-7H-pyrazolo[4,3-e][l,2,4]triazolo[1,5-c]pyrimidin-5-amine;
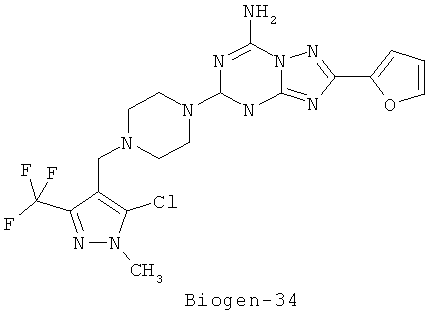
- Biogen-34: 5-[4-[[5-chlorol-1-methyl-3-(trifluoromethyl)-1H-pyrazol-4-yl]methyl]-1-piperazinyl]-2-(2-furanyl)-[1,2,4]triazolo[1,5-α][1,3,5]triazin-7-amine;
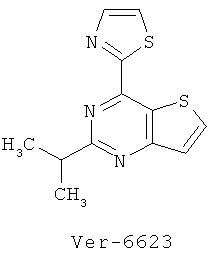
- Ver-6623:2-isopropyl-4-(thiazol-2-yl)thieno[3,2-d]pyrimidine;
- MSX-2:3-(3-hydroxypropyl)-7-methyl-8-(m-methoxystyryl)-1-propargylxanthine;
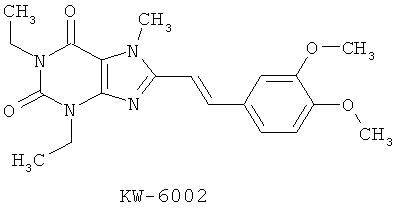
- KW-6002: (E)1,3-diethyl-8-(3,4-dimethoxystyryl)-7-methylxanthine;
- DMPX: 3,7-dimethyl-1-propargylxanthine,
для которых подробно изучены фармакологические профайлы на крысах и сравнены А2А рецепторные активности и селективности к другим аденозиновым рецепторам.


Поиск высокоэффективных и селективных антагонистов А2А рецепторов является одним из основных направлений создания новых фармакологических средств для лечения заболеваний ЦНС, в частности болезни Паркинсона, онкологических заболеваний и воспалительных процессов. В этой связи актуальным является разработка новых антагонистов A2A рецепторов, фармацевтических композиций и лекарственных препаратов, а также способов их получения и применения.
Ниже приведены определения терминов, которые использованы в описании этого изобретения.
«Адъювант» (adjuvant) - вещество или комплекс веществ, используемое для усиления иммунного ответа или усиливающее действие лекарственных средств.
«Азагетероцикл» означает ароматическую или неароматическую моноциклическую или полициклическую систему, содержащую в цикле, по крайней мере, один атом азота. Азагетероцикл может иметь один или более «заместителей циклической» системы.
«Алкенил» означает алифатическую линейную или разветвленную углеводородную группу, содержащую от 2 до 7 атомов углерода и включающую, по крайней мере, одну углерод-углеродную двойную связь.
Разветвленная, означает, что к линейной алкенильной цепи присоединены один или несколько низших алкильных групп, таких как метил, этил или пропил. Алкильная группа может иметь один или несколько заместителей, например, таких как галоген, алкенилокси, циклоалкил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероаралкилокси, гетероциклил, гетероциклилалкилокси, алкоксикарбонил, аралкоксикарбонил,
гетроаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетеоцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил.
Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил и циклогексилбутенил.
«Алкенилокси» означает алкенил-O-группу, в которой алкенил определен в данном разделе. Предпочтительным алкенилокси группами являются аллилокси и 3-бутенилокси.
«Алкенилоксиалкил» означает алкенил-O-алкилгруппу, в которой алкил и алкенил определены в данном разделе.
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «низших алкильных» заместителей. Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей»), включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонилгетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил,
гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1NC(=O)-, Rk aRk+1 aNC(=S)-, Rk aRk+1 aNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетеоцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил, метоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk a k+1 aNC(=O)-, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Алкинил» означает алифатическую линейную или разветвленную углеводородную группу, содержащую от 2 до 12 атомов углерода и включающую, по крайней мере, одну углерод-углеродную тройную связь.
Разветвленная означает, что к линейной алкинильной цепи присоединены один или несколько низших алкильных групп, таких как метил, этил или пропил. Алкильная группа может иметь один или несколько заместителей, например, таких как галоген, алкенилокси, циклоалкил, циано, гидрокси, алкокси, лкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероаралкилокси, гетероциклил, гетероциклилалкилокси, алкоксикарбонил, аралкоксикарбонил, гетроаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, бензилоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными алкенильными группами являются этенил, пропенил, н-бутенил, изо-бутенил, 3-метилбут-2-енил, н-пентенил, бута-1,3-диин и гекса-1,3,5-триин.
«Алкокси» означает алкил-O-группу, в которой алкил определен в данном разделе. Предпочтительным алкилоксигруппами являются метокси, этокси, н-пропокси, изо-пропокси и н-бутокси.
«Аминогруппа» означает Rk aRk+1 aN-группу, замещенную или незамещенную «заместителем аминогруппы», Rk a и Rk+1 a, значение которых определено в данном разделе, например амино (H2N-), метиламино, диэтиламино, пирролидино, морфолино, бензиламино или фенетиламино.
«Антагонисты» означают лиганды, которые связываются с рецепторами определенного типа и не вызывают активного клеточного ответа. Антагонисты препятствуют связыванию агонистов с рецепторами и тем самым блокируют передачу специфического рецепторного сигнала.
«Антидепрессант» означает лекарственное средство, предназначенное для лечения депрессии.
«Арил» означает ароматическую моноциклическую или полициклическую систему, включающую от 6 до 14 атомов углерода, преимуществено от 6 до 10 атомов углерода. Арил может содержать один или более «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями арильных групп являются фенил или нафтил, замещенный фенил или замещенный нафтил. Арил может быть аннелирован с неароматической циклической системой или гетероциклом.
«Галоген» означает фтор, хлор, бром и йод. Предпочтительными яляются фтор, хлор и бром.
«Гетероциклил» означает ароматическую или неароматическую насыщенную моноциклическую или полициклическую систему, включающую от 3 до 10 атомов углерода, преимущественно от 5 до 6 атомов углерода, в которой один или несколько атомов углерода заменены на гетероатом, такой как азот, кислород, сера. Приставка «аза», «окса» или «тиа» перед гетероциклилом означает наличие в циклической системе атома азота, атома кислорода или атома серы соответственно. Гетероциклил может иметь один или несколько «заместителей циклической системы», которые могут быть одинаковыми или разными. Атомы азота и серы, находящиеся в гетероциклиле, могут быть окислены до N-оксида, S-оксида или S-диоксида. Представителями гетероциклилов являются пиперидин, пирролидин, пиперазин, морфолин, тиоморфолин, тиазолидин, 1,4-диоксан, тетрагидрофуран, тетрагидротиофен и др.
«Гидрат» означает стехиометрическую или нестехиометрическую композицию вещества (соединения) или его соли с водой.
«Депрессия» означает большую депрессию; эпизодическую, хроническую и рецидивирующую формы большой депрессии; дистимическое расстройство (дистимию); циклотимию; аффективные расстройства; синдром сезонного аффективного расстройства; биполярные расстройства, включая биполярные расстройства I и II типа; а также другие депрессивные расстройства и состояния. Термин депрессия означает также депрессивные состояния, сопровождающие болезнь Альцгеймера, васкулярную деменцию; расстройства настроения, индуцированные алкоголем и веществами; шизоаффективные расстройства депрессивного типа; расстройства адаптации. Кроме того, депрессия включает депрессивные состояния онкологических больных; при болезни Паркинсона; депрессию после инфаркта миокарда; депрессию бесплодных женщин; педиатрическую депрессию; послеродовую депрессию; а также другие депрессивные состояния, сопровождающие соматические, неврологические и прочие заболевания.
«Заместитель» означает химический радикал, который присоединяется к скэффолду (фрагменту), например «заместитель алкильный», «заместитель аминогруппы», «заместитель карбамоильный», «заместитель циклической системы», значения которых определены в данном разделе.
«Заместитель аминогруппы» означает заместитель, присоединенный к аминогруппе. Заместитель аминогруппы представляет собой водород, алкил, циклоалкил, арил, гетероарил, гетероциклил, ацил, ароил, алкилсульфонил, арилсульфонил, гетероарилсульфонил, алкиламинокарбонил, ариламинокарбонил, гетероариламинокарбонил, гетероциклиламинокарбонил, алкиламинотиокарбонил, ариламинотиокарбонил, гетероариламинотиокарбонил, гетероциклиламинотиокарбонил, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил. Значение «заместителей аминогруппы» определено в данном разделе.
«Заместитель циклической системы» означает заместитель, присоединенный к ароматической или неароматической циклической системе, включая водород, алкилалкенил, алкинил, арил, гетероарил, аралкил, гетероаралкил, гидрокси, гидроксиалкил, амино, аминоалкил, алкокси, арилокси, ацил, ароил, галоген, нитро, циано, карбокси, алкоксикарбонил, арилоксикарбонил, аралкоксикарбонил, алкилоксиалкил, арилоксиалкил, гетероциклилоксиалкил, арилалкилоксиалкил, гетероциклилалкилоксиалкил, алкилсульфонил, арилсульфонил, гетероциклилсульфонил, алкилсульфинил, арилсульфинил, гетероциклилсульфинил, алкилтио, арилтио, гетероциклилтио, гетероциклилтио, алкилсульфонилалкил, арилсульфонилалкил, гетероциклилсульфонилалкил, алкилсульфинилалкил, арилсульфинилалкил, гетероциклилсульфинилалкил, алкилтиоалкил, арилтиоалкил, гетероциклилтиоалкил, арилалкилсульфонилалкил, гетероциклилалкилсульфонилалкил, арилалкилтиоалкил, гетероциклилалкилтиоалкил, циклоалкил, циклоалкенил, гетероциклил, гетероцикленил, амидино,
Rk aRk+1 aN-, Rk aN=, Rk aRk+1 aN-алкил-, Rk aRk+1 aNC(=O)- или Rk aRk+1 aNSO2-, где Rk a и Rk+1 a представляют собой независимо друг от друга «заместители аминогруппы», значение которых определено в данном разделе, например, водород, необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, или необязательно замещенный гетероаралкил, или заместитель Rk aRk+1 aN-, в котором Rk a может быть ацил или ароил, а значение Rk+1 a определено выше, или «заместителями циклической системы» являются Rk aRk+1 aNC(=O)- или Rk aRk+1 aNSO2-, в которых Rk a и Rk+1 a вместе с атомом азота, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетероцикленил.
«Когнитивные расстройства или нарушения когнитивных функций (cognitive disorder)» означают нарушение (ослабление) умственных возможностей, включающих внимание, память, мышление, познание, обучение, речевые, мыслительные, исполнительные и творческие способности, ориентацию во времени и пространстве, в частности когнитивные расстройства, связанные с болезнями Альцгеймера, Паркинсона и Гантингтона; старческое слабоумие; возрастные расстройства памяти (age-associated memory impairment, AAMI); дисметаболические энцефалопатии; психогенные нарушения памяти; амнезия; амнестические расстройства; транзиторная глобальная амнезия; диссоциативная амнезия; васкулярная деменция; легкие (или умеренные) когнитивные нарушения (mild cognitive impairment, MCI); синдром нарушения внимания с гиперактивностью (attention deficit hyperactivity disorder, AD/HD); когнитивные нарушения, сопровождающие психотические заболевания, эпилепсию, делирий, аутизм, психозы, синдром Дауна, биполярные расстройства и депрессию; СПИД-ассоциированная деменция; деменция при гипотиреоидизме; деменция, индуцированная алкоголем, веществами, вызывающими зависимость, и нейротоксинами; деменция, сопровождающая нейродегенеративные заболевания, например мозжечковую дегенерацию и амиотрофический латеральный склероз; когнитивные расстройства, развивающиеся при инсульте, инфекционных и онкологических заболеваниях головного мозга, а также при черепно-мозговых травмах; нарушения когнитивных функций, ассоциированные с аутоиммунными и эндокринными заболеваниями; и прочие когнитивные расстройства.
«Лекарственное начало» (лекарственная субстанция, лекарственное вещество, drug-substance) означает физиологически активное вещество синтетического или иного происхождения (биотехнологического, растительного, животного, микробного и прочего), обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции), в виде таблеток, капсул, инъекций, мазей и др. готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Лиганды» (от латинского ligo - связывать) представляют собой химические вещества (малая молекула, неорганический ион, пептид, белок и прочее), способные взаимодействовать с рецепторами, которые трансформируют это взаимодействие в специфический сигнал.
«Нейродегенеративное заболевание (НЗ)» означает специфическое состояние и заболевание, характеризующиеся повреждением и первичной гибелью популяций нервных клеток в определенных областях центральной нервной системы. Нейродегенеративные заболевания включают, но не ограничивают, болезни Альцгеймера и Паркинсона; болезнь (хорею) Хантингтона; рассеянный склероз; мозжечковую дегенерацию; амиотрофический латеральный склероз; деменцию с тельцами Леви; спинальную мускульную атрофию; периферическую нейропатию; губчатый энцефалит («коровье бешенство», Creutzfeld-Jakob Disease); СПИД-ассоциированную деменцию; мультиинфарктную деменцию; лобно-височную деменцию; лейкоэнцефалопатию (болезнь исчезающей белого вещества); хронические нейродегенеративные заболевания; инсульт; ишемическое, реперфузионное и гипоксическое повреждение мозга; эпилепсия; церебральная ишемия; глаукома; черепно-мозговая травма; синдром Дауна; энцефаломиелит; менингит; энцефалит; нейробластома; шизофрения; депрессия. Кроме того, нейродегенеративные заболевания включают патологические состояния и расстройства, развивающиеся при гипоксии, злоупотреблении веществами, вызывающими зависимость, при воздействии нейротоксинов, инфекционных и онкологических заболеваниях головного мозга, а также нейрональные повреждения, ассоциированные с аутоиммунными и эндокринными заболеваниями; и прочие нейродегенеративные процессы.
«Низший алкил» означает линейный или разветвленный алкил с 1-5 атомами углерода.
«Ноотропы» или «ноотропики», они же нейрометаболические стимуляторы - вещества, принимаемые для улучшения умственных способностей.
«Психические расстройства» (психические заболевания) - это болезни или болезненные состояния, связанные с нарушением и/или расстройством психики. Психические расстройства включают аффективные расстройства (биполярные аффективные расстройства, большая депрессия, гипомания, малая депрессия, маниакальный синдром, синдром Котара, циклотимия, шизоаффективное расстройство и др.); интеллектуально-мнестические расстройства, мании (гипомания, графомания, клептомания, магазиномания, мания преследования, мономания, порнографомания, эротомания и др.); расстройство множественной личности, аменцию, белую горячку, бред, бредовый синдром, галлюцинаторный синдром, галлюцинации, галлюциноз, гомицидоманию, делирий, иллюзию, кверулянтство, клиническую ликантропию, макропсию, манихейский бред, микропсию, наркоманию, нервную анорексию, онейроидный синдром, пароноид, паранойю, парафрению, псевдогаллюцинации, психоз, синдром Котара, шизоаффективное расстройство, шизотипическое расстройство, шизофрению, шизофреноподобное расстройство, шизофреноморфное расстройство, синдром Шребера, Даниэль Пауля; фобии (агарофобию, арахнофобию, аутофобию, верминофобию, гидрозофобию, гидрофобию, демофобию, зоофобию, канцерофобию, клаустрофобию, климакофобию, ксенофобию, мизофобию, радиофобию, светобоязнь, сколицефобию, скотофобию, социофобию, тетрафобию, трискаидефобию, эротофобию); алкогольные психозы, алкогольный палимпсест, аллотриофагию, афазию, графоманию, диссоциативные фуги, диссоциативные расстройства, дисфории, интернет-зависимости, ипохондрию, истерию, копрофемию, манию преследования, меланхолию, мизантропию, обсессию, панические атаки, синдром Аспергера, синдром Капгра, синдром Мюнхгаузена, синдром Ретта, синдром Фреголи, синдром дефицита внимания и гиперактивности, синдром навязчивых состояний, синдром последствий хронической наркотизации, синдром психического автоматизма, синдром раннего детского аутизма, сумашествие, тафофилию, тревожные состояния, синдром Хикикомори, эротографоманию и др.
«Психотические заболевания» - это все виды шизофрении; шизофреноподобные заболевания; шизотипические расстройства; шизоаффективные расстройства, включая биполярный и депрессивный типы; бредовые расстройства, включая бред отношения, преследования, величия, ревности, эротомании, а также ипохондрический, соматический, смешанный и недифференцируемый бред; кратковременные психотические расстройства; индуцированные психотические расстройства; индуцированные веществами психотические расстройства; а также другие психотические расстройства.
«Рецепторы» (от латинского recipere - получать, узнавать) представляют собой биологические макромолекулы, расположенные на цитоплазматической мембране клетки или внутриклеточно, способные специфически взаимодействовать с ограниченным набором физиологически активных веществ (лигандов) и трансформировать сигнал об этом взаимодействии в определенный клеточный ответ.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение формулы I и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлимых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как, парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
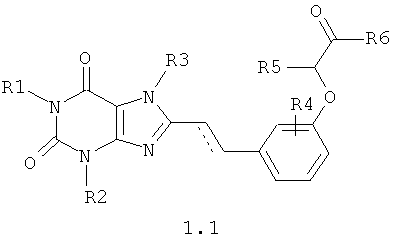
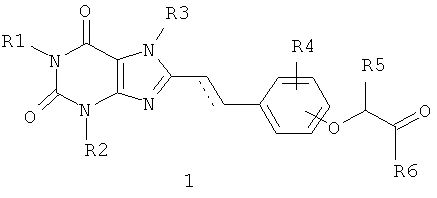
Предметом данного изобретения являются замещенные феноксиуксусные кислоты, их эфиры и амиды, включающие 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, общей формулы 1, а также их фармацевтически приемлемые соли,
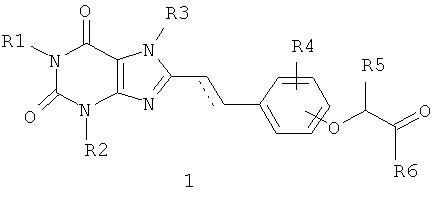
где R1, R2 и R3, необязательно одновременно, представляют собой водород, С1-С5алкил, С3-С5алкенил, или С3-С5алкинил;
R4 представляет собой водород, атом галогена, гидроксил, C1-С3алкил, C1-С3алкилокси;
R5 представляет собой водород, C1-С3алкил, группу -C(O)R6;
R6 представляет собой гидроксил, С1-С3алкилокси, С3-С5алкенилокси, С3-С5алкинилокси, необязательно замещенную аминогруппу, где заместители, необязательно одинаковые, выбираются из водорода, С1-С5алкила, необязательно замещенного моно- или диалкиламиногруппой, алкоксигруппой, 5-6-членным насыщенным гетероциклилом, содержащим 1-2 гетероатома, выбранных из азота и кислорода; пиридила, или фенила, необязательно замещенного 1-3 метоксигруппами; или необязательно замещенный 6-членный, необязательно аннелированный с 5-членным ненасыщенным гетероциклом, насыщенный гетероциклил, содержащий 2 атома азота, где заместители выбираются из C1-C5 алкила, необязательно замещенного 5-членным гетероарилом, содержащим 1-3 гетероатома, выбранных из азота и кислорода; или 6-членного необязательно насыщенного гетероциклила, содержащего 1-2 атома азота, необязательно замещенного C1-С5 алкилом, оксо, необязательно замещенным фенилом;
пунктирная линия с сопровождающей ее сплошной линией 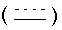 представляет (одинарную, двойную или тройную связь;
представляет (одинарную, двойную или тройную связь;
исключая {4-[2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-уксусную кислоту и этиловый эфир {4-[2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-уксусной кислоты.
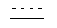
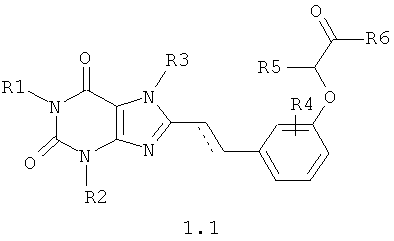
Согласно данному изобретению предпочтительными замещенными феноксиуксусными кислотами их эфирами и амидами общей формулы 1 являются соединения общей формулы 1.1 и 1.2,
в которых R1, R2, R3, R4, R5, R6 и пунктирная линия с сопровождающей ее сплошной линией  имеют значение, указанное для соединений общей формулы 1.
имеют значение, указанное для соединений общей формулы 1.

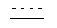
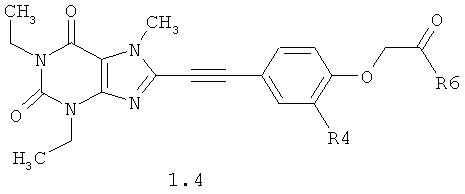
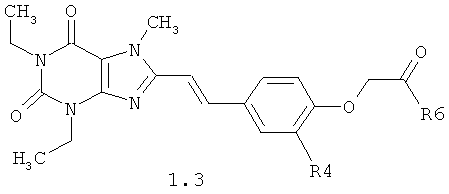
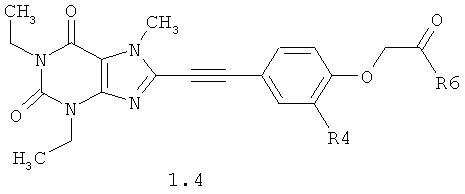
Более предпочтительными замещенными феноксиуксусными кислотами их эфирами и амидами общей формулы 1 являются также соединения общей формулы 1.3 и 1.4, в которых R6 имеет значение указанное выше, а R4 представляет собой водород или метоксигруппу.
Согласно данному изобретению более предпочтительными соединениями являются
метиловый эфир{5-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1.1.1,
{4-[(Е)-2-(1,3-диэтил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1.2.0(1),
{4-[(Е)-2-(1,3-диэтил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-уксусную кислоту 1.2.0(2),
метиловый эфир 2-(4-(2-(1,3диэтил-7 метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-этил)фенокси)-уксусной кислоты 1.2.0(3),
2-(4-(2-(1,3диэтил-7 метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-этил)фенокси)-уксусной кислоты 1.2.0(4),
метиловый эфир {4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-уксусной кислоты 1.3.2,
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-ацетамид 1.3.3,
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N,N-ди-(2-метоксиэтил)-ацетамид 1.3.4,
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-(2-диметиламиноэтил)-N-метил-ацетамид 1.3.5,
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-(3-морфолин-4-илпропил)-ацетамид 1.3.6,
1,3-диэтил-8-((Е)-2-{4-[2-(4-изопропил-пиперазин-1-ил)-2-оксо-этокси]-фенил}-винил)-7-метил-3,7-дигидро-пурин-2,6-дион 1.3.7,
1,3-диэтил-7-метил-8-[(Е)-2-(4-{2-оксо-2-[4-(1,3,6-триметил-2,4-диоксо-1,2,3,4-тетрагидро-пиримидин-5-ил)-пиперазин-1-ил]-этокси}-фенил)-винил]-3,7-дигидро-пурин-2,6-дион 1.3.9,
1,3-диэтил-8-{(Е)-2-[4-(2-{4-[6-(2-метокси-5-фтор-фенил)-пиримидин-4-ил]-пиперазин-1-ил}-2-оксо-этокси)-фенил]-винил}-7-метил-3,7-дигидро-пурин-2,6-дион 1.3.10,
1,3-диэтил-7-метил-8-[(Е)-2-(4-{2-оксо-2-[4-(6-фенил-пиримидин-3-ил)-пиперазин-1-ил]-этокси}-фенил)-винил]-3,7-дигидро-пурин-2,6-дион 1.3.11,
8-{(Е)-2-[4-(2-{4-[3-(3,4-диметокси-фенил)-[1,2,4]оксадиазол-5-илметил]-пиперазин-1-ил}-2-оксо-этокси)-фенил]-винил}-1,3-диэтил-7-метил-3,7-дигидро-пурин-2,6-дион 1.3.12.
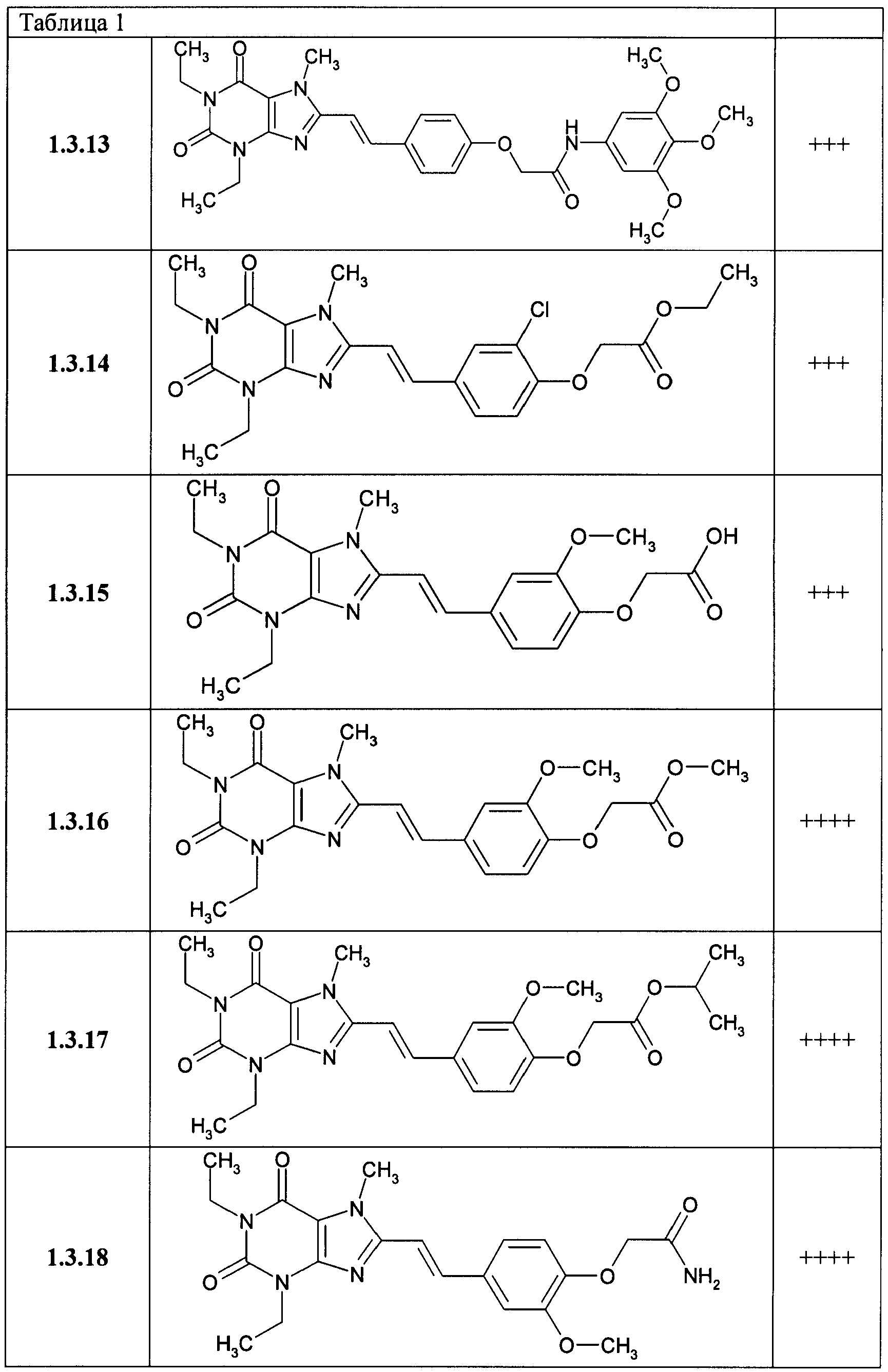
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-(3,4,5-триметоксифенил)-ацетамид 1.3.13,
{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-хлор-фенокси}-уксусной кислоты 1.3.14,
{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1.3.15,
метиловый эфир {4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1.3.16,
изо-пропиловый эфир {4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1.3.17,
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-ацетамид 1.3.18,
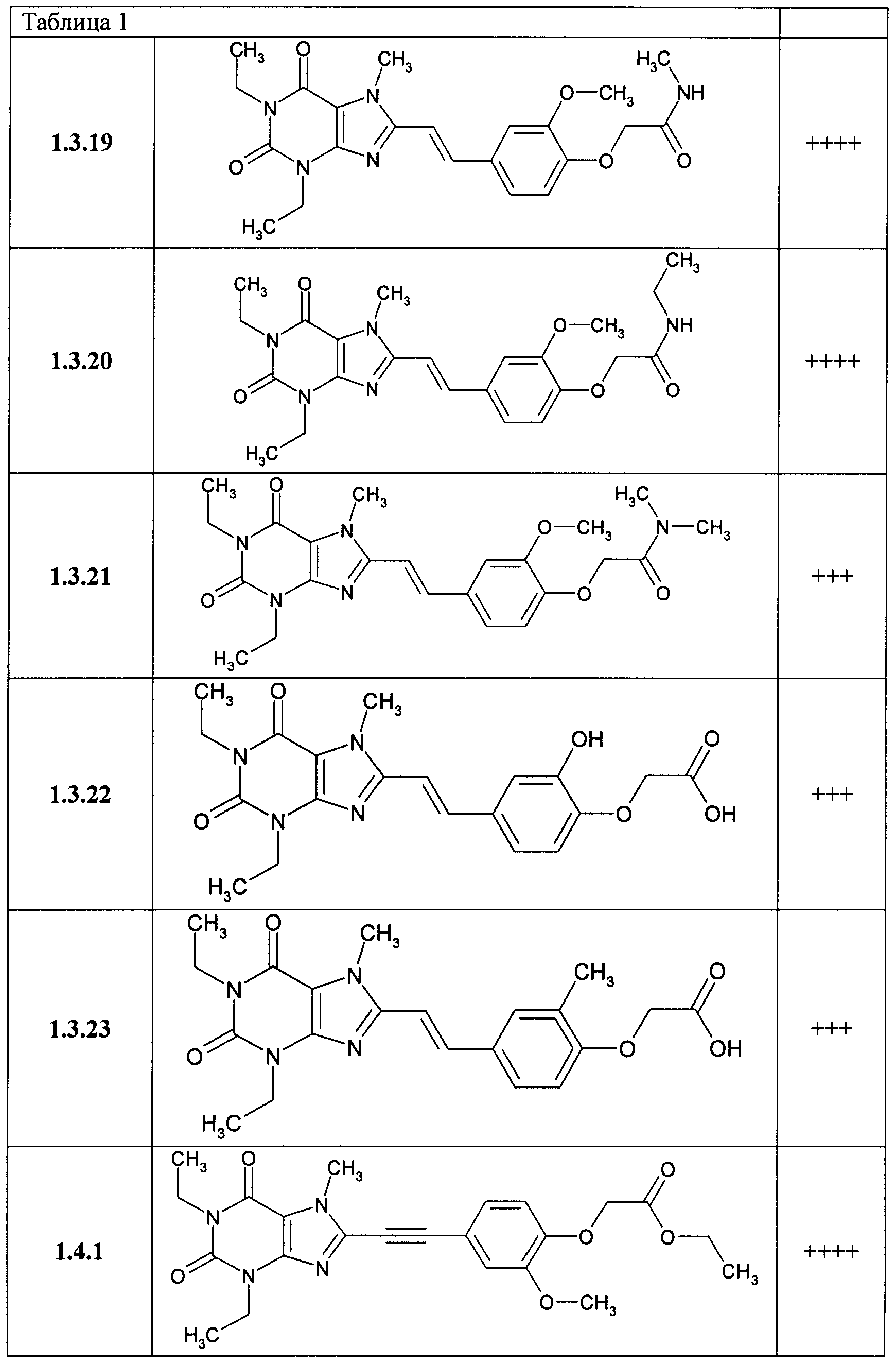
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-метил-ацетамид 1.3.19,
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-этил-ацетамид 1.3.20,
2-{4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N,N-диметил-ацетамид 1.3.21,
этиловый эфир [4-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-илэтинил)-2-метокси-фенокси]-уксусной кислоты 1.4.1,
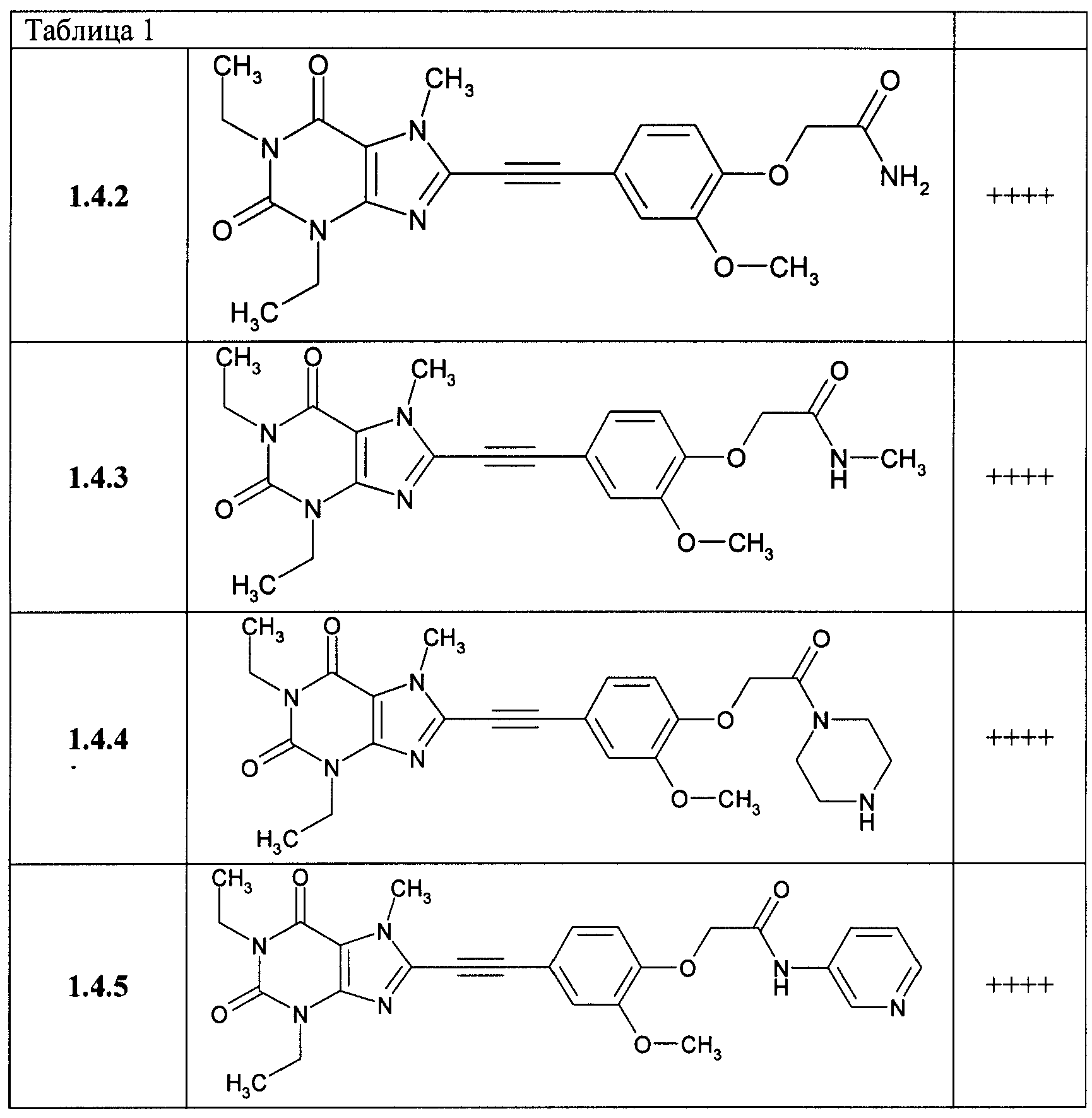
[4-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-илэтинил)-2-метокси-фенокси]-ацетамид 1.4.2,
[4-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-илэтинил)-2-метокси-фенокси]-N-метил-ацетамид 1.4.3,
1,3-диэтил-8-[3-метокси-4-(2-оксо-2-пиперазин-1-ил-этокси)-фенилэтинил]-7-метил-3,7-дигидро-пурин-2,6-дион 1.4.4,
[4-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-илэтинил)-2-метокси-фенокси]-N-пиридин-3-ил-ацетамид 1.4.5.
Предметом данного изобретения является способ получения замещенных феноксиуксусных кислот, включающих 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, общей формулы 1а, ацилированием 5,6-диамино-1Н-пиримидин-2,4-дионов общей формулы 3 кислотами общей формулы 4 в присутствии соответствующих реагентов, например, О-(бензотриазол-1-ил)-N,N,N',N'-тетрагидроурония тетрафторбората или 1-гидроксибензтриазола N-(3-(диметиламино)пропил)-N'-этилкарбодиимида, циклизацией образующихся соединений общей формулы 5 в феноксиуксусные кислоты общей формулы 1а,
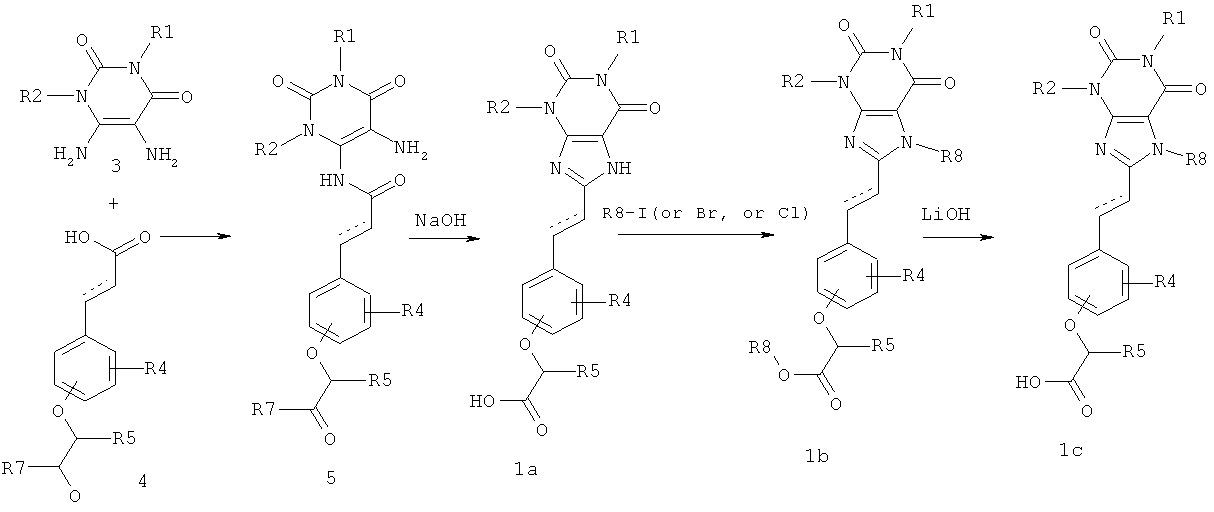
где R1, R2, R4, R5 и пунктирная линия с сопровождающей ее сплошной линией  имеют значение, указанное для соединений общей формулы 1; R7 представляет собой необязательно замещенный С1-С5алкилокси, необязательно замещенный С3-С5алкенилокси, необязательно замещенный С3-С5алкинилокси или аминогруппа, R8 представляет собой необязательно замещенный и необязательно насыщенный С1-С5алкил.
имеют значение, указанное для соединений общей формулы 1; R7 представляет собой необязательно замещенный С1-С5алкилокси, необязательно замещенный С3-С5алкенилокси, необязательно замещенный С3-С5алкинилокси или аминогруппа, R8 представляет собой необязательно замещенный и необязательно насыщенный С1-С5алкил.
Согласно данному изобретению предпочтительный способ получения необязательно замещенных амидов замещенных феноксиуксусных кислот, включающих 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, общей формулы 1d, заключается во взаимодействии метиловых эфиров общей формулы 1bb с аммиаком, первичными или вторичными аминами общей формулы 6,
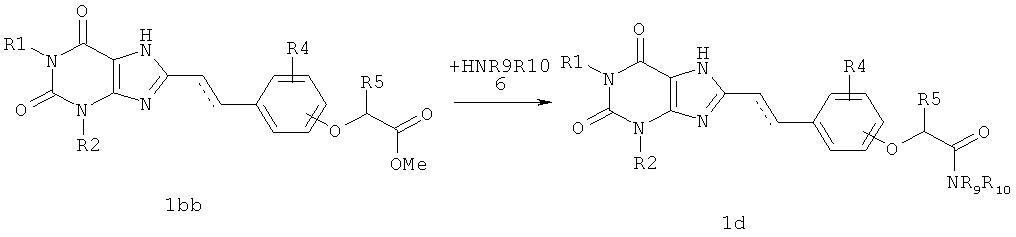
где R1, R2, R4 R5 и пунктирная линия с сопровождающей ее сплошной линией  имеют значение, указанное для соединений общей формулы 1; R9 и R10 необязательно одинаковые и представляют собой необязательно замещенный С1-С5алкил, необязательно замещенный С3-С5алкенил, необязательно замещенный С3-С5алкинил.
имеют значение, указанное для соединений общей формулы 1; R9 и R10 необязательно одинаковые и представляют собой необязательно замещенный С1-С5алкил, необязательно замещенный С3-С5алкенил, необязательно замещенный С3-С5алкинил.
Согласно данному изобретению предпочтительный способ получения необязательно замещенных амидов замещенных феноксиуксусных кислот, включающих 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, общей формулы 1d, заключается во взаимодействием кислот общей формулы 1c с аммиаком, первичными или вторичными аминами общей формулы 6 в присутствии 1-гидроксибензотриазола, N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорида и диизопропилэтиламина,
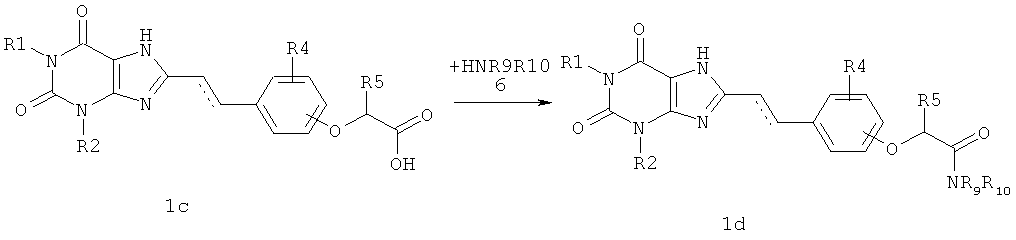
где R1, R2, R4 R5 и пунктирная линия с сопровождающей ее сплошной линией  имеют значение, указанное для соединений общей формулы 1; R9 и R10 необязательно одинаковые и представляют собой водород, необязательно замещенный С1-С5алкил, необязательно замещенный С3-С5алкенил, необязательно замещенный С3-С5алкинил или необязательно замещенный гетероциклил, включающий один или два атома азота.
имеют значение, указанное для соединений общей формулы 1; R9 и R10 необязательно одинаковые и представляют собой водород, необязательно замещенный С1-С5алкил, необязательно замещенный С3-С5алкенил, необязательно замещенный С3-С5алкинил или необязательно замещенный гетероциклил, включающий один или два атома азота.
Предметом данного изобретения являются новые антагонисты аденозинового A2A рецептора, представляющие собой замещенные феноксиуксусные кислоты, их эфиры и амиды, включающие 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, общей формулы 1, их фармацевтически приемлемые соли.
Антагонистическую активность новых соединений общей формулы 1 и их фармацевтически приемлемых солей по отношению к аденозиновому A2A рецептору проводили ex vitro в функциональном тесте на клетках. В эксперименте использовали клетки линии ValiScreen cell line (PerkinElmer, США), экспрессирующей рекомбинантный человеческий аденозиновый рецептор типа A2A.
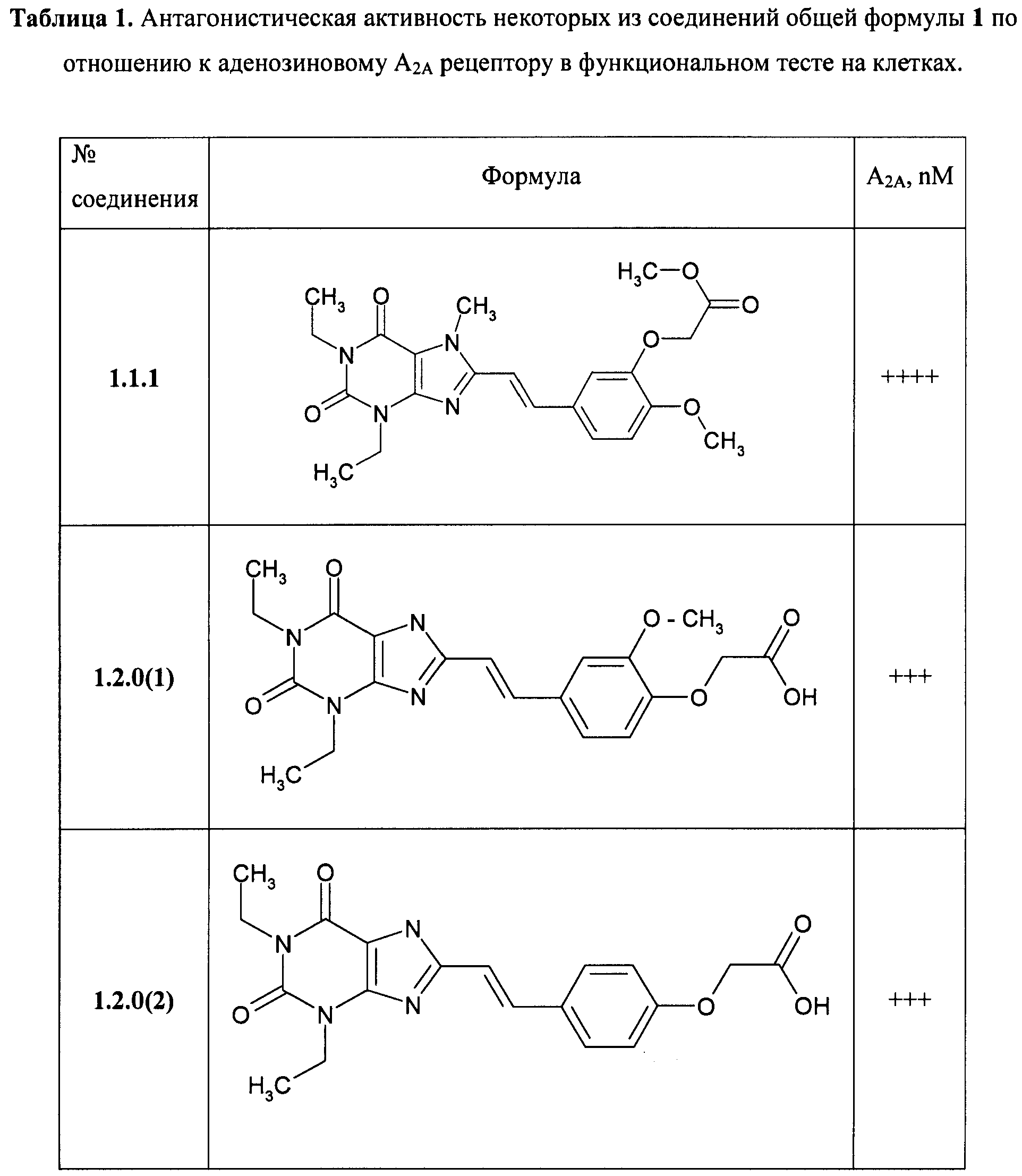
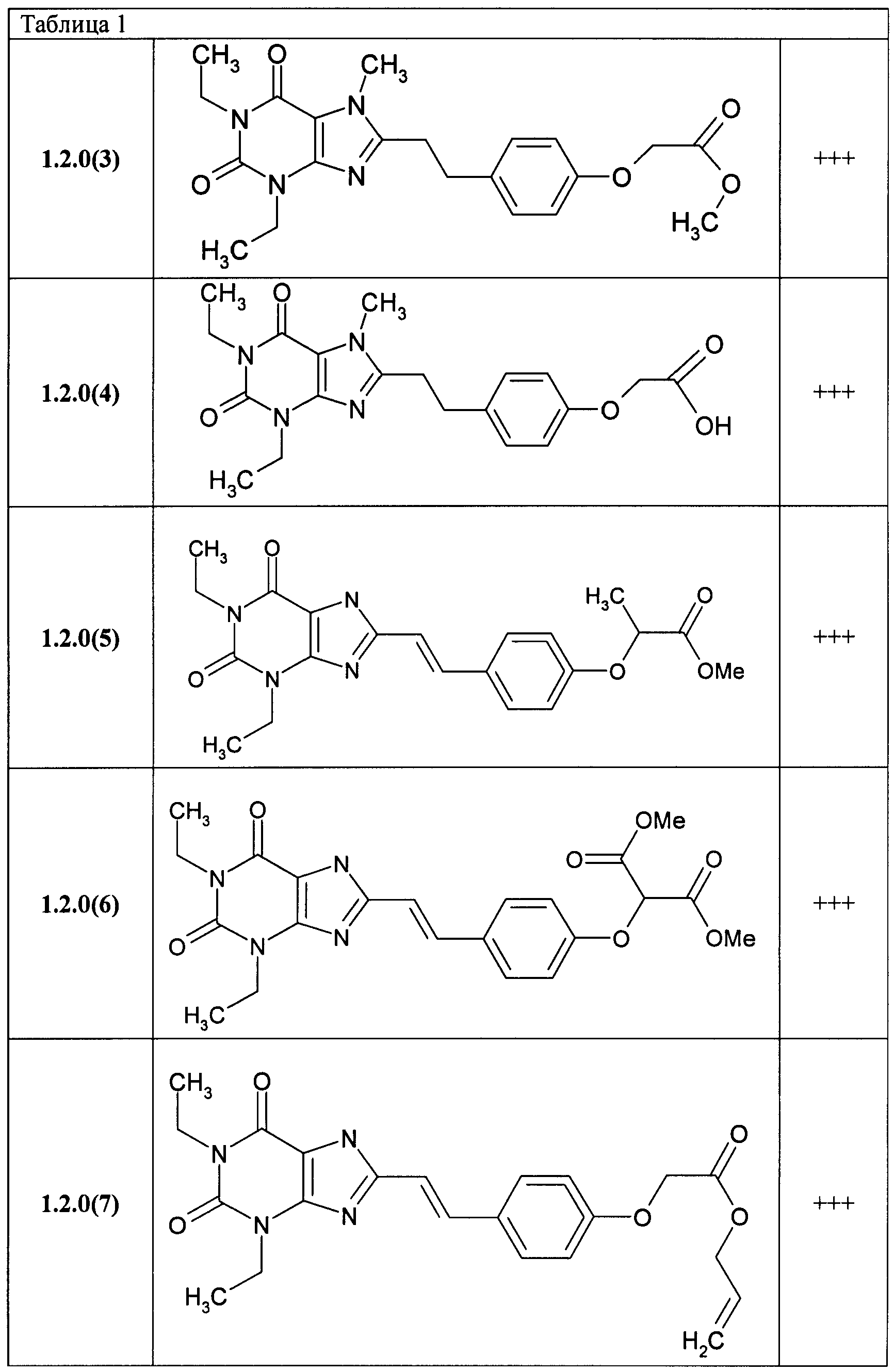
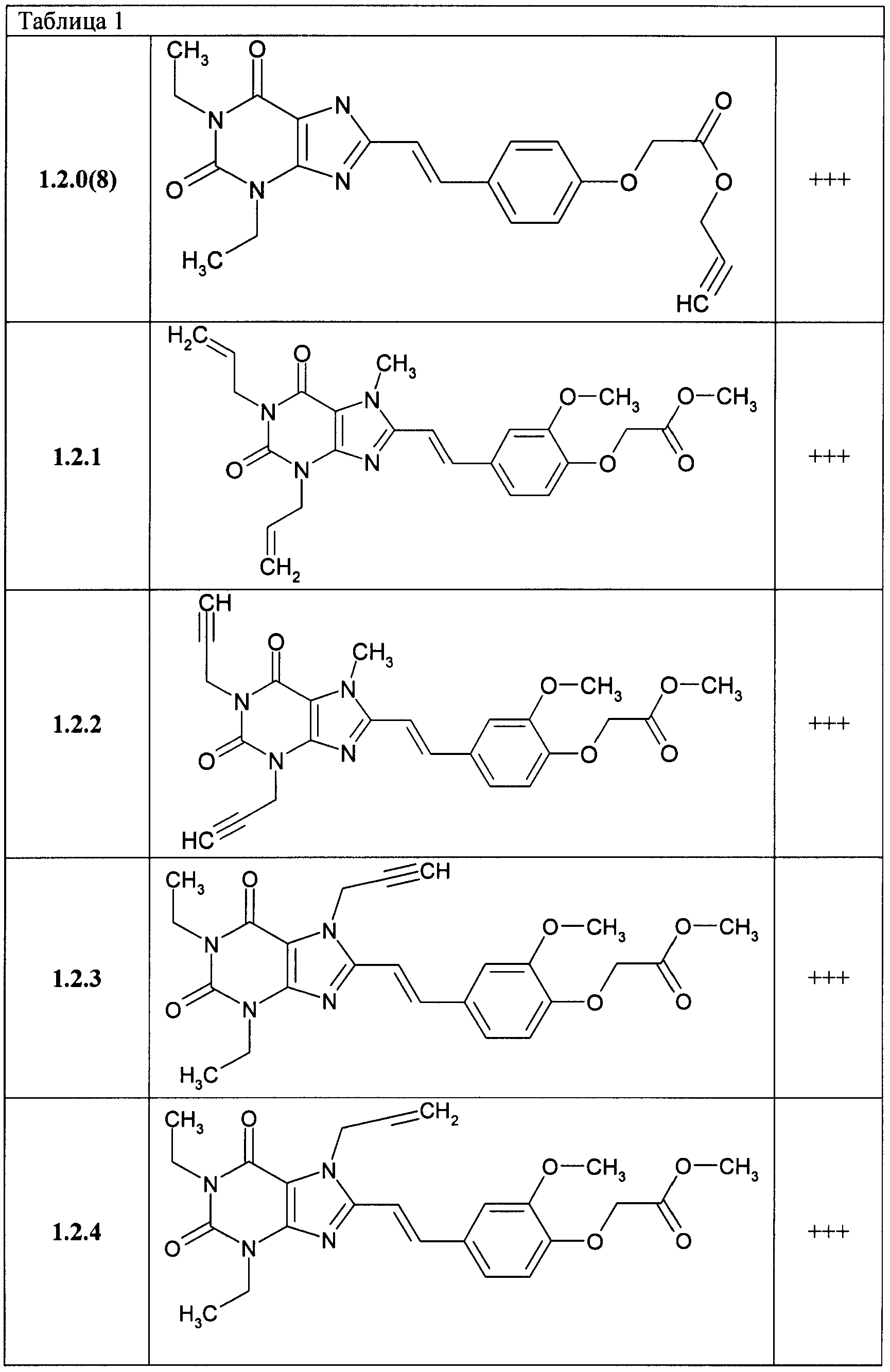
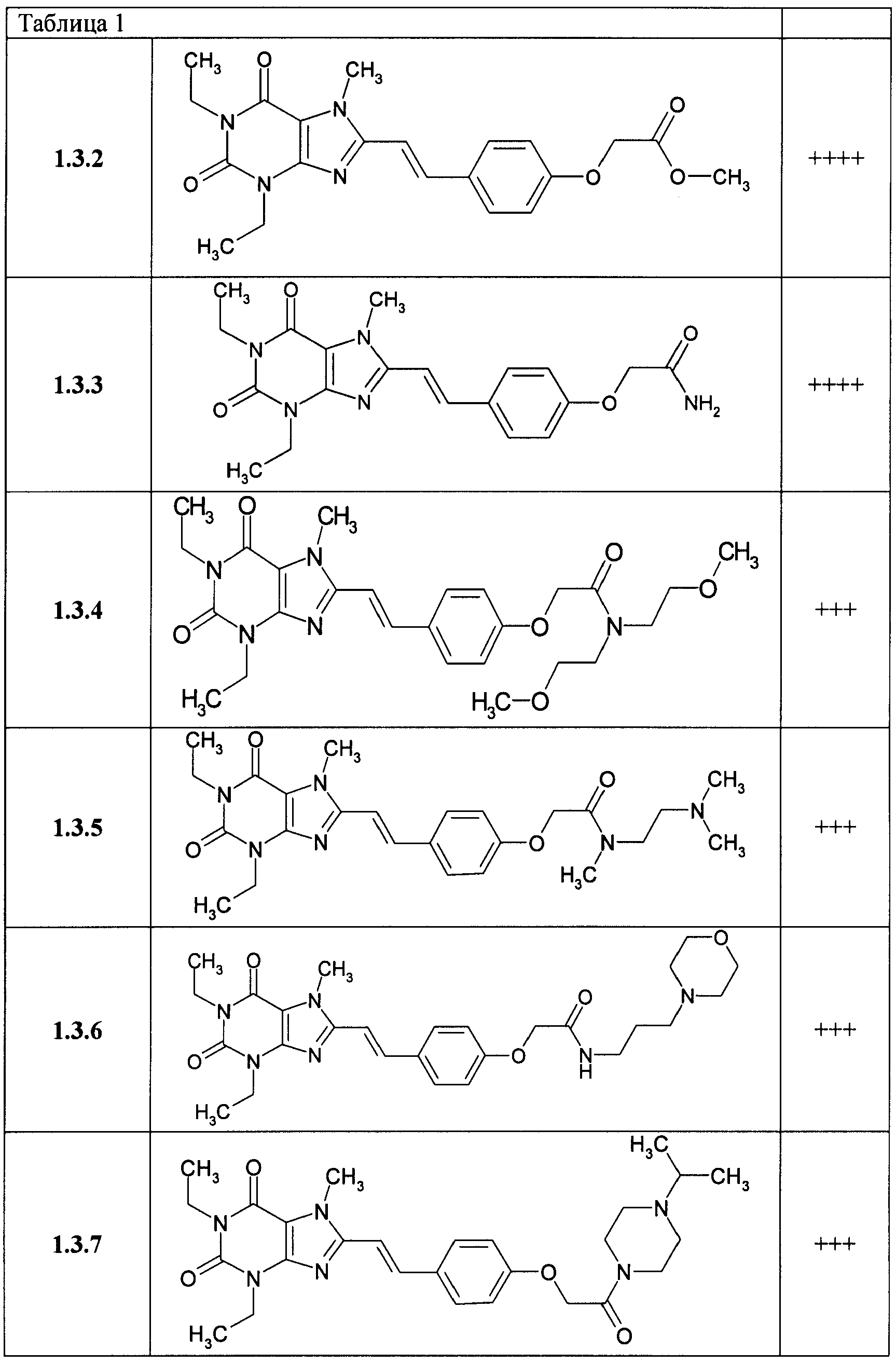
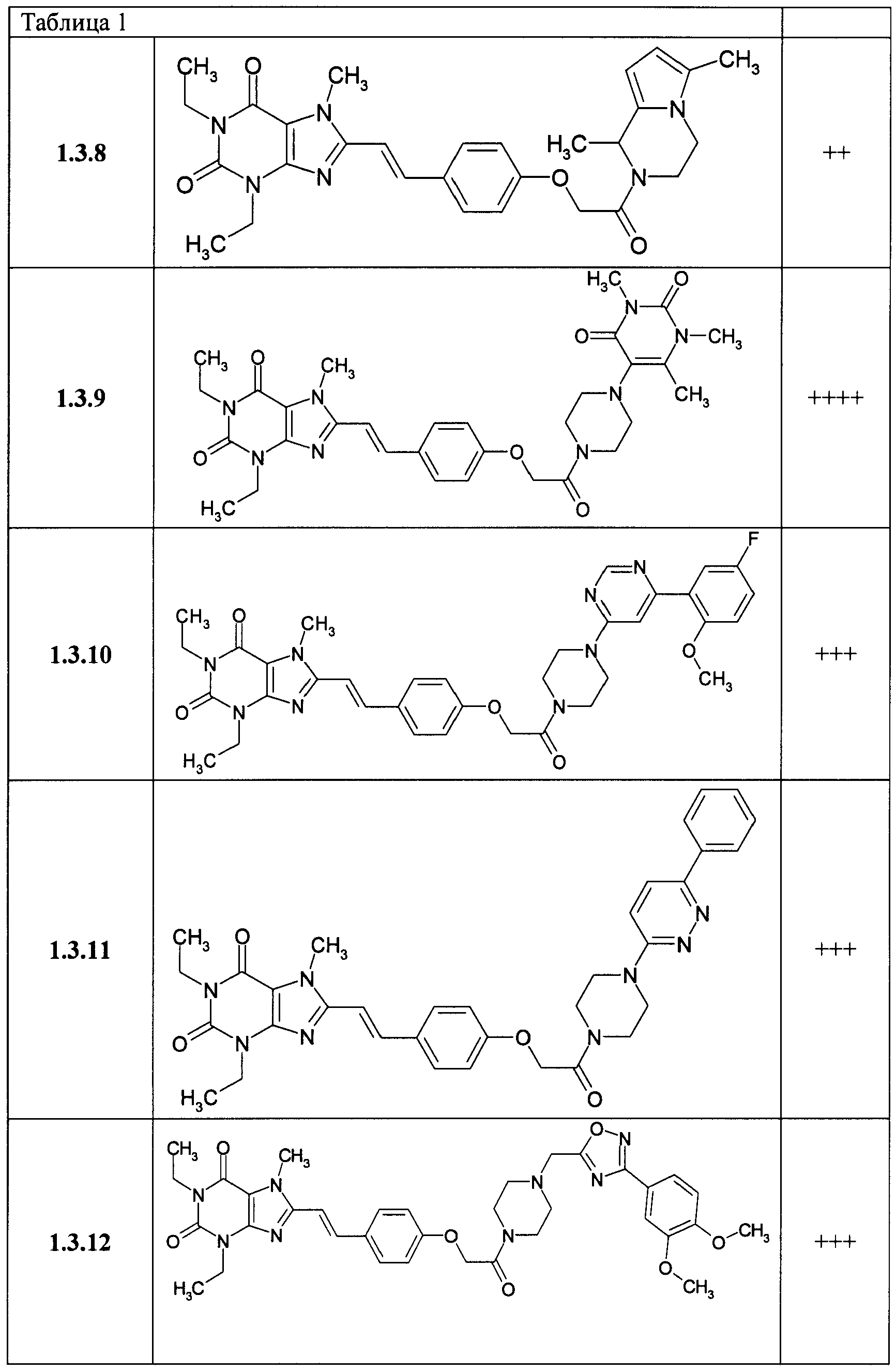
В таблице 1 представлены данные по активности К; для некоторых из соединений общей формулы 1, подтверждающие их высокую антагонистическую активность по отношению к аденозиновому A2A рецептору: + соответствует K1>50 nM, ++ соответствует K1 от 20 до 50 nM, +++ соответствует K1 от 10 до 20 nM и ++++ соответствует K1<10 nM.
Предметом данного изобретения являются соединения общей формулы 1, представляющие собой лекарственное начало (субстанцию) для приготовления фармацевтических композиций и готовых лекарственных форм для профилактики и лечения заболеваний центральной нервной системы, онкологических, вирусных и бактериальных заболеваний у теплокровных животных и людей.
Согласно данному изобретению новые соединения общей формулы 1 представляют собой средство (адъювант) для усиления иммунного ответа или действия лекарственных средств при комбинаторном лечении онкологических, вирусных и бактериальных заболеваний.
Предметом данного изобретения является фармацевтическая композиция, обладающая антагонистической активностью по отношению к аденозиновому A2A рецептору, включающая в качестве лекарственного начала (субстанции) или средства (адъюванта) соединения общей формулы 1 или их фармацевтически приемлемые соли и/или гидраты в терапевтически эффективном количестве.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция, наряду с соединением общей формулы 1 или его фармацевтически приемлемой солью, по настоящему изобретению может включать и другие активные субстанции, в том числе обладающие противогриппозной активностью, при условии, что они не вызывают нежелательных эффектов.
При необходимости использования фармацевтической композиции по настоящему изобретению в клинической практике она может смешиваться с традиционными фармацевтическими носителями.
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в том числе: в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, бесцветные агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Предметом данного изобретения является способ получения фармацевтической композиции смешением с инертным наполнителем и/или растворителем, по крайней мере, одного лекарственного начала (субстанции) общей формулы 1 или его фармацевтически приемлемой соли в терапевтически эффективном количестве.
Для определения селективности взаимодействия к аденозиновому A2A рецептору проводился радиолигандный анализ взаимодействия соединений общей формулы 1 с аденозиновыми A1, A2A, A2B и А3 рецепторами.
Радиолигандный анализ взаимодействия соединений общей формулы 1 с аденозиновыми A1, A2A, A2B и А3 рецепторами показал их высокую селективность по отношению к аденозиновому A2A рецептору.
Так, например, в условиях конкурентного радиолигандного связывания активность метилового эфира {4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1.3.16 по отношению к аденозиновому A2A рецептору в 131 раз выше его активности по отношению к аденозиновому A1 рецептору, в 148 раз выше его активности по отношению к аденозиновому A2B рецептору и в 1159 раз выше его активности по отношению к аденозиновому А3 рецептору. Для сравнения ниже представлены данные по активности и селективности соединения 1.3.16 и известного лиганда KW-6002, который использовался в качестве препарата сравнения, в условиях радиолигандного анализа.
Как видно из этих данных, лиганд 1.3.16 по отношению к аденозиновому A2A рецептору превосходит известный лиганд KW-6002 как по активности, так и по селективности.
|
Предметом данного изобретения являются способ селективного ингибирования активности аденозинового А2А рецептора, заключающийся в контактировании образца, содержащего аденозиновый А2А рецептор, с композицией, содержащей антагонист аденозинового А2А рецептора, представляющий собой замещенную феноксиуксусную кислоту, ее эфир или амид, включающий 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент общей формулы 1, ее фармацевтически приемлемую соль и/или гидрат.
Предметом данного изобретения является лекарственное средство, обладающее антагонистической активностью по отношению к аденозиновому A2A рецептору, в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, предназначенное для профилактики и лечения заболеваний центральной нервной системы, онкологических, вирусных и бактериальных заболеваний у людей и теплокровных животных, включающее в свой состав новое лекарственное начало (субстанцию) общей формулы 1 или фармацевтическую композицию в терапевтически эффективном количестве, а также для профилактики и лечения болезни Паркинсона, когнитивных расстройств, депрессий и воспалительных процессов.
В соответствии с данным изобретением способ профилактики и лечения заболеваний центральной нервной системы, онкологических заболеваний, инфекционных заболеваний и сепсиса у животных и людей заключается во введении пациенту нового лекарственного средства, или новой фармацевтической композиции в терапевтически эффективном количестве.
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно). Клиническая дозировка средства общей формулы 1 у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10~500 мг, предпочтительно 50~300 мг. Поэтому во время приготовления из фармацевтической композиции лекарственного средства по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10~500 мг средства общей формулы 1, предпочтительно 50~300 мг. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно, от одного до шести раз).
Изобретение иллюстрируется, но не ограничивается следующими примерами.
Пример 1. Синтез соединений общей формулы 1а. К раствору 1 ммоль (198 мг) 1,3-диэтил-5,6-диаминоурацила 3 и 15 ммоль кислоты 4 в 8 мл диметилформамида добавляли 1,5 ммоль (372 мг) о-(бензотриазол-1-ил)-N,N,N',N'-тетрагидроурония тетрафторбората.
Смесь перемешивали ночь при комнатной температуре, выливали в воду, экстрагировали этилацетатом. Органический слой промывали водой, высушивали над безводным сульфатом натрия, упаривали досуха. Остаток хроматографировали на силикагеле смесью дихлорметана с метанолом. Получали с выходом 26-92% амид 6, который (0,1 ммоль) суспендировали в 8 мл метанола, добавляли 8 мл 4N водного раствора гидроксида натрия. Смесь перемешивали 1,5 часа при 80-90°С. Охладили, нейтрализовали 18% водным раствором соляной кислоты до рН 7-8. Выпавший осадок феноксиуксусной кислоты, включающей 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, общей формулы 1а, отфильтровали (выход 42-92%).
{4-[(Е)-2-(1,3-Диэтил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусная кислота 1а.1=(1.2.0(1)) - LC MS: найдено 415 (М+1), вычислено 415 (М+1). {4-[(Е)-2-(1,3-Диэтил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-уксусная кислота 1а.2=(1.2.0(2)) - LC MS: найдено 385 (М+1), вычислено 385 (М+1).
Пример 2. Синтез соединений общей формулы 1b. Смесь кислоты 1а (0,44 ммоль), 4 мл диметилформамида 132 г (1 ммоль) прокаленного карбоната калия и 2,2 ммоль йодистого алкила перемешивали 2 часа при 70°С, добавляли еще 1,1 ммоль йодистого алкила, еще перемешивали 2 часа при 70°С. Охлаждали, добавляли воду, отфильтровывали выпавший осадок, который растворяли в подходящем растворителе, полученный раствор фильтровали через слой силикагеля, а полученный фильтрат упаривали в вакуме. Получали с выходом 31-54% эфир феноксиуксусной кислоты, включающий 2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-иловый фрагмент, общей формулы 1b.
Метиловый эфир {4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1b.1=(1.3.16). LC MS: найдено 443 (М+1), вычислено 443 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 7,61 (д, J=16,4 Гц, 1Н), 7,45 (с, 1Н), 7,24 (м, 2Н), 6,90 (д, J=8 Гц, 1Н), 4,83 (с, 2Н), 4,05 (м, 5Н), 3,89 (м, 5Н), 1,25 (т, J=6,4 Гц, 3Н), 1,12 (т, J=6,8 Гц, 3Н).
Метиловый эфир {4-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-уксусной кислоты 1b.2=(1.3.2). LC MS: найдено 412 (М+1), вычислено 412 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 7,73 (д, J=8 Гц, 1Н), 7,62 (д, J=15,6 Гц, 1Н), 7,19 (д, J=16 Гц, 1Н), 6,98 (д, J=8,8 Гц, 2Н), 4,86 (с, 2Н), 4,06 (к, J=6,4 Гц, 2Н), 4,01 (с, 3Н), 3,91 (к, J=6,8 Гц, 2Н), 3,71 (с, 3Н), 1,25 (т, J=6,8 Гц, 3Н), 1,12 (т, J=6,8 Гц, 3Н).
Метиловый эфир {5-[(Е)-2-(1,3-диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1H-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусной кислоты 1b.3=(1.1.1). LC MS: найдено 443 (М+1), вычислено 443 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 7,58 (д, J=15,2 Гц, 1Н), 7,37 (м, 2Н), 7,18 (д, J=15,6 Гц, 1Н), 7,03 (д, J=8 Гц, 1Н), 4,87 (с, 2Н), 4,06 (к, J=7,2 Гц, 2Н), 4,01 (с, 3Н), 3,91 (к, J=7,2 Гц, 2Н), 3,82 (с, 3Н), 3,72 (с, 3Н), 1,25 (т, J=7,2 Гц, 3Н), 1,13 (т, J=6,8 Гц, 3Н).
Этиловый эфир [4-[(1,3-диэтил-2,3,6,7-тетрагидро-7-метил-2,6-диоксо-1Н-пурин-8-ил)этинил]-2-метоксифенокси]-уксусной кислоты (1.4.1). LCMS (М+1) 455 1Н ЯМР (DMSO-D6, 400 МГц) δ 1.22 (т, J1=7.00, J2=2.88, 9H), 3.84 (т, J1=9.40, J2=0.25, 3Н), 3.95 (д, J=13.35, 3Н), 4.05 (д, J=7.06, 4H), 4.23 (д, J=4.15, 2Н), 4.69 (т, J1=16.30, J2=0.17, 2Н), 6.84 (т, J1=2.00, J2=0.72, 1Н), 6.97 (м, 2Н).
Этиловый эфир [2-хлор-4-[(Е)-2-(1,3-диэтил-2,3,6,7-тетрагидро-7-метил-2,6-диоксо-1Н-пурин-8-ил)этенил]фенокси]-уксусной кислоты (1.3.14). LCMS (М+1) 461 1H ЯМР (DMSO-D6, 400 МГц) δ 1.22 (уш.т, J1=7.00, J2=2.88, 9H), 4.00 (д, J=13.35, 3Н), 4.07 (д, J=7.06, 4H), 4.25 (д, J=4.15, 2Н), 4.61 (т, J1=16.30, J2=0.17, 2Н), 6.97 (д, J=0.87, 1Н), 7.01 (т, J1=15.60, J2=0.60, 1Н), 7.31 (м, 1Н), 7.44 (м, 1Н), 7.45 (т, J1=8.60, J2=2.20, 1Н).
Пример 3. Синтез соединений общей формулы 1с. К раствору 0,34 ммоль эфира 1b в 2 мл метанола прибавили 0,4 мл 1Н раствора гидроксида лития. Смесь перемешивали 16 часов при комнатной температуре. Упаривали досуха, остаток растворяли в воде, промывали эфиром. Осторожно добавляли 6Н раствор соляной кислоты до рН 7-8, отфильтровывали выпавший осадок. Получают кислоту 1с с выходом 41-71%.
{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-уксусная кислота (1.3.15). LC MS: найдено 429 (М+1), вычислено 429 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 7,63 (д, J=15,6 Гц, 1Н), 7,44 (с, 1Н), 7,26 (д, J=8 Гц, 1Н), 7,22 (д, J=16 Гц, 1Н), 6,87 (д, J=8,4 Гц, 1Н), 4,72 (с, 2Н), 4.06 (к, J=7,2 Гц, 2Н), 4,02 (с, 3Н), 3,91 (к, J=7,2 Гц, 2Н), 3,86 (с, 3Н), 1,25 (т, J=6,8 Гц, 3Н), 1,12 (т, J=6,4 Гц, 3Н).
Пример 4. Общий способ получения амидов 1d. В пробирку, содержащую суспензию 0,226 ммоль метилового эфира общей формулы 1bb в 2 мл метанола или этанола насыщали или прибавляли соответствующее количество амина. Пробирку закрывали, грели 10 часов при температуре 50°С, затем охладили, отфильтровали выпавший осадок. Получали амид Id с выходом 29-58%.
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-фенокси}-ацетамид 1d.1=(1.3.3). LC MS: найдено 398 (М+1), вычислено 398 (M+1).
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-ацетамид 1d.2=(1.3.18). LC MS: найдено 428 (M+1), вычислено 428 (M+1). 1H ЯМР (DMSO-D6, 400 МГц) δ: 7,62 (д, J=15,6 Гц, 1Н), 7,33 (м, 5Н), 6,93 (д, J=8,8 Гц, 1Н), 4,48 (с, 2Н), 4,05 (м, 5Н), 3,91 (м, 5Н), 1,26 (т, J=6,4 Гц, 3Н), 1,13 (т, J=6,4 Гц, 3Н).
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-метил-ацетамид 1d.3=(1.3.19). LC MS: найдено 442 (M+1), вычислено 442 (M+1). 1H ЯМР (DMSO-D6, 400 МГц) δ: 7,62 (д, J=15,6 Гц, 1Н), 7,33 (м, 5Н), 6,93 (д, J=8,8 Гц, 1Н), 4,48 (с, 2Н), 4,05 (м, 5Н), 3,91 (м, 5Н), 1,26 (т, J=6,4 Гц, 3Н), 1,13 (т, J=6,4 Гц, 3Н).
2-{4-[(Е)-2-(1,3-Диэтил-7-метил--2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-этил-ацетамид 1d.4=(1.3.20). LC MS: найдено 456 (M+1), вычислено 456 (M+1). 1H ЯМР (DMSO-D6,400 МГц) δ: 7,92 (м, 1Н), 7,62 (д, J=15,6 Гц, 1Н), 7,44 (с, 1Н), 7,24 (м, 2Н), 6,92 (д, J=7,6 Гц, 1Н), 4,48 (с, 2Н), 4,04 (м, 5Н), 3,90 (м, 5Н), 3,16 (т, J=5,6 Гц, 2Н), 1,26 (т, J=6 Гц, 3Н), 1,12 (т, J=6 Гц, 3Н), 1,04 (т, J=6,4 Гц, 3Н).
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N,N-диметил-ацетамид 1d.5=(1.3.21). LC MS: найдено 456 (M+1), вычислено 456 (M+1). 1H ЯМР (DMSO-D6, 400 МГц) δ: 7,62 (д, J=15,6 Гц, 1Н), 7,43 (с, 1Н), 7,22 (м, 2Н), 6,86 (д, J=8 Гц, 1Н), 4,83 (с, 2Н), 4,06 (к, J=5,6 Гц, 2Н), 4,02 (с, 3Н), 3,91 (к, J=6,8 Гц, 2Н), 3,87 (с, 3Н), 3,01 (с, 3Н), 2,85 (с, 3Н), 1,26 (т, J=6,4 Гц, 3Н), 1,13 (т, J=6,8 Гц, 3Н).
Пример 5. Общий способ получения амидов 1d. К смеси 30,5 мг (0,226 ммоль, 2 экв.) 1-гидроксибензотриазола, 43,3 мг (0,226 ммоль, 2 экв.) N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорида и 45 мг (0,113 ммоль, 1 экв.) исходной кислоты N-(3-диметиламинопропил)-N'-этилкарбодиимид гидрохлорида 1с добавляли в 1,8 мл ДМФА. Полученную смесь перемешивали при комнатной температуре 1 час. Затем добавляли последовательно 0,170 ммоль (1,5 экв.) амин 6 и необходимое количество диизопропилэтиламина. Реакционную массу выдерживали 12 ч при комнатной температуре, затем смешивали ее с 50 мл 10% Na2CO3. Если продукт выпадал в виде осадка, осадок отфильтровывали, промывали 2 раза водой на фильтре, сушили на воздухе. В случае мелкодисперсного осадка, отделение проводили центрифугированием. Если продукт получался в виде масла, проводили экстракцию дихлорметаном, органическую фазу промывали 1 раз водой, осушали безводным Na2SO4 и упаривали на роторном испарителе. Дальнейшую очистку проводили либо перекристаллизацией из этанола, либо колоночной хроматографией, используя системы растворителей хлороформ - метанол в соотношениях от 40:1 до 10:1. Получали амиды 1d с выходом 26-89%.
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N,N-ди-(2-метоксиэтил)-ацетамид 1d.6=(1.3.4). LC MS: найдено 514 (М+1), вычислено 514 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 7,71 (д, J=8,4 Гц, 2Н), 7,61 (д, J=15,6 Гц, 1Н), 7,18 (д, J=16 Гц, 1Н), 6,92 (д, J=8,8 Гц, 2Н), 4,93 (с, 2Н), 4,06 (к, J=7,2 Гц, 2Н), 4,00 (с, 3Н), 3,91 (к, J=6,8 Гц, 2Н), 3,53 (м, 4Н), 3,46 (м, 2Н), 3,42 (м, 2Н), 3,33 (с, 3Н), 3,24 (с, 3Н), 1,25 (т, J=7,2 Гц, 3Н), 1,12 (т, J=6,4 Гц, 3Н).
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-(2-диметиламиноэтил)-N-метил-ацетамид 1d.7=(1.3.5). LC MS: найдено 483 (М+1), вычислено 483 (М+1). LCMS (М+1) 483 1Н ЯМР (DMSO-D6, 400 МГц) δ 1.22 (уш.т, J1=7.00, J2=2.88, 6H), 2.17 (т, J1=13.35, J2=0.98, 6H), 2.43 (т, J1=13.29, J2=6.21, 2Н), 3.00 (д, J=14.23, 3Н), 3.62 (д, J=8.79, 2Н), 4.00 (д, J=13.35, 3Н), 4.07 (д, J=7.06, 4Н), 4.63 (т, J1=14.95, J2=0.23, 2Н), 6.91 (м, 2Н), 6.94 (м, 1Н), 7.33 (д, J=0.25, 1Н), 7.46 (д, J=8.60, 2Н).
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-(3-морфолин-4-илпропил)-ацетамид 1d.8=(1.3.6). LC MS: найдено 525 (М+1), вычислено 525 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 8,11 (т, J=6,4 Гц, 1Н), 7,75 (д, J=8,4 Гц, 2Н), 7,61 (д, J=15,6 Гц, 1Н), 7,21 (д, J=15,6 Гц, 1Н), 7,00 (д, J=8,4 Гц, 2Н), 4,52 (с, 2Н), 4,05 (к, J=6,4 Гц, 2Н), 4,01 (с, 3Н), 3,92 (к, J=6,8 Гц, 2Н), 3,54 (м, 4Н), 3,17 (к, J=6,4 Гц, 2Н), 2,28 (м, 4Н), 2,24 (т, J=6,8 Гц, 2Н), 1,58 (п, J=6,8 Гц, 2Н), 1,25 (т, J=7,2 Гц, 3Н), 1,12 (т, J=6,8 Гц, 3Н).
1,3-Диэтил-8-((Е)-2-{4-[2-(4-изопропил-пиперазин-1-ил)-2-оксо-этокси]-фенил}-винил)7-метил-3,7-дигидро-пурин-2,6-дион 1d.9=(1.3.7). LC MS: найдено 509 (М+1), вычислено 509 (М+1). LCMS (М+1) 509 1H ЯМР (DMSO-D6, 400 МГц) δ 1.10 (т, J1=6.28, J2=1.13, 6Н), 1.22 (уш.т, J1=7.00, J2=2.88, 6H), 2.40 (м, 2Н), 2.48 (м, 2Н), 2.70 (м, 1Н), 3.38 (м, 2Н), 3.45 (м, 2Н), 4.00 (т, J1=13.35, J2=0.25, 3Н), 4.05 (д, J=7.06, 4H), 4.63 (т, J1=14.00, J2=0.23, 2Н), 6.90 (т, J1=2.20, J2=0.50, 2Н), 6.94 (т, J1=15.60, J2=0.70, 1Н), 7.29 (д, J=0.25, 1Н), 7.45 (т, J1=8.60, J2=0.50, 2Н).
8-((Е)-2-{4-[2-(1,6-диметил-3,4-дигидро-1Н-пирроло[1,2-а]пиразин-2-ил)-2-оксо-этокси]-нил}-винил)-1,3-диэтил-7-метил-3,7-дигидро-пурин-2,6-дион 1d.10=(1.3.8). LC MS: найдено 531 (М+1), вычислено 531 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 7,73 (д, J=8,4 Гц, 2Н), 7,61 (д, J=16 Гц, 1Н), 7,19 (д, J=15,6 Гц, 1Н), 6,99 (м, 2Н), 5,73 (с, 2Н), 5,44, 5,24 (2 м, 1Н), 4,99 (м, 2Н), 4,56, 4,34 (2 м, 1Н), 3,42 (м, 1Н), 4,06 (м, 2Н), 4,00 (м, 3Н), 3,90 (м, 2Н), 3,76 (м, 1Н), 3,57 (м, 1Н), 2,12 (с, 3Н), 1,48, 1,32 (2 м, 3Н), 1,25 (т, J=7,2 Гц, 3Н), 1,14 (т, J=6 Гц, 3Н).
1,3-Диэтил-7-метил-8-[(Е)-2-(4-{2-оксо-2-[4-(1,3,6-триметил-2,4-диоксо-1,2,3,4-тетрагидро-пиримидин-5-ил)-пиперазин-1-ил]-этокси}-фенил)-винил]-3,7-дигидро-пурин-2,6-дион 1d.11=(1.3.9). LC MS: найдено 619 (М+1), вычислено 619 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 8,61 (с, 1Н), 7,73 (д, J=8,4 Гц, 2Н), 7,62 (м, 2Н), 7,34 (с, 1Н), 7,28 (с, 1Н), 7,19 (м, 2Н), 6,99 (д, J=8,4 Гц, 2Н), 4,96 (с, 2Н), 4,05 (к, J=7,2 Гц, 2Н), 4,00 (с, 3Н), 3,91 (к, J=6,4 Гц, 2Н), 3,85 (с, 3Н), 3,77 (м, 2Н), 3,69 (м, 2Н), 3,61 (м, 4H), 1,2 (т, J=7,2 Гц, 3Н), 1,12 (т, J=6,4 Гц, 3Н).
1,3-Диэтил-8-{(Е)-2-[4-(2-{4-[6-(2-метокси-5-фтор-фенил)-пиримидин-4-ил]-пиперазин-1-ил}-2-оксо-этокси)-фенил]-винил}-7-метил-3,7-дигидро-пурин-2,6-дион 1d.12=(1.3.10). LC MS: найдено 669 (М+1), вычислено 669 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 8,61 (с, 1Н), 7,73 (д, J=8,4 Гц, 2Н), 7,62 (м, 2Н), 7,34 (с, 1Н), 7,28 (с, 1Н), 7,19 (м, 2Н), 6,99 (д, J=8,4 Гц, 2Н), 4,96 (с, 2Н), 4,05 (к, J=7,2 Гц, 2Н), 4,00 (с, 3Н), 3,91 (к, J=6,4 Гц, 2Н), 3,85 (с, 3Н), 3,77 (м, 2Н), 3,69 (м, 2Н), 3,61 (м, 4H), 1,2 (т, J=7,2 Гц, 3Н), 1,12 (т, J=6,4 Гц, 3Н).
1,3-Диэтил-7-метил-8-[(Е)-2-(4-{2-оксо-2-[4-(6-фенил-пиримидин-3-ил)-пиперазин-1-ил]-этокси}-фенил)-винил]-3,7-дигидро-пурин-2,6-дион 1d.13=(1.3.11). LC MS: найдено 621 (М+1), вычислено 621 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 8,03 (д, J=7,2 Гц, 2Н), 7,98 (д, J=10 Гц, 1Н), 7,73 (д, J=7,2 Гц, 2Н), 7,62 (д, J=15,2 Гц, 1Н), 7,49 (м, 3Н), 7,41 (м, 1Н), 7, 19 (д, J=15,6 Гц, 1Н), 7,00 (д, J=6,8 Гц, 2Н), 4,98 (с, 2Н), 4,06 (м, 2Н), 4,00 (с, 3Н), 3,91 (м, 2Н), 3,78 (м, 2Н), 3,65 (м, 6Н), 1,25 (м, 3Н), 1,18 (м, 3Н).
8-{(Е)-2-[4-(2-{4-[3-(3,4-Диметокси-фенил)-[1,2,4]оксадиазол-5-илметил]-пиперазин-1-ил}-2-оксо-этокси)-фенил]-винил}-1,3-диэтил-7-метил-3,7-дигидро-пурин-2,6-дион 1d.14=(1.3.12). LC MS: найдено 685 (М+1), вычислено 685 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ: 7,70 (д, J=8,4 Гц, 2Н), 7,60 (д, J=12,4 Гц, 2Н), 7,48 (с, 1Н), 7,17 (д, J=15,6 Гц, 1Н), 7,12 (д, J=9,2 Гц, 1Н), 6,95 (д, J=8 Гц, 2Н), 4,88 (с, 2Н), 4,02 (м, 7Н), 3,91 (м, 2Н), 3,82 (м, 6Н), 3,50 (м, 4Н), 2,61 (м, 2Н), 2,53 (м, 2Н), 1,25 (м, 3Н), 1,10 (м, 3Н).
2-{4-[(Е)-2-(1,3-Диэтил-7-метил-2,6-диоксо-2,3,6,7-тетрагидро-1Н-пурин-8-ил)-винил]-2-метокси-фенокси}-N-(3,4,5-триметоксифенил)-ацетамид 1d.15=(1.3.13). LC MS: найдено 564 (М+1), вычислено 564 (М+1). 1Н ЯМР (DMSO-D6, 400 МГц) δ:. 9,98 (уш, 1Н), 7,68 (м, 3Н), 7,11 (м, 5Н), 4,71 (с, 2Н), 3,99 (м, 6Н), 3,71 (м, 10Н), 1,23 (м, 3Н), 1,10 (м, 3Н).
2-[4-[(1,3-Диэтил-2,3,6,7-тетрагидро-7-метил-2,6-диоксо-1Н-пурин-8-ил)этинил]-2-метоксифенокси]-ацетамид, (1.4.2). LCMS (М+1) 426 1Н ЯМР (DMSO-D6, 400 МГц) δ 1.22 (т, J1=7.00, J2=2.88, 6Н), 3.84 (т, J1=9.40, J2=0.25, 3Н), 3.95 (д, J=13.35, 3Н), 4.02 (д, J=7.06, 4Н), 4.55 (т, J1=15.10, J2=0.17, 2Н), 6.96 (м, 1Н), 7.03 (т, J1=2.00, J2=0.72, 1Н), 7.15 (д, J=8.00, 1Н), 7.42 (т, J1=2.60, J2=1.33, 2Н).
2-[4-[(1,3-Диэтил-2,3,6,7-тетрагидро-7-метил-2,6-диоксо-1Н-пурин-8-ил)этинил]-2-метоксифенокси]-N-метил-ацетамид (1.4.3). LCMS (М+1) 440 1H ЯМР (DMSO-D6, 400 МГц) δ 1.23 (т, J1=7.00, J2=2.88, 6Н), 2.68 (д, J=14.23, 3Н), 3.84 (т, J1=9.40, J2=0.25, 3Н), 3.95 (д, J=13.35, 3Н), 4.05 (д, J=7.06, 4Н), 4.45 (т, J1=14.00, J2=0.23, 2Н), 6.97 (м, 1Н), 7.03 (т, J1=2.00, J2=0.72, 1Н), 7.13 (д, J=8.00, 1Н), 7.85 (м, 1Н).
1-[[4-[(1,3-Диэтил-2,3,6,7-тетрагидро-7-метил-2,6-диоксо-1Н-пурин-8-ил)этинил]-2-метоксифенокси]ацетил]-пиперазин (1.4.4). LCMS (М+1) 495 +Н ЯМР (DMSO-D6, 400 МГц) δ 1.23 (т, J1=7.00, J2=2.88, 6Н), 2.82 (м, 2Н), 2.98 (м, 2Н), 3.27 (м, 2Н), 3.35 (м, 2Н), 3.68 (м, 1Н), 3.84 (т, J1=9.40, J2=0.25, 3Н), 3.95 (д, J=13.35, 3Н), 4.04 (д, J=7.06, 4Н), 4.73 (т, J1=14.00, J2=0.23, 2Н), 6.96 (м, 1Н), 7.03 (т, J1=2.00, J2=0.72, 1Н), 7.13 (д, J=8.00, 1Н).
2-[4-[(1,3-диэтил-2,3,6,7-тетрагидро-7-метил-2,6-диоксо-1Н-пурин-8-ил)этинил]-2-метоксифенокси]-N-3-пиридинил-ацетамид (1.4.5). LCMS (М+1) 503 1Н ЯМР (DMSO-D6, 400 МГц) δ 1.22 (т, J1=7.00, J2=2.88, 6Н), 3.84 (т, J1=9.40, J2=0.25, 3Н), 3.95 (д, J=13.35, 3Н), 4.06 (д, J=7.06, 4H), 4.58 (м, 2Н), 6.97 (м, 2Н), 7.03 (т, J1=2.00, J2=0.72, 1H), 7.13 (д, J=8.00, 1H), 7.32 (м, 1H), 8.32 (т, J1=7.70, J2=1.30, 1H), 8.39 (д, J=4.60, 1H), 8.60 (м, 1H).
Пример 6. Изучение антагонистической активности соединений общей формулы 1 и их фармацевтически приемлемых солей по отношению к аденозиновому A2A рецептору. Антагонистическую активность новых соединений общей формулы 1 и их фармацевтически приемлемых солей по отношению к аденозиновому А2А рецептору проводили ex vitro в функциональном тесте на клетках. В эксперименте использовали клетки линии ValiScreen cell line (PerkinElmer, США), экспрессирующей рекомбинантный человеческий аденозиновый рецептор типа A2A. При стимуляции рецепторов в этих клеток агонистом CGS 21680 (Tocris) активируется аденилатциклаза, что, в свою очередь, приводит к увеличению синтеза внутриклеточного циклического аденозинмонофосфата (цАМФ). Количество цАМФ определялось с помощью технологии LANCE (LANCE Ultra cAMP kit, PerkinElmer). По способности испытуемых соединений снижать количество цАМФ, синтезируемого в присутствии CGS 21680, оценивали их антагонистическую активность. В качестве стандарта (соединения сравнения) использовали описанный в литературе антагонист KW 6002 (Axon Medchem, Netherlands).
Клетки культивировали в среде DMEM (ПанЭко, Россия) с добавками 10% FBS (Biological Industries), смеси пенициллин/стрептомицина (ПанЭко) и G418 (Sigma) при температуре 37°С в атмосфере 5% CO2. Перед экспериментом клетки снимали с культурального флакона раствором Версена (ПанЭко) и суспендировали в буфере SB2 (среда Хэнкса+5 мМ HEPES (рН 7,4)+0,1% BSA+200 uM Ro-20-1734+2U/mL ADA (adenosine deaminase)) до плотности 0,2 миллиона клеток в миллилитре. К клеточной суспензии добавляли 1:150 (по объему) ULightTM-anti-cAMP Antibody (PerkinElmer) и эту смесь разливали в белые 384-луночные планшеты (PerkinElmer) по 5 мкл (1000 клеток) в каждую лунку.
Тестируемые соединения растворяли в ДМСО до концентрации 6.32 мМ и готовили 3.16-кратные серийные разведения в ДМСО. Приготовленные серийные разведения разбавляли в 50 раз буферным раствором SB1 (среда Хэнкса+5 мМ HEPES (рН 7,4)+0,1% BSA). Полученные растворы соединений в SB1 буфере смешивали в пропорции 1:1 с раствором CGS 21680 (12.64 нМ), предварительно приготовленным в буфере SB3 (SB1+0.1% Pluronic F127). Полученные смеси испытуемых соединений с агонистом добавляли (по 5 мкл в дупликатах) в лунки плашки, содержащие по 5 мкл клеток (как описано выше) и плашки инкубировали 30 минут при комнатной температуре. Каждая плашка содержала также по 16 лунок для каждого контроля (МАКС и МИН). МАКС - клетки с 3.16 нМ CGS 21680 (концентрация агониста, соответствующая ЕС90, то есть концентрации, вызывающей 90% активность клеток); сигнал от этих лунок использовался в расчетах как 100% активность (0% ингибирования). МИН - клетки со смесью 3.16 нМ CGS 21680 и 2 мкМ KW 6002 (концентрация антагониста, соответствующая IC100, то есть концентрации, вызывающей 100% подавление активности клеток); сигнал от этих лунок использовался в расчетах как 0% активность (100% ингибирования). Кроме этого, каждая плашка содержала лунки (в 4-х повторах), где клетки обрабатывались агонистом (CGS 21680) при разных его концентрациях. Конечная концентрация ДМСО во всех лунках равнялась 1%.
Образующийся в клетках цАМФ определяли количественно при помощи набора LANCE Ultra cAMP kit (PerkinElmer, США) в соответствии с методикой, рекомендованной производителем. Флуоресцентный сигнал измеряли на приборе Victor3V (PerkinElmer), снабженном встроенной программой для измерения LANCE High Count.
Кажущееся сродство тестируемых соединений определяли по формуле
Ki=IC50/(1+L/KD),
где IC50 - концентрация антагониста, при которой активность аденилатциклазы составляет 50% от максимальной, L - концентрация CGS 21680, при которой проводятся измерения (3.16 nM) и Ко - кажущаяся константа сродства CGS 21680, количественно соответствующая величине EC50 (концентрация полумаксимальной стимуляции клеток) для CGS 21680 и определенная по кривым стимуляции накопления цАМФ в клетках при разных концентрациях агониста.
В таблице 1 представлены данные по активности Кi некоторых представителей соединений общей формулы 1.
Пример 7. Радиолигандный анализ взаимодействия соединений общей формулы 1 с аденозиновыми A1, A2A, A2B и А3 рецепторами. Радиолигандный анализ взаимодействия соединений общей формулы 1 с аденозиновыми A1, A2A, A2B и А3 рецепторами проводили для определения селективности взаимодействия соединений общей формулы 1 с аденозиновым А2А рецептором. При определении взаимодействия исследуемых соединений с аденозиновым A2A рецептором использовали мембранные препараты, полученные из эмбриональных клеток почек человека, экспрессирующих рекомбинантный человеческий А2А рецептор. Экспрессия рецептора составляла 7 пмоль/мг белка. В качестве радиолиганда использовали [3H]CGS 21680 при концентрации 0.05 мкМ. Растворы испытуемых соединений готовили так же, как описано в процедуре для функционального теста с тем различием, что вместо среды SB1, использовали буфер следующего состава: 50 mM Tris-HCl, рН 7.4, 10 mM MgCl2, 1 mM EDTA, 2 U/mL Adenosine Deaminase. Мембранные препараты инкубировали в присутствии смеси тестируемых соединений и [3H]CGS 21680 в течение 90 мин при 25°С и смеси фильтровали на стекломикроволоконных фильтрах GF (Millipor, USA). Радиоактивность на фильтрах определяли с помощью жидкостинцилляционного счетчика MicroBeta (PerkinElmer, USA). Неспецифическое связывание измеряли в присутствии 50 мкМ NECA, которое составляло не более 15% от общего связывания. Сродство тестируемых соединений определяли по формуле
Ki=IC50/(1+L/KD),
где IC50 - концентрация антагониста, при которой связывание [3H]CGS 21680 снижается до 50% от максимального, L - концентрация [3H]CGS 21680, при которой проводятся измерения (50 nM), и KD - константа сродства [3H]CGS 21680, количественно соответствующая величине ЕС50 (концентрация полумаксимального связывания) для [3H]CGS 21680, и определенная по кривым радиоактивного связывания при разных концентрациях [3H]CGS 21680 (KD=64 нМ).
Аналогично исследовали взаимодействия новых соединений общей формулы 1 с аденозиновыми A1, A2B и А3 рецепторами в условиях, представленных ниже.
|
|
|
Радиолигандный анализ взаимодействия соединений общей формулы 1 с аденозиновыми A1, A2A, A2B и А3 рецепторами показал их высокую селективность по отношению к аденозиновому А2А рецептору (Таблица 2).