Результат интеллектуальной деятельности: СРЕДСТВО, ОБЛАДАЮЩЕЕ РЕГЕНЕРАТИВНОЙ АКТИВНОСТЬЮ
Вид РИД
Изобретение
Изобретение относится к медицине, конкретно к фармакологии и клеточным технологиям.
Известно большое количество средств, обладающих регенеративной активностью (метилурацил, солкосерил, облепиховое масло, натрия нуклеинат и др.) [1, 2].
Недостатком данных средств является зачастую их недостаточная эффективность [2].
Задачей, решаемой настоящим изобретением, является расширение арсенала средств, обладающих выраженной регенеративной активностью.
Поставленная задача достигается применением зонгорина в качестве средства, обладающего регенеративной активностью.
Новым в предлагаемом изобретении является использование в качестве средства, обладающего регенеративной активностью, зонгорина.
Используемое оригинальное средство - зонгорин - разработано и получено ФГБУ «НИИ фармакологии» СО РАМН (г. Томск) совместно с Национальным исследовательским Иркутским Государственным Техническим Университетом (г. Иркутск) и представляло собой 0,00025% водный раствор данного алкалоида. Зонгорин извлекался и идентифицировался из растительного сырья (травы растений семейства лютиковых) в виде свободных оснований экстракцией стандартным методом [3].
Полученные в последние годы сведения о свойствах и закономерностях жизнедеятельности поли(мульти)потентных клеток-предшественников открыли возможность развития нового направления в лечении многих заболеваний - клеточной терапии [4]. При этом наиболее физиологичным подходом к решению задач регенеративной медицины является фармакологическая стимуляция постнатальных эндогенных стволовых клеток (СК) [5]. Причем активация последних может являться следствием как прямого воздействия фармакологических агентов на прогениторные элементы, так и результатом стимуляции клеток микроокружения тканей, опосредованно определяющей ускоренное течение репаративных процессов [5, 6].
Ранее нами было показано ускорение заживления ран кожи комплексными экстрактами и алкалоидной фракцией живокости высокой [7]. При этом максимальный ранозаживляющий эффект наблюдался при использовании суммы алкалоидов, среди которых доминирующим является элатин [8]. В то же время с помощью метода тонкослойной хроматографии в алкалоидной фракции было установлено содержание других алкалоидов, в том числе зонгорина. Зонгорин (C22H33NO3),
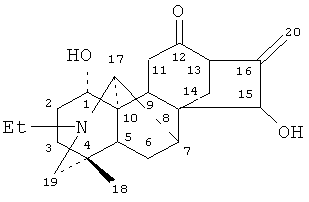
представляет собой гетероциклическое азотсодержащее органическое соединение растительного происхождения. Чаще всего его извлекают из растений рода Аконит, хотя он встречается и в других растениях [7, 9]. Он является типичным антидепрессантом [10], обладает слабым периферическим М- и Н-холинолитическим действием, адренопозитивным и центральным М-холинонегативным эффектом. При этом влияние зонгорина на процессы регенерации тканей не изучено. Эксперимент показал непредсказуемые результаты.
Факт применения зонгорина с достижением нового технического результата, заключающегося в стимуляции регенерации тканей, для специалиста не является очевидным.
Новые свойства не вытекают явным образом из уровня техники в данной области и не обнаружены в патентной и научно-технической литературе.
Предлагаемое изобретение может быть использовано в медицине.
Исходя из вышеизложенного, следует считать заявляемое техническое решение соответствующим критериям: «Новизна», «Изобретательский уровень», «Промышленная применимость».
Эксперименты были проведены на 92 беспородных мышах-самцах. Животные получены из питомника отдела экспериментального биомедицинского моделирования ФГБУ «НИИ фармакологии» СО РАМН.
Исследования проводили в соответствии с правилами лабораторной практики (GLP), Приказом МЗСР РФ №708н от 23.08.2010 «Об утверждении правил лабораторной практики», Федеральным Законом от 12 апреля 2010 г. №61-ФЗ «Об обращении лекарственных средств», «Руководством по экспериментальному (доклиническому) изучению новых фармакологических веществ» (Москва, 2005).
Пример 1
Регенеративную активность предлагаемого средства и механизмы его действия изучали на модели плоскостной кожной раны [11]. На депилированном участке спины у мышей под легким эфирным наркозом вырезали лоскут кожи размером 10×10 мм. Для моделирования более длительного заживления струп с экспериментальной раны регулярно (через сутки) снимали.
Предлагаемое средство получали из травы аконита байкальского и живокости высокой. Надземная часть растений, собранная в период цветения в Иркутской области, измельчалась до размера частиц менее 5 мм, обрабатывалась раствором карбоната натрия и подвергалась непрерывной экстракции хлороформом в течение 5 суток. Хлороформный экстракт упаривали до небольшого объема и тщательно экстрагировали 5% серной кислотой. Кислотную вытяжку подщелачивали карбонатом натрия до рН 9-10 и последовательно экстрагировали сначала эфиром, затем хлороформом. Эфирный экстракт упаривали досуха, растворяли в небольшом количестве эфира и хроматографировали на дезактивированной окиси алюминия в системе гексан-ацетон (90→50%). Эфирорастворимую фракцию подвергли дробной экстракции буферными растворами с увеличивающимися значениями рН. Эфирный раствор, оставшийся после экстракции наиболее щелочным буфером, упаривали досуха и хроматографировали на окиси алюминия в системе гексан-метанол до элюции зоноргина, происходящей после выхода напелина. Вещество растворяли в дистиллированной воде до конечной концентрации 0,00025%.
Полученное средство применяли наружно, начиная с первого дня после моделирования раны, ежедневно в течение всего периода заживления. Раствор наносили в объеме 30 мкл. В качестве средств сравнения использовали гель «Солкосерил» (Ай Си Эн Швейцария АГ, Швейцария) и «Облепиховое масло» (ОАО Нижфарм, Россия), которые применяли по той же схеме и в эквивалентном количестве, что и раствор зонгорина.
Критериями стимулирующего регенерацию действия служили средний диаметр раны и результаты гистологического исследования биоптатов кожи мышей, полученных на 3, 5 и 15-е сутки из края раневого дефекта. Биопсийные образцы раневого дефекта кожи окрашивали гематоксилин-эозином, В каждом препарате оценивали: рельеф регенерата кожи, степень и характер инфильтрации, наличие и выраженность отека, количество новообразованных сосудов, волосяных фолликулов и потовых желез. Изучали такие патоморфологические процессы, как акантоз, гиперкератоз, дискератоз [12]. На 3-и и 5-е сут методом клонирования определяли содержание мезенхимальных клеток-предшественников (КОЕ-Ф) в раневой поверхности [13], а также методом колониеобразования в тест-системе изучали продукцию гуморальных факторов стромальными клетками кожи (колониеобразующую активность супернатантов адгезирующих клеток с раневой поверхности в отношении КОЕ-Ф костного мозга) [13]. Кроме того, определяли прямое влияние зонгорина на КОЕ-Ф. Для этого его вносили в культуру миелокариоцитов в концентрации 100 нМоль/мл, после чего на 7-е сут подсчитывали количество колоний [13]. Обработку результатов проводили методом вариационной статистики с использованием t критерия Стьюдента и непараметрического U критерия Манна-Уитни.
В ходе эксперимента заживление ран у контрольных животных отмечалось к 18 сут опыта. Использование зонгорина способствовало значительному ускорению процессов регенерации. Заживление дефекта в данном случае наблюдалось к 13 сут опыта, в то время как при применении средств сравнения таковое отмечалось лишь к 16 сут. При этом в опытной группе (зонгорин) имело место наиболее выраженное снижение размера ран. В данном случае величина исследуемого параметра на 3, 5 и 7-е сут уменьшалась на 11%, 13% и 18% от контроля соответственно (табл.1). Более того, зонгорин существенно увеличивал (на 86%) скорость заживления раны в начальные сроки эксперимента, которая в период с 1 по 3-й сут составляла 0,69 мм/сут, а в контроле - 0,37 мм/сут.
При гистологическом исследовании на 3-й день после воздействия во всех группах на поверхности раны обнаруживался лейкоцитарно-некротический слой, содержащий фибрин, под которым находился тонкий слой грануляционной ткани с большим количеством клеточных элементов: в основном нейтрофилов и макрофагов. Воспалительный процесс распространялся на нижележащий слой поперечнополосатых мышц. Межмышечные прослойки были отечны и инфильтрированы лейкоцитами. По краям раны отек и гиперемия дермы, разрастание эпидермиса, который содержал 8-10 слоев однородных, недифференцированных крупных клеток округлой формы и толстый роговой слой. На 5-е сут новообразованный эпителий по краям раны представлял собой пласт клеток неодинаковой толщины без вертикальной анизоморфности. Передний край эпителия был истончен и в виде клина наползал на рану, а в грануляционной ткани отмечалось большое количество капилляров, имеющих вертикальный ход. При этом наружное применение зонгорина и средств сравнения существенно снижало лейкоцитарную инфильтрацию краев раны, дермы и нижележащих тканей на 3-е сут опыта, но наиболее значимые изменения имели место при использовании предлагаемого средства. Кроме того, лишь использование зонгорина увеличивало на 5-е сут эксперимента количество фибробластов в слое грануляций, которые при этом образовывали значительные по размеру тяжи клеток.
При этом анализ морфологических процессов, протекающих в области раневого дефекта кожи мышей на 15-е сут, показал, что в контрольной группе имело место формирование неполноценного регенерата. В подавляющем большинстве случаев поверхностный эпителий наблюдался не на всем протяжении, встречались небольшие участки отслойки эпидермиса от дермы с наличием субэпидермальных щелей, отмечалось резкое утолщение эпителиального пласта с нечеткой дифференцировкой слоев и увеличение количества базального, зернистого и рогового слоев. Внутриэпителиально обнаруживались нейтрофильные лейкоциты с формированием микроабсцессов, наблюдались слабовыраженные явления акантоза, гипер- и дискератоза. Подлежащая ткань была представлена созревающими грануляциями с умеренной гистиоцитарно-лейкоцитарной инфильтрацией, явлением отека и очагами кровоизлияний в верхних слоях дермы. Во всех образцах в прилежащей к зоне дефекта ткани отмечается малое количество волосяных фолликулов и потовых желез. Регенерат кожи у животных контрольной группы характеризовался умеренным воспалением, что привело к усиленной пролиферации эпителия, для которой характерны атипические разрастания и изменения эпителия в виде акантоза, гипер- и дискератоза. Изучение гистоструктуры раневого дефекта в группе животных, получавших терапию зонгорином, показал во всех случаях формирование полноценного эпителизированного соединительнотканного рубца. В остальных образцах (группы сравнения) эпителиальный слой был резко неравномерный, с утолщением в зоне дефекта за счет клеток базального слоя. Подлежащая ткань - грануляционная, местами с очаговой умеренной нейтрофильной инфильтрацией. В области, прилежащей к дефекту, во всех образцах ткани отмечалось умеренное количество волосяных фолликулов и потовых желез. При этом количество животных, у которых произошла полная эпителизация при использовании средств сравнения, было значительно ниже, чем при применении предлагаемого средства, когда эпителизация наблюдалось в 100% случаев (табл.2).
Изучение механизмов регенеративного действия зонгорина выявило их выраженное влияние на резидентные клетки-предшественники. Применение алкалоида сопровождалось существенным увеличением числа КОЕ-Ф в раневой поверхности (табл.3). При этом значения данного показателя были наиболее высокими на 3-е сут опыта.
Аналогичные по характеру изменения регистрировались при изучении интенсивности дифференцировки родоначальных элементов. Зоноргин увеличивал индекс созревания (табл.4). Причем возрастание данного показателя наблюдалось на фоне повышения продукции ростовых факторов стромальными клетками кожи (табл.5). В то же время было выявлено и выраженное прямое влияние данного алкалоида на прогениторные клетки. Внесение зонгорина в культуру миелокариоцитов сопровождалось значительным увеличением выхода в метилцеллюлозной среде числа КОЕ-Ф (табл.6). Изучение влияния средств сравнения на данные параметры не выявило статистически значимых изменений их динамики (табл.3-6).
В целом, полученные результаты свидетельствуют о наличии выраженной регенеративной активности у зонгорина. При этом в основе его терапевтического действия лежит активация функций резидентных мезенхимальных предшественников (содержащих в своем составе, помимо стромальных прекурсоров, мультипотентные (истинные) СК, способные дифференцироваться в эпителиоциты [6]), связанная с прямым влиянием алкалоида на предшественники и повышением выработки ростовых факторов стромальными клетками кожи. Выявленная специфика механизмов действия данного алкалоида указывает на высокую перспективность разработки на его основе средства для регенеративной медицины [6].
|
|
|
|
|
|
Источники информации
1. Машковский М.Д. Лекарственные средства: 15-е изд. - М.: OO «Изд-во Новая Волна», 2008. - 1206 с.
2. Котельников В.П. Раны и их лечение. - М., Знание. 1991. - 123 с.
3. Погодаева Н.Н., Жапова Ц., Верещагин А.Л., Горшков А.Г., Семенов А.А. / Изучение алкалоидного состава некоторых видов сибирских аконитов // Раст. ресурсы, вып. 2, 2000 г., С.79-84.
4. Бабаева А.Г. Регенерация: факты и перспективы. - М., Изд-во РАМН, 2009. - 336 с.
5. Дыгай A.M., Зюзьков Г.Н., Жданов В.В. и др. Иммобилизированный гранулоцитарный колониестимулирующий фактор. Фармакологические свойства и перспективы использования. - Томск: Изд-во: OOO «Печатная мануфактура», 2011. - 149 с.
6. Дыгай A.M., Зюзьков Г.Н. Клеточная терапия: новые подходы // Наука в России - Москва: Изд-во «Наука», 2009. - Том. 169. - №1. С.4-8.
7. Нестерова Ю.В., Поветьева Т.Н., Нагорняк Ю.Г., Перова А.В., Андреева Т.И., Рослякова Е.П., Суслов Н.И. Механизмы влияния комплексных и выделенных веществ на репаративную активность тканей в эксперименте // Экспериментальная и клиническая фармакология. - 2009. - Т.72, №3. - С.40-43.
8. Муравьева Д.А., Самылина И.А., Яковлев Г.П. Фармакогнозия: Учебник 3-е изд. М.: Медицина, 2002.
9. Осадчий С.А., Ганбаатар Ж., Шульц Э.Э., Толстиков Г.А. Алкалоиды сибирских видов живокости и аконита и их превращения // Материалы Первой Международной конференции "Химия и биологическая активность азотистых гетероциклов и алкалоидов" (том 1) Москва, 9-12 октября 2001 г.
10. Нестерова Ю.В., Поветьева Т.Н., Суслов Н.И. и др Антидепрессантная активность дитерпеновых алкалоидов аконита байкальского // Бюллетень экспериментальной биологии и медицины, 2011. Том 151, №4. С.406-409.
11. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под общей редакцией член-корр. РАМН, проф. Р.У.Хабриева. - 2-изд., перераб. и доп. - М.: ОАО «Издательство «Медицина», 2005. - 832 с.
12. Микроскопическая техника. / Под ред. Д.С.Саркисова. М., 1996.
13. Гольдберг Е.Д., Дыгай A.M., Шахов В.П. Методы культуры ткани в гематологии. Томск, 1992.
Применение зонгорина в качестве средства, обладающего регенеративной активностью.
