Результат интеллектуальной деятельности: СПОСОБ ОТДЕЛЕНИЯ 5'-ИНОЗИНАТА ДИНАТРИЯ
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к способу отделения 5'-инозината динатрия от микробной культуры.
Уровень техники
Нуклеотиды, производные пурина, такие как инозинат динатрия (5'-инозинат динатрия, IMP2Na), используют в качестве сырья для профилактического лечения нарушений обмена веществ, стимуляторов роста и противораковых препаратов в фармацевтическом секторе, а также они являются важными веществами, используемыми в качестве пищевых добавок, например, приправы в пищевой промышленности. Инозинат динатрия получают методом экстракции из мяса рыбы инозиновой кислоты (IMP), вещества, природно присутствующего в мясе, рыбе и т.д., методом ферментативного разложения РНК, методом микробной ферментации, сочетанием метода ферментации и метода синтеза, сочетанием химического разложения и синтеза РНК и т.д.
Было проведено много исследований по способу получения инозиновой кислоты, которая является исходным материалом для производства инозината динатрия. Чтобы получить 5'-инозинат динатрия, обладающий такими качествами, которые подходят для использования в качестве пищевой добавки, инозиновую кислоту необходимо очистить от примесей.
Что касается способа культивирования микроорганизмов и получения 5'-инозината динатрия из их культуры, в процессе кристаллизации можно использовать органический растворитель. Однако необходимо использовать много органических растворителей, и соответственно требуется взрывозащищенное оборудование и средства защиты для рабочих. Кроме того, для удаления органического растворителя может потребоваться процесс дистилляции и потребуется соответствующее оборудование. Соответственно, существует потребность в альтернативе такому способу.
Описание воплощений
Техническая задача
В настоящем изобретении предложен способ отделения 5'-инозината динатрия, включающий: культивирование микроорганизмов, продуцирующих 5'-инозиновую кислоту; доведение рН культурального бульона микроорганизмов до 7,4-8,0; концентрирование культурального бульона с отрегулированным рН с образованием кристаллов 5'-инозината динатрия; отделение кристаллов 5'-инозината динатрия от культурального бульона, содержащего кристаллы 5'-инозината динатрия, и промывку кристаллов путем приведения отделенных кристаллов 5'-инозината динатрия в контакт с гидрофильным органическим растворителем.
Решение задачи
Термин «5'-инозиновая кислота» представляет собой нуклеозид-монофосфат, также называемый инозин-монофосфатом (IMP). Термины «5'-инозиновая кислота» и «ее соль» используют взаимозаменяемо. Соль включает «5'-инозинат» или 5'-инозинат динатрия.
Используемый в этом документе термин «культура» относится к продукту, полученному путем культивирования микроорганизма. Культура может содержать микробные клетки или их метаболиты. Метаболиты могут находиться как внутриклеточно, так и внеклеточно. Метаболиты могут быть метаболитами нуклеиновых кислот.Метаболиты нуклеиновых кислот могут представлять собой 5'-инозиновую кислоту или ее соль.
Используемый здесь термин «культуральный бульон» относится к жидкой части, полученной путем удаления микробных клеток из культуры. Культуральный бульон может содержать продукты, выделенные или полученные из микроорганизмов. Культуральный бульон может содержать растворимые продукты. Культуральный бульон может содержать 5'-инозиновую кислоту или ее соль.
В одном из аспектов настоящего изобретения предложен способ отделения 5'-инозината динатрия, включающий: культивирование микроорганизмов, продуцирующих 5'-инозиновую кислоту; доведение рН культурального бульона микроорганизмов до 7,4-8,0; концентрирование культурального бульона с отрегулированным рН с образованием кристаллов 5'-инозината динатрия; отделение кристаллов 5'-инозината динатрия от культурального бульона, содержащего кристаллы 5'-инозината динатрия, и промывку кристаллов путем приведения отделенных кристаллов 5'-инозината динатрия в контакт с гидрофильным органическим растворителем.
Способ может включать получение культурального бульона путем удаления тела клетки из микробной культуры, содержащей 5'-инозиновую кислоту.
При получении культурального бульона микроорганизм может представлять собой микроорганизм, продуцирующий 5'-инозиновую кислоту. Микроорганизм может представлять собой генетически сконструированный микроорганизм для увеличения способности продуцировать 5'-инозиновую кислоту. Микроорганизмы могут представлять собой бактерии. Микроорганизм может представлять собой грамположительную или грамотрицательную бактерию. Бактерия может представлять собой бактерию рода Corynebacterium или рода Escherichia. Бактерия может представлять собой С.glutamicum, С.ammoniagenes или£". coli. Микроорганизм может быть предназначен для высвобождения 5'-инозиновой кислоты за пределы клетки.
Микробная культура может быть получена путем культивирования микроорганизма в среде в условиях, обеспечивающих получение 5'-инозиновой кислоты. Микробная культура может содержать 5'-инозиновую кислоту. Среда может быть известной средой, используемой для ферментации 5'-инозиновой кислоты. Среда может содержать источник углерода, источник азота и следовые элементы. Среда может содержать патоку или иммерсионный раствор кукурузы. Среда может представлять собой среду LB. Среда может содержать на 1 л дистиллированной воды 46 г глюкозы, 30 г фруктозы, 10 г дрожжевого экстракта, 18 г KH2PO4, 42 г K2HPO4, 6 г мочевины, 10 г MgSO4*7H2O, 30 мкг биотина и 5 мг гидрохлорида тиамина.
Микробная культура может содержать 5'-инозиновую кислоту в количестве от 0,5 мас. % до 20 мас. %, от 1,0 мас. % до 20 мас. %, от 2,5 мас. % до 20 мас. %, от 5 мас. % до 20 мас. % или от 5 мас. % до 10 мас. %, в расчете на общую массу культуры. 5'-инозиновая кислота может присутствовать во внеклеточной среде. Микробная культура может иметь рН от 6 до 9. Микробная культура может не подвергаться ионообменной хроматографии или кристаллизации с использованием органического растворителя, например, метанола.
Удаление тела клетки представляет собой удаление клеток или клеточного дебриса из жидких компонентов в культуре. Удаление тела клетки может быть выполнено известным способом. Удаление тела клетки может быть выполнено путем фильтрации, центрифугирования или их сочетания. Способ может включать регулирование рН культурального бульона от 7,4 до 8,0.
Регулирование рН можно выполнять путем добавления кислоты или основания в культуральный бульон. Кислота может представлять собой соляную кислоту. Основание может представлять собой NaOH. Значение рН может составлять от 7,4 до 8,0, от 7,6 до 8,0, от 7,8 до 8,0, от 7,4 до 7,8 или от 7,4 до 7,6.
Способ может включать концентрирование культурального бульона с отрегулированным рН для образования кристаллов 5'-инозината динатрия. Концентрирование может представлять собой процесс кристаллизации, в котором культуральный бульон концентрируют для превращения 5'-инозиновой кислоты в кристаллы 5'-инозината динатрия. Этот процесс кристаллизации осуществляют путем простого увеличения концентрации 5'-инозиновой кислоты в культуральном бульоне путем концентрирования культурального бульона, и в нем не используют органический растворитель. Неиспользуемый здесь органический растворитель может представлять собой гидрофильный органический растворитель. Неиспользуемый здесь гидрофильный органический растворитель может представлять собой С1-С5 спирт или смесь воды и С1-С5 спирта. Спирт может представлять собой по меньшей мере один, выбранный из группы, состоящей из метанола, этанола, пропанола, изопропанола и их смеси. Неиспользуемый здесь гидрофильный органический растворитель может представлять собой этанол. Концентрация этанола может составлять от 50% до 70% по объему в воде.
Концентрирование культурального бульона с отрегулированным рН может быть направлено на уменьшение количества влаги в культуральном бульоне. Концентрирование может представлять собой выпаривание влаги путем нагревания культурального бульона. Концентрирование можно проводить в отношении культурального бульона при температуре 50°С или выше, 60°С или выше, 70°С или выше, 80°С или выше, 90°С или выше, от 50°С до 90°С, от 50°С до 80°С, от 50°С до 70°С, от 50°С до 60°С, от 60°С до 90°С, от 60°С до 80°С, от 60°С до 70°С или от 60°С до 65°С.Концентрирование можно выполнять в виде концентрирования при пониженном давлении. Концентрирование можно выполнять до образования кристаллов 5'-инозината динатрия путем повышения концентрации 5'-инозиновой кислоты в культуральном бульоне. Концентрирование можно проводить до тех пор, пока концентрация 5'-инозиновой кислоты в культуральном бульоне не станет от 380 г/л до 600 г/л, от 400 г/л до 550 г/л, от 400 г/л до 500 г/л, от 400 г/л до 475 г/л или от 425 г/л до 475 г/л. Концентрирование можно проводить до тех пор, пока не образуются кристаллы 5'-инозината динатрия и культуральный бульон не будет иметь форму суспензии, содержащей кристаллы. В дальнейшем суспензионный раствор, содержащий кристаллы, также называют «суспензией кристаллов». Используемый здесь термин «суспензия» относится к смеси твердых веществ, например, кристаллов, суспендированных в жидкости, обычно в воде, с удельным весом более 1. Кристаллы могут иметь размер частиц от 20 мкм до 400 мкм.
Способ может дополнительно включать концентрирование культурального бульона перед регулированием рН культурального бульона. При этом концентрировании 5'-инозинат динатрия может не образовываться в культуральном бульоне или может по существу не образовываться. Концентрирование может быть направлено на уменьшение количества влаги в культуральном бульоне. Концентрирование может быть направлено на выпаривание влаги путем нагревания культурального бульона. Концентрирование можно проводить до тех пор, пока концентрация 5'-инозиновой кислоты в культуральном бульоне не станет от 150 г/л до 360 г/л. При концентрировании концентрация 5'-инозиновой кислоты может составлять от 150 г/л до 360 г/л, от 200 г/л до 300 г/л, от 220 г/л до 280 г/л или от 240 г/л до 280 г/л. Концентрирование можно проводить на культуральном бульоне при температуре от 50°С и выше, 60°С и выше, 70°С и выше,°С и выше, 90°С и выше, от 50°С до 90°С, от 50°С до 80°С, от 50°С до 70°С, от 50°С до 60°С, от 60°С до 90°С, от 60°С до 80°С, от 60°С до 70°С или от 60°С до 65°С.
Концентрирование может заключаться в проведении концентрирования при пониженном давлении. Способ может дополнительно включать охлаждение культурального бульона, включающего кристаллы, образовавшиеся после концентрирования. Охлаждение можно проводить при температуре от 25°С до 45°С, от 25°С до 40°С, от 25°С до 35°С или от 25°С до 30°С.Охлаждение можно осуществлять путем охлаждения суспензии кристаллов с постоянной скоростью. Охлаждение можно проводить при температуре охлаждения в течение от 1,0 до 3,0 ч, например, от 1,5 до 2,5 ч или 2 ч. Постоянная скорость охлаждения может составлять от 8,0°С/ч до 17,0°С/ч, например, от 10,0°С/ч до 15,0°С/ч, от 1,0°С/ч до 14,0°С/ч, от 2,0°С/ч до 13,0°С/ч, или примерно 12,5°С/ч. Охлаждение можно проводить, в то время как образовавшуюся суспензию кристаллов вводят в стеклянную пробирку с рубашкой и перемешивают. Когда охлаждение проводят при более низкой температуре, растворимость снижается, и может быть извлечено больше кристаллов.
Кроме того, когда охлаждение выполняют с однородной скоростью, можно получить более твердый и качественный кристалл. Способ может дополнительно включать старение кристаллов путем выдержки суспензии при температуре охлаждения после завершения охлаждения. Выдержку можно проводить в течение от 1 ч до 5 ч, от 1 ч до 4 ч, от 1 ч до 3 ч, от 1,5 ч до 2,5 ч или примерно 2 ч. Выдержку можно проводить, в то время как суспензию кристаллов вводят в стеклянную пробирку с рубашкой и перемешивают.
Способ может дополнительно включать отделение кристаллов 5'-инозината динатрия от культуральной жидкости, содержащей образовавшиеся кристаллы 5'-инозината динатрия.
Отделение кристалла можно выполнять известным способом отделения кристаллов в пределах объема, не выходящего за рамки целей настоящего изобретения. Отделение кристаллов можно выполнять, например, центрифугированием, фильтрацией или их сочетанием. Центрифугирование можно проводить при скорости вращения от 100 g до 1000 g, от 100 g до 800 g, от 100 g до 500 g, от 300 g до 1000 g или от 500 g до 1000 g. Центрифугирование можно проводить в течение времени вращения от 10 до 30 минут.
Способ может включать промывку кристаллов путем приведения отделенных кристаллов 5'-инозината динатрия в контакт с гидрофильным органическим растворителем.
В процессе промывки приведение в контакт может включать смешивание кристаллов с гидрофильным органическим растворителем. Промывка может быть направлена на снижение количества примесей путем удаления примесей из кристалла. Гидрофильный органический растворитель может представлять собой С1-С5 спирт или смесь воды и С1-С5 спирта. Спирт может представлять собой метанол, этанол, пропанол, изопропанол, бутанол, пентанол или их смесь. Гидрофильный органический растворитель может иметь концентрацию от 50% до 70%, от 60% до 70%, от 55,0% до 65,0% или 60% по объему в воде. Гидрофильный органический растворитель может представлять собой этанол или смесь воды и этанола. Этанол может иметь преимущество в том, что он недорог и имеет низкую токсичность. Гидрофильный органический растворитель может составлять от 10% до 50%, например, от 20% до 50%, от 15% до 40%, от 20% до 40%, от 25% до 40%, от 25% до 35%, или от 25% до 50% объема образовавшегося образца, содержащего кристаллы.
В способе отделение кристалла и промывку кристалла можно выполнять одновременно. Кроме того, отделение кристалла и промывку кристалла можно выполнять раздельно.
Способ по настоящему изобретению может дополнительно включать удаление красящего материала путем приведения промытых кристаллов в контакт с активированным углем в водном растворителе. Приведение в контакт может представлять собой смешивание промытых кристаллов с активированным углем в водном растворителе и выдерживание с ним. Водный растворитель может представлять собой воду.
Удаление красящего материала может включать растворение промытых кристаллов в воде до концентрации от 250 г/л до 500 г/л и добавление к водному раствору, содержащему кристаллы, от 0,1% до 10% активированного угля, исходя из массы 5'-инозиновой кислоты. Приведение в контакт можно проводить при температуре от 40°С до 80°С.
Преимущества изобретения
В соответствии со способом отделения 5'-инозината динатрия согласно настоящему изобретению можно эффективно отделить кристаллы 5'-инозината динатрия. В частности, согласно способу, поскольку органический растворитель используют только в процессе промывки, количество органического растворителя невелико. Согласно способу, отделенные кристаллы 5'-инозината динатрия имеют высокий выход отделения и высокую чистоту.
В частности, регулируя рН культурального бульона, можно значительно повысить выход отделения кристаллов 5'-инозината динатрия. Кроме того, приводя отделенные кристаллы 5'-инозината динатрия в контакт с гидрофильным органическим растворителем для промывки кристаллов можно предотвратить снижение выхода по сравнению со случаем промывки водой, при этом улучшается цвет образующихся кристаллов и значительно снижается количество вредных органических растворителей в кристалле. Соответственно, может быть обеспечена экономическая целесообразность.
Осуществление изобретения
Далее настоящее изобретение описано более подробно с помощью примеров. Однако эти примеры предназначены только для иллюстративных целей, и объем защиты настоящего изобретения не ограничивается этими примерами.
Пример 1. Ферментация IMP и выделение IMP из культуры
1. Получение IMP и культивирование микроорганизмов
Corynebacterium glutamicum инокулировали в ферментационном инкубаторе объемом 30 л, содержащем 18 л среды, и культивировали при 31°С в течение 140 ч для образования в культуре 5'-инозиновой кислоты (IMP). 5'-инозиновая кислота секретировалась наружу клетки и присутствовала в культуральном бульоне. Среда имела начальный рН, составляющий 7,2, и содержала на 1 л дистиллированной воды 46 г глюкозы, 30 г фруктозы, 10 г дрожжевого экстракта, 18 г KH2PO4, 42 г K2HPO4, 6 г мочевины, 10 г MgSO4*7H2O, 30 мкг биотина и 5 мг гидрохлорида тиамина. рН конечной культуры составлял 6,8.
После доведения рН до 10,5 путем добавления 50 мас. % NaOH к полученной культуре клетки удаляли путем фильтрации через микрофильтр и получали надосадочную жидкость. Концентрацию 5'-IMP в надосадочной жидкости измеряли с помощью ВЭЖХ. Надосадочная жидкость содержала 140 г/л 5'-IMP.
2. Образование кристаллов 5'-инозината динатрия
2 л фильтрата помещали в роторный испаритель (N-1110V: EYELA, Япония), выпаривали влагу из фильтрата и концентрировали фильтрат до достижения концентрации 5'-IMP 260 г/л. Выпаривание проводили с помощью вакуумного регулятора NVC-2200 при внутреннем давлении испарителя 16 кПа (120 мм рт.ст.), температуре сосуда 65°С и скорости испарения 1 л/час. В это время температура фильтрата внутри сосуда составляла 55°С. Этот процесс концентрирования далее называют «первичным концентрированием».
Полученный концентрированный фильтрат имел рН 9,0 и температуру 55°С. Изменение рН исходного фильтрата с 10,5 до 9,0, по-видимому, связано с удалением аммиака в процессе выпаривания.
Затем к 1077 мл полученного концентрированного фильтрата добавляли 4,5 мл 35 об. % соляной кислоты на 1 л полученного концентрированного фильтрата для доведения рН до 7,4 и поддерживали температуру на уровне 55°С. В дальнейшем этот процесс называют «процессом регулирования рН».
1082 мл концентрированного фильтрата, рН которого был отрегулирован, помещали в роторный испаритель, и в тех же условиях, что описаны выше, концентрированный фильтрат концентрировали до пересыщенного раствора, в котором 460 г/л кристаллов 5'-IMP и жидкости в фильтрате смешивали, то есть получали состояние суспензии. Здесь концентрация «460 г/л» 5'-IMP означает количество растворенных кристаллов как 5'-IMP, так и 5'-IMP2Na. В результате ионы 5'-IMP и 2Na+ в 608 мл пересыщенного раствора осаждались в виде кристаллов 5'-инозината динатрия (далее также «5'-IMP2Na»), и, таикм образом, концентрированный фильтрат становился вязкой суспензией, в которой твердые кристаллы были смешаны с жидким фильтратом, (далее также называемой «суспензией»). Сразу после завершения кристаллизации температура полученной суспензии составляла 55°С, а ее рН составлял 8,0. Этот процесс далее называют «процессом вторичного концентрирования и кристаллизации». То есть, поскольку кристаллы 5'-IMP2Na образовались в результате вторичного концентрирования и процесса кристаллизации, это указывает на то, что 5'-1МР можно превратить в кристаллы 5'-IMP2Na путем концентрирования без использования органического растворителя. Это значимый эффект, который является неожиданным для специалиста в данной области техники.
608 мл суспензии наливали в стеклянную пробирку с рубашкой, сверху устанавливали мешалку (eyela, zz-2121) и охлаждали суспензию со скоростью охлаждения от 12,5°С/ч до 30°С в течение 2 ч при перемешивании со скоростью 200 об/мин. Сиеклянную пробирку с рубашкой использовали для охлаждения суспензии с постоянной скоростью. После окончания охлаждения проводили выдержку при 30°С в течение 2 часов при перемешивании суспензии, содержащейся в стеклянной пробирке с рубашкой. Этот процесс соответствует процессу старения, позволяющему продолжить рост кристаллов. Далее этот процесс называют «процессом охлаждения и старения».
3. Извлечение кристаллов 5'-инозината динатрия
Кристаллы 5'-IMP2Na выделяли из полученной состаренной суспензии. В частности, 608 мл полученной состаренной суспензии помещали в корзиночный сепаратор H-110F (KOKUSAN Co. Ltd., Япония) и центрифугировали при 340xg в течение 20 минут. В центрифуге H-110F установлена перфорированная корзина, которая подключена к внешнему источнику вращения. Перфорированная корзина изготовлена из полиамидной фильтровальной ткани из мультифиламентного волокна, и воздухопроницаемость фильтра составляет 250 л/м2/с при 0,2 кПа (2 мбар). В результате центрифугирования было получено 300 г кека, содержащего кристаллы IMP2Na, который был приготовлен удалением жидкости из суспензии.
Затем туда распыляли 150 мл 60 об. % водного раствора этанола для промывки кристаллов IMP2Na (далее также называемой «промывкой этанолом»). В результате промывки было извлечено 272 г кристаллов 5'-IMP2Na и затем их сушили при комнатной температуре в течение 24 часов с получением 265 г высушенных столбчатых кристаллов 5'-IMP2Na. Этот кристалл 5'-IMP2Na также называют кристаллом 7,5 гидрата 5'-IMP2Na.
Были измерены чистота и коэффициент пропускания полученного высушенного кристалла 5'-IMP2Na. В результате высушенный кристалл 5'-IMP2Na имел выход 94,6%, чистоту 95,7% и коэффициент пропускания 86,10%. Выход и чистоту рассчитывали по следующей формуле.
Уравнение 1
Выход = масса полученного кристалла 5'-IMP2Na/Macca кристалла 5'-IMP2Na в 2 л фильтрата × 100
Для определения чистоты каждый из 1,0 г высушенного кристалла 5'-IMP2Na и 1,0 г стандартного кристалла 5'-IMP2Na (Sigma, ≥9,0% (ВЭЖХ)) растворяли в 1 л трижды дистиллированной воды для получения концентрации 1,0 г/л испытуемой группы и концентрации 1,0 г/л раствора стандартного продукта, соответственно. 5 мкл испытуемого раствора и 5 мкл стандартных растворов загружали в колонку в системе Agilent 1260 Infinity Quaternary LC (Agilent Technology Inc.). Колонка представляла собой колонку Shiseido CAPCELLPAK C18 ACR (150 мм ×x 4,6 мм, 3 мкм). Затем при 254 нм измеряли коэффициент поглощения элюата, вытекающего при подаче 2 об. % ацетонитрила / 98 об. % фосфатного буфера (рН 2,4) в колонку при скорости потока 1 мл/мин. Фосфатный буфер содержал 2 г/л фосфата аммония, 0,2 г/л фосфата тетрабутиламмония и 0,82 г/л фосфорной кислоты. В это время температура была 35°С. Эти условия ВЭЖХ также использовали для измерения концентрации 5-IMP в фильтрате. В результате чистоту рассчитывали по следующей формуле.
Уравнение 2
Чистота = масса 5'-IMP/масса твердых веществ × 100
Кроме того, в прямоугольную ячейку прибора CARY 100 UV-VIS (Agilent Technology Inc.) помещали раствор, полученный путем растворения испытуемой группы в воде с концентрацией 5 (масс/об.) %, для измерения коэффициента пропускания, и его коэффициент пропускания измеряли при 420 нм.
В качестве контроля 1 испытуемой группы кристаллы 5'-IMP2Na извлекали таким же образом, как описано выше, за исключением того, что в «извлечении кристаллов 5'-инозината динатрия» не использовали 60 об. % водный раствор этанола в процессе промывки (далее также это называют «без промывки»). В результате полученный очищенный кристалл 5'-IMP2Na имел сухую массу 266 г, выход 95%, чистоту 86,40% и коэффициент пропускания 40,48%.
В качестве контроля 2 испытуемой группы кристаллы 5'-IMP2Na извлекали таким же образом, как описано выше, за исключением того, что в «извлечении кристаллов 5'-инозината динатрия» использовали деионизированную воду в количестве 25% по отношению к объему суспензии кристаллов 5'-IMP2Na вместо 60 об. % водного раствора этанола (далее также это называют «промывкой водой»). В результате полученный очищенный кристалл 5'-IMP2Na имел сухую массу 240 г, выход 85,7%, чистоту 94,64% и коэффициент пропускания 72,72%.
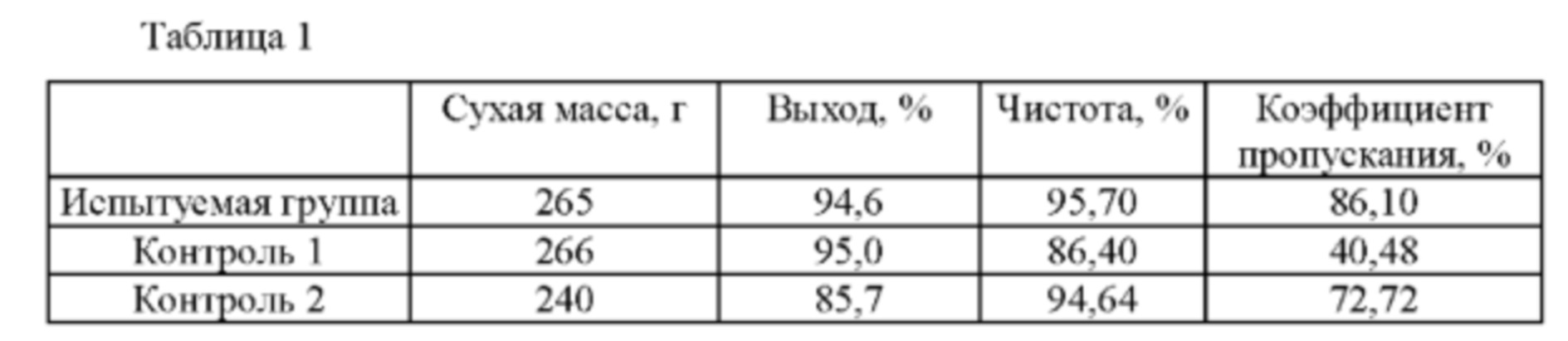
В таблице 1 показаны сухая масса, выход, чистота и коэффициент пропускания кристаллов 5'-IMP2Na, полученных для испытуемой группы, контроля 1 и контроля 2. Как показано в таблице 1, когда использовали 60 об. % водный раствор этанола в процессе отделения кристаллов, чистота и коэффициент пропускания кристаллов улучшались одновременно по сравнению со случаем, когда промывку не проводили, или со случаем промывки водой. В частности, в случае испытуемой группы чистота увеличивалась на 10,8% и 1,1%, а коэффициент пропускания увеличивался на 112,7% и 18,4% по сравнению с контролем 1 и контролем 2, соответственно. Это увеличение чистоты и коэффициента пропускания является значимым эффектом, который является неожиданным в свете предшествующего уровня техники. В частности, тот факт, что коэффициент пропускания увеличивался на 112,7% и 18,4%, указывает на то, что полученный кристалл 5'-IMP2Na может легко соответствовать пищевым стандартам. Более подробно, чтобы соответствовать стандартам для пищевых продуктов, коэффициент пропускания должен быть на уровне 98%, а для получения этого уровня пропускания для контроля 1 и контроля 2 необходимо провести перекристаллизацию два или более раз, тогда как испытуемая группа может достичь стандарта для пищевых продуктов уже при проведении одной дополнительной перекристаллизации. Кроме того, чтобы довести контроль 1 и контроль 2 до уровня испытуемой группы, требуется увеличение количества промывок, а степень извлечения может снизиться.
4. Влияние рН на процесс кристаллизации
В этом разделе было подтверждено влияние рН раствора на кристаллизацию 5'-1МР в процессе кристаллизации.
В частности, рН доводили до 7,2 путем добавления 35 об. % соляной кислоты к 2000 мл концентрированного фильтрата (рН 9,0), полученного после «первичного концентрирования» в разделе «2. Образование кристаллов 5'-инозината динатрия», и температуру поддерживали на уровне 55°С.
2000 мл концентрированного фильтрата, рН которого был отрегулирован, помещали в роторный испаритель, и в тех же условиях, что описаны выше, концентрированный фильтрат концентрировали до пересыщенного раствора, в котором 400 г/л 5'-IMP кристаллов и жидкости в фильтрате были перемешаны, то есть получали состояние суспензии. Здесь концентрация «400 г/л» 5'-IMP означает количество кристаллов как 5'-IMP, так и 5'-IMP2Na. В результате ионы 5'-IMP и 2Na+в 608 мл пересыщенного раствора выпадали в осадок в виде кристаллов 5'-IMP2Na, а концентрированный фильтрат становился вязкой суспензией, в которой были перемешаны твердые кристаллы и жидкий фильтрат (далее также называемой «суспензией»). Сразу после завершения кристаллизации температура полученной суспензии составляла 55°С, а ее рН составлял 8,0.
608 мл суспензии наливали в стеклянную пробирку с рубашкой, сверху устанавливали мешалку (eyela, zz-2121) и охлаждали суспензию со скоростью охлаждения от 12,5°С/ч до 30°С в течение 2 ч при перемешивании со скоростью 200 об/мин. Стеклянную пробирку с рубашкой использовали для охлаждения суспензии с постоянной скоростью. После окончания охлаждения проводили выдержку при 30°С в течение 2 ч при перемешивании суспензии, содержащейся в стеклянной пробирке с рубашкой. Этот процесс соответствует процессу старения, позволяющему продолжить рост кристаллов. Далее этот процесс называют «процессом охлаждения и старения».
рН 608 мл охлажденного фильтрата доводили до 7,4-9,0 с помощью 35 об. % соляной кислоты и 50% раствора NaOH. Надосадочную жидкость фильтрата при каждом рН загружали в прибор для ВЭЖХ, как описано выше, и элюировали для измерения концентрации 5'-1МР в фильтрате. В таблице 2 показана концентрация 5'-1МР в фильтрате в зависимости от рН.

Как показано в таблице 2, концентрация 5'-1МР была самой низкой при рН от 7,4 до 8,0. В таблице 2 низкая растворимость при рН от 7,4 до 8,0 означает, что кристаллы 5'-IMP2Na хорошо образуются в этом интервале рН.
5. Влияние органического растворителя, концентрации и количества, используемых при
отделении кристаллов 5'-инозината динатрия В этом разделе, в отношении раздела «3. Извлечение 5'-инозината динатрия», было подтверждено влияние других органических растворителей вместо 60 об. % водного раствора этанола, концентрации и количества на растворимость 5'-IMP, цвет кристаллов 5'-IMP2Na и чистоту кристаллов 5'-IMP2Na, количество влаги и коэффициент поглощения.
(1) Растворимость 5'-IMP в зависимости от органических растворителей и коэффициент поглощения раствора, в котором растворяют кристаллы
608 мл состаренной суспензии, полученной в разделе «2. Образование кристаллов 5'-инозината динатрия», помещали в 1000 мл органического растворителя, показанного в таблице 3, и перемешивали при 25°С в течение 1 ч, чтобы обеспечить возможность растворения 5ЧМР в суспензии в органическом растворителе. Этот раствор центрифугировали при 1500 об/мин в течение 10 минут для получения надосадочной жидкости.
После этого концентрацию 5'-IMP в надосадочной жидкости измеряли с помощью ВЭЖХ. Кристаллы отделяли, как описано в разделе «3. Извлечение кристаллов 5'-инозината динатрия», и растворяли в воде с получением 5 (мае./об.) водного раствора и измеряли их коэффициент поглощения при 420 нм. Поскольку основные примеси в кристалле были желто-коричневого цвета, для измерения количества этих красящих веществ было выбрано поглощение при 420 нм. Поглощение измеряли с использованием прибора CARY 100 UV-VIS (Agilent Technology Inc.).
В таблице 3 показана растворимость 5'-1МР в соответствии с типом и концентрацией органического растворителя. В таблицах 3 и 4 представлены % по объему.
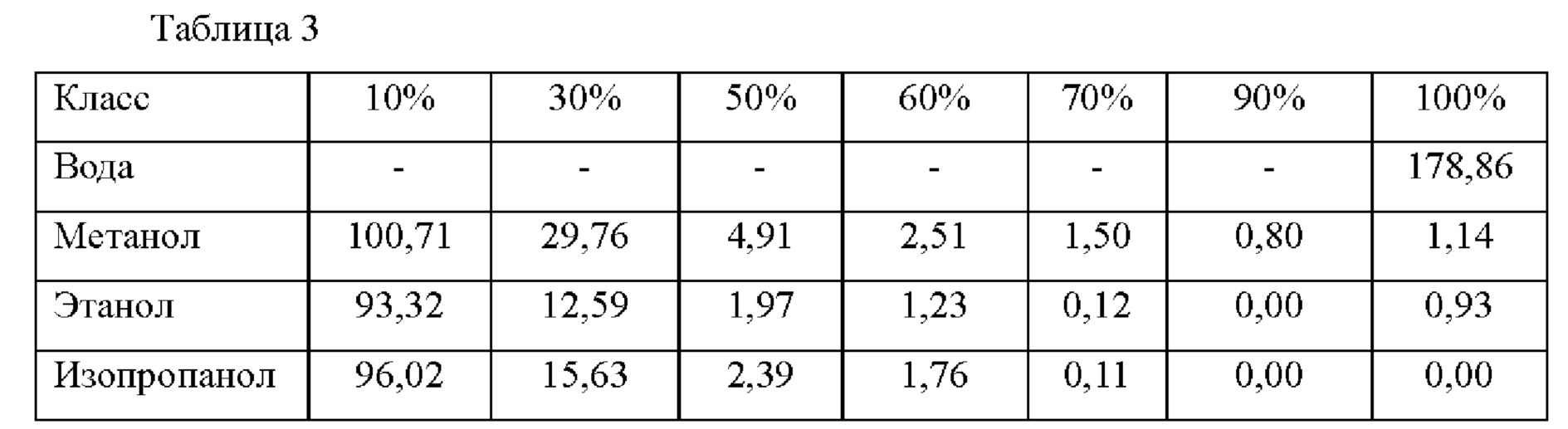
В таблице 4 показан коэффициент поглощения раствора, полученного посредством растворения кристаллов 5'-IMP2Na с использование различных типов и концентраций органических растворителей и в воде.
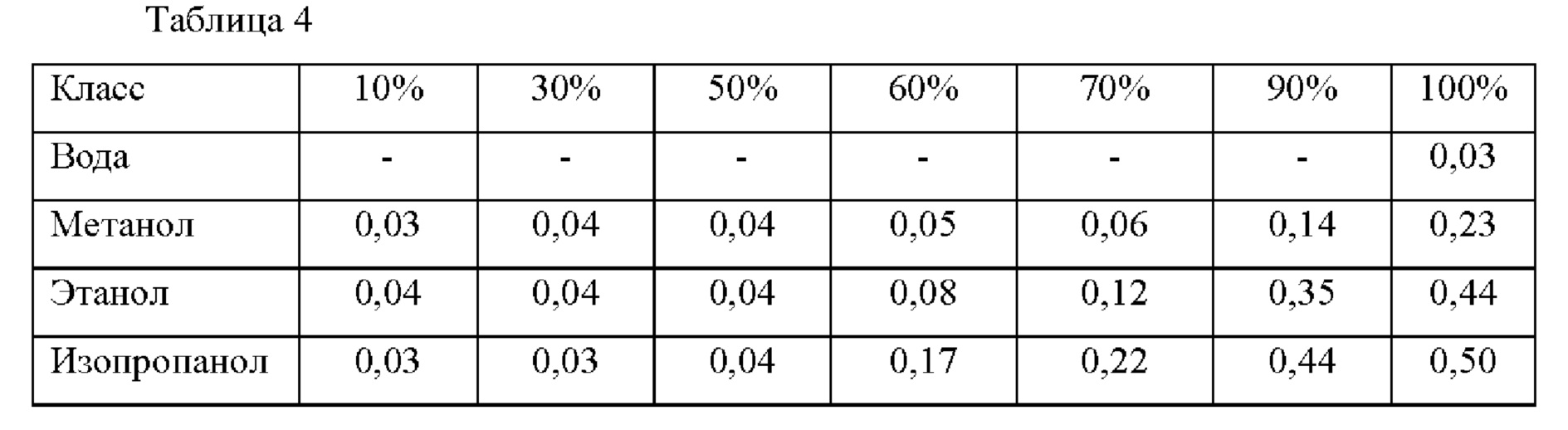
Как показано в таблицах 3 и 4, когда концентрация гидрофильного органического растворителя составляла 50% и 70%, было подтверждено, что концентрация 5'-IMP в маточном растворе была низкой, и коэффициент поглощения промытых кристаллов был низким.
(2) Характеристики кристаллов в соответствии с количеством органического растворителя
Кристаллы 5'-IMP2Na отделяли и измеряли чистоту кристаллов, влажность кристаллов и коэффициент поглощения таким же образом, как описано выше, за исключением того, что количество 60 об. % водного раствора этанола, используемое в разделе «3. Извлечение кристаллов 5'-инозината динатрия», изменяли на от 0 об. % до 40 об. % по отношению к объему суспензии. Влажность кристаллов измеряли методом сушки в термостате, при котором массу измеряли до и после сушки при 125°С в течение 3 ч в термостате. Чистоту кристаллов и коэффициент поглощения определяли, как описано выше.
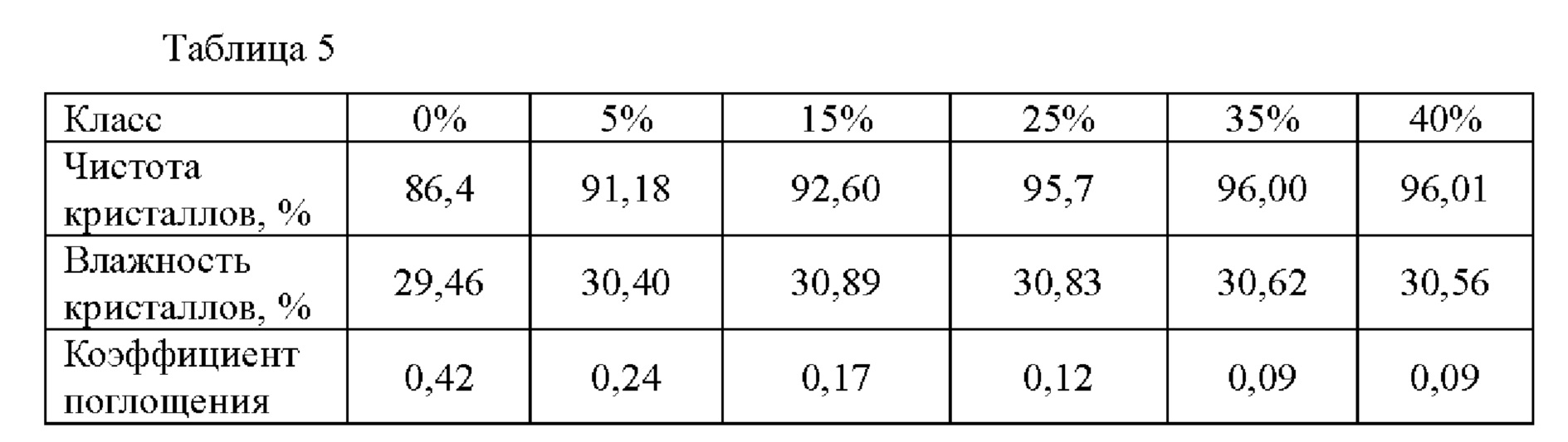
Как показано в таблице 5, в случае 60 об. % водного раствора этанола, который является промывным раствором, когда его количество составляет 25% или более, например, от 25% до 35% от объема суспензии кристаллов, чистота кристаллов, влажность кристаллов и коэффициент поглощения одновременно улучшались.

