Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, СОДЕРЖАЩЕЙ ЦИННАРИЗИН
Вид РИД
Изобретение
Изобретение относится к фармацевтической промышленности и может быть использовано для получения лекарственной формы циннаризина пролонгированного действия. Композиция содержит микрокапсулы, состоящие из циннаризина, подходящего фармацевтического носителя и полимерной матрицы.
Известны химические, физические и физико-химические способы, с помощью которых фармацевтические субстанции в виде микрочастиц можно включить в полимерную капсулу (Солодовник В.Г. Микрокапсулирование / В.Г. Солодовник - М.: Химия. - 1980 - 216 с.; Wischke С, Schwendeman S.P. Principles of encapsulating hydrophobic drugs in PLA/PLGA. International Journal of Pharmaceutics Volume 364, Issue 2, & December 2008, Pages 298-327). В данных способах соединения для введения в микрокапсулу диспергируют в растворителе, содержащем материал, который способен образовывать оболочку. На последней стадии получения происходит удаление растворителя из микрочастиц с дальнейшим получением капсул с заданными свойствами (Freitas S. Microencapsulation by solvent extraction/evaporation: reviewing the state of the art of microsphere preparation process technology / S. Freitas, H.P. Merkle, B. Gander // J. of Controlled Release. - 2005 - V. 102. - P. 313-332; Akagi T. Biodegradable nanoparticles as vaccine adjuvants and delivery systems: regulation of immune responses by nanoparticle-based vaccine / T. Akagi, M. Baba, M. Akashi // Advances in Polymer Science. - 2012 - V. 247. - P. 31-64; Hammad U. Microencapsulation: process, techniques and applications/ U. Hammad [et al.] // International J. of Research in Pharmaceutical and Biomedical Sciences. - 2011 - V. 2, №2. - P. 474-481; Кедик С.A. Получение полимерных микрочастиц с биологически активными веществами методом распылительной сушки / С.А. Кедик, М.Д. Сапельников // Вестник ВГУ. - 2014 - №2 - С 28-32).
Получение микрокапсул методом эмульгирования описано в патенте РФ 2326655. Для этого водный раствор лекарственного вещества эмульгируют в органической фазе (тип первичной эмульсии - масло-в-воде), далее соединяют первичную эмульсию и гидрофильную фазу, которая состоит из водного раствора стабилизатора эмульсии. Для удаления растворителя и получения целевого продукта используют выпаривание. Для стабилизации вторичной эмульсии применяют полиглюкин.
Известны способы удаления растворителя из водной среды дисперсионной системы микрочастиц при нагревании или при понижении давления (патент США 3891570, патент США 3691090).
Описан способ получения микрочастиц, где действующее вещество и биоразлагаемый полимер растворяют в органическом растворителе или смеси растворителей с дальнейшим смешением с водной фазой и получением эмульсии типа масло-в-воде. Удаление растворителя из полученного продукта проводят выпариванием при повышенной температуре или при пониженном давлении (патент РФ 2178695, патент РФ 2433818).
Наиболее близким по техническому решению к заявляемому способу получения является получение микрокапсул пентоксифиллина на основе поли-D,L-лактид-ко-гликолида (патент РФ 2702012). Микрокапсулы пентоксифиллина получают способом первичной эмульсии путем растворения действующего и вспомогательного вещества в небольшом объеме хлороформа с последующим введением полученного раствора в водный раствор ПАВ (3% водный раствор поливинилового спирта) при постоянном перемешивании на гомогенизаторе со скоростью 20000 об/мин. Для удаления хлороформа из полученной первичной эмульсии образовавшиеся микрокапсулы отмывают и отделяют центрифугированием в течение 24 часов. Образовавшиеся микрокапсулы отмывают и отделяют центрифугированием. Полимерным материалом оболочки микрочастиц данного изобретения является поли-D,L-лактид-ко-гликолид (сополимер поли-D,L-молочнрд кислоты и гликолевой кислоты). Молярное соотношение лактида к гликолиду составляет 50:50. Полученные микрочастицы количественно переносят в мерную колбу, добавляют 2 мл 1% раствора маннита и доводят объем раствора в колбе водой очищенной до метки - итоговая суспензия.
На наш взгляд, недостатками данного способа является то, что конечным продуктом синтеза микрочастиц пентоксифиллина является суспензия, точность дозирования данной лекарственной формы может иметь погрешность. Предлагаемый нами способ подразумевает лиофильную сушку получившейся суспензии, в качестве криопротектора предлагается использовать маннит, что позволит максимально точно рассчитать необходимую терапевтическую дозу инновационной фармацевтической композиции, содержащей циннаризин.
Технической задачей предлагаемого изобретения является получение точно дозируемой лекарственной формы циннаризина пролонгированного действия на основе сополимера молочной и гликолевой кислот.
Технический результат достигается при использовании предложенного способа, который состоит в следующем.
Точные навески активного вещества и полимерного материала растворяют в небольшом объеме хлороформа, затем по каплям вводят полученный раствор в воду очищенную, содержащую ПАВ при постоянном перемешивании при помощи гомогенизатора со скоростью 20000 об/мин. В качестве ПАВ используют 3% водный раствор поливинилового спирта (ПВС). После этого из полученной первичной эмульсии полностью удаляют хлороформ, взбалтывая ее в течение 24 часов, образовавшиеся микрокапсулы отмывают водой очищенной и отделяют центрифугированием, получившуюся суспензию подвергают лиофильной сушке, в качестве криопротектора используется маннит. В результате получаются микрокапсулы, которые по размерам практически одинаковы (размер частиц 300±50 нм).
В данном изобретении в качестве полимерного носителя оболочки микрочастиц является сополимер поли-D,L-молочной кислоты и гликолевой кислоты - поли-D,L-лактид-ко-гликолид. Молярное соотношение лактида к гликолиду 50:50.
Полученная первичная эмульсия является стабильной, и поэтому растворитель после первой стадии можно частично удалить из органической фазы. Растворитель удаляют при температуре 20°С, это позволяет поддерживать скорость удаления растворителя оптимальной. На первой стадии растворитель удаляется от 10 до 90%.
Первичную эмульсию получают механическим взбалтыванием. Для этого используют методику капсулирования активного агента для получения микрочастиц с контролируемым высвобождением лекарственного средства с помощью гомогенизатора. Для получения конечной субстанции эмульсию подвергают лиофильной сушке, в качестве криопротектора используют маннит.
Высушенная субстанция содержит микрочастицы, включающие активное лекарственное вещество, капсулированное в полимерном материале.
Микрочастицы, полученные предлагаемым способом, имеют сферическую форму, хотя могут быть и неправильной формы. Размер полученных микрочастиц составляет 300±50 нм (фиг. 1). Можно смешивать разные размеры или типы частиц с тем, чтобы давать пациенту активный агент по многофазной схеме и/или схеме, которая обеспечивает введение разных агентов в разное время, или смесь агентов одновременно.
Предлагаемый способ получения фармацевтической композиции с циннаризином характеризуется следующими примерами.
Пример 1. Точную навеску циннаризина (0,01 г) и поли-D,L-лактид-ко-гликолида (0,03 г) помещают в колбу, добавляют 2 мл хлороформа и перемешивают до полного растворения. Отдельно готовят 0,5% раствор ПВС, для чего 0,25 г ПВС помещают в термостойкую колбу, добавляют 50 мл горячей воды очищенной, затем медленно растворяют при нагревании на водяной бане. После этого раствор охлаждают до температуры 20°С, а затем подвергают гомогенизации при скорости 20000 об/мин. в течение 5 минут. Далее вводят по каплям через шприц емкостью 3 мл с иглой 0,36×12 мм раствор, содержащий растворенный циннаризин и поли-D,L-лактид-ко-гликолид, в течение 20 минут. С целью уменьшения потери циннаризина И поли-D,L-лактид-ко-гликолида емкость, содержащую данные растворы, промывают 1 мл хлороформа и вводят в конечный раствор тем же способом. Полученную первичную эмульсию взбалтывают в течение 24 часов до полного удаления хлороформа. Для подтверждения отсутствия хлороформа в полученной эмульсии к 0,1 мл полученного раствора прибавляют 4 капли раствора бромтимолового синего. При наличии хлороформа в полученном растворе должно наблюдаться сине-фиолетовое окрашивание. В полученном растворе хлороформ отсутствует.
Полученные микрочастицы центрифугируют со скоростью 8000 об/мин. в течение 10 минут, после чего декантат сливают, а микрочастицы промывают водой очищенной и центрифугируют (4 раза). Полученные микрочастицы количественно переносят в мерную колбу вместимостью 25 мл, добавляют 2 мл 1% раствора маннита и доводят объем раствора в колбе водой очищенной до метки - итоговая суспензия. Далее итоговую суспензию помещают в колбу для лиофилизации и подключают к лиофильной сушилке, при температуре -50°С и давлении 0,035 мБар, в течение 3-4 суток до полного удаления водной фазы. Технологический выход пролонгированной лекарственной формы циннаризина составляет - 53,2%.
Пример 2. Точную навеску циннаризина (0,02 г) и поли-D,L-лактид-ко-гликолида (0,02 г) помещают в колбу, добавляют 2 мл хлороформа и перемешивают до полного растворения. Отдельно готовят 0,5% раствор ПВС, для чего 0,25 г ПВС помещают в термостойкую колбу, добавляют 50 мл горячей воды очищенной, затем медленно растворяют при нагревании на водяной бане до конца. После этого раствор охлаждают до температуры 20°С, а затем подвергают гомогенизации при скорости 20000 об/мин. в течение 5 минут. Далее вводят по каплям через шприц емкостью 3 мл с иглой 0,36×12 мм раствор, содержащий растворенный циннаризин и поли-D,L-лактид-ко-гликолид, в течение 20 минут. С целью уменьшения потери циннаризина и поли-D,L-лактид-ко-гликолида емкость, содержащую данные растворы, промывают 1 мл хлороформа и вводят в конечный раствор тем же способом. Полученную первичную эмульсию взбалтывают в течение 24 часов до полного удаления хлороформа. Для подтверждения отсутствия хлороформа в полученной эмульсии к 0,1 мл полученного раствора прибавляют 4 капли раствора бромтимолового синего. При наличии хлороформа в полученном растворе должно наблюдаться сине-фиолетовое окрашивание. В полученном растворе хлороформ отсутствует.
Полученные микрочастицы центрифугируют со скоростью 8000 об/мин. в течение 10 минут, после чего декантат сливают, а микрочастицы промывают водой очищенной и центрифугируют (4 раза). Полученные микрочастицы количественно переносят в мерную колбу вместимостью 25 мл, добавляют 2 мл 1% раствора маннита и доводят объем раствора в колбе водой очищенной до метки - итоговая суспензия. Далее итоговую суспензию помещают в колбу для лиофилизации и подключают к лиофильной сушилке, при температуре -50°С и давлении 0,035 мБар, в течение 3-4 суток до полного удаления водной фазы. Технологический выход пролонгированной лекарственной формы циннаризина составляет - 51,2%.
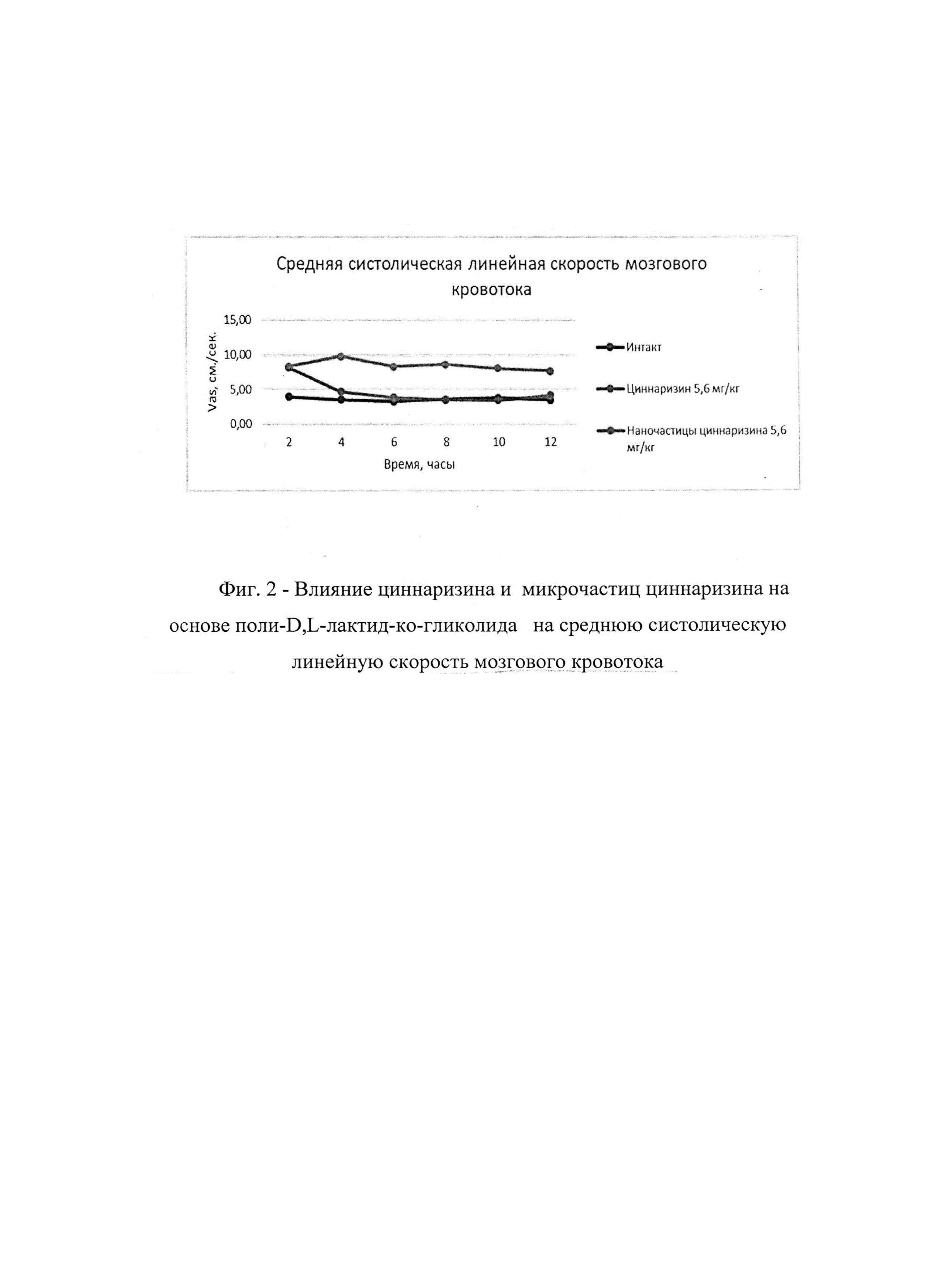
Изучение пролонгированного действия микрочастиц циннаризина на основе поли-DL-лактид-ко-гликолида проводилось in vivo. Исследование изменения уровня мозгового кровотока выполнено на 108 половозрелых крысах-самцах линии Wistar массой 240-260 грамм. В ходе выполнения исследования экспериментальные группы формировали с применением рандомизированного подхода. В эксперимент включались крысы с условно-средней поведенческой активностью, определяемой визуально. Животные были разделены на 3 экспериментальные группы (n=36 каждая): интактная группа крыс; группа животных, получавших циннаризин; группа крыс, которой вводили наночастицы циннаризина на основе поли-D,L-лактид-ко-гликолида. Внутри каждой группы были сформированы подгруппы животных (n=6), у которых регистрировали изменение уровня мозгового кровотока в следующем временном интервале: 2 часа, 4 часа, 6 часов, 8 часов, 10 часов и 12 часов. Временные промежутки были выбраны с учетом фармакокинетических особенностей циннаризина (максимальная концентрация препарата в крови обнаруживается через 1-3 часа после перорального введения). В работе в качестве исследуемого образца выступали микрочастицы циннаризина на основе поли-D,L-лактид-ко-гликолида. Референтным препаратом служила субстанция циннаризина в дозе 5,6 мг/кг. Исследуемый образец вводили однократно per os через атравматичный желудочный зонд (препарат сравнения вводился аналогично) в эквивалентной референтному препарату дозе. Анализ изменения мозговой гемодинамики производили методом ультразвуковой допплерографии (таблица 1, фиг. 2).
У группы животных, получавших референтный препарат циннаризин, через 2 часа после итнрагастрального введения препарата сравнения относительно интактной группы крыс отмечено повышение показателя средней систолической линейной скорости мозгового кровотока (Vas) - в 2,1 раза (р<0,05). Через 4 часа после введения референтного препарата циннаризина в сравнении с интактной группой крыс отмечено увеличение показателя Vas - на 33,5% (р<0,05), в то время как остальные изучаемые параметры статистически значимых изменений относительно интактной группы животных не претерпели. По истечении 6-ти часов с момента введения референтного препарата циннаризина и изучаемых микрокапсул циннаризина у группы крыс, получавших препарат сравнения циннаризин, в сравнении с интактной группой животных статистически значимых изменений параметров линейной и объемной церебральной гемодинамики не установлено. В тоже время применение микрочастиц циннаризина способствовало увеличению показателей мозгового кровотока Vas сравнении с интактной группой крыс в 2,6 раза (р<0,05). У группы животных, получавших циннаризин после 8-ми часов экспозиции в сравнении с интактной группой при применении микрочастиц циннаризина параметры церебральной гемодинамики Vas оставались стабильными и превосходили аналогичные показатели интактной группы животных в 2,5 раза (р<0,05). При введении крысам микрочастиц циннаризина через 10 часов экспозиции показатели церебральной гемодинамики превосходили аналогичные параметры интактной группы животных: Vas - в 2,3 раза (р<0,05). У группы крыс, которым вводили циннаризин по истечении 12-ти часов с момента введения препарата отмечено полное восстановление церебральной гемодинамики до уровня интактных животных (статистически значимых отличий между интактной группой крыс и животными, получавшими циннаризин, по показателям линейной и объемной скорости кровотока не установлено. В тоже время у крыс на фоне применения микрочастиц циннаризина параметры мозгового кровотока превосходили показатели интактной группы животных: Vas - в 2,2 раза (р<0,05).
Фармакологический ответ в виде увеличения скорости мозгового кровотока (линейных и объемных показателей) при введении наночастиц циннаризина был более стабильным на всем протяжении регистрации данных, что предполагает наличие пролонгированного эффекта у изучаемых микрочастиц циннаризина на основе поли-D,L-лактид-ко-гликолида.
Настоящее изобретение предлагает пролонгированную лекарственную форму циннаризина в смеси с фармацевтическим носителем для применения в медицинской практике.
Предлагаемый способ имеет преимущества по сравнению с прототипом: полученные частицы имеют минимальный разброс частиц по их размерам (300×50 нм); полученная первичная эмульсия является устойчивой; растворитель быстро удаляется при липофильной сушке, что позволит максимально точно рассчитать необходимую терапевтическую дозу инновационной фармацевтической композиции, содержащей циннаризин.
Полученная пролонгированная форма циннаризина имеет длительность действия от 2 до 12 часов. Длительность действия может варьировать в зависимости от соотношения полимер: лекарство, композиции полимера и размера частиц. Важным преимуществом данного изобретения является то, что практически весь лекарственный препарат попадает в организм пациента вследствие биологического распада полимера. При этом незначительный интервал изменений концентраций циннаризина при применении наночастиц на основе поли-D,L-лактид-ко-гликолида может способствовать нивелированию экстрапирамидных нарушений при проводимой терапии, что в свою очередь выгодно отличает разрабатываемую лекарственную форму циннаризина от уже имеющихся на фармацевтическом рынке лекарственных препаратов, содержащих в качестве основного действующего вещества блокатор кальциевых каналов - циннаризин.