Результат интеллектуальной деятельности: Способ прогнозирования индивидуального риска развития посттравматической эпилепсии
Вид РИД
Изобретение
Изобретение относится к медицине, в частности к неврологии, эпилептологии и может быть использовано для оценки индекса индивидуального риска формирования эпилепсии после перенесенной черепно-мозговой травмы.
Эпилепсия является одним из распространенных неврологических заболеваний. В последнее время большое внимание уделяется клеточно-молекулярным механизмам эпилептогенеза, где важную роль играют NMDA-рецепторы. NMDA-рецепторный комплекс состоит из двух NR1 и двух NR2 субъединиц, кодируемых генами GRIN1 и GRIN2A. По данным литературы известны генетические ассоциации гена GRIN2A с роландической эпилепсией, электрическим эпилептическим статусом во сне (ESES) и синдромом Драве [Батышева Т.Т, Квасова О.В., Трепилец С.В., Бадалян О.В., Бурд С.Г., Трепилец В.М., Балканская С.В., Глазкова С.В., Платонова А.Н. Методические рекомендации №27 «Современные подходы к диагностике и лечению детей, ассоциированных с электрическим эпилептическим статусом медленного сна ESES», Москва, 2015; 5-10; Белоусова Е.Д. Генетика эпилепсии: зачем и как обследовать детей с эпилепсией. Неврология, нейропсихиатрия, психосоматика. 2014; (спецвыпуск 1):4-8]. Частота встречаемости пациентов с эпилепсией в популяции по разным оценкам составляет 0,52% (данные ВОЗ).
Существует множество факторов риска, способствующих формированию эпилепсии. Одним из основных является черепно-мозговая травма (ЧМТ). По данным ВОЗ, частота развития посттравматической эпилепсии (ПТЭ) достигает 20%. В связи с этим актуален поиск прогностических маркеров развития ПТЭ.
Известны способы прогнозирования развития симптоматической эпилепсии после перенесенных вирусных энцефалитов с учетом клинических симптомов в сочетании с изменениями на электроэнцефалограмме (ЭЭГ) и фокальными поражениями коры головного мозга по данным нейровизуализирующих исследований [Wang-Tso Lee, Tsui-Wen Yu et al. Risk factors for postencephalitic epilepsy in children: a hospital-based study in Taiwan // Eur J of Paediatr Neurol, 2007; 11: 302-309].
Недостатки данного способа: наличие разнообразных клинических симптомов, дифференцирующих особенности заболевания у конкретного пациента; способ не учитывает выраженность воспалительных компонентов, которые являются основой патогенеза нейроинфекций.
Известен способ прогнозирования риска развития симптоматической эпилепсии при нейроинфекциях у детей, заключающийся в оценке риска развития эпилепсии путем определения уровня альфа-1 антитрипсина в цереброспинальной жидкости и выявления очаговой эпилептиформной активности при 2-часовом ЭЭГ-мониторинге в остром периоде заболевания [Патент РФ №2652967 Аксенова А.И., Горелик Е.Ю., Войтенков В.Б., Скрипченко Н.В.]. К недостаткам указанного способа относится инвазивность метода, необходимость госпитализации пациента.
В патентных источниках отсутствуют способы прогнозирования риска развития эпилепсии после перенесенной ЧМТ. Существует ряд критериев, с помощью которых возможен прогноз развития ПТЭ. Отмечается зависимость развития эпилептической болезни от тяжести черепно-мозговой травмы, от локализации эпилептического очага, наличия очаговых изменений по данным КТ и МРТ, соответствующая им эпилептиформная и пароксизмальная активность на ЭЭГ. Однако не всегда имеющиеся критерии сопровождаются развитием ПТЭ, что может свидетельствовать о роли наследственной предрасположенности к эпилептическим припадкам.
Технический результат: объективизация способа, доступность, повышение точности прогнозирования индивидуального риска развития посттравматической эпилепсии.
Указанный результат достигается путем определения генетических маркеров в ДНК больного ПТЭ методом полимеразной цепной реакции, с последующим сопоставлением с таблицей индексов индивидуального риска (ИИР) развития посттравматической эпилепсии для конкретного генотипа. При значении ИИР более 1,03 делают вывод о высоком индивидуальном риске развития ПТЭ, равном или менее 1,03 - об отсутствии индивидуального риска развития ПТЭ.
Способ осуществляют следующим образом:
У обследуемого больного проводится забор венозной крови в объеме 5-7 мл в пробирки, содержащие ЭДТА в качестве антикоагулянта, независимо от приема пищи. Затем проводится выделение ДНК из полученных проб при помощи коммерческого набора ДНК-Экстран-1 ЗАО «Синтол», Россия. Для этого в 1,5 мл пробирку (Eppendorf) вносят 100 мкл анализируемого образца крови и 300 мкл лизирующего раствора (0,5% раствор саркозила и протеиназы К 20 мг/мл в ацетатном буфере рН 7,5) для гемолиза эритроцитов. Далее добавляют сорбент (каолин), перемешивают на вортексе в течение 5 секунд и осаждают капли центрифугированием при 1000 об/мин, трижды повторяют процедуру промывки пробы от белков и липидов, удаляя надосадочную жидкость. Нуклеиновые кислоты остаются на сорбенте. Затем проводится экстракция адсорбированных ДНК ТЕ-буфером (смесь 10 мМ трис- HCI и 1 мМ ЭДТА (рН=8,0).
Экстракт подвергают центрифугированию, полученная надосадочная жидкость содержит очищенную ДНК. Полученный препарат ДНК готов к внесению в реакционную смесь для полимеразной цепной реакции (ПЦР). ПЦР проводят на детектирующем амплификаторе с гибридизационно-флуоресцентной детекцией в режиме «реального времени» с использованием готовых наборов праймеров и зондов производства Thermo Fisher Scientific Applied Biosystems, США, где в качестве праймеров использованы участки ДНК: гена GRIN1 (rs 1126442) и GREN2A (rs 1969060). Проводят реакцию амплификации, которая достигается тем, что для исследования аллелей каждого гена у отдельного человека готовят реакционную смесь. В каждую лунку планшетки вносят 0,1 мкл готовой смеси праймеров и зондов для выбранных генов: GRIN1 (rs 1126442) и GRIN2A (rs 1969060). В планшетку в каждую лунку добавляют остальные компоненты, необходимые для осуществления ПЦР, согласно инструкции коммерческого набора 2,5 х Реакционная смесь для проведения ПЦР (ЗАО «Синтол», Россия), нуклеотиды (дезоксинуклеотидтрифосфаты: по 10 мМ д АТФ, д ТТФ, дГТФ, дЦТФ), буфера (100 мМ трис-HCI- буфера, 500 мМ КCI, 40 мМ MgCI2) и Tag F полимеразы. Соответственно объем реакционной смеси составляет 25 мкл. Планшетка плотно закрывается и устанавливается в амплификатор.
При проведении ПЦР амплификация и детекция осуществляется на детектирующем амплификаторе CFX96 фирмы Bio-Rad, США. Используется универсальная программа амплификации, подобранная производителем реактивов. Она включает в себя несколько этапов: 1 этап - активация TaqF-полимеразы (режим «горячего старта») продолжается 15 мин при 95°С; 2 этап - установочные циклы амплификации без измерения флуоресценции (5 циклов); 3 этап - рабочие циклы амплификации с измерением флюоресценции (40 циклов). Каждый цикл амплификации включает в себя денатурацию ДНК (5 с при 95°С), отжиг праймеров (20 с при 60°С) и саму реакцию полимеризации ДНК (15 с при 72°С). Регистрация сигнала флюоресценции, возникающего при накоплении продуктов амплификации участков ДНК проводится в режиме «реального времени» после стадии отжига праймеров для выбранных генов по каналу VIC - для детекции одного из аллельных вариантов генов, и по каналу FAM - для альтернативного варианта.
Результаты интерпретируются на основании наличия (или отсутствия) пересечения кривой флюоресценции с установленной на заданном уровне пороговой линией, что соответствует наличию (или отсутствию) значения порогового цикла (N) в соответствующей графе в таблице результатов, отображаемой в программном обеспечении для амплификатора CFX96. По соотношению пороговых циклов, полученных по двум каналам детекции, определяют состояние генов GRIN1 и GRIN2A в исследуемом участке ДНК Т (-3499) С методом аллельной дискриминации. Возможны два варианта состояния гена: гомозиготное - в случае, когда одно из значений порогового цикла не определяется (ниже пороговой линии) и гетерозиготное - в случае, когда имеются два значения пороговых циклов и по этим каналам получены параболические кривые флюоресценции. В зависимости от того, накопление какого продукта амплификации происходит в реакции, устанавливают гетерозиготное, или нормальное гомозиготное, или вариантное гомозиготное состояние генов GRIN1 (rs 1126442) и GRIN2A (rs 1969060).
Прогнозирование индивидуального риска развития ПТЭ оценивают по гомозиготному состоянию генов пациента. Проводят сопоставление выявленных гомозиготных генотипов АА и GG гена GRIN2A (rs 1969060), генотипа АА гена GRIN1 (rs 1126442) с таблицей индексов индивидуального риска (ИИР) развития ПТЭ. При значении ИИР более 1,03 делают вывод о высоком индивидуальном риске развития ПТЭ, равном или менее 1,03 - об отсутствии индивидуального риска развития ПТЭ.
Способ апробирован при исследовании 138 пациентов с верифицированным диагнозом эпилепсия (66 человек с ПТЭ, 72 человека с идиопатической эпилепсией (ИЭ), а также 66 человек с перенесенной ЧМТ без развития эпилепсии), у которых проведен подсчет распределения генотипов (в абсолютном и процентном соотношении) для каждого гена в группах, как представлено в таблице 1.
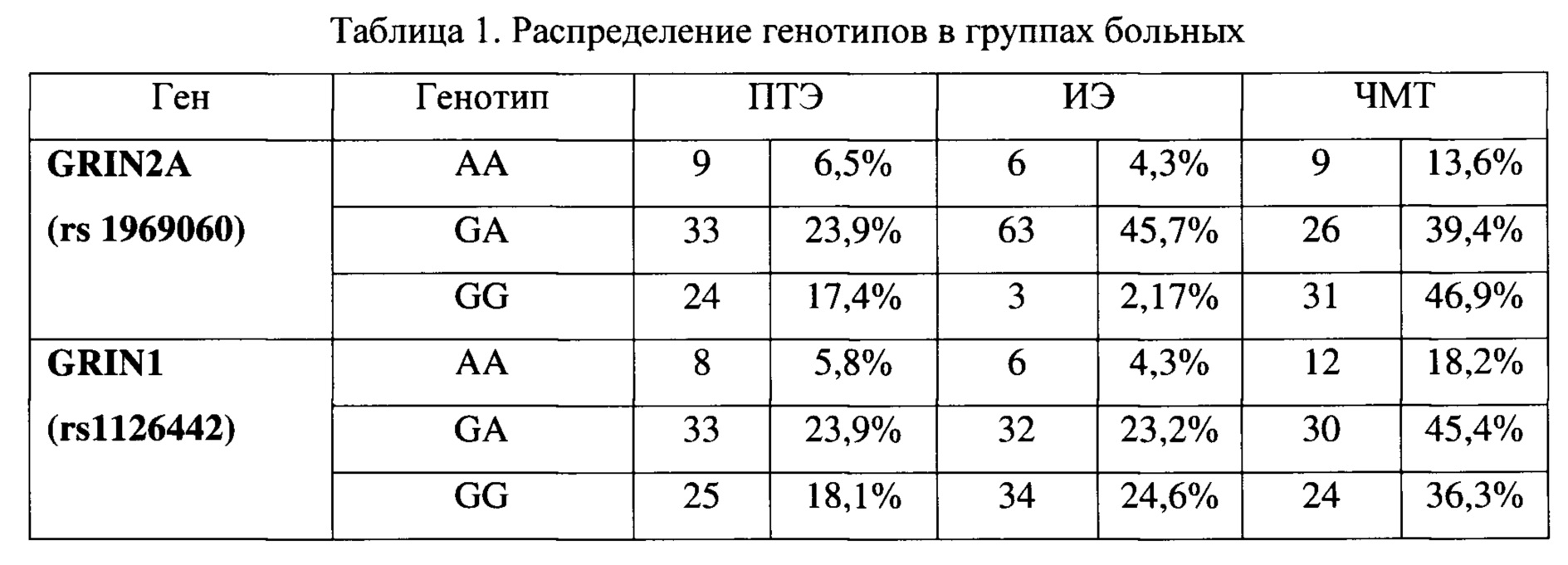
Для определения ИИР по каждому генотипу была предварительно рассчитана частота встречаемости генотипов в популяции, участвующих в развитии заболевания в зависимости от среднего популяционного риска, значение которого известного как 0,52%: средний популяционный риск / процентное соотношение генотипа в общей популяции (пример расчета частоты встречаемости генотипа АА гена GRIN2A в популяции: 0,52% / 6,5%=0,08%).
Также рассчитывался средний популяционный риск для конкретного генотипа по формуле: частота встречаемости генотипа в популяции + средний популяционный риск: (средний популяционный риск для генотипа АА гена GRIN2A: 0,08%+0,52%=0,6%).
Используя данное значение, проведен расчет ИИР развития заболевания у обследуемых: 0,52% / 0,6%=1,15 (ИИР для генотипа АА гена GRIN 2А). При значении ИИР более 1,03 достоверно увеличивается индивидуальный риск развития эпилепсии, менее или равном 1,03 - риск развития заболевания отсутствует, прогноз благоприятный. Данный расчет индекса индивидуального риска проведен для каждого генотипа (таблица 2).
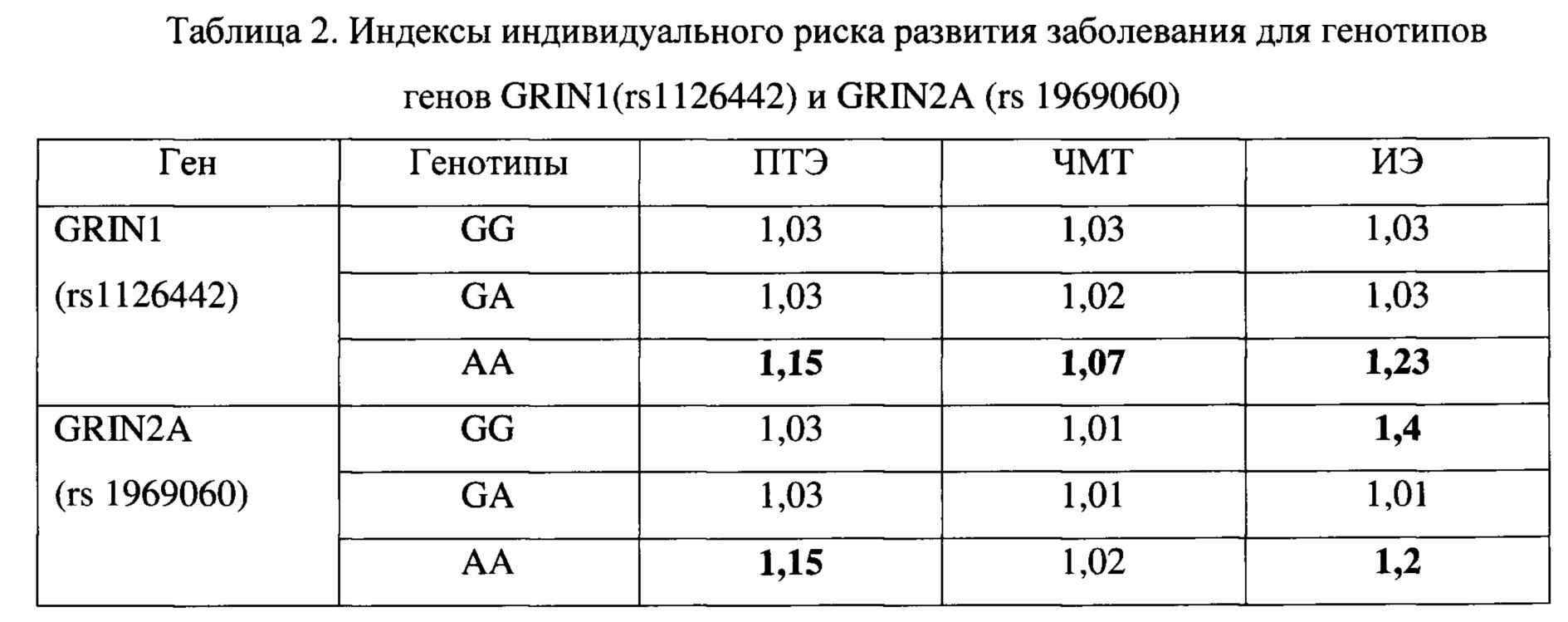
Как видно из таблицы 2, преобладает гомозиготный генотип АА гена GRIN1 у пациентов во всех группах, что указывает на высокий риск развития эпилепсии, в том числе после полученной ЧМТ, в отличие от других генотипов.
У пациентов с ИЭ и ПТЭ преобладает гомозиготный генотип АА гена GRIN2A, а у пациентов с ИЭ - гомозиготный генотип GG гена GRIN2A. Следовательно, при наличии генотипов GG и/или АА гена GRIN2A констатируется высокий риск развития эпилепсии, в том числе посттравматической.
Примеры конкретного выполнения
Пример 1
Пациент В., 40 лет. Диагноз: Последствия тяжелой ЧМТ, хроническая субдуральная гематома, перелом затылочной кости от 2016 г, атактический, астено-невротический синдромы. Три года назад, был избит, получил травму с потерей сознания. Был доставлен в нейрохирургическое отделение, где установлен диагноз ЧМТ средней степени тяжести, ушиб головного мозга, субдуральное кровоизлияние, перелом затылочной кости. При проведении КТ головного мозга выявлена субдуральная гематома. Через 3 месяца после перенесенной ЧМТ разворачивается первый локализованный приступ с последующими билатеральными тонико-клоническими судорогами, с постприступной амнезией. Наследственный анамнез по эпилептической болезни не отягощен. Осмотрен неврологом, противоэпилептические препараты не принимал. По данным МРТ: кистозно-атрофические изменения. Признаки хронической субдуральной гематомы. ЭЭГ не выявила эпилептиформную активность. Неврологический статус: сухожильные рефлексы с рук и ног равные. Чувствительность не нарушена. В позе Ромберга неустойчив, координаторные пробы выполняет неуверенно. Эмоционально лабилен: раздражителен, вспыльчив, периодически использует адаптол, с положительным эффектом. В ходе наблюдения за пациентом повторных пароксизмальных событий не отмечается.
Проведена ПЦР, которая выявила наличие гомозиготного генотипа GG гена GRIN2A (rs 1969060), ИИР равен 1,01, что свидетельствует об отсутствии риска развития посттравматической эпилепсии.
Пример 2
Пациент С., 33 года. Диагноз: Последствия ЧМТ средней степени тяжести от 2016 года, дебют посттравматической эпилепсии, тонико-клонические приступы. Неоднократно в анамнезе присутствуют ЧМТ легкой степени тяжести, по данным медицинской документации констатируются сотрясения головного мозга, последнее 2 года назад, был избит.После ЧМТ в течение нескольких часов потеря сознания. Был доставлен в нейрохирургическое отделение, где при помощи КТ выявлены признаки наружной заместительной гидроцефалии, при проведении ЭЭГ регистрировалось региональное замедление бифронтально, без эпилептиформной активности. Через 1 год на фоне стрессовой ситуации на работе, разворачивается первый приступ с потерей сознания, сопровождающийся судорогами, приступ амнезирован. При повторном проведении ЭЭГ эпилептиформная активность не выявлена. Через 6 месяцев развивается повторный тонико-клонический приступ. При очередном ЭЭГ-обследовании зарегистрирован очаг эпилептиформной активности (комплексы острая-медленная волна) в лобных отведениях. При дальнейшем наблюдении данные пароксизмы не повторялись. Неврологический статус без очаговой неврологической симптоматики. Походка обычная. Эмоциональный фон лабильный: пациент раздражителен, вспыльчив, отмечает трудности при засыпании. Методом ПЦР у данного пациента выявлен гомозиготный генотип АА гена GRIN1 (rs 1126442), ИИР равен 1,15, что соответствует высокому риску развития посттравматической эпилепсии.
Пример 3
Пациент, 41 г. Диагноз: Посттравматическая эпилепсия после перенесенной ЧМТ (2014 г.), фокальные приступы с переходом в билатеральные тонико-клонические, медикаментозная ремиссия 2 года. Четыре года назад, перенес ЧМТ, упал в подъезде, кратковременно терял сознание. Доставлен в нейрохирургическое отделение, проведена КТ, которая не выявила очаговых нарушений ткани головного мозга. При проведении ЭЭГ выявляется пароксизмальная активность, истинной эпилептиформной активности не регистрируется. В связи с полученными данными ЭЭГ-обследования, был назначен финлепсин 200 мг в сутки, в течение 6 месяцев. Затем препарат был отменен. Через 1 месяц после отмены препарата развивается первый приступ потери сознания, с дальнейшей амнезией. Еще через 3 месяца, после стрессовой ситуации на работе и на фоне недостатка ночного сна, развивается второй эпилептический приступ. При проведении ЭЭГ эпилептиформная активность также не обнаружена. Затем приступы разворачивались с регулярностью 1 раз в 3-4 месяца. Наследственность по эпилепсии не отягощена. Назначен вновь препарат финлепсин в дозе 800 мг в сутки (с постепенной титрацией дозы), на фоне чего приступы были купированы. Отмечается ремиссия в течение 2-х лет. Неврологический статус без патологических изменений. Эмоциональный фон спокойный.
Методом ПЦР выявлен гомозиготный генотип АА гена GRIN1 (rs 1126442), ИИР равен 1,15, риск развития ПТЭ - высокий.
Способ прогнозирования индивидуального риска развития посттравматической эпилепсии, характеризующийся тем, что образец ДНК, выделенный из венозной крови пациента, исследуют по полиморфизмам генов, используя в качестве праймеров участок ДНК генов GRIN1 (rs1126442) и GRIN2A (rs1969060), для каждого из указанных полиморфизмов устанавливают гетерозиготное, или нормальное гомозиготное, или вариантное гомозиготное состояние генотипов АА и GG исследуемых генов, далее проводят сопоставление выявленных гомозиготных генотипов АА гена GRIN1 (rs1126442), или АА гена GRIN2A (rs1969060), или GG гена GRIN2A (rs1969060) с таблицей 2 для конкретного генотипа и при значении индекса более 1,03 делают вывод о высоком индивидуальном риске развития посттравматической эпилепсии, равном или менее 1,03, - об отсутствии индивидуального риска развития посттравматической эпилепсии.
