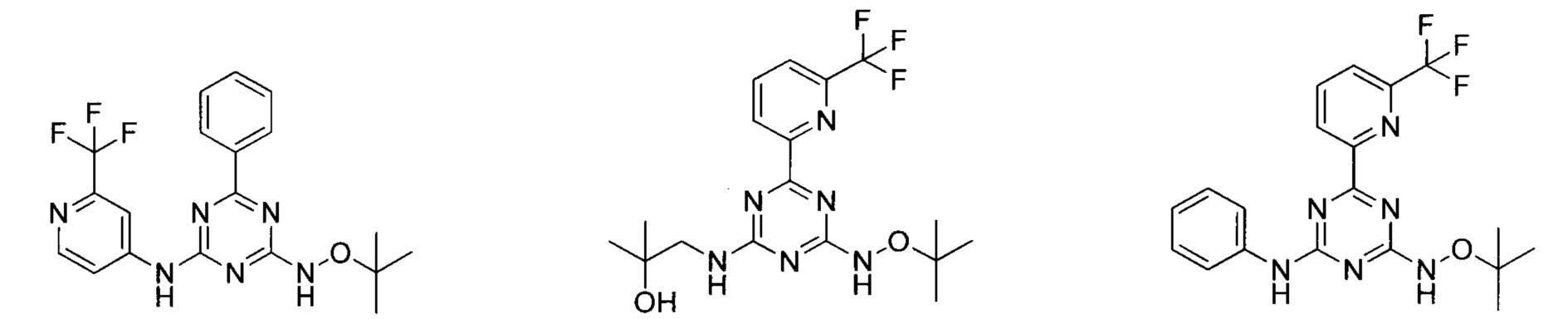
Результат интеллектуальной деятельности: ПРОИЗВОДНОЕ 1,3,5-ТРИАЗИНА И СПОСОБ ЕГО ПРИМЕНЕНИЯ
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Эта заявка претендует на приоритет по Китайской Патентной Заявке на Изобретение No. 201510459126.Х, поданной в Государственное Ведомство по Интеллектуальной Собственности Китайской Народной Республики 30 июля 2015 года, полное содержание которой включено в настоящий документ путем отсылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящая заявка относится к фармацевтической области и более конкретно к производному 1,3,5-триазина и способу его применения.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Являясь наиболее важным ключевым ферментом во внутриклеточном цикле трикарбоновой кислоты, IDH (полное название: изоцитратдегидрогеназа) может катализировать окислительное декарбоксилирование изолимонной кислоты до 2-оксоглутарата (т.е., α-кетоглутаровой кислоты). Исследования показали, что многие опухоли (такие как глиома, саркома и острый миелоцитарный лейкоз) имеют мутацию IDH в остатке аргинина в каталитическом центре (IDH1/R132H, IDH2/R140Q и IDH2/R172K). Мутированная IDH приобретает новую способность катализировать превращение α-кетоглутаровой кислоты (α-KG) в 2-гидроксиглутаровую кислоту (2-HG). Исследования показали, что структура α-кетоглутаровой кислоты аналогична структуре 2-гидроксиглутаровой кислоты, и 2-HG конкурирует с α-KG, тем самым уменьшая активность α-KG-зависимых ферментов и приводя к высокому метилированию хроматина. Считается, что такое суперметилирование препятствует нормальной дифференцировке клеток и приводит к чрезмерной пролиферации незрелых клеток, что приводит к раковым заболеваниям.
В 2013 году Agios Pharmaceuticals сообщала об ингибиторе IDH2/R140Q AGI-6780 (Science, 2013, 340, 622-626) и ингибиторе IDH1/R132H AGI-5198 (Science, 2013, 340, 626-630), и в WO 2015017821 раскрыт другой ингибитор IDH2/R140Q AG-221. AGI-6780 и AGI-5198 могут ингибировать образование 2-HG в клетках, несущих наиболее распространенный мутант IDH2 и наиболее распространенный мутант IDH1, соответственно. Эти молекулы не только ингибируют образование 2-HG, но также индуцируют дифференцирование аномально пролиферативных раковых клеток человека в культуре. Лечение лейкозных клеток, несущих мутант IDH2, с помощью AGI-6780, и лечение клеток глиомы, несущих мутант IDH1, с помощью AGI-5198, приводит к увеличенной экспрессии зрелых маркеров в этих клетках. Более того, исследователи обнаружили, что AGI-5198 может ингибировать скорость роста клеток глиомы либо путем обработки клеточных культур с помощью AGI-5198, либо путем перорального введения AGI-5198 мышам с трансплантированной опухолью.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте настоящая заявка относится к соединению формулы I:
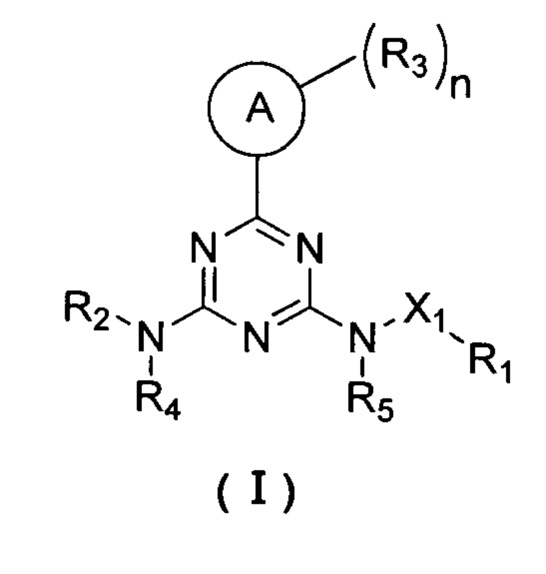
где:
кольцо А выбирается из бензольного кольца или 5- или 6-членного гетероароматического кольца, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S;
X1 выбирается из NH или О;
R1 выбирается из группы, состоящей из водорода, C1-6 алкила, C2-6 алкенила, С2-6 алкинила и С3-6 циклоалкила, где алкил, алкенил, алкинил или циклоалкил могут быть необязательно замещены одним или несколькими R6;
R2 выбирается из группы, состоящей из фенила, 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S, бензила, C1-6 алкила, C1-6 алкокси и C3-6 циклоалкила, и может быть необязательно замещен одним или несколькими R7;
каждый R3 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила;
R4 и R5 независимо выбираются из группы, состоящей из водорода, C1-6 алкила и C3-6 циклоалкила;
каждый R6 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, C1-6 алкила, C3-6 циклоалкила, фенила и 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S, и фенил или гетероарил могут быть необязательно замещен одним или несколькими R8;
каждый R7 и каждый R8 независимо выбираются из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила; и
n представляет собой 0, 1, 2 или 3;
или его фармацевтически приемлемой соли или гидрата.
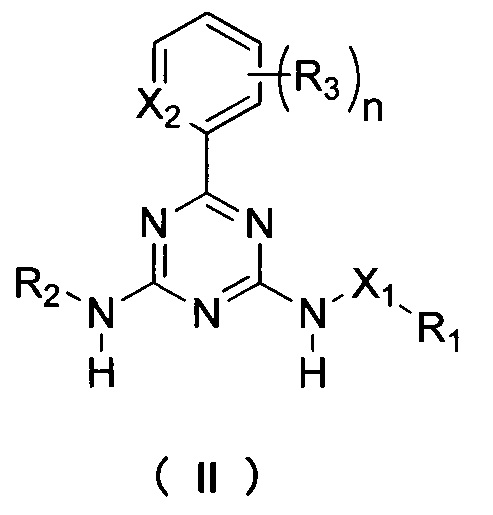
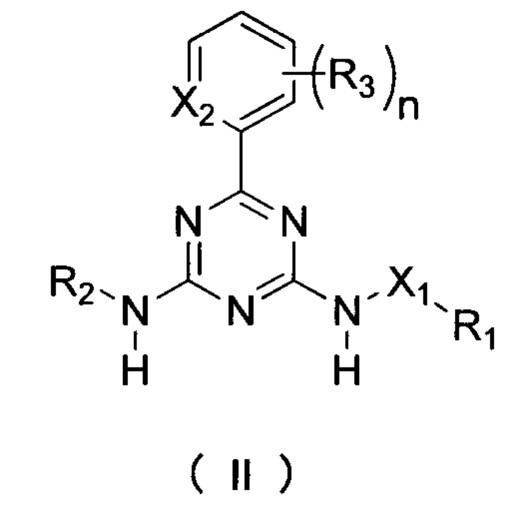
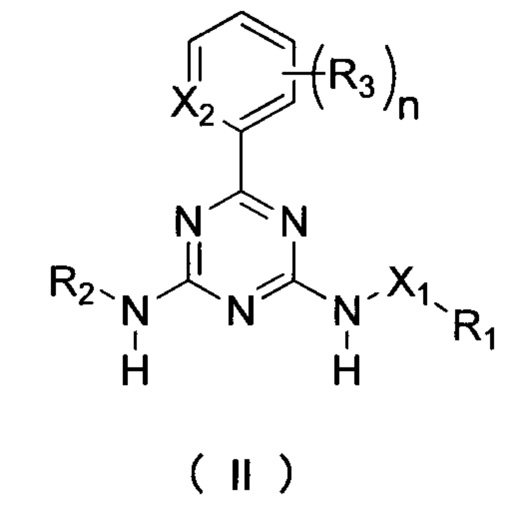
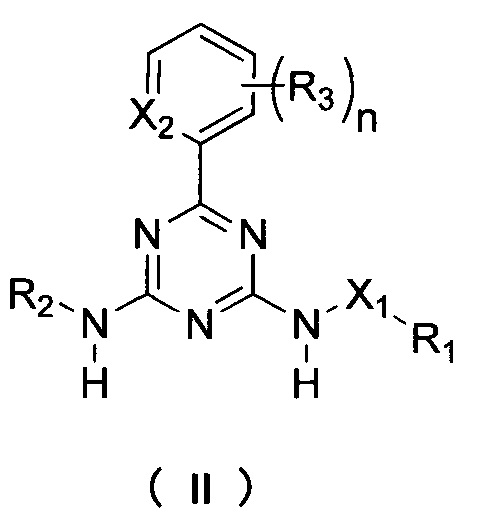
В другом аспекте настоящая заявка относится к соединению формулы II:

где:
X1 выбирается из NH или О;
Х2 выбирается из N или СН;
R1 выбирается из группы, состоящей из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила и C3-6 циклоалкила, где алкил, алкенил, алкинил или циклоалкил могут быть необязательно замещены одним или несколькими R6;
R2 выбирается из группы, состоящей из фенила, пиридила, бензила, C1-6 алкила, C2-6 алкокси и C3-6 циклоалкила, и может быть необязательно замещен одним или несколькими R7;
каждый R3 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила;
каждый R6 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, CF3, C1-6 алкила, C3-6 циклоалкила, фенила и 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S, и фенил или гетероарил могут быть необязательно замещен одним или несколькими R8;
каждый R7 и каждый R8 независимо выбираются из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила; и
n представляет собой 0, 1, 2 или 3;
или его фармацевтически приемлемой соли или гидрата.
В еще одном аспекте настоящая заявка относится к фармацевтической композиции, которая содержит терапевтически эффективное количество соединения формулы I или соединения формулы II или его фармацевтически приемлемой соли или гидрата, и один или несколько фармацевтически приемлемых носителей или эксципиентов.
В еще одном аспекте настоящая заявка относится к способу лечения рака, индуцированного мутацией IDH2, включающему введение субъекту, нуждающемуся в этом, соединения формулы I или соединения формулы II или его фармацевтически приемлемой соли или гидрата, или его фармацевтической композиции.
В еще одном аспекте настоящая заявка относится к применению соединения формулы I или соединения формулы II, или его фармацевтически приемлемой соли или гидрата, или его фармацевтической композиции при получении лекарственного средства для лечения рака, вызванного мутациями IDH2.
В еще одном аспекте настоящая заявка относится к соединению формулы I или соединению формулы II, или его фармацевтически приемлемой соли или гидрату, или его фармацевтической композиции для применения при лечении рака, вызванного мутациями IDH2.
В некоторых вариантах выполнения настоящей заявки мутация IDH2 представляет собой мутацию IDH2/R140Q или мутацию IDH2/R172K.
ПОДРОБНОЕ ОПИСАНИЕ
В нижеследующем описании некоторые конкретные детали включены для обеспечения полного понимания различных раскрытых вариантов выполнения изобретения. Однако специалистам в данной области техники будет понятно, что варианты выполнения изобретения могут быть осуществлены на практике без одной или нескольких из этих конкретных деталей или с другими способами, компонентами, материалами и т.п.
Если контекст не требует иного, то в описании и последующей формуле изобретения термин «содержать» и его английские вариации, такие как «содержит» и «содержащий», должны толковаться в открытом и инклюзивном смысле, то есть как «включая, но без ограничения».
Ссылка в этом описании на «один вариант выполнения изобретения», или «вариант выполнения изобретения», или «другой вариант выполнения изобретения», или «некоторые варианты выполнения изобретения» означает, что конкретный ссылочный элемент, структура или характеристики, описанные в связи с вариантом выполнения изобретения, включены, по меньшей мере, в один вариант выполнения изобретения. Соответственно, наличие фазы «в одном варианте выполнения изобретения», или «в варианте выполнения изобретения», или «в другом варианте выполнения изобретения», или «в некоторых вариантах выполнения изобретения» в разных местах по всему описанию не обязательно относится к одному и тому же варианту выполнения изобретения. Кроме того, конкретные элементы, структуры или характеристики могут быть объединены любым подходящим способом в одном или нескольких вариантах выполнения изобретения.
Следует отметить, что, как используется в этом описании и прилагаемой формуле изобретения, единственные формы «а», «an» и «the» включают множественные ссылки, если содержание явно не указывает на иное. Так, например, ссылка на реакцию, в которой участвует «катализатор», включает в себя один катализатор, или два, или более катализаторов. Если в настоящем документе иное прямо не указано, следует также отметить, что термин «или» обычно используется в его смысле, включая «и/или», если только содержание явно не указывает на иное.
ОПРЕДЕЛЕНИЯ
Если не указано иное, следующие термины и фразы, используемые в настоящем документе, имеют следующие значения. Конкретный термин или фраза не считаются неясными или неопределенными, если они не определены специально. Его следует понимать в соответствии с его общим значением. Используемое здесь торговое наименование относится к соответствующему продукту или его активному ингредиенту.
Термин «необязательный» или «необязательно» означает, что описанное впоследствии событие или обстоятельство может или не может произойти, и что описание включает случаи, когда происходит указанное событие или обстоятельство, и случаи, когда указанное событие или обстоятельство не происходит. Например, выражение, что этил «необязательно» замещен галогеном, означает, что этил может быть незамещенным (CH2СН3), монозамещенным (таким как CH2CH2F), полизамещенным (таким как CHFCH2F, CH2CHF2 и так далее) или полностью замещенным (CF2CF3). Специалист в данной области техники поймет, что в отношении любой группы, содержащей один или несколько заместителей, любое замещение или способ замещения, которые пространственно невозможны и/или не могут быть синтезированы, не будут включены.
Используемое в настоящем документе выражение Cm-n означает, что этот фрагмент имеет m-n углеродных атомов. Например, «C3-10 циклоалкил» означает, что указанный циклоалкил имеет от 3 до 10 атомов углерода. «С0-6 алкилен» означает, что указанный алкилен имеет от 0 до 6 атомов углерода, и алкилен представляет собой химическую связь, когда группа имеет 0 атомов углерода.
Численный диапазон в настоящем документе относится к каждому из целых чисел в этом заданном диапазоне. Например, «C1-10» означает, что группа может иметь 1 атом углерода, 2 атома углерода, 3 атома углерода, 4 атома углерода, 5 атомов углерода, 6 атомов углерода, 7 атомов углерода, 8 атомов углерода, 9 атомов углерода или 10 атомов углерода.
Термин «замещенный» означает, что один или несколько атомов водорода на данном атоме замещены заместителем при условии, что данный атом имеет нормальное валентное состояние, а соединение после замещения является стабильным. Когда заместитель представляет собой кето (т.е., =O), что означает замену двух атомов водорода, замена кето не будет происходить в ароматической группе.
Когда любой вариант (такой как R) имеет место более одного раза в композиции или структуре соединения, он определяется независимо в каждом случае. Поэтому, например, если группа замещена от 0 до 2R, тогда группа может быть необязательно замещена не более чем двумя R, и R имеет независимый вариант в каждом случае. Кроме того, комбинация заместителей и/или их вариантов допускается только в том случае, если такая комбинация приведет к стабильному соединению.
Если не указано иное, термин «гетеро» означает гетероатом или гетероатомную группу (т.е., группу, содержащую гетероатом), то есть атомы, за исключением атомов углерода и водорода, или группу атомов, содержащую такие атомы. Гетероатом независимо выбирается из группы, состоящей из кислорода, азота, серы, фосфора, кремния, германия, алюминия и бора. В варианте выполнения изобретения, в котором участвуют два или более гетероатома, два или более гетероатома могут быть одинаковыми или части или все два или более гетероатома могут быть разными.
Термин «галоген» или «гало» относится к любой группе из фторо, хлоро, бромо и йодо.
Термин «гидрокси» относится к -ОН.
Термин «циано» относится к -CN.
Термин «амино» относится к -NH2, -NH(алкил) и -N(алкил)2, а конкретные примеры амино включают, но без ограничения, -NH2, -NHCH3, -NHСН(СН3)2, -N(CH3)2, -NHC2H5, -N(CH3)C2H5 и т.п.
Термин «алкил» относится к насыщенной алифатической углеводородной группе с прямой или разветвленной цепью, состоящей из атомов углерода и атомов водорода, такой как метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил и децил. Конкретный алкил включает все его изомеры. Например, пропил включает -CH2CH2СН3 и -СН(CH3)2. Например, бутил включает -CH2CH2CH2СН3, -СН(СН3)(CH2СН3), -С(СН3)3 и -СН2СН(CH3)2. Термин «C1-8 алкил» относится к алкилу с 1-8 атомами углерода. Термин «C1-6 алкил» относится к алкилу с 1-6 атомами углерода. Термин «C1-4 алкил» относится к алкилу с 1-4 атомами углерода. Термин «С1-3 алкил» относится к алкилу с 1-3 атомами углерода. «Алкил», «C1-8 алкил», «C1-6 алкил», «C1-4 алкил» и «C1-3 алкил» могут быть незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галоген и амино.
Термин «алкенил» относится к алифатической углеводородной группе с прямой или разветвленной цепью, содержащей от 2 до 12 атомов углерода и имеющей одну или несколько двойных связей. Примеры алкенила включают, но без ограничения, этенил, аллил, пропенил, 2-бутенил и 3-гексенил. Один из двухсвязных атомов углерода может быть необязательно местом присоединения алкенильного заместителя.
Термин «алкинил» относится к алифатической углеводородной группе с прямой или разветвленной цепью, содержащей от 2 до 12 атомов углерода и имеющей одну или несколько тройных связей. Примеры алкинила включают, но без ограничения, этинил, пропаргил и 3-гексинил. Один из трехсвязанных атомов углерода может быть необязательно местом присоединения алкинильного заместителя.
Термин «циклоалкил» относится к моноциклической насыщенной алифатической углеводородной группе, состоящей исключительно из атомов углерода и атомов водорода, такой как С3-20 циклоалкил, предпочтительно С3-6 циклоалкил, такой как циклопропил, циклобутил, циклопентил и циклогексил. Циклоалкил может быть незамещенным или замещенным, и заместитель включает, но без ограничения, алкил, алкокси, циано, карбокси, арил, гетероарил, амино, галоген, сульфонил, сульфинил, фосфорил, гидрокси и т.п.
Термин «алкокси» относится к -О-алкильной группе.
Термин «гетероароматическое кольцо» относится к моноциклическому или конденсированному кольцу, содержащему от 5 до 12 кольцевых атомов, таких как 5, 6, 7, 8, 9, 10, 11 или 12 кольцевых атомов, где 1, 2, 3 или 4 кольцевых атомов выбраны из группы, состоящей из N, О и S, а остальная часть атома (атомов) кольца является атомом углерода, и кольцо имеет полностью сопряженную систему пи-электронов.
Термин «гетероарил» относится к оставшейся группе после удаления одного атома водорода из молекулы «гетероараматического кольца». Гетероарил может быть незамещенным или замещенным, и заместитель включает, но без ограничения, алкил, алкокси, арил, аралкил, амино, галоген, гидрокси, циано, нитро, карбонил, гетероалициклическую группу и т.п. Неограничивающие примеры незамещенного гетероарила включают, но без ограничения, пирролил, фурил, тиенил, пиразолил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, оксадиазолил, тиадиазолил, индолил, бензофурил, бензотиенил, бензоксазолил, бензотиазолил, бензоимидазолил, пиридил, пиримидил, пиразинил, пиридазинил, хинолил, изохинолил, триазолил, тетразолил, триазинил, птеридинил и т.д.
Термин «фармацевтически приемлемый» относится к соединению, материалу, композиции и/или дозированной форме, которые применимы для контакта с тканями человека и животного без чрезмерной токсичности, раздражения, аллергической реакции или других проблем или осложнений в рамках подтвержденного врачебного мнения и соизмеримы с приемлемым соотношением польза/риск.
Термин «фармацевтически приемлемый носитель» относится к тем носителям, которые не вызывают существенной стимуляции организма и не ухудшают биологическую активность и свойства активного соединения. «Фармацевтически приемлемый носитель» также относится к инертному веществу, которое вводится вместе с активным ингредиентом и полезно для его введения, включая, но без ограничения, любые скользящие вещества, подслащивающие агенты, разбавители, консерванты, краски/красители, ароматизирующие агенты, поверхностно-активные вещества, смачивающие агенты, диспергаторы, разрыхлители, суспендирующие агенты, стабилизаторы, изотонические агенты, растворители и эмульгаторы, которые были одобрены Государственным Управлением по Контролю за Продуктами и Лекарственными Средствами как приемлемые для использования на людях или животных (таких как скот). Неограничивающие примеры указанного носителя включают карбонат кальция, фосфат кальция, различные сахара и крахмалы, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли. Другая информация о носителе может быть найдена в Remington: The Science and Practice of Pharmacy, 21st Ed., Lippincott, Williams & Wilkins (2005), содержание которой включено настоящий документ путем ссылки.
Термин «эксципиент» обычно относится к носителю, разбавителю и/или среде, используемым для приготовления эффективной фармацевтической композиции.
Что касается лекарственного средства или фармакологически активного агента, термин «эффективное количество» или «терапевтически эффективное количество» относится к количеству лекарственного средства или агента, которое не является токсичным, но достаточным для достижения желаемого эффекта. Для пероральной лекарственной формы в настоящей заявке «эффективное количество» активного вещества в фармацевтической композиции относится к количеству, которое требуется для достижения желаемого эффекта в комбинации с другим активным веществом в композиции. Эффективное количество может определяться индивидуально в зависимости от возраста и общего состояния субъекта, а также конкретного активного вещества. Соответствующее эффективное количество в конкретном случае может быть определено специалистом в данной области техники посредством рутинного тестирования.
Термин «активный ингредиент», «терапевтический агент», «активное вещество» или «активный агент» относится к химическому веществу, которое может эффективно лечить целевые расстройства, заболевания или состояния.
Термин «пациент» или «субъект» включает человека и животное, такое как млекопитающее (такое как примат, корова, лошадь, свинья, собака, кошка, мышь, крыса, кролик, коза, овца, домашняя птица и т.д.).
СОЕДИНЕНИЕ В СООТВЕТСТВИИ С ОБЩИМИ ФОРМУЛАМИ
В одном аспекте настоящая заявка относится к соединению формулы I:
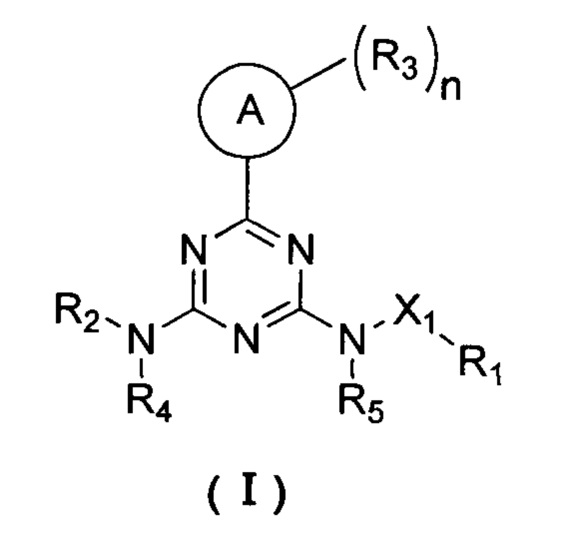
где:
кольцо А выбирается из бензольного кольца или 5- или 6-членного гетероароматического кольца, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S;
X1 выбирается из NH или О;
R1 выбирается из группы, состоящей из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила и C3-6 циклоалкила, где алкил, алкенил, алкинил или циклоалкил могут быть необязательно замещены одним или несколькими R6;
R2 выбирается из группы, состоящей из фенила, 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S, бензила, C1-6 алкила, C1-6 алкокси и C3-6 циклоалкила, и может быть необязательно замещен одним или несколькими R7;
каждый R3 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила;
R4 и R5 независимо выбираются из группы, состоящей из водорода, C1-6 алкила и C3-6 циклоалкила;
каждый R6 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, C1-6 алкила, C3-6 циклоалкила, фенила и 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S, и фенил или гетероарил могут быть необязательно замещены одним или несколькими R8;
каждый R7 и каждый R8 независимо выбираются из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила; и
n представляет собой 0, 1, 2 или 3;
или его фармацевтически приемлемой соли или гидрату.
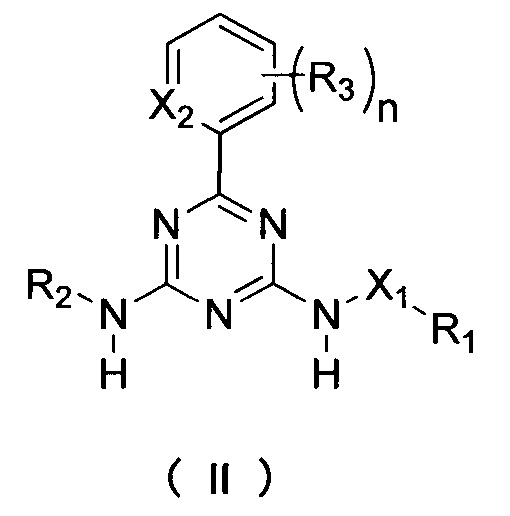
В варианте выполнения настоящей заявки соединение формулы II представляет собой:
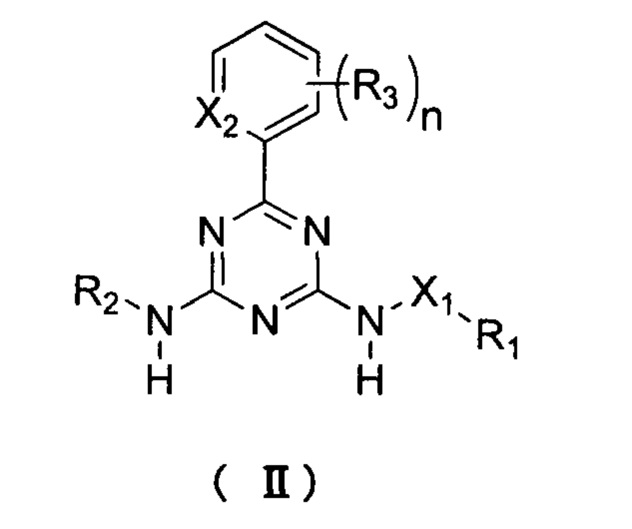
где:
X1 выбирается из NH или О;
Х2 выбирается из N или СН;
R1 выбирается из группы, состоящей из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила и C3-6 циклоалкила, где алкил, алкенил, алкинил или циклоалкил могут быть необязательно замещены одним или несколькими R6;
R2 выбирается из группы, состоящей из фенила, пиридила, бензила, C1-6 алкила, C1-6 алкокси и C3-6 циклоалкила, и может быть необязательно замещен одним или несколькими R7;
каждый R3 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила;
каждый R6 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, CF3, C1-6 алкила, C3-6 циклоалкила, фенила и 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S, и фенил или гетероарил могут быть необязательно замещены одним или несколькими R8;
каждый R7 и каждый R8 независимо выбираются из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила; и
n представляет собой 0, 1, 2 или 3;
или его фармацевтически приемлемую соль или гидрат.
В варианте выполнения настоящей заявки предпочтительным является соединение формулы II или его фармацевтически приемлемая соль или гидрат, где:
X1 выбирается из О;
Х2 выбирается из N или СН;
R1 выбирается из группы, состоящей из водорода, C1-6 алкила, C2-6 алкенила, С2-6 алкинила и С3-6 циклоалкила, где алкил, алкенил, алкинил или циклоалкил могут быть необязательно замещены одним или несколькими R6;
R2 выбирается из группы, состоящей из фенила, пиридила, бензила, C1-6 алкила, C1-6 алкокси и C3-6 циклоалкила, и может быть необязательно замещен одним или несколькими R7;
каждый R3 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила;
каждый R6 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, CF3, C1-6 алкила, C3-6 циклоалкила, фенила и 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, выбранные из группы, состоящей из N, О и S, и фенил или гетероарил могут быть необязательно замещены одним или несколькими R8;
каждый R7 и каждый R8 независимо выбирается из группы, состоящей из галогена, гидрокси, амино, C1-3 галогеналкила, циано, C1-6 алкила и C3-6 циклоалкила; и
n представляет собой 0, 1 или 2.
В одном варианте выполнения настоящей заявки предпочтительным является соединение формулы II или его фармацевтически приемлемая соль или гидрат, где X1 представляет собой О; R1 выбирается из C1-6 алкила и может быть необязательно замещен одним или несколькими R6; и каждый R6 независимо выбирается из группы, состоящей из гидрокси, фенила и С3-6 циклоалкила. Более предпочтительно, R1 выбирается из группы, состоящей из метила, этила, пропила и бутила, и может быть необязательно замещен 1 или 2 R6; и каждый R6 независимо выбирается из группы, состоящей из гидрокси, фенила и циклопропила.
В одном варианте выполнения настоящей заявки предпочтительным является соединение формулы II или его фармацевтически приемлемая соль или гидрат, где X1 представляет собой О; R2 выбирается из группы, состоящей из фенила, пиридила, бензила, метила, этила, пропила, бутила, метокси, этокси, пропокси и бутокси, и может быть необязательно замещен 1 или 2 R7; и каждый R7 независимо выбирается из группы, состоящей из гидрокси, C1-3 галогеналкила и C1-6 алкила. Более предпочтительно, R2 выбирается из группы, состоящей из фенила, пиридила, бензила, пропила, бутила и этокси, и может быть необязательно замещен одним или несколькими R7; и каждый R7 независимо выбирается из гидрокси или трифторметила.
В одном варианте выполнения настоящей заявки предпочтительным является соединение формулы II или его фармацевтически приемлемая соль или гидрат, где X1 представляет собой О; n равно 0 или 1; и R3 представляет собой C1-3 галогеналкил. Более предпочтительно, n равно 0 или 1 и R3 выбирается из трифторметила.
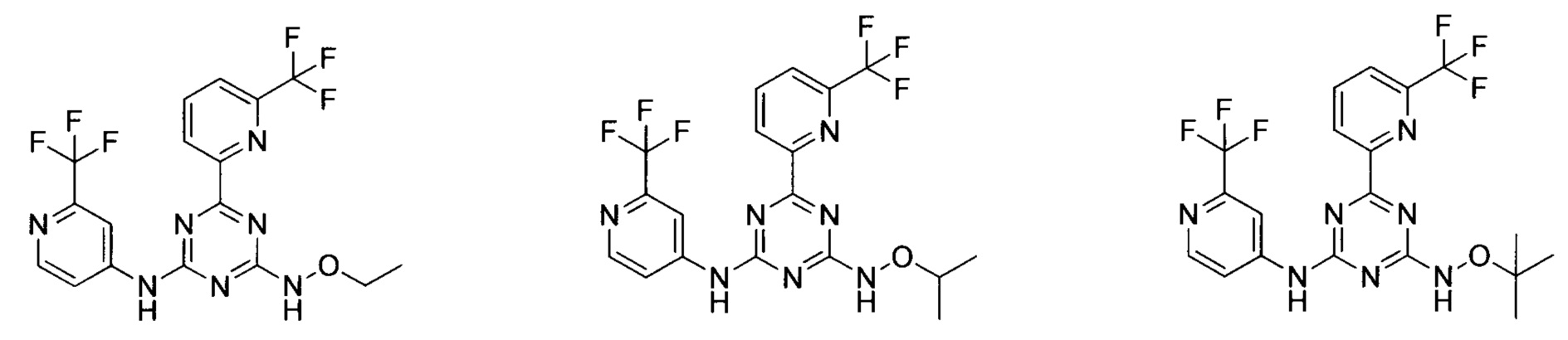
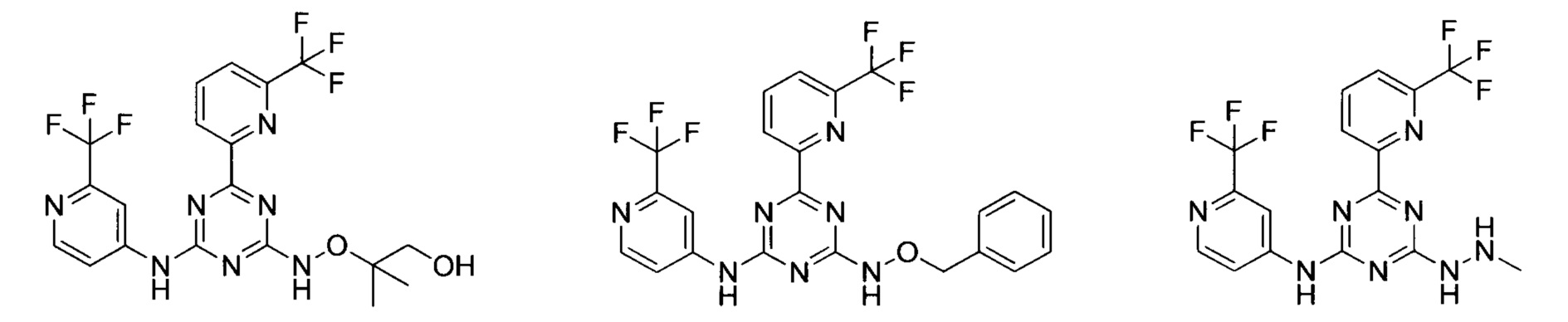
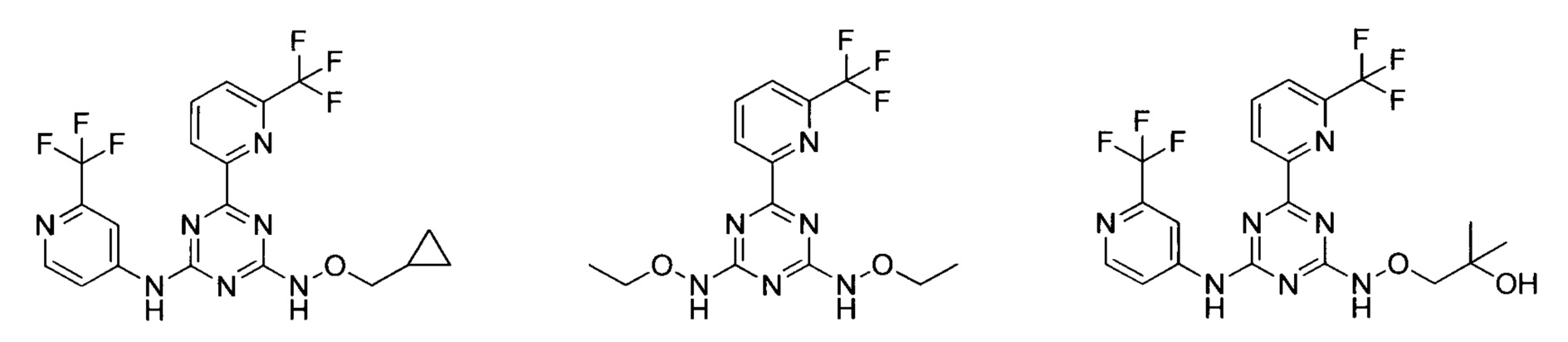
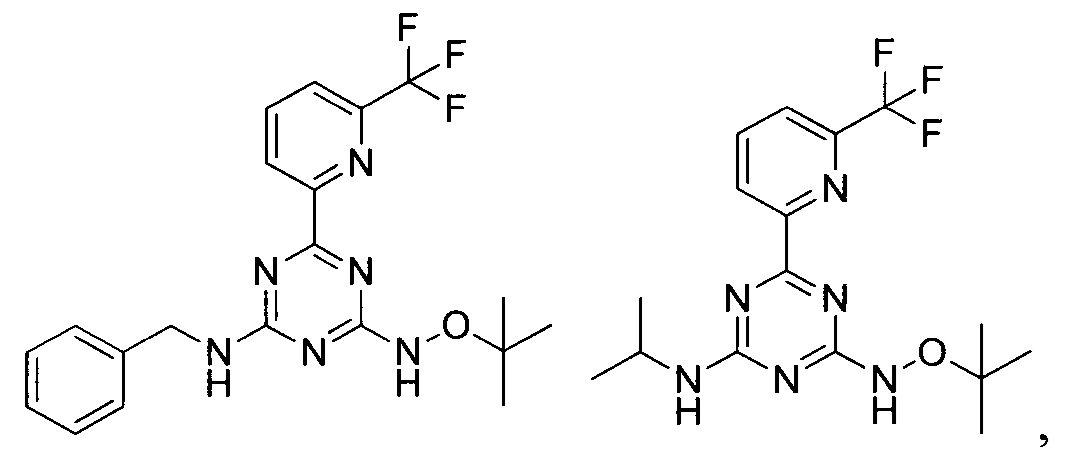
В варианте выполнения настоящей заявки предпочтительными являются следующие соединения:
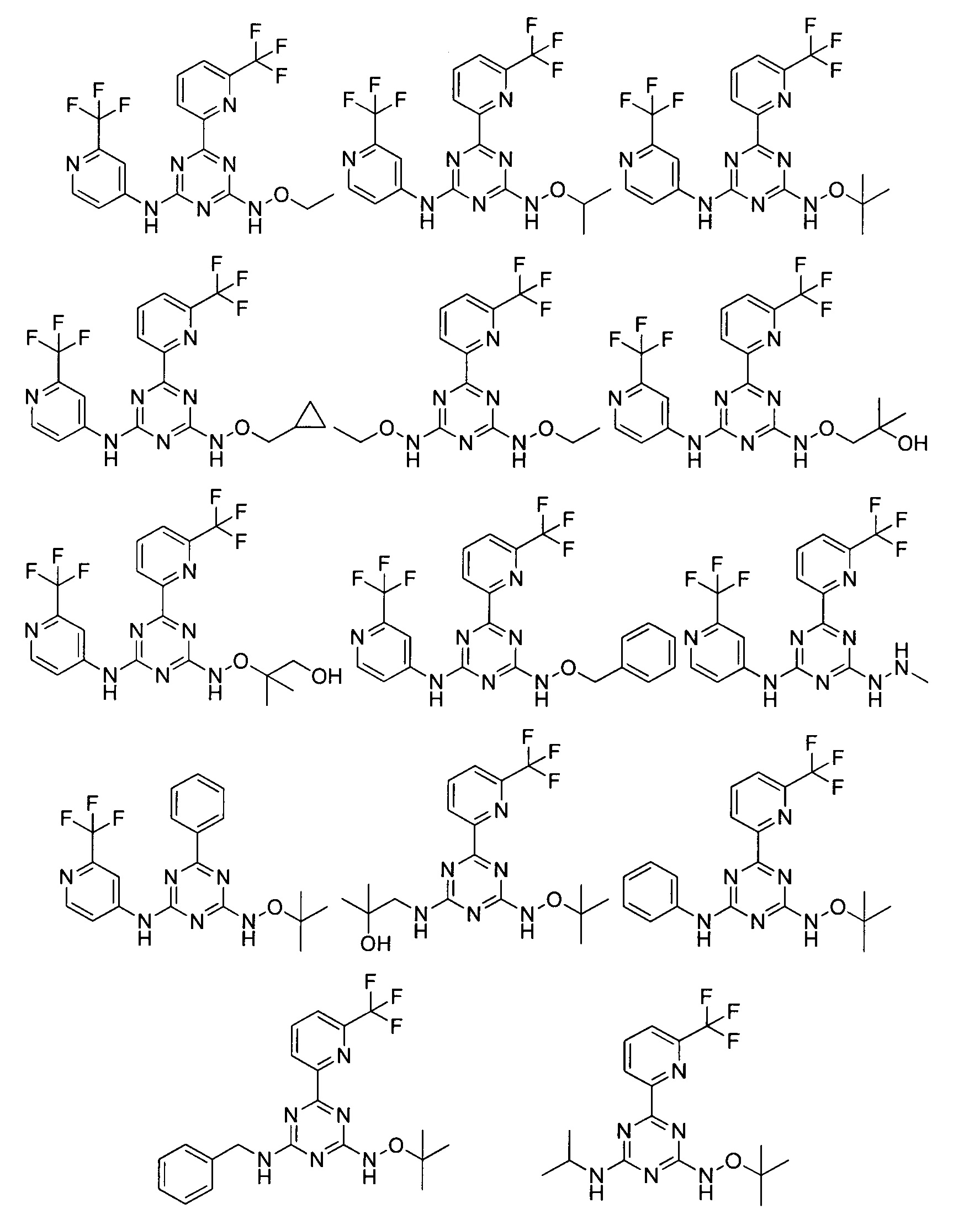
или их фармацевтически приемлемые соли или гидрат.
Фармацевтически приемлемые соли соединения формулы I или соединения формулы II могут относиться, например, к солям металлов, аммониевым солям, солям, образованным с органическими основаниями, солям, образованным с неорганическими кислотами, солям, образованным с органическими кислотами, солям, образованным с основными или кислотными аминокислотами, и т.п. Неограничивающие примеры солей металлов включают, но без ограничения, соли щелочных металлов, такие как соли натрия, соли калия и так далее; соли щелочноземельных металлов, такие как соли кальция, соли магния и соли бария; соли алюминия и т.п. Неограничивающие примеры солей, образованных с органическими основаниями, включают, но без ограничения, соли, образованные с триметиламином, триэтиламином, пиридином, метилпиридином, 2,6-диметилпиридином, этаноламином, диэтаноламином, триэтаноламином, циклогексиламином, дициклогексиламином и т.п. Неограничивающие примеры солей, образованных с неорганическими кислотами, включают, но без ограничения, соли, образованные с соляной кислотой, бромоводородной кислотой, азотной кислотой, серной кислотой, фосфорной кислотой и т.п. Неограничивающие примеры солей, образованных с органическими кислотами, включают, но без ограничения, соли, образованные с муравьиной кислотой, уксусной кислотой, трифторуксусной кислотой, фумаровой кислотой, щавелевой кислотой, яблочной кислотой, малеиновой кислотой, винной кислотой, лимонной кислотой, янтарной кислотой, метансульфоновой кислотой, бензолсульфоновой кислотой, 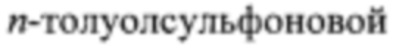 кислотой и т.п. Неограничивающие примеры солей, образованных с основными аминокислотами, включают, но без ограничения, соли, образованные с аргинином, лизином, орнитином и т.п. Неограничивающие примеры солей, образованных с кислотными аминокислотами, включают, но без ограничения, соли, образованные с аспарагиновой кислотой, глутаминовой кислотой и т.п.
кислотой и т.п. Неограничивающие примеры солей, образованных с основными аминокислотами, включают, но без ограничения, соли, образованные с аргинином, лизином, орнитином и т.п. Неограничивающие примеры солей, образованных с кислотными аминокислотами, включают, но без ограничения, соли, образованные с аспарагиновой кислотой, глутаминовой кислотой и т.п.
Фармацевтически приемлемые соли по настоящей заявке могут быть получены из исходного соединения, содержащего кислотную или основную группу, посредством обычного химического способа. Как правило, такие соли могут быть получены в результате реакции соединения в форме свободной кислоты или свободного основания со стехиометрическим подходящим основанием или кислотой в воде, органическом растворителе или в их смеси. Как правило, предпочтительной является неводная среда, такая как эфир, этилацетат, этанол, изопропанол, ацетонитрил и т.п.
Соединение формулы I или соединение формулы II по настоящей заявке может существовать в несольватированной или сольватированной форме, включая гидратную форму. В общем, сольватированная форма эквивалентна несольватированной форме, обе из которых включены в объем настоящей заявки. Соединение формулы I или соединение формулы II по настоящей заявке может существовать в полиморфной или аморфной форме.
Соединение формулы I или соединение формулы II по настоящей заявке может иметь асимметричный атом углерода (оптический центр) или двойную связь. Рацематы, диастереомеры, геометрические изомеры и индивидуальные изомеры - все включены в объем настоящей заявки.
Графические изображения рацемических, амбискалемических и скалемических или энантиомерно чистых соединений в настоящей заявке получены из Maehr, J.Chem. Ed. 1985, 62: 114-120. Если не указано иное, сплошные и пунктирные клинья используются для обозначения абсолютной конфигурации стереоцентра. Когда соединение формулы I или соединение формулы II по настоящей заявке содержит олефиновую двойную связь (связи) или другой геометрический асимметричный центр (центры), то, если не указано иное, геометрические изомеры Е и Z также охвачены. Аналогично, все таутомерные формы также охвачены в рамках настоящей заявки.
Соединение формулы I или соединение формулы II по настоящей заявке могут иметь особые геометрические или стереоизомерные формы. Такие соединения, включая цис- и транс-изомеры, (-)- и (+)-энантиомеры, (R)- и (S)-энантиомеры, диастереомеры, (D)-изомеры, (L)-изомеры и рацемическая смесь и другие их смеси, такие как энантиомерно или диастереоизомерно обогащенные смеси, все включены в объем настоящей заявки. В заместителе могут присутствовать дополнительные асимметрические атомы углерода, такие как алкил и другие. Все эти изомеры и их смеси также включены в объем настоящей заявки.
Оптически активные (R)- и (S)-изомеры и D и L изомеры могут быть получены хиральным синтезом, или хиральным реагентом, или другими общепринятыми способами. Если требуется энантиомер соединения по настоящей заявке, то его можно получить асимметрическим синтезом или дериватизацией с помощью хирального вспомогательного вещества, в котором желаемый чистый энантиомер получают путем отделения полученной диастереомерной смеси и расщепления вспомогательной группы. Альтернативно, молекула, содержащая основную функциональную группу (такую как амино) или кислотную функциональную группу (такую как карбокси), образует диастереомерную соль с подходящей кислотой или основанием, имеющими оптическую активность, и затем диастереомерное разделение проводят фракционной кристаллизацией или хроматографией, которые хорошо известны специалисту в данной области техники, для получения чистого энантиомера. Кроме того, разделение энантиомеров и диастереомеров обычно проводят с помощью хроматографии, в которой используется хиральная стационарная фаза, и необязательно объединяют со способом химического разделения (например, с образованием карбамата из амина).
Соединение формулы I или соединение формулы II по настоящей заявке может содержать атомный изотоп с неприродным соотношением на одном или более атомах, составляющих указанное соединение. Например, соединение может быть изотопно мечено радиоизотопами, такими как тритий (3Н), йод-125 (125I) или углерод-14 (14С). Все изотопные вариации соединения формулы I или соединения формулы II по настоящей заявке независимо от того, являются ли они радиоактивными или нет, включены в объем настоящей заявки.
ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
В другом аспекте настоящая заявка относится к фармацевтической композиции, включающей соединение формулы I, или соединение формулы II, или его фармацевтически приемлемую соль, или гидрат и один или несколько фармацевтически приемлемых носителей или эксципиентов. Фармацевтическая композиция по настоящему изобретению может дополнительно содержать один или несколько дополнительных терапевтических агентов.
Фармацевтическая композиция по настоящему изобретению может быть получена путем объединения соединения формулы I, или соединения формулы II, или его фармацевтически приемлемой соли, или гидрата в соответствии с настоящей заявкой с соответствующими фармацевтически приемлемыми носителями или эксципиентами. Например, фармацевтическая композиция по настоящему изобретению может быть приготовлена в виде твердых, полутвердых, жидких или газообразных составов, таких как таблетки, пилюли, капсулы, порошки, гранулы, мази, эмульсии, суспензии, растворы, суппозитории, инъекции, ингалянты, гели, микросферы, аэрозоли и т.п.
Типичные пути введения соединения формулы I или соединения формулы II или его фармацевтически приемлемой соли, или гидрата, или его фармацевтической композиции по настоящему изобретению включают, но без ограничения, пероральное, ректальное, трансмукозальное, энтеральное или местное, трансдермальное, ингаляционное, парентеральное, подъязычное, внутривагинальное, интраназальное, внутриглазное, внутрибрюшинное, внутримышечное, подкожное и внутривенное введение.
Фармацевтическая композиция по настоящему изобретению может быть изготовлена с использованием способа, хорошо известного специалисту в данной области техники, такого как обычный способ смешивания, способ растворения, способ гранулирования, способ изготовления драже, способ измельчения, способ эмульгирования, способ лиофилизации и т.п.
Для перорального введения фармацевтическая композиция может быть получена путем смешивания соединения формулы I, или соединения формулы II, или его фармацевтически приемлемой соли, или гидрата с фармацевтически приемлемыми носителями или эксципиентами, хорошо известными специалисту в данной области техники. Такие носители или эксципиенты позволяют получить соединение формулы I, или соединение формулы II, или его фармацевтически приемлемую соль, или гидрат в виде таблеток, пилюль, леденцов, драже, капсул, жидкостей, гелей, кашиц, суспензии и т.п., которые используются для перорального введения пациенту.
Твердая пероральная фармацевтическая композиция может быть приготовлена обычным способом смешивания, наполнения или таблетирования. Например, ее можно получить смешиванием соединения формулы I, или соединения формулы II, или его фармацевтически приемлемой соли или гидрата с твердым эксципиентом, необязательно измельчением полученной смеси, при необходимости, добавлением других подходящих вспомогательных веществ и последующей обработкой смеси в гранулы для получения ядер для таблетки или драже. Соответствующие вспомогательные вещества включают, но без ограничения, связующие вещества, разбавители, дезинтегрирующие агенты, смазывающие вещества, скользящие вещества, подслащивающие агенты, ароматизаторы и т.п., такие как микрокристаллическая целлюлоза, раствор глюкозы, слизь из акации, раствор желатина, сахарозная и крахмальная паста; тальк, крахмал, стеарат магния, стеарат кальция или стеариновая кислота; лактоза, сахароза, крахмал, маннит, сорбит или дикальцийфосфат; диоксид кремния; поперечносшитая натриевая соль карбоксиметилцеллюлозы, прежелатинизированный крахмал, гликолят крахмала натрия, альгиновая кислота, кукурузный крахмал, картофельный крахмал, метилцеллюлоза, агар, карбоксиметилцеллюлоза, сшитый поливинилпирролидон и т.п. Ядра драже могут быть необязательно покрыты с использованием общеизвестного способа в области фармацевтики, особенно с использованием энтеросолюбильного покрытия.
Фармацевтическая композиция по настоящему изобретению также может быть адаптирована для парентерального введения, такого как стерильный раствор, суспензия или лиофилизированный продукт в соответствующей единичной дозированной форме. Для приготовления дозированных форм, подходящих для парентерального введения, можно использовать подходящий эксципиент, такой как наполнитель, буферный агент или поверхностно-активное вещество.
ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ
В другом аспекте настоящая заявка относится к способу лечения опухолей, индуцированных мутацией IDH2, включающему введение субъекту, нуждающемуся в этом, соединения формулы I, или соединения формулы II, или его фармацевтически приемлемой соли, или гидрата, или его фармацевтической композиции.
В еще одном аспекте настоящая заявка относится к применению соединения формулы I, или соединения формулы II, или его фармацевтически приемлемой соли, или гидрата, или его фармацевтической композиции при получении лекарственного средства для лечения рака, вызванного мутациями IDH2.
В еще одном аспекте настоящая заявка относится к соединению формулы I, или соединению формулы II, или его фармацевтически приемлемой соли, или гидрату, или его фармацевтической композиции для применения при лечении рака, вызванного мутациями IDH2.
В некоторых вариантах выполнения настоящей заявки мутация IDH2 представляет собой мутацию IDH2/R140Q или мутацию IDH2/R172K.
В некоторых вариантах выполнения настоящей заявки рак, вызванный мутацией IDH2, выбран из группы, состоящей из глиобластомы (нейроглиомы), миелодиспластического синдрома (MDS), миелопролиферативного новообразования (MPN), острой миелогенной лейкемии (AML), саркомы, меланомы, немелкоклеточного рака легкого, хондросаркомы, рака желчных протоков и ангиоиммунобластной неходжкинской лимфомы (NHL). В более конкретных вариантах выполнения изобретения рак, подлежащий лечению, выбирается из группы, состоящей из нейроглиомы, миелодиспластического синдрома (MDS), миелопролиферативного новообразования (MPN), острого миелогенного лейкоза (AML), меланомы, хондросаркомы, ангиоиммунобластной неходжкинской лимфомы (NHL), и т.д., предпочтительно, включая острый миелоидный лейкоз (AML) или саркому.
Соединение формулы I, или соединение формулы II, или его фармацевтически приемлемая соль, или его фармацевтическая композиция могут быть введены любым подходящим путем и способом, например, путем перорального введения или парентерального введения (таким как внутривенное введение). Соединение формулы I, или соединение формулы II, или его фармацевтически приемлемая соль, или его фармацевтическая композиция могут быть введены субъекту, нуждающемуся в этом, в терапевтически эффективном количестве. Соединение формулы I или соединение формулы II вводят в дозировке от около 0,0001 до около 20 мг/кг массы тела в день, такой как от около 0,001 до около 10 мг/кг массы тела/день.
Частота введения соединения формулы I или соединения формулы II по настоящей заявке зависит от потребностей пациента, например, один раз в день, или два раза в день, или более раз в день. Введение может быть с перерывами. Например, пациент получает ежедневную дозу соединения формулы I или соединения формулы II в течение нескольких дней, но затем не получает ежедневную дозу соединения формулы I или соединения формулы II в течение периода в несколько или более дней.
ПОЛУЧЕНИЕ
Соединение формулы I или соединение формулы II по настоящей заявке можно получить с помощью различных синтетических способов, хорошо известных специалистам в данной области техники, включая конкретные варианты выполнения, проиллюстрированные ниже, варианты выполнения, образованные комбинацией таких конкретных вариантов выполнения с другими химическими способами синтеза, и эквивалентов, хорошо известных специалисту в данной области техники. Предпочтительные варианты выполнения изобретения включают, но без ограничения, рабочие Примеры в настоящей заявке.
Химическая реакция в конкретных вариантах выполнения настоящей заявки проводится в подходящем растворителе, который должен быть подходящим для химического превращения (превращений), и требуемого реагента (реагентов), и материала (материалов) в настоящей заявке. Чтобы получить соединение формулы I или соединение формулы II по настоящей заявке, специалисту в данной области техники иногда требуется сделать модификацию или выбор стадии (стадий) синтеза или процедуры (процедур) реакции на основе существующих вариантов выполнения изобретения.
Соединение формулы II по настоящей заявке может быть получено специалистом в области органического синтеза с использованием стандартного способа по следующей схеме:
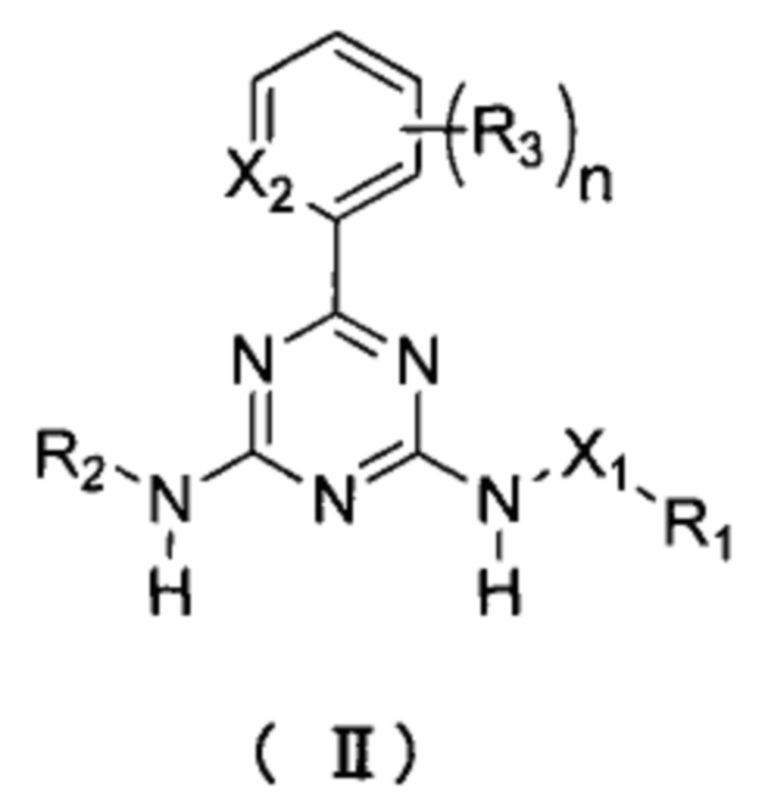
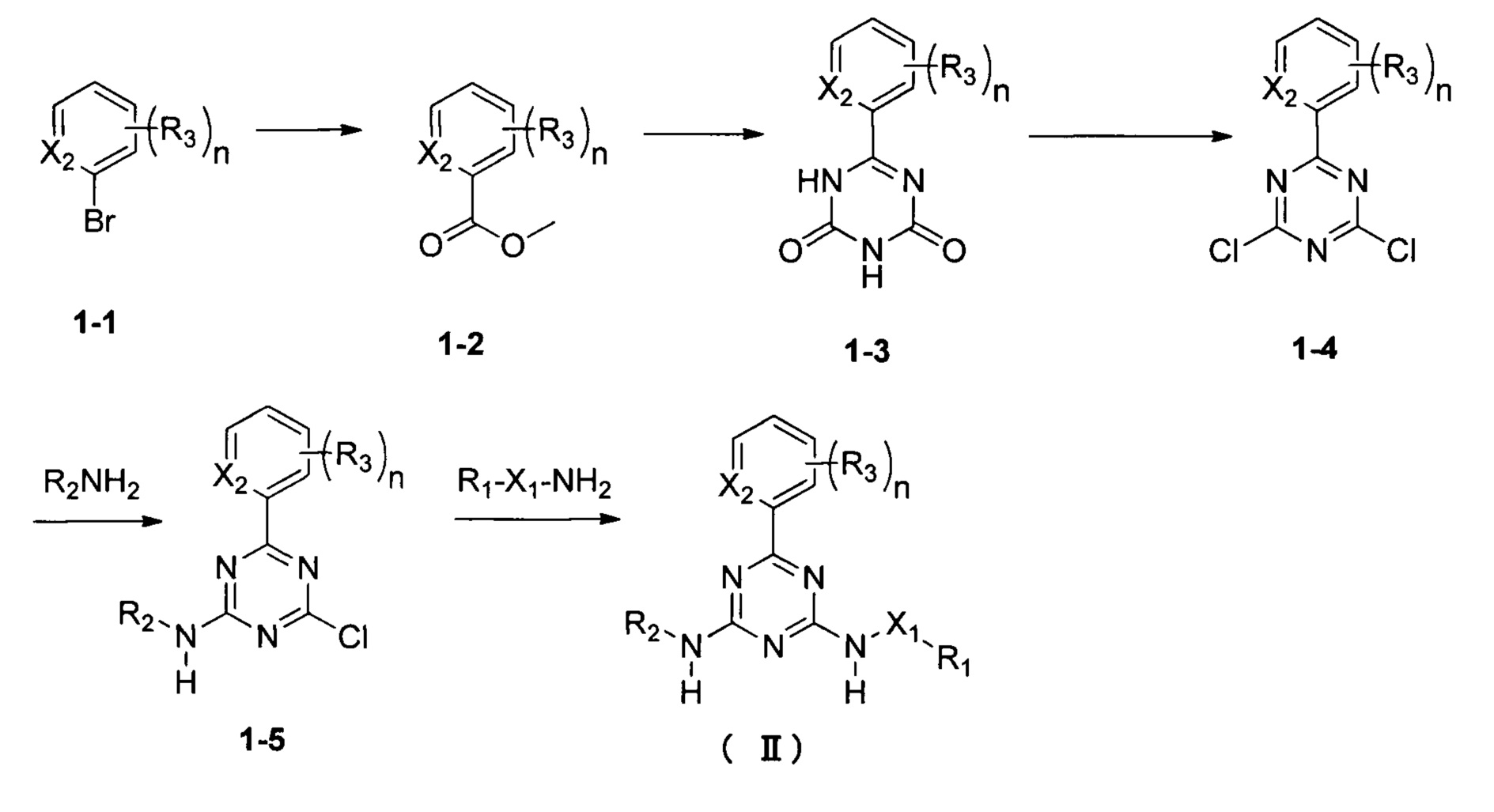
Соединение 1-2 получают путем ацилирования соединения 1-1; соединение 1-3 получают реакцией соединения 1-2 с биуретом; соединение 1-4 получают путем хлорирования соединения 1-3; соединение 1-5 получают путем аминирования соединения 1-4 амином, замещенным группой R2; и соединение формулы II получают путем аминирования соединения 1-5 амином, замещенным группой R2-X1.
ПРИМЕРЫ
Следующие конкретные примеры представлены для того, чтобы позволить специалистам в данной области техники более четко понять и выполнять изобретение. Они не должны толковаться как ограничение объема изобретения, но являются простыми иллюстрациями и типичными выриантами изобретения. Специалисты в данной области техники поймут, что для получения соединений по настоящей заявке существуют другие пути синтеза, а приведенные ниже примеры являются неограничивающими.
Все операции с сырьем, которое подвержено окислению или гидролизу, проводятся в защитной азотной атмосфере. Если не указано иное, сырье, используемое в настоящей заявке, коммерчески доступно и непосредственно используется без дополнительной очистки.
Колоночную хроматографию проводили с использованием силикагеля (200-300 меш), полученного от Qingdao Chemical Co., Ltd. Тонкослойную хроматографию проводили с использованием готовых пластин (силикагель 60 PF254, 0,25 мм), изготовленных Е. Merck. Разделение хиральных соединений и измерение энантиомерной чистоты (ее) проводили с использованием Agilent LC 1200 series (колонка: CHIRALPAK AD-H, ∅4,6×250 мм, 5 мкм, 30°С). ЯМР-спектр снимали с использованием спектрометра ядерного магнитного резонанса Varian VNMRS-400; и LC/MS выполняли с использованием FINNIGAN Thermo LCQ Advantage MAX, Agilent LC 1200 series (колонка: Waters Symmetry C18, ∅4,6×50 мм, 5 мкм, 35°C) и ионного режима ESI (+).
Экспериментальный Раздел
Пример 1. 4-(этоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин
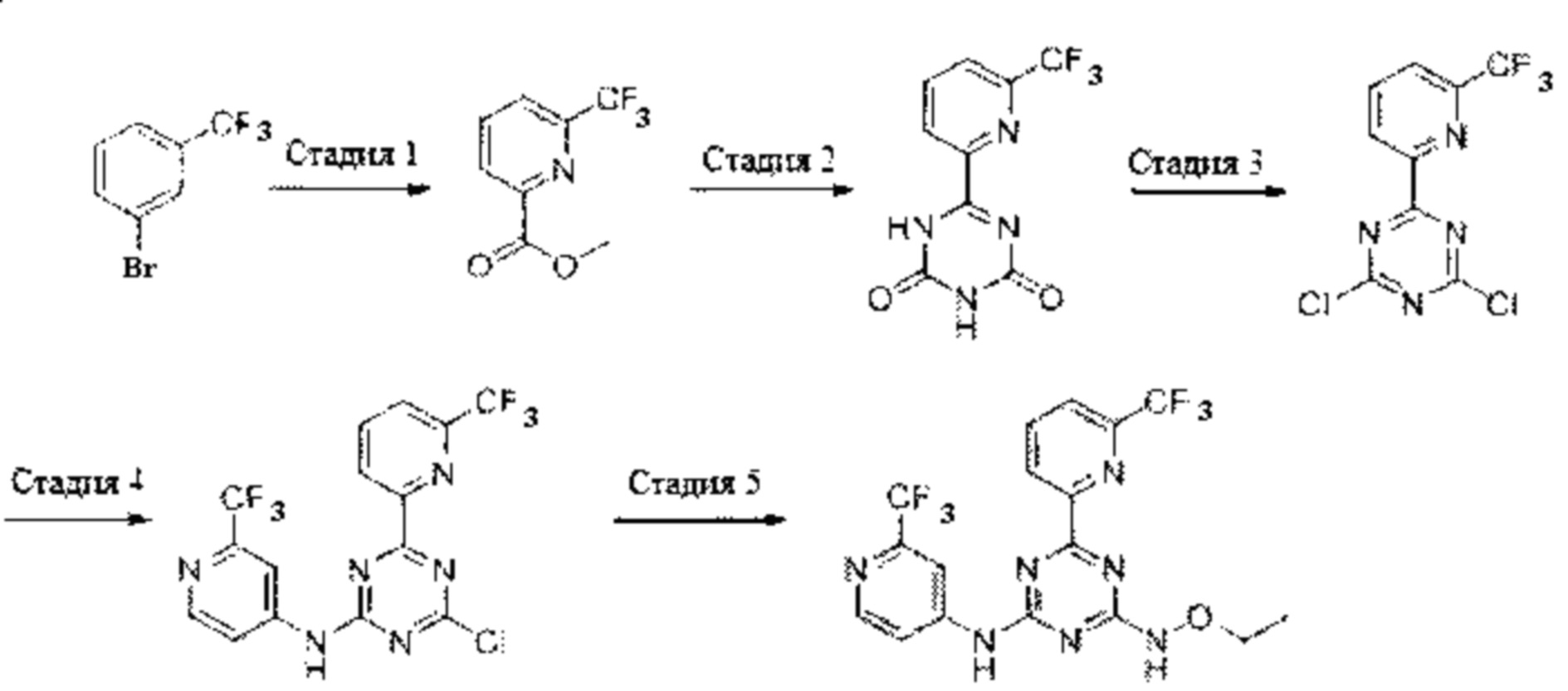
Стадия 1: Метил-6-трифторметилпиридин-2-карбоксилат

Под защитой газообразного азота к раствору 2-бром-6-трифторметилпиридина (1,48 г, 6,55 ммоль) в метаноле (50,0 мл) последовательно добавляли ацетат палладия (74,0 мг, 0,33 ммоль), 1,1'-бис(дифенилфосфино)ферроцен (363,0 мг, 0,655 ммоль) и триэтиламин (0,92 г, 9,8 ммоль) и подвергали взаимодействию при температуре 60°С в течение 18 часов в атмосфере монооксида углерода (2 атм). По окончании реакции реакционный раствор охлаждали до комнатной температуры и фильтровали. Фильтрат концентрировали в вакууме и полученный остаток очищали колоночной хроматографией на силикагеле с получением метил 6-трифторметилпиридин-2-карбоксилата (0,9 г, выход 67,0%).
Стадия 2: 6-(6-трифторметилпиридин-2-ил)-1,3,5-триазин-2,4(1Н,3Н)-дион
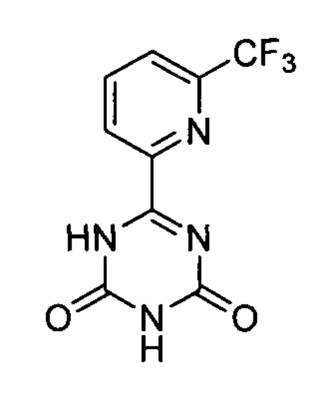
Под защитой газообразного азота к раствору этоксида натрия (11,2 г, 165,0 ммоль) в этаноле (200 мл) последовательно добавляли метил 6-трифторметилпиридин-2-карбоксилат (10,0 г, 48,7 ммоль) и биурет (4,2 г, 40,7 ммоль). Реакционную смесь кипятили с обратным холодильником в течение 2 часов и затем охлаждали до комнатной температуры. Реакционный раствор концентрировали под вакуумом и полученный остаток выливали в воду и доводили до рН 7 с помощью 6 моль/л раствора HCl. После отфильтровывания образовавшегося твердого вещества осадок на фильтре промывали водой и затем сушили с получением 6-(6-трифторметилпиридин-2-ил)-1,3,5-триазин-2,4(1H,3H)-диона (5,0 г, выход 47,5%).
Стадия 3: 2,4-дихлор-6-(6-трифторметилпиридин-2-ил)-1,3,5-триазин
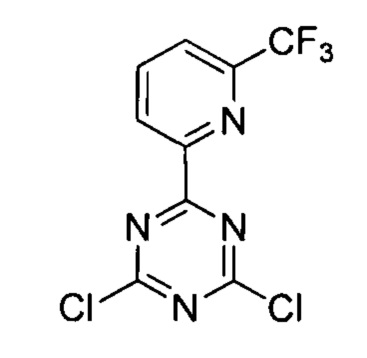
Под защитой газообразного азота смешанный раствор 6-(6-трифторметилпиридин-2-ил)-1,3,5-триазин-2,4(1H,3H)-диона (15,0 г, 58,1 ммоль) и фосфора оксихлорида (200 мл) подвергали взаимодействию в течение 2 часов при температуре 100°С и затем охлаждали до комнатной температуры. Реакционный раствор концентрировали под вакуумом. Полученный остаток выливали в насыщенный водный раствор бикарбоната натрия и экстрагировали этилацетатом (2×100 мл). Органическую фазу сушили над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали под вакуумом с получением 2,4-дихлор-6-(6-трифторметилпиридин-2-ил)-1,3,5-триазина (10,0 г, выход 58,3%).
Стадия 4: 4-хлор-6-(6-трифторметилпиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин

К раствору 2,4-дихлор-6-(6-трифторметилпиридин-2-ил)-1,3,5-триазина (5,0 г, 16,9 ммоль) в тетрагидрофуране (100 мл) добавляли 4-амино-2-трифторметилпиридина (3,3 г, 20,3 ммоль) и бикарбоната натрия (2,14 г, 25,3 ммоль). Реакционную смесь подвергали взаимодействию в течение 8 часов при температуре 70°С и затем охлаждали до комнатной температуры. Реакционный раствор концентрировали под вакуумом и полученный остаток очищали колоночной хроматографией на силикагеле с получением 4-хлор-6-(6-трифторметилпиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амина (6,5 г, выход 91,2%).
Стадия 5: 4-(этоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин
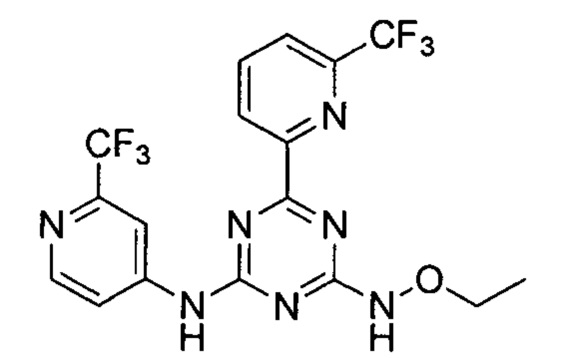
К раствору 4-хлор-6-(6-трифторметилпиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амина (50,0 мг, ммоль) в тетрагидрофуране (20 мл) добавляли этоксиамина гидрохлорид (12,0 мг, 0,18 ммоль) и бикарбонат натрия (40,0 мг, 0,48 ммоль). Реакционную смесь подвергали взаимодействию в течение 8 часов при температуре 70°С и затем охлаждали до комнатной температуры. Реакционный раствор концентрировали под вакуумом и полученный остаток очищали колоночной хроматографией на силикагеле с получением 4-(этоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амина (40,0 мг, выход 80,0%). 1H-ЯМР (400 МГц, CDCl3): δ=8.66-8.58 (m, 2Н), 8.49 (s, 1Н), 8.32 (s, 1H), 8.10 (t, J=7.9 Гц, 1H), 7.94 (s, 1H), 7.88 (d, J=7.8 Гц, 1H), 7.62 (d, J=3.7 Гц, 1H), 4.19 (q, J=7.0 Гц, 2H), 1.41 (t, J=7.1 Гц, 3Н).
Пример 2: 4-(изопропиламино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин
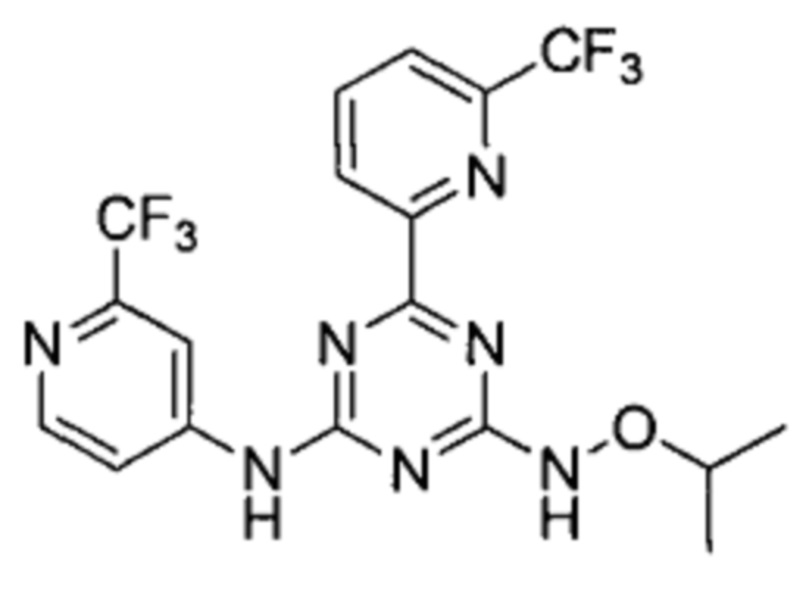
4-(изопропиламино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=11.35 (s, 1Н), 10.85 (s, 1Н), 8.66 (s, 1Н), 8.56 (d, J=5.6 Гц, 2Н), 8.32 (t, J=7.9 Гц, 1Н), 8.11 (d, J=7.6 Гц, 1Н), 8.03 (s, 1Н), 4.28-4.06 (m, 1Н), 1.23 (d, J=14.5 Гц, 6Н).
Пример 3: 4-(трет-бутоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин
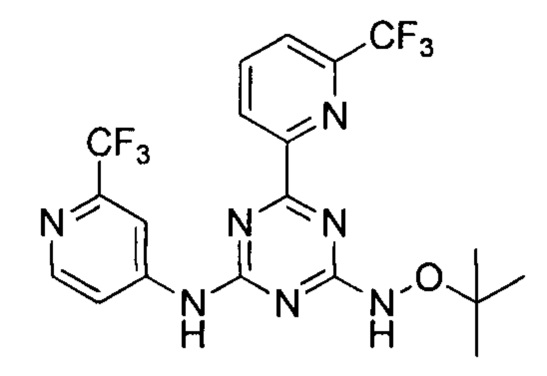
4-(трет-бутоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1H-ЯМР (400 МГц, ДМСО-d6): δ=11.00 (s, 1Н), 10.84 (s, 1Н), 8.74 (s, 1Н), 8.57 (t, J=6.5 Гц, 2Н), 8.31 (t, J=7.9 Гц, 1Н), 8.11 (d, J=7.7 Гц, 1Н), 7.99 (s, 1Н), 1.28 (s, 9Н).
Пример 4: 4-((циклопропилметокси)амино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин
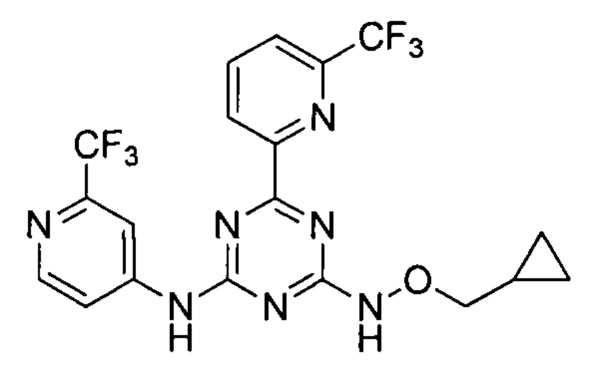
4-((циклопропилметокси)амино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин получают в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=11.4 (s, 1Н), 10.9 (s, 1Н), 8.61 (s, 1Н), 8.57 (d, J=5.6 Гц, 2Н), 8.32 (t, J=7.9 Гц, 1Н), 8.17-8.09 (m, 2Н), 3.77 (d, J=7.1 Гц, 2Н), 3.15 (d, J=5.2 Гц, 1Н), 0.87-0.76 (m, 2Н), 0.57-0.47 (m, 2Н).
Пример 5: N,N'-(6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2,4-диил)бис(О-этоксиамино)
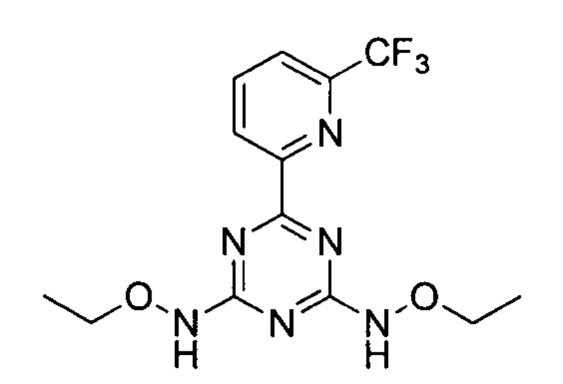
N,N'-(6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2,4-диил)бис(O-этоксиамино) получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=10.96 (s, 2Н), 8.48 (d,.J=7.8 Гц, 1H), 8.24 (t, J=7.9 Гц, 1Н), 8.04 (d, J=7.7 Гц, 1H), 3.90 (q, J=7.0 Гц, 4Н), 1.30-1.06 (m, 6Н).
Пример 6: 2-метил-1-(((4-(6-(трифторметил)пиридин-2-ил)-6-((2-(трифторметил)пиридин-4-ил)амино)-1,3,5-триазин-2-ил)амино)окси)изопропан-2-ол
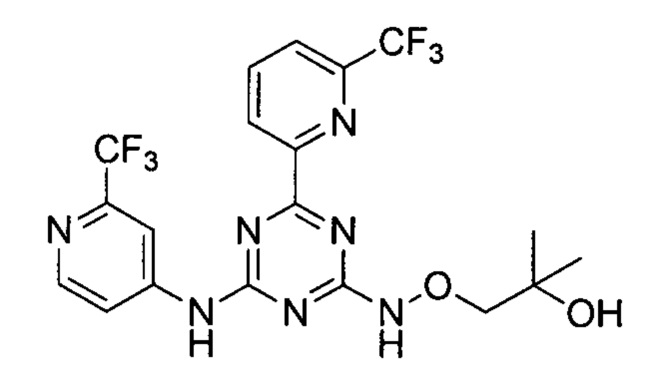
2-метил-1-(((4-(6-(трифторметил)пиридин-2-ил)-6-((2-(трифторметил)пиридин-4-ил)амино)-1,3,5-триазин-2-ил)амино)окси)изопропан-2-ол получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, CDCl3): δ=8.59 (dd, J=10.7, 6.7 Гц, 2Н), 8.29 (s, 1H), 8.09 (t, J=7.8 Гц, 1H), 7.87 (d, J=7.8 Гц, 1H), 7.73 (s, 1H), 4.00 (s, 2H), 1.62 (s, 1H), 1.32 (s, 6H).
Пример 7: 2-метил-2-(((4-(6-(трифторметил)пиридин-2-ил)-6-((2-(трифторметил)пиридин-4-ил)амино)-1,3,5-триазин-2-ил)амино)окси)изопропан-1-ол
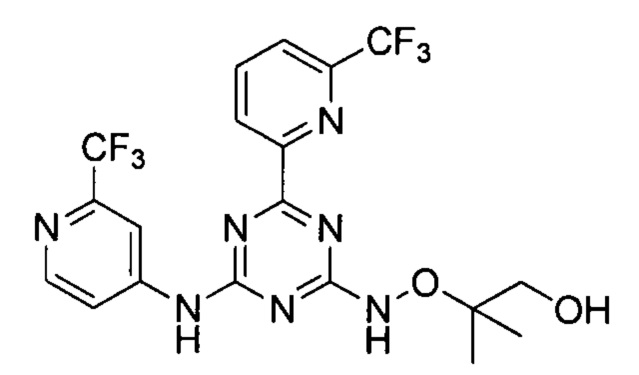
2-метил-1-(((4-(6-(трифторметил)пиридин-2-ил)-6-((2-(трифторметил)пиридин-4-ил)амино)-1,3,5-триазин-2-ил)амино)окси)изопропан-1-ол получали в соответствии со способом синтеза, описанным в Примере 1. 1H-ЯМР (400 МГц, ДМСО-dб): δ=10.80 (s, 1Н), 8.54 (d, J=5.8 Гц, 1Н), 8.29 (t, J=7.9 Гц, 3Н), 8.08 (m, 2Н), 5.38 (s, 1Н), 4.56 (s, 1Н), 3.54-3.39 (m, 2Н), 1.27-1.10 (m, 6Н).
Пример 8: 4-((бензилокси)амино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин

4-((бензилокси)амино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=11.52 (s, 1Н), 10.91 (s, 1Н), 8.60 (s, 2Н), 8.56 (d, J=5.4 Гц, 1H), 8.36 (t, J=7.9 Гц, 1Н), 8.15 (d, J=7.7 Гц, 2Н), 7.52 (s, 2Н), 7.47-7.35 (m, 3Н), 5.04 (s, 2Н).
Пример 9: 4-(2-метилгидразино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин
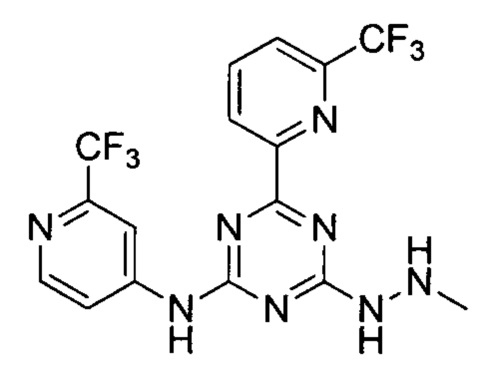
4-(2-метилгидразино)-6-(6-(трифторметил)пиридин-2-ил)-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1H-ЯМР (400 МГц, ДМСО-d6): δ=10.76 (s, 1Н), 8.67 (s, 1Н), 8.56 (d, J=5.5 Гц, 1Н), 8.30 (t, J=1.9 Гц, 1Н), 8.11 (d, J=7.7 Гц, 2Н), 7.93 (s, 1H), 5.39 (s, 1Н), 5.21 (s, 1Н), 3.40 (s, 3H).
Пример 10: 4-(трет-бутоксиамино)-6-фенил-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин
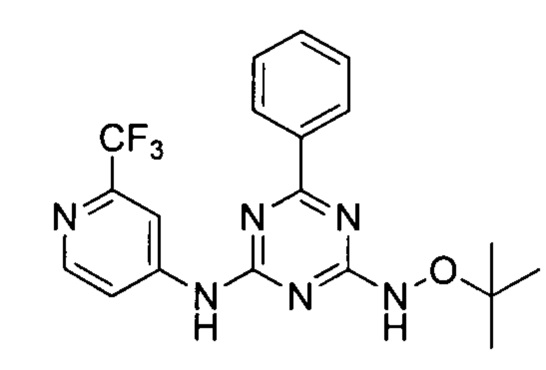
4-(трет-бутоксиамино)-6-фенил-N-(2-(трифторметил)пиридин-4-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=10.59 (d, 2Н), 8.59 (m, 1Н), 8.55 (m, 1Н), 8.32 (m, 2Н), 8.00 (m, 1Н), 7.56 (m, 3Н), 1.41-0.95 (m, 9Н).
Пример 11: 1-((4-(трет-бутоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-ил)амино)-2-метилпропан-2-ол
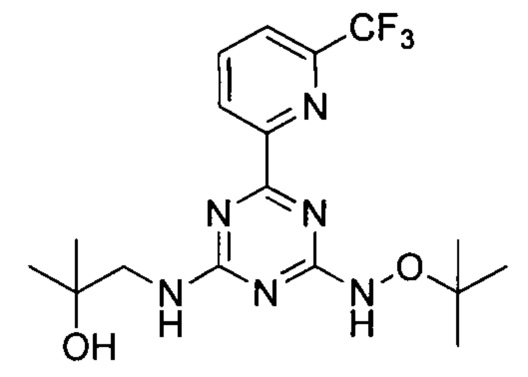
1-((4-(трет-бутоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-ил)амино)-2-метилпропан-2-ол получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=10.29 (d, 2Н), 8.53 (d, J=7.9 Гц, 1Н), 8.28 (t, J=7.9 Гц, 1Н), 8.13-8.03 (m, 1Н), 4.86 (s, 1Н), 3.39 (m, 2Н), 1.27 (m, 9Н), 1.07 (m, 6Н).
Пример 12: 4-(трет-бутоксиамино)-N-фенил-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-амин
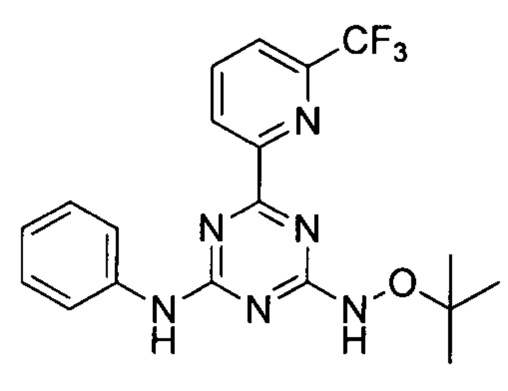
4-(трет-бутоксиамино)-N-фенил-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=10.62 (s, 1Н), 10.12 (s, 1Н), 8.57 (d, J=7.9 Гц, 1Н), 8.31 (t, J=7.8 Гц, 1Н), 8.10 (d, J=7.2 Гц, 1H), 7.99 (m, 2Н), 7.32 (t, J=7.9 Гц, 2Н), 7.03 (t, J=7.4 Гц, 1Н), 1.29 (s, 9Н).
Пример 13: N-бензил-4-(трет-бутоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-амин
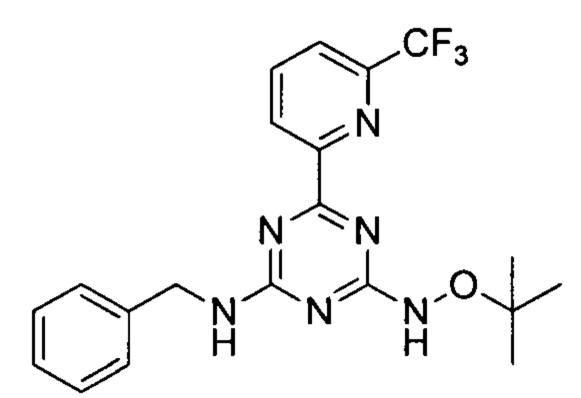
N-бензил-4-(трет-бутоксиамино)-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=10.26 (s, 2Н), 8.50 (dd, J=13.2, 5.0 Гц, 2Н), 8.33-8.18 (m, 1Н), 8.05 (d, J=7.8 Гц, 1H), 7.37 (d, J=7.0 Гц, 1H), 7.31 (dd, J=10.1, 4.8 Гц, 2H), 7.22 (t, J=7.2 Гц, 1H), 4.55 (d, J=6.2 Гц, 2H), 1.18 (s, 9H).
Пример 14: 4-(трет-бутоксиамино)-N-изопропил-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-амин

4-(трет-бутоксиамино)-N-изопропил-6-(6-(трифторметил)пиридин-2-ил)-1,3,5-триазин-2-амин получали в соответствии со способом синтеза, описанным в Примере 1. 1Н-ЯМР (400 МГц, ДМСО-d6): δ=10.16 (s, 2Н), 8.49 (d, J=8.1 Гц, 1H), 8.04 (d, J=7.4 Гц, 1Н), 7.83 (d, J=7.9 Гц, 1Н), 4.16 (m, 1Н), 1.24 (m, 9Н), 1.18 (m, 6Н).
Экспериментальный Пример 1: Определение Ингибирующей Активности IDH2
Ингибирующую активность соединений по настоящему изобретению в отношении IDH2 (R172K, 40-конец) определяли с использованием следующего способа, что было выражено как значения IC50, т.е., концентрации соединений, необходимых для достижения 50% ингибирования активности IDH2.
Материалы и Способы:
Ингибирующую активность соединения в отношении IDH2 (R172K, 40-конец) определяли по снижению хелперного фактора NADPH. Испытуемое соединение предварительно инкубировали с ферментом и NADPH, а затем реакцию инициировали добавлением a-KG и проводили в течение 120 минут в линейном режиме. Затем реакцию останавливали добавлением диафоразы (липоамиддегидрогеназы) и соответствующего субстрата резазурина. Диафораза прекратила реакцию IDH2m, уменьшив доступный хелперный фактор NADPH, который окислял NADPH до NADP и восстанавливал резазурин до высоко флуоресцентного резоруфина. Количество оставшегося хелперного фактора NADPH после определенного времени реакции определяли количественно через легко обнаруживаемый флуорофор.
В частности, 2,5 мкл разбавленного испытуемого соединения с 3-кратным градиентом добавляли в 384-луночный планшет, а затем добавляли 5 мкл реакционного буфера (20 мМ Трис-HCl, РН7,5, 150 мМ NaCl, 10 мМ MgCl2, 10 мМ MnCl2, 0,4 мг/мл BSA и 2 мМ DTT), содержащего 80 нМ IDH2 (R172K, 40-конец) и 40 мкМ NADPH. Затем полученную тестовую смесь инкубировали в течение 120 минут при температуре 23°С и затем добавляли 2,5 мкл реакционного буфера, содержащего 4 мМ a-KG, для инициирования реакции. После инкубирования в течение 120 минут при комнатной температуре добавляли 5 мкл приготовленной в реакционном буфере терминирующей смеси (0,4 ед/мл диафоразы и 40 мкМ резазурина) для превращения резазурина в резоруфин для определения оставшегося NADPH. После инкубирования в течение 10 минут при температуре 23°С значение флуоресценции определяли посредством Flexstation 3 в Ех535/Em595.
Ингибирующая активность тестируемого соединения в отношении IDH2 показана в Таблице 1.
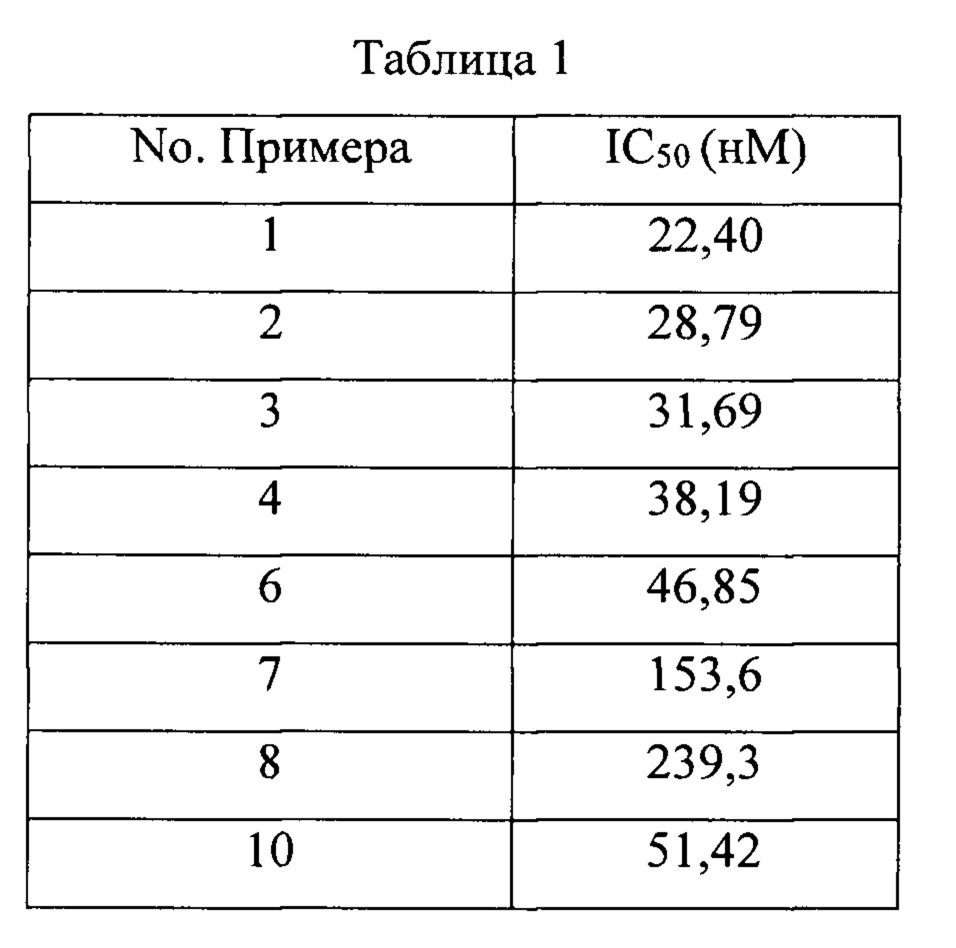
Экспериментальный Пример 2: Измерение Фармакокинетических Параметров
Фармакокинетические параметры соединений по настоящей заявке определяли с использованием следующего способа.
В этом исследовании использовали здоровых взрослых самцов крыс (7-9 недель). Один раз каждой группе животных (3 самца крыс) внутрижелудочно вводилась разовая доза 5 мг/кг. Перед этим исследованием животные в группе внутрижелудочного введения голодали в течение ночи. Период голодания был от 10 часов до введения до 4 часов после введения.
Образцы крови брали через 0,25, 0,5, 1, 2, 4, 6, 8 и 24 ч после введения. Животных анестезировали изофлураном с использованием устройства для анестезии животных, а затем из дна венозного сплетения были взяты 0,3 мл образцов цельной крови. Образцы крови помещали в гепариновые антикоагулянтные пробирки и центрифугировали в течение 5 мин при 4°С и 4000 об/мин. Полученную плазму переносили в центрифужные пробирки и хранили при -80°С до анализа.
Для анализа образцов плазмы использовался верифицированный метод LC-MS/MS. Данные о зависимости концентрации в плазме животных от времени анализировали с использованием программного обеспечения WinNonlin (Professional Edition, version 6.3; Pharsight Company). Для анализа концентрации использовали бескомпартментную модель. Вычисляли фармакокинетические параметры соединений. Как показано в Таблице 2, соединение в Примере 3 обладает улучшенным метаболизмом in vivo и более длительным периодом полувыведения и имеет более высокую концентрацию в плазме, чем ингибитор IDH2 AG-221 в той же дозе.