Результат интеллектуальной деятельности: ПРОИЗВОДНЫЕ ХИНАЗОЛИНА, ИНДУЦИРУЮЩИЕ ФЕРРОПТОЗ В МЕТАСТАТИЧЕСКИХ КЛЕТКАХ МЕЛАНОМЫ И РАКА ТОЛСТОЙ КИШКИ
Вид РИД
Изобретение
Изобретение относится к области медицины и фармацевтической химии и касается производных хиназолина, индуцирующих ферроптоз в метастатических опухолевых клетках. Первое сообщение о ферроптозе, железо-зависимой программируемой гибели клетки, появилось в 2012 г (Dixon S. J., Stockwell В. R. Ferroptosis: an iron-dependent form of nonapoptotic cell death. Cell, 2012; 49:1060-1072). Присутствие железа в свободном состоянии в клетке способствует накоплению активных форм кислорода (АФК) в результате окисления Fe2+ в Fe3+. Ввиду высокой химической активности АФК вызывают перекисное окисление некоторых полиненасыщенных кислот клетки с образованием гидропероксидов. Ферроптоз по морфологическим, биохимическим и генетическим особенностям отличается от апоптоза, генетически программируемой гибели клетки 1 типа и аутофагии, гибели клетки 2 типа.
В клинике на сегодняшний день нет препарата, индуцирующего ферроптоз в опухолевых клетках. Золотым стандартом в доклинических исследованиях продолжает оставаться эрастин. К ферроптозу оказались весьма чувствительны диффузная крупноклеточная В-лимфома, светлоклеточный рак почки, гепатоцеллюлярная карцинома, рак панкреатической железы, рак шейки матки, рак предстательной железы, остеосаркома и рак яичника. В этих типах рака сочетание эрастина с цитотоксическими противоопухолевыми препаратами, темозоломидом, цисплатином, цитарабином, доксорубицином, адриамицином значительно уменьшало объем экспериментальной опухоли, растущей в мышах (Вартанян А. Метаболизм железа, ферроптоз, рак. Росс. Биотер. Журн, 2017; 16(3)6 14-20).
Исследования последних лет привели нас к осознанию факта, что за развитие злокачественного процесса отвечает крайне небольшая популяция самообновляющихся и медленно пролиферирующих клеток, получивших название «стволовые клетки опухоли» (СКО). Эффективность противоопухолевой терапии оценивается способностью уменьшать объем опухоли. Но даже если мы отмечаем полную регрессию опухоли, всегда остается возможность ее повторного роста, потому что лечение было направлено на удаление основной популяции клеток опухоли - пролиферирующих клеток, а не СКО. Обнаруженные недавно данные о том, что захват железа заметно повышен у стволовых клеток глиобластомы по сравнению с не стволовыми клетками глиобластомы, чрезвычайно важны (Schonberg D. L., Miller Т. Е., Wu Q.et al. Preferential Iron Trafficking Characterizes Glioblastoma Stem-like Cells. Cancer Cell, 2015; 28:441-55). По всей видимости, железо может принимать активное участие в терапии, направленной на СКО.
С переходом опухоли в фазу метастатического роста цитотоксическая терапия, направленная на гибель пролиферирующих клеток по типу апоптоза или аутофагии, практически не работает. Задачей заявляемого изобретения является создание новых соединений на основе хиназолина, индуцирующих ферроптоз в метастазирующих клетках меланомы и рака толстой кишки.
Хиназолины, конденсированные гетероциклы, представляют значительный интерес в онкологии вследствие широкого спектра их биологических свойств. В частности, эрастин, классический индуктор ферроптоза, также является производным хиназолина. Структура заявляемых соединений представляет собой производные 3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)хиназолин-4(3H)-онов, где к атому кислорода в 3-м положении присоединены различные бензиловые эфиры уксусной кислоты.
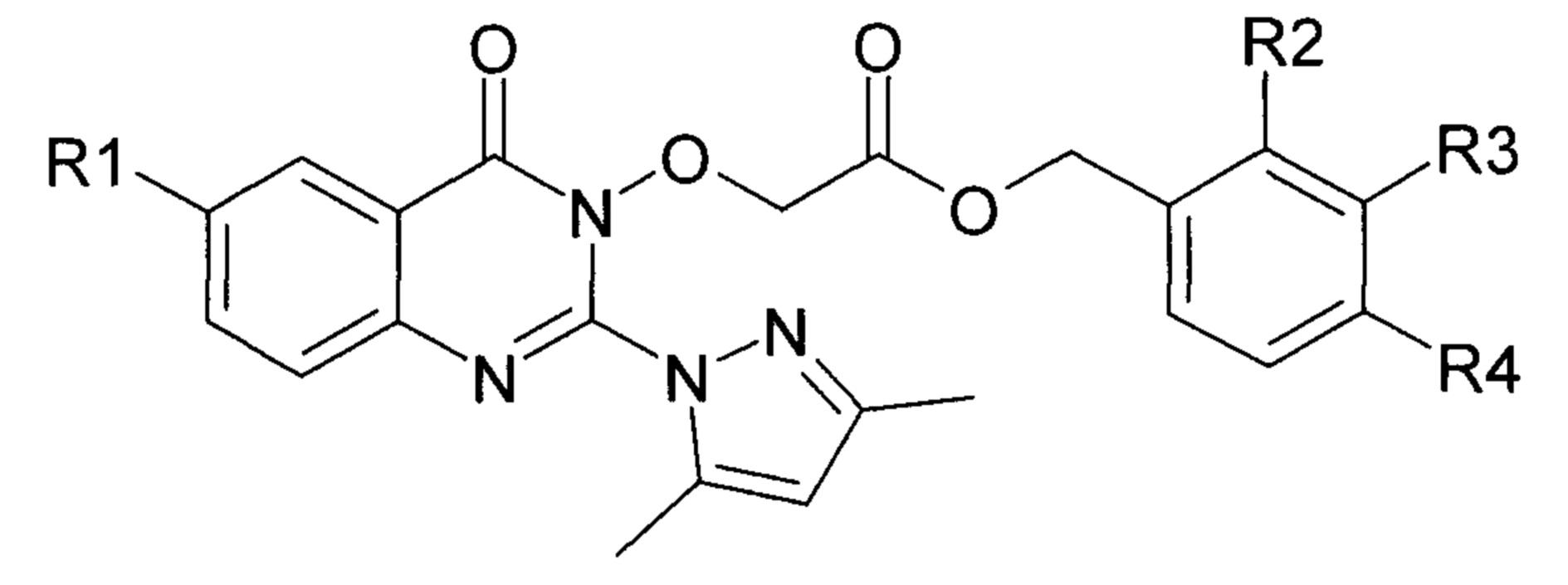
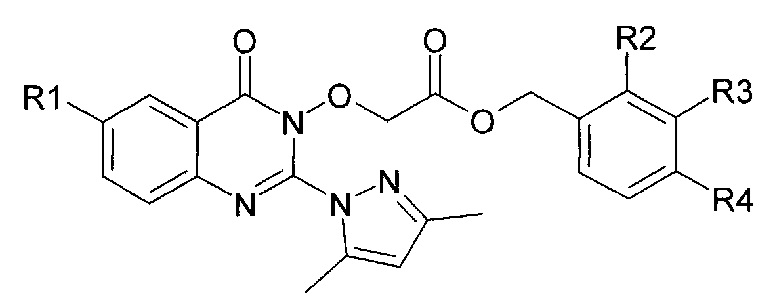
Заявляемые соединения соответствуют следующей общей формуле I:

где R1 представляет собой водород или галоген;
R2, R3, R4 также представлены водородом или галогеном.
Исследована способность производных хиназолина общей формулы I индуцировать ферроптоз в метастазирующих опухолевых клетках.
Соединение 1:
бензил 2-((2-(3,5-диметил-1H-пиразол-1-ил)-4-оксохиназолин-3(4H)-ил)окси)ацетат

Соединение 2:
бензил 2-((2-(3,5-диметил-1H-пиразол-1-ил)-6-хлор-4-оксохиназолин-3(4H)-ил)окси)ацетат

Соединение 3:
2-фторбензил 2-((2-(3,5-диметил-1H-пиразол-1-ил)-4-оксохиназолин-3(4H)-ил)окси)ацетат

Соединение 4:
2-фторбензил 2-((2-(3,5-диметил-1H-пиразол-1-ил)-6-хлор-4-оксохиназолин-3(4H)-ил)окси)ацетат

Соединение 5:
4-хлорбензил 2-((2-(3,5-диметил-1H-пиразол-1-ил)-4-оксохиназолин-3 (4H)-ил)окси)ацетат

Соединения (1-5) получали алкилированием производных 3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)хиназолин-4(3H)-онов бензиловыми эфирами 2-галоген-уксусной кислоты, предпочтительно в среде диметилформамида или диметилсульфоксида, при комнатной температуре в присутствии основания, преимущественно гидроксида натрия, карбоната калия или бикарбоната натрия. В качестве исходных соединений были использованы производные 3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)хиназолин-4(3H)-онов, полученные по методу, описанной в патенте РФ №2451683.
Для сравнительной оценки активности заявляемых соединений было дополнительно синтезировано соединение 6, отличающееся от предыдущих 1-5 соединений отсутствием ароматического фрагмента рядом с карбоксильной частью молекулы (эфиры бензиловых спиртов):
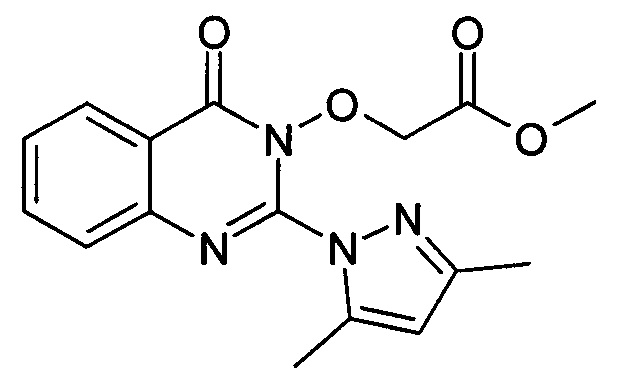
Соединение 6: метил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата
Полученные соединения охарактеризованы данными спектров 1Н-ЯМР. Спектры ЯМР 1Н зарегистрированы на спектрометре «Bruker AVANCE III NanoBay» (360 МГц) в диметилсульфоксиде-d6, в режиме стабилизации по дейтерию, термостабилизация - 25°С. Температуры плавления определяли на приборе марки "MeltingPoint М-565" (BUCHI).
Ниже приводятся более подробно иллюстрирующие изобретение примеры:
Получение бензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата (соединение 1)
К раствору 256 мг (1.0 момль) 3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)хиназолин-4(3H)-она в 5 мл диметилсульфоксида добавляют 138 мг (1.0 ммоль) мелкоизмельченного карбоната калия и по каплям вносят 185 мг (1.1 ммоль) бензилового эфира хлоруксусной кислоты. Перемешивают при комнатной температуре 12 часов, выливают в 15 мл холодной воды, отфильтровывают осадок, промывают на фильтре 2 раза по 10 мл воды и затем 10 мл гексана. Сушат на воздухе. Выход 347 мг (86 %) белых кристаллов. Т. пл. 121-123°С. Спектр 1Н NMR (360 MHz, DMSO-d6, δ м.д.) 8.20 (d, J=8.0 Hz, 1H), 7.88 (t, J=8.4 Hz, 1H), 7.79 (d, J=8.4 Hz, 1H), 7.61 (t, J=8.4 Hz, 1H), 7.34 - 7.39 (m, 5H), 6.12 (s, 1H), 6.12 (s, 1H), 5.22 (s, 2H), 5.15 (s, 2H), 2.44 (s, 3H), 2.10 (s, 3H).
Получение бензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-6-хлор4-оксохиназолин-3(4Н)-ил)окси)ацетата (соединение 2)
Соединение 2 получено аналогично соединению 1 из 256 мг 3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)-6-хлорхиназолин-4(3H)-она и 185 мг (1.1 ммоль) бензилового эфира хлоруксусной кислоты. Выход 387 мг (88.2%). Т. пл. 125-126°С. Спектр 1H NMR (360 MHz, DMSO-d6, δ м.д.) 8.14 (d, J=3.1 Hz, 1H), 7.91 (dd, 4.2, 1.4 Hz, 2H), 7.75 (d, J=6.0 Hz, 1H), 7.34 - 7.40 (m, 5H), 6.15 (s, 1H), 5.23 (s, 1H), 5.15 (s, 1H), 2.42 (s, 1H), 2.09 (s, 1H).
Получение 2-фторбензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата (соединение 3)
Соединение 3 получено аналогично соединению 1 из 256 мг 3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)хиназолин-4(3H)-она и 271 мг 2-фторбензилового эфира бромуксусной кислоты. Выход 301 мг (71.3%). Т. пл. 99-100°С. Спектр 1Н NMR (360 MHz, DMSO-d6 δ м.д.) 8.18 (d, J=8.0 Hz, 1H), 7.90 (t, J=8.4 Hz, 1H), 7.70 (d, J=8.4 Hz, 1H), 7.60 (t, J=8.4 Hz, 1H), 7.40 - 7.49 (m, 2H), 7.18 - 7.30(m, 2H), 6.12 (s, 1H), 5.23 (s, 2H), 5.15 (s, 2H), 2.43 (s, 3H), 2.10 (s, 3H).
Получение 2-фторбензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-6-хлор-4-оксохиназолин-3(4Н)-ил)окси)ацетата (соединение 4)
Соединение 4 получено аналогично соединению 1 из 291 мг3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)-6-хлорхиназолин-4(3H)-она и 271 мг 2-фторбензилового эфира бромуксусной кислоты. Выход 333 мг (72.9%). Т. пл. 106-107°С. Спектр 1Н NMR (360 MHz, DMSO-d6, δ м.д.) 8.13 (d, J=2.1 Hz, 1H), 7.92 (dd, 4.2, 1.4 Hz, 2H), 7.73 (d, J=6.0 Hz, 1H), 7.40 - 7.50 (m, 2H), 7.17 - 7.30 (m, 2H), 6.14 (s, 1H), 5.23 (s, 1H), 5.15 (s, 1H), 2.41 (s, 1H), 2.09 (s, 1H).
Получение 4-хлорбензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата (соединение 5)
Соединение 5 получено аналогично соединению 1 из 256 мг 3-гидрокси-2-(3,5-диметил-1H-пиразол-1-ил)хиназолин-4(3H)-она и 189 мг 4-хлорбензилового эфира бромуксусной кислоты. Выход 332 мг (75.8%). Т. пл. 121-123°С. Спектр 1Н NMR (360 MHz, DMSO-d6, δ м.д.) 8.20 (d, J=8.0 Hz, 1H), 7.90 (t, J=8.4 Hz, 1H), 7.72 (d, J=8.4 Hz, 1H), 7.60 (t, J=8.4 Hz, 1H), 7.38 - 7.54 (m, 2H),, 6.10 (s, 1H), 5.23 (s, 2H), 5.14 (s, 2H), 2.44 (s, 3H), 2.10 (s, 3H).
Получение метил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата (соединение 6)
Соединение 6 получено аналогично соединению 1. К 256 мг (1.0 момль) 3-гидрокси-2-(3,5-диметил-1Н-пиразол-1-ил)хиназолин-4(3Н)-она добавляли 168 мг (1.1 ммоль) метилового эфира бромуксусной кислоты. Выход 284 мг (76.5%). Т. пл. 135-137°С. Спектр 1Н NMR (360 MHz, DMSO-d6, δ м.д.) 8.19 (d, J=8.0 Hz, 1H), 7.87 (t, J=8.4 Hz, 1H), 7.79 (d, J=8.4 Hz, 1H), 7.60 (t, J=8.4 Hz, 1H), 6.12 (s, 1H), 5.22 (s, 2H), 4.65 (s, 3H), 2.45 (s, 3H), 2.11 (s, 3H).
В исследовании были использованы соединения (1-6) следующей структуры:
(1). бензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси) ацетата (2).бензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-6-хлор4-оксохиназолин-3(4Н)-ил)окси)ацетата
(3). 2-фторбензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата
(4). 2-фторбензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-6-хлор-4-оксохиназолин-3(4Н)-ил)окси) ацетата
(5). 4-хлорбензил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата;
(6). метил 2-((2-(3,5-диметил-1Н-пиразол-1-ил)-4-оксохиназолин-3(4Н)-ил)окси)ацетата.
Изобретение иллюстрируется фигурами 1(А-Н) и 2 (А-Н).
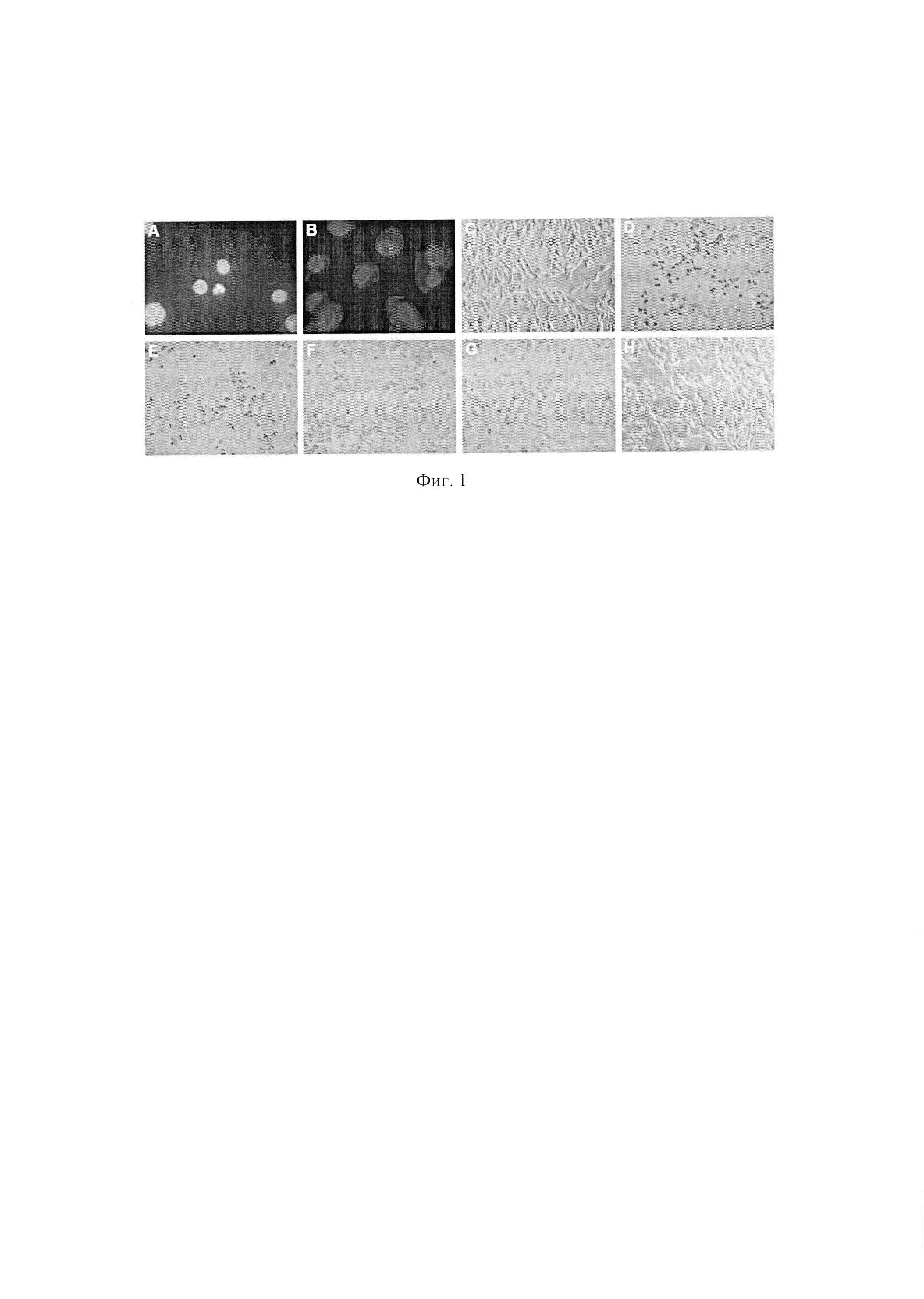
На фиг. 1 представлено подтверждение гибели Mel Z клеток по типу ферроптоз. (А.В) Окрашивание ядер Mel Z клеток DAPI. А, клетки росли с 1 мкМ цисплатина в течение 24 ч, видна фрагментация ядра, характерная для апоптоза, В, клетки росли с 1 мкМ соединения В, отсутствует фрагментация ядра; С, контрольные Mel Z клетки, фазово-контрастное изображение; D, клетки росли с 10 мкМ эрастина; Е, клетки росли с 10 мкМ соединения 1; F, клетки росли с 10 мкМ соединения 2 в присутствии zVAD-fmk; G, клетки росли с 10 мкМ соединения 2 в присутствии хлорокина; Н, клетки росли с 10 мкМ соединения 2 в присутствии DFO.
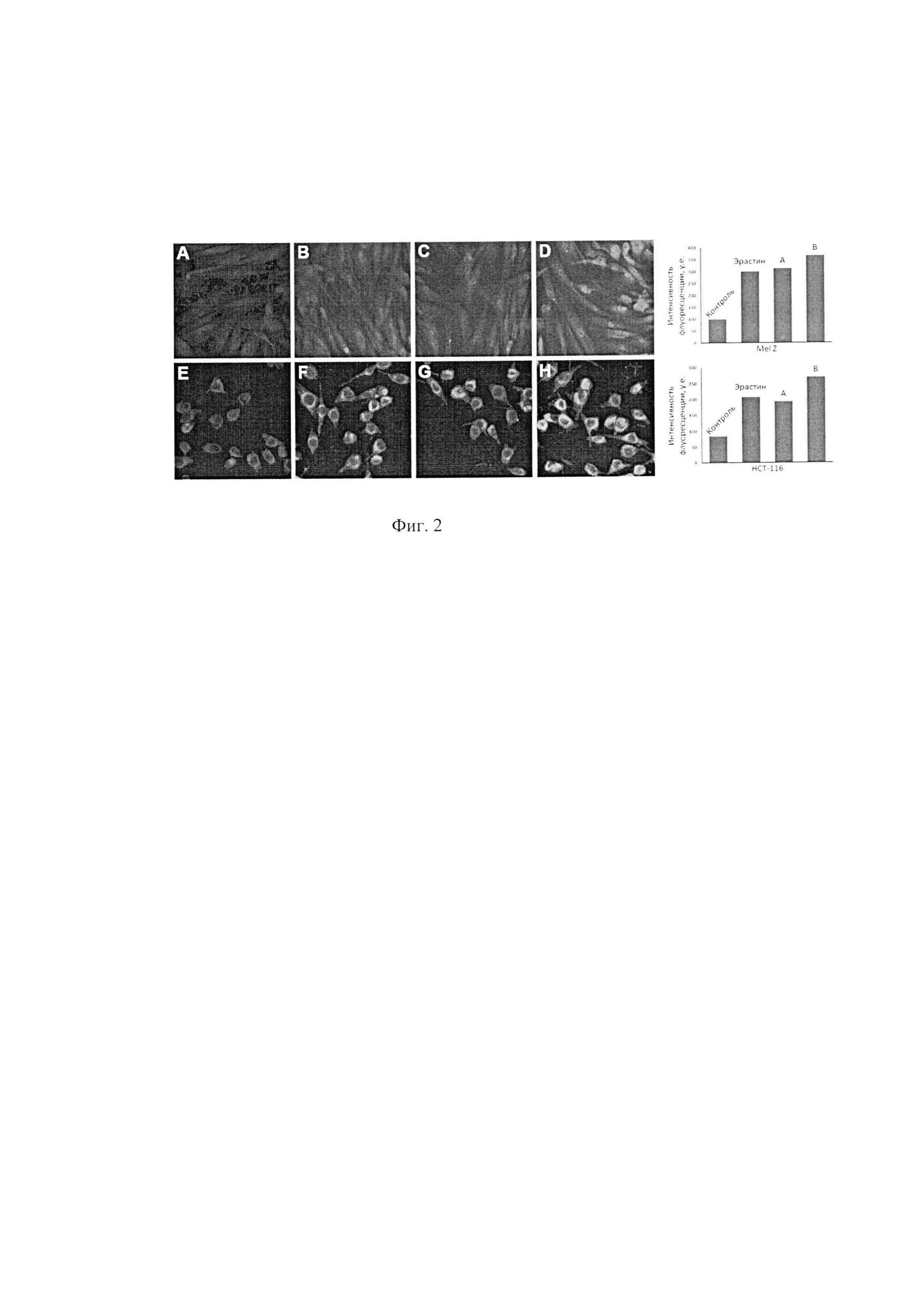
На фиг. 2 представлены влияния производных хиназолина на индукцию ферроптоза in vitro. A-D - Интенсивность флуоресценции BODIPY С-11 в Mel Z клетках. А, контроль; В, клетки росли с 10 мкМ эрастина; С, 10 мкМ соединения 1 и 2, 10 мкМ соединения В. Е-Н -Интенсивность флуоресценции BODIPY С-11 в НСТ-116 клетках. Е, контроль; F, клетки росли с 10 мкМ эрастина; G, с 10 мкМ соединения 1; Н, с 10 мкМ соединения 2.
Подтверждение гибели клетки по типу ферроптоз
В работе были использованы клетки меланомы Mel Z, полученные из метастатических узлов больных диссеминированной меланомой, проходивших лечение в ФГБУ «НМИЦ онкологии им Н.Н. Блохина», Минздрава России и клетки рака толстой кишки человека НСТ-116 (АТСС® CCL-247™). НСТ-116 - клетки эпителиальной морфологии, способные метастазировать в моделях ксенографтов. В предварительных экспериментах были протестированы 0.1, 1.0 и 10 мкМ эрастина на способность индуцировать гибель клеток меланомы и рака толстой кишки. При концентрации 0.1 мкМ эрастин не индуцировал гибель клеток ни в клетках меланомы, ни в клетках рака толстой кишки. Незначительная активность наблюдалась при концентрации 1.0 мкМ. Массивную гибель клеток Mel Z и НСТ-116 вызывало 10 мкМ эрастина. В дальнейших исследованиях в качестве контроля мы использовали 10 мкМ эрастина. Соединения 1-6 тестировали при 0.1, 1.0 и 10 мкМ. Ни одно из 6 соединений не индуцировало гибель клеток при концентрации 0.1 мкМ. Незначительная активность при 1.0 мкМ (менее 15%) наблюдалась для соединений 1 и 2. И все 6 соединений индуцировали гибель клеток при концентрации 10 мкМ. В дальнейших экспериментах ферроптоз индуцировали 10 мкМ соединений 1-6.
Окислительный стресс, являющийся следствием дисбаланса про- и антиоксидантных систем клетки и отражающийся в избыточном образовании в клетке АФК, приводит к клеточной гибели по типу апоптоз. Итогом апоптоза - генетически программируемой клеточной гибели I типа - является уплотнение хроматина и фрагментация ДНК с образованием апоптотических телец, ограниченных плазматической мембраной. Mel Z клетки выращивали в полной среде RPMI 1640 при 5% содержании СО2 и температуре 37°С. Через 24 ч к клеткам добавляли 10 мкМ эрастина или соединения (1-6) и инкубировали еще 24 ч. Далее клетки промывали фосфатным буфером и ядра окрашивали DAPI. Можно видеть, что гибель клетки, индуцируемая этими соединениями, отличается по морфологическим признакам от апоптоза - отсутствует конденсация ядра и
фрагментация ДНК (фиг. 1, А-В). Вторым подтверждением не апоптотической гибели клетки явилось не чувствительность гибели клеток, индуцированной соединением 2 в присутствии 50 мкМ пан-каспазного ингибитора апоптоза zVAD-fmk (C-F). Посредством аутофагии - программированной гибели клетки 2 типа - клетка избавляется от поврежденных органелл и долгоживущих белков, регулируя состав цитозоля и размеры эндоплазматической сети. На гибель клеток меланомы Mel Z, индуцированную соединением 2, не оказывал влияния и 20 мкМ ингибитора аутофагии - хлорокин (Рис. 1, G). Однако, 100 мкМ дефероксамина (DFO), хелатора железа, практически полностью блокировало гибель клеток меланомы (фиг. 1, Н), индуцированную соединением 2. Аналогичная закономерность наблюдалась и для клеток рака толстой кишки НСТ-116 (данные не приводятся). Таким образом, наблюдаемая нами массивная гибель клеток меланомы и рака толстой кишки, индуцированная производными хиназолина - это гибель клеток по типу ферроптоз.
Исследование влияния производных хиназолина на индукцию ферроптоза in vitro.
Концепция о том, что характерной особенностью ферроптоза является железо-зависимое перекисное окисление липидов, сегодня принята всеми.
Клетки меланомы Mel Z или рака толстой кишки НСТ-116 растили в полной среде RPMI 1640 в 24-луночном планшете. Через 24 ч роста клеток в СО2 инкубаторе при 37°С добавляли 10 мкМ эрастина или 10 мкМ соединений 1-6 и инкубировали 5 ч. В качестве контроля использовали клетки, растущие в полной среде RPMI 1640 без индукторов ферроптоза. Затем среду заменяли свежей, не содержащей сыворотки, и добавляли 5 мкМ C11-BODIPY (581/591) - индикатора перекисного окисления липидов. C11-BODIPY - это флуорофор, который, переходя из тиоэфира в сульфоксид, меняет флуоресцентные характеристики: убывает поглощение красного цвета и нарастает поглощение зеленого. После инкубирования с флуоресцентной меткой в течение 30 мин клетки трижды промывали фосфатным буфером. Интенсивность флуоресценци определяли на флуоресцентном микроскопе IN Cell Analyzer (GE Healthcare,США) при 510-550 нм.
Уровень перекисного окисления липидов в клетках меланомы, индуцируемого 10 мкМ соединениями 3-6 и в клетках рака толстой кишки, приближался к значениям, вызываемым эрастином (84.5±3%, 91±5%, 88.5±5% и 70.4±4%). Ситуация существенно не менялась и на клетках метастазирующей меланомы Mel Z (85.7±3%, 93.4±5%, 80.2±5% и 77.1±4%). При индукции ферроптоза 10 мкМ соединения 1, уровень перекисного окисления липидов в клетках меланомы незначительно превышал активность эрастина, а в клетках рака толстой кишки был равен эффекту эрастина. При той же концентрации соединение 2 превышало уровень перекисного окисления липидов, индуцированного эрастином на 22±2%, и 30±2%,% в Mel Z и НСТ-116, соответственно. Соединения 2 были отобраны для дальнейшей работы с ними, как с потенциально противоопухолевым препаратом для лечения метастазирующей опухоли.