Результат интеллектуальной деятельности: КОМБИНАЦИИ СОЕДИНЕНИЙ, МОДУЛИРУЮЩИХ NMDA-РЕЦЕПТОР
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка заявляет приоритет по предварительной заявке на патент США №61/989183, поданной 6 мая 2014 г., которая включена в данный документ в полном объеме посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[0002] N-Метил-D-аспартатный (NMDA) рецептор (NMDA-рецептор) представляет собой постсинаптический ионотропный рецептор, который чувствителен, среди прочего, к возбуждающим аминокислотам глутамату и глицину и синтетическому соединению NMDA. NMDA-рецептор контролирует поток как двухвалентных, так и одновалентных ионов в постсинаптическую нейронную клетку через канал, связанный с рецептором (Foster et al., Nature 1987, 329:395-396; Mayer et al., Trends in Pharmacol. Sci. 1990, 11:254-260). NMDA-рецептор вовлечен в установление нейрональной архитектуры и синаптической взаимосвязи при развитии и может участвовать в модифицировании синапсов, связанном с предшествующим опытом. Дополнительно, полагают, что NMDA-рецепторы вовлечены в долгосрочную потенциацию и расстройства центральной нервной системы.
[0003] NMDA-рецептор играет ключевую роль в синаптической пластичности, которая лежит в основе многих высших когнитивных функций, таких как запоминание, удержание в памяти и обучение, а также в некоторых когнитивных путях и в ощущении боли (Collingridge et al., The NMDA Receptor, Oxford University Press, 1994). Дополнительно, некоторые свойства NMDA-рецепторов свидетельствуют о том, что они могут быть вовлечены в обработку информации мозгом, которая лежит в основе сознания.
[0004] NMDA-рецептор привлекает особый интерес, поскольку он, по-видимому, вовлечен в широкий спектр расстройств ЦНС. Например, при ишемии головного мозга, вызванной инсультом или травматическим повреждением, из поврежденных или обедненных кислородом нейронов выделяется избыточное количество возбуждающей аминокислоты глутамата. Этот избыток глутамата связывается с NMDA-рецепторами, которые открывают свои управляемые лигандами ионные каналы; в свою очередь входящий поток кальция создает высокий уровень внутриклеточного кальция, который активирует биохимический каскад, приводящий к деградации белков и гибели клеток. Полагают, что это явление, известное как эксайтотоксичность, также ответственно за неврологическое повреждение, связанное с другими расстройствами: от гипогликемии и остановки сердечной деятельности до эпилепсии. Дополнительно, существуют предварительные сообщения, указывающие на подобное вовлечение в хроническую нейродегенерацию при болезнях Хантингтона, Паркинсона и Альцгеймера. Продемонстрировано, что активация NMDA-рецептора ответственна за судороги после инсульта, а в некоторых моделях эпилепсии показано, что активация NMDA-рецептора необходима для возникновения эпилептического припадка. Также было установлено вовлечение NMDA-рецептора в невропсихиатрические заболевания, поскольку блокирование Са++-канала NMDA-рецептора анестезирующим средством для животных РСР (фенциклидином) вызывает у людей психотическое состояние, подобное шизофрении (рассмотрено в Johnson,K. and Jones, S., 1990). Кроме того, NMDA-рецепторы также вовлечены в несколько типов пространственного обучения.
[0005] Полагают, что NMDA-рецептор состоит из нескольких белковых цепей, встроенных в постсинаптическую мембрану. Первые два типа субъединиц, обнаруженные на данный момент, образуют большую внеклеточную область, которая, возможно, содержит большинство аллостерических центров связывания, несколько трансмембранных областей, образующих петлю и свернутых так, что образуется пора или канал, который проницаем для Са++, и область терминальной карбоксильной группы. Открытие и закрытие канала регулируется связыванием различных лигандов с доменами (аллостерическими центрами) белка, расположенными на внеклеточной поверхности. Полагают, что связывание с лигандами приводит к конформационному изменению всей структуры белка, что в конечном итоге выражается в открытии, частичном открытии, частичном закрытии или закрытии канала.
[0006] Антагонисты NMDA-рецептора действуют так, что оказывают антагонистический эффект или ингибируют действие N-метил-D-аспартатного рецептора (NMDA-рецептора). Однако сниженная функция NMDA-рецептора может быть связана с отрицательными побочными эффектами, в том числе с теми, которые влияют на когнитивные способности.
[0007] Недавно был описан улучшенный частичный агонист NMDA-рецептора, имеющий название GLYX-13. GLYX-13 в качестве примера представлен следующей структурной формулой:
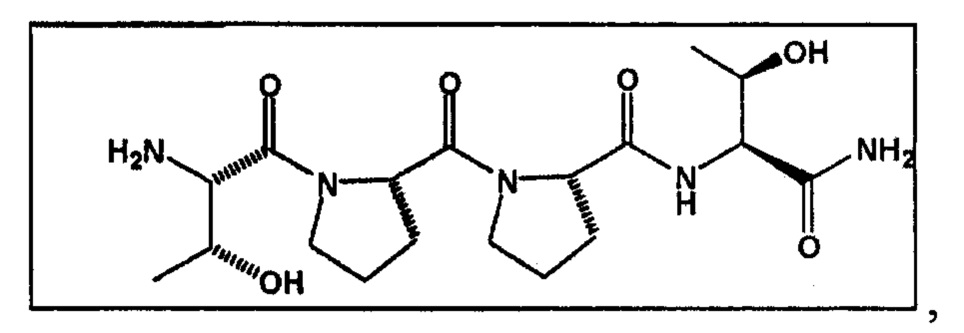
с молекулярной массой 413,47 и химической формулой C18H31N5O6. GLYX-13 демонстрирует ноотропную, нейропротекторную и антиноцицептивную активность и усиливает способность к обучению, память и познавательную способность in vivo.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] Характерной особенностью данного изобретения являются комбинации, которые содержат один или более антагонистов NMDA-рецептора и GLYX-13 (каждый из которых в данном документе иногда упоминается как «компонент»). Положительное действие комбинации основано, в частности, на том наблюдении, что введение GLYX-13 (например, однократная доза) может вызвать обратное развитие и/или предотвратить когнитивное нарушение, вызванное антагонистом NMDA-рецептора (например, нарушение распознавания нового объекта, вызванное антагонистом NMDA-рецептора; например, вызванное повторяющимися дозами антагониста NMDA-рецептора). Комбинации могут дополнительно содержать один или более других биологически активных ингредиентов (например, один или более антидепрессантов) и/или одно или более фармацевтически приемлемых вспомогательных веществ и/или носителей. Компоненты комбинации (иногда также упоминаются в данном документе как химические структурные элементы или химические соединения) можно вводить пациенту последовательно (каждый компонент вводят в различное время) или практически одновременно. Понятно, что компоненты могут присутствовать в одном и том же фармацевтически приемлемом носителе и, следовательно, их можно вводить одновременно. В альтернативном варианте каждый из компонентов может присутствовать в отдельном фармацевтическом носителе, таком как традиционные лекарственные формы для перорального применения или формы для парентерального применения (или один компонент может быть в форме для перорального применения, а другой - в форме для парентерального), которые можно вводить или одновременно, или последовательно. В некоторых вариантах реализации изобретения особенно эффективным является предварительное лечение GLYX-13 (т.е. до введения одного или более антагонистов NMDA-рецептора).
[0009] Следовательно, в одном аспекте изобретения предложены способы осуществления значительного обратного развития или предотвращения когнитивного нарушения у пациента, которому интенсивно кратковременно вводят антагонист NMDA-рецептора, включающие введение эффективного количества GLYX-13.
[0010] В другом аспекте изобретения предложены способы лечения когнитивного нарушения у пациента, нуждающегося в этом, включающие введение эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. Когнитивное нарушение может возникать вследствие одной или более причин из: недостатка когнитивных способностей, врожденных патологий, фактора(-ов) окружающей среды или приема лекарственных средств, и включать, но не ограничиваясь ими, нарушения способности к обучению и/или дислексию. В некоторых вариантах реализации изобретения введение эффективного количества GLYX-13 производят до или после интенсивного кратковременного введения одного или более антагонистов NMDA-рецептора. В других вариантах реализации изобретения введение эффективного количества GLYX-13 производят практически одновременно с интенсивным кратковременным введением одного или более антагонистов NMDA-рецептора.
[0011] В дополнительном аспекте изобретения предложены способы лечения расстройства, патологического состояния или заболевания, в том числе, но не ограничиваясь ими: неврологических или других заболеваний (например, инсульта, психоза, боли (невропатической боли), депрессии (клинической депрессии), болезни Паркинсона и болезни Альцгеймера); заболевания центральной нервной системы (например, нейродегенеративного заболевания, инсульта, травматического повреждения головного мозга и повреждения спинного мозга); шизофрении; и/или депрессии (например, резистентной депрессии), которые включают введение эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. В некоторых вариантах реализации изобретения GLYX-13 и один или более антагонистов NMDA-рецептора вводят практически одновременно. В других вариантах реализации изобретения GLYX-13 и один или более антагонистов NMDA-рецептора вводят последовательно, например, GLYX-13 вводят до или после одного или более антагонистов NMDA-рецептора.
[0012] В одном аспекте изобретения предложены фармацевтически приемлемые композиции, которые содержат GLYX-13, один или более антагонистов NMDA-рецептора и одно или более фармацевтически приемлемых вспомогательных веществ или носителей.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
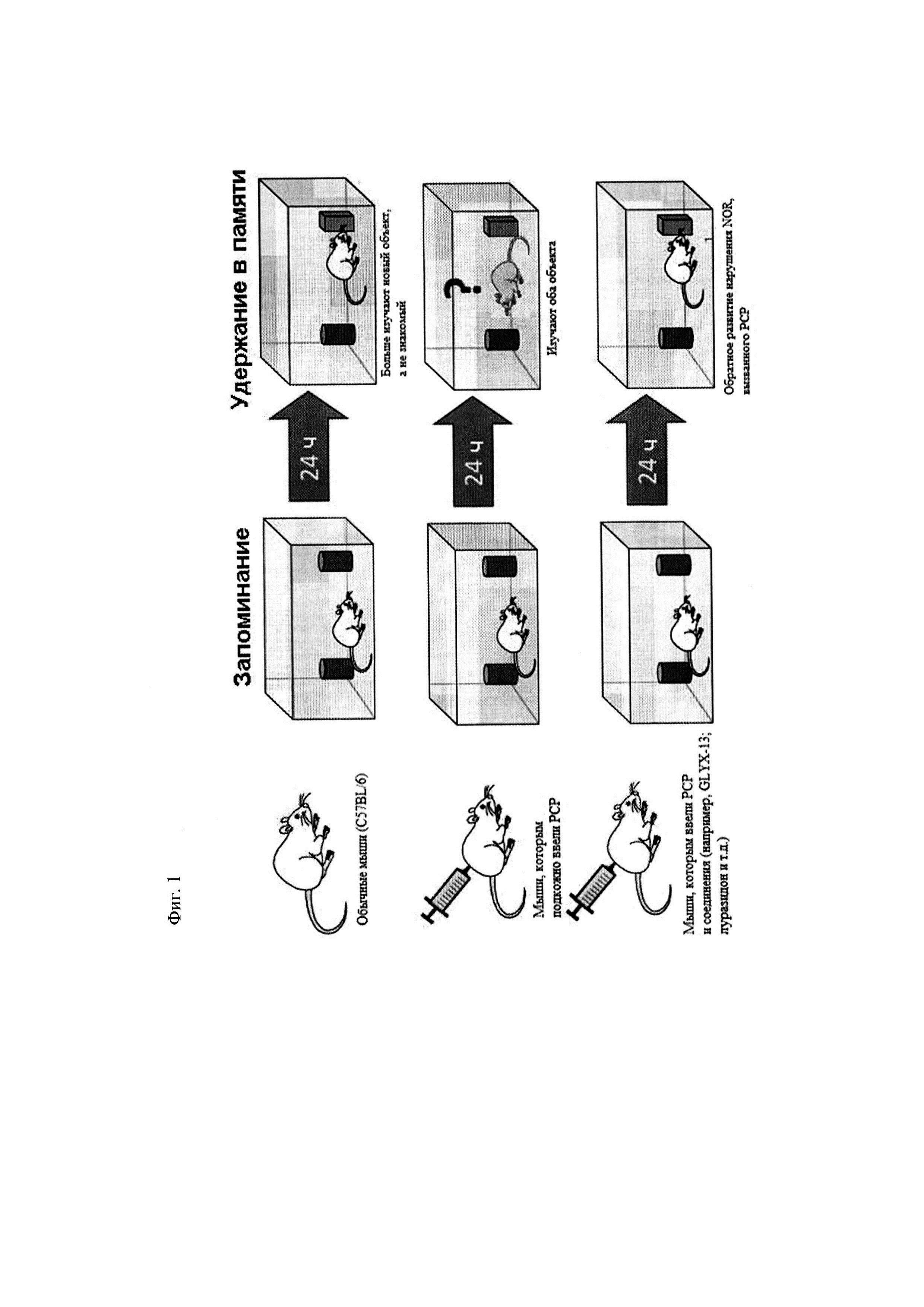
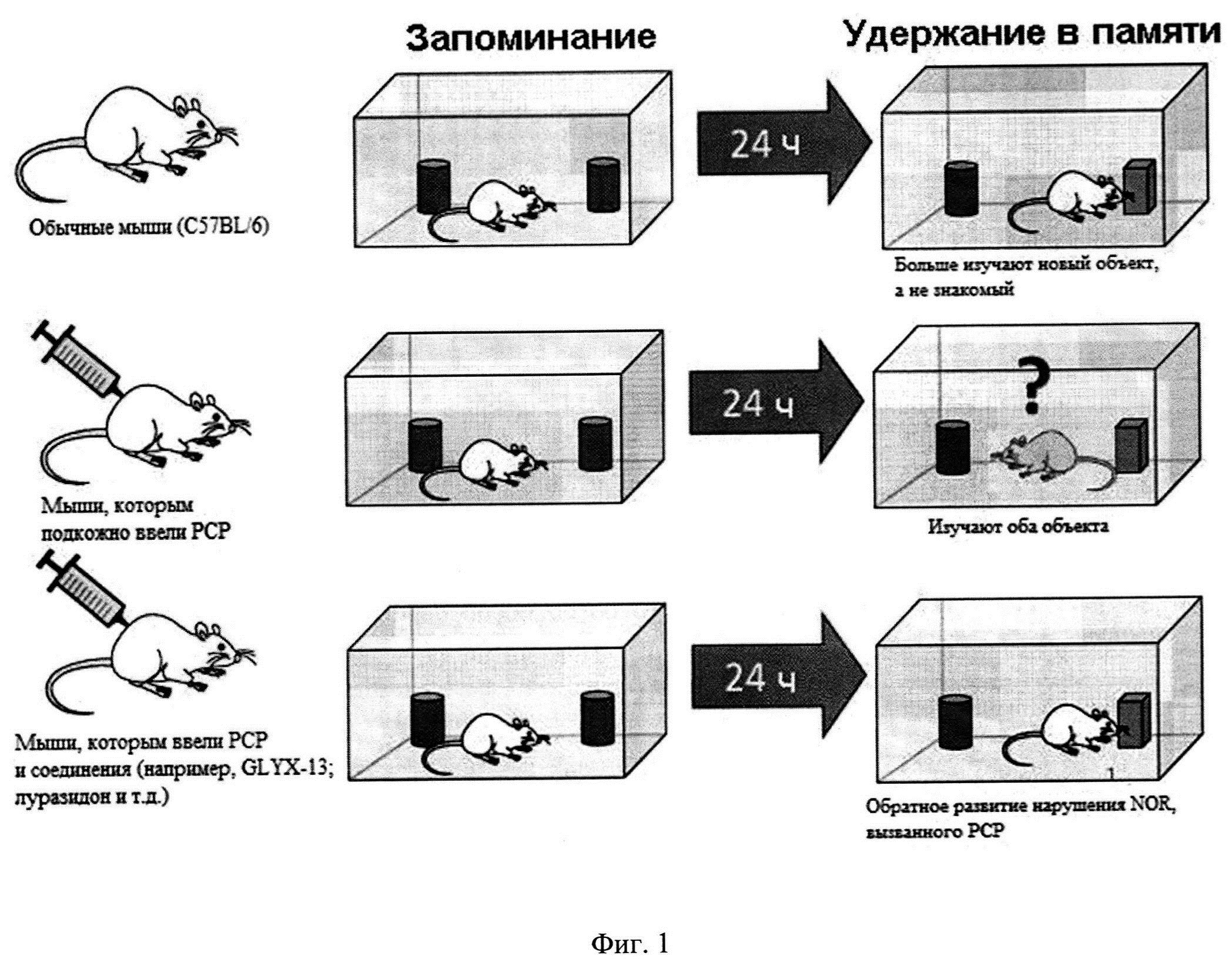
[0013] Фиг. 1 представляет собой диаграмму, дающую общее представление о модели распознавания нового объекта.
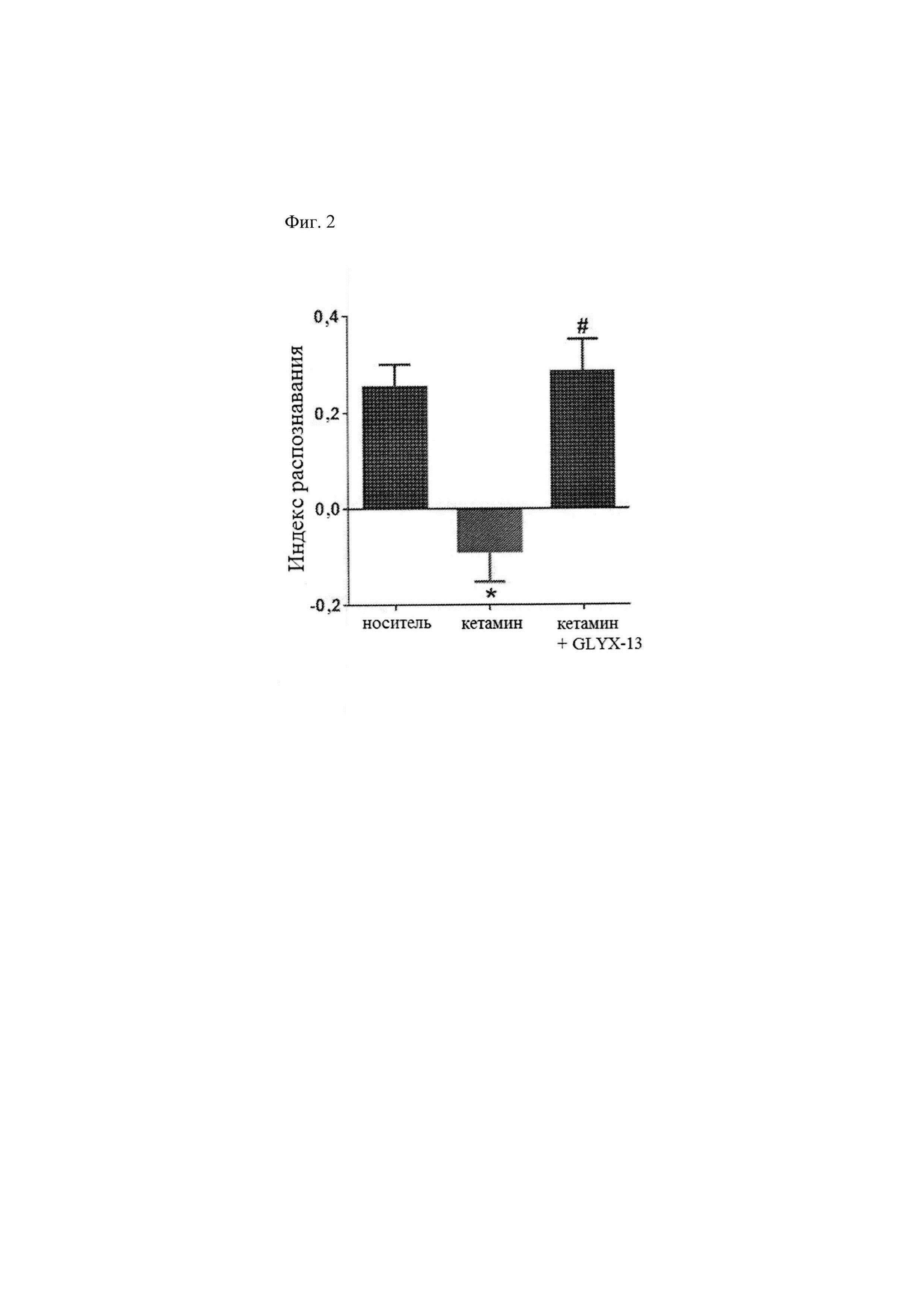
[0014] Фиг. 2 иллюстрирует среднее значение ± СОС (SEM) показателя индекса различения (DI) при проведении теста распознавания нового объекта у взрослых самцов мышей C57BL/6, которым предварительно вводили два раза в день инъекцию кетамина (30 мк/кг интраперитонеально) в течение 7 дней подряд, а затем инъекцию стерильного раствора хлорида натрия (носителя) за 1 час до проведения теста (группа, получавшая кетамин), инъекцию GLYX-13 (1 мг/кг внутривенно) за 1 час до проведения теста (группа, получавшая GLYX-13 + кетамин), или инъекции стерильного раствора хлорида натрия дважды в день в течение 7 дней и инъекцию носителя за 1 час до проведения теста. Индекс различения рассчитывали с использованием следующей формулы: (время, затраченное на изучение нового объекта - время, затраченное на изучение знакомого объекта)/ (общее время, затраченное на изучение и нового, и знакомого объектов). N=8-10 на группу. * р<0,001, значимое уменьшение DI по сравнению с группой, получавшей носитель, # р<0,001, значимое обратное изменение DI по сравнению с группой, получавшей кетамин (критерий PLSD Фишера по полученным результатам). Данные на фиг. 2 демонстрируют, что GLYX-13 (1 мг/кг внутривенно) вызывает обратное развитие хронического нарушения распознавания новых объектов у мышей, вызванного кетамином.
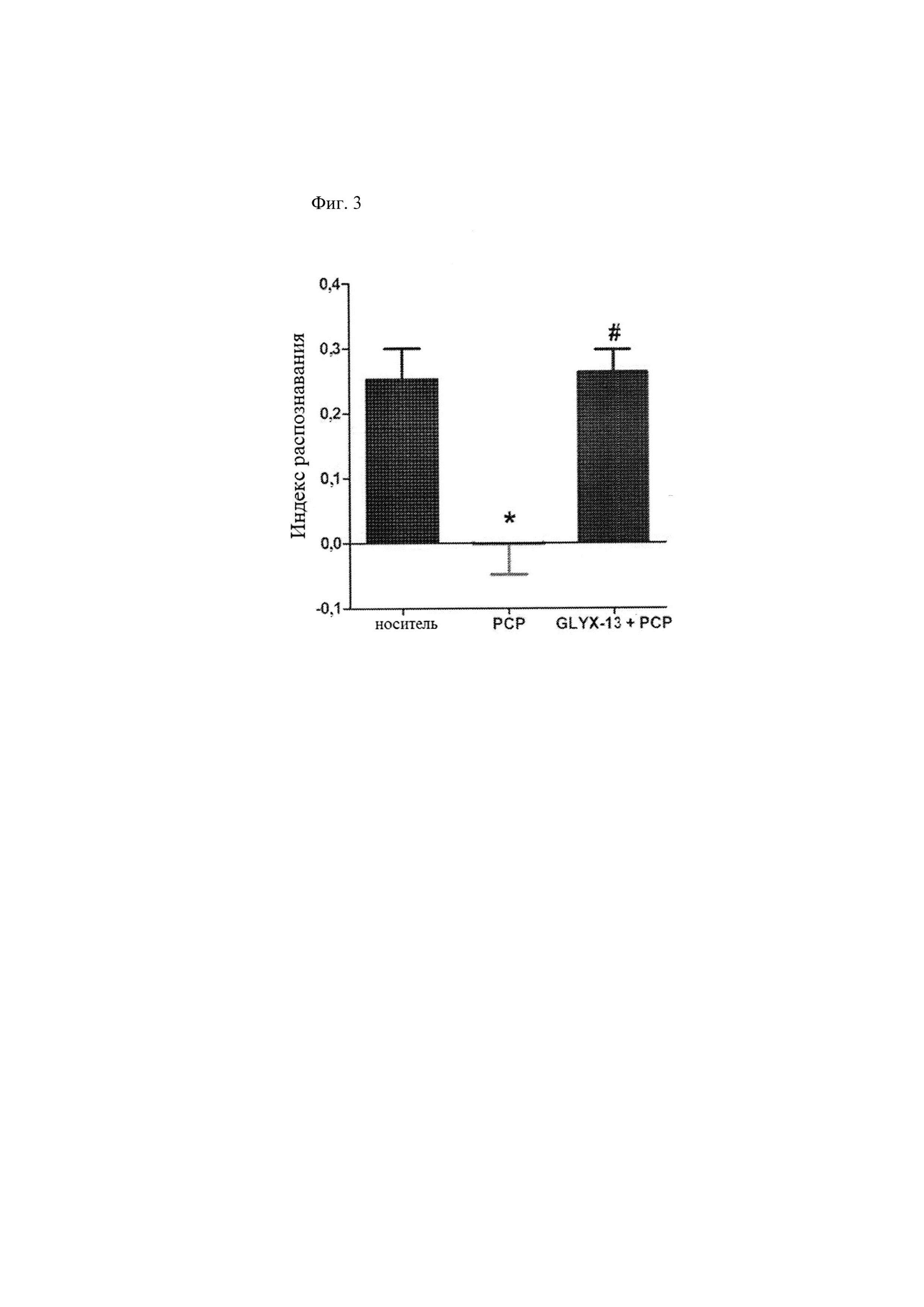
[0015] Фиг. 3 иллюстрирует среднее значение ± СОС показателя индекса различения при проведении теста распознавания нового объекта у взрослых самцов мышей C57BL/6, которым предварительно вводили два раза в день инъекцию РСР (10 мк/кг интраперитонеально) в течение 7 дней подряд, а затем инъекцию стерильного раствора хлорида натрия (носителя) за 1 час до проведения теста (группа, получавшая РСР), инъекцию GLYX-13 (1 мг/кг внутривенно) за 1 час до проведения теста (группа, получавшая GLYX-13 + РСР), или инъекции стерильного раствора хлорида натрия дважды в день в течение 7 дней и инъекцию носителя за 1 час до проведения теста. Индекс различения рассчитывали с использованием следующей формулы: (время, затраченное на изучение нового объекта - время, затраченное на изучение знакомого объекта)/ (общее время, затраченное на изучение и нового, и знакомого объектов). =8-10 на группу. * р<0,001, значимое уменьшение DI по сравнению с группой, получавшей носитель, # р<0,001, значимое обратное изменение DI по сравнению с группой, получавшей РСР (критерий PLSD Фишера по полученным результатам). Данные на фиг. 3 демонстрируют, что GLYX-13 (1 мг/кг внутривенно) вызывает обратное развитие хронического нарушения распознавания новых объектов у мышей, вызванного фенциклидином.
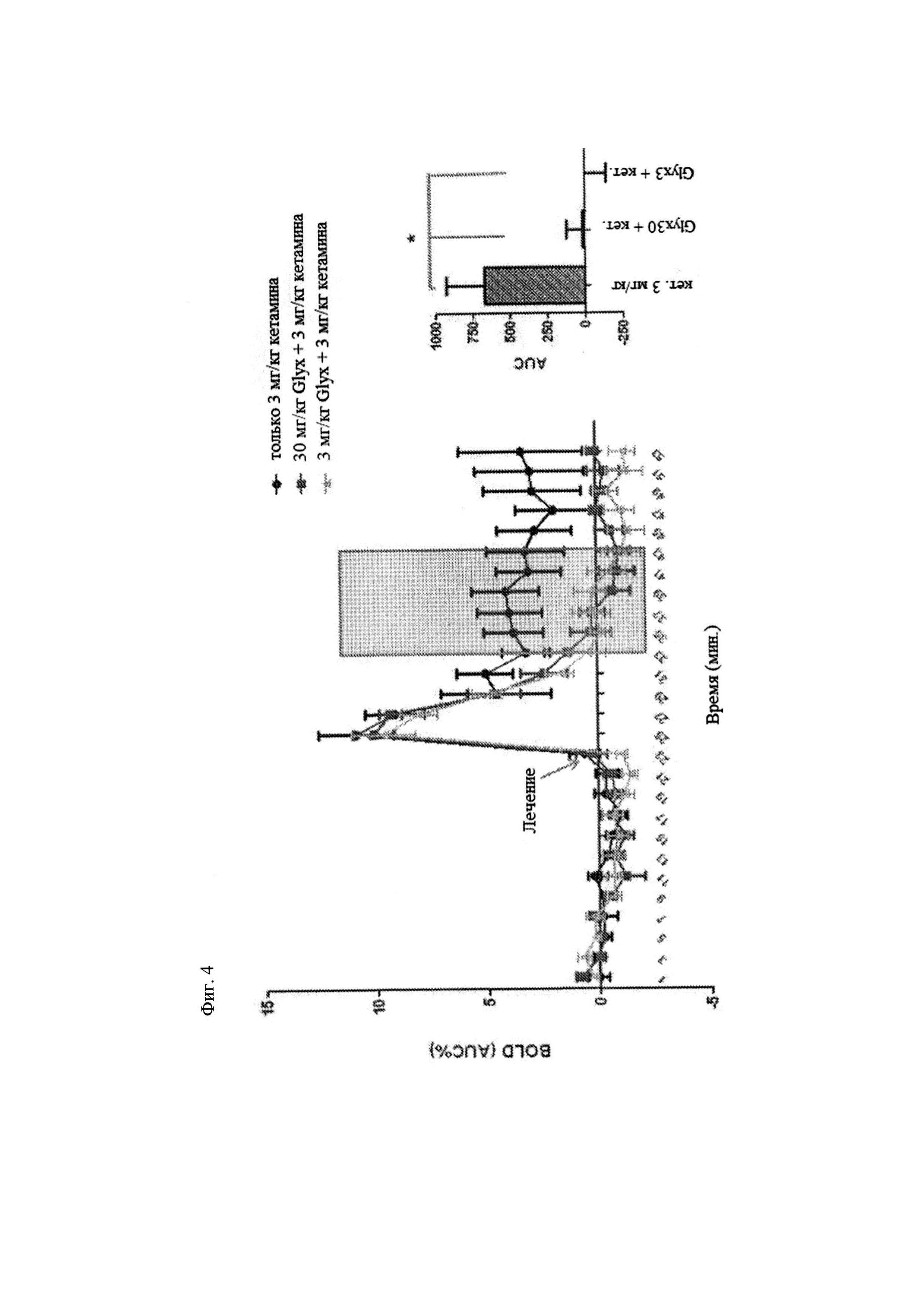
[0016] Фиг. 4 демонстрирует значимое ослабление ответа при предварительном лечении с использованием 3 мг/кг и 30 мг/кг GLYX-13 в соматосенсорной коре с последующим введением кетамина. Диаграмма слева демонстрирует среднюю зависимость от времени ROI SCtx. Диаграмма справа демонстрирует значимость в заштрихованном временном интервале, Р=0,0186, 1-факторный ANOVA; критерий Тьюки по полученным результатам.
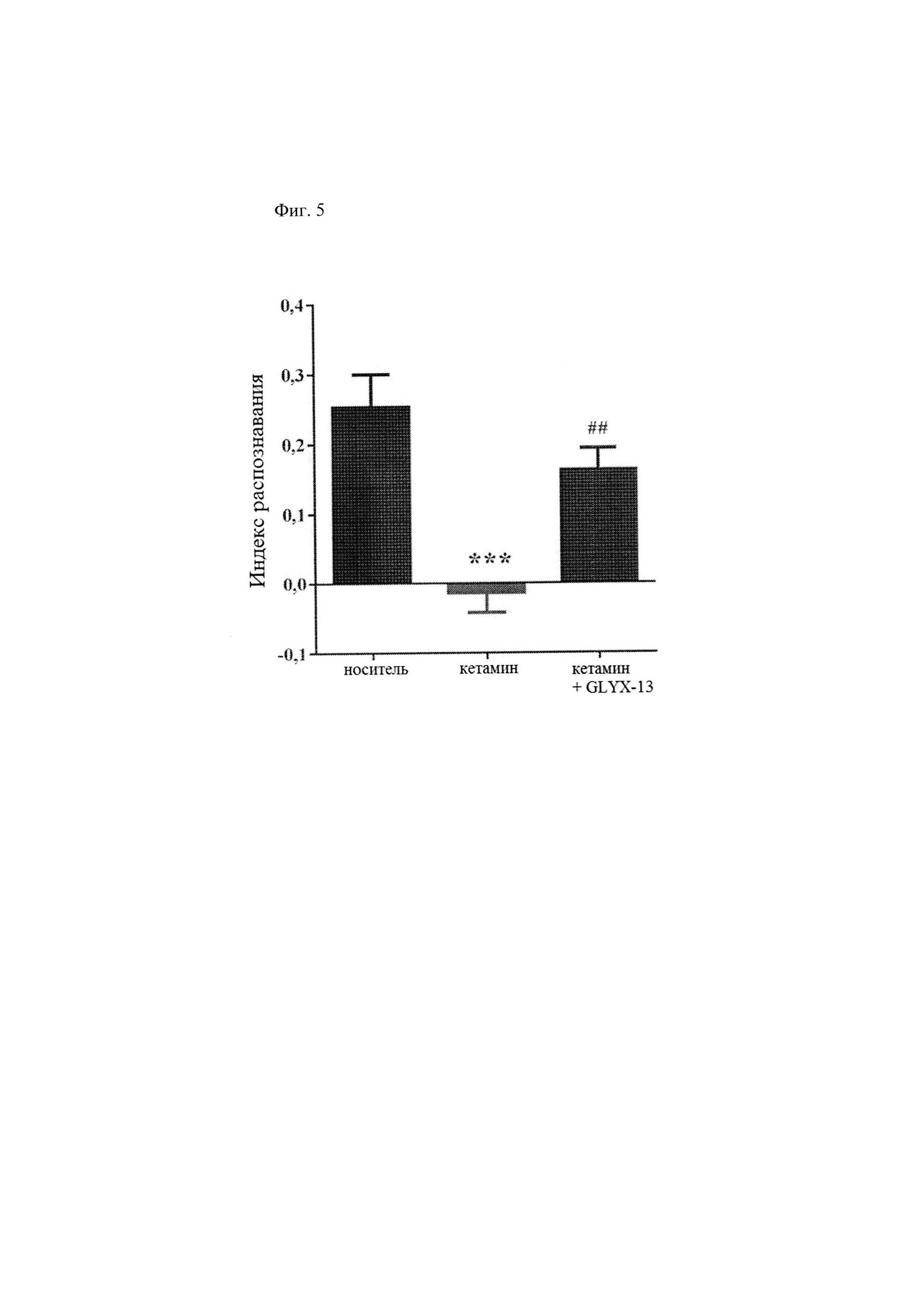
[0017] Фиг. 5 иллюстрирует среднее значение ± СОС показателя индекса различения при проведении теста распознавания нового объекта у взрослых самцов мышей C57BL/6, которым предварительно за 30 мин. до введения кетамина (10 мг/кг подкожно) вводили GLYX-13 (3 мг/кг внутривенно), а через 20 мин. проводили тест. Индекс различения рассчитывали с использованием следующей формулы: (время, затраченное на изучение нового объекта - время, затраченное на изучение знакомого объекта)/ (общее время, затраченное на изучение и нового, и знакомого объектов). N=8-11 на группу. *** р<0,0001, значимое уменьшение DI по сравнению с группой, получавшей носитель, ## р<0,01, значимое обратное изменение DI по сравнению с группой, получавшей кетамин (критерий PLSD Фишера по полученным результатам). Данные на фиг. 5 демонстрируют, что GLYX-13 (3 мг/кг внутривенно) вызывает обратное развитие острого нарушения распознавания новых объектов у мышей, вызванного кетамином (10 мг/кг подкожно).
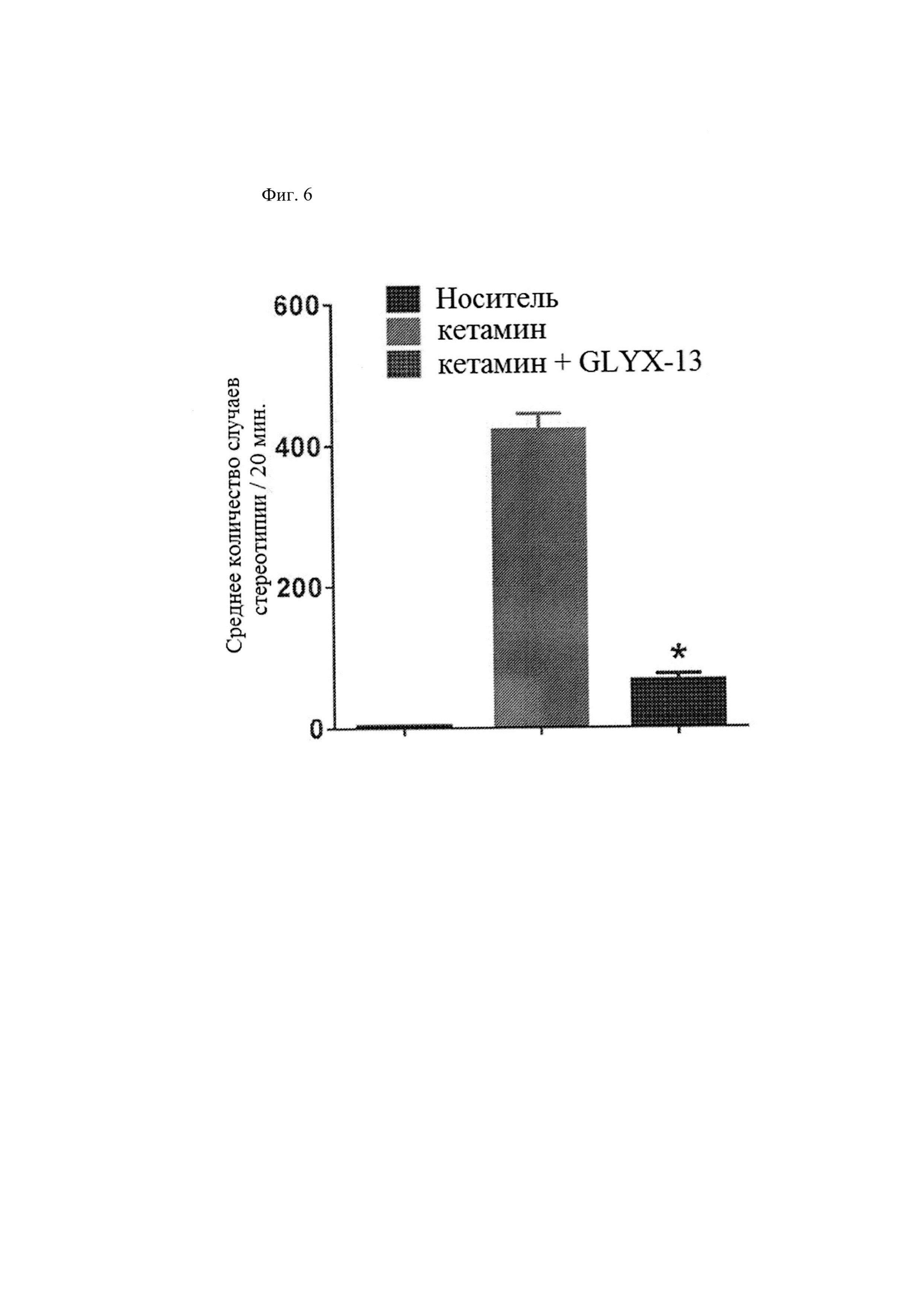
[0018] Фиг. 6 иллюстрирует среднее (±СОС) количество случаев стереотипии (движение по кругу и качание головой) на открытом пространстве у самцов крыс линии Спрег-Доули в возрасте 2-3 месяца, которым за 30 мин. до введения кетамина (10 мг/кг внутривенно) вводили GLYX-13 (3 мг/кг внутривенно). Животным, получавшим носитель, вводили инъекции раствора хлорида натрия (носителя) вместо инъекций GLYX-13 и кетамина. Животных помещали на открытое пространство непосредственно после введения последней дозы, и анализировали поведение в течение 20 мин. N=8-12. Данные на фиг. 6 демонстрируют, что GLYX-13 (3 мг/кг внутривенно) ингибирует стереотипию у крыс, вызванную кетамином (10 мг/кг внутривенно).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0019] Характерной особенностью данного изобретения являются комбинации, которые содержат один или более антагонистов NMDA-рецептора и GLYX-13 (каждый из которых в данном документе иногда упоминается как «компонент»). Положительное действие комбинации основано, в частности, на том наблюдении, что введение GLYX-13 (например, однократная доза) может вызвать обратное развитие и/или предотвратить когнитивное нарушение, вызванное антагонистом NMDA-рецептора (например, нарушение распознавания нового объекта, вызванное антагонистом NMDA-рецептора; например, вызванное повторяющимися дозами антагониста NMDA-рецептора). Комбинации могут дополнительно содержать один или более других биологически активных ингредиентов (например, один или более антидепрессантов) и/или одно или более фармацевтически приемлемых вспомогательных веществ и/или носителей. Компоненты комбинации (иногда также упоминаются в данном документе как химические структурные элементы или химические соединения) можно вводить пациенту последовательно (каждый компонент вводят в различное время) или практически одновременно. Понятно, что компоненты могут присутствовать в одном и том же фармацевтически приемлемом носителе и, следовательно, их можно вводить одновременно. В альтернативном варианте каждый из компонентов может присутствовать в отдельном фармацевтическом носителе, таком как традиционные лекарственные формы для перорального применения или формы для парентерального применения (или один компонент может быть в форме для перорального применения, а другой - в форме для парентерального), которые можно вводить или одновременно, или последовательно. В некоторых вариантах реализации изобретения особенно эффективным является предварительное лечение GLYX-13 (т.е. до введения одного или более антагонистов NMDA-рецептора).
[0020] «GLYX-13 » представлен следующей формулой:
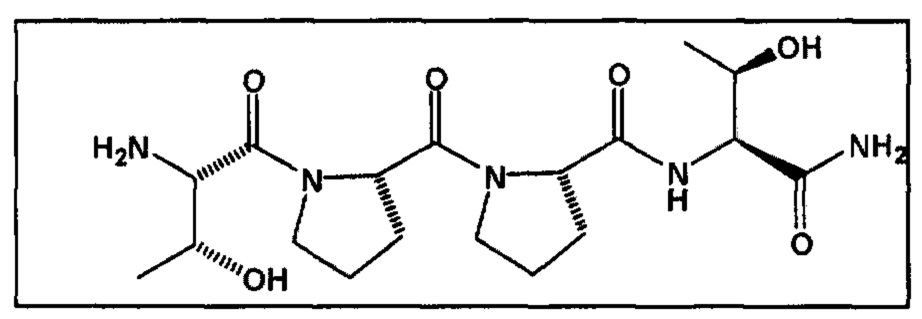
и включает полиморфы, гидраты, сольваты, свободное основание и/или пригодные соли вышеприведенного соединения.
[0021] «Лечение» включает любой результат, например уменьшение, снижение, изменение или устранение, который приводит к облегчению патологического состояния, заболевания, расстройства и тому подобного.
[0022] Термин «алкокси», при использовании в данном документе, относится к неразветвленной или разветвленной алкильной группе, присоединенной к кислороду (алкил-О-). Типовые алкокси-группы включают, но не ограничиваясь ими, алкокси группы с 1-6 или 2-6 атомами углерода, упомянутые в данном документе как С1-С6 алкокси и С2-С6 алкокси, соответственно. Типовые алкокси-группы включают, но не ограничиваясь ими, метокси, этокси, изопропокси и т.д.
[0023] Термин «алкил», при использовании в данном документе, относится к насыщенному неразветвленному или разветвленному углеводороду, такому как неразветвленная или разветвленная группа с 1-6, 1-4 или 1-3 атомами углерода, упомянутая в данном документе как C1-С6алкил, С1-С4алкил и С1-С3алкил, соответственно. Типовые алкильные группы включают, но не ограничиваясь ими, метил, этил, пропил, изопропил, 2-метил-1 -пропил, 2-метил-2-пропил, 2-метил-1-бутил, 3-метил-1-бутил, 3-метил-2-бутил, 2,2-диметил-1-пропил, 2-метил-1-пентил, 3-метил-1-пентил, 4-метил-1-пентил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 2,2-диметил-1-бутил, 3,3-диметил-1-бутил, 2-этил-1-бутил, бутил, изобутил, трет-бутил, пентил, изопентил, неопентил, гексил и т.д. Термин «галогеналкил», при использовании в данном документе, относится к насыщенным неразветвленным или разветвленным алкильным группам, в которых один или более атомов водорода алкильной группы замещены одним или более независимо выбранными галогенами. Термин «галогеналкил» охватывает алкильные группы, в которых все атомы водорода алкильной группы замещены независимо выбранными галогенами (иногда упомянутые как «пергалогенированные» алкильные группы). Типовые галогеналкильные группы включают, но не ограничиваясь ими, CH2F, CH2CH2Cl, CF3, CHFCH2Cl.
[0024] Термины «галогено» или «галоген», при использовании в данном документе, относятся к F, Cl, Br или I.
[0025] Термин «оксо», при использовании в данном документе, относится к радикалу =O.
[0026] При использовании в данном документе, оба термина «антагонист NMDA-рецептора» и «антагонист NMDAR», как правило, относятся к химическому структурному элементу, который способен связываться с сайтом связывания глицина NMDA-рецептора и действует как антагонист, или ингибитор, функций N-метил-D-аспартатного рецептора (NMDA-рецептора).
[0027] «Фармацевтически или фармакологически приемлемый» включает соединения и композиции, которые не вызывают побочной, аллергической или другой неблагоприятной реакции при введении животному или человеку в случае необходимости. Для введения людям препараты должны отвечать стандартам стерильности, пирогенности, общей безопасности и чистоты в соответствии с требованиями отдела биологических стандартов FDA.
[0028] Термин «фармацевтически приемлемый носитель» или «фармацевтически приемлемое вспомогательное вещество», при использовании в данном документе, относится ко всем без исключения растворителям, дисперсионным средам, покрытиям, агентам, обеспечивающим изотоничность, и агентам, замедляющим всасывание, и тому подобному, которые совместимы с фармацевтическим введением. Использование таких сред и агентов для фармацевтически активных веществ хорошо известно в данной области техники. Комбинации, описанные в данном документе, могут также содержать другие активные соединения, обеспечивающие вспомогательное, дополнительное или усиливающее действие.
[0029] Термин «фармацевтическая композиция», при использовании в данном документе, относится к композиции, содержащей по меньшей мере один из компонентов комбинаций, описанных в данном документе, вместе с одним или более фармацевтически приемлемыми носителями и/или вспомогательными веществами.
[0030] «Индивид», «пациент» или «субъект» используются взаимозаменяемо и включают любое животное, в том числе млекопитающих, предпочтительно мышей, крыс, других грызунов, кроликов, собак, кошек, свиней, крупный рогатый скот, овец, лошадей или приматов, а наиболее предпочтительно - людей. Комбинации изобретения можно вводить, как описано в данном документе, млекопитающему, такому как человек, но можно также вводить другим млекопитающим, таким как животные, нуждающиеся в ветеринарном лечении, например домашние животные (например, собаки, кошки и тому подобное), сельскохозяйственные животные (например, коровы, овцы, свиньи, лошади и тому подобное) и лабораторные животные (например, крысы, мыши, морские свинки и тому подобное). В некоторых вариантах реализации изобретения млекопитающее, которое лечат в соответствии со способами данного изобретения, представляет собой млекопитающее, которому необходимо лечение, например, боли или депрессии.
[0031] Термин «эффективное количество» относится к количеству рассматриваемого компонента, которое будет вызывать биологический или медицинский отклик в ткани, системе, у животного или человека, необходимый исследователю, ветеринару, врачу или другому специалисту. В качестве примера эффективное количество может представлять собой количество, эффективное для лечения любого заболевания, расстройства и патологического состояния, описанного в данном документе. В альтернативном варианте эффективное количество может относиться к количеству, необходимому для достижения требуемого терапевтического и/или профилактического эффекта, такому как количество GLYX-13, которое вызывает обратное развитие и/или предотвращает когнитивное нарушение, вызванное антагонистом NMDA-рецептора (например, нарушение распознавания нового объекта, вызванное антагонистом NMDA-рецептора; например, вызванное повторяющимися дозами антагониста NMDA-рецептора).
[0032] Термин «фармацевтически приемлемая(-ые) соль(-и)», при использовании в данном документе, относится к солям кислотных или основных групп, которые могут присутствовать в соединениях, используемых в комбинациях настоящего изобретения. Соединения, включенные в комбинации настоящего изобретения, которые имеют основную природу, способны образовывать большое количество солей с различными неорганическими и органическими кислотами. Кислоты, которые можно использовать для получения фармацевтически приемлемых солей присоединения кислоты таких основных соединений, представляют собой те, которые образуют нетоксичные соли присоединения кислоты, т.е. соли содержащие фармакологически приемлемые анионы, в том числе, но не ограничиваясь ими, соли маната, оксалата, хлорида, бромида, иодида, нитрата, сульфата, гидросульфата, фосфата, кислого фосфата, изоникотината, ацетата, лактата, салицилата, цитрата, тартрата, олеата, танната, пантотената, гидротартрата, аскорбата, сукцината, малеата, гентизината, фумарата, глюконата, глюкуроната, сахарата, формиата, бензоата, глутамата, метансульфоната, этансульфоната, бензолсульфоната, n-толуолсульфоната и памоата (т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоата)). Соединения, содержащиеся в комбинациях согласно настоящему изобретению, которые имеют кислотную природу, способны образовывать соли присоединения основания с различными фармакологически приемлемыми катионами. Примеры таких солей включают соли щелочных или щелочноземельных металлов, в частности соли кальция, магния, натрия, лития, цинка, калия и железа. Соединения, содержащиеся в комбинациях согласно настоящему изобретению, которые содержат основный или кислотный фрагмент, могут также образовывать фармацевтически приемлемые соли с различными аминокислотами. Соединения, включенные в комбинации настоящего изобретения, могут содержать как кислотную, так и основную группы; например, одну аминогруппу и одну карбоксильную группу. В таком случае соединение может существовать в виде соли присоединения кислоты, цвиттер-иона или соли присоединения основания.
[0033] Соединения, содержащиеся в комбинациях согласно настоящему изобретению, могут содержать один или более хиральных центров и/или двойных связей, а следовательно, существовать в виде геометрических изомеров, энантиомеров или диастереомеров. Энантиомеры и диастереомеры могут быть обозначены символами «(+)», «(-)», «R» или «S» в зависимости от конфигурации заместителей вокруг стереогенного атома углерода, но специалистам в данной области понятно, что структура может неявно указывать на хиральный центр. Также у соединений по настоящему изобретению могут быть геометрические изомеры, обусловленные расположением заместителей вокруг двойной связи углерод-углерод или расположением заместителей вокруг циклоалкильного или гетероалкильного кольца. Заместители вокруг двойной связи углерод-углерод могут пребывать в «Z» или «E» конфигурации, причем термины «Z» и «Е» используются в соответствии со стандартами IUPAC. Если не указано иное, структуры с изображением двойных связей охватывают как «E», так и «Z» изомеры. В альтернативном варианте заместители вокруг двойной связи углерод-углерод могут быть обозначены как «цис» или «транс», где «цис» представляет расположение заместителей на одной и той же стороне относительно двойной связи, а «транс» представляет расположение заместителей на противоположных сторонах относительно двойной связи. Расположение заместителей в карбоциклическом кольце может быть также обозначено как «цис» или «транс». Термин «цис» представляет расположение заместителей на одной и той же стороне относительно плоскости кольца, а термин «транс» обозначает расположение заместителей на противоположных сторонах относительно плоскости кольца. Смеси соединений, в которых заместители расположены как по одну сторону, так и на противоположных сторонах относительно плоскости кольца обозначены «цис/транс».
[0034] Соединения, содержащиеся в комбинациях согласно настоящему изобретению, могут существовать в сольватированной, а также в несольватированной формах с фармацевтически приемлемыми растворителями, такими как вода, этанол и тому подобное, и предполагается, что изобретение охватывает как сольватированную, так и несольватированную формы. В одном варианте реализации изобретения соединение является аморфным. В одном варианте реализации изобретения соединение представляет собой одну полиморфную модификацию. В другом варианте реализации изобретения соединение представляет собой смесь полиморфных модификаций. В другом варианте реализации изобретения соединение находится в кристаллической форме.
[0035] Термин «пролекарство» относится к соединениям, которые превращаются in vivo с образованием описанного соединения или фармацевтически приемлемой соли, гидрата или сольвата соединения. Превращение может происходить по различным механизмам (таким как эстеразный, амидазный, фосфатазный, окислительный и/или восстановительный метаболизм) в различных местоположениях (таких как полость кишечника или при прохождении через кишечник, кровь или печень). Про лекарства хорошо известны в данной области техники (например, см. Rautio, Kumpulainen, et al., Nature Reviews Drug Discovery 2008, 7, 255). Например, если соединение по данному изобретению или фармацевтически приемлемая соль, гидрат или сольват соединения содержит карбоксильную функциональную группу, пролекарство может являться сложным эфиром, полученным путем замещения атома водорода кислотной группы такой группой, как (С1-С8)алкил, (С2-С12)алканоилоксиметил, 1-(алканоилокси)этил, содержащий от 4 до 9 атомов углерода, 1-метил-1-(алканоилокси)этил, содержащий от 5 до 10 атомов углерода, алкоксикарбонилоксиметил, содержащий от 3 до 6 атомов углерода, 1-(алкоксикарбонилокси)этил, содержащий от 4 до 7 атомов углерода, 1-метил-1-(алкоксикарбонилокси)этил, содержащий от 5 до 8 атомов углерода, N-(алкоксикарбонил)аминометил, содержащий от 3 до 9 атомов углерода, 1-(N-(алкоксикарбонил)амино)этил, содержащий от 4 до 10 атомов углерода, 3-фталидил, 4-кротонолактонил, гамма-бутиролактон-4-ил, ди-N,N-(С1-С2)алкиламино(С2-С3)алкил (такой как β-диметиламиноэтил), карбамоил-(С1-С2)алкил, N,N-ди(С1-С2)алкилкарбамоил-(С1-С2)алкил и пиперидино-, пирролидино- или морфолино(С2-С3)алкил.
Комбинация компонентов
[0036] GLYX-13 можно получить с помощью хорошо известных рекомбинантных или синтетических способов, таких как описанные в патентах США №5763393 и 4086196, которые включены в данный документ в полном объеме посредством ссылки. Также предусмотрены полиморфы, гидраты, гомологи, сольваты, свободные основания и/или пригодные соли GLYX 13, такие как, но не ограничиваясь этим, ацетатная соль. Пептид может быть в циклической или нециклической формах, что дополнительно описано в патенте США №5763393. В некоторых вариантах реализации изобретения аналог GLYX-13 может включать вставку или делецию фрагмента в одной или более группах Thr или Pro, такую как делеция фрагмента СН2, ОН или NH2. В других вариантах реализации изобретения GLYX-13 может быть необязательно замещен одним или более галогенами, С1-С3 алкилом (необязательно замещенным галогеном или аминогруппой), гидроксилом и/или аминогруппой. Другие соединения, предусмотренные для использования в данном изобретении, включают частичные агонисты глицинового сайта NMDA-рецептора, описанные в патентах США №5763393, 6107271 и в Wood et al., Neuro. Report, 19, 1059-1061, 2008, полное содержание которых включено в данный документ посредством ссылки.
[0037] Необходимо понимать, что пептиды, описанные в данном документе, могут включать как природные и неприродные аминокислоты, например все природные аминокислоты (или их производные), все неприродные аминокислоты (или их производные) или смесь природных и неприродных аминокислот. Например, одна, две, три или более аминокислот в GLYX-13 независимо могут иметь d- или l-конфигурацию.
[0038] В некоторых вариантах реализации изобретения антагонист NMDA-рецептора выбран из группы, состоящей из кетамина, мемантина, ланицемина (AZD6765), CERC-301, декстрометорфана, декстрорфана, фенциклидина, дизоцилпина (МК-801), амантадина, ифенпродила, AV-101, AZD 6423 и рилузола, или их фармацевтически приемлемых солей, или их пролекарств. Также предусмотрены производные вышеупомянутых антагонистов NMDA-рецептора.
[0039] В некоторых вариантах реализации изобретения антагонист NMDA-рецептора имеет формулу (I):
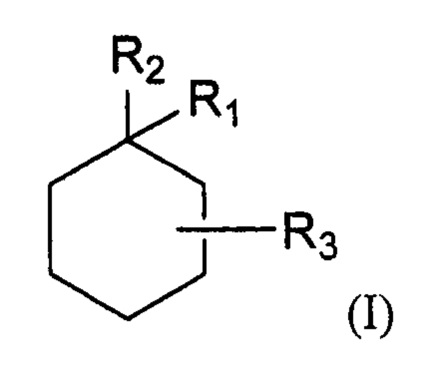
где:
R1 представляет собой фенил, тиенил или бензотиенил, каждый из которых необязательно замещен 1-3 заместителями, независимо выбранными из группы, состоящей из галогена; -ОН; NRaRb, где каждый из Ra и Rb независимо выбран из Н и С1-С3 алкила; С1-С3 алкила; и С1-С3 алкокси; R2 представляет собой -NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-С6 алкила, который необязательно замещен -ОН или С1-С3 алкокси; или Rc и Rd вместе с атомом азота, к которому каждый присоединен, образуют 5-7-членное кольцо, которое необязательно замещено 1-2 независимо выбранными С1-С3 алкилами; и
R3 представляет собой Н, оксо или С1-С3 алкил; или его фармацевтически приемлемую соль, или его пролекарство.
[0040] В некоторых вариантах реализации изобретения R1 представляет собой фенил, который необязательно замещен 1-3 заместителями, независимо выбранными из группы, состоящей из галогена; -ОН; NRaRb, где каждый из Ra и Rb независимо выбран из Н и С1-С3 алкила; С1-С3 алкила; и С1-С3 алкокси. Например, R1 может представлять собой фенил, 3-гидроксифенил, 3-метоксифенил, 3-аминофенил, 3-метилфенил, 4-фторфенил, 4-гидроксифенил, 3-метоксифенил или 2-хлорфенил. В других вариантах реализации изобретения R1 представляет собой необязательно замещенный тиенил или необязательно замещенный бензотиенил.
[0041] В некоторых вариантах реализации изобретения R2 представляет собой -NRcRd, причем каждый из Rc и Rd независимо выбран из Н и С1-С6 алкила, который необязательно замещен -ОН или С1-С3 алкокси, например Н и C1-С6 алкила, например Н и С1-С3 алкила, например один из Rc и Rd представляет собой Н, а другой представляет собой С1-С3 алкил. Например, R2 может представлять собой -NH(C1-C3 алкил), такой как -NH(СН3). В других вариантах реализации изобретения R2 представляет собой -NRcRd, где Rc и Rd вместе с атомом азота, к которому каждый присоединен, образует 5-7-членное кольцо, которое необязательно замещено 1-2 независимо выбранными С1-С3 алкилами, такое как пиперидинил.
[0042] В некоторых вариантах реализации изобретения R3 представляет собой Н или оксо.
[0043] В некоторых вариантах реализации изобретения:
R1 представляет собой фенил, который необязательно замещен 1-3 заместителями, независимо выбранными из группы, состоящей из галогена; -ОН; NRaRb, где каждый из Ra и Rb независимо выбран из Н и С1-С3 алкила; С1-С3 алкила; и С1-С3 алкокси (например, R1 представляет собой фенил, 3-гидроксифенил, 3-метоксифенил, 3-аминофенил, 3-метилфенил, 4-фторфенил, 4-гидроксифенил, 3-метоксифенил или 2-хлорфенил);
R2 представляет собой -NRcRd, где каждый из Rc и Rd независимо выбран из Н и C1-С6 алкила, который необязательно замещен -ОН или С1-С3 алкокси; например Н и C1-С6 алкила, например Н и С1-С3 алкила; например, один из Rc и Rd представляет собой Н, а другой представляет собой С1-С3 алкил; например R2 может представлять собой -NH(С1-С3 алкил), такой как -NH(СН3); и
R3 представляет собой Н или оксо (например, оксо).
[0044] В некоторых вариантах реализации изобретения:
R1 представляет собой фенил, который необязательно замещен 1 -3 заместителями, независимо выбранными из группы, состоящей из галогена; -ОН; NRaRb, где каждый из Ra и Rb независимо выбран из Н и С1-С3 алкила; С1-С3 алкила; и С1-С3 алкокси (например, R1 представляет собой фенил, 3-гидроксифенил, 3-метоксифенил, 3-аминофенил, 3-метилфенил, 4-фторфенил, 4-гидроксифенил, 3-метоксифенил или 2-хлорфенил);
R2 представляет собой -NRcRd, где Rc и Rd вместе с атомом азота, к которому каждый присоединен, образуют 5-7-членное кольцо, которое необязательно замещено 1-2 независимо выбранными С1-С3 алкилами, такое как пиперидинил; и R3 представляет собой Н или оксо (например, Н).
[0045] В некоторых вариантах реализации изобретения R1 представляет собой фенил, R2 представляет собой пиперидинил, a R3 представляет собой Н. Например, соединение может представлять собой фенциклидин.
[0046] В некоторых вариантах реализации изобретения R1 представляет собой 2-хлорфенил, R2 представляет собой -NH(СН3), a R3 представляет собой оксо. Например, соединение может представлять собой кетамин, например (S)-кетамин.
[0047] В некоторых вариантах реализации изобретения антагонист NMDA-рецептора представляет собой мемантин или амантадин. В некоторых вариантах реализации изобретения антагонист NMDA-рецептора представляет собой дизоцилпин (MK-801). В некоторых вариантах реализации изобретения антагонист NMDA-рецептора представляет собой декстрометорфан или декстрорфан. В некоторых вариантах реализации изобретения антагонист NMDA-рецептора представляет собой ланицемин (AZD6765), CERC-301 или ифенпродил. В некоторых вариантах реализации изобретения антагонист NMDA-рецептора представляет собой AV-101 или AZD 6423.
[0048] В некоторых вариантах реализации изобретения антагонист NMDA-рецептора выбран из группы, состоящей из закиси азота, атомоксетина, декстраллорфана, дифенидина, этициклидина, гациклидина, ибогаина, метоксетамина, нитромемантина, ролициклидина, теноциклидина, метоксидина, тилетамина, нерамексана, элипродила, этоксадрола, дексоксадрола, метадона, WMS-2539, NEFA, ремацемида, делуцемина, 8А-PDHQ, аптиганеля (церестата, CNS-1102), HU-211, ремацемида, ринкофиллина, ТК-40, траксопродила (CP-101,606), 1-аминоциклопропанкарбоновой кислоты (АСРС), кинуреновой кислоты или ее производного, 2-карбокситетрагидрохинолина или его производного, 2-карбоксииндола или его производного, 4-гидрокси-2-хинолина или его производного, 4-гидроксихинолина или его производного, хиноксалин-2,3-диона или его производного, трициклических антагонистов, лакосамида, L-фенилаланина, мидафотеля и аптиганеля, или их фармацевтически приемлемых солей, или их пролекарств.
[0049] См. также, например, те, которые описаны в Kvist et. al., J. Biol. Chem. 2013 288: 33124-33135, которая включена в данный документ в полном объеме посредством ссылки. См. также, например, те, которые описаны в Traynelis et al., Pharmacological Reviews 2010, 62, 405, которая включена в данный документ в полном объеме посредством ссылки (например, CGP-61594; CGP-58411; АСЕА-1011 и 1021; L-701,324; (R)-AP5; (R)-AP7; РМРА; (R)-CPP; NVP-AAM077; PPDA; (R)-a-AA; PBPD; UBP141; CGS-19755 (селфотел); CGP-43487; CGP-40116; конантокины, например Br, G, Pr1, Pr2, Pr3, R и T; радипродил; и MK-0657).
[0050] В некоторых вариантах реализации изобретения антагонист NMDA-рецептора представляет собой кинуреновую кислоту или ее производное, 2-карбокситетрагидрохинолин или его производное, 2-карбоксииндол или его производное, 4-гидрокси-2-хинолин или его производное, 4-гидроксихинолин или его производное, хиноксалин-2,3-дион или его производное или трициклический антагонист. Примеры таких соединений описаны в данном документе и, например, в Danysz et al., Pharmacological Reviews 1998, 50, 597, которая включена в данный документ в полном объеме посредством ссылки.
Способы
[0051] В одном аспекте изобретения предложены способы осуществления значительного обратного развития или предотвращения когнитивного нарушения у пациента, которому интенсивно кратковременно вводят антагонист NMDA-рецептора, включающие введение эффективного количества GLYX-13.
[0052] В другом аспекте изобретения предложены способы лечения когнитивного нарушения у пациента, нуждающегося в этом, включающие введение эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. Когнитивное нарушение может возникать вследствие одной или более причин из: недостатка когнитивных способностей, врожденных патологий, фактора(-ов) окружающей среды или приема лекарственных средств, и включать, но не ограничиваясь ими, нарушения способности к обучению и/или дислексию. В некоторых вариантах реализации изобретения эффективное количество GLYX-13 вводят до или после интенсивного кратковременного введения одного или более антагонистов NMDA-рецептора. В других вариантах реализации изобретения эффективное количество GLYX-13 вводят практически одновременно с интенсивным кратковременным введением одного или более антагонистов NMDA-рецептора.
[0053] В дополнительном аспекте изобретения предложены способы лечения расстройства, патологического состояния или заболевания, в том числе, но не ограничиваясь ими: неврологических или других заболеваний (например, инсульта, психоза, боли (например, невропатической боли), депрессии (например, клинической депрессии), болезни Паркинсона и болезни Альцгеймера); заболевания центральной нервной системы (например, нейродегенеративного заболевания, инсульта, травматического повреждения головного мозга и повреждения спинного мозга); шизофрении; и/или депрессии (например, резистентной депрессии), которые включают введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. Другие иллюстративные патологические состояния включают, но не ограничиваясь ими, нарушение способности к обучению, аутическое расстройство, синдром дефицита внимания с гиперактивностью, тревожное расстройство, мигрень, синдром Туретта, фобию, посттравматическое стрессовое расстройство, деменцию, нарушения памяти, связанные с возрастом, СПИД-деменцию, болезнь Хантингтона, спастичность, миоклонию, мышечный спазм, биполярное расстройство, невропатическую боль, расстройство, связанное со злоупотреблением психоактивными веществами, недержание мочи, ишемию, специфические нарушения способности к обучению, эпилептические припадки, судороги после инсульта, ишемию головного мозга, гипогликемию, остановку сердечной деятельности и эпилепсию. В некоторых вариантах реализации изобретения GLYX-13 и один или более антагонистов NMDA-рецептора вводят практически одновременно. В других вариантах реализации изобретения GLYX-13 и один или более антагонистов NMDA-рецептора вводят последовательно, например, GLYX-13 вводят до или после одного или более антагонистов NMDA-рецептора.
[0054] Предусмотренные способы включают способ лечения аутизма и/или расстройства аутистического спектра у пациента, нуждающегося в этом, включающий введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. В варианте реализации изобретения предусмотрен способ уменьшения симптомов аутизма у пациента, нуждающегося в этом, включающий введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. Например, при введении комбинации могут уменьшать частоту возникновения одного или более симптомов аутизма, таких как избегание визуального контакта, неспособность к социализации, дефицит внимания, плохое настроение, гиперактивность, патологическое восприятие звуков, неправильная речь, нарушение сна и персеверация. Указанное снижение частоты возникновения может быть измерено относительно частоты возникновения у индивида, не проходившего лечение, или у индивидов, не проходивших лечение.
[0055] В некоторых вариантах реализации изобретения пациенты, страдающие от аутизма, страдают также от другого медицинского состояния, такого как синдром ломкой Х-хромосомы, туберозный склероз, синдром врожденной краснухи и нелеченая фенилкетонурия.
[0056] В некоторых вариантах реализации изобретения предусмотрены способы лечения расстройства у пациента, нуждающегося в этом, причем указанное расстройство выбрано из группы, состоящей из: ишемии головного мозга, инсульта, травмы головного мозга, опухолей головного мозга, острой невропатической боли, хронической невропатической боли, расстройств сна, привыкания к наркотическим средствам, депрессии, расстройств центрального зрения, алкогольного абстинентного синдрома, тревожного расстройства, неспособности к запоминанию и обучению, аутизма, эпилепсии, СПИД-деменции, множественной системной атрофии, прогрессирующего супрануклеарного паралича, атаксии Фридрейха, синдрома Дауна, синдрома ломкой X-хромосомы, туберозного склероза, оливопонтоцеребеллярной атрофии, церебрального паралича, неврита зрительного нерва, обусловленного действием лекарственного средства, периферической невропатии, миелопатии, ишемической ретинопатии, диабетической ретинопатии, глаукомы, остановки сердечной деятельности, поведенческих расстройств, расстройств побуждений, заболевания Альцгеймера, потери памяти, сопровождающей болезнь Альцгеймера на ранней стадии, синдрома дефицита внимания, СДВГ, шизофрении, облегчения опиатной, никотиновой, алкогольной зависимости, травматического повреждения головного мозга, повреждения спинного мозга, посттравматического стрессового синдрома и хореи Хантингтона, которые включают введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора.
[0057] В некоторых вариантах реализации в данном изобретении предусмотрены способы лечения синдрома дефицита внимания, СДВГ (синдрома дефицита внимания с гиперактивностью), шизофрении, тревожного расстройства, облегчения опиатной, никотиновой и/или алкогольной зависимости (например, способ лечения такой зависимости или облегчения побочных эффектов отказа от такой зависимости), повреждения спинного мозга, диабетической ретинопатии, травматического повреждения головного мозга, посттравматического стрессового синдрома и/или хореи Хантингтона, у пациента, нуждающегося в этом, включающие введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. Например, пациенты, страдающие от шизофрении, зависимости (например, алкогольной или опиатной), аутизма, хореи Хантингтона, травматического повреждения головного мозга, повреждения спинного мозга, посттравматического стрессового синдрома или диабетической ретинопатии, могут страдать вследствие измененной экспрессии или функций NMDA-рецептора.
[0058] Например, в данном документе предложен способ лечения депрессии у пациента, нуждающегося в этом, включающий введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. В некоторых вариантах реализации изобретения пациента, устойчивого к лечению, определяют как пациента, которого лечили по меньшей мере двумя типами антидепрессантов до введения комбинаций, описанных в данном документе. В других вариантах реализации изобретения пациент, устойчивый к лечению, представляет собой пациента, который не желает или не способен переносить побочные эффекты по меньшей мере одного типа лечения с использованием анти депрессантов.
[0059] Наиболее распространенные депрессивные состояния включают большое депрессивное расстройство и дистимическое расстройство. Другие депрессивные состояния развиваются при особых обстоятельствах. Такие депрессивные состояния включают, но не ограничиваясь ими, психотическую депрессию, послеродовую депрессию, сезонное аффективное расстройство (SAD), расстройство настроения, депрессии, вызванные хроническими медицинскими состояниями, такими как рак или хроническая боль, химиотерапия, хронический стресс, посттравматические стрессовые расстройства и биполярное расстройство (или маниакально-депрессивное расстройство).
[0060] Резистентная депрессия возникает у пациентов, страдающих от депрессии, которые устойчивы к стандартным фармакологическим способам лечения, в том числе к трициклическим антидепрессантам, ИМАО, СИОЗС и ингибиторам двойного и тройного захвата и/или анксиолитическим средствам, а также к нефармакологическим способам лечения, таким как психотерапия, электроконвульсивная терапия, стимуляция блуждающего нерва и/или транскраниальная магнитная стимуляция Пациент, устойчивый к лечению, может быть определен как пациент, который не ощущает облегчения одного или более симптомов депрессии (например, постоянная тревога или грусть, ощущения беспомощности, безнадежности, пессимизм), несмотря на проведение одного или более стандартных фармакологических или нефармакологических способов лечения. В некоторых вариантах реализации изобретения пациент, устойчивый к лечению, представляет собой пациента, который не ощущает ослабление одного или более симптомов депрессии, несмотря на проведение лечения с помощью двух различных антидепрессантов. В других вариантах реализации изобретения пациент, устойчивый к лечению, представляет собой пациента, который не ощущает ослабление одного или более симптомов депрессии, несмотря на проведение лечения с помощью четырех различных антидепрессантов. Пациент, устойчивый к лечению, также может быть определен как пациент, который не желает или не способен переносить побочные эффекты одного или более стандартных фармакологических или нефармакологических способов лечения.
[0061] Еще в одном аспекте изобретения предложен способ усиления обезболивания и оказания анальгетического действия животному. В некоторых вариантах реализации изобретения предложены способы для лечения невропатической боли. Невропатическая боль может быть острой или хронической. В некоторых случаях невропатическая боль может быть связана с таким патологическим состоянием, как герпес, ВИЧ, травматическое повреждение нервов, инсульт, постишемическая боль, фибромиалгия, симпатическая рефлекторная дистрофия, комплексный регионарный болевой синдром, повреждение спинного мозга, воспаление седалищного нерва, фантомная боль в ампутированных конечностях, диабетическая невропатия и невропатическая боль, вызванная раком и химиотерапией. Также предусмотрены способы усиления обезболивания и оказания анальгезирующего действия пациенту.
[0062] В некоторых вариантах реализации изобретения предложены способы лечения шизофрении. Например, с использованием способов и композиций, предусмотренных в данном документе, можно лечить параноидальную шизофрению, шизофрению дезорганизованного типа (т.е. гебефреническую шизофрению), кататоническую шизофрению, шизофрению недифференцированного типа, остаточную шизофрению, постшизофреническую депрессию и простую шизофрению. С использованием композиций, предусмотренных в данном документе, можно также лечить психозы, такие как шизоаффективные расстройства, бредовые расстройства, кратковременные психотические расстройства, индуцированные психотические расстройства и психотические расстройства с бредом или галлюцинациями.
[0063] Параноидальная шизофрения может характеризоваться наличием бреда или слуховых галлюцинаций, но отсутствием нарушения мышления, дезорганизованного поведения или аффективного уплощения. Бред может представлять собой бред преследования и/или бред величия, но в дополнение к этим, могут присутствовать и другие темы, такие как ревность, религиозность, или соматизация.
[0064] Шизофрения дезорганизованного типа может характеризоваться наличием и расстройства мышления, и аффективного уплощения.
[0065] Кататоническая шизофрения может характеризоваться тем, что субъект может быть практически неподвижным или демонстрировать возбужденные бесцельные движения. Симптомы могут включать кататонический ступор и восковую гибкость.
[0066] Шизофрения недифференцированного типа может характеризоваться наличием психотических симптомов, но критерии для параноидальной, дезорганизованной или кататонической формы не выполняются.
[0067] Остаточная шизофрения может характеризоваться тем, что интенсивность позитивных симптомов только низкая.
[0068] Постшизофреническая депрессия может характеризоваться возникновением депрессивного эпизода после шизофрении, при этом некоторые незначительные симптомы шизофрении могут оставаться.
[0069] Простая шизофрения может характеризоваться постепенным и прогрессирующим развитием главных негативных симптомов без истории психотических эпизодов.
[0070] В некоторых вариантах реализации изобретения предложены способы лечения психотических симптомов, которые могут присутствовать при других психических расстройствах, в том числе, но не ограничиваясь ими, при биполярном расстройстве, пограничном личностном расстройстве, лекарственной интоксикации и психозе, вызванном лекарственными средствами.
[0071] В другом варианте реализации изобретения предложены способы лечения бреда (например, «непричудливого»), который может присутствовать, например, при бредовом расстройстве.
[0072] Также предложены способы лечения социальной самоизоляции при патологических состояниях, включающих, но не ограничиваясь ими, социальное тревожное расстройство, уклоняющееся расстройство личности и шизотипическое расстройство личности.
[0073] Дополнительно, предложены способы лечения обсессивно-компульсивного расстройства (ОКР).
[0074] Также в данном документе предложен способ модулирования экспрессии гена-мишени аутизма в клетке, включающий приведение клетки в контакт с комбинациями, описанными в данном документе, например с эффективным количеством GLYX-13 и одного или более антагонистов NMDA-рецептора. Экспрессия гена аутизма может быть выбрана, например, из АВАТ, АРОЕ, CHRNA4, GABRA5,GFAP, GRIN2A, PDYN и PENK. В другом варианте реализации изобретения предложен способ модулирования синаптической пластичности у пациента, страдающего от расстройства, связанного с синаптической пластичностью, включающий введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора.
[0075] В другом варианте реализации изобретения предложен способ лечения болезни Альцгеймера или, например, лечения потери памяти, например, сопровождающей болезнь Альцгеймера на ранней стадии, у пациента, нуждающегося в этом, включающий введение комбинаций, описанных в данном документе, например эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора. В настоящем документе предложен также способ модулирования амилоидного белка Альцгеймера (например, бела-амилоидного пептида, например, изоформы Аβ1-42) in vitro или in vivo (например, в клетке), включающий приведение в контакт указанного белка с комбинациями, описанными в данном документе, например с эффективным количеством GLYX-13 и одного или более антагонистов NMDA-рецептора. Например, в некоторых вариантах реализации изобретения GLYX-13 или другое описанное соединение может блокировать способность такого амилоидного белка ингибировать долгосрочную потенциацию в гиппокампальных срезах, а также апоптическую гибель нейронных клеток. В некоторых вариантах реализации изобретения описанное соединение (например, GLYX-13) может обеспечивать нейропротекторные свойства для пациента, страдающего от болезни Альцгеймера, нуждающегося в этом, например, может обеспечивать терапевтический эффект в отношении гибели нейронных клеток, связанной с поздней стадией болезни Альцгеймера.
[0076] В некоторых вариантах реализации изобретения пациент представляет собой человека, например ребенка.
[0077] Настоящее описание подразумевает «комбинированную терапию», которая включает (но не ограничиваясь этим) совместное введение эффективного количества GLYX-13 и одного или более антагонистов NMDA-рецептора, как часть конкретной схемы лечения, предназначенной для обеспечения благоприятного эффекта от совместного действия данных терапевтических агентов. Благоприятный эффект комбинации включает, но не ограничиваясь этим, фармакокинетическое или фармакодинамическое совместное действие, возникающее вследствие комбинирования терапевтических агентов. Введение этих терапевтических агентов в комбинации, как правило, проводят в течение определенного периода времени (обычно дни, недели, месяцы или года в зависимости от выбранной комбинации). Предполагается, что комбинированная терапия включает введение большого количества терапевтических агентов последовательно, т.е. когда каждый терапевтический агент вводят в различное время, а также введение этих терапевтических агентов, или по меньшей мере двух из этих терапевтических агентов, практически одновременно. Практически одновременное введение может быть осуществлено, например, путем введения субъекту одной таблетки или капсулы с установленным соотношением терапевтических агентов или несколько капсул по одной для каждого из терапевтических агентов. Последовательное или практически одновременное введение каждого терапевтического агента можно осуществлять любым пригодным путем, в том числе, но не ограничиваясь ими, перорально, внутривенно, внутримышечно или путем прямой абсорбции через ткани слизистой оболочки. Терапевтические агенты можно вводить одним и тем же путем или различными путями. Например, первый терапевтический агент выбранной комбинации можно вводить путем внутривенной инъекции, тогда как другие терапевтические агенты комбинации можно вводить перорально. В альтернативном варианте, например, все терапевтические агенты можно вводить перорально или все терапевтические агенты можно вводить путем внутривенной инъекции.
[0078] Комбинированная терапия также может включать введение терапевтических агентов, как описано выше, в дополнительной комбинации с другими биологически активными ингредиентами и немедикаментозными способами лечения. Если комбинированная терапия дополнительно включает немедикаментозное лечение, оно может проводиться в любое подходящее время настолько долго, пока не будет достигнут благоприятный эффект от совместного действия комбинации терапевтических агентов и немедикаментозного лечения. Например, в соответствующих случаях благоприятный эффект все еще наблюдается, возможно дни или даже недели, когда временно не применяют немедикаментозное лечение, а только вводят терапевтические агенты.
[0079] В некоторых вариантах реализации изобретения один или более компонентов комбинаций, описанных в данном документе, можно вводить пациенту парентерально, в том числе, но не ограничиваясь этим, подкожно и внутривенно. В некоторых вариантах реализации изобретения один или более компонентов комбинаций, описанных в данном документе, можно также вводить путем медленной регулируемой внутривенной инфузии или путем высвобождения из имплантированного устройства. В некоторых вариантах реализации изобретения наблюдается значительное улучшение, например, когнитивных функций пациента, через 1 час, 2 часа, 4 часа, 8 часов, 12 часов, через 1 день, через 1 неделю, через 2 дня, через 3 дня, через 4 дня, через 5 дней, через 6 дней или даже через 8 дней после одной (единственной) дозы GLYX-13.
[0080] Терапевтически эффективное количество описанного соединения, необходимое для использования при лечении, зависит от природы аутистического расстройства, которое подвергают лечению, желательной продолжительности лечения, возраста и состояния пациента и в конечном итоге определяется лечащим врачом. Однако, как правило, дозы, применяемые при лечении взрослых людей, находятся в интервале от около 0,01 мг/кг до около 1000 мг/кг в сутки (например, от около 0,01 мг/кг до около 100 мг/кг в сутки, от около 0,01 мг/кг до около 10 мг/кг в сутки, от около 0,1 мг/кг до около 100 мг/кг в сутки, от около 0,1 мг/кг до около 50 мг/кг в сутки, от около 0,1 мг/кг до около 10 мг/кг в сутки) каждого компонента комбинаций, описанных в данном документе. В некоторых вариантах реализации изобретения дозы GLYX-13, применяемые при лечении взрослых людей, как правило, находятся в интервале от около 0,01 мг/кг до около 100 мг/кг в сутки (например, от около 0,01 мг/кг до около 10 мг/кг в сутки, от около 0,1 мг/кг до около 100 мг/кг в сутки, от около 0,1 мг/кг до около 50 мг/кг в сутки, от около 0,1 мг/кг до около 10 мг/кг в сутки, около 1 мг/кг в сутки). В некоторых вариантах реализации изобретения дозы антагониста NMDA-рецептора, применяемые при лечении взрослых людей, как правило, находятся в интервале от около 0,01 мг/кг до около 100 мг/кг в сутки (например, от около 0,1 мг/кг до около 100 мг/кг в сутки, от около 0,1 мг/кг до около 50 мг/кг в сутки, около 10 мг/кг в сутки или около 30 мг/кг в сутки). Требуемую дозу возможно вводить в виде однократной дозы, или в виде многократных доз, которые вводят через подходящие интервалы, например в виде двух, трех, четырех или более субдоз в сутки.
[0081] Ряд факторов может приводить к тому, что каждый компонент комбинаций, описанных в данном документе, вводят в широком интервале дозировок. При использовании в комбинации с другими терапевтическими агентами, дозировки соединений по настоящему изобретению могут быть относительно более низкими. В некоторых вариантах реализации изобретения дозировка GLYX-13 может составлять от около 1 нг/кг до около 100 мг/кг. Дозировка GLYX-13 может представлять собой любую дозировку, в том числе, но не ограничиваясь этим, около 1 мкг/кг, 25 мкг/кг, 50 мкг/кг, 75 мкг/кг, 100 мкг/кг, 125 мкг/кг, 150 мкг/кг, 175 мкг/кг, 200 мкг/кг, 225 мкг/кг, 250 мкг/кг, 275 мкг/кг, 300 мкг/кг, 325 мкг/кг, 350 мкг/кг, 375 мкг/кг, 400 мкг/кг, 425 мкг/кг, 450 мкг/кг, 475 мкг/кг, 500 мкг/кг, 525 мкг/кг, 550 мкг/кг, 575 мкг/кг, 600 мкг/кг, 625 мкг/кг, 650 мкг/кг, 675 мкг/кг, 700 мкг/кг, 725 мкг/кг, 750 мкг/кг, 775 мкг/кг, 800 мкг/кг, 825 мкг/кг, 850 мкг/кг, 875 мкг/кг, 900 мкг/кг, 925 мкг/кг, 950 мкг/кг, 975 мкг/кг, 1 мг/кг, 2,5 мг/кг, 5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг, 35 мг/кг, 40 мг/кг, 45 мг/кг, 50 мг/кг, 60 мг/кг, 70 мг/кг, 80 мг/кг, 90 мг/кг или 100 мг/кг.
[0082] В некоторых вариантах реализации описанное соединение, например GLYX-13, может быть введено в количестве, которое вызывает обратное развитие и предотвращает нарушение когнитивных функций.
[0083] Описанные соединения могут быть частью жидкого или твердого состава, например водных или масляных суспензий, растворов, эмульсий, сиропов и/или настоев. Композиции также могут быть составлены в виде сухого продукта для восстановления с помощью воды или другого пригодного носителя перед использованием. Такие жидкие препараты могут содержать добавки, в том числе, но не ограничиваясь ими, суспендирующие агенты, эмульгаторы, неводные носители и консерванты. Супендирующие агенты включают, но не ограничиваясь ими, сорбитовый сироп, метилцеллюлозу, сироп, содержащий глюкозу/сахар, желатин, гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу, гель стеарата алюминия и гидрогенизированные пищевые жиры. Эмульгаторы включают, но не ограничиваясь ими, лецитин, сорбитанмоноолеат и гуммиарабик. Неводные носители включают, но не ограничиваясь ими, пищевые масла, миндальное масло, фракционированное кокосовое масло, маслянистые сложные эфиры, пропиленгликоль и этиловый спирт.Консерванты включают, но не ограничиваясь ими, метил- или пропилгидроксибензоат и сорбиновую кислоту. Предусмотренные соединения также могут быть включены в состав для парентерального введения, в том числе, но не ограничиваясь этим, путем инъекции или непрерывной инфузии. Составы для инъекции могут быть в форме суспензий, растворов или эмульсий в масляных или водных носителях и могут содержать агенты для составов, в том числе, но не ограничиваясь ими, суспендирующие, стабилизирующие и диспергирующие агенты. Композиция также может быть получена в порошковой форме для восстановления с помощью пригодного носителя, в том числе, но не ограничиваясь ими, стерильной апирогенной воды (например, воды для инъекций).
[0084] В некоторых вариантах реализации изобретения описанные соединения, например GLYX-13, могут являться частью водной композиции, которая пригодна для внутривенной инъекции. В некоторых вариантах реализации изобретения такие композиции могут включать: (i) от 60 мг/мл до около 200 мг/мл (например, от около 125 мг/мл до около 175 мг/мл; например, около 150 мг/мл или около 75 мг/мл) фармацевтически активного соединения, имеющего формулу:
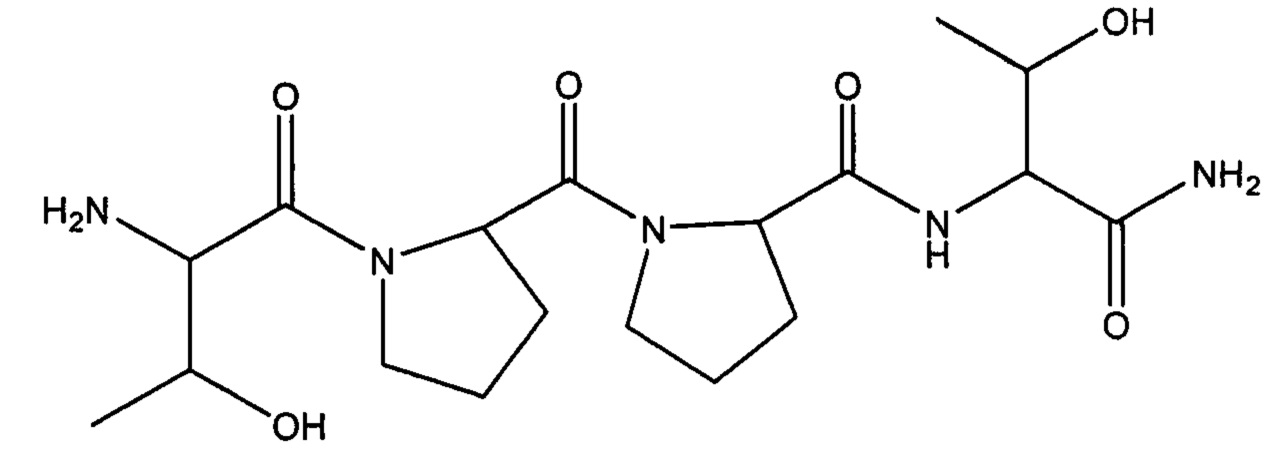 ; или его фармацевтически приемлемой соли; (ii) воду (например, воду для инъекций); и (iii) кислоту; причем стабильная водная композиция имеет рН от около 3,9 до около 5,5 (например, от около 4,0 до около 5,0, от около 4,2 до около 5,0, от около 4,1 до около 4,7, от около 4,2 до около 4,8, около 4,0, около 4,5) при 25°С. В некоторых вариантах реализации изобретения такие композиции могут быть помещены в емкость (например, предварительно заполненный шприц или флакон), из которой количество соединения извлекается в виде по меньшей мере одной однократной дозы. В некоторых вариантах реализации изобретения однократная доза может иметь объем от около 1 мл до около 4 мл (например, 3 мл).
; или его фармацевтически приемлемой соли; (ii) воду (например, воду для инъекций); и (iii) кислоту; причем стабильная водная композиция имеет рН от около 3,9 до около 5,5 (например, от около 4,0 до около 5,0, от около 4,2 до около 5,0, от около 4,1 до около 4,7, от около 4,2 до около 4,8, около 4,0, около 4,5) при 25°С. В некоторых вариантах реализации изобретения такие композиции могут быть помещены в емкость (например, предварительно заполненный шприц или флакон), из которой количество соединения извлекается в виде по меньшей мере одной однократной дозы. В некоторых вариантах реализации изобретения однократная доза может иметь объем от около 1 мл до около 4 мл (например, 3 мл).
[0085] В некоторых вариантах реализации изобретения композиции могут включать от около 200 мг до около 500 мг (например, около 450 мг; около 375; или около 225 мг) фармацевтически активного соединения.
[0086] В некоторых вариантах реализации изобретения кислота может выбрана из группы, состоящей из фумаровой кислоты, яблочной кислоты, молочной кислоты, хлористоводородной кислоты, бромистоводородной кислоты, уксусной кислоты, лимонной кислоты, фосфорной кислоты, азотной кислоты, серной кислоты и аскорбиновой кислоты. В некоторых вариантах реализации изобретения кислота предоставляет хлорид-ионы в водную композицию (например, хлористоводородная кислота).
[0087] В некоторых вариантах реализации изобретения при введении пациенту дозы водной жидкой композиции, которая содержит около 150 мг/мл фармацевтически активного соединения и имеет объем около 3 мл, у указанного пациента достигается физиологическая осмоляльность от около 800 мОсмоль/кг до около 900 мОсмоль/кг. В других вариантах реализации изобретения при введении пациенту дозы стабильной водной жидкой композиции, которая содержит около 75 мг/мл фармацевтически активного соединения и имеет объем около 3 мл, у указанного пациента достигается физиологическая осмоляльность от около 375 мОсмоль/кг до около 475 мОсмоль/кг.
[0088] ПРИМЕРЫ
[0089] Тест распознавания нового объекта («NOR») у мышей был основан на (Hashimoto К, Fujita Y, Shimizu Е, Iyo М (2005). Phencyclidine-induced cognitive deficits in mice are improved by subsequent subchronic administration of clozapine, but not haloperidol. European journal of pharmacology 519(1-2): 114-117). См. также, например, Rajagopal, et al., Current Pharmaceutical Design 2014, 20, 1. Ящик NOR представляет собой открытый ящик, изготовленный из органического стекла (длина 52 см; ширина 52 см; высота 31 см). Размеры ящика, который мы использовали для мышей, был идентичным тому, который использовали для крыс. Ящик располагали на высоте приблизительно 30 см над полом. Стенки ящика имели белый фон, в отличие от черного фона в исследованиях NOR с крысами. Мы обнаружили, что мыши C57BL/6 более активно изучают пространство на белом фоне по сравнению с черным. Три дня до теста мышей в течение часа приучали к пустому месту проведения теста NOR. Тест NOR у мышей проводят подобно ранее использованному NOR в исследовании с крысами за исключением того, что длительность исследований запоминания и удержания в памяти составляла 10 мин., с интервалом между исследованиями (ITI), составляющим 24 часа, в течение которого мыши находились в обычных клетках, тогда как в случае крыс исследования запоминания и удержания в памяти по длительности составляли три минуты, разделенные ITI, составляющим одну минуту (Horiguchi М, Meltzer HY (2012). The role of 5-HT1A receptors in phencyclidine (PCP)-induced novel object recognition (NOR) deficit in rats. Psychopharmacology 221(2): 205-215). Мы сравнили продолжительности исследований запоминания и удержания в памяти 3, 5 и 10 мин. и обнаружили, что продолжительность 10 минут являлась оптимальной для получения надежных данных. Затем оба исследования оценивали слепым методом.
[0090] Все данные выражали в виде среднего ± СОС. Данные изучения анализировали с помощью двухфакторного дисперсионного анализа (ANOVA). С его помощью обнаруживали основной эффект лечения лекарственным веществом, основной эффект задания и взаимодействие между лечением лекарственным веществом и изучением объекта. Когда был обнаружен значимый эффект, по полученным результатам проводили дополнительный анализ с использованием t-критерия Стьюдента для сравнения времени, затраченного на изучение нового и знакомого объектов. Первичной конечной точкой являлся индекс различения (DI). Значения DI (новый-знакомый/новый + знакомый) анализировали с использованием однофакторного ANOVA, а затем критерия Бонферрони, когда с помощью ANOVA обнаруживали значимый эффект.
[0091] Данные на фиг. 2 демонстрируют, что GLYX-13 (1 мг/кг внутривенно) вызывает обратное развитие хронического нарушения распознавания новых объектов у мышей, вызванного кетамином. Данные на фиг. 3 демонстрируют, что GLYX-13 (1 мг/кг внутривенно) вызывает обратное развитие хронического нарушения распознавания новых объектов у мышей, вызванного фенциклидином. Фиг. 4 демонстрирует значимое ослабление ответа при предварительном лечении с использованием 3 мг/кг и 30 мг/кг GLYX-13 в соматосенсорной коре с последующим введением кетамина. Данные на фиг. 5 демонстрируют, что предварительное лечение с использованием GLYX-13 (3 мг/кг внутривенно) вызывает обратное развитие острого нарушения распознавания новых объектов у мышей, вызванного кетамином (10 мг/кг подкожно). Данные на фиг. 6 демонстрируют, что GLYX-13 (3 мг/кг внутривенно) ингибирует стереотипию у крыс, вызванную кетамином (10 мг/кг внутривенно).
[0092] Специалисты в данной области техники обнаружат или способны установить с использованием не более чем обычного экспериментирования много эквивалентов конкретных вариантов реализации изобретения, описанных в данном документе. Подразумевается, что такие эквиваленты охвачены нижеприведенной формулой изобретения.
[0093] Содержания всех патентов, опубликованных патентных заявок, веб-сайтов и других источников, цитируемых в данном документе, явно включены в данный документ в полном объеме посредством ссылки.