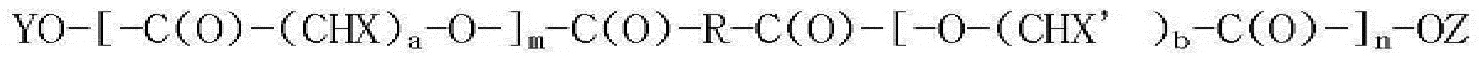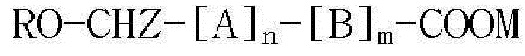Результат интеллектуальной деятельности: ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНИОННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ
Данное раскрытие относится к фармацевтической композиции, содержащей анионное лекарственное средство и доставляющей его и способу ее получения.
УРОВЕНЬ ТЕХНИКИ
Безопасные и эффективные технологии доставки лекарственного средства давно были изучены для лечения с использованием анионных лекарственных средств, особенно нуклеиновой кислоты, а также были разработаны различные системы доставки и технологии доставки. В частности, были разработаны технологии доставки с использованием вирусной системы доставки, используя аденовирус или ретровирус и т.д. и невирусной системы доставки, используя катионные липиды, катионные полимеры и т.д.
Однако технология, использующая вирусную систему доставки подвержена рискам, таким как неспецифическая иммунная реакция и т.д., и известно о наличии ряда проблем в коммерческом использовании из-за сложного производственного процесса. Поэтому недавние исследования развивались в направлении невирусной системы доставки с использованием катионных липидов или катионных полимеров для преодоления этих недостатков. Хотя невирусная система доставки менее эффективна, чем вирусная система доставки, она имеет меньше побочных эффектов и производство дешевле, чем у вирусной системы доставки.
Было проведено много исследований по невирусной системе доставки, используемой для доставки нуклеиновой кислоты, и наиболее представительные ее примеры включают комплекс катионного липида и нуклеиновой кислоты (липоплекс) и комплекс поликатионного полимера и нуклеиновой кислоты (полиплекс). Много исследований по катионным липидам или поликатионным полимерам было выполнено в связи с тем, что они стабилизируют анионные лекарственные средства путем образования комплекса посредством электростатических взаимодействий с анионным лекарственным средством и облегчают доставку в клетки (De Paula D, Bentley MV, Mahato RI, Hydrophobization and bioconjugation for enhanced siRNA delivery and targeting, RNA 13 (2007) 431-56; Gary DJ, Puri N, Won YY, Polymer-based siRNA delivery: Perspectives on the fundamental and phenomenological distinctions from polymer-based DNA delivery, J Control Release 121 (2007) 64-73).
Однако, если катионные липиды или поликатионные полимеры, исследованные к настоящему времени, используют в количестве, необходимом для получения достаточных эффектов, может произойти серьезная токсичность, хотя и меньше, чем при вирусной системе доставки, и, следовательно, она может быть непригодной для терапевтического использования. И хотя комплекс липид-нуклеиновая кислота, который образует комплекс через связь между катионным липидом и нуклеиновой кислотой для доставки нуклеиновой кислоты в клетки, широко используется в экспериментах с клеточной линией, он не образует структуру, которая может быть стабильной в крови, и, следовательно, он не может быть использован в живом организме (смотри US 6458382).
Кроме того, изучается система доставки с использованием нуклеиновой кислоты, непосредственно конъюгированной с липидом или полимером, но если липид или полимер непосредственно конъюгированы с нуклеиновой кислотой, существуют трудности с точки зрения эффективности конъюгации или контроля качества. Кроме того, эффективность доставки нуклеиновой кислоты еще не была четко подтверждена.
Следовательно, требуется разработать технологию доставки анионного лекарственого средства с использованием минимального количества катионного полимера или катионного липида для снижения токсичности, которое будет являться стабильным в крови и жидкости организма, и с обеспечением доставки в клетки с получением достаточных эффектов. Между тем были предприняты различные попытки использовать амфифильный блок-сополимер в качестве системы доставки лекарственного средства, который может солюбилизировать слабо водорастворимое лекарственное средство путем образования полимерной мицеллы и стабилизировать слабо водорастворимое лекарственное средство в водном растворе (международная публикация № WO 1997/010849). Этот амфифильный блок-сополимер может солюбилизировать гидрофобное слабо водорастворимое лекарственное средство путем образования полимерной мицеллы, имеющей гидрофобную внутреннюю часть. Однако, в связи с тем, что гидрофильное лекарственное средство, такое как анионная нуклеиновая кислота, не может быть включено в полимерную мицеллу, она не подходит для доставки анионного лекарственного средства, включающего нуклеиновую кислоту. Также существовало раскрытие композиции для доставки анионного лекарственного средства, которое образует комплекс нуклеиновой кислоты и катионного липида посредством электростатического взаимодействия для захвата комплекса в мицеллярную структуру амфифильного блок-сополимера. Однако необходимы улучшения в отношении стабильности нуклеиновой кислоты в крови и специфического нацеливания на раковые ткани.
В корейском патенте № 1296326 раскрыта композиция для доставки анионного лекарственного средства, содержащая анионное лекарственное средство; катионный липид; амфифильный блок-сополимер и полимолочную кислоту, где анионное лекарственное средство образует комплекс с катионным липидом, и комплекс захватывается в мицеллярную структуру амфифильного блок-сополимера и полимолочной кислоты. Однако, в связи с тем, что полимолочная кислота, используемая в этом патенте, представляет собой обычный полимер полимолочной кислоты, имеющий карбоксильную группу на конце, доставка лекарственного средства неэффективна.
Между тем, многие болезни являются результатом сверхэкспрессии генов заболеваний или экспрессии мутированных генов. Поскольку миРНК (малая интерферирующая РНК) ингибирует экспрессию специфических генов сиквенс-специфичным способом, ее выделяют как терапевтическое лекарственное средство на основе нуклеиновой кислоты. В частности, ожидается, что миРНК преодолеет проблемы антисмыслового нуклеотида или рибозима, поскольку миРНК обладает большей эффективностью и более точной селективностью по генам, чем антисмысловой нуклеотид или рибозим. миРНК представляет собой короткую двухцепочечную молекулу РНК и она ингибирует экспрессию соответствующих генов путем расщепления мРНК генов, имеющих комплементарную ей последовательность (McManus and Sharp, Nature Rev. Genet. 3:737 (2002), Elbashir, et al., Genes Dev. 15:188 (2001)).
Однако, несмотря на эти преимущества, известно, что миРНК быстро разрушается под действием нуклеазы в крови и быстро выводится из организма через почки. Также известно, что миРНК не может легко пройти клеточную мембрану, потому что она сильно отрицательно заряжена. Поэтому для использования миРНК в качестве терапевтического агента необходимо разработать систему доставки, которая может стабилизировать миРНК в крови, эффективно доставлять ее в клетки-мишени или ткани и еще не проявлять токсичности.
СОДЕРЖАНИЕ ИЗОБРЕТЕНИЯ
РЕШЕННЫЕ ПРОБЛЕМЫ
Для решения проблем, описанных выше, одной целью настоящего изобретения является предоставление композиции для доставки анионного лекарственного средства, содержащей мицеллярную структуру, содержащую соль полимолочной кислоты, для того чтобы эффективно доставлять анионные лекарственные средства в организм.
Другой целью настоящего изобретения является обеспечение применения композиции для доставки анионных лекарственных средств.
Еще одной целью настоящего изобретения является предоставление способа доставки анионных лекарственных средств, содержащего введение композиции.
Вместе с тем еще одной целью настоящего изобретения является предоставление способа получения фармацевтической композиции, способной эффективно доставлять анионные лекарственные средства в организм.
ТЕХНИЧЕСКИЕ СПОСОБЫ РЕШЕНИЯ ПРОБЛЕМ
Один вариант осуществления настоящего изобретения относится к композиции для доставки анионного лекарственного средства, содержащей мицеллярную структуру, содержащую соль полимолочной кислоты, для того чтобы эффективно доставлять анионные лекарственные средства в организм, применение композиции для доставки анионных лекарственных средств и способ доставки анионных лекарственных средств, содержащий введение композиции.
Композиция для доставки анионного лекарственного средства, содержащая мицеллярную структуру в соответствии с вариантом осуществления настоящего изобретения, содержит мицеллярную структуру амфифильного блок-сополимера и соли полимолочной кислоты, которая включает в себя комплекс лекарственного средства и катионного соединения. В частности, композиция содержит анионное лекарственное средство в качестве активного ингредиента; катионное соединение; амфифильный блок-сополимер; и соль полимолочной кислоты, где анионное лекарственное средство образует комплекс с катионным соединением посредством электростатического взаимодействия, и комплекс заключается (захватывается) в мицеллярную структуру амфифильного блок-сополимера и соли полимолочной кислоты.
Композиция является водорастворимой и содержит соль полимолочной кислоты в качестве компонента мицеллярной структуры. Поэтому в случае введения в организм композиция повышает стабильность в крови, и ее можно эффективно доставить на целевой участок, особенно в раковую ткань, избегая ретикулоэндотелиальной системы (РЭС). Следовательно, композиция была бы полезна для избегания РЭС и/или улучшения направленного действия.
В качестве другого варианта осуществления настоящего изобретения способ получения композиции для доставки анионного лекарственного средства может содержать (а) растворение анионного лекарственного средства, катионного соединения, амфифильного блок-сополимера и соли полимолочной кислоты в способном к смешению с водой органическом растворителе или смешанном растворителе из водного раствора и органического растворителя; (b) удаление слоя органического растворителя со стадии (а); и (c) добавление водного раствора к смеси со стадии (b), где органический растворитель удаляют, с образованием мицелл.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
Фармацевтическая композиция для доставки анионного лекарственного средства в соответствии с вариантом осуществления настоящего изобретения способна улучшить стабильность анионного лекарственного средства в крови или жидкости организма путем изолирования анионного лекарственного средства от внешней среды с использованием катионного соединения и мицеллярной структуры, состоящей из амфифильного блок-сополимера и соли полимолочной кислоты. Поэтому фармацевтическая композиция способна улучшить стабильность анионного лекарственного средства в крови или жидкости организма при введении в организм. Особенно фармацевтическая композиция помогает анионному лекарственному средству избежать ретикулоэндотелиальной системы (РЭС), для того чтобы эффективно доставляться в клетки.
КРАТКОЕ РАЗЪЯСНЕНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 представлена схематическая структура системы доставки на основе полимерной мицеллы, в которую анионное лекарственное средство и катионное соединение заключены в соответствии с вариантом осуществления настоящего изобретения.
На фиг. 2 представлен результат ЯМР измерения PLANa, полученной в соответствии с примером получения 8.
СПОСОБЫ ИЗОБРЕТЕНИЯ
В дальнейшем настоящее изобретение будет разъяснено подробно.
Среди компонентов композиции варианта осуществления настоящего изобретения анионное лекарственное средство и катионное соединение заключается (захватываются) в мицеллярную структуру амфифильного блок-сополимера и соли полимолочной кислоты. Схематическая структура полимерной мицеллярной системы, в которую заключается (захватываются) аннионное лекарственное средство и катионное соединение, показана на фиг. 1. Ссылаясь на фиг. 1, комплекс анионного лекарственного средства и катионного соединения образуется посредством электростатического взаимодействия между анионным лекарственным средством и катионным соединением. Образованный комплекс анионного лекарственного средства и катионного соединения заключается (захватывается) в мицеллярную структуру амфифильного блок-сополимера и соли полимолочной кислоты.
Как показано на фиг. 1, мицеллярная структура образуется из амфифильного блок-сополимера и соли полимолочной кислоты. В водной окружающей среде гидрофильная часть амфифильного блок-сополимера образует внешнюю стенку мицеллы, а гидрофобная часть амфифильного блок-сополимера и соль полимолочной кислоты, независимый ингредиент, образуют внутреннюю стенку мицеллы. Анионное лекарственное средство и катионное соединение захватываются внутрь сформированной мицеллы. Комплекс анионного лекарственного средства и катионного соединения захватывается в мицеллярную структуру, образованную из амфифильного блок-сополимера и соли полимолочной кислоты, так что он может иметь улучшенную стабильность в крови или жидкости организма. Согласно одному варианту осуществления размер частиц мицеллы может составлять от 10 до 200 нм, предпочтительно от 10 до 150 нм. Кроме того, стандартный заряд мицеллярной частицы может составлять от -20 до 20 мВ, предпочтительно от -10 до 10 мВ. Размер частиц и стандартный заряд определяются с учетом стабильности мицеллярной структуры, содержания составляющих ингредиентов, абсорбции анионных лекарственных средств организме и удобства стерилизации в качестве фармацевтической композиции.
Анионное лекарственное средство в качестве активного ингредиента в композиции варианта осуществления настоящего изобретения может включать в себя любой материал, который отрицательно заряжен в водном растворе и обладает фармакологической активностью. В соответствии с одним вариантом осуществления анионное свойство может быть обеспечено, по меньшей мере, одной функциональной группой, выбранной из групп, состоящих из карбоксильной группы, фосфатной группы и сульфатной группы. В соответствии с одним вариантом осуществления анионное лекарственное средство может быть мультианионным лекарственным средством, таким как пептид, белок или гепарин, или нуклеиновая кислота.
Кроме того, нуклеиновая кислота может быть дезоксирибонуклеиновой кислотой рибонуклеиновой кислотой или лекарственным средством на основе нуклеиновой кислоты, в которой каркас, сахар или основание химически модифицирован или конец модифицирован. Более конкретными примерами могут быть нуклеиновая кислота, выбранная из группы, состоящей из РНК, ДНК, миРНК, аптамера, антисмыслового ОДН (олигодезоксинуклеотида), антисмысловой РНК, рибозима и ДНКзима и т.д. И каркас, сахар или основание нуклеиновой кислоты могут быть химически модифицированными или конец может быть модифицирован с целью повышения стабильности в крови или ослабления иммунных реакций и тому подобного. В особенности, часть сложной фосфодиэфирной связи нуклеиновой кислоты может быть замещена фосфоротиоатной или боранофосфатной связью, или 2'-ОН-позиции части рибозных оснований могут включать в себя, по меньшей мере, один вид модифицированного нуклеотида, в который вводят различные функциональные группы, такие как метильная группа, метоксиэтильная группа, фтор и тому подобное.
Кроме того, по меньшей мере, один конец нуклеиновой кислоты может быть модифицирован одним или более выбранными из группы, состоящей из холестерина, токоферола и C10-24 жирной кислоты. В случае миРНК, например, 5' или 3' конец, или оба конца смысловой и/или антисмысловой цепи могут быть модифицированы, и предпочтительно конец смысловой цепи может быть модифицирован.
Холестерин, токоферол и C10-24 жирная кислота могут включать в себя их аналоги, производные и метаболиты.
миРНК относится к двухцепочечной РНК или одноцепочечной РНК, имеющей двухцепочечную форму в одноцепочечной РНК, которая может уменьшать или ингибировать экспрессию гена-мишени, опосредуя деградацию мРНК, комплементарной к последовательности миРНК, если миРНК существует в той же самой клетке, что и ген-мишень. Связь между двойными цепями осуществляется посредством водородной связи между нуклеотидами, не все нуклеотиды в двойных цепях должны быть комплиментарно связаны с соответствующими нуклеотидами, а обе нити могут быть разделены или не могут быть разделены. В соответствии с одним вариантом осуществления длина миРНК может составлять примерно от 15 до 60 нуклеотидов (означающее число нуклеотидов одной двухцепочечной РНК, то есть число пар оснований, а в случае одноцепочечной РНК это означает длину двойных нитей в одноцепочечной РНК), в частности примерно от 15 до 30 нуклеотидов и более в особенности примерно от 19 до 25 нуклеотидов.
В соответствии с одним вариантом осуществления двухцепочечная миРНК может иметь ʺвыступʺ из 1-5 нуклеотидов на одном или обоих 3' или 5' концах. В соответствии с другим вариантом осуществления она может быть ʺтупой без выступаʺ на обоих концах. В частности, она может быть миРНК, раскрытой в патентной публикации США № 2002/0086356 или в патенте США № 7056704 (включенном в настоящее описание в виде ссылок).
Кроме того, миРНК может иметь симметричную структуру с одинаковой длиной двух нитей или может иметь несимметричную структуру с одной нитью короче другой. В частности, она может быть несимметричной молекулой миРНК двойных нитей, состоящая из 19-21 нуклеотидов (nt) антисмысловой области; и от 15 до 19 nt (нуклеотидов) смысловой области, имеющей последовательность, комплементарную антисмысловой области, где 5' конец антисмысловой области является тупым концом, а 3' конец антисмысловой области имеет выступ из 1-5 нуклеотидов. В частности, она может быть миРНК, раскрытой в международной публикации № WO 09/078685.
Анионное лекарственное средство варианта осуществления настоящего изобретения предпочтительно включено в состав в количестве от 0,001 до 10 масс.%, в особенности от 0,01 до 5 масс.% из расчета на общую массу композиции. Если содержание составляет менее 0,001 масс.% количество системы доставки слишком велико по сравнению с лекарственным средством, и, таким образом, системой доставки могут быть вызваны побочные эффекты. Если оно превышает 10 масс.%, стабильность мицеллы может быть снижена, а скорость потерь при стерилизации фильтрованием может быть увеличена, поскольку мицелла слишком велика.
В соответствии с одним вариантом осуществления катионное соединение образует комплекс с анионным лекарственным средством посредством электростатических взаимодействий, и комплекс заключается (захватывается) в мицеллярной структуре амфифильного блок-сополимера. Поэтому катионное соединение может включать в себя любой тип соединения, способного образовывать комплекс с анионным лекарственным средством посредством электростатического взаимодействия и, например, может включать в себя липиды и полимеры. Катионный липид может включать в себя N,N-диолеил-N,N-диметиламмонийхлорид (DODAC), N,N-дистеарил-N,N-диметиламмонийбромид (DDAB), N-(1-(2,3-диолеилокси)пропил-N,N,N-триметиламмонийхлорид (DOTAP), N,N-диметил-(2,3-диолеилокси)пропиламин (DODMA), N,N,N-триметил-(2,3-диолеоилокси)пропиламин (DOTMA), 1,2-диацил-3-триметиламмонийпропан (TAP), 1,2-диацил-3-диметиламмонийпропан (DAP), 3β-[N-(N',N',N'-триметиламиноэтан)карбамоил]холестерин (TC-холестерин), 3β-[N-(N',N'-диметиламиноэтан)карбамоил]холестерин (DC-холестерин), 3β-[N-(N'-монометиламиноэтан)карбамоил] холестерин (MC-холестерин), 3β-[N-(аминоэтан)карбамоил]холестерин (AC-холестерин), холестериноксипропан-1-амин (COPA), N-(N'-аминоэтан)карбамоилпропановый токоферол (AC-токоферол), N-(N'-метиламиноэтан) карбамоилпропановый токоферол (MC-токоферол) или их комбинацию. Если используют такой катионный липид, для того чтобы снизить токсичность, вызванную катионным липидом, может быть предпочтительным использование менее поликатионного липида с высокой плотностью заряда, а более в особенности, только одна функциональная группа способная проявлять положительный заряд в водном растворе может быть введена в молекулу. Поэтому в предпочтительном варианте осуществления катионный липид может быть, по меньшей мере, одним, выбранным из группы, состоящей из 3β-[N-(N',N',N'-триметиламиноэтан)карбамоил]холестерина (TC-холестерина), 3β-[N-(N',N'-диметиламиноэтан)карбамоил]холестерина (DC-холестерина), 3β-[N-(N'-монометиламиноэтан)карбамоил]холестерина (MC-холестерина), 3β-[N-(аминоэтан)карбамоил]холестерина (AC-холестерина), N-(1-(2,3-диолеилокси)пропил-N,N,N-триметиламмонийхлорида (DOTAP), N,N-диметил-(2,3-диолеилокси)пропиламина (DODMA) и N,N,N-триметил-(2,3-диолеилокси)пропиламина (DOTMA). С другой стороны катионный полимер может быть выбран из группы, состоящей из хитозана, гликолевого хитозана, протамина, полилизина, полиаргинина, полиамидоамина (PAMAM), полиэтиленимина, декстрана, гиалуроновой кислоты, альбумина, полимерного полиэтиленимина (PEI), полиамина и поливиниламина (PVAm) и предпочтительно может быть, по меньшей мере, одним, выбранным из полимерного полиэтиленимина (PEI), полиамина и поливиниламина (PVА).
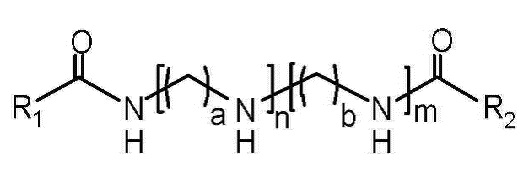
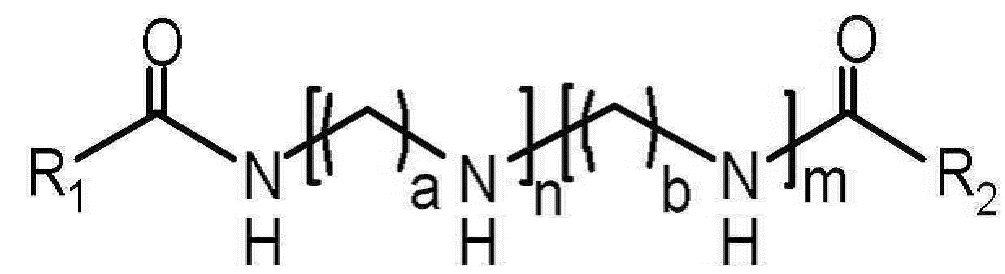
В одном варианте осуществления катионный липид может быть представлен следующей формулой 7:
[Формула 7]
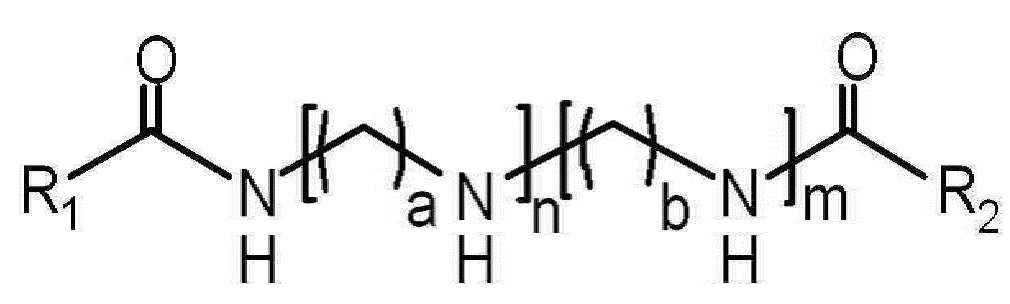
где каждый из n и m составляет от 0 до 12, при условии, что 2≤n + m≤12, каждый из a и b составляет от 1 до 6, и каждый из R1 и R2 независимо выбран из группы, состоящей из насыщенных и ненасыщенных C11-25 углеводородов. Предпочтительно n и m могут быть независимо друг от друга от 1 до 9 и 2≤n + m≤10. Предпочтительно a и b составляют от 2 до 4.
Предпочтительно R1 и R2 независимо выбран из группы, состоящей из лаурила, миристила, пальмитила, стеарила, арахидила, бегенила, лигноцерила, керотила, миристолеила, пальмитолеила, сапиенила, олеила, линолеила, арахидонила, эйкозапентаенила, эруцила, докозагексаенила и керотила.
Конкретными примерами катионного липида может быть, по меньшей мере, один, выбранный из группы, состоящей из 1,6-диолеоилтриэтилентетрамида, 1,8-дилинолеоилтетраэтиленпентамида, 1,4-димиристолеоилдиэтилентриамида, 1,10-дистеароилпентаэтиленгексамида и 1,10-диолеоилпентаэтиленгексамида.
Катионное соединение, используемое в варианте осуществления настоящего изобретения, может быть включено в состав в количестве от 0,01 до 50 масс.% и в особенности от 0,1 до 10 масс.% из расчета на общую массу композиции. Если содержание составляет менее 0,01 масс.%, его может быть недостаточным для образования комплекса с анионным лекарственным средством. Если оно превышает 50 масс.%, мицелла может быть слишком большой и, таким образом, стабильность мицеллы может быть снижена, а скорость потерь при стерилизации фильтрованием может быть увеличена.
Катионное соединение связывается с анионным лекарственным средством посредством электростатических взаимодействий, для того чтобы образовать комплекс. В соответствии с одним вариантом осуществления соотношение количеств электрического заряда катионного соединения (N) и анионного лекарственного средства (P) (N/P: соотношение положительного электрического заряда катионного соединения к отрицательному электрическому заряду анионного лекарственного средства) составляет от 0,1 до 128, в особенности от 0,5 до 64, более в особенности от 1 до 32, более в особенности от 1 до 24 и наиболее в особенности от 6 до 24. Если соотношение (N/P) менее 0,1, может быть трудным образовать комплекс, включающий достаточное количество анионного лекарственного средства. С другой стороны, если соотношение (N/P) превышает 128, может быть вызвана токсичность.
В соответствии с одним вариантом осуществления амфифильный блок-сополимер может представлять собой блок-сополимер типа А-В, включающий гидрофильный блок А и гидрофобный блок В. Блок-сополимер типа A-B образует полимерную мицеллу типа ядро-оболочка в водном растворе, где гидрофобный блок B образует ядро (внутреннюю стенку), а гидрофильный блок А образует оболочку (внешнюю стенку).
В этом отношении гидрофильный блок А может быть, по меньшей мере, одним, выбранным из группы, состоящей из полиалкиленгликоля, поливинилового спирта, поливинилпирролидона, полиакриламида и их производных. Гидрофильный блок А может быть, по меньшей мере, одним, выбранным из группы, состоящей из монометоксиполиэтиленгликоля, моноацетоксиполиэтиленгликоля, полиэтиленгликоля, сополимера полиэтилена и пропиленгликоля и поливинилпирролидона. Гидрофильный блок А может иметь среднечисленную молекулярную массу от 200 до 50000 дальтон, в особенности от 1000 до 20000 дальтон и более в особенности от 1000 до 5000 дальтон.
Если необходимо, функциональная группа или лиганд, которые могут связываться с определенной тканью или клеткой, или функциональная группа, способная ускорять внутриклеточную доставку, могут быть химически конъюгированы с концом гидрофильного блока А, для того чтобы контролировать распределение системы доставки на основе полимерной мицеллы, которая образуется из амфифильного блок-сополимера и соли полимолочной кислоты в организме, или для повышения эффективности доставки системы доставки на основе мицеллы в клетки. Функциональная группа или лиганд может быть, по меньшей мере, одной(им), выбранной(ым) из группы, состоящей из моносахарида, полисахарида, витаминов, пептидов, белков и антитела к рецептору клеточной поверхности. В более конкретных примерах функциональная группа или лиганд может быть, по меньшей мере, одной(им), выбранной(ым) из группы, состоящей из анисамида, витамина B9 (фолиевой кислоты), витамина B12, витамина A, галактозы, лактозы, маннозы, гиалуроновой кислоты, RGD-пептида, NGR-пептида, трансферрина, антитела к рецептору трансферрина и т.д.
Гидрофобный блок В представляет собой биосовместимый и биоразлагаемый полимер, и он может быть, по меньшей мере, одним, выбранным из группы, состоящей из сложного полиэфира, полиангидрида, полиаминокислоты, сложного полиортоэфира и полифосфазина. Более конкретные их примеры могут включать в себя полилактид, полигликолид, поликапролактон, полидиоксан-2-он, сополимер полилактида и гликолида, сополимер полилактида и полидиоксан-2-она, сополимер полилактида и поликапролактона и сополимер полигликолида и поликапролактона. В соответствии с другим вариантом осуществления гидрофобный блок B может иметь среднечисленную молекулярную массу от 50 до 50000 дальтон, в особенности от 200 до 20000 дальтон и более в особенности от 1000 до 5000 дальтон. И для увеличения гидрофобности гидрофобного блока, для улучшения стабильности мицеллы, токоферол, холестерин или C10-24 жирная кислота могут быть химически конъюгированы с гидроксильной группой на конце гидрофобного блока.
Амфифильный блок-сополимер, содержащий гидрофильный блок (А) и гидрофобный блок (В), может быть включен в состав в количестве от 40 до 99,98 масс.%, в особенности от 85 до 99,8 масс.%, и более в особенности от 90 до 99,8 масс.%, из расчета на общую сухую массу частицы. Если содержание амфифильного блок-сополимера составляет менее 40 масс.%, мицелла может стать настолько большой, что стабильность мицеллы может быть снижена, а потеря во время стерилизации фильтрованием может быть увеличена. Если оно превышает 99,98 масс.%, содержание анионного лекарственного средства, которое может быть включено в состав, может стать слишком маленьким.
В соответствии с другим вариантом осуществления амфифильный блок-сополимер может включать в себя от 40 до 70 масс.% гидрофильного блока (А) и в особенности от 50 до 60 масс.% гидрофильного блока (А) из расчета на массу сополимера. Если соотношение гидрофильного блока (А) составляет менее 40 масс.%, растворимость полимера в воде является низкой и, таким образом, может быть трудым образовать мицеллу. Поэтому соотношение гидрофильного блока (А) предпочтительно составляет не менее 40 масс.%, для того чтобы обеспечить достаточную растворимость в воде для сополимера с образованием мицеллы. Если оно превышает 70 масс.%, гидрофильность может быть слишком высокой и, таким образом, стабильность полимерной мицеллы может стать слишком низкой, и может быть сложным солюбилизировать комплекс анионного лекарственного средства и катионного липида. Поэтому в свете стабильности мицеллы соотношение гидрофильного блока (А) предпочтительно составляет не более 70 масс.%.
В соответствии с одним вариантом осуществления амфифильный блок-сополимер позволяет заключить комплекс анионного лекарственного средства и катионного липида в мицеллярной структуре в водном растворе, где соотношение массы комплекса анионного лекарственного средства и катионного липида (a) к массе амфифильного блок-сополимера (b) [a/b * 100; (масса анионного лекарственного средства+масса катионного липида)/массу амфифильного блоксополимера * 100] может составлять от 0,001 до 100 масс.%, в особенности от 0,01 до 50 масс.% и более в особенности от 0,1 до 10 масс.%. Если массовое соотношение составляет менее 0,001 масс.%, содержание комплекса анионного лекарственного средства и катионного липида может стать слишком низким и, таким образом, может быть трудым обеспечить достаточное содержание анионного лекарственного средства. Если оно превышает 100 масс.%, мицеллярная структура соответствующего размера может не образовываться с учетом молекулярной массы амфифильного блок-сополимера и количества комплекса анионного лекарственного средства и липида.
Мицеллярная структура в композиции в соответствии с вариантом осуществления настоящего изобретения содержит соль полимолочной кислоты (например, PLANa). Соль полимолочной кислоты распределяется по ядру (внутренней стенке) мицеллы, для того чтобы повысить гидрофобность ядра и стабилизировать мицеллу и в то же время помочь избежать ретикулоэндотелиальной системы (РЭС) в организме. То есть анион карбоновой кислоты в соли полимолочной кислоты эффективно связывается с катионным комплексом, для того чтобы уменьшить поверхностный заряд полимерной мицеллы. Таким образом, положительный заряд поверхностного потенциала полимерной мицеллы будет меньше, чем у полимерной мицеллы, которая не содержит соль полимолочной кислоты, и таким образом она может быть менее захвачена ретикулоэндотелиальной системой и эффективно доставлена в целевые участки (например, раковые клетки, воспалительные клетки и т.д.).
Соль полимолочной кислоты, которая является независимым компонентом из амфифильного блок-сополимера, является компонентом внутренней стенки мицеллы и может иметь среднечисленную молекулярную массу от 500 до 50000 дальтон и в особенности от 1000 до 50000 дальтон. Если среднечисленная молекулярная масса составляет менее 500 дальтон, соли полимолочной кислоты не легко продолжать находиться в ядре (внутренней стенке) мицеллы, потому что гидрофобность слишком низкая. Если среднечисленная молекулярная масса превышает 50000 дальтон, полимерная мицелла может быть слишком большой.
Соль полимолочной кислоты может быть использована в количестве от 10 до 200 массовых частей, в особенности от 10 до 100 массовых частей и более в особенности от 30 до 60 массовых частей на 100 массовых частей амфифильного блок-сополимера. Если содержание соли полимолочной кислоты превышает 200 массовых частей на 100 массовых частей амфифильного блок-сополимера, размер мицеллы может быть слишком большим и, таким образом, стерилизованная мембранная фильтрация становится затруднительной. Если содержание соли полимолочной кислоты составляет менее 1 массовой части на 100 масовых частей амфифильного блок-сополимера, трудно получить желаемый эффект.
В соответствии с одним вариантом осуществления композиция варианта осуществления настоящего изобретения может содержать от 10 до 1000 массовых частей амфифильного блок-сополимера и от 5 до 500 массовых частей соли полимолочной кислоты на 1 массовую часть анионного лекарственного средства. Предпочтительно амфифильный блок-сополимер может составлять от 50 до 800 массовых частей и более предпочтительно от 100 до 500 массовых частей. Предпочтительно соль полимолочной кислоты может составлять от 10 до 300 массовых частей и более предпочтительно от 50 до 100 массовых частей.
В соответствии с одним вариантом осуществления конец соли полимолочной кислоты, противоположный концу, где образуется соль, может быть замещен одним, выбранным из группы, состоящей из гидроксила, ацетокси, бензоилокси, деканоилокси, пальмитоилокси и C1-2 алкокси.
В соответствии с одним предпочтительным вариантом осуществления соль полимолочной кислоты может быть выбрана из группы, состоящей из формул 1-6, как представлено ниже.
[Формула 1]
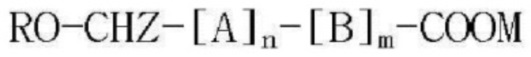
где A представляет собой -COO-CHZ-; B представляет собой -COO-CHY-, -COO-CH2CH2CH2CH2CH2- или -COO-CH2CH2OCH2; R представляет собой атом водорода или ацетил, бензоил, деканоил, пальмитоил, метил или этил; каждый из Z и Y представляет собой атом водорода или метил, или фенил; M представляет собой Na, K или Li; n является целым числом от 1 до 30; и m является целым числом от 0 до 20;
[Формула 2]
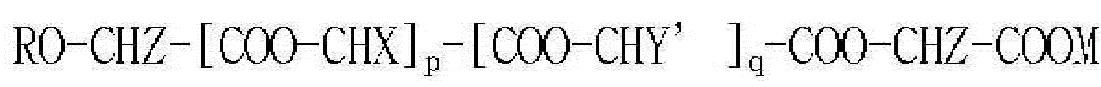
где X представляет собой метил; Y' представляет собой атом водорода или фенил; p является целым числом от 0 до 25, q является целым числом от 0 до 25, при условии, что p+q является целым числом от 5 до 25; R представляет собой атом водорода или ацетил, бензоил, деканоил, пальмитоил, метил или этил; M представляет собой Na, K или Li; и Z представляет собой атом водорода, метил или фенил;
[Формула 3]
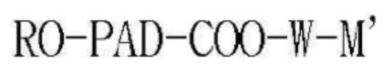
где W-M' представляет собой 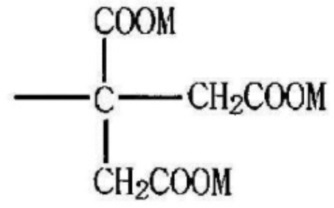 или
или 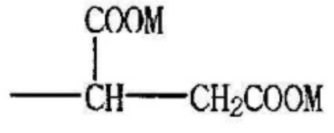 ; PAD выбран из группы, состоящей из D,L-полилактида, D-полилактида, полиминдальной кислоты, сополимера D,L-лактида и гликолевой кислоты, сополимера D,L-лактида и миндальной кислоты, сополимера D,L-лактида и капролактона и сополимера D,L-лактида и 1,4-диоксан-2-она; R представляет собой атом водорода или ацетил, бензоил, деканоил, пальмитоил, метил или этил; и M независимо представляет собой Na, K или Li;
; PAD выбран из группы, состоящей из D,L-полилактида, D-полилактида, полиминдальной кислоты, сополимера D,L-лактида и гликолевой кислоты, сополимера D,L-лактида и миндальной кислоты, сополимера D,L-лактида и капролактона и сополимера D,L-лактида и 1,4-диоксан-2-она; R представляет собой атом водорода или ацетил, бензоил, деканоил, пальмитоил, метил или этил; и M независимо представляет собой Na, K или Li;
[Формула 4]
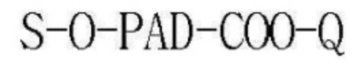
где S представляет собой 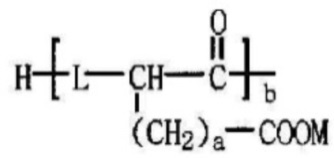 ; L представляет собой -NR1- или -О-, где R1 представляет собой атом водорода или C1-10 алкил; Q представляет собой CH3, CH2CH3, CH2CH2CH3, CH2CH2CH2CH3 или CH2C6H5; a является целым числом от 0 до 4; b является целым числом от 1 до 10; M представляет собой Na, K или Li; и PAD является, по меньшей мере, одним, выбранным из группы, состоящей из D,L-полилактида, D-полилактида, полиминдальной кислоты, сополимера D,L-лактида и гликолевой кислоты, сополимера D,L-лактида и миндальной кислоты, сополимера D,L-лактида и капролактона и сополимера D,L-лактида и 1,4-диоксан-2-она;
; L представляет собой -NR1- или -О-, где R1 представляет собой атом водорода или C1-10 алкил; Q представляет собой CH3, CH2CH3, CH2CH2CH3, CH2CH2CH2CH3 или CH2C6H5; a является целым числом от 0 до 4; b является целым числом от 1 до 10; M представляет собой Na, K или Li; и PAD является, по меньшей мере, одним, выбранным из группы, состоящей из D,L-полилактида, D-полилактида, полиминдальной кислоты, сополимера D,L-лактида и гликолевой кислоты, сополимера D,L-лактида и миндальной кислоты, сополимера D,L-лактида и капролактона и сополимера D,L-лактида и 1,4-диоксан-2-она;
[Формула 5]
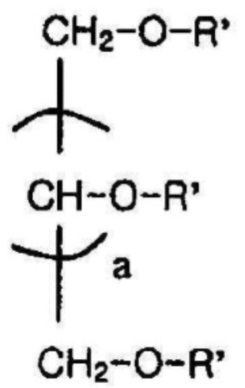 или
или 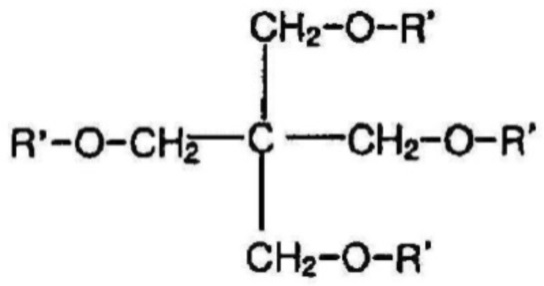
где R' представляет собой -PAD-O-C(O)-CH2CH2-C(O)-OM, где PAD выбран из группы, состоящей из D,L-полилактида, D-полилактида, полиминдальной кислоты, сополимера D,L-лактида и гликолевой кислоты, сополимера D,L-лактида и миндальной кислоты, сополимера D,L-лактида и капролактона и сополимера D,L-лактида и 1,4-диоксан-2-она, M представляет собой Na, K или Li; и a является целым числом от 1 до 4; и
[Формула 6]
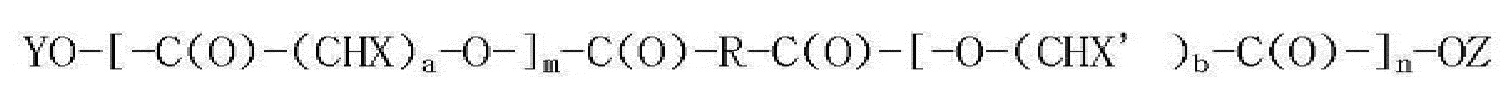
где X и X' независимо представляют собой водород, C1-10 алкил или C6-20 арил; Y и Z независимо представляют собой Na, K или Li; m и n независимо являются целыми числами от 0 до 95, при условии, что 5 < m+n < 100; a и b независимо являются целыми числами от 1 до 6; и R представляет собой -(CH2)k-, C2-10 двухвалентный алкенил, C6-20 двухвалентный арил или их комбинацию, где k представляет собой целое число от 0 до 10.
Соль полимолочной кислоты предпочтительно представляет собой соединение формулы 1 или формулы 2.
В одном варианте осуществления настоящего изобретения композиция может дополнительно содержать фузогенный липид в количестве от 0,01 до 50 масс.% и в особенности от 0,1 до 10 масс.% из расчета на общую массу композиции для повышения эффективности доставки анионного лекарственного средства в клетки.
Фузогенный липид образует комплекс анионного лекарственного средства, катионного липида и фузогенного липида посредством электростатического взаимодействия, когда он смешивается с комплексом анионного лекарственного средства и катионного липида. Комплекс, содержащий фузогенный липид, заключается (захватывается) в мицеллярную структуру амфифильного блок-сополимера. В одном варианте осуществления фузогенный липид может быть выбран из группы, состоящей из фосфолипида, холестерина, токоферола и их комбинаций.
В частности, фосфолипид может быть, по меньшей мере, одним, выбранным из группы, состоящей из фосфатидилэтаноламина (PE), фосфатидилхолина (PC) и фосфатидной кислоты. Фосфатидилэтаноламин (PE), фосфатидилхолин (PC) и фосфатидная кислота могут быть в форме, объединенной с одной или двумя С10-24 жирными кислотами. Холестерин и токоферол могут включать в себя аналоги, производные и метаболиты каждого из холестерина и токоферола.
В частности, фузогенный липид может быть выбран из группы, состоящей из дилауроилфосфатидилэтаноламина, димиристоилфосфатидилэтаноламина, дипальмитоилфосфатидилэтаноламина, дистеароилфосфатидилэтаноламина, диолеоилфосфатидилэтаноламина, дилинолеоилфосфатидилэтаноламина, 1-пальмитоил-2-олеоилфосфатидилэтаноламина, 1,2-дифитаноил-3-sn-фосфатидилэтаноламина, дилауроилфосфатидилхолина, димиристоилфосфатидилхолина, дипальмитоилфосфатидилхолина, дистеароилфосфатидилхолина, диолеоилфосфатидилхолина, дилинолеоилфосфатидилхолина, 1-пальмитоил-2-олеоилфосфатидилхолина, 1,2-дифитаноил-3-sn-фосфатидилхолина, дилауроилфосфатидной кислоты, димиристоилфосфатидной кислоты, дипальмитоилфосфатидной кислоты, дистеароилфосфатидной кислоты, диолеоилфосфатидной кислоты, дилинолеоилфосфатидной кислоты, 1-пальмитоил-2-олеоилфосфатидной кислоты, 1,2-дифитаноил-3-sn-фосфатидной кислоты, холестерина, токоферола и их комбинации.
В соответствии с одним предпочтительным вариантом осуществления фузогенный липид может быть, по меньшей мере, одним, выбранным из группы, состоящей из диолеоилфосфатидилэтаноламина (DOPE), 1,2-дипальмитолеоил-sn-глицеро-3-фосфохолина (DPPC), 1,2-диолеоил-sn-глицеро-3-фосфохолина (DOPC) и 1,2-дипальмитолеоил-sn-глицеро-3-фосфоэтаноламина (DPPE) и т.д.
В соответствии с одним вариантом осуществления настоящего изобретения композиция, которая содержит комплекс анионное лекарственное средство-катионное соединение, захваченный в мицеллярную структуру амфифильного блок-сополимера и соли полимолочной кислоты, может быть введена по пути кровеносного сосуда, в мышцу, подкожно, перорально, костную, трансдермальную или локальную ткань и тому подобное, и ее можно приготовить в различных рецептурах для перорального или парентерального введения. Примеры рецептуры для перорального введения могут включать в себя таблетки, капсулы, порошок и жидкость, а примеры рецептуры для парентерального введения могут включать в себя глазные капли и инъекцию. В соответствии с одним предпочтительным вариантом осуществления композиция может представлять собой рецептуру для инъекции. Например, если соединение лиофилизировано, оно может быть восстановлено дистиллированной водой для инъекции, 0,9%-ным физиологическим раствором, 5%-ным водным раствором декстрозы и тому подобным, чтобы разработать рецептуру для инъекции.
Другой вариант осуществления настоящего изобретения предлагает способ получения фармацевтической композиции, содержащей амфифильную блок-сополимерную мицеллу, содержащую анионное лекарственное средство.
В соответствии с одним вариантом осуществления способ получения композиции для доставки анионного лекарственного средства, содержащая анионное лекарственное средство, катионный липид, амфифильный блок-сополимер и соль полимолочной кислоты, может содержать:
(а) растворение анионного лекарственного средства, катионного соединения, амфифильного блок-сополимера и соли полимолочной кислоты в способном к смешению с водой органическом растворителе или смешанном растворителе из водного раствора и органического растворителя;
(b) удаление слоя органического растворителя из смеси со стадии (а); и
(c) добавление водного раствора к смеси со стадии (b), где органический растворитель удаляют с образованием мицелл.
В частности, на стадии (а) анионное лекарственное средство, катионное соединение, амфифильный блок-сополимер и соль полимолочной кислоты смешивают в способном к смешению с водой органическом растворителе или смешанном растворителе из водного раствора и органического растворителя, для того чтобы образовать комплекс. В частности, способный к смешению с водой органический растворитель может быть, по меньшей мере, одним, выбранным из группы, состоящей из ацетона, этанола, метанола и уксусной кислоты, а органический растворитель в смешанном растворителе может быть, по меньшей мере, одним, выбранным из группы, состоящей из этилацетата, ацетонитрила, метиленхлорида, хлороформа и диоксана. Водным раствором может быть дистиллированная вода, вода для инъекции или буфер. Смешанное соотношение органического растворителя и водного раствора в смешанном растворителе не может быть особо ограничено. Например, исходя из объема, соотношение органического растворителя и водного раствора в смешанном растворителе может составлять от 1:0,1 до 50 и более в особенности от 1:0,5 до 10 (объем органического растворителя:объем водного раствора), но к тому же оно не может быть ограничено.
На стадии (b) органический растворитель можно удалить из смеси, полученной на стадии (а) выпариванием.
Оставшуюся смесь растворяют в водном растворе на стадии (с) после того, как органический растворитель, выпаривают, в результате чего комплекс анионного лекарственного средства и катионного соединения захватывается в мицеллярную структуру амфифильного блок-сополимера и соли полимолочной кислоты. Вид и количество водного раствора описаны выше.
В соответствии с другим вариантом осуществления способ может дополнительно содержать стадию (d) для лиофилизации путем добавления вспомогательного средства для лиофилизации после стадии (с).
В соответствии с другим вариантом осуществления способ получения может дополнительно содержать способ стерилизации раствора полимерной мицеллы со стадии (с) с использованием стерильного фильтра перед лиофилизацией на стадии (d).
Вспомогательное средство для лиофилизации, используемое в варианте осуществления настоящего изобретения, добавляют, для того чтобы помочь лиофилизированной композиции поддерживать форму сгустка или помочь композиции расплавиться быстро и равномерно во время процесса восстановления после лиофилизации композиции амфифильного блок-сополимера. В частности, вспомогательное средство для лиофилизации может быть, по меньшей мере, одним, выбранным из группы, состоящей из лактозы, маннита, сорбита и сахарозы. Количество вспомогательного средства для лиофилизации может составлять от 1 до 90 масс.% и более в особенности от 10 до 60 масс.% из расчета на общую сухую массу лиофилизированной композиции.
В соответствии со способом варианта осуществления настоящего изобретения готовят композицию, в которой комплекс анионного лекарственного средства и катионного соединения захватывается в мицеллярную структуру амфифильного блок-сополимера и соли полимолочной кислоты. В частности, мицеллярная частица в полученной композиции стабильна в крови и имеет размер частиц от 10 до 200 нм и в особенности от 10 до 150 нм.
ПОДРОБНОЕ ОПИСАНИЕ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В дальнейшем настоящее изобретение будет подробно объяснено со ссылкой на следующие примеры. Однако эти примеры предназначены только для иллюстрации изобретения и его объем не ограничивается ими каким-либо образом.
[Пример получения 1] Синтез 1,6-диолеоилтриэтилентетрамида
Указанное в заголовке соединение синтезировали и идентифицировали в соответствии с процедурой, описанной в примере 1 международной публикации № WO 2012-091523.
[Примеры получения 2 и 3] Полимеризация блок-сополимера mPEG-PLA (монометоксиэтиленгликоль-полилактид) (A-B)
mPEG-PLA, имеющего среднечисленную молекулярную массу 5000-4000 дальтон синтезировали в соответствии с процедурой, описанной в примере получения 1 международной публикации № WO 2012-091523 [пример получения 2].
Блок-сополимер mPEG-PLA, имеющего среднечисленную молекулярную массу 2000-1750 дальтон синтезировали в соответствии с тем же способом с использованием монометоксиполиэтиленгликоля (молекулярной массой 2000 дальтон или менее, NOF corporation) [Пример получения 3].
[Примеры получения 4 и 5] Полимеризация mPEG-PLA-токоферола
mPEG-PLA-токоферол (среднечисленной молекулярной массой 5000-4000-530 дальтон) получали в соответствии с процедурой, описанной в примере получения 2 международной публикации № WO 2012-091523 [пример получения 4].
mPEG-PLA-токоферол, имеющего среднечисленную молекулярную массу 2000-1750-530 дальтон получали в соответствии с тем же способом [пример получения 5].
[Примеры получения 6 и 7] Синтез полимолочной кислоты (PLA)
PLA (среднечисленной молекулярной массой 1700 дальтон) получали в соответствии с процедурой, описанной в примере получения 8 корейского патента № 1296326 и выход составлял 87% [пример получения 6].
PLA, имеющую среднечисленную молекулярную массу 4000 дальтон получали путем взаимодействия в течение 24 часов в соответствии с тем же способом. Очищенную PLA подтверждали с помощью 1H-ЯМР, и выход составлял 85% [пример получения 7].
[Примеры получения 8 и 9] Синтез натриевой соли D,L-полимолочной кислоты (PLANa)
150 мл Ацетонитрила добавляли к 100 г полимолочной кислоты (среднечисленной молекулярной массой 1700), полученной из примера получения 6 для растворения полимолочной кислоты. К ним медленно добавляли 150 мл водного бикарбоната натрия (0,1 г/мл) и смесь перемешивали при 60°C в течение 2 часов при 100 об/мин. К ним добавляли 15 г хлорида натрия при комнатной температуре и перемешивали, чтобы расплавить, а слой водного раствора удаляли с использованием делительной воронки.
100 мл дистиллированной воды и 10 г хлорида натрия добавляли к оставшемуся слою органического растворителя и перемешивали, чтобы расплавить. Слой органического растворителя собирали с использованием делительной воронки. Органический растворитель и дистиллированную воду полностью удаляли путем фракционной перегонки полученного слоя органического растворителя при 80°C в течение 2 часов в условиях вакуума.
После этого к ним добавляли 150 мл безводного ацетона для растворения полимера, а нерастворенный осадок удаляли фильтрованием. Ацетон удаляли фракционной перегонкой при 80°С в течение 2 часов в условиях вакуума. В результате получали 69 г очищенной натриевой соли полимолочной кислоты. Очищенную натриевую соль полимолочной кислоты идентифицировали с помощью ЯМР (пример получения 8).
Натриевую соль полимолочной кислоты получали из полимолочной кислоты (среднечисленной молекулярной массой 4000), полученной из примера получения 7 (пример получения 9).
[Сравнительный пример 1] Получение полимерной мицеллы, содержащей миРНК/1,6-диолеоилтриэтилентетрамид (dioTETA)/mPEG-PLA-токоферол (2k-1,7k)
1,89 мг 1,6-dio-ТЕТА (соотношение N/P: 18) растворяли в 94,63 мкл хлороформа и 100 мкг миРНК растворяли в 80 мкл дистиллированной воды. 60 мг mPEG-PLA-токоферола (2k-1,7k) растворяли в 200 мкл хлороформа. Добавляли 505,37 мкл хлороформа до тех пор, пока объемное соотношение органического слоя к водному слою не достигло 10. миРНК добавляли по каплям к смеси раствора, в которой 1,6-dioТЕТА и mPEG-PLA-токоферол растворяли в хлороформе, и смесь превращали в эмульсию с использованием соникатора. Эмульсию добавляли по каплям к 2320 мкл дистиллированной воды и превращали в сложную эмульсию с использованием соникатора. Полученную сложную эмульсию помещали в 1-горлую круглую колбу и перегоняли при пониженном давлении в роторном испарителе для селективного удаления хлороформа, для того чтобы получить полимерные мицеллы, содержащие миРНК/1,6-диолеоилтриэтилентетрамид (dioTETA)/mPEG-PLA-токоферол (2k-1,7k) (смотри таблицу 1).
Таблица 1
|
(Соотношение выражается в порядке количества миРНК в мкг, соотношении N/P и количества полимера в мг. То же самое будет применено к таблицам ниже).
[Сравнительный пример 2] Получение полимерной мицеллы, содержащей миРНК/1,6-диолеоилтриэтилентетрамид (dioTETA)/mPEG-PLA-токоферол (2k-1,7k)/PLA (1,7k)
2,52 мг 1,6-dioТЕТА (соотношение N/P: 16) растворяли в 126,18 мкл хлороформа и 150 мкг миРНК растворяли в 120 мкл дистиллированной воды. 9 мг PLA-COOH (1,7k) растворяли в 180 мкл хлороформа и 30 мг mPEG-PLA-токоферола (2k-1,7k) растворяли в 100 мкл хлороформа. Добавляли 813,82 мкл хлороформа до тех пор, пока объемное соотношение органического слоя к водному слою не достигло 10. 1,564 мкл хлороформа добавляли к 20 мкл раствора хлороформа, в котором растворяли 30 мг mPEG-PLA-токоферола, что соответствовало 6 мг mPEG-PLA-токоферола (20 масс.%) и смесь помещали в 1-горлую круглую колбу. После этого растворитель удаляли перегонкой при пониженном давлении в роторном испарителе.
Раствор dioTETA, раствор PLA и раствор 24 мг mPEG-PLA-токоферола смешивали и к ним по каплям добавляли водный раствор миРНК, для того чтобы получить эмульсию с использованием соникатора. Эмульсию помещали в 1-горлую круглую колбу с 6 мг mPEG-PLA-токоферола, и растворитель удаляли дистилляцией при пониженном давлении в роторном испарителе. Полимерные мицеллы, содержащие миРНК/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLA, получали путем добавления 3 мл дистиллированной воды в колбу и растворения посредством осторожного встряхивания колбы (смотри таблицу 2).
Таблица 2
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLA)
[Примеры 1 и 2] Получение композиции, содержащей миРНК/1,6-диолеоилтриэтилентетрамид (dioTETA)/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)
2,52 мг 1,6-dioТЕТА растворяли в 126,18 мкл хлороформа и 150 мкг миРНК растворяли в 120 мкл дистиллированной воды. 9 мг PLANa (1,7k) растворяли в 180 мкл хлороформа и 30 мг mPEG-PLA-токоферола (2k-1,7k) растворяли в 100 мкл хлороформа. Добавляли 813,82 мкл хлороформа до тех пор, пока объемное соотношение органического слоя к водному слою не достигло 10. 1,564 мкл хлороформа добавляли к 20 мкл раствора 30 мг mPEG-PLA-токоферола в хлороформе, что соответствовало 6 мг mPEG-PLA-токоферола (20 масс.%) и смесь помещали в 1-горлую круглую колбу. После этого растворитель удаляли перегонкой при пониженном давлении в роторном испарителе.
Раствор dioTETA, раствор PLANa и раствор 24 мг mPEG-PLA-токоферола смешивали и к ним по каплям добавляли водный раствор миРНК, для того чтобы получить эмульсию с использованием соникатора. Эмульсию помещали в 1-горлую круглую колбу с 6 мг mPEG-PLA-токоферола, и растворитель удаляли перегонкой при пониженном давлении в роторном испарителе.
Композицию, содержащую миРНК/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa получали добавлением 3 мл дистиллированной воды в колбу и растворением, посредством осторожного встряхивания колбы. Полимерная мицелла 2 была приготовлена таким же образом, как описано выше, с использованием различных количеств dioTETA и PLANa.
Таблица 3
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLANa)
[Примеры 3-6] Получение композиции, содержащей миРНК/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)
Композиции 3-6, содержащие миРНК/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k) получали таким же образом, как в примере 1, с использованием различных количеств dioТЕТА или mPEG-PLA-токоферола (2k-1,7k).
Композиции, полученные в примерах 3-6, перечислены в таблице 4 ниже:
Таблица 4
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLANa)
[Примеры 7 и 8] Получение композиции, содержащей миРНК/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)
Композиции 7 и 8, содержащие миРНК/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k) получали таким же образом, как в примере 1, используя различные количества PLANa (1,7k) (смотри таблицу 5).
Таблица 5
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLANa)
[Экспериментальный пример 1] Сравнение размера частиц и поверхностного заряда мицеллы миРНК/dioTETA/mPEG-PLA-токоферола (2k-1,7k)/PLANa (1,7k) в зависимости от изменения соотношения композиции
Для подтверждения образования наночастиц в зависимости от соотношения миРНК/dioTETA (соотношение N/P), количества амфифильного блок-сополимера (2k-1,7k) и количества PLANa (1,7k) измеряли размер и поверхностный заряд мицелл. Размер частиц измеряли с помощью ДРС (динамическое рассеяние света). В частности, в качестве источника света использовали He-Ne-лазер и Zetasizer Nano ZS90 (MALVERN) эксплуатировали в соответствии с инструкцией производителя.
Размер и поверхностный заряд мицелл из примеров 1-4, имеющих различные соотношения N/P приведены в таблице 6 ниже:
Таблица 6
|
Размер и поверхностный заряд мицелл из примеров 1, 5 и 6, имеющих различные количества амфифильного блок-сополимера (2k-1,7k) приведены в таблице 7 ниже:
Таблица 7
Изменения количества mPEG-PLA-токоферола (2k-1,7k)
|
Размер и поверхностный заряд мицелл из примеров 1, 7 и 8, имеющих различное количество PLANa (1,7k), приведены в таблице 8 ниже:
Таблица 8
Изменение количества PLA-COONa (1,7k)
|
[Примеры 9-11] Получение композиции, содержащей миРНК/dioTETA/mPEG-PLA-токоферол/PLANa
Полимерные мицеллы 9, 10 и 11 получали таким же образом, как в примере 1, за исключением того, что вместо mPEG-PLA-токоферола (2k-1,7k) использовали mPEG-PLA-токоферол (5k-4k) или вместо PLANa (1,7k) использовали PLANa (4k).
Таблица 9
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLANa)
[Экспериментальный пример 2] Сравнение размера частиц и поверхностного заряда миацеллы миРНК/dioTETA/mPEG-PLA-токоферола/PLANa в соответствии с изменением композиции и соотношения композиции
Размер и поверхностный заряд мицелл из примеров 1, 9, 10 и 11 измеряли таким же образом, как в экспериментальном примере 1 для подтверждения образования наночастиц в зависимости от молекулярной массы амфифильного блок-сополимера и PLA-COONa. Результаты представлены в таблице 10 ниже:
Таблица 10
|
[Пример 12] Получение композиции, содержащей миРНК-холестерин/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)
Композицию, содержащую миРНК-холестерин/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k) получали таким же образом, как в примере 1, используя миРНК-холестерин. Растворитель удаляли из смеси перегонкой при пониженном давлении в роторном испарителе. Композицию получили добавлением 3 мл дистиллированной воды в колбу и растворением, посредством осторожного встряхивания колбы.
[Пример 13] Получение композиции, содержащей миРНК-PEG/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)
Композицию, содержащую миРНК-PEG/dioTETA/mPEG-PLA-токоферол (2k-1,7k) /PLANa (1,7k) получали таким же образом, как в примере 1, используя миРНК-PEG. Растворитель удаляли из смеси перегонкой при пониженном давлении в роторном испарителе. Композицию получили добавлением 3 мл дистиллированной воды в колбу и растворением, посредством осторожного встряхивания колбы.
Композиции, полученные в примерах 12 и 13, приведены в таблице 11 ниже:
Таблица 11
|
(Полимер 1: mPEG-PLA-токоферол, Полимер 2: PLANa)
[Пример 14] Получение композиции, содержащей миРНК/bPEI/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)
0,3 мг bPEI растворяли в 15 мкл дистиллированной воды и 150 мкг миРНК растворяли в 120 мкл дистиллированной воды. Водный раствор bPEI и водный раствор миРНК смешивали в 105 мкл водного раствора HBS (10 мМ HEPES, 1 мМ NaCl). 9 мг PLANa (1,7k) растворяли в 180 мкл хлороформа и 30 мг mPEG-PLA-токоферола (2k-1,7k) растворяли в 100 мкл хлороформа. Добавляли 2,140 мкл хлороформа до тех пор, пока объемное соотношение органического слоя к водному слою не достигло 10. 1,564 мкл хлороформа добавляли к 20 мкл раствора 30 мг mPEG-PLA-токоферола в хлороформе, что соответствовало 6 мг mPEG-PLA-токоферола (20 масс.%) и их помещали в 1-горлую круглую колбу. После этого растворитель удаляли перегонкой при пониженном давлении в роторном испарителе.
Раствор PLANa и раствор 24 мг mPEG-PLA-токоферола смешивали и к ним по каплям добавляли водный раствор HBS, содержащий bPEI и миРНК, для того чтобы получить эмульсию с использованием соникатора. Эмульсию помещали в 1-горлую круглую колбу с 6 мг mPEG-PLA-токоферола, и растворитель удаляли перегонкой при пониженном давлении в роторном испарителе. Композицию, содержащую миРНК/bPEI/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k) получали добавлением 6 мл дистиллированной воды в колбу и растворением посредством осторожного встряхивания колбы (смотри таблицу 12).
Таблица 12
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLANa)
[Примеры 15 и 16]. Получение композиции, содержащей миРНК/катионный липид/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)
Композицию 9, содержащую миРНК/1,10-диолеоилпентаэтиленгексамид (dioPEHA)/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k) и композицию 10, содержащую миРНК/1,8-дилинолеоилтетраэтиленпентамид (dilTEPA)/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k) получали таким же образом, как в примере 1, с использованием другого катионного липида (смотри таблицу 13).
Таблица 13
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLANa)
[Примеры 17 и 18]. Получение композиции, содержащей миРНК-PEG/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)/DOPE (диолеоилфосфатидилэтаноламин)
Композицию, содержащую миРНК-PEG/dioTETA/mPEG-PLA-токоферол (2k-1,7k)/PLANa (1,7k)/DOPE, получали таким же образом, как в примере 1, используя миРНК-PEG. DOPE использовали в том же количестве как, или в четыре раза больше, чем dioTETA. Растворитель удаляли из смеси перегонкой при пониженном давлении в роторном испарителе. Композицию получали добавлением 3 мл дистиллированной воды в колбу и растворением посредством осторожного встряхивания колбы (таблица 14).
Таблица 14
|
(Полимер 1: mPEG-PLA-токоферол, полимер 2: PLANa)
[Экспериментальный пример 3]. Сравнение размера и поверхностного заряда мицелл миРНК/катионный материал/амфифильный блок-сополимер/PLANa(/DOPE)
Размер и поверхностный заряд мицелл измеряли таким же образом, как в экспериментальном примере 1 для подтверждения образования наночастиц в зависимости от видов миРНК и катионного материала и присутствия PLANa или DOPE. Результаты представлены в таблице 15 ниже:
Таблица 15
|
[Экспериментальный пример 4]. Анализ концентрации в крови мицелл миРНК/катионный материал/амфифильный блок-сополимер/PLANa
Рецептуру, полученную в экспериментальном примере 1, вводили животным, и образцы крови собирали через 0,5 и 6 часов после введения. Концентрацию в крови мицелл анализировали с помощью RT (обратная транскрипция) и qRT-PCR (количественная ПЦР с детекцией в реальном времени), как показано ниже.
Рецептуру вводили внутривенно в мышь Balb/c в количестве 1 мг/кг и кровь собирали через 0,5 и 6 часов, соответственно. Кровь центрифугировали при 13000 об/мин, при 4°С в течение 15 минут и супернатант собирали в новую пробирку. В общей сложности приготовили 11 концентраций в диапазоне от 4 мкМ до 0,00256 мкМ в PBS для стандартных рецептур. 1 мкл разбавленной стандартной рецептуры добавляли на 96-луночную планшету для ПЦР и добавляли 9 мкл сыворотки мыши Balb/c и 90 мкл 0,25%-ного triton X-100. После добавления 90 мкл 0,25%-ного Triton X-100 к 10 мкл экспериментального образца крови проводили этап предварительной обработки для высвобождения системы доставки. После того, как рецептура была высвобождена, выделенная миРНК была синтезирована как кДНК через RT (обратная транскрипция), и qRT-PCR (Bio-Rad CFX96 в системе реального времени) была выполнена с использованием синтезированной кДНК.
Анализ осуществляли с использованием программного обеспечения Bio-Rad CFX Manager.
Таблица 16
|
Как можно видеть в таблице 16, через 0,5 часа концентрация в крови рецептур, полученных в примерах 1 и 2, была в 5-8 раз выше, чем в сравнительных примерах 1 и 2. Таким образом, стабильность рецептуры варианта осуществления настоящего изобретения в крови была подтверждена как превосходная.
[Экспериментальный пример 5] Распределение in vivo мицеллы миРНК/катионный материал/амфифильный блок-сополимер/PLANa в ткани
Определяли количество полимерной мицеллы миРНК/dioTETA/mPEG-PLA-токоферол/ PLANa в ткани печени и раковой ткани в организме.
Клеточную линию рака яичника человека A2780cis вводили подкожно в голую мышь Balb/c для получения мышей, зараженных раком. Рецептуру вводили внутривенно в дозе 1 мг/кг один раз в два дня, всего четырежды. Через 24 часа после последнего введения ткань печени и раковую ткань экстрагировали и взвешивали по 200 мг каждую, затем помещали в 1,8 мл 0,25%-ного Triton Х-100 и измельчали гомогенизатором ткани. Для стандартного образца ткани вводили физиологический раствор и ткани измельчали таким же образом. В общей сложности приготовили 11 концентраций в диапазоне от 4 мкМ до 0,00256 мкМ в PBS для стандартных рецептур. На 96-луночный планшет для ПЦР добавляли 99 мкл измельченной стандартной ткани и 1 мкл разбавленной стандартной рецептуры. Образцы тканей, подлежащие анализу, добавляли в количестве 100 мкл и проводили стадию предварительной обработки для высвобождения рецептур. Выделенная миРНК была синтезирована как кДНК через RT (обратная транскрипция), и qRT-PCR (Bio-Rad CFX96 в системе реального времени) была выполнена с использованием синтезированной кДНК. Анализ осуществляли с использованием программного обеспечения Bio-Rad CFX Manager.
Результаты анализа представлены в таблице 17 ниже.
Таблица 17
|
Как показано в таблице 17, в примере 2 в соответствии с вариантом осуществления настоящего изобретения распределение полимерной мицеллы было снижено в ткани печени, но увеличилось в раковой ткани по сравнению со сравнительным примером 1. Эти результаты подтверждают, что полимерная мицелла, содержащая PLANa варианта осуществления настоящего изобретения способна в особенности нацеливаться на раковую ткань.
[Экспериментальный пример 6]. Активность in vivo мицеллы миРНК/катионный материал/амфифильный блок-сополимер/PLANa (способность к репрессии гена)
Активность in vivo полимерных мицелл миРНК/dioTETA/mPEG-PLA-токоферол/PLANa определяли путем измерения репрессии генов.
В голую мышь Balb/c трансплантировали секции рака легкого A549 человека с получением мыши, зараженной раком. Рецептуры вводили внутривенно в дозе 0,5 мг/кг один раз в два дня, всего трижды. Для контроля вводили физиологический раствор. Каждую рецептуру вводили пяти (5) мышам. Через 24 часа после последнего введения раковые ткани экстрагировали и изначально измельчали с использованием ступки в присутствии жидкого азота. После этого ткани снова измельчали с использованием гомогенизатора QIAGEN (TissueLyser). 10 мг раковой ткани, которую дважды измельчили, обрабатывали 600 мкл приготовленного рабочего гомогенизирующего раствора (гомогенизирующий раствор 600 мкл+протеиназа К (23 мг/мл) 6 мкл), чтобы выделить HPRT мРНК из клеток. После приготовления образцов, как указано выше, их анализировали с использованием набора для анализа на основе разветвленной ДНК в соответствии с инструкцией изготовителя (метод анализа для Panomics bDNA).
Также был проанализирован GAPDH мРНК, ген, который не подвержен воздействию HPRT миРНК. Средние значения относительной экспрессии HPRT миРНК в раковых тканях рассчитывали путем коррекции измеренного количества HPRT мРНК. Результаты анализа представлены в таблице 18 ниже.
Таблица 18
|
Как показано в таблице 18, пример 2 в соответствии с вариантом осуществления настоящего изобретения ингибировал in vivo экспрессию мРНК гена-мишени HPRT на 54% при раке.