Результат интеллектуальной деятельности: РАДИОСЕНСИБИЛИЗИРУЮЩЕЕ СРЕДСТВО
Вид РИД
Изобретение
Изобретение относится к области медицины, в частности онкологии, а именно к веществам, обладающим радиосенсибилизирующей активностью, и, например, может быть использовано для лучевой терапии в комплексном лечении онкозаболеваний.
Современная лучевая терапия предполагает применение субмаксимальных доз облучения, избирательное облучение опухоли при минимальном воздействии на окружающие нормальные ткани. Однако снижение доз уменьшает эффективность, а повышение суммарных доз для улучшения эффекта сопровождается повышенным риском осложнений. Одним из подходов к повышению эффективности и снижению побочных эффектов при лучевой терапии является повышение радиочувствительности опухолей. Это достигается применением радиосенсибилизаторов, то есть усилителей биологического действия ионизирующего излучения.
Известно радиосенсибилизирующее вещество для лечения онкологических заболеваний [RU 2166945 C1, МПК (2000.01) A61K31/52, A61K9/20, A61K9/22, A61P35/00, опубл. 20.05.2001], содержащее 8-бромкофеин и растворитель. В качестве растворителя использован полиоксиэтиленсорбитан монолеат, или полиоксиэтиленсорбитан стеарат, или полиоксиэтиленсорбитан монолаурат, или полиоксиэтиленсорбитан монопальмитат, или полиоксиэтиленсорбитан моностеарат, или полиоксиэтиленсорбитан тристеарат. При этом оно дополнительно содержит метилцеллюлозу, стеарат кальция или магния и крахмал при следующем соотношении ингредиентов, мас. %:
|
Исходный 8-бромкофеин плохо растворяется в воде и биологических средах организма.
Известно использование оксиглицина лития для повышения радиосенсибилизации тканей животных [RU 2498799 C2, МПК (2006.01) A61K31/205, A61P43/00, опубл. 20.11.2013]. Для этого животному перед радиоактивным облучением парентерально вводят литиевую соль оксиглицина в дозах от 40 до 120 мг на 1 кг живой массы тела.
Данное соединение растворимо в воде и умеренно-токсично (ЛД50 > 1000 мг/кг).
Известно применение проксифеина в качестве радиосенсибилизирующего средства для комбинированного лечения онкологических заболеваний [SU 1826184 A1, МПК (1998.06) A61K31/52, A61P35/00, опубл. 1998.06.27].
Техническим результатом предложенного изобретения является расширение арсенала радиосенсибилизирующих средств.
Технический результат достигается применением аскорбата лития с формулой LiC6H7O6 по новому назначению в качестве радиосенсибилизирующего средства.
Аскорбат лития является водорастворимым и малотоксичным соединением со средней летальной дозой LD50>4000 мг/кг.
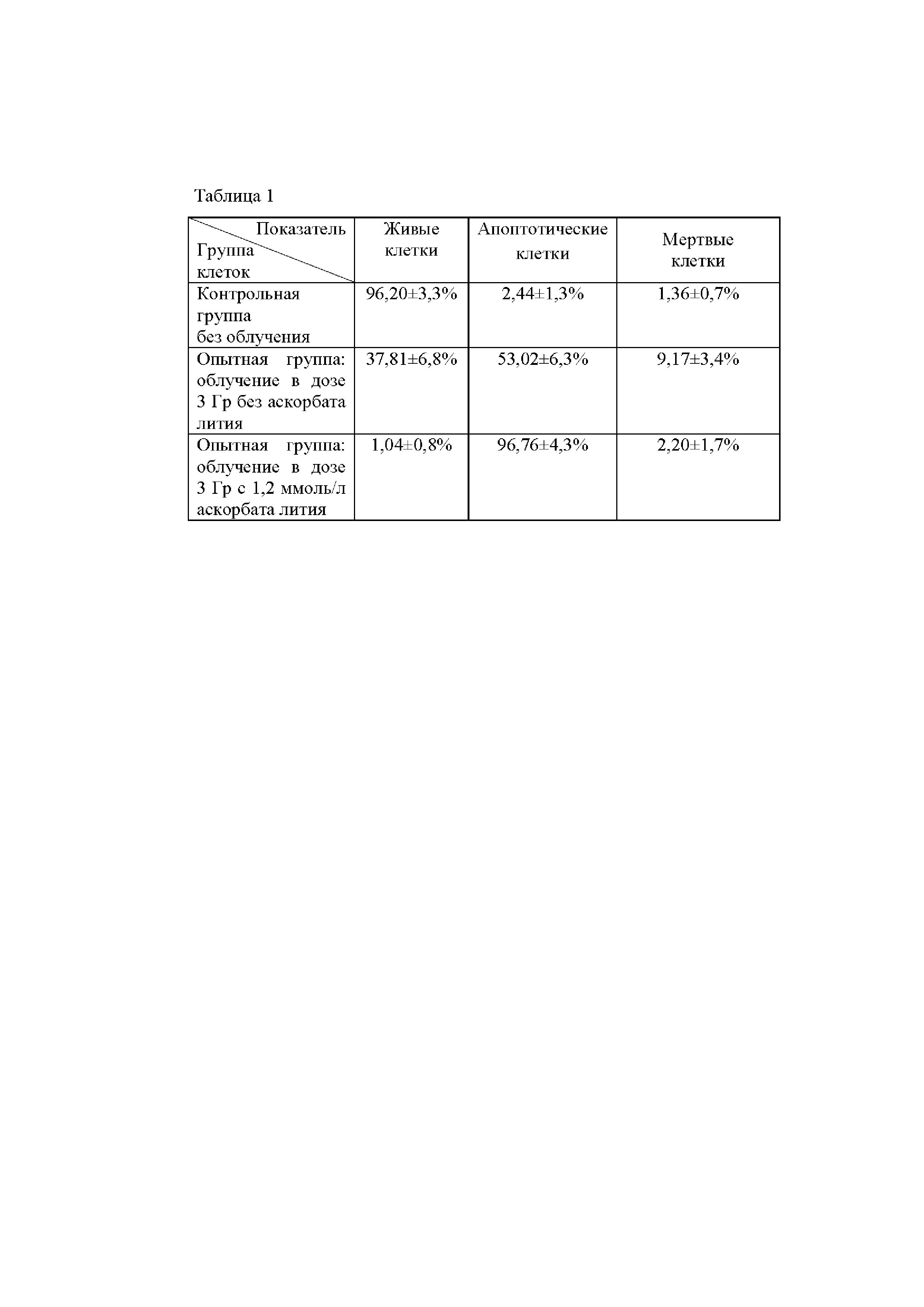
В таблице 1 представлены результаты оценки радиосенсибилизирующих свойств аскорбата лития.
Исследование радиосенсибилизирующих свойств аскорбата лития оценивали до и после лучевого воздействия по уровню жизнеспособности опухолевой клеточной культуры.
Готовили рабочий раствор препарата, для чего растворили 52,3 мг аскорбата лития в 5 мл физиологического раствора. В качестве тестовой клеточной линии использовали культуру клеток Jurkat (суспензионная опухолевая линия Т-лимфобластной лейкемии человека) в среде RPMI 1640, с добавлением 10% эмбриональной телячьей сыворотки и антибиотиков (пенициллин-стрептомицин). Суспензию клеток в концентрации 500 тыс. кл/мл разливали в стерильные пробирки Эппендорфа (1,5 мл) по 975 мкл. Далее добавляли 25 мкл раствора аскорбата лития в физиологическом растворе, получая конечную концентрацию препарата в среде 1,2 ммоль/л, что соответствует установленной терапевтической концентрации лития. В контрольные образцы вносили 25 мкл физиологического раствора. Клетки выдерживали 60 минут в СО2 инкубаторе при 37°С в среде 5% углекислого газа. Далее проводили облучение на рентгеновской установке с интенсивностью 20 мГр/сек в суммарной дозе 3 Гр. После чего клетки переносили в 96-луночный планшет и инкубировали в течение 48 часов при 37°С в среде 5% углекислого газа. Для учета результатов проводили определение уровня жизнеспособных клеток и мертвых клеток перед облучением и через 48 часов после облучения.
Состояние клеток учитывали методом проточной цитофлуориметрии, оценивая количество жизнеспособных клеток, погибших клеток и апоптотических клеток с использованием набора флуоресцентных красителей, набор Annexin V-FITC Apoptosis Detection Kit, (Abcam, Великобритания) на цитометре «CytoFlex» (Beckman Coulter, США). Для этого клетки извлекали из планшета, осаждали центрифугированием (5 мин, 200g) и ресуспендировали в красящем буфере, содержащем смесь аннексин V - FITC и пропидий иодид. Далее цитофлуометрически подсчитывали живые клетки (отрицательные по обоим красителям), погибающие клетки в состоянии апоптоза (аннексин V-FITC-положительные), и некротические мертвые клетки, окрашиваемые только пропидий иодидом.
Результаты определения уровня жизнеспособности культуры клеток Jurkat через 48 часов после лучевого воздействия в дозе 3 Гр с применением и без применения аскорбата лития представлены в таблице 1. Как видно из таблицы 1 процент жизнеспособных клеток после лучевого воздействия в дозе 3 Гр при инкубации с 1,2 ммоль/л аскорбата лития был статистически значимо ниже по сравнению с облучением без аскорбата лития (p<0,001).
Применение аскорбата лития с формулой LiСНО в качестве радиосенсибилизирующего средства.