Результат интеллектуальной деятельности: Способы очистки и/или вирусной инактивации
Вид РИД
Изобретение
Настоящее изобретение относится к способам очистки белков (или белковых продуктов) и/или способам вирусной дезактивации белков (или белковых продуктов). Настоящее изобретение относится к способам очистки гликопротеинов (или гликопротеиновых продуктов) и/или способам вирусной дезактивации гликопротеинов (или гликопротеиновых продуктов). Белки/гликопротеины могут представлять собой, например рекомбинантные гликопротеины, такие как FSH (фолликулостимулирующий гормон), hCG (человеческий хорионический гонадотропин) или LH (лютеинизирующий гормон), продуцируемые в клетках-хозяевах. Белки/гликопротеины могут иметь происхождение из мочи.
Множество гликопротеинов используют в терапевтических лечениях. Например, гонадотропины представляют собой класс гликопротеинов, которые используют в лечении бесплодия. Гонадотропины представляют собой группу гетеродимерных гликопротеиновых гормонов, которые регулируют гонадную функцию у мужчин и женщин. Они включают фолликулостимулирующий гормон (FSH), лютеинизирующий гормон (LH) и хорионический гонадотропин (CG).
FSH и hCG, экстрагированные из мочи беременных женщин и женщин в постменопаузе, используют в течение многих лет при лечении бесплодия. Получение FSH и hCG, экстрагированных из мочи, включает сбор и обработку больших количеств мочи.
В качестве альтернативы продуктам, имеющим происхождение из мочи, доступны рекомбинантные варианты FSH и hCG. Одобренные в настоящее время продукты (Gonal-F, Ovitrelle от Merck Serono; Puregon от MSD) продуцируются (экспрессируются) в клетках яичника китайского хомячка (СНО).
Авторы настоящего изобретения разработали рекомбинантный FSH и рекомбинантный hCG, оба из которых экспрессируются в клеточной линии PER.C6®. Продукт FSH, имеющий происхождение из клеточной линии PER.C6®, и способы его получения раскрыты в Международных заявках на патенты №№ PCT/GB 2009/000978 (опубликованной как WO 2009/127826 A) и РСТ/ЕР 2012/065507 (опубликованной как WO 2013/020996). Этот продукт (FE 999049) прошел фазу 3 клинических испытаний в Европе. Продукт hCG, имеющий происхождение из клеточной линии PER.C6®, и способ его получения раскрыты в PCT/GB 2010/001854 (опубликованной как WO 2011/042688).
Авторы настоящего изобретения разработали методики, которые могут быть использованы для очистки, например, рекомбинантного FSH и рекомбинантного hCG, продуцированных в линиях клеток млекопитающих (например рекомбинантные FSH, раскрытые в WO 2009/127826 A и WO 2013/020996, и рекомбинантные hCG, раскрытые в WO 2011/042688).
В соответствии с настоящим изобретением в первом аспекте предложен способ очистки белка [например гликопротеина, например рекомбинантного гликопротеина, (например рекомбинантного) гонадотропина, (например рекомбинантного) FSH, hCG или LH], включющий стадию обработки белка [например гликопротеина, например рекомбинантного гликопротеина, (например рекомбинантного) гонадотропина, (например рекомбинантного) FSH, hCG или LH] комбинацией каприловой кислоты и этанола.
Способ может включать обработку раствора белка [например в воде, буфере или другой среде (например буфере; 100 мМ ацетате аммония, 30-50 мМ NaCl, рН 9-рН 9,5)] комбинацией каприловой кислоты и этанола. Этот способ может включать обработку раствора белка (например гликопротеина) в буфере (например буфере ацетате аммония) при рН от 6,5 до 12, например рН от 7,5 до 10, например рН от 9 до 9,5.
Стадию обработки гликопротеина комбинацией каприловой кислоты и этанола можно осуществлять при кислотном рН, например при от рН 2 до рН 6,5, например от рН 3 до рН 6,5, например от рН 4 до рН 6 (например рН 5,5±0,1) предпочтительно от рН 4,5 до рН 5,5]. Использование кислотных условий (например рН 4-рН 6) является следствием активности каприловой кислоты. Каприловая кислота может инактивировать оболочечные вирусы путем нарушения вирусной мембраны; последнее обеспечивается незаряженной формой каприловой кислоты, которая может проникать через вирусную гидрофобную мембрану. Каприловая кислота не заряжена при рН, который является близким к ее рКа (рН 4,9). При ΔрН на 1 единицу до (приблизительно рН 5,9), 100% молекул каприловой кислоты отрицательно заряжены, и, таким образом, менее эффективны для вирусной инактивации.
Белок может представлять собой рекомбинантный белок или белок, имеющий происхождение из мочи. Белок может представлять собой гликопротеин. Белок/гликопротеин может представлять собой гонадотропин, например FSH, hCG или LH. Гликопротеин может представлять собой рекомбинантный гликопротеин, например рекомбинантный гонадотропин, например рекомбинантный FSH, hCG или LH. Предпочтительно, белок/гликопротеин представляет собой рекомбинантный гликопротеин (например рекомбинантный гонадотропин, например рекомбинантный FSH, hCG или LH), продуцированный в клетке (клеточной линии) способом, включающим культивирование клетки (клеточной линии) в подходящей среде и сбор рекомбинантного гликопротеина из указанной клетки (клеточной линии) и/или указанной среды (например сбор рекомбинантного белка из супернатанта клеточной культуры). Клетка (клеточная линия) может представлять собой клетку (клеточную линию) млекопитающего, например клетку (линию) СНО, клетку (линию) PER.C6®, клетку (линию) HEK293, клетку (линию) НТ1080, клетку (линию) COS, клетку (линию) NOS, клетку (линию) SP20 и тому подобные. Предпочтительно, клетка (клеточная линия) представляет собой клетку (линию) PER.C6®.
Гликопротеины (гонадотропины, FSH, hCG, LH и тому подобные.), имеющие происхождение из мочи или рекомбинантные, как правило, находятся в форме раствора/суспензии в среде. Гликопротеин может быть представлен в виде единичной изоформы или в виде смеси изоформ, как хорошо известно в области техники. Здесь термины белок, гликопротеин, гонадотропин, FSH, hCG, LH и тому подобные охватывают раствор или суспензию, содержащую белок, гликопротеин, гонадотропин, FSH, hCG, LH и тому подобные. Здесь термины белок, гликопротеин, гонадотропин, FSH, hCG, LH и тому подобные охватывают раствор или суспензию, содержащую белок, гликопротеин, гонадотропин, FSH, hCG, LH и тому подобные, где белок, гликопротеин, гонадотропин, FSH, hCG, LH и тому подобные представлены в виде единичной изоформы или в виде смеси изоформ. Таким образом, термин FSH охватывает раствор или суспензию, содержащую FSH (например где FSH представлен в виде единичной изоформы или в виде смеси изоформ).
Здесь фраза "обработка белка (гликопротеина, гонадотропина, FSH, hCG, LH и тому подобных) комбинацией каприловой кислоты и этанола" означает применение как каприловой кислоты, так и этанола в отношении белка (гликопротеина, гонадотропина, FSH, hCG, LH и тому подобных), таким образом, что на белок (гликопротеин, гонадотропин, FSH, hCG, LH и тому подобные) одновременно воздействуют как каприловой кислотой, так и этанолом. Таким образом, эта фраза охватывает методики, где добавляют каприловую кислоту и этанол, в виде смеси или в виде двух отдельных реактивов, к раствору белка (гликопротеина, гонадотропина, FSH, hCG, LH и тому подобных), таким образом, что раствор представляет собой смесь каприловой кислоты, этанола и белка (гликопротеина, гонадотропина, FSH, hCG, LH и тому подобных); эта фраза также охватывает другие методики, где каприловая кислота и этанол действуют на белок (гликопротеин, гонадотропин, FSH, hCG, LH и тому подобные) одновременно.
Авторы изобретения неожиданно обнаружили, что обработка раствора, содержащего рекомбинантный белок/гликопротеин (например рекомбинантный FSH, рекомбинантный hCG), этанолом и каприловой кислотой, например комбинацией 20 мМ каприловой кислоты/30% этанола при кислотном рН, может приводить к денатурации некоторых вирусов (вызывая их инактивацию) и/или осаждение других вирусов и белков клеток-хозяев (примесей). Раствор затем может быть центрифугирован или профильтрован (для удаления осажденных вирусов и/или белков клеток-хозяев, например с использованием глубинного фильтра, такого как стеклянный фильтр), таким образом, что супернатант включает очищенный гликопротеин (например рекомбинантный FSH, рекомбинантный hCG) для последующей обработки и применения. Авторы изобретения обнаружили, что обработка раствора, содержащего рекомбинантный гликопротеин (например рекомбинантный FSH, рекомбинантный hCG), этанолом и каприловой кислотой может (1) инактивировать оболочечный вирус; и/или (2) очистить от безоболочечного вируса путем осаждения (осажденный вирус затем может быть удален посредством последующей стадии центрифугирования или фильтрования при помощи, например стекловолоконного фильтра); и/или (3) удалять белки, имеющие отношение к хозяину, путем осаждения (осажденные белки, имеющие отношение к хозяину, затем могут быть удалены посредством последующей стадии центрифугирования или фильтрования при помощи, например стекловолоконного фильтра). Этот относительно простой способ обработки и фильтрования обеспечивает замечательное удаление примесей (от 64% до 79% примесей клетки-хозяина удаляются в этом способе) при минимальной потере продукта гликопротеина (т.е. высокий выход).
Применение каприловой кислоты и этанола (например при очистке/вирусной инактивации рекомбинантного FSH и/или рекомбинантного hCG) обладает другими преимуществами. Во-первых, комбинация каприловой кислоты и этанола может укорачивать способ очистки, поскольку одна стадия может обладать двойной функцией: вирусной инактивации и осаждения, а также осаждения белков клетки-хозяина. Во-вторых, как описано выше, каприловая кислота наиболее активна в отношении вирусной инактивации при рН приблизительно 4,9, но этот низкий рН теоретически может повреждать рекомбинантный продукт FSH (путем диссоциации молекулы и тому подобного). В соответствии с уравнением Хендерсона-Хассельбаха при рН 5,5 приблизительно 20% СА (каприловая кислота) не заряжены, что обеспечивает хороший баланс вирусной инактивации с уменьшенным риском повреждения рекомбинантного FSH; добавление ЕЮН (например 30% ЕЮН) компенсирует потерю активности каприловой кислоты в этих условиях, которые менее вредны для белка. Наконец, комбинация каприловой кислоты/EtOH дает возможность для использования меньшей концентрации EtOH (например 30%), что чрезвычайно важно в способе получения из-за безопасности.
Концентрация каприловой кислоты может составлять от 10 мМ до 30 мМ каприловой кислоты, например от 18 мМ до 25 мМ каприловой кислоты, например от 19 мМ до 23 мМ каприловой кислоты, например 20 мМ каприловая кислота. EtOH может составлять от 20% до 50% EtOH, например от 25% до 50% EtOH, например от 30% до 50% EtOH, например 30% EtOH. Этот способ может включать стадию обработки гликопротеина 30%-50% этанолом и 18 мМ-25 мМ каприловой кислотой, например 20 мМ каприловой кислотой и 30% этанолом.
Способ может включать обработку белка (гликопротеина) этанолом и каприловой кислотой в течение периода инкубации от 1 минуты до 6 ч при температуре 23±2°C при перемешивании (например для вирусной инактивации при наблюдаемом осаждении), например обработку белка (гликопротеина) этанолом и каприловой кислотой в течение периода инкубации от 0,5 ч до 1 ч при температуре 23±2°C при перемешивании (например для вирусной инактивации при наблюдаемом осаждении). Этот способ может включать обработку белка (гликопротеина) этанолом и каприловой кислотой при температуре 4°-8°C в течение периода инкубации от 1 минуты до 32 ч без перемешивания (эта стадия может продолжить/обеспечить возможность для осаждения белков клетки-хозяина (НСР) и безоболочечных вирусов), например обработку белка (гликопротеина) этанолом и каприловой кислотой при температуре 4°-8°C в течение периода инкубации от 14 ч до 16 ч без перемешивания (эта стадия может продолжить/обеспечить возможность для осаждения НСР и безоболочечных вирусов). В предпочтительном примере этот способ включает обработку белка (гликопротеина) этанолом и каприловой кислотой в течение периода инкубации от 0,5 ч до 1 ч при температуре 23±2°C при перемешивании с последующим уменьшением температуры до 4°-8°C и последующей инкубацией в течение 16±2 часов, например от 14 ч до 16 ч без перемешивания.
Способ может включать обработку белка (гликопротеина) этанолом и каприловой кислотой в течение 1 ч ± 10 мин при рН 5,5±0,1 и температуре 23±2°C.
Способ может включать дополнительную стадию центрифугирования или фильтрования белка (гликопротеина) (раствора) с последующей обработкой каприловой кислотой и этанолом (например через глубинный фильтр, например стекловолоконный фильтр).
Способ может включать дополнительную стадию концентрирования белка (гликопротеина) (раствора) до желаемой концентрации (белка/гликопротеина) и/или другие (например последующие) стадии очистки/приготовления.
В соответствии с настоящим изобретением в дополнительном аспекте предложен способ вирусной инактивации в белке [например гликопротеине, например рекомбинантном гликопротеине, (например рекомбинантном) гонадотропине, (например рекомбинантном) FSH, hCG или LH)], включающий стадию обработки белка [например гликопротеина, например рекомбинантного гликопротеина, (например рекомбинантного) гонадотропина, (например рекомбинантного) FSH, hCG или LH] комбинацией каприловой кислоты и этанола.
Способ может включать обработку раствора гликопротеина [например в воде, буфере или другой среде (например буфере; 100 мМ ацетате аммония, 30-50 мМ NaCl, рН 9-рН 9,5)] комбинацией каприловой кислоты и этанола. Этот способ может включать обработку раствора белка (например гликопротеина) в буфере (например буфере ацетате аммония) при рН от 6,5 до 12, например рН от 7,5 до 10, например рН от 9 до 9,5.
Стадию обработки гликопротеина комбинацией каприловой кислоты и этанола можно проводить при кислотном рН, например от рН 2 до рН 6,5, например от рН 3 до рН 6,5, например от рН 4 до рН 6 (например рН 5,5±0,1), предпочтительно от рН 4,5 до рН 5,5]. Применение кислотных условий (например рН 4-рН 6) является следствием активности каприловой кислоты. Каприловая кислота может инактивировать оболочечные вирусы путем нарушения вирусной мембраны; последнее обеспечивается незаряженной формой каприловой кислоты, которая может проникать через гидрофобную мембрану вируса. Каприловая кислота не заряжена при рН, который является близким к ее рКа (рН 4,9). При ΔрН на 1 единицу до (приблизительно рН 5,9), 100% молекул каприловой кислоты отрицательно заряжены и, таким образом, менее эффективны для вирусной инактивации.
Концентрация каприловой кислоты может представлять собой от 10 мМ до 30 мМ каприловую кислоту, например от 18 мМ до 25 мМ каприловую кислоту, например от 19 мМ до 23 мМ каприловую кислоту, например 20 мМ каприловую кислоту. EtOH может составлять от 20% до 50% EtOH, например от 25% до 50% EtOH, например от 30% до 50% EtOH, например 30% EtOH. Этот способ может включать стадию обработки гликопротеина от 30% до 50% этанолом и от 18 мМ до 25 мМ каприловой кислотой, например 20 мМ каприловой кислотой и 30% этанолом.
Способ может включать обработку белка (гликопротеина) этанолом и каприловой кислотой в течение периода инкубации от 1 минуты до 6 ч при температуре 23±2°C при перемешивании, например обработку белка (гликопротеина) этанолом и каприловой кислотой в течение периода инкубации от 0,5 ч до 1 ч при температуре 23±2°C при перемешивании. Этот способ может включать обработку белка (гликопротеина) этанолом и каприловой кислотой при температуре 4°-8°C в течение периода инкубации от 1 минуты до 32 ч без перемешивания, например обработку белка (гликопротеина) этанолом и каприловой кислотой при температуре 4°-8°C в течение периода инкубации от 14 ч до 16 ч без перемешивания. В предпочтительном примере способ включает обработку гликопротеина этанолом и каприловой кислотой в течение периода инкубации от 0,5 ч до 1 ч при температуре 23±2°C при перемешивании с последующим уменьшением до температуры 4°-8°C и последующую инкубацию в течение от 14 ч до 16 ч без перемешивания.
Способ может включать обработку белка (гликопротеина) этанолом и каприловой кислотой в течение 1 ч ± 10 мин при рН 5,5±0,1 и температуре 23±2°C.
Способ может включать еще дополнительную центрифугирования или фильтрования белка (гликопротеина) (раствора) с последующей обработкой каприловой кислотой и этанолом (например через стекловолоконный фильтр).
Способ может включать дополнительную стадию концентрирования белка (гликопротеина) (раствора) до желаемой концентрации (белка/гликопротеина) и/или другие (например последующие) стадии очистки/приготовления.
Белок может представлять собой рекомбинантный белок или белок, имеющий происхождение из мочи. Белок может представлять собой гликопротеин. Белок/гликопротеин может представлять собой гонадотропин, например FSH, hCG или LH. Белок/гликопротеин может представлять собой рекомбинантный гликопротеин, например рекомбинантный гонадотропин, например рекомбинантный FSH, hCG или LH. Предпочтительно белок/гликопротеин представляет собой рекомбинантный гликопротеин (например рекомбинантный гонадотропин, например рекомбинантный FSH, hCG или LH), продуцированный в клетке (клеточной линии) способом, включающим культивирование клетки (клеточной линии) в подходящей среде и сбор рекомбинантного гликопротеина из указанной клетки (клеточной линии) и/или указанной среды (например сбор рекомбинантного белка из супернатанта клеточной культуры. Клетка (клеточная линия) может представлять собой клетку млекопитающего (клеточную линию), клетку (линию) СНО, клетку (линию) PER.C6®, клетку (линию) HEK293, клетку (линию) НТ1080, клетку (линию) COS, клетку (линию) NOS, клетку (линию) SP20 и тому подобные. Предпочтительно, клетка (клеточная линия) представляет собой клетку (линию) PER.C6®.
В соответствии с настоящим изобретением в дополнительном аспекте предложен белок, который очищен и/или подвергнут вирусной инактивации способом, описанным выше. Белок может представлять собой рекомбинантный белок или белок, имеющий происхождение из мочи. Белок может представлять собой гликопротеин. Гликопротеин может представлять собой рекомбинантный гликопротеин, например рекомбинантный гонадотропин, например рекомбинантный FSH, hCG или LH. Предпочтительно, гликопротеин представляет собой рекомбинантный гликопротеин (например рекомбинантный гонадотропин, например рекомбинантный FSH, hCG или LH), продуцированный в клетке (клеточной линии) способом, включающим культивирование клетки (клеточной линии) в подходящей среде и сбор рекомбинантного гликопротеина из указанной клетки (клеточной линии) и/или указанной среды (например сбор рекомбинантного белка из супернатанта клеточной культуры). Клетка (клеточная линия) может представлять собой клетку млекопитающего (клеточную линию), клетку (линию) СНО, клетку (линию) PER.C6®, клетку (линию) HEK293, клетку (линию) НТ1080, клетку (линию) COS, клетку (линию) NOS, клетку (линию) SP20 и тому подобные. Предпочтительно, клетка (клеточная линия) представляет собой клетку (линию) PER.C6®.
В соответствии с настоящим изобретением в дополнительном аспекте предложена фармацевтическая композиция [например для лечения (применения в лечении) бесплодия], содержащая белок (например гликопротеин, например рекомбинантный гликопротеин, например рекомбинантный FSH, рекомбинантный hCG), который очищен и/или подвергнут вирусной инактивации способом, описанным выше.
В соответствии с настоящим изобретением в дополнительном аспекте предложен способ лечения (например бесплодия), включающий стадию введения пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей белок (например гликопротеин, например рекомбинантный гликопротеин, например рекомбинантный FSH, рекомбинантный hCG), который очищен и/или подвергнут вирусной инактивации способом, описанным выше.
Лечение бесплодия может включать вспомогательные репродуктивные технологии (ART), стимуляцию овуляции или внутриматочное осеменение (IUI). Фармацевтическая композиция может быть использована, например при медицинских показаниях, при которых используют известные препараты FSH, LH, hCG.
Продукт или композиция могут быть приготовлены в виде хорошо известных композиций для любого пути введения лекарственного средства, например перорального, ректального, парентерального, трансдермального (например пластырная технология), внутривенного, внутримышечного, подкожного, интрацистернального, интравагинального, внутрибрюшинного, локального (порошки, мази или капли) или в виде буккального или назального спрея. Типичная композиция содержит фармацевтически приемлемый ночитель, такой как водный раствор, нетоксичные эксципиенты, включая соли и консерванты, буферы и тому подобное, как описано среди прочего в Remington's Pharmaceutical Sciences fifteenth edition (Matt Publishing Company, 1975), на страницах 1405-1412 и 1461 - 87, и Национальном формуляре XIV, четырнадцатое издание (American Pharmaceutical Association, 1975).
Примеры подходящих водных и неводных фармацевтических носителей, разбавителей, растворителей или наполнителей включают воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и тому подобные), карбоксиметилцеллюлозу и их подходящие смеси, растительные масла (такие как оливковое масло), и инъецируемые органические эфиры, такие как этилолеат.
Композиции по настоящему изобретению также могут содержать добавки, такие как, без ограничения, консерванты, увлажнители, эмульгаторы, поверхностно-активные вещества и диспергирующие агенты. Антибактериальные и противогрибковые агенты могут быть включены для предупреждения роста микробов и включают, например /w-крезол, бензиловый спирт, парабен, хлорбутанол, фенол, сорбиновую кислоту и тому подобные. Если включен консервант, то предпочтительны бензиловый спирт, фенол и/или м-крезол; тем не менее, консервант никоим образом не ограничен этими примерами. Кроме того, может быть желательно включать изотонические агенты, такие как сахара, хлорид натрия и тому подобные. Продукт или композиция может дополнительно включать соль, содержащую фармацевтически приемлемый катион щелочного металла, выбранный из группы, состоящей из солей Na+ или K+, или их комбинации. Предпочтительно, соль представляет собой соль Na+, например NaCl или Na2SO4.
Предпочтительно, продукт или композиция содержит гликопротеин и один или более чем один из полисорбата 20, L-метионина, фенола, динатрийсульфата и буфера фосфата натрия, сахарозы и цитратных буферов.
Инъецируемые композиции могут быть стерилизованы, например путем фильтрования через удерживающий бактерии фильтр или путем включения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной инъецируемой среде непосредственно перед применением. Инъецируемые композиции можно поставлять в любом подходящем контейнере, например флаконе, предварительно заполненном шприце, картриджах для инъекции и тому подобных.
Композиция может быть приготовлена для единичного применения или для множественного применения (многократная доза). Если продукт или композиция приготовлены для множественного применения, то предпочтительно, чтобы был включен консервант. Если включен консервант, то предпочтителен бензиловый спирт, фенол и/или м-крезол; однако консервант никоим образом не ограничен этими примерами. Продукт или композиция, приготовленные для единичного применения или множественного применения, могут дополнительно включать соль, содержащую фармацевтически приемлемый катион щелочного металла, выбранный из группы, состоящей из солей Na+ или K+, или их комбинации. Предпочтительно, соль представляет собой соль Na+, например NaCl или Na2SO4.
Продукт или композиция могут быть включены в контейнер, такой как флакон, предварительно заполненный картридж (например для однократного введения или множественного применения) или инъецирующее устройство, такое как "ручка", например, для введения множества доз.
Флаконы могут быть упакованы в блистерную упаковку или другие средства для поддержания стерильности. Любой продукт может возможно содержать инстукрции по применению композиций FSH (и, например, hCG, если он присутствует). рН и точную концентрацию различных компонентов фармацевтической композиции корректируют в соответствии со стандартной в данной области техники практикой. См. GOODMAN and GILMAN's THE PHARMACOLOGICAL BASIS FOR THERAPEUTICES, 7th ed. В предпочтительном воплощении композиции по изобретению поставляют в виде композиций для парентерального введения. Общие способы приготовления парентеральных композиций известны в области техники и описаны в REMINGTON; THE SCIENCE AND PRACTICE OF PHARMACY, выше, на стр. 780-820. Парентеральные композиции можно поставлять в жидкой композиции или в виде твердого вещества, которое смешивают со стерильной инъецируемой средой непосредственно перед введением. В особенно предпочтительном воплощении парентеральные композиции поставляют в стандартной лекарственной форме для облегчения введения и единообразия дозы.
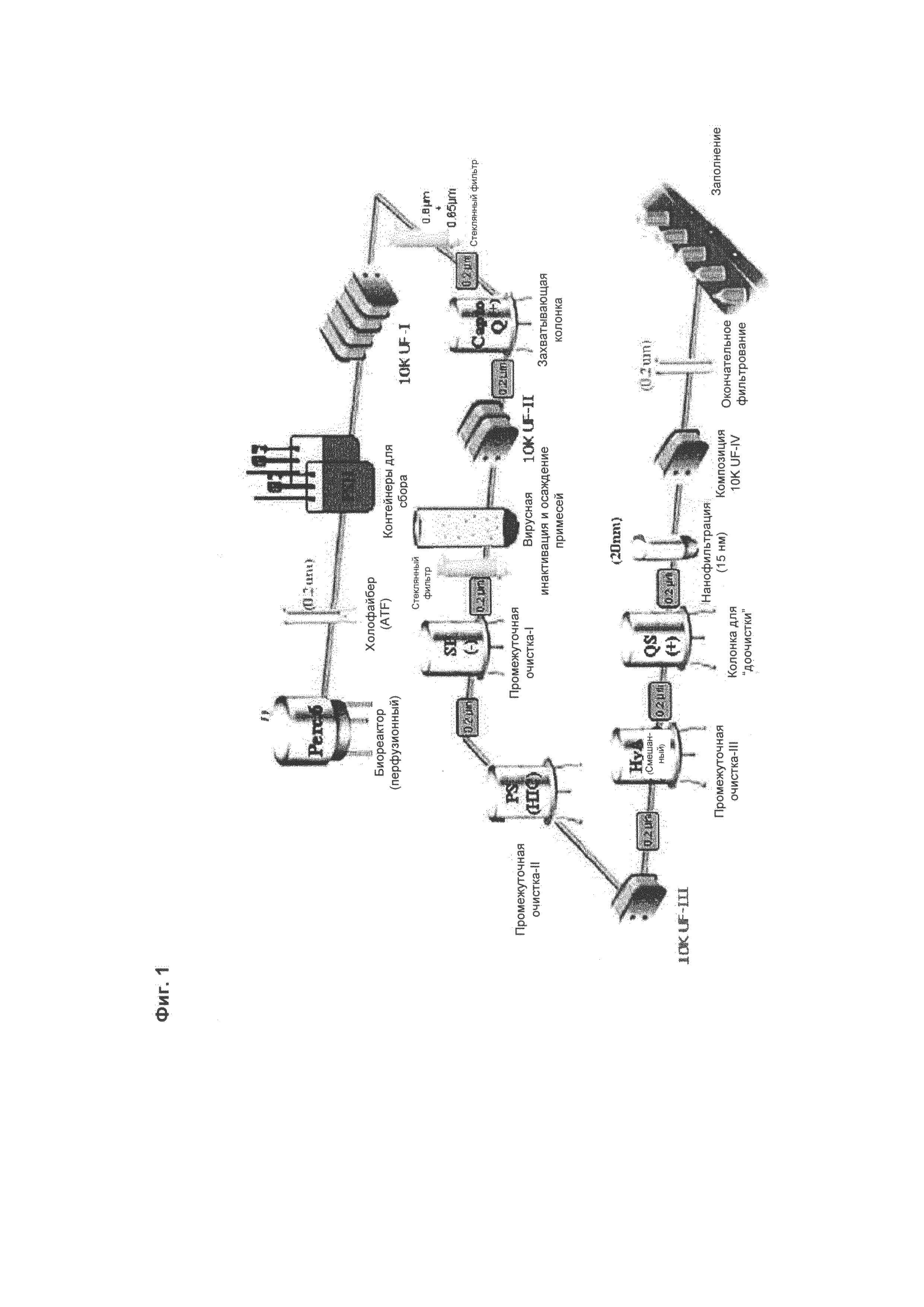
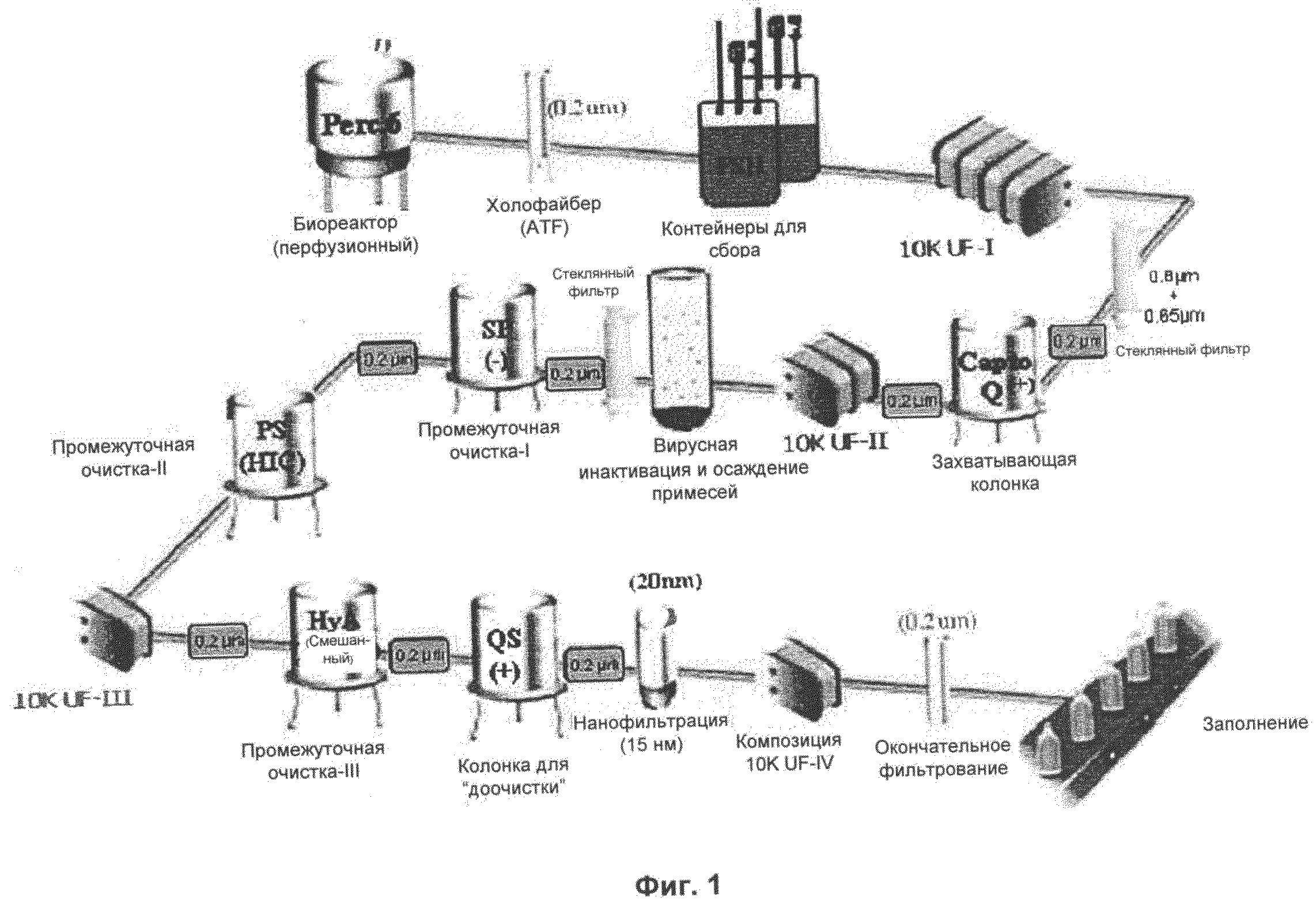
Настоящее изобретение далее будет описано со ссылкой на приложенные графические материалы, где: Фиг. 1 демонстрирует схему способа очистки рекомбинантного FSH (вирусная дезактивация) в соответствии с воплощением настоящего изобретения;
Фиг. 2 демонстрирует картину геля с последующей качественной оценкой удаления примесей для различных обработанных UF2-AD (ультрафильтрация после диализа) образцов FSH, анализируемых посредством 12% редуцирующего PAGE (электрофорез в полиакриламидном геле), где дорожка 1 представляет собой маркеры LMW (низкая молекулярная масса), дорожка 2 представляет собой буфер для образца, дорожка 3 представляет собой UF2-AD, дорожка 4 представляет собой UF2-AD плюс 10 мМ СА (каприловая кислота), рН 5,5, дорожка 5 представляет собой UF2-AD плюс 10 мМ СА, 30% этанол, рН 5,5, дорожка 6 представляет собой буфер для образца, дорожка 7 представляет собой MW (молекулярную массу) низкого диапазона, дорожка 8 представляет собой UF2-AD, дорожка 9 представляет собой UF2-AD плюс 20 мМ СА, рН 5,5 и дорожка 10 представляет собой UF2-AD плюс 20 мМ СА, 30% этанол рН 5,5 (см. пример 3); и
Фиг. 3 демонстрирует картину геля с последующей качественной оценкой удаления примесей для различных обработанных образцов hCG, анализируемых посредством 12% редуцирующего PAGE (электрофорез в полиакриламидном геле), где дорожка 1 представляет собой маркеры LMW (низкая молекулярная масса), дорожка 2 представляет собой содержащий hCG Harvest-AD (собираемый материал после диализа), дорожка 3 является NR - не релевантной, дорожка 4 представляет собой супернатант [Harvest-AD плюс 15 мМ СА рН 5,0], и дорожка 5 представляет собой супернатант [Harvest-AD плюс 20 мМ СА плюс 10% этанол рН 5,0], см. пример 4.
Пример 1
Фиг. 1 демонстрирует обзор всего способа очистки рекомбинантного FSH. Как можно видеть на Фиг. 1, рекомбинантный FSH экспрессируется в клеточной линии PER.C6®, сконструированной посредством способов, раскрытых в WO 2013/020996 и WO 2009/127826 A, с использованием биореактора.
В биореактор загружают клетки, и рост клеток стимулируют посредством способов, известных специалистам в данной области техники, и биореактор функционирует в перфузионном режиме для получения и непрерывного сбора рекомбинантного FSH с использованием системы Hollofibre (ATF4), поставляемой Repligen. Загрузку по меньшей мере 1×106 клеток/мл в общем объеме 4±1 литра осуществляют в среде 6GRO. Продукцию осуществляют в среде ProPer-1, и продукт из биореактора собирают в полиэтиленовые контейнеры. Таким образом, в этом примере белок (гликопротеин) представляет собой рекомбинантный гликопротеин (рекомбинантный FSH), продуцируемый в клеточной линии PER.C6® способом, включающим культивирование клеточной линии в подходящей среде (среда ProPer-1) и сбор рекомбинантного гликопротеина из среды (посредством сбора рекомбинантного белка из супернатанта клеточной культуры).
Собираемый из биореактора продукт объединяют и подвергают стадии ультрафильтрации/диафильтрации через фильтр 10 кДа (UF1), которая уменьшает концентрацию собираемого продукта, кондиционирует собираемый продукт (в отношении рН и проводимости) для хроматографии Capto-Q и удаляет пигменты и низкомолекулярные компоненты из культуральной среды. Концентрат фильтруют через стекловолоконный фильтр 0,8+0,65 мкм для очистки раствора способа (см. Фиг. 1), и затем подвергают фильтрации через фильтр 0,2 мкм для контроля бионагрузки. Затем используют анионообменную хроматографию Capto-Q посредством способов, хорошо известных в области техники, для захвата рекомбинантного FSH и для удаления ДНК, эндотоксина, белков клеток-хозяев и примесей, связанных с процессом. Дополнительную фильтрацию через фильтр 0,2 мкм осуществляют для контроля бионагрузки.
Профильтрованный элюат Capto-Q подвергают дополнительной ультрафильтрации/диафильтрации через фильтр 10 кДа (UF2) для обессоливания и уменьшения объема перед очисткой/вирусной инактивацией посредством способов, хорошо известных в области техники.
Стадия СА/EtOH
Концентрат после UF2 представляет собой раствор рекомбинантного FSH в буфере (100 мМ ацетат аммония, 30 мМ NaCl, рН 9,3 - рН 9,7). рН белкового раствора сначала уменьшают с рН 9,3 - рН 9,7 до рН 6,3±0,3 при 23±2°C при перемешивании, затем обрабатывают комбинацией 20 мМ каприловая кислота/30% этанол (СА/EtOH), а затем дополнительно доводят рН до 4,5-5,6 (рН доводят при помощи 1М HCl). После этой обработки белковый раствор оставляют инкубироваться в течение 0,5 ч - 1 ч при 23±2°C при перемешивании (в течение этого времени осуществляется вирусная инактивация, и обнаруживается белый осадок в виде хлопьев). К концу 0,5 ч - 1 ч температуру белкового раствора уменьшают до 4°-8°C, и раствор инкубируют в течение еще 14 ч - 18 ч, например от 14 до 16 ч, без перемешивания (это обеспечивает продолжение осаждения НСР и безоболочечных вирусов). Стадия обработки СА/ЕТОН имеет тройную активность: (1) инактивация оболочечного вируса; (2) очистка от безоболочечного вируса посредством осаждения с последующей стадией очистки, предназначенной для удаления осадка; и (3) удаление белков, имеющих отношение к хозяину, посредством осаждения.
Осажденные примеси (безоболочечный вирус и белок, имеющий отношение к хозяину) удаляют посредством стадии фильтрования через стекловолоконный фильтр 0,8+0,65 микрометров, где стадия фильтрования, также очищает раствор рекомбинантного FSH.
Дополнительное фильтрование через фильтр 0,2 мкм осуществляют в качестве контроля бионагрузки.
Раствор затем подвергают катионообменной хроматографии на основе сульфопропил-сефарозы (SP-FF) посредством способов, хорошо известных в области техники, для удаления каприловой кислоты, этанола и дополнительных белков клетки-хозяина. Еще одно фильтрование через фильтр 0,2 мкм осуществляют для контроля бионагрузки с последующей дополнительной стадией очистки с использованием фенил-сефарозной хроматографии с гидрофобным взаимодействием (PS-FF) для удаления свободных субъединиц рекомбинантного FSH и белков клетки-хозяина.
Элюат PS подвергают третьей стадии ультрафильтрации/диафильтрации через фильтр 10 кДа (UF3) для удаления соли и кондиционирования раствора для следующей стадии. Дополнительное фильтрование через фильтр 0,2 мкм осуществляют в качестве контроля бионагрузки перед гидроксиапатитной адсорбционной хроматографии (НуА), предназначенной для удаления диссоциированных субъединиц FSH и основных гетеродимеров, с последующим дополнительным фильтрованием через фильтр 0,2 мкм, проводимым в качестве контроля бионагрузки.
"Стадию доочистки" путем анионообменной хроматографии на Q-сефарозе (QS-FF) осуществляют в режиме связывание/элюция для удаления белков хозяина, ДНК, эндотоксинов и возможных вирусов. Осуществляют дополнительное фильтрование через фильтр 0,2 мкм для контроля бионагрузки до объединения QS MP и нанофильтрования для удаления возможных вирусов. Супернатант подвергают четвертой стадии ультрафильтрации/диафильтрации (UF4) через фильтр 10 кДа для концентрирования рекомбинантного FSH до 0,5-1,1 мг/мл, а затем добавляют полисорбат 20 до конечной концентрации 0,005 мг/мл. Эти стадии представляют собой стадии диализа и корректирования буфера, которые хорошо известны в области техники. Рекомбинантный FSH подвергают окончательной стадии фильтрования через фильтр 0,2 мкм перед аликвотированием в первичную упаковку и хранением при -20°C до перевозки.
Авторы изобретения обнаружили, что обработка каприловой кислотой/этанолом способна значительно уменьшить содержание примесей, имеющих отношение к хозяину. В соответствии с различными производственными сериями (данные не представлены) от 64 до 79% примесей имеющих отношение к хозяину, удаляют посредством описанной выше стадии СА/EtOH (и последующего фильтрования через стекловолоконный фильтр), при получении высокого выхода, составляющего приблизительно от 90 до 95% FSH. Это представляет собой значительное уменьшение содержания примесей, имеющих отношение к хозяину, которое осуществляют посредством простого способа при минимальной потере белкового продукта (продукт гликопротеин).
Замечательная эффективность очистки от вируса на этой стадии обобщена в Таблице 1, которая демонстрирует обобщение 1одю коэффициентов уменьшения, находящиеся в диапазоне от 4,25 или больше до 5,41 или больше. Log коэффициент уменьшения (LRF) 4 Log10 или больше (например до 8 Log10 или больше) обычно рассматривают как высокий, надежный и эффективный.
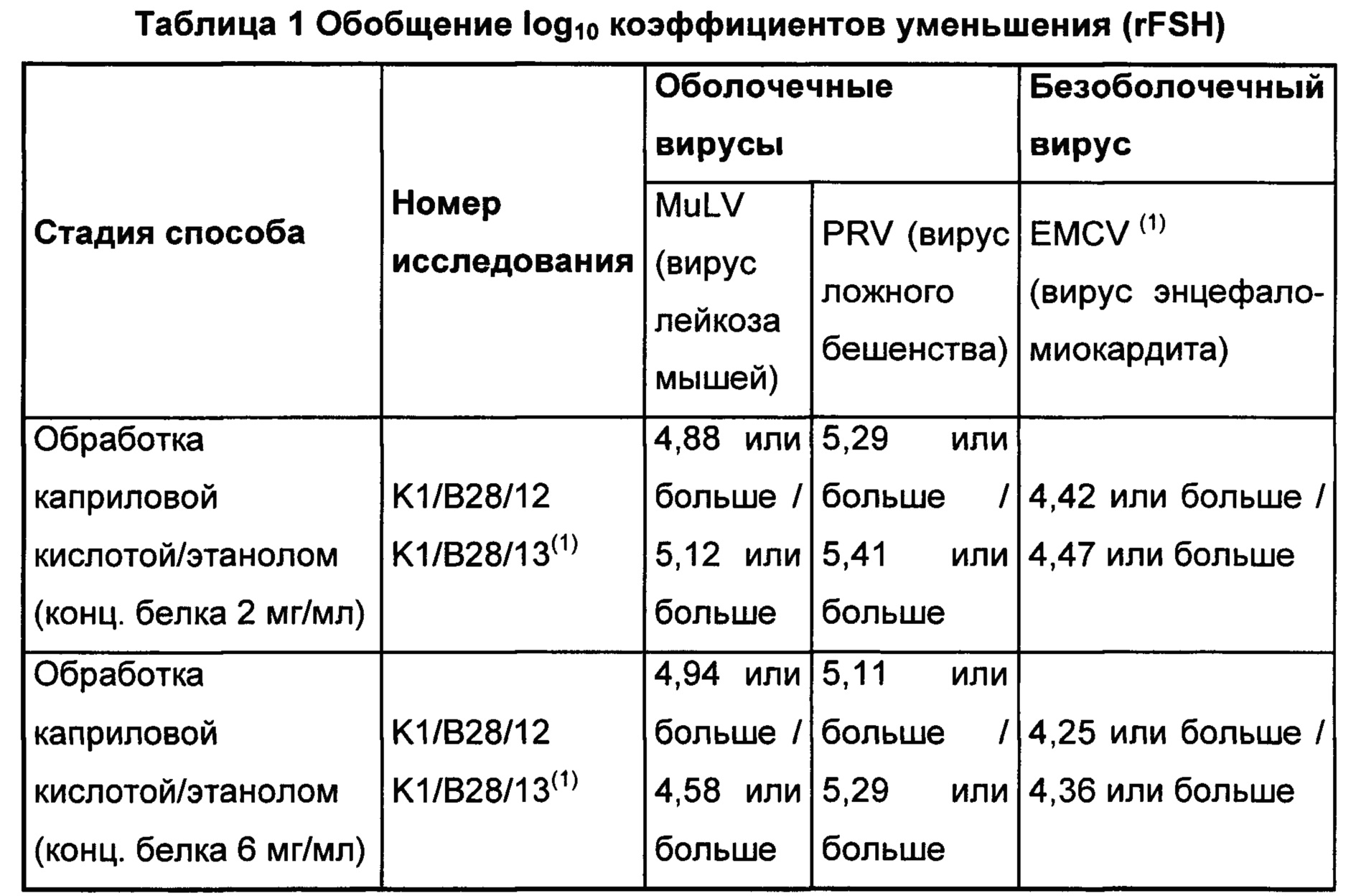
(1) Исследование с EMCV включает фильтрование через стекловолоконный фильтр после обработки.
Приведенный выше пример относится к rFSH, но специалисту в данной области техники понятно, что данный описанный выше способ [например стадия СА/EtOH (и последующее фильтрование через стекловолоконный фильтр)] легко применим к очистке/вирусной инактивации других белков (например гликопротеинов), например rhCG [например rhCG, продуцированных в клеточной линии PER.C6®, способом, изложенным в PCT/GB 2010/001854 (опубликованной как WO 2011/042688)].
Пример 2
В еще одном примере способа по изобретению предложен способ очистки/вирусной инактивации hCG. Способ, аналогичный Примеру 1 выше (за исключением стадии катионообменной хроматографии на основе сульфопропил-сефарозы (SP-FF)), использовали для очистки/вирусной инактивации rhCG, продуцированного в клеточной линии PER.C6 способом в соответствии с PCT/GB 2010/001854 (опубликованной как WO 2011/042688). Авторы изобретения обнаружили, что химическая инактивация посредством каприловой кислоты и этанола при кислотном рН, то есть с использованием стадии СА/EtOH, описанной в Примере 1, удаляла приблизительно 65% примесей, не относящихся к hCG (посредством осаждения), при высоком выходе, составляющем приблизительно 90% hCG.
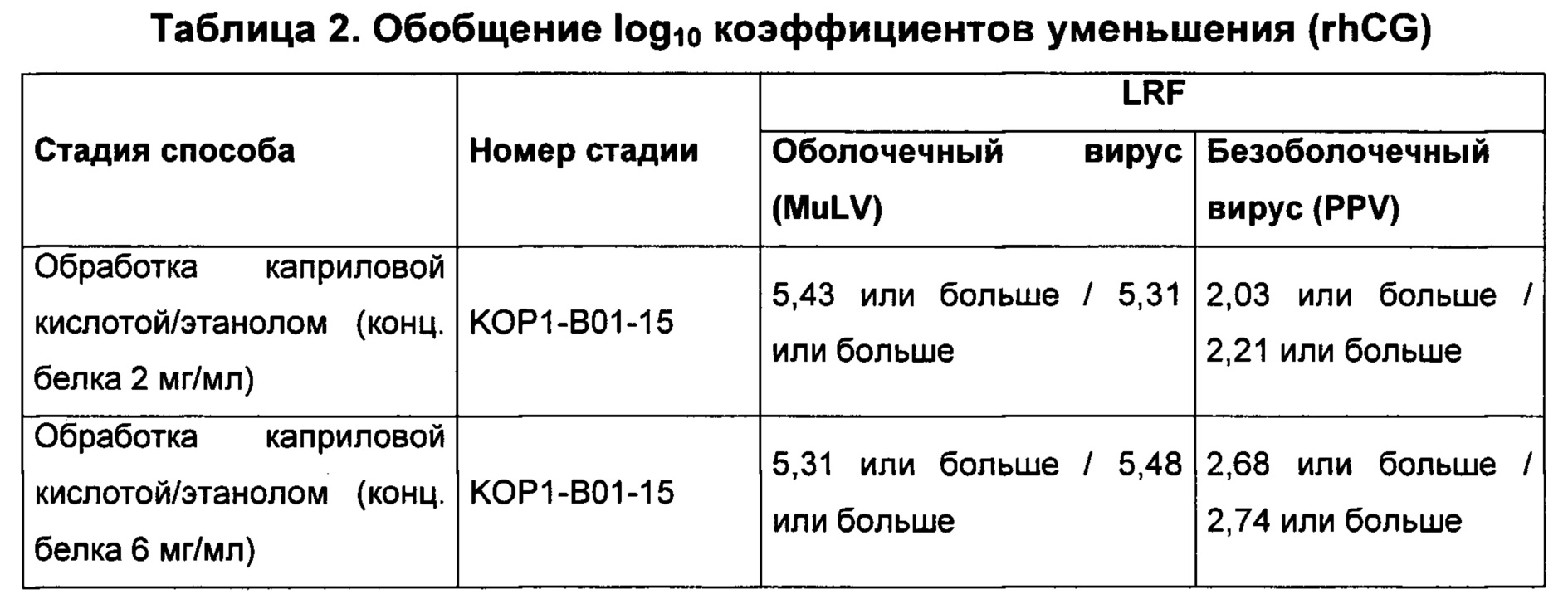
Превосходная эффективность очищения от вируса стадии СА/EtOH в примере обобщена в Таблице 2. Вирусная инактивация MuLV была эффективной, как определено при помощи высокого LRF, полученного в диапазоне от 5,31 или больше до 5,48 или больше. LRF в диапазоне от 2,03 или больше до 2,74 или больше получали для обработки СА/EtOH и удаления осадка.
Пример 3: Оценка условий осаждения для удаления примесей в растворе, содержащем rFSH
Описание эксперимента:
Промежуточный продукт UF2-AD (ультрафильтрация после диализа) получали с использованием способа очистки rFSH в соответствии с Примером 1 (до стадии СА/EtOH), содержащем 100 мМ ацетат аммония плюс 30 мМ NaCl при рН 9,50±0,20, 11,00±0,50 мС/см. Его аликвотировали, и каждую аликвоту подвергали условиям дифференцированного осаждения для удаления примесей (rFSH растворим в растворе). Проверенные условия осаждения были следующими:
1. UF2-AD без обработки (контроль)
2. UF2-AD плюс 10 мМ каприловая кислота (СА), рН 5,5
3. UF2-AD плюс 10 мМ СА, 30% этанол, рН 5,5
4. UF2-AD плюс 20 мМ СА, рН 5,5
5. UF2-AD плюс 20 мМ СА, 30% этанол, рН 5,5
Все обработанные образцы инкубировали в течение 30 мин при RT (комнатной температуре) при перемешивании, а затем дополнительно инкубировали в течение 30 мин без перемешивания. Дополнительное инкубирование проводили при 2-8°C в течение 16-20 ч. Образующиеся осадки удаляли посредством центрифугирования, а супернатанты собирали.
Рабочие параметры процесса осаждения:
Выделение rFSH
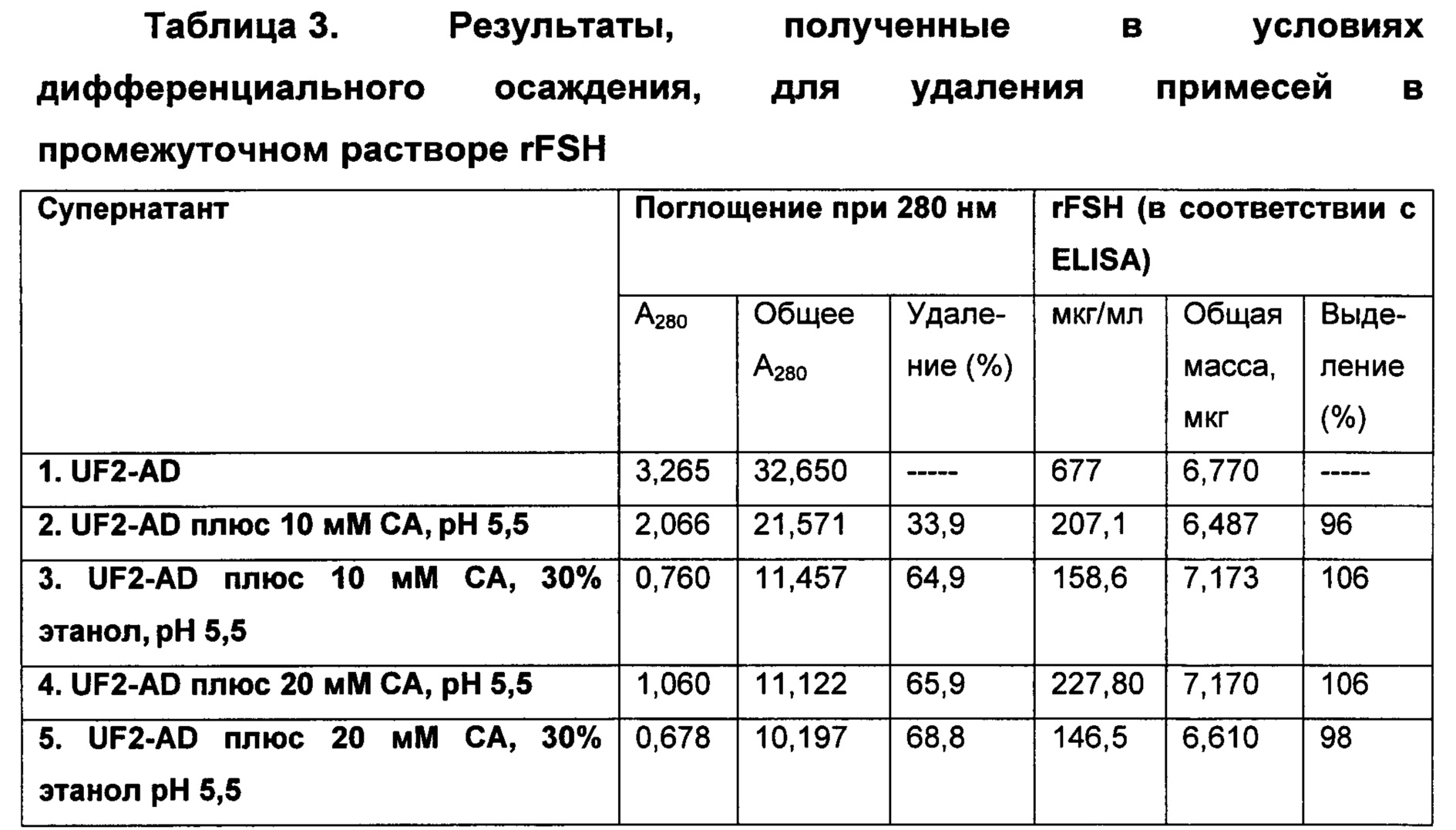
Концентрацию rFSH во всех образцах определяли посредством ELISA (иммуноферментный анализ) FSH и рассчитывали выходы каждого образца после обработки, и они изложены в Таблице 3.
Как видно из Таблицы 3, 96%, 106%, 106% и 98% rFSH в растворах способа UF2-AD выделялось после осаждения 10 мМ СА, 10 мМ СА плюс 30% этанол, 20 мМ СА и 20 мМ СА плюс 30% этанол, соответственно. Это указывает на то, что rFSH не осаждается и остается растворимым в растворе.
Удаление примесей
Измеряли поглощение при 280 нм в не обработанном UF2-AD и в каждом из супернатантов обработанных UF2-AD, и рассчитывали удаление примесей, как изложено в Таблице 3. 33,9%, 64,9%, 65,9% и 68,8% общих примесей в соответствии с Агво в UF2-AD удалялось после осаждения 10 мМ СА, 10 мМ СА плюс 30% этанол, 20 мМ СА и 20 мМ СА плюс 30% этанол, соответственно.
Необработанный UF2-AD и супернатанты различных обработанных UF2-AD подвергали 12%редуцирующему PAGE (электрофорез в полиакриламидном геле) для качественной оценки удаления примесей. Картина геля представлена на Фиг. 2. Супернатант, полученный после осаждения 10 мМ СА плюс 30% этанол (дорожка 5) и 20 мМ СА плюс 30% этанол рН 5,5 (дорожка 10), по существу является более чистым по сравнению с супернатантом, полученным после осаждения 10 мМ СА рН 5,5 (дорожка 4) и 20 мМ СА (дорожка 9), соответственно. Последнее демонстрирует синергетический эффект добавления этанола к каприловой кислоте на стадии осаждения.
Выводы об эксперименте:
1. Осаждение UF2-AD посредством этанола и каприловой кислоты приводило к более чистому продукту по сравнению с продуктом, получаемым при использовании только каприловой кислоты.
2. Комбинация этанола и каприловой кислоты не осаждает rFSH, который остается растворимым в растворе, что означает, что данная стадия представляет собой стадию очистки с высоким выходом и вирусной инактивацией.
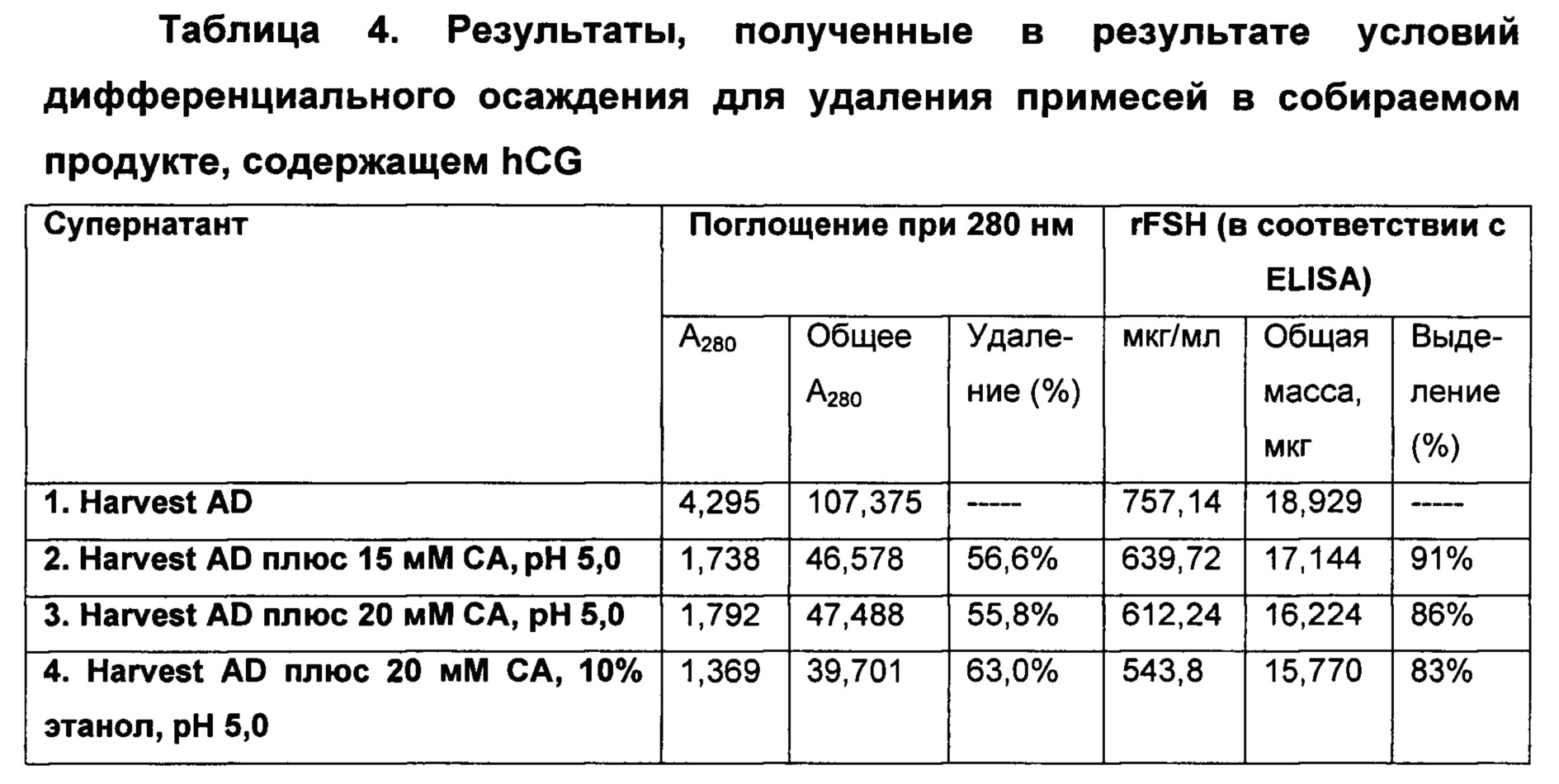
Пример 4: Оценка условий осаждения для удаления примесей в содержащем hCG собираемом продукте
Описание эксперимента:
Содержащий hCG собираемый продукт концентрировали приблизительно в 40 раз и подвергали диализу в 100 мМ глицине, 50 мМ NaCl рН 9,0, буфере 6 мСм/см при помощи системы ультрафильтрации (UF) через фильтр 10 кДа. В конце UF выделенный белковый раствор, материал Harvest-AD (после диализа), аликвотировали, и каждую аликвоту подвергали условиям дифференциального осаждения для удаления примесей (тогда как hCG остается растворимым в растворе). Протестированные условия осаждения представляют собой следующие (Таблица 4):
1. Harvest-AD без обработки в качестве контроля;
2. Harvest-AD плюс 15 мМ СА, рН 5,0
3. Harvest-AD плюс 20 мМ СА, рН 5,0
4. Harvest-AD плюс 20 мМ СА плюс 10% этанол, рН 5,0.
Все обработанные образцы инкубировали в течение 1 ч при RT при перемешивании. Полученные осадки удаляли посредством центрифугирования, тогда как супернатанты собирали.
Рабочие параметры процесса осаждения:
Выделение hCG
Определяли концентрацию hCG в необработанном собранном материале и в каждом из супернатантов обработанных Harvest AD, и выделение рассчитывали в соответствии, как подробно изложено в Таблице 4.
Удаление примесей
Определяли поглощение при 280 нм (А280) в необработанном собранном материале и в каждом из супернатантов обработанных Harvest AD, и удаление примесей рассчитывали, как подробно изложено в Таблице 4.
Необработанный собираемый материал и супернатанты различных обработанных Harvest AD подвергали 12% редуцирующему PAGE (электрофорез в полиакриламидном геле) для качественной оценки удаления примесей. Картина геля представлена на Фиг. 3.
Обсуждение:
1. Выделение hCG - 91%, 86% и 83% hCG в Harvest-AD выделяли после осаждения 15 мМ СА, 20 мМ СА и 20 мМ СА плюс 10% этанол, соответственно.
2. Удаление примесей в соответствии с А280 - 56,6%, 55,8% и 63,0% общего А280 в Harvest-AD удалялось после осаждения 15 мМ СА, 20 мМ СА и 20 мМ СА плюс 10% этанол, соответственно.
3. Удаление примесей при помощи геля - супернатант, полученный после осаждения посредством 20 мМ СА плюс 10% этанол при рН 5,0 (дорожка 5), по существу является более чистым относительно супернатанта, полученного после осаждения посредством 15 мМ СА при рН 5,0 (дорожка 4)
Выводы:
1. Осаждение содержащего hCG собираемого материала путем добавления этанола и каприловой кислоты приводит к более чистому продукту по сравнению с продуктом, получаемым при использовании только каприловой кислоты.