Результат интеллектуальной деятельности: Способ выбора тактики лечения миомы матки и ее сочетания с аденомиозом у женщин
Вид РИД
Изобретение
Предлагаемое изобретение относится к медицине, а именно к гинекологии и может быть использовано для выбора тактики лечения у пациенток с миомой матки, в том числе ее сочетания с аденомиозом. Вероятность рецидивов миомы матки, ухудшение репродуктивного здоровья и утрата фертильности после оперативного лечения наиболее распространенной доброкачественной опухоли матки (18-40%) требуют пристального внимания к женщинам, заинтересованным в деторождении.
Традиционные устои оперативной гинекологии существенно видоизменились с появлением технологических новинок: конкуренцию радикальной гистерэктомии составляют органосохраняющие малоинвазивные эндоскопические и эндоваскулярные вмешательства. Однако изобилие существующих методик лечения миомы матки в отсутствие оптимальных критериев доступа и объема оперативного вмешательства стало предметом конфронтационных воззрений об эффективности каждой технологии лечения.
Приоритетности лапароскопических миомэктомий при субсерозной миоме матки противостоят устойчиво высокие показатели разрывов матки в родах по рубцу, указывая на необходимость стратификации выбора технологии лечения с учетом репродуктивных планов. По определению, выбор базируется на ряде факторов: симптомы, размеры и локализация опухоли, количество миоматозных узлов, желание пациентки сохранить матку и репродуктивную функцию.
Дефицит и противоречивость информации о безопасности и эффективности современных методик делает затруднительным продуктивное использование возможностей малоинвазивной хирургии, требует детального анализа принципов, преимуществ, недостатков и рисков технологий, направленных на устранение или сокращение перфузии в тканях миомы матки. Многолетнее изучение причин неэффективного лечения миомы матки и ее сочетания с аденомиозом привело к выводу о том, что удаление узлов не решает проблему рецидивов миоматозного роста (от 2,5% до 23%, по разным данным), что связывают с отсутствием алгоритмизированного подхода.
Для прогнозирования риска развития рецидивов миомы матки и ее сочетания с аденомиозом была построена модель бинарной логистической регрессии - пошагового включения/исключения с выбором наиболее значимых факторов по данным клинико-анамнестичесхого и лабораторно-инструментального обследования. Разработанная математическая модель позволила сформировать группы повышенного риска рецидивов миомы матки и ее сочетания с аденомиозом с пограничным значением p: p>0,5 имеет место высокий риск, p<0,5 - низкий.
Аналогом предложенного способа является способ определения прогноза рецидивов миомы матки и восстановления фертильности, описанный коллективом авторов Кыргызского научного центра репродукции человека при МЗ Кыргызской Республики [Третьякова Н.В., Рыскельдиева В.Т., Гурьянов В.Г. Рецидив лейомиомы матки у женщин: частота и прогноз // Современные проблемы науки и образования. - 2018. - №5; DOI: 10.17513/spno.28035].
За ближайший аналог принят способ определения прогноза рецидива миомы матки, описанный в статье «Рецидив лейомиомы матки у женщин: частота и прогноз», опубликованной в журнале «Современные проблемы науки и образования» сотрудниками Кыргызского научного центра репродукции человека при МЗ Кыргызской Республики. Недостатком способа является то, что он имеет только информационную ценность, но не предполагает изменений в тактике ведения пациенток, направленных на уменьшение сроков реабилитации и улучшение репродуктивного прогноза. Кроме того, в качестве факторов риска рассматривают только анамнестические данные (возраст, вес, семейное положение, наличие занятости, родов, абортов, самопроизвольных выкидышей, неразвивающихся беременностей, наличие кистозных образований придатков матки в анамнезе, хронические воспалительные заболевания органов малого таза, нарушения менструального цикла, псевдоэрозии шейки матки, перенесенные оперативные вмешательства, на органах малого таза, заболевания мочевыделительной системы заболевания органов дыхания, заболевания со стороны сердечно-сосудистой системы, желудочно-кишечного тракта, сосудов, заболевания эндокринной системы, заболевания крови, заболевания органов зрения), и не учитываются данные психо-эмоционального и иммунологического статуса, морфологические, лабораторно-инструментальные данные. Также способ-аналог не ставит задачу улучшения качества жизни пациенток после проведенного лечения.
Задачами изобретения являются:
1. включение в определение прогноза рецидива миомы матки и ее сочетания с аденомиозом достоверно значимые анамнестические, клинические, иммунологические, морфологические и лабораторно-инструментальные показатели, а также данные психо-эмоционального статуса:
2. уменьшение сроков реабилитации пациенток и восстановления репродуктивной функции после миомэктомии:
3. снижение частоты рецидивов миомы матки и ее сочетания с аденомиозом после органосохраняющего лечения;
4. улучшение качества жизни пациенток с миомой матки и ее сочетанием с аденомиозом за счет персонифицированного подхода к выбору тактики лечения и снижения частоты повторных хирургических вмешательств.
Сущность изобретения заключается в том, что у женщины при комплексном обследовании предварительно выявляют факторы риска рецидива миоматозного роста - коэффициенты регрессии (k) в соответствии с таблицей 1: множественные узлы (k1), анемию средней степени тяжести (k2), бактериальную обсемененность цервикального канала с рецидивирующим бактериальным вагинозом (k3), обсемененность цервикального канала и инфицирование миоматозных узлов (k4), умеренную экспрессию Ki-67 (k5), умеренную или высокую экспрессию рецепторов к прогестерону (k6), умеренную или высокую экспрессию рецепторов к виментину (k7), умеренную или высокую экспрессию рецепторов к коллагену (k8), наличие сосудистых анастомозов между маткой и яичниками или другими сосудами (k9), реакцию хронического стресса (k10), реакцию тренировки (k11), гипс реактивность (k12), гиперреактивность (k13), гиперплазию эндометрия (k14), полиморфизм D гена GSTP1 (k15), нулевой вариант гена GSTT1 (k16), проведенную предварительно комплексную реабилитацию (k17), диаметр сосудов со стенкой - более 99,6 μm (k18), нулевой вариант гена GSTM1 (k19), константа (k20); затем индивидуальную степень риска рецидива заболевания вычисляют по формуле:
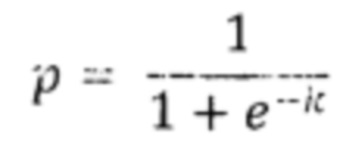
где е - основание натурального логарифма, k - сумма коэффициентов регрессии факторов риска, выявленных у данной пациентки, и константы k20, и при условии p<0,5 определяют низкий риск рецидива заболевания и последующее хирургическое вмешательство, а при p≥0,5 определяют высокий риск рецидива заболевания и тактику, включающую расширенную предоперационную подготовку - лечение анемии, восстановление нормобиоценоза, коррекцию аномальных адаптационных реакций, гипо- или гиперреактивности, затем выбирают тактику хирургического доступа: при заинтересованности в беременности - в пользу лапаротомии, а при незаинтересованности в беременности - лапароскопическое удаление клинически значимых узлов, затем проводят расширенную послеоперационную реабилитацию - противорецидивную гормонотерапию, коррекцию аномальной иммунореактивности, цитокинового профиля, метаболическую терапию.
Технический результат: предлагаемый способ предполагает включение в определение прогноза рецидива миомы матки и ее сочетания с аденомиозом достоверно значимых анамнестических, клинических, иммунологических, морфологических и лабораторно-инструментальных показателей, а также данных психо-эмоционального статуса. Таким образом, за счет расширения комплекса учитываемых показателей и персинификации подхода, способ позволяет уточнять тактику лечения и снизить частоту рецидивов миомы матки и ее сочетания с аденомиозом, уменьшить сроки реабилитации пациенток и восстановления репродуктивной функции после миомэктомии, улучшить качество жизни пациенток с миомой матки, в том числе в сочетании с аденомиозом.
Способ актуален, учитывая рост количества пациенток с миомой матки и нереализованной репродуктивной функцией, что обусловлено глобальными изменениями в репродуктивном поведении современных женщин (увеличение возраста первых родов), высокой частотой гормонального дисбаланса на фоне хронического стресса, а также повышением требований пациенток к качеству жизни.
Способ осуществляют следующим образом. Для пациенток с наличием миомы матки, в том числе в сочетании с аденомиозом, расширяют диагностический комплекс на всех этапах - дооперационном, интраоперационном и послеоперационном (раннем и позднем).
На этапе подготовки к операции определяют следующие факторы риска (эхографические, лабораторные): множественность узлов, наличие гиперплазии эндометрия, сосудистых анастомозов между маткой и яичниками или другими сосудами, наличие анемии средней степени тяжести, бактериальной обсемененности цервикального канала с рецидивирующим бактериальным вагинозом, обсемененность цервикального канала и инфицирование миоматозных узлов. В пользу последней свидетельствуют наличие хламидийной инфекции, анаэробных микроорганизмов (гарднереллы), уреаплазменная и/или микоплазменная инфекция, инфицирование вирусом простого герпеса, данные 3D-допплерометрии. При патогистологическом и иммуногистохимическом исследовании возможно выявление умеренной экспрессии маркера Ki-67, умеренную или высокую экспрессию рецепторов к прогестерону, умеренную или высокую экспрессию рецепторов к виментину, умеренную или высокую экспрессию рецепторов к коллагену, а также наличие сосудов, диаметр которых со стенкой превышает 99,6 μm. К генетическим маркерам рецидива миомы матки относят полиморфизм D гена GSTP1, нулевой вариант гена GSTT1, нулевой вариант гена GSTM1 Также определяют иммунологические предикторы рецидиве в «ложного» роста узлов - реакцию хронического стресса, наличие гипореактивности, а также предикторы рецидивов «истинного» роста узлов - гиперреактивность, реакция тренировки. Учитывается также факт проведенной комплексной реабилитации.
Затем индивидуальную степень риска рецидива заболевания вычисляют по формуле:
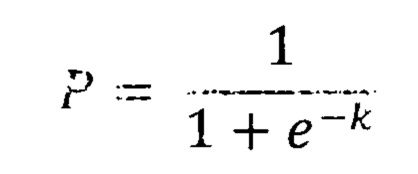
где P - вероятность наступления исхода (рецидива миомы матки), е - основание натурального логарифма, k - сумма константы k20 и коэффициентов регрессии факторов риска, выявленных у данной пациентки. Значения коэффициентов регрессии различных факторов риска указаны в таблице 1.

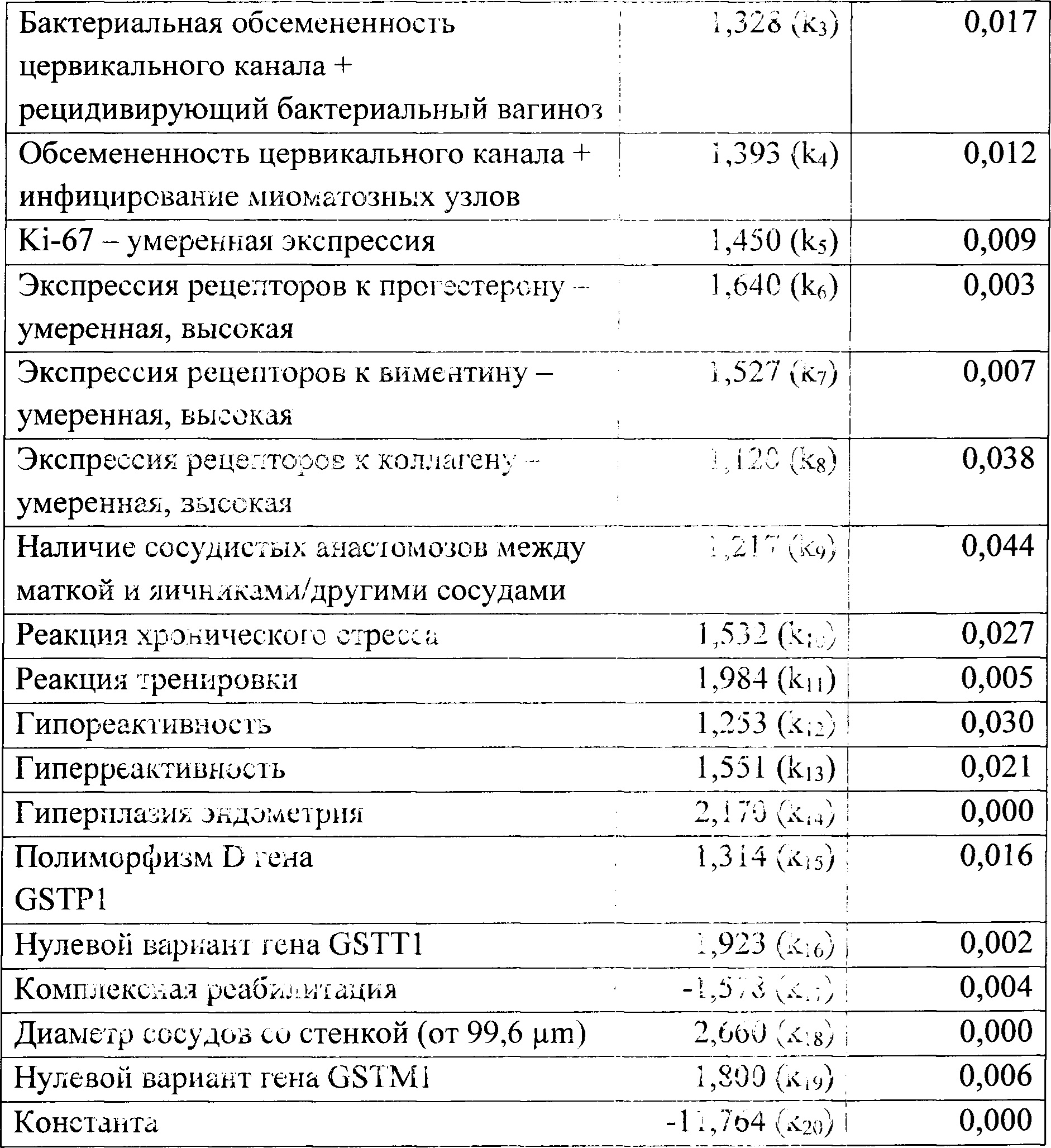
При условии р<0,5 определяют низкий риск рецидива заболевания, и дальнейшая тактика лечения будет включать в себя лапароскопическую миомэктомию и предгравидарную подготовку согласно существующим стандартам оказания медицинской помощи женщинам с миомой матки и аденомиозом. При условии р≥0,5 определяют высокий риск рецидива заболевание и тогда выбирают тактику включающую расширенную предоперационную подготовку - лечение анемии (антианемическая терапия препаратами железа по общепринятым схемам), восстановление нормобиоценоза (пероральные препараты эубиотиков, санация влагалища с последующим курсом вагинальных пробиотиков), коррекцию аномальных адаптационных реакций (лечебная физкультура, физиотерапия, психотерапия), гипо- или гиперреактивности (коррекция иммунологического профиля).
Затем осуществляют повторное обследование пациентки с целью оценки эффективности проведенной терапии и повторный расчет степени риска рецидива миомы матки. При сохраняющемся высоком риске и заинтересованности пациентки в наступлении беременности выбор тактики хирургического доступа делают в пользу лапаротомии, которая позволит удалить все узлы и улучшит прогноз фертильности. При низком же риске рецидива после повторного расчета и незаинтересованности пациентки в беременности оптимальной тактикой будет лапароскопическое удаление клинически значимых узлов
При исследовании удаленных узлов можно выявить такие предикторы рецидива миомы матки, как умеренную экспрессию маркера Ki-67, умеренную или высокую экспрессию рецепторов прогестерона, умеренную или высокую экспрессию виментина, умеренную и высокую экспрессию коллагена IV типа, диаметр сосудов миоматозных узлов со стенкой - более 99,6 μm. Данную информацию используют для дальнейшего расчета риска рецидива миоматозного роста и определения дальнейшей тактики лечения и реабилитации пациентки.
В послеоперационном периоде обеим группам проводят расширенную послеоперационную реабилитацию - противорецидивную гормонотерапию (агонисты гонадотропин-релизинг гормона, диеногестсодержащие препараты), коррекцию аномальной иммунореактивности (дальнейшую коррекцию иммунологического профиля), цитокинового профиля (иммуномодуляторы), восстановительную терапию (метаболический курс, физиотерапия, психотерапия) терапию. Длительность и интенсивность реабилитационных мероприятий зависит от окончательной степени риска рецидива, определенной с учетом всех данных о пациентке. Так, появление в отдаленном послеоперационном периоде такого фактора риска, как гиперпластический процесс эндометрия, так же свидетельствует о высоком риске рецидивирования миоматозного роста, что требует увеличения интенсивности и длительности послеоперационной реабилитации.
Способ апробирован в течение 3-х лет на 100 женщинах с миомой матки, в том числе в сочетании с аденомиозом. Высокий риск рецидива был определен у 38 наблюдаемых, низкий - у 62. Для всех пациенток был проведен индивидуальный подбор тактики лечения (предоперационная подготовка, выбор хирургического доступа, послеоперационная реабилитация) на основании определенной по разработанной модели степени риска. Среди пациенток с высоким риском рецидива миомы матки 49,5% планировали беременность в течение 2 лет после операции, клиническая беременность наступила у 64,3% из них. Среди пациенток с низким риском рецидива планировали беременность 58,4%, в течение 2 лет клиническая беременность была отмечена у 68,4% из них. В течение 5 лет наблюдения в группе с определенным высоким риском рецидива миомы матки появление новых узлов было отмечено у 4,5% наблюдаемых, в группе же с низким риском рецидива - у 5,1%. Разница между группами по таким показателям, как наступление беременности и рецидива миомы матки оказалась статистически незначима (р>0,05).
Пример. Пациентка Г., 39 лет обратилась в клинико-диагностическое отделение с жалобами на постоянное чувство тяжести в низу живота, боль при половом контакте, учащенное мочеиспускание, частые вагиниты. В анамнезе - 4 беременности, из них 2 - срочные роды, без особенностей, 2 - артифициальные аборты в малых сроках, без особенностей. Пациентка беременность в будущем не планировала. При комплексном обследовании были выявлены такие факторы риска рецидива как: множественные узлы (k1=1,219) и признаки аденомиоза по данным УЗИ, анемия умеренной степени тяжести (k2=1,989), бактериальный вагиноз (k3=1,328), полиморфизм D гена GSTP1 (k15=1,314), нулевой вариант гена GSTT1 (k16=1,923), гиперреактивность (k13=1,551), ангиографические признаки множественных анастомозов между маткой и яичниками (k9=1,217), реакция тренировки (k11=1,984), Сумма k1, k2, k3, k10, k15 и константы k20 (-11,764) равна - 0,76]. При вычислении по формуле значение Р было определено равным 0,68.
Согласно существующим нормативным актам в качестве предоперационной подготовки была произведена гистероскопия с биопсией эндометрия, результаты ПГИ - хронический эндометрит умеренной степени активности В предоперационном периоде был проведен курс противовоспалительной терапии (эмпирическая антибактериальная терапия препаратами широкого спектра активности, нестероидные противовоспалительные препараты, санация влагалища суппозиториями с антисептиком с последующим восстановлением нормальной микрофлоры влагалища суппозиториями с пробиотиком), гормонотерапия (2 инъекции агониста гонадотропин-релизинг гормона с интервалом 28 дней), коррекция реакции адаптационного профиля (иммуномодулирующая терапия).
Хирургическое лечение было проведено в объеме лапароскопии, миомэктомии (были удалены 3 узла, диаметр которых превышал 3 см, 2 оставшихся узла - интерстициальные, диаметром 1-1,5 см, что клинически не значимо) с ушиванием стенок матки двухрядным узловым швом монофиламентной нитью. По данным морфометрии ПГИ в срезах ткани удаленных узлов было умеренное количество сосудов, диаметр которых со стенкой превышал 99,6 μm (k18=2,660). По данным ИГХ-исследования узлов были выявлены: умеренная экспрессия рецепторов к прогестерону (k6=1,640) и коллагену (k8=1,120). В послеоперационном периоде была проведена комплексная реабилитация (k17=-1,578) в объеме: метаболическая терапия (препараты магния, меди, цинка, железа, витамина С), гормонотерапия (были продолжены инъекции агонистов гонадотропин-релизинг гормона - до 6 с интервалом 28 дней), коррекция реакции адаптационного профиля (лечебная физкультура, физиотерапия, психотерапия), антианемическая терапия. Повторное исследование иммунологического профиля показало отсутствие гиперреактивности и реакции тренировки.
Таким образом, повторное определение риска рецидива после операции показало следующие результаты: полиморфизм D гена GSTP1 (k15=1,314) нулевой вариант гена GSTT1 (k16=1,923), ангиографические признаки множественных анастомозов между маткой и яичниками (k9=1,217), умеренное количество сосудов, диаметр которых со стенкой превышал 99.6 μm (k18=2,660), умеренная экспрессия рецепторов к прогестерону (k6=1,640) и коллагену (k8=1,120), проведенная комплексная реабилитация (k17=-1,578). Сумма данных факторов с константой k20 составила - -3,468. При вычислении по формуле значение Р было определено равным 0,03.
По окончании гормонотерапии был рекомендован прием комбинированных оральных контрацептивов, содержащих диеногест, длительно. При ежегодных контрольных осмотрах в течение 5 лет после операции был обнаружен умеренный регресс (уменьшение объема до 50% от первоначального) оставшихся двух миоматозных узлов, признаков роста новых узлов не отмечено Пациентка также отметила значительное уменьшение выраженности исходных симптомов после комплексного лечения, вплоть до полного их исчезновения через 1 год после операции.
Пример. Пациентка С., 27 лет обратилась в клинико-диагностическое отделение с жалобами на отсутствие беременности в браке, обильные и болезненные менструации, боль при половом контакте. В анамнезе - 1 беременность, артифициальный аборт в малых сроках, без осложнений. Миома матки была впервые обнаружена 1 год назад, рост узла за этот период составил 50% от первоначального. При комплексном обследовании были выявлены такие факторы риска рецидива, как: анемия умеренной степени тяжести (k2=1,989), бактериальный вагиноз (k3=1,328), наличие активного кровотока в узле (множественные сосудистые анастомозы) (k9=1,217), признаки аденомиоза по данным УЗИ, реакция тренировки (k11=1,984), нулевой вариант гена GSTM1 (k19=1,800). Сумма коэффициентов регрессии данных факторов риска и константы k20 составила - -3,446. При вычислении по формуле значение Р было определено равным 0,03.
Согласно существующим нормативным актам в качестве предоперационной подготовки была произведена гистероскопия с биопсией эндометрия, результаты ПГИ - хронический эндометрит слабой степени активности. В предоперационном периоде был проведен курс противовоспалительной терапии (эмпирическая антибактериальная терапия препаратами широкого спектра активности, нестероидные противовоспалительные препараты, санация влагалища суппозиториями с антисептиком с последующим восстановлением нормальной микрофлоры влагалища суппозиториями с пробиотиком), коррекция адаптационного профиля (k17=-1,578).
Хирургическое лечение было проведено в объеме лапароскопии, миомэктомии с ушиванием стенок матки двухрядным непрерывным швом самофиксирующейся нитью. По данным ИГХ узлов были выявлены: умеренная экспрессия маркера пролиферации Ki-67 (k5=1,450).
Таким образом, повторное определение риска рецидива после операции показало следующие результаты: нулевой вариант гена GSTM1 (k17=1,800), ангиографические признаки множественных анастомозов между маткой и яичниками (k9=1,217), умеренная экспрессия маркера пролиферации Ki-67 (k5=1,450), проведенная комплексная реабилитация (k17=-1,578). Сумма данных факторов с константой k20 составила - -8,875. При вычислении по формуле значение Р было определено равным 0,0001.
В связи с чем пациентке была рекомендована контрацепция комбинированными оральными контрацептивами в течение 6 месяцев, с параллельной предгравидарной подготовкой (прием препаратов фолиевой кислоты, железа, йода), после чего - планирование беременности. Беременность наступила самостоятельно через 5 месяцев планирования, завершилась срочными родами живым плодом. При ежегодных контрольных осмотрах в течение 5 лет после операции признаков рецидива миоматозного роста не отмечено. Пациентка отмечала полное купирование исходных симптомов после комплексного лечения.