Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ И МЕТИЛАКРИЛАТА
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к катализу с использованием твердых кислот и в частности к способу получения акриловой кислоты и метилакрилата с использованием в качестве исходного вещества реакции диметоксиметана и оксида углерода (II).
УРОВЕНЬ ТЕХНИКИ
Акриловая кислота является простейшим представителем непредельных карбоновых кислот. Акриловая кислота высокой чистоты обладает характерным резким запахом и крайне коррозионно-активна. Являясь важным химическим сырьем, она широко используется в синтезе различных соединений и производстве смол. В современном мире отрасль производства акриловой кислоты и акрилатов остается важной частью нефтехимической промышленности.
Способы синтеза акриловой кислоты в основном включают 1) этиленхлоргидриновый способ: сначала этиленхлоргидрин и цианид натрия используются в качестве исходных реактивов для получения 3-гидроксипропаннитрила в присутствии основного катализатора, затем 3-гидроксипропаннитрил дегидратируют в присутствии серной кислоты с образованием акрилонитрила, который затем подвергается гидролизу или алкоголизу с образованием акриловой кислоты или акрилата; 2) гидроксипропаннитрильный способ: этот способ разработан на основе этиленхлоргидринового за той разницей, что синтез 3-гидроксипропаннитрила происходит иначе с помощью реакции раскрытия кольца окиси этилена под действием синильной кислоты; 3) способ Реппе под высоким давлением и модифицированный способ Реппе: акриловую кислоту для этерификации получают при взаимодействии ацетилена, оксида углерода (II) и воды с использованием в качестве катализатора никелевой или медной соли, а затем подвергают реакции этерификации с различными спиртами для получения акрилатов; 4) кетеновый способ: кетен (полученный из ацетона и уксусной кислоты) реагирует с безводным формальдегидом с образованием β-пропиолактона, который затем изомеризуется при контакте с горячей фосфорной кислотой с образованием акриловой кислоты; 5) способ с использованием формальдегида и уксусной кислоты: реакция альдольной конденсации формальдегида с уксусной кислотой проводится для синтеза акриловой кислоты напрямую; 6) способ гидролиза алкилнитритов; 7) этиленовый способ: реакция окислительного карбонилирования этилена оксидом углерода (II) и кислородом в присутствии благородного металла в качестве катализатора проводится для синтеза акриловой кислоты; 8) способ прямого окисления пропилена: подразделяется на одноступенчатый и двухступенчатый, при этом на первой ступени двухступенчатого способа пропилен окисляется с образованием акролеина, а на второй ступени акролеин окисляют дальше с образованием акриловой кислоты; 9) способ окисления пропана: пропан используется как исходное вещество, в качестве катализатора используется оксид металла, и пропан напрямую окисляется с образованием акриловой кислоты; 10) этиленоксидный метод: присоединение оксида углерода (II) к окиси этилена напрямую с получением акриловой кислоты, то есть реакция карбонилирования окиси этилена. Среди упомянутых выше 10 способов получения акриловой кислоты этиленхлоргидриновый, гидроксипропаннитрильный, кетеновый способы и способ Реппе постепенно были исключены из-за высокой стоимости производства при низкой производительности и высокой токсичности. Что касается способов с использованием этилена, пропана и этиленоксида, как стабильность и селективность катализатора, так и процесс катализа еще не продуманы до конца, и на данный момент не сообщалось о крупномасштабном производстве. На сегодняшний день в мире единственным способом крупномасштабного производства акриловой кислоты является способ окисления пропилена.
Способ окисления пропилена был впервые использован компанией UCC в 1969 году в Соединенных Штатах для создания первого производственного комплекса, после чего были успешно созданы производственные агрегаты для получения акриловой кислоты окислением пропилена японскими компаниями Nippon Shokubai Kagaku Kogyo (MCC) в 1970 году, Mitsubishi Chemical Corporation (NSKK) в 1973 году и американской компанией Celanese в 1973 году. В настоящее время все мировые компании, владеющие производственными процессами для получения акриловой кислоты окислением пропилена, используют процесс двухступенчатого окисления.
Следовательно, большое значение имеет разработка способа синтеза, допускающего получение акриловой кислоты и метилакрилата из недорогого сырья с высокой степенью конверсии и селективностью.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задачей настоящей заявки является обеспечение способа получения акриловой кислоты и метилакрилата, в котором в качестве исходных веществ используют недорогие диметоксиметан (ДММ) и оксид углерода (II), и в качестве катализатора - твердая кислота, для получения акриловой кислоты и метилакрилата с высокой селективностью.
В данном способе исходный газ, содержащий диметоксиметан и оксид углерода (II), пропускают через реактор, заполненный катализатором на основе молекулярного сита, для проведения реакции получения акриловой кислоты в качестве основного продукта, а также метилакрилата, метилацетата и уксусной кислоты. После разделения получают, соответственно, уксусную кислоту, метилацетат, акриловую кислоту и метилакрилат.
Согласно некоторым предпочтительным вариантам реализации данного изобретения реакцию проводят при температуре реакции от 180°С до 400°С, при давлении от 0,1 МПа до 15,0 МПа, объемно-массовая скорость подачи диметоксиметана в исходном газе составляет от 0,05 ч-1 до 10,0 ч-1, а объемный процент диметоксиметана в исходном газе составляет от 0,1% до 95%.
В настоящей заявке процесс реакции диметоксиметана с оксидом углерода (II) с образованием уксусной кислоты, метилацетата, акриловой кислоты и метилакрилата проходит следующим образом:
1) диметоксиметан реагирует с протонной кислотой, образованной твердой кислотой (в порах молекулярного сита), с образованием в результате хемосорбции соединения твердой кислоты (молекулярного сита) и метоксиметила, а также с одновременным образованием метанола;
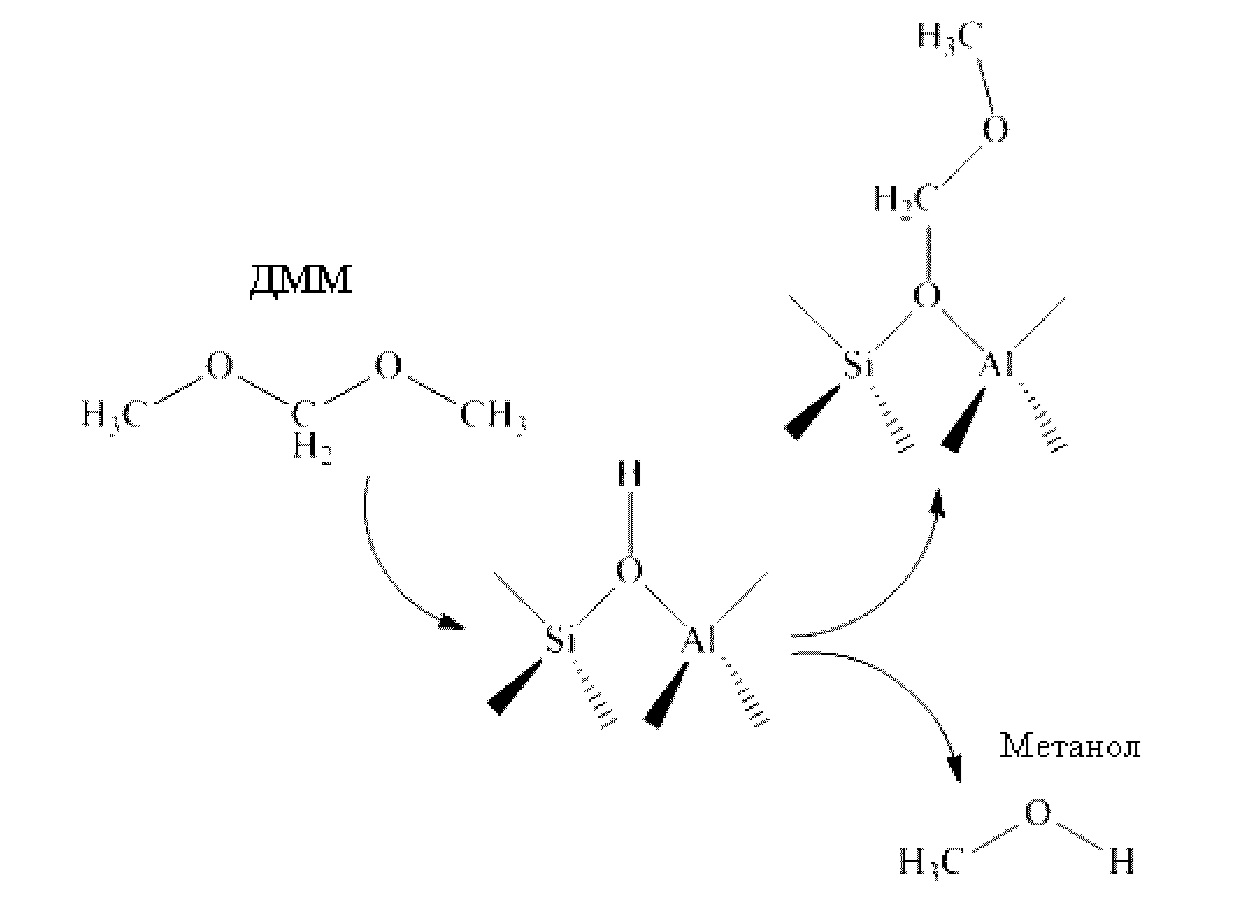
2) образовавшийся метанол реагирует с избытком протонной кислоты, образованной твердой кислотой (в порах молекулярного сита), с образованием в результате хемосорбции соединения твердой кислоты с метилом и воды;
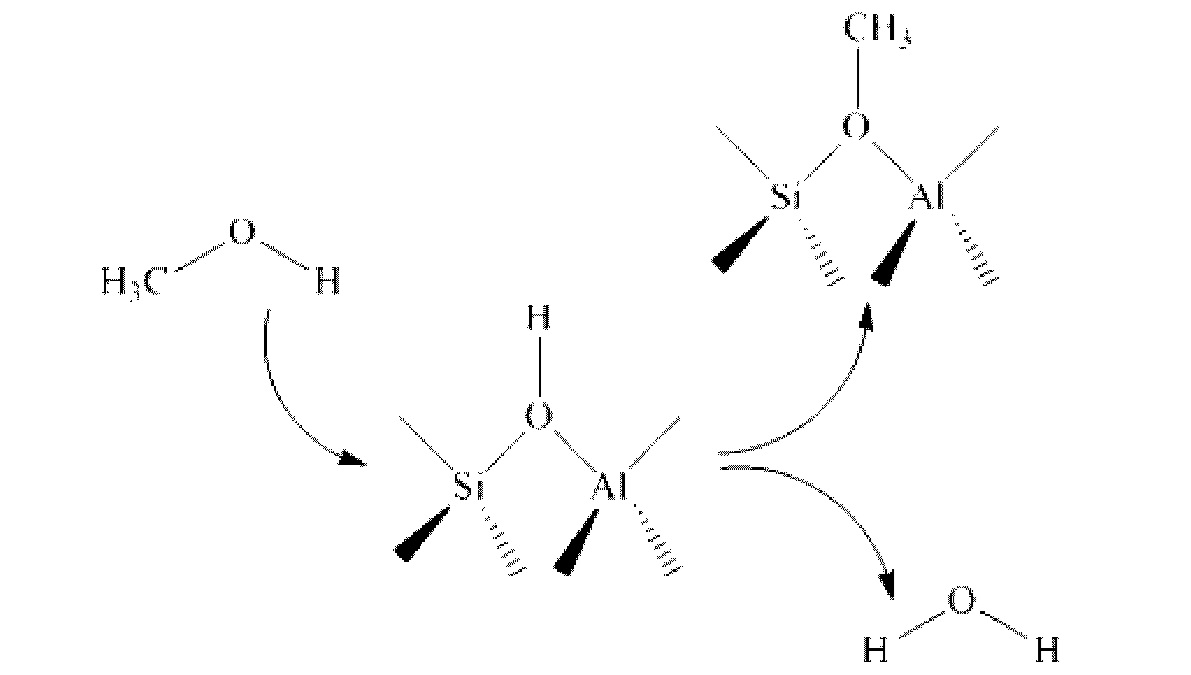
3) СО может напрямую встраиваться в адсорбированную на твердой кислоте (молекулярном сите) метоксиметильную группу с образованием метоксиацетильной группы;
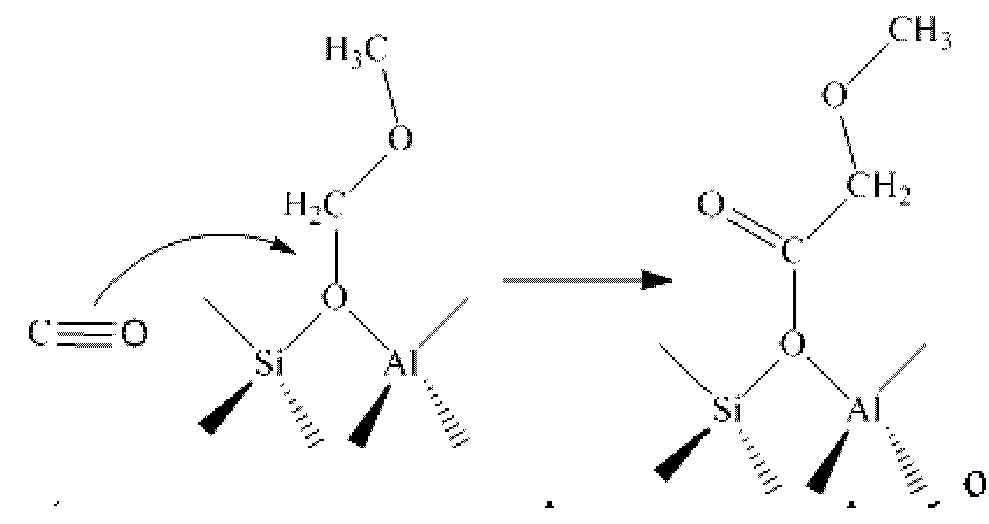 в адсорбированную на твердой кислоте (молекулярном сите) метальную группу с образованием ацетильной группы;
в адсорбированную на твердой кислоте (молекулярном сите) метальную группу с образованием ацетильной группы;
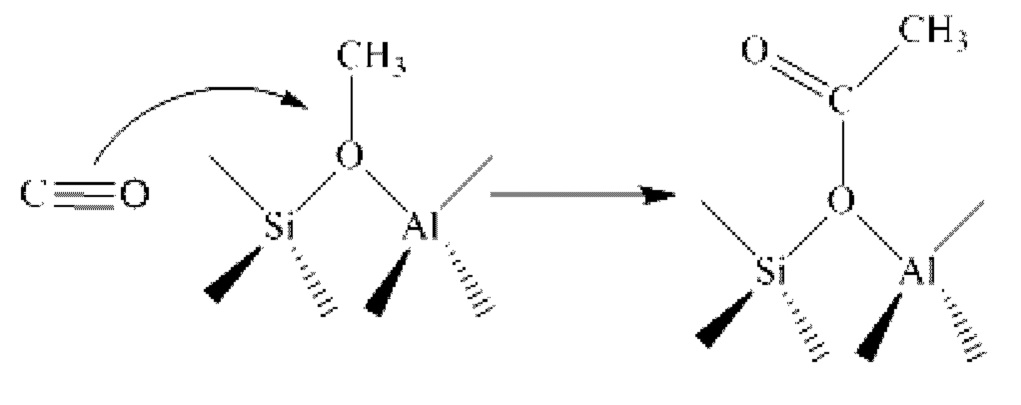
5) адсорбированная на твердой кислоте (молекулярном сите) метоксиметильная группа может подвергаться реакции диспропорционирования с диметоксиметаном с образованием адсорбированной на молекулярном сите диметоксиметильной группы и диметилового эфира;
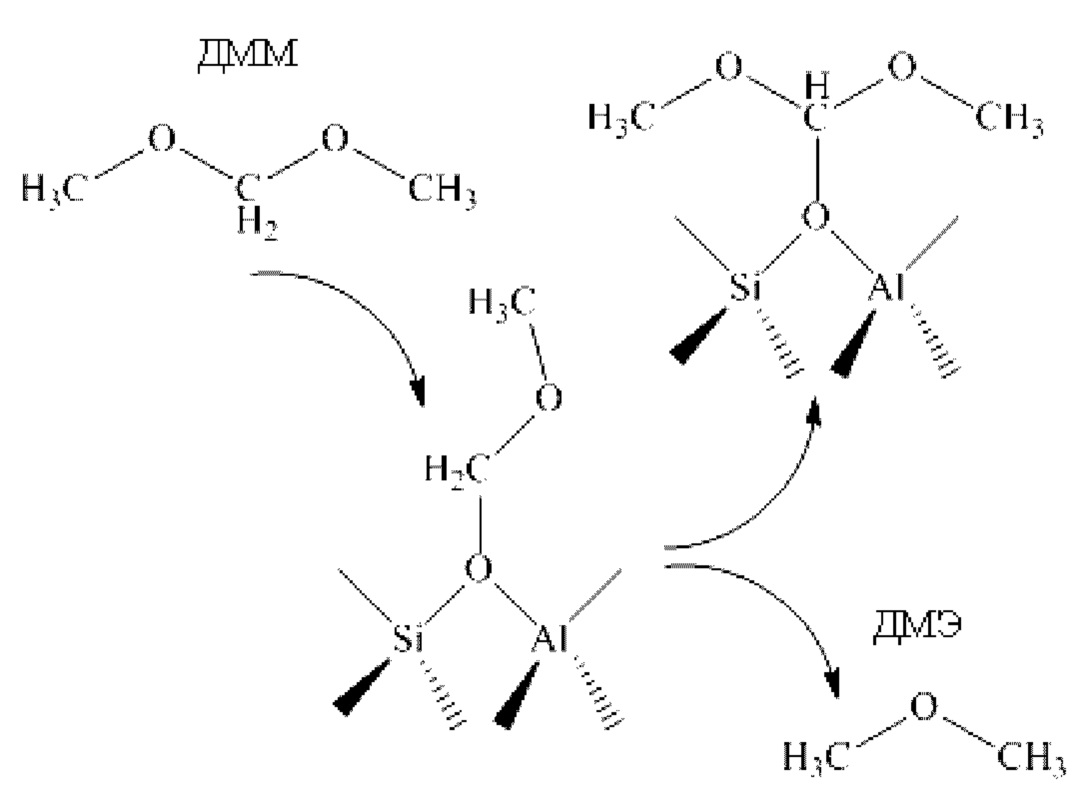
6) адсорбированная на твердой кислоте (молекулярном сите) диметоксиметильная группа может образовывать под действием воды диметиловый эфир, формальдегид и свободную твердую кислоту (молекулярное сито) с кислотной группой;
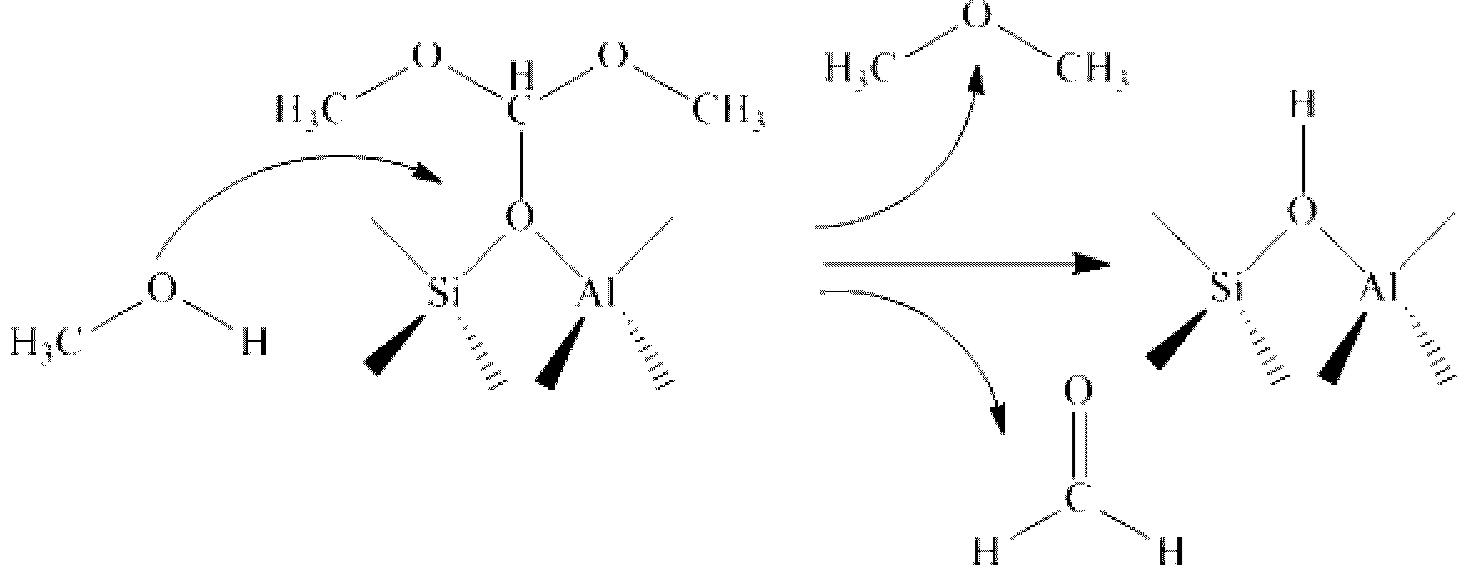
7) адсорбированная на твердой кислоте (молекулярном сите) метоксиацетильная группа может вступать в реакцию этерификации с диметилоксиметаном с образованием метилметоксиацетата и адсорбированной на молекулярном сите метоксиметильной группы; также адсорбированная на твердой кислоте (молекулярном сите) метоксиацетильная группа может вступать в реакцию этерификации с диметиловым эфиром с образованием метилметоксиацетата и адсорбированной на молекулярном сите метокси группы; в то же время адсорбированная на молекулярном сите метоксиацетильная группа также может реагировать с водой с образованием метоксиуксусной кислоты и свободной твердой кислоты (молекулярного сита) с кислотной группой (последние две реакции протекают по схожему механизму и не могут проходить в отдельности друг от друга);
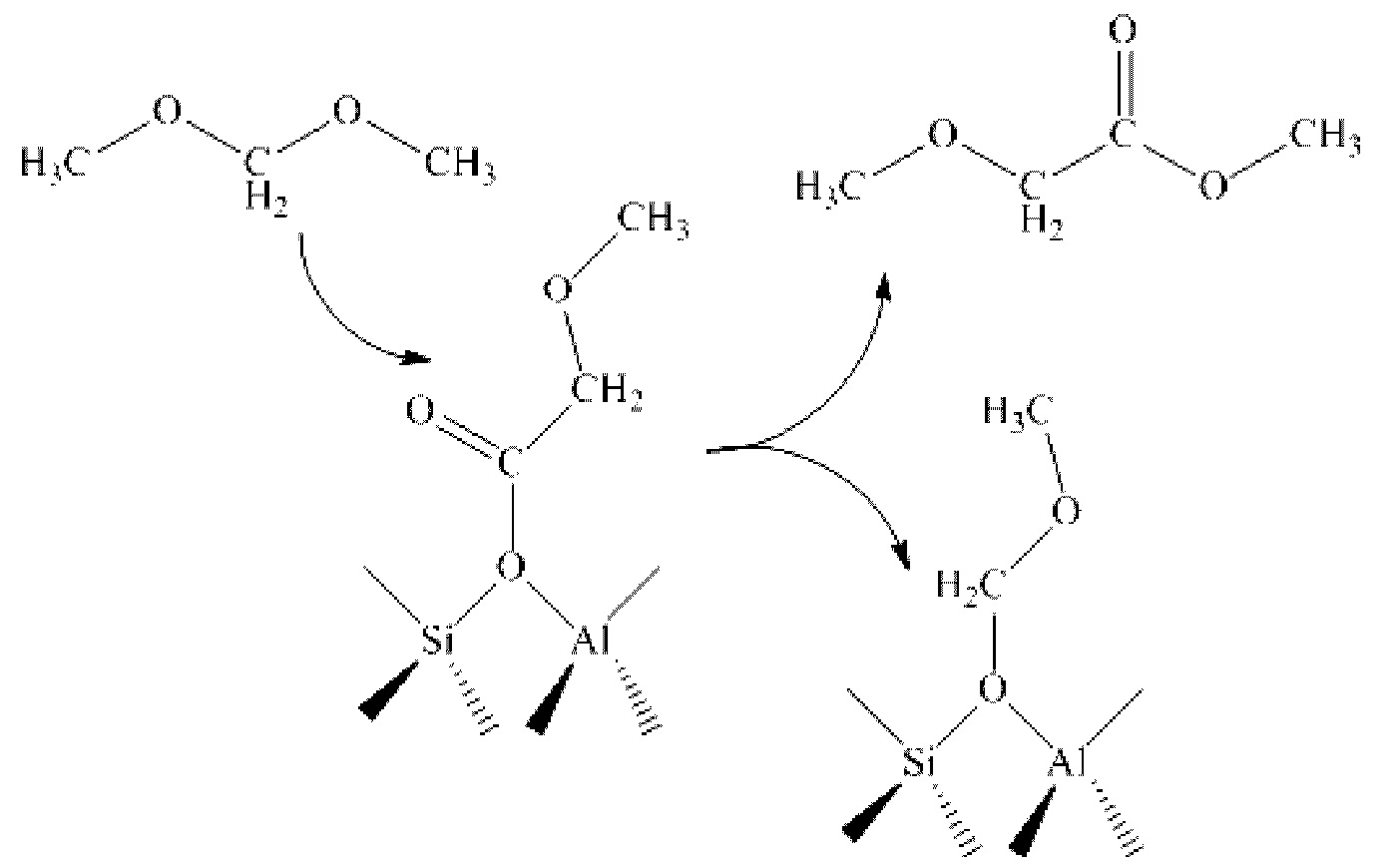
подобным образом
В) адсорбированная на твердой кислоте (молекулярном сите) метильная группа может вступать в реакцию этерификации с диметиловым эфиром с образованием метилацетата и адсорбированной на молекулярном сите метоксигруппы; также адсорбированная на твердой кислоте (молекулярном сите) метильная группа может вступать в реакцию этерификации с диметилоксиметаном с образованием метилацетата и адсорбированной на молекулярном сите метокси метальной группы; в то же время адсорбированная на молекулярном сите ацетильная группа также может реагировать с водой или метиловым спиртом с образованием уксусной кислоты и свободной кислотной группы молекулярного сита или адсорбированных метильных групп соответственно (последние две реакции протекают по схожему механизму и не могут проходить в отдельности друг от друга);
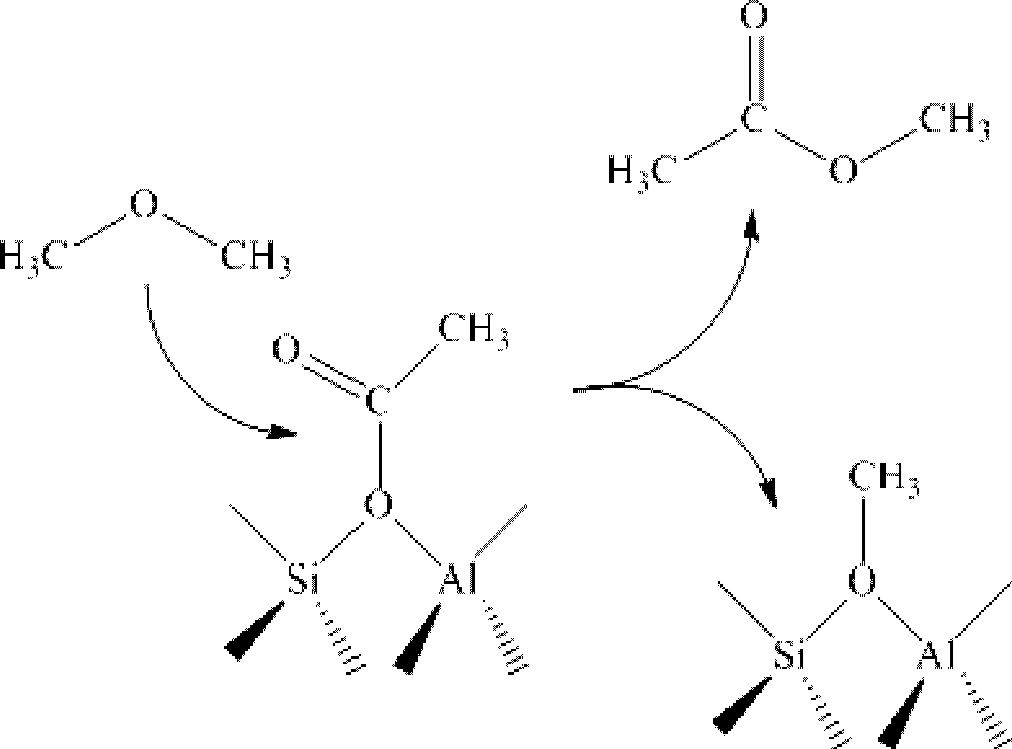
9) образовавшиеся уксусная кислота или метилацетат могут подвергаться реакции альдольной конденсации с формальдегидом с образованием акриловой кислоты и метилакрилата.
Согласно приведенным выше механизмам реакции, посредством термодинамических и кинетических факторов, включающих управление различными условиями температуры и давления реакции, а также различное соотношение состава сырья, возможно направленное получение продуктов таким образом, что они могут быть произведены в соответствие со следующим уравнением. В идеальных условиях среди продуктов общая селективность акриловой кислоты по углероду составляет 60%, а общая селективность уксусной кислоты по углероду - 40% без образования других побочных продуктов. Если селективность продукта рассчитать по диметоксиметану в качестве сырья одностадийной реакции, селективность акриловой кислоты по углероду составляет 50%, и селективность уксусной кислоты по углероду - 50%.
С3Н8О2(диметоксиметан) + 2СО = С3Н4О2(акриловая кислота) + С2Н4О2(уксусная кислота)
В фактических реакциях метилакрилат и метилацетат частично образуются в качестве продуктов в связи с неполным гидролизом метилацетата.
Среди продуктов реакции массовая доля акриловой кислоты составляет от 0,1% до 70%, массовая доля метилакрилата варьирует от 0,1% до 30%, массовая доля уксусной кислоты составляет от 0,1% до 60%, и массовая доля метилакрилата составляет от 0,1% до 40%.
Катализатором в виде молекулярного сита может быть один или более из группы, состоящей из молекулярного сита ZSM-35, молекулярного сита ZSM-5, MOR морденитного молекулярного сита и молекулярного сита ЕМТ.
Эфиры, которые получаются в ходе этого способа, могут затем быть гидролизованы с образованием соответствующих карбоновых кислот, включая гидролиз метилакрилата с образованием соответствующей акриловой кислоты и гидролиз метилацетата с образованием соответствующей уксусной кислоты.
Эфиры и карбоновые кислоты, получаемые данным способом, могут затем быть гидрированы с образованием соответствующих спиртов, включая гидрирование метилакрилата и акриловой кислоты с образованием, соответственно, пропанола и гидрирование метилацетата и уксусной кислоты с образованием, соответственно, этанола.
Предпочтительное атомное соотношение кремния к алюминию в катализаторе на основе молекулярного сита составляет от 3 до 100 (Si/Al).
Предпочтительное атомное соотношение кремния к алюминию в молекулярном сите ZSM-35 составляет от 20 до 50 (Si/Al).
Предпочтительное атомное соотношение кремния к алюминию в молекулярном сите ZSM-5 составляет от 20 до 60 (Si/Al).
Предпочтительное атомное соотношение кремния к алюминию в мордените составляет от 10 до 30 (Si/Al).
Предпочтительное атомное соотношение кремния к алюминию в цеолите ЕМТ составляет от 5 до 20 (Si/Al).
Молекулярное сито может быть получено тепловой обработкой, гидротермальным синтезом, обработкой неорганическими кислотами, обработкой органическими кислотами, обработкой фтором и хелатной обработкой или газо-адсорбционной деалюминизацией и обогащением кремнием.
Молекулярные сита различной топологии содержат один или большее количество металлов из группы, состоящей из галлия, железа, меди или серебра; способы внедрения могут включать синтез in situ, ионный обмен металлов или внедрение импрегнацией; содержание металла составляет от 0,01% масс. до 10,0% масс. от общей массы катализатора в пересчете на элементарный металл.
Предпочтительное содержание металла составляет от 0,05% масс. до 1,0% масс. от общей массы катализатора.
Молекулярные сита-катализаторы различной топологии содержат связующее, связующим может быть одно любое или большее количество веществ, выбранное из группы, состоящей из алюминия оксида, кремния диоксида и магния оксида, при этом содержание связующего составляет от 0% масс. до 70% масс. от общей массы катализатора.
Предпочтительная температура реакции составляет от 220°С до 300°С.
Предпочтительное давление в ходе реакции составляет от 5 МПа до 10 МПа.
Предпочтительная объемно-массовая скорость подачи диметоксиметана в исходном газе составляет от 0,3 ч-1 до 2,0 ч-1.
Предпочтительное содержание диметоксиметана в исходном сырье составляет от 0,5% до 30%.
Исходный газ включает диметоксиметан, оксид углерода (II), водород и инертный газ, при этом объемное содержание оксида углерода (II) составляет от 50% до 95%, объемное содержание водорода составляет от 0% до 50%, а объемное содержание инертного газа составляет от 0% до 50%. Инертный газ содержит любое одно или более веществ, выбранных из группы, состоящей из азота, гелия, аргона, углерода диоксида, метала и этана.
В качестве реактора может выступать реактор с неподвижным слоем, реактор с псевдоожиженным слоем или корпусной реактор.
Положительные эффекты, которые могут быть достигнуты при помощи настоящей заявки, включают:
1) Согласно способу, предложенному в настоящей заявке, акриловую кислоту
и метилакрилат синтезируют с высокой селективностью из недорогого диметоксиметана и оксида углерода (II) в качестве исходного сырья, при этом побочными продуктами являются метилацетат и уксусная кислота.
2) Согласно способу, предложенному в настоящей заявке,
продуктами реакции являются уксусная кислота, метилацетат, акриловая кислота и метилакрилат, и эти четыре продукта легко разделяют при нормальном давлении благодаря большой разнице в температуре кипения, так что акриловая кислота и метилакрилат с высокой добавленной стоимостью могут быть получены с низкими энергозатратами и низкой ценой.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
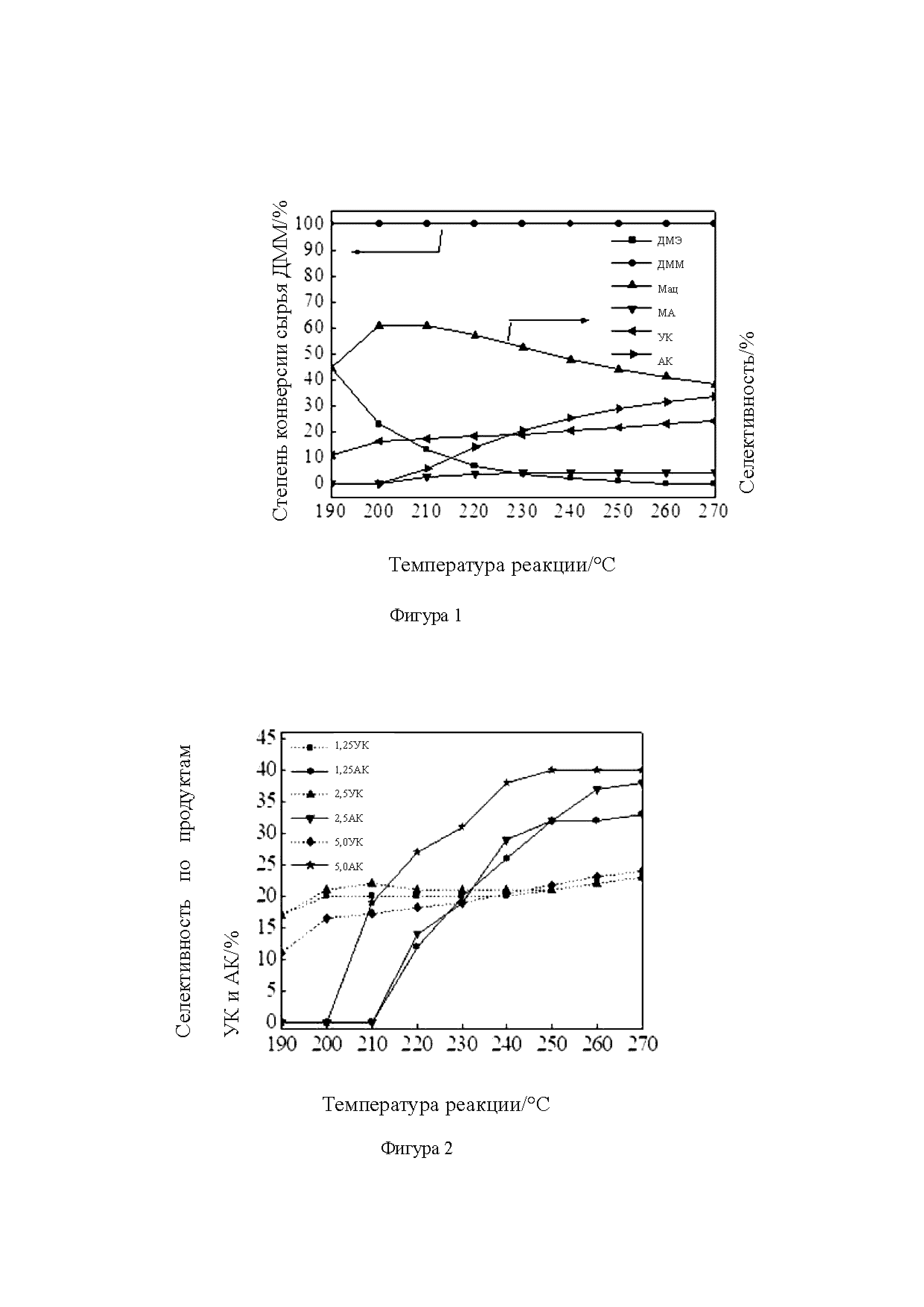
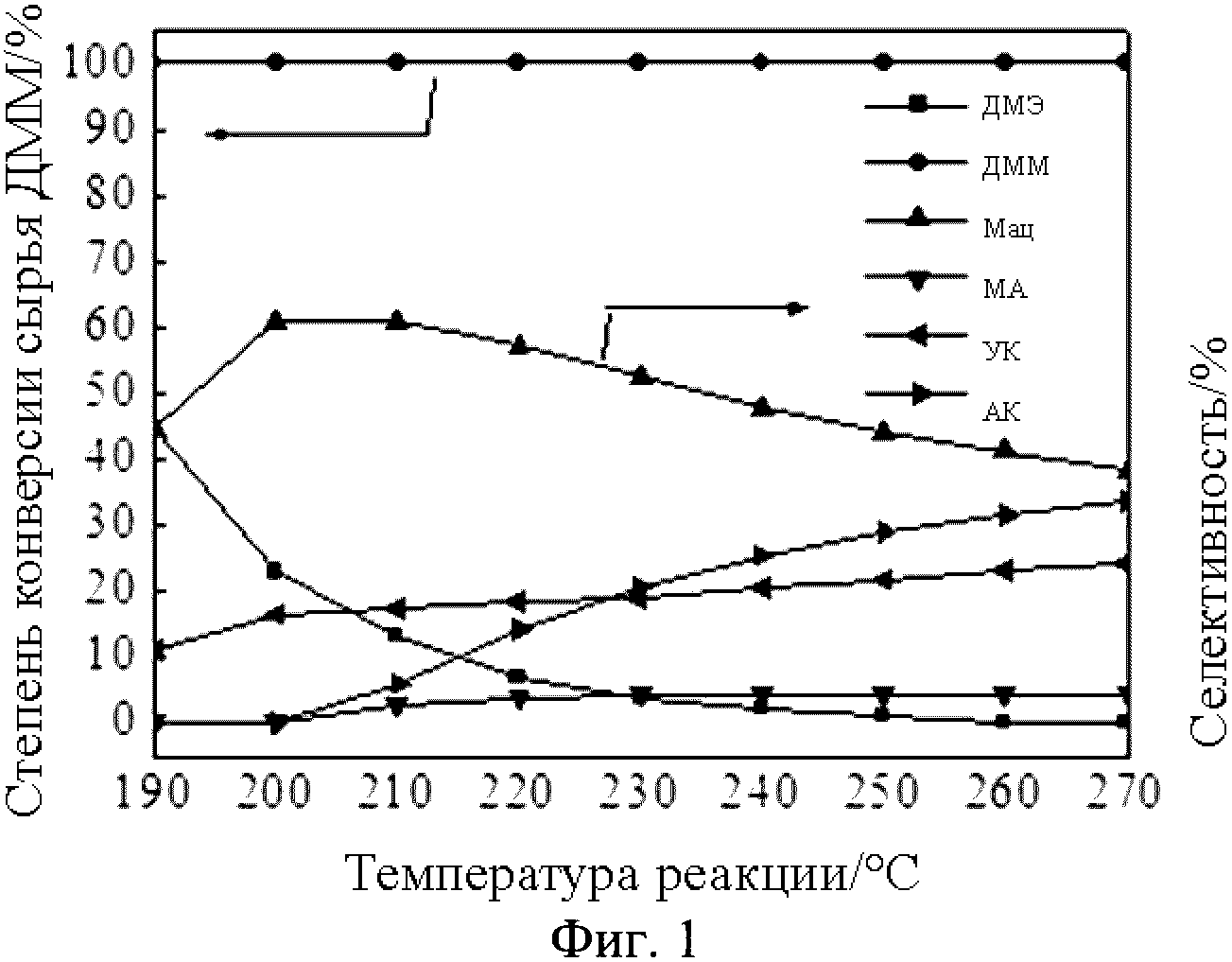
Фигура 1 представляет собой график, показывающий коэффициент конверсии исходного вещества диметоксиметана (ДММ) и селективности продуктов в зависимости от температуры при общем давлении 5,0 МПа, парциальном давлении оксида углерода (II) 2,5 МПа и парциальном давлении ДММ 1,25×10-2 МПа на молекулярном сите H-MOR в Примере 1.
Фигура 2 представляет собой график, показывающий отношение между общим давлением реакции и селективностью продуктов уксусной кислоты и акриловой кислоты как функцию от температуры реакции на молекулярном сите H-MOR в Примере 3.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТА РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
Настоящая заявка будет описана далее на приведенных ниже примерах. Следует понимать, что приведенные ниже примеры являются исключительно иллюстративными и не ограничивают настоящее изобретение каким-либо образом.
Все исходные вещества и катализаторы в примерах к настоящей заявке были заказаны коммерческим образом, если не указано иное.
Методы анализа в примерах к настоящей заявке следующие:
Исходные вещества и продукты реакции были проанализированы на газовом хроматографе Agilent 7890А производства компании Agilent с использованием капиллярной колонки FFAP производства Agilent.
Согласно варианту реализации настоящей заявки использовался реактор с неподвижным слоем, масса загрузки катализатора находилась в пределах от 0,5 до 3,0 г, температура реакции находилась в пределах от 180°С до 350°С, а давление реакции находилось в пределах от 0,1 МПа до 10 МПа. Исходное вещество диметоксиметан загружали в реактор двумя путями подачи:
В первом варианте оксид углерода (II) переносил насыщенный пар диметоксиметана при различных температурах водяной бани (от 0°С до 50°С) в реактор с неподвижным слоем, чтобы получить исходный газ с различным объемным содержанием диметоксиметана. Способ расчета давления насыщенного пара сырья диметилового эфира этиленгликоля при различных температурных условиях показан в Формуле II:
ln(p1*/p2*)=-ΔvapHm ΔVарН/8.3145×(1/T1-1/T2) Формула II
где p1* and р2* давление насыщенного пара диметоксиметана при различной температуре (T1, Т2) соответственно. Известно, что диметоксиметан имеет молярную удельную теплоту парообразования и конденсации ΔvapHm 43.99 кДж/моль и температуру кипения 42,3°С, таким образом может быть рассчитано давление насыщенного пара диметоксиметана при любой температуре. Количество субстанции исходного сырья диметоксиметана, поступающего в реактор за единицу времени, может быть рассчитано исходя из давления насыщенного пара.
Во втором варианте, жидкое сырье диметоксиметана напрямую закачивали в реактор с неподвижным слоем с помощью насоса с постоянным расходом при объемной скорости потока от 0,1 мл/мин до 10 мл/мин. При этом варианте объемное содержание диметоксиметана в исходном газе, входящем в реактор для контакта с катализатором составляло от 0,1% до 100%.
Коэффициент конверсии и селективность в примерах к настоящей заявке рассчитываются следующим образом:
Степень конверсии диметоксиметана = [(количество моль диметоксиметана в исходном сырье) - (количество моль диметоксиметана в выгрузке)] ÷ (количество моль диметоксиметана в исходном сырье)×(100%)
Селективность по акриловой кислоте = 2/3 [(количество моль углерода в акриловой кислоте в выгрузке) ÷ (количество моль углерода в диметоксиметане в исходном сырье)] - (количество моль углерода в диметоксиметане в выгрузке)×(100%)
Селективность по метилакрилату = 3/4 [(количество моль углерода в метилакрилате в выгрузке) ÷ (количество моль углерода в диметоксиметане в исходном сырье)] - (количество моль углерода в диметоксиметане в выгрузке)×(100%)
Селективность по уксусной кислоте=1/2 [(количество моль углерода в уксусной кислоте в выгрузке) ÷ (количество моль углерода в диметоксиметане в исходном сырье)] - (количество моль углерода в диметоксиметане в выгрузке)×(100%)
Селективность по метилацетату = 2/3 [(количество моль углерода в метилацетате в выгрузке) ÷ (количество моль углерода в диметоксиметане в исходном сырье)] - (количество моль углерода в диметоксиметане в выгрузке)×(100%)
Приготовление катализатора
Н-морденитный катализатор
По 100 г молекулярных сит на основе кальцинированного Na-морденитного цеолита с молярной долей атомов алюминия 5, 6,5, 25 и 50 соответственно, трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали, обжигали при 550°С в течение 4 часов и подвергали экструзии, чтобы получить катализаторы с размером гранул 20-40 меш.
Ga-морденитный катализатор
100 г молекулярных сит на основе кальцинированного галлий-содержащего Na-морденитного цеолита (атомное соотношение кремния к алюминию 5) трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали, обжигали при 550°С в течение 4 часов и подвергали экструзии, чтобы получить катализаторы с размером гранул 20-40 меш.
Fe-морденитный катализатор
100 г молекулярных сит на основе кальцинированного железосодержащего Na-морденитного цеолита (атомное соотношение кремния к алюминию 6,5) трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали, обжигали при 550°С в течение 4 часов и подвергали экструзии, чтобы получить катализаторы с размером гранул 20-40 меш.
Н-морденитный катализатор, импрегнированный металлами
Катализатор, содержащий нанесенные металлы готовили способом ипрегнации равными объемами. Каждую навеску 4,32 г Fe(NO3)3, 4,32 г Сu(МО3)2⋅3Н2O и 3,04 г AgNO3⋅3H2O растворяли в 18 мл деионизированной воды для приготовления водных растворов соответствующих нитратов. 20 г молекулярных сит на основе Н-морденитного цеолита с соотношением кремний-алюминий, равным 25, помещали в водный раствор железа нитрата и оставляли на 24 часа. Полученный образец высушивали в печи при 120°С в течение 12 часов. После сушки образец помещали в муфельную печь, нагревали до 550°С с шагом 2°С в минуту и затем обжигали в течение 4 часов для получения катализатора.
Металл-морденитный катализатор, полученный ионным обменом
20 г Н-морденита и 300 мл водного раствора железа нитрата (0,15 моль) помещали в колбу и перемешивали при охлаждении и нагревании с обратным холодильником при 80°С в течение 2 часов, при этом соотношение твердая фаза-жидкость составило 1:15. Получившийся продукт разделяли фильтрацией, промывали деионизированной водой, повторяли перечисленные выше шаги дважды и высушивали при 120°С в течение 12 часов. После сушки образец помещали в муфельную печь, нагревали до 550°С с шагом 2°С в минуту и затем обжигали в течение 4 часов для получения катализатора.
Формование Н-морденитного катализатора
80 г Na-морденита с атомным соотношением кремния к алюминию 6,5, 28 г псевдобемита и 10% разведенную азотную кислоту смешивали до однородности и формовали экструзией, затем обжигали, трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали и обжигали при 550°С в течение 4 часов, чтобы получить катализатор.
80 г Na-морденита с атомным соотношением кремния к алюминию 4, 20 г оксида магния и 10% разведенную азотную кислоту смешивали до однородности и формовали экструзией, затем обжигали, трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали и обжигали при 550°С в течение 4 часов, чтобы получить катализатор.
80 г Na-морденита с атомным соотношением кремния к алюминию 4,50 г тонкоодисперсного осажденного диоксида кремния и 10% разведенную азотную кислоту смешивали до однородности и формовали экструзией, затем обжигали, трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали и обжигали при 550°С в течение 4 часов, чтобы получить катализатор.
Катализатор H-ZSM-35
По 100 г кальцинированных молекулярных сит Na-ZSM-35 с атомным соотношением кремния к алюминию 20, 35 и 50 соответственно, трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали, обжигали при 550°С в течение 4 часов и подвергали экструзии, чтобы получить катализаторы с размером гранул 20-40 меш.
Катализатор H-ZSM-5
По 100 г кальцинированных молекулярных сит Na-ZSM-5 с атомным соотношением кремния к алюминию 20, 40 и 60 соответственно, трижды подвергали реакции обмена с раствором нитрата аммония концентрации 0,5 моль/л (по 2 часа каждый раз), промывали деионизированной водой, высушивали, обжигали при 550°С в течение 4 часов и подвергали экструзии, чтобы получить катализаторы с размером гранул 20-40 меш.
Катализатор Н-ЕМТ
Синтетические молекулярные сита Н-ЕМТ с атомным соотношением кремния к алюминию 5, 10 и 20 соответственно, подвергали экструзии, чтобы получить катализаторы с размером гранул 20-40 меш.
Пример 1
Молекулярное сито H-MOR с соотношением кремния к алюминию Si/Al=6,5 таблетировали под давлением 40 МПа и дробили на гранулы 20-40 меш для получения катализатора. 0,4 г катализатора загрузили в реактор с неподвижным слоем для предварительной подготовки. Условия предварительной подготовки катализатора были следующими: объемная скорость потока N2 составила 30 мл/мин, а температуру поднимали от 25°С до 500°С за 150 минут и поддерживали на значении 500°С в течение 180 минут.
Реакционный газ состоял из трех потоков и обеспечивалась общая объемная скорость потока 100 мл/мин. Сырьевой материал диметоксиметана вносили в реактор посредством монооксида углерода с объемной скоростью потока 10 мл/мин при температуре водяной бани 30°С; объемная скорость потока другого потока чистого монооксида углерода составили 0 мл/мин, 10 мл/мин, 40 мл/мин и 90 мл/мин соответственно; объемная скорость третьего потока азота составила 90 мл/мин, 80 мл/мин, 50 мл/мин и 0 мл/мин соответственно. Общее давление в ходе реакции составило 5,0 МПа. Температуру реакции поддерживали на уровне 190°С на протяжении 300 минут, а затем увеличивали до 200°С за 5 минут, поддерживали на 200°С в течение еще 300 минут, а затем увеличивали до 210°С за 5 минут. Согласно описанному выше правилу, температуру поднимали вплоть до 270°С с шагом в 10°С, удерживая на 300 минут на каждом уровне. Парциальное давление сырьевого материала диметоксиметана составило около 1.25×10-2 МПа (0,0125 атм), а общее парциальное давление монооксида углерода составило приблизительно 0,5, 1,0, 2,5 и 5,0 МПа.
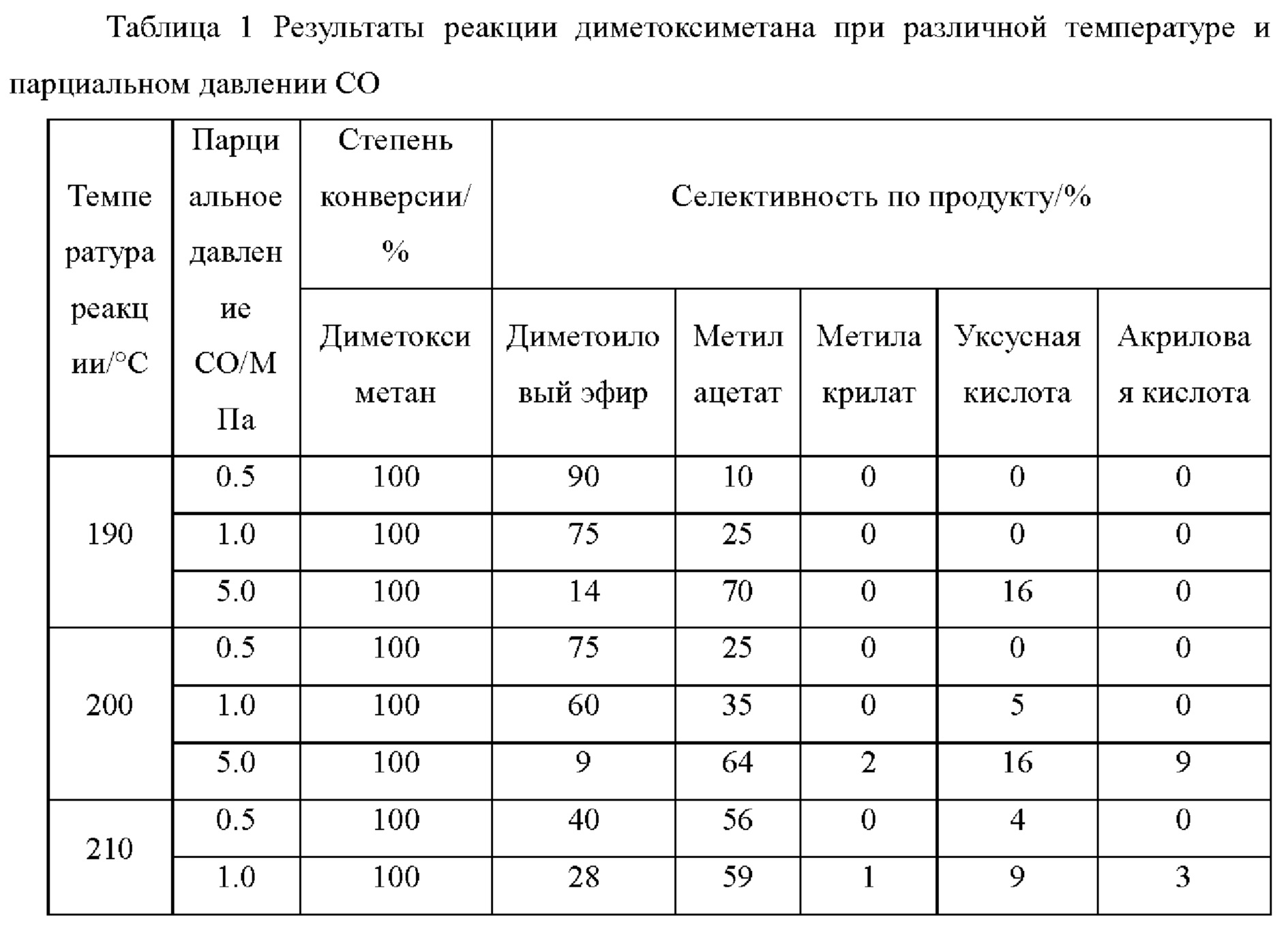
График степени конверсии сырья ДММ и селективности продуктов в зависимости от температуры при парциальном давлении монооксида углерода, равном 2,5 МПа, показан на Фигуре 1. Как можно увидеть из Фиг. 1, при температуре реакции выше 190°С на катализаторе H-MOR (соотношение Si/Al=6,5) степень конверсии сырья ДММ близка к 100%. По существу, образуются пять продуктов, а именно диметиловый эфир (ДМЭ), метилацетат (МАц), уксусная кислота (УК), метилакрилат (МА) и акриловая кислота (АК). Селективность по продуктам диметилового эфира и метилацетата постепенно снижается при повышении температуры реакции. При достижении температуры реакции 240°С диметиловый эфир практически не образуется; когда температура реакции достигает 270°С, селективность по метилацетату снижается до 40%. При температуре реакции выше 200°С среди продуктов образуется небольшое количество акриловой кислоты, селективность по которой увеличивается с увеличением температуры реакции, при этом наибольшая селективность достигает 35% при достижении температуры реакции 270°С. Продукт метилакрилата сопровождается образованием акриловой кислоты, и его селективность остается стабильной около 3%. Селективность по продукту уксусной кислоты также постепенно увеличивается с увеличением температуры, однако неочевидным образом, и селективность увеличивается с 10% до 23% от начальных 190°С до 270°С соответственно.
Таблица 1 показывает распределение продукта в виде функции от температуры реакции при парциальном давлении ДММ 1,25×10-2 МПа (0,0125 атм) и парциальном давлении монооксида углерода 0,5 МПа, 1,0 МПа и 5,0 МПа, соответственно. Из Таблицы 1 понятно, что при всех этих условиях, степень конверсии сырья ДММ близка к 100% и селективность по продукту акриловой кислоты становится выше при постоянной температуре реакции при увеличении парциального давления монооксида углерода. Когда парциальное давление монооксида углерода составляет 5,0 МПа, при 240°С селективность акриловой кислоты достигает 37%. Парциальное давление СО имеет небольшое влияние на селективность уксусной кислоты и селективность уксусной кислоты по сути устанавливается на уровне 20-25%.
Пример 2
Молекулярное сито H-MOR с соотношением кремния к алюминию Si/Al=6,5 таблетировали под давлением 40 МПа и дробили на гранулы 20-40 меш для получения катализатора. 0,4 г катализатора загрузили в реактор с неподвижным слоем для предварительной подготовки. Условия предварительной подготовки катализатора были следующими: объемная скорость потока N2 составила 30 мл/мин, а температуру поднимали от 25°С до 500°С за 150 минут и поддерживали на значении 500°С в течение 180 минут.
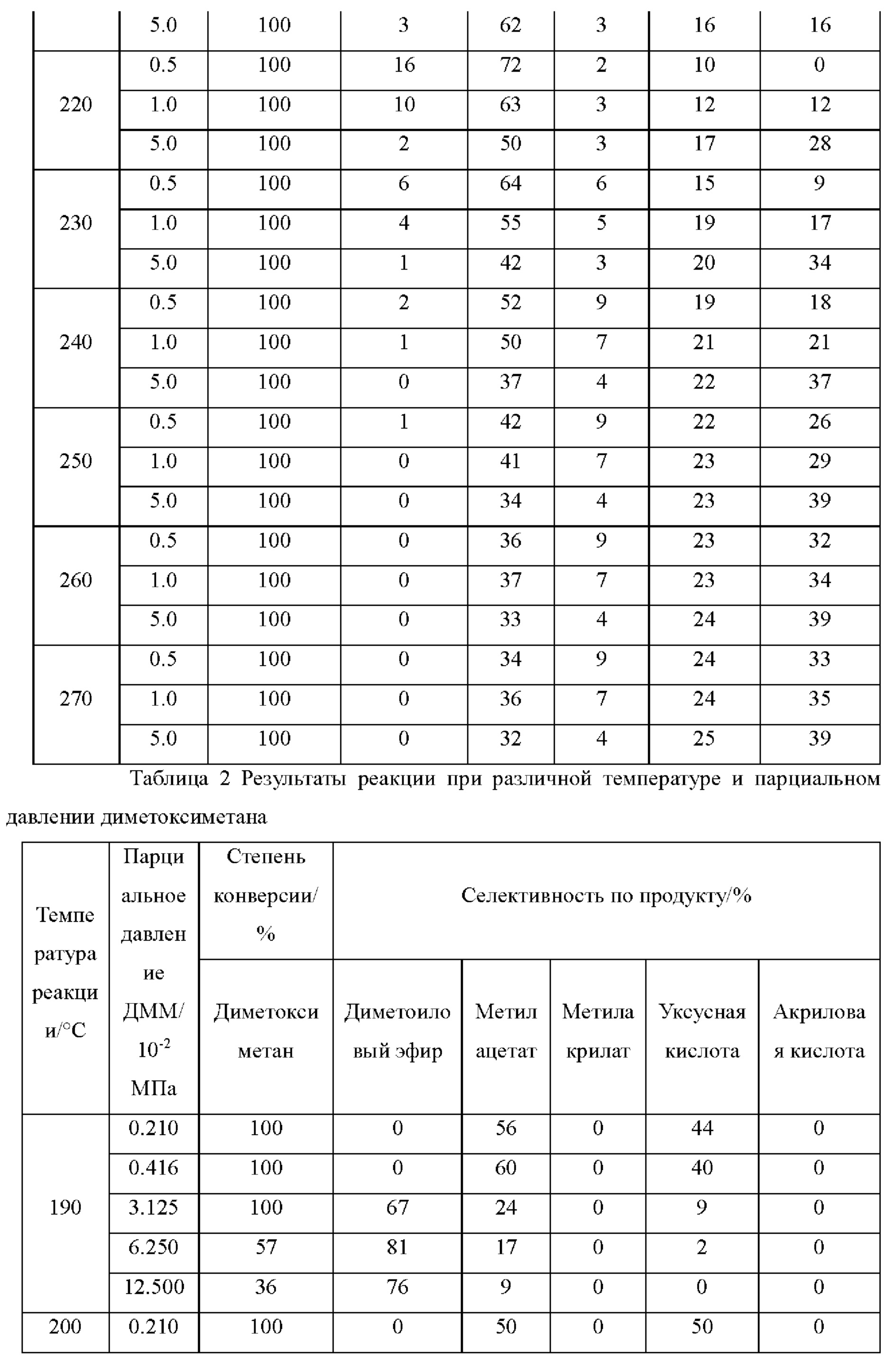
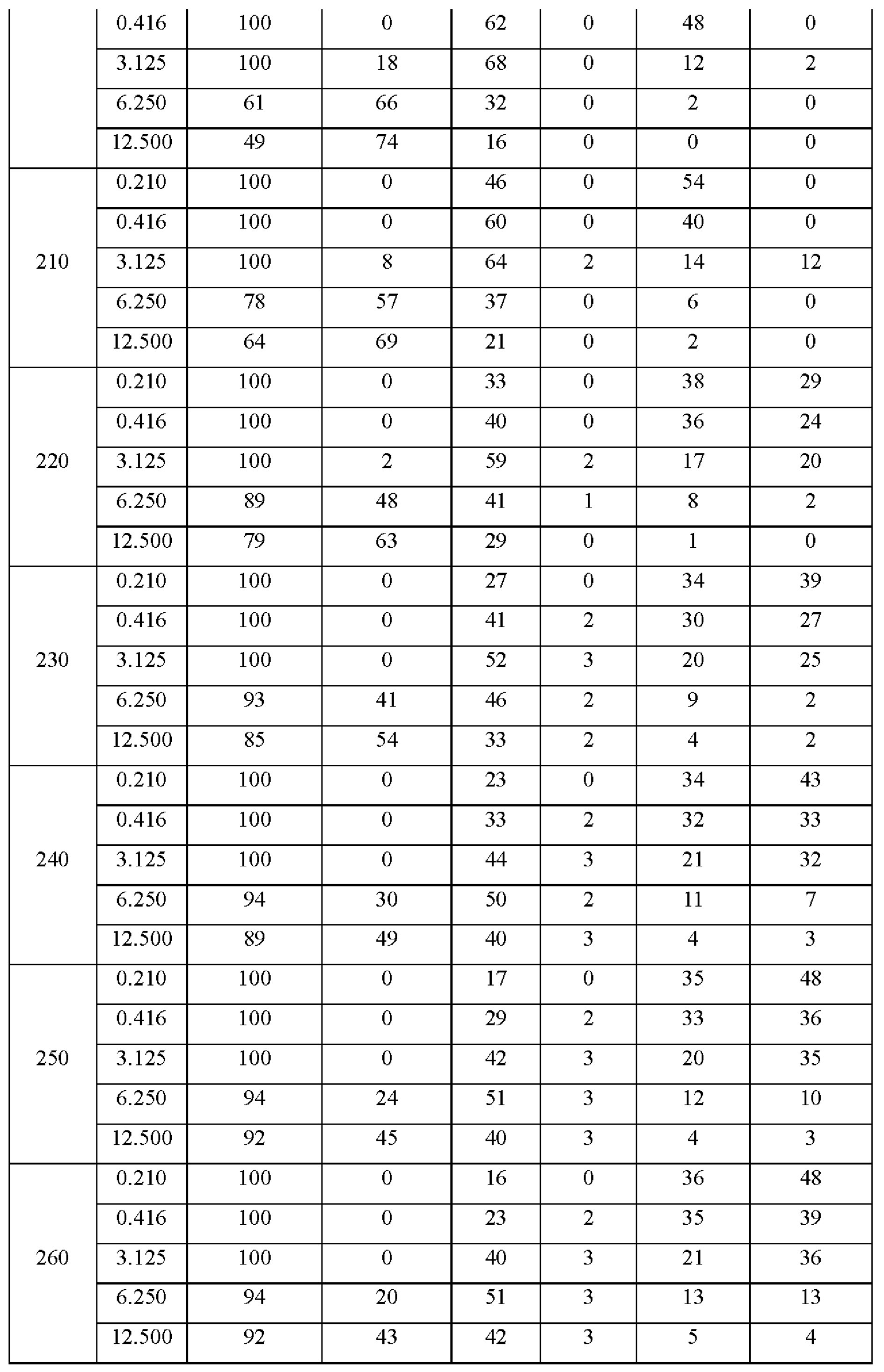
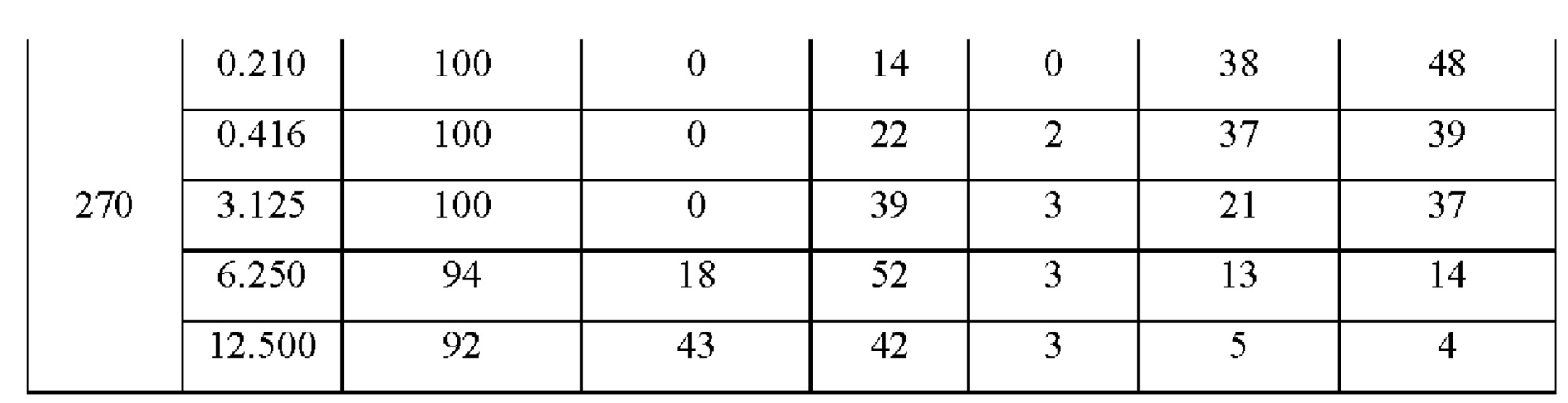
Реакционный газ состоял из двух газовых потоков и обеспечивалась общая объемная скорость потока 100 мл/мин. Сырьевой материал диметоксиметана вносили в реактор посредством монооксида углерода с объемной скоростью потока 2 мл/мин, 5 мл/мин, 25 мл/мин, 50 мл/мин и 100 мл/мин при температуре водяной бани от 0°С до 30°С; объемная скорость потока другого потока чистого монооксида углерода составили 98 мл/мин, 95 мл/мин, 75 мл/мин, 50 мл/мин и 0 мл/мин соответственно. Общее давление в ходе реакции составило 5,0 МПа. Температуру реакции поддерживали на уровне 190°С на протяжении 300 минут, а затем увеличивали до 200°С за 5 минут, поддерживали на 200°С в течение еще 300 минут, а затем увеличивали до 210°С за 5 минут. Согласно описанному выше правилу, температуру поднимали вплоть до 270°С с шагом в 10°С, удерживая на 300 минут на каждом значении. Парциальное давление сырьевого материала диметоксиметана составило 0,21×10-2 МПа (0,0021 атм), 0,416×10-2 МПа (0,00416 атм), 1,25×10-2 МПа (0,0125 атм), 3,125×10-2 МПа (0,3125 атм), 6,25×10-2 МПа (0.625 атм) и 12,5×10-2 МПа (0,125 атм) соответственно. На Фигуре 1 показаны данные реакции для сырья ДММ при парциальном давлении 1,25×10-2 МПа (0,0125 атм), остальные данные по реакции показаны в Таблице 2. Когда парциальное давление ДММ ниже, чем 3,125×10-2 МПа, степень конверсии ДММ близка к 100% при любой температуре реакции. Когда парциальное давление ДММ ниже, чем 3,125×10-2 МПа, степень конверсии ДММ постепенно увеличивается с повышением температуры реакции. Когда парциальное давление ДММ составляет 0,21×10-2 МПа, а температура реакции составляет 190°С, продуктами становятся метилацетат и уксусная кислота, с селективностью 56% и 44%, соответственно. С повышением температуры реакции селективность по метилацетату и уксусной кислоте постепенно снижается, при этом образуется акриловая кислота и метилакрилат, и селективность по акриловой кислоте увеличивается с повышением температуры реакции. При температуре реакции больше или равной 250°С, селективность по акриловой кислоте достигает максимума в 48% и остается по существу неизменной при дальнейшем увеличении температуры реакции. При температуре реакции выше 250°С при увеличении парциального давления ДММ до 0,416×10-2 МПа селективность по акриловой кислоте устанавливается на уровне 40%. С увеличением парциального давления ДММ при постоянных температурных условиях селективность по акриловой кислоте постепенно снижается. Когда парциальное давление ДММ составляет 12,5×10-2 МПа, а температура реакции 270°С, селективность по акриловой кислоте составляет только 4%.
Пример 3
Молекулярное сито H-MOR с соотношением кремния к алюминию Si/Al=6,5 таблетировали под давлением 40 МПа и дробили на гранулы 20-40 меш для получения катализатора. 0,4 г катализатора загрузили в реактор с неподвижным слоем для предварительной подготовки. Условия предварительной подготовки катализатора были следующими: объемная скорость потока N2 составила 30 мл/мин, а температуру поднимали от 25°С до 500°С за 150 минут и поддерживали на значении 500°С в течение 180 минут.
Реакционный газ состоял из двух газовых потоков и обеспечивалась общая объемная скорость потока 100 мл/мин. Молярное соотношение СО к ДММ поддерживали на уровне 400:1 регулированием температуры водяной бани сырья ДММ и объемной скорости потока газа-носителя СО (с целью обеспечить постоянную площадь пика ДММ на хроматограмме). Общее давление реакции было исправлено до значений 1,25 МПа, 2,5 МПа и 5,0 МПа, соответственно. Температуру реакции поддерживали на уровне 190°С на протяжении 90 минут, а затем увеличивали до 200°С за 5 минут, поддерживали на 200°С в течение еще 90 минут, а затем увеличивали до 210°С за 5 минут. Согласно описанному выше правилу, температуру поднимали вплоть до 270°С с шагом в 10°С, удерживая на 90 минут на каждом значении. График степени конверсии сырья ДММ и селективности по продуктам уксусной кислоты и акриловой кислоты в зависимости от температуры показан на Фигуре 2. В случае, когда соотношение СО и ДММ поддерживается фактически на постоянном уровне, селективность по уксусной кислоте остается фактически неизменной с постепенным увеличением общего давления реакции. Тем не менее, при общем давлении реакции 5,0 МПа, селективность по продукту акриловой кислоты значительно выше, чем селективность по акриловой кислоте при общем давлении 1,25 МПа и 2,5 МПа при той же температуре. Это можно объяснить тем, что в ходе реакции альдольной конденсации уменьшается количество молекул, и повышенное давление реакции способствует тому, что она идет в прямом направлении.
Пример 4
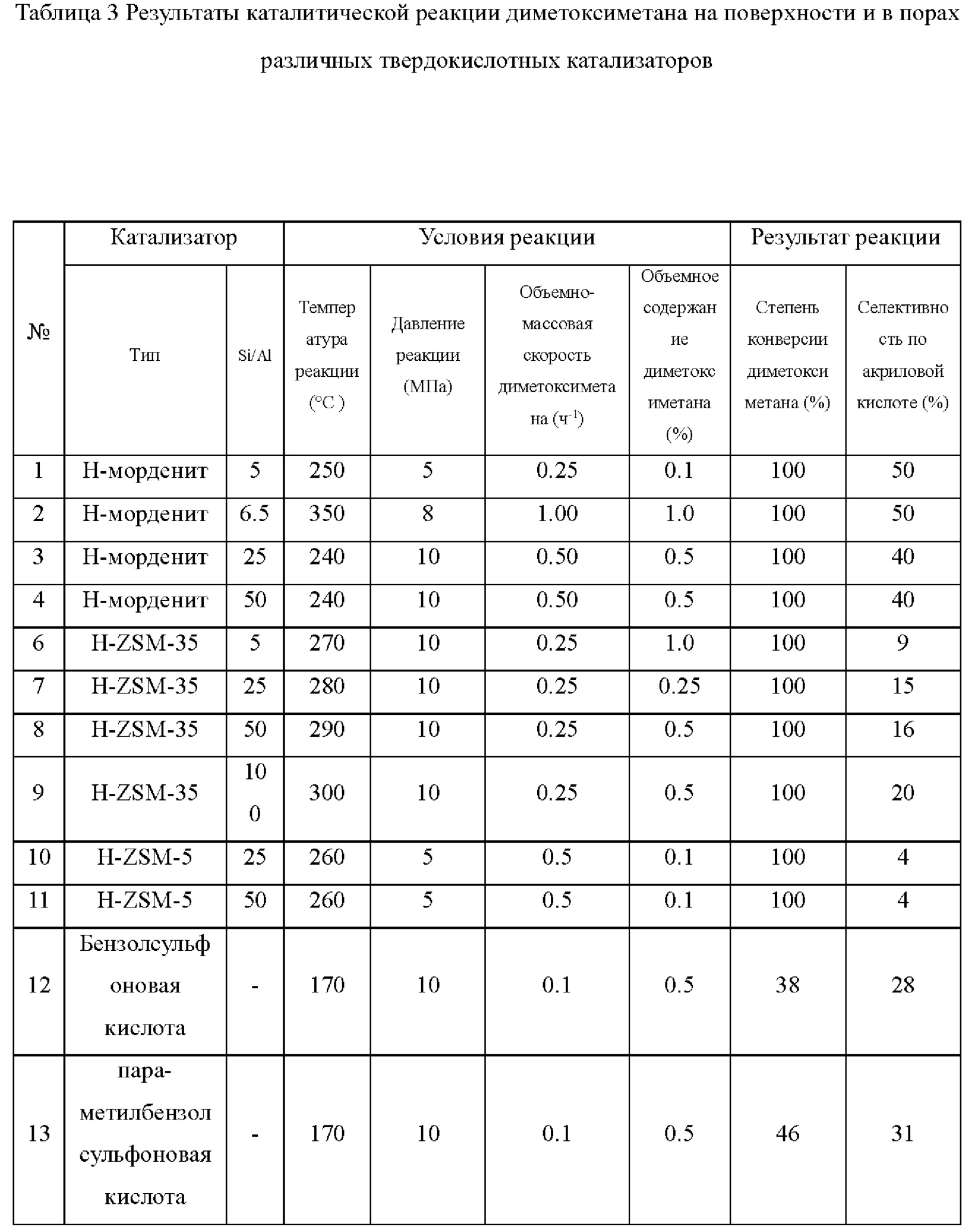
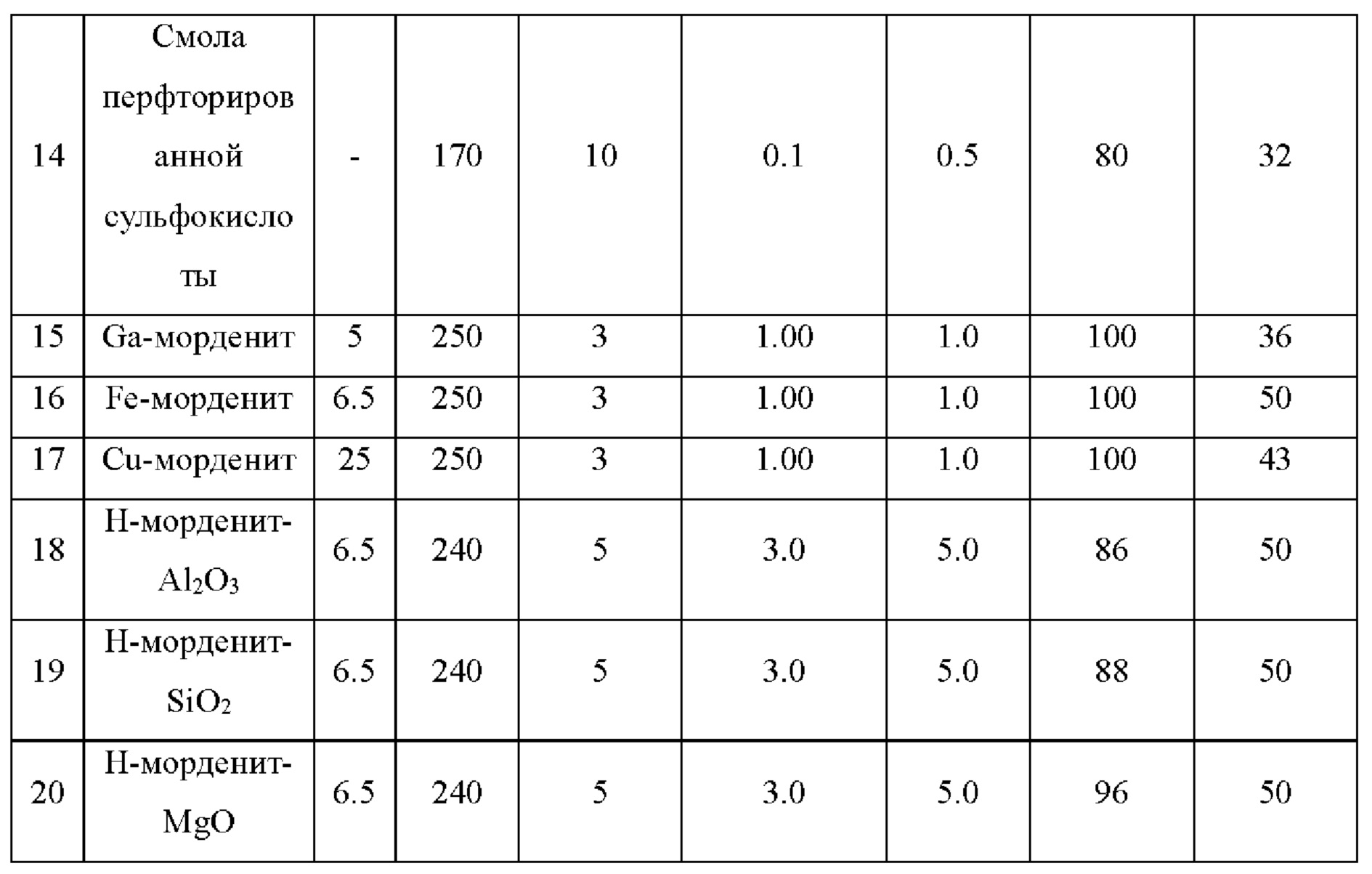
Использовали реактор с неподвижным слоем, масса загрузки катализатора находилась в пределах от 0,1 до 5,0 г. Молекулярные сита с различным соотношением кремний-алюминий с топологиями MWW, FER, MFI, MOR, FAU и ВЕА, включающими Н-МСМ-22, H-ZSM-35, H-ZSM-5, H-MOR, H-Y, H-Beta и модифицированные металлами Ga-морденит, Fe-морденит, Cu-морденит, а также формованные катализаторы Н-морденит-Аl2О3, Н-морденит-SiO2 и Н-морденит-MgO таблетировали при давлении 40 МПа и дробили на гранулы 20-40 меш для получения катализатора. В Таблице 3 представлены результаты для катализаторов на основе кислотных смол и катализаторов на основе твердой сульфокислоты при температуре реакции от 180°С до 350°С, давлении реакции от 0,1 МПа до 10 МПа, массо-объемной скорости сырья ДММ от 0,05 ч-1 до 10 ч-1 и объемном проценте от 0,1% до 100%.
Выше приведены лишь некоторые варианты реализации настоящей заявки, которые не ограничивают настоящее изобретение каким-либо образом. Несмотря на то, что настоящая заявка раскрыта предпочтительными вариантами реализации, такими как выше, они тем не менее не ограничивают настоящее изобретение. Небольшие изменения и модификации, задействующие техническое содержание, описанные выше, сделанные опытным специалистом в данной области без отклонения от технологического решения данной заявки, равноценны эквивалентному варианту реализации и попадают в объем технического решения.