Результат интеллектуальной деятельности: Способ получения соединения δ*-BiO в системе BiO-SiO
Вид РИД
Изобретение
Способ относится к области химии и может быть использован в качестве: эффективного адсорбента для удаления токсичных соединений селена из воды; эффективного адсорбента для очистки водных растворов от изотопов радиоактивного йода; супер ионного проводника; эффективного фотокатализатора для деградации и минерализации атразина в водном растворе, а также удаления оксида азота из воздуха.
В работе [Long Liu, Ning Chen, Yong Lei, Xuyan Xue, Lina Li, Jiancheng Wang, Sridhar Komarneni, Huaiyong Zhu and Dongjiang Yang. Micronanostructured δ-Bi2O3 with surface oxygen vacancies as superior adsorbents for SeOx2- ions // DOI: https://doi.org/10.1016/j.jhazmat.2018.08.025] был предложен гидротермальный способ синтеза δ*-Bi2O3. Для этого 4 ммоль Bi(NO3)3⋅5H2O и 20 ммоль NH2CH2COOH растворяли в 60 мл деионизированной воды, а затем энергично перемешивали в течение 5 мин. при комнатной температуре. Затем смесь обрабатывали ультразвуком в течение 30 минут ультразвуковым генератором. Далее смесь помещали в автоклав из нержавеющей стали с тефлоновым покрытием вместимостью 100 мл. Автоклав герметизировали и нагревали при 140°С в течение 24 часов. Затем автоклав, естественно, охлаждали до комнатной температуры. Наконец, продукты промывали абсолютным этанолом и деионизированной водой несколько раз, а затем сушили в вакууме при 60°С в течение 24 часов.
Однако, при использовании данного способа не достигается:
1. быстрое получение искомой фазы, т.к. указанный способ является не только более трудоемким, в виду большого количества технологических операций, но еще и очень длительным по времени (более 50 часов);
2. использование в аналоге дополнительного оборудования (автоклав, ультразвуковые генераторы, вакуумные печи и т.д.), усложняет и удорожает процесс получения фазы;
3. введение в раствор дополнительных компонентов реакции, а также постоянное его перемещение (промывка и т.д.) создают существенный риск загрязнения конечного материала посторонними веществами.
Похожие способы синтеза δ*-Bi2O3, имеющие схожие с данным аналогом недостатки и основанные на гидротермальном синтезе, также подробно рассмотрены в работах:
1. Ye Xiong, Baokang Dang, Chao Wang, Hanwei Wang, Shouwei Zhang, Qingfeng Sun, Xijin Xu. Cellulose Fibers Constructed Convenient Recyclable 3D Graphene-Formicary-like δ-Bi2O3 Aerogels for the Selective Capture of Iodide // doi:10.1021/acsami.7b03516;
2. Long Liu, Wei Liu, Xiaoliang Zhao, Daimei Chen, Rongsheng Cai, Weiyou Yang, Sridhar Komarneni and Dongjiang Yang. Selective Capture of Iodide from Solutions by Microrosette-like δ-Bi2O3 // doi:10.1021/am504000n;
3. Yue Yin, Feng Li, Qingfeng Zhan, Dongmei Jiang and Ruizhi Chen. Synthesis of δ-Bi2O3/Bi2MoO6 composites with enhanced photocatalytic activity by hydrothermal method // DOI: https://doi.org/10.1016/j.materresbull.2018.03.021.
В работе [Hanggara Sudrajat, Pornapa Sujaridworakun. Low-temperature synthesis of δ-Bi2O3 hierarchical nanostructures composed of ultrathin nanosheets for efficient photocatalysis // Materials & Design 130 (2017) 501-511] предложен золь-гель способ с интеза. Для этого 1 ммоль Bi(NO3)3⋅5H2O и 0,4 ммоль NH4VO3 сначала растворяли в 10 мл HNO3. Раствор разбавляли деионизированной (DI) водой до достижения конечного объема 50 мл. После интенсивного перемешивания в течение 30 минут к раствору добавляли NaOH до достижения конечного рН 12, образуя бледно-желтый осадок. Затем суспензию подвергали нагреванию при 70°С в течение 30 ч. без перемешивания в закрытом реакторе. Конечный продукт, собирали путем центрифугирования, промывали водой DI, а затем этанолом, сушили в печи при 100°С в течение 24 часов и, наконец, измельчали в агатовой ступке.
Однако, при использовании данного способа не достигается:
1. быстрое получение искомой фазы, т.к. указанный способ является не только более трудоемким, в виду большого количества технологических операций, но еще и очень длительным по времени (более 54 часов);
2. использование в аналоге дополнительного оборудования усложняет и удорожает процесс получения фазы;
3. введение в раствор дополнительных компонентов реакции, а также постоянное его перемещение (промывка и т.д.) создают существенный риск загрязнения конечного материала посторонними веществами.
Следует также отметить еще несколько способов синтеза δ*-Bi2O3, имеющих схожие со всеми вышеперечисленными аналогами недостатки:
1. Shijin Zhu, Lilin Lu, Zaiwang Zhao, Tian Wang, Xiaoying Liu, Haijun Zhang, Fan Dong, Yuxin Zhang. Mesoporous Ni-doped δ-Bi2O3 Microspheres for Enhanced Solar-driven Photocatalysis: A Combined Experimental and Theoretical Investigation // doi:10.1021/acs.jpcc.7b01608 (сольвотермический способ);
2. Juan Zhang, Qiaofeng Han, Xin Wang, Junwu Zhu, Guorong Duan. Synthesis of δ-Bi2O3 microflowers and nanosheets using СН3СОО(BiO) self-sacrifice precursor // Materials Letters 162 (2016) 218-22 (химический способ);
3. Juan С. Medina, Monserrat Bizarro, Phaedra Silva-Bermudez, Mauro Giorcelli, Alberto Tagliaferro, Sandra E. Rodil. Photocatalytic discoloration of methyl orange dye by δ-Bi2O3 thin films // DOI: doi:10.1016/j.tsf.2016.05.034 (магнетронное распыление);
4. Jia Xu and Jingyue Liu. Facet-Selective Epitaxial Growth of δ-Bi2O3 on ZnO Nanowires // DOI: 10.1021/acs.chemmater.6b01739 (осаждение из паровой фазы).
Общий вывод по аналогам: указанные аналоги в большинстве своем требуют очень большого количества технологических операций с использованием дополнительного дорогостоящего оборудования, дополнительных компонентов реакции, а также весьма длительны по времени. При этом часть из них совершенно не рассчитана на получение больших объемов продукта. Это влечет за собой большие затраты, сильно усложняет и удорожает получение соединения δ*-Bi2O3.
Наиболее близким к заявляемому способу является способ, описание которого приведено в работе [Майер А.А., Фомченков Л.П., Горащенко Н.Г., Грачева Н.А. Исследование высокотемпературного синтеза соединений висмута со структурой силленита // Труды МХТИ им. Д.И. Менделеева. 1973. Т. 76. С. 85-89], где предложили способ синтеза соединения δ*-Bi2O3 из расплава. Для этого исходные реагенты Bi2O3 и SiO2 (содержание SiO2 в навеске 12-20% мол.) помещали в платиновый тигель, механически смешивали, нагревали до температур свыше 900°С (судя по тому, что время выдержки не указано - работа велась с очень малыми объемами вещества - не больше нескольких граммов). Далее расплав охлаждали до 790°С со скоростью не более 10°С/мин., после чего продолжали охлаждение с такой же скоростью уже до комнатной температуры. Особым условием охлаждения является полное отсутствие встряхивания и вибрации, которые могут привести к распаду соединения δ*-Bi2O3.. Данный способ взят за прототип.
Однако, при использовании данного способа не достигается: быстрое получение искомой фазы, т.к. указанный способ довольное длителен по времени (медленное охлаждение с печью).
Основная задача изобретения состоит в повышении эффективности процесса получения δ*-Bi2O3, а также снижения временных затрат на его получение.
Для достижения поставленной задачи, заявляемый «Способ получения соединения δ*-Bi2O3 в системе Bi2O3-SiO2» содержит следующую совокупность существенных признаков, сходных с прототипом:
1. использование в качестве одних из исходных реагентов чистых Bi2O3 и SiO2;
2. необходимость доведения смеси исходных реагентов до расплавленного состояния;
3. отсутствие дополнительных компонентов реакции и дополнительного оборудования.
По отношению к заявляемому способу указанный прототип имеет следующие отличительные признаки и недостатки: невозможно быстрое получение искомой фазы, т.к. указанный способ требует длительного времени охлаждения (скорости не выше 10°С/мин.).
Между отличительными признаками и решаемой задачей существует следующая причинно-следственная связь.
Выбор граничных параметров соотношения исходных реагентов (80±1,5 мол. %. Bi2O3-72±1,5 мол. %. Bi2O3 и 20±1,5 мол. %. SiO2 - 28±1,5 мол. % SiO2), обусловлен особенностью строения метастабильной системы Bi2O3-SiO2, реализуемой из температурной области «С» [Жереб В.П. Физико-химические исследования метастабильных равновесий в системах Bi2O3-ЭО2, где Э - Si, Ge, Ti. Автореферат диссертации … к.х.н. - М.: ИОНХ АН СССР. 1980. - 22 с.]. По данной диаграмме заметно, что область существования соединения δ*-Bi2O3 находится как раз в области составов от 20 до 28 мол. % SiO2 (±1,5 мол. %). При других содержании оксида кремния (SiO2) выше или ниже указанного предела, возможны значительные загрязнения конечного продукта посторонними фазами.
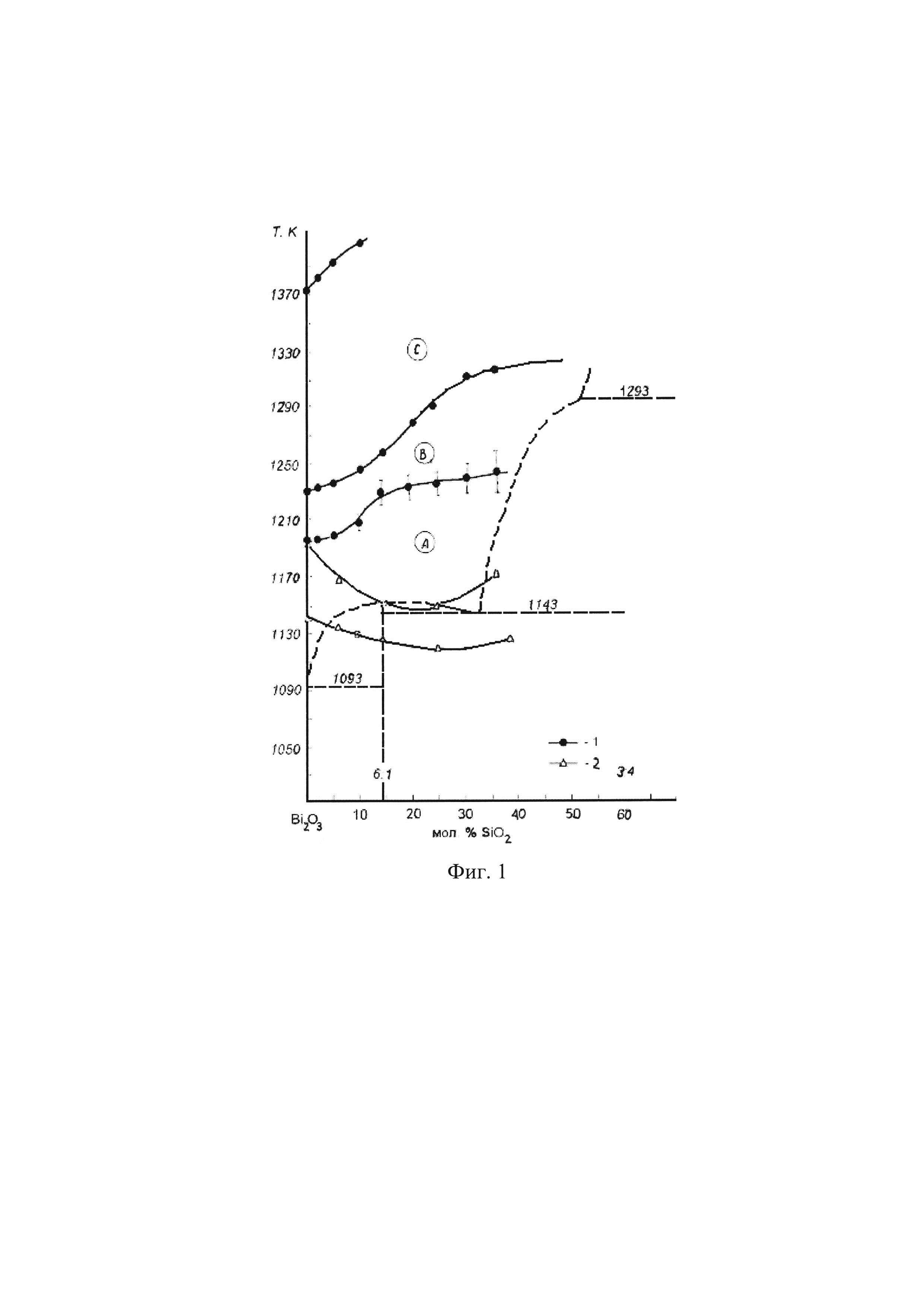
Выбор граничных параметров температуры начала охлаждения расплава (890°С±20°С - 1160±20°С) обусловлен высокотемпературными областями расплава, каждая из которых имеет свое, особенное строение. Известно, что на фазовой диаграмме системы Bi2O3-SiO2 область расплава может быть разделена на 3 температурные зоны А, В и С (фиг. 1) [Каргин В.П. Жереб В.П., Скориков В.М. Стабильное и метастабильное равновесия в системе Bi2O3-SiO2 // Журнал неорганической химии. 1991. Т. 36. №10. С. 2611-2616]. Нами было установлено, что из всех трех зон, независимо от скорости охлаждения, удается получить соединение δ*-Bi2O3.
Нижний диапазон температур (890°С±20°С) выбран согласно диаграмме (фиг. 1) и обозначает нижнюю границу С-зоны. Нагрев же выше верхнего диапазона температур (1160°С±20°С) возможен, но является нецелесообразным в виду более высоких энергетических затрат и более быстрого износа материала тигля.
Выбор граничных параметров выдержки при заданном интервале температур (не менее 15 минут), должен обеспечивать полное взаимное растворение исходных компонентов друг в друге. Увеличение времени выдержки растет с увеличением массы справляемых в тигле исходных компонентов (масса навески), т.к. большему количеству материала, требуется больше времени на прогрев.
Выбор граничных параметров охлаждения (3-1000°С/сек.) обусловлен тем, что при соблюдении указанных режимов нагрева и выдержки, а также отсутствии факторов, способных нарушить метастабильное состояние переохлаженного расплава (термический "удар"; встряхивание тигля; вибрация; контакт переохлажденного расплава с кристаллами стабильных фаз и т.п.), охлаждать расплав можно с любой скоростью, вплоть до закалки с тиглем в воду. В этом и состоит одно из главных отличий от прототипа - получать данное соединение (δ*-Bi2O3) можно не только медленным охлаждением с печью, но и ускоренно (при соблюдении всех, указанных в заявляемом способе, условий).
Способ иллюстрируется графически, где:
Фиг. 1 - Температурные зоны 1 в области расплава на фазовой диаграмме стабильного равновесия 2 системы Bi2O3-SiO2;
Фиг. 2 - Фазовая диаграмма метастабильных равновесий системы Bi2O3-SiO2, построенная по результатам охлаждения расплава от температур, лежащих в зоне С;
Фиг. 3 - Результаты микроструктурного анализа образца δ*-Bi2O3, состава 22 мол. % SiO2 (система Bi2O3-SiO2), полученного заявляемым способом, увеличение - 50 крат;
Фиг. 4 - Результаты микроструктурного анализа образца δ*-Bi2O3, состава 22 мол. % SiO2 (система Bi2O3-SiO2), полученного заявляемым способом, увеличение - 500 крат;
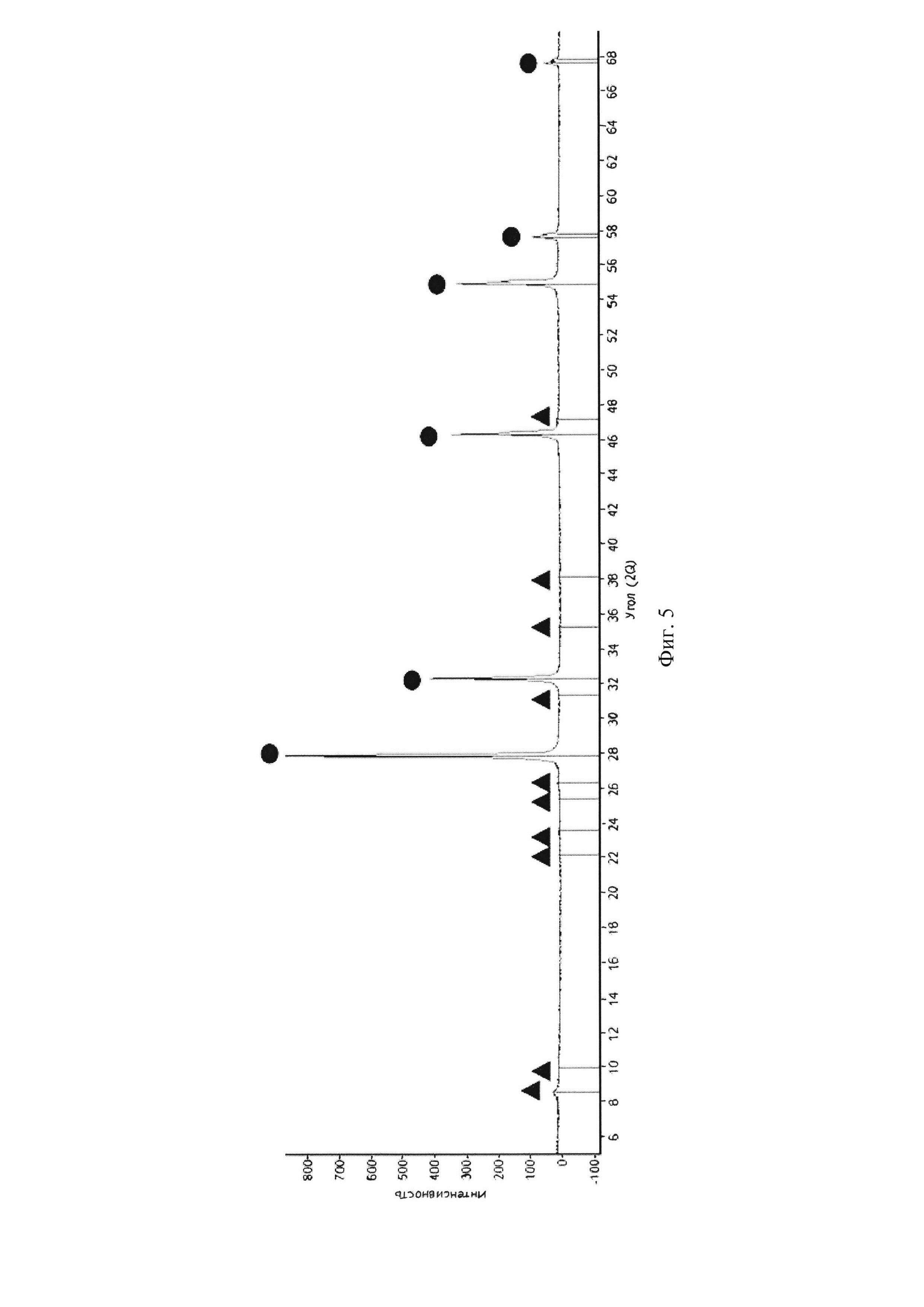
Фиг. 5 - Результаты рентгенофазового анализа образца δ*-Bi2O3, состава 22 мол. % SiO2 (система Bi2O3-SiO2), полученного заявляемым способом, где черный круг - пики соответствующие соединению δ*-Bi2O3, черный треугольник - примесному соединению Si32O64 (его содержание не превышает 1,5% по массе, что является вполне приемлемым результатом чистоты конечного продукта).
Сущность изобретения поясняется диаграммой, а также результатами рентгенофазового и микроструктурного анализа.
Нами было установлено, что при сплавлении исходных реагентов, где их соотношение в навеске 80±1,5 мол. %. Bi2O3 - 72±1,5 мол. %. Bi2O3 и 20±1,5 мол. %. SiO2 - 28±1,5 мол. % SiO2, в температурном интервале 890°С±20°С - 1160±20°С, выдержке в нем не менее 15 минут и последующим охлаждении со скоростью 3-1000°С/сек., при отсутствии внешних факторов, способных механически нарушить метастабильное состояние переохлажденного расплава (термический "удар"; встряхивание тигля; вибрация; контакт переохлажденного расплава с кристаллами стабильных фаз и т.п.) - приводит к надежному формированию соединения δ*-Bi2O3. Это связано с тем, что при данном содержании оксида кремния, соединение δ*-Bi2O3 имеет максимальную устойчивость и при грамотном подборе режима термической обработки расплава, способно сохраняться до комнатной температуры. Нагрев и выдержка (режимы указаны выше), формирует определенное строение расплава, которое, при дальнейшем охлаждении, и приводит к формированию соединения δ*-Bi2O3. Чтобы его сохранить до комнатной температуры требуется отсутствие внешних факторов, способных механически нарушить метастабильное состояние переохлажденного расплава (термический "удар"; встряхивание тигля; вибрация; контакт переохлажденного расплава с кристаллами стабильных фаз и т.п.). При этом просто перемещать тигель с расплавом, например, для погружения в закалочную среду или выгрузку из печи на воздух, можно - это не влечет за собой никаких негативных последствий.
Также следует пояснить, что термин «термический удар», как негативный фактор, понимается только тогда, когда он контактно воздействует непосредственно на сам расплав (например, при выливании его из тигля, или же попадание инородного вещества в расплав). Термический же удар, направленный на тигель в котором находится расплав (например, при закалке в воду), не приводит ни к каким негативным последствиям.
Полученные данные подтверждаются рентгенофазовым (фиг. 5) и микроструктурным анализом (фиг. 3-4). Микроструктура полученного заявляемым способом соединения (фиг. 3-4), имеет однофазную структуру с ярко выраженным дендритным характером. По показаниям рентгенофазового анализа (фиг. 5) в структуре присутствует незначительное количество (не более 1,5% по массе) выделившегося оксида кремния (Si32O64), что является допустимым и не сказывается на качестве конечного продукта.
По результатам проведенных анализов, можно сделать вывод о том, что решающую роль в получении соединения δ*-Bi2O3 играет предварительная термическая обработка расплава, а также отсутствие внешних факторов, способных механически нарушить метастабильное состояние переохлажденного расплава (термический "удар"; встряхивание тигля; вибрация; контакт переохлажденного расплава с кристаллами стабильных фаз и т.п.).
Заявляемый «Способ получения соединения δ*-Bi2O3 в системе Bi2O3-SiO2» может быть реализован с помощью следующих материальных объектов:
1. печь - нагревательное устройство с рабочей камерой, обеспечивающее нагревание материала до заданной температуры в интервале до 1160°С;
2. платиновый тигель.
Пример конкретного выполнения:
1. в качестве исходных компонентов берем порошки оксида висмута (Bi2O3) и диоксида кремния (SiO2) в соотношении 78:22 мол. %;
2. исходные реагенты помещаем в платиновый тигель и перемешиваем платиновым шпателем или металлической ложкой;
3. нагреваем смесь до 1160°С с выдержкой 1 час;
4. закаливаем расплав с тиглем в воду;
5. извлекаем готовое закристаллизовавшееся соединение δ*-Bi2O3 из тигля.
Как показали результаты опытной проверки, при использовании заявляемого способа обеспечивается достижение следующих результатов:
1. получено соединение с формулой δ*-Bi2O3 с минимальным содержанием посторонних примесных фаз (не более 1,5% по массе);
2. показана возможность получать данное соединение даже с очень высокими скоростями охлаждения;
3. заявляемый способ требует намного меньше времени на синтез, чем все известные современные аналоги, приведенные выше, что существенно снижает не только временные, но также и экономические затраты на производство.
4. заявляемый способ не требует никакого дополнительного оборудования, только тигель и печь. Это существенно упрощает процесс синтеза и делает его экономически более выгодным.
Способ получения соединения δ-BiO в системе BiO-SiO, включающий предварительное механическое смешивание исходных компонентов, нагрев, выдержку и охлаждение, отличающийся тем, что исходные компоненты смешивают при соотношении (в мол. %), равном (72-81,5)BiO и (28-18,5)SiO, после быстрого механического смешивания компонентов смесь помещают в платиновый тигель, нагревают до 885-1180°С, выдерживают в течение 15-60 минут, после чего охлаждают со скоростью 3-1000°С/сек в отсутствие факторов, нарушающих метастабильное состояние переохлаждённого расплава, таких как термический удар, встряхивание тигля, вибрация, контакт переохлаждённого расплава с кристаллами стабильных фаз.