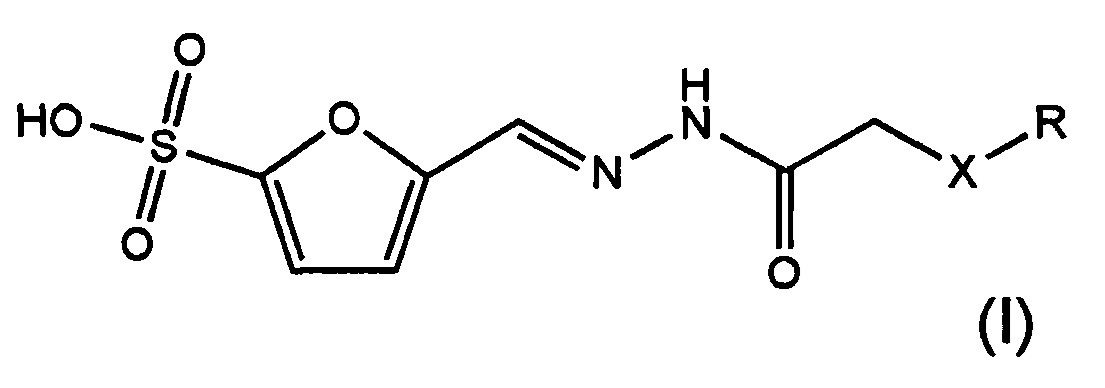
Результат интеллектуальной деятельности: ПРИМЕНЕНИЕ ФУРАНСУЛЬФОНАТОВ ДЛЯ ИНГИБИРОВАНИЯ ТРАНСКЕТОЛАЗЫ ПАТОГЕНА Mycobacterium tuberculosis
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к области медицинской химии, фармакологии, медицины и касается применения ряда сульфозамещенных химических соединений в качестве ингибиторов транскетолазы патогенной бактерии Mycobacterium tuberculosis, являющейся возбудителем туберкулеза.
Уровень техники
Транскетолаза является ключевым ферментом пентозофосфатного пути метаболизма углеводов у бактерий, который обеспечивает перенос двухуглеродного фрагмента с кетозы (субстрат-донор) на альдозу (субстрат-акцептор) с помощью кофактора тиаминдифосфата [Kochetov G.A., Solovjeva O.N. (2014) Biochim. Biophys. Acta, 1844, 1608-1618; Fullam E., Pojer F., Bergfors Т., Jones T.A., Cole S.T. (2012) Open Biol., 2, 110026]. Важность транскетолазы для жизнедеятельности возбудителя туберкулеза Mycobacterium tuberculosis была доказана путем подавления экспрессии данного фермента [Kolly G.S., Sala С., Vocat A., Cole S.T. (2014) FEMS Microbiol. Lett., 358, 30-35]. В частности, транскетолаза Mycobacterium tuberculosis катализирует образование D-рибозо-5-фосфата, который необходим для строительства клеточной стенки [Wolucka В.А. (2008) FEBS J., 275, 2691-2711]. Анализ научной литературы и патентных документов показал, что сульфозамещенные соединения для ингибирования транскетолазы из Mycobacterium tuberculosis ранее не применялись, и не было описано их свойство подавлять рост бактерии Mycobacterium tuberculosis. Окситиамин является наиболее известным среди немногочисленных ингибиторов транскетолазы человека (противоопухолевая мишень) [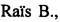 Comin В., Puigjaner J., Brandes J.L., Creppy E., Saboureau D., Ennamany R,. Lee W.N., Boros L.G., Cascante M. (1999) FEBS Lett., 456, 113-118], однако он не оказывает влияния на микобактериальный фермент [Fullam Е., Pojer F., Bergfors Т., Jones Т.А., Cole S.T. (2012) Open Biol., 2, 110026].
Comin В., Puigjaner J., Brandes J.L., Creppy E., Saboureau D., Ennamany R,. Lee W.N., Boros L.G., Cascante M. (1999) FEBS Lett., 456, 113-118], однако он не оказывает влияния на микобактериальный фермент [Fullam Е., Pojer F., Bergfors Т., Jones Т.А., Cole S.T. (2012) Open Biol., 2, 110026].
Раскрытие изобретения
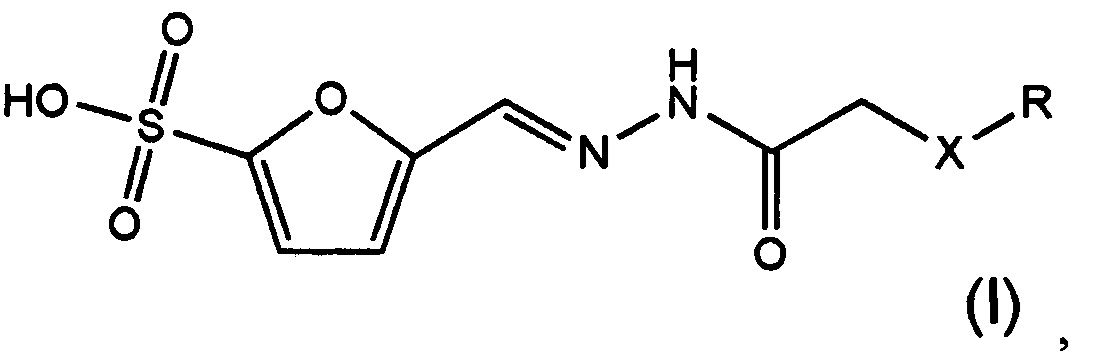
Технической задачей изобретения является применение сульфозамещенных химических соединений (фурансульфонатов) в качестве ингибиторов транскетолазы из Mycobacterium tuberculosis. Технический результат заключается в эффективном подавлении активности очищенного фермента, а также в торможении роста возбудителя туберкулеза. Поставленная техническая задача решается тем, что в качестве средства для ингибирования транскетолазы из Mycobacterium tuberculosis предлагается использовать сульфозамещенные соединения формулы (I):
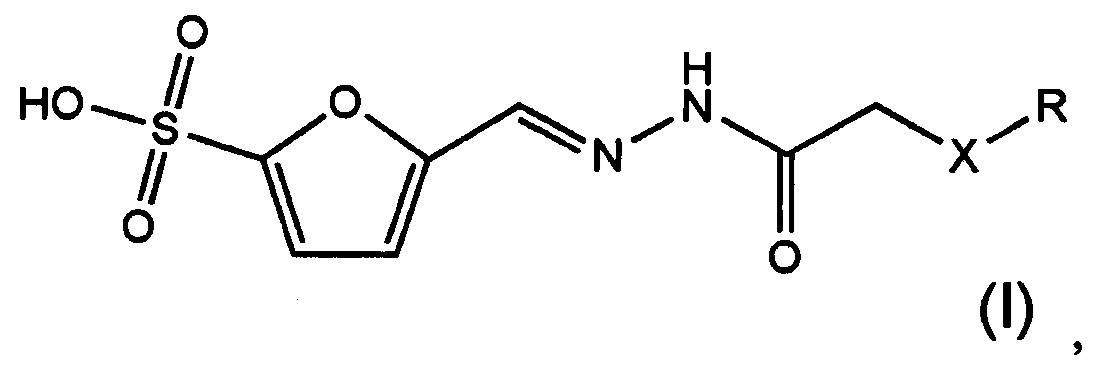
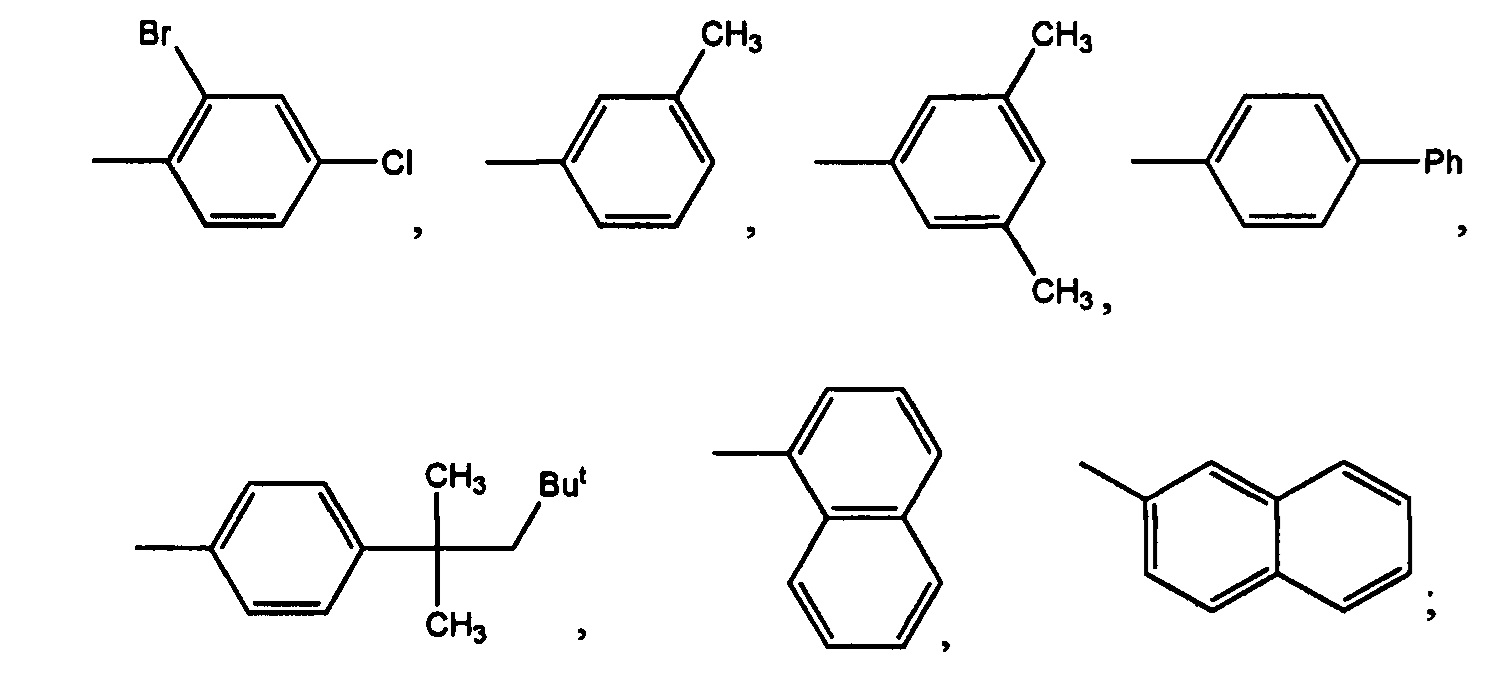
где X представляет собой -NH- или -О-, R представляет собой следующие гидрофобные группы:
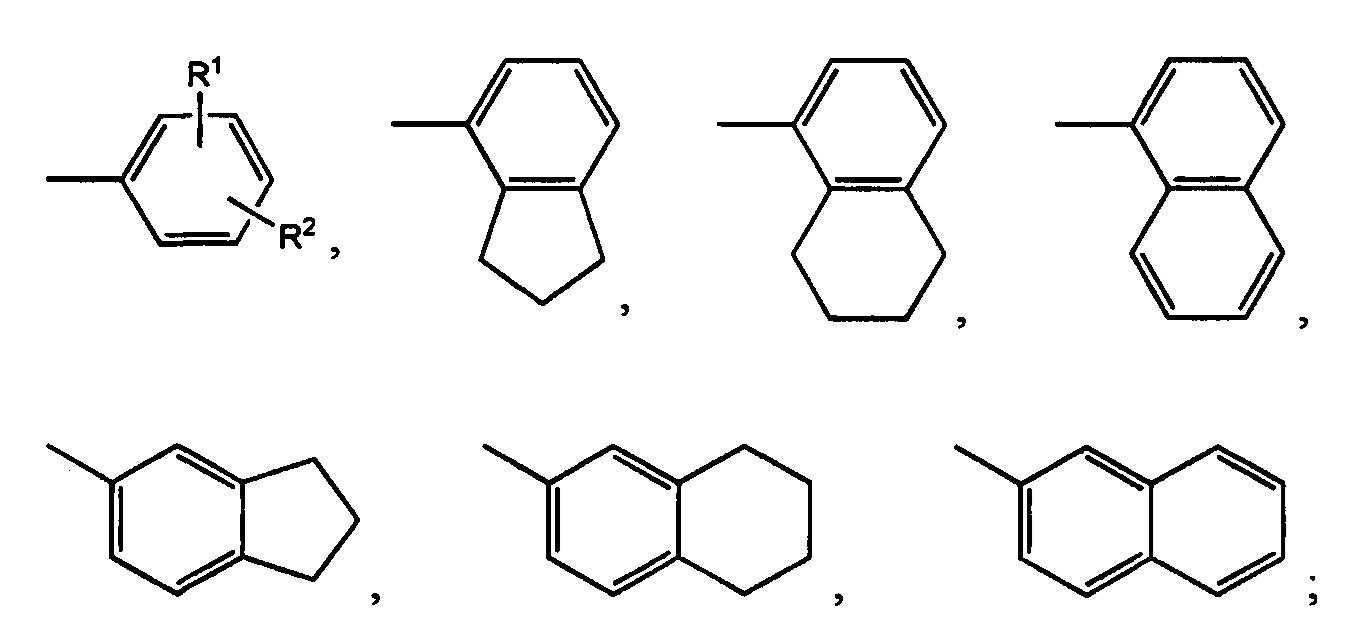
R1, R2 представляют собой независимо друг от друга следующие группы: -Н, галоген, -CH3, -С2Н5, -С3Н7, -СН(CH3)2, -CH(CH3)2R3, -С4Н9, -СН2-СН(СН3)2, -СН(СН3)-С2Н5, -С(СН3)3, -С5Н11, -С2Н4-СН(СН3)2, -СН2-СН(СН3)-С2Н5, -СН(СН3)-С3Н7, -СН(СН3)-СН(СН3)2, -СН2-С(СН3)3, -С(СН3)2-С2Н5, -СН(С2Н5)2, -СН=СН2, -СН2-СН=СН2, -СН=СН-СН3, -С2Н4-СН=СН2, -СН2-СН=СН-СН3, -СН=СН-С2Н5, цикло-С3Н5, цикло-С4Н7, цикло-С5Н9, цикло-С6Н11, -Ph;
R3 представляет собой следующие группы: -С3Н7, -СН(СН3)2, -С4Н9, -СН2-СН(СН3)2, -СН(СН3)-С2Н5, -С(СН3)3, -С5Н11, -С2Н4-СН(СН3)2, -СН2-СН(СН3)-С2Н5, -СН(СН3)-С3Н7, -СН(СН3)-СН(СН3)2, -СН2-С(СН3)3, -С(СН3)2-С2Н5, -СН(С2Н5)2.
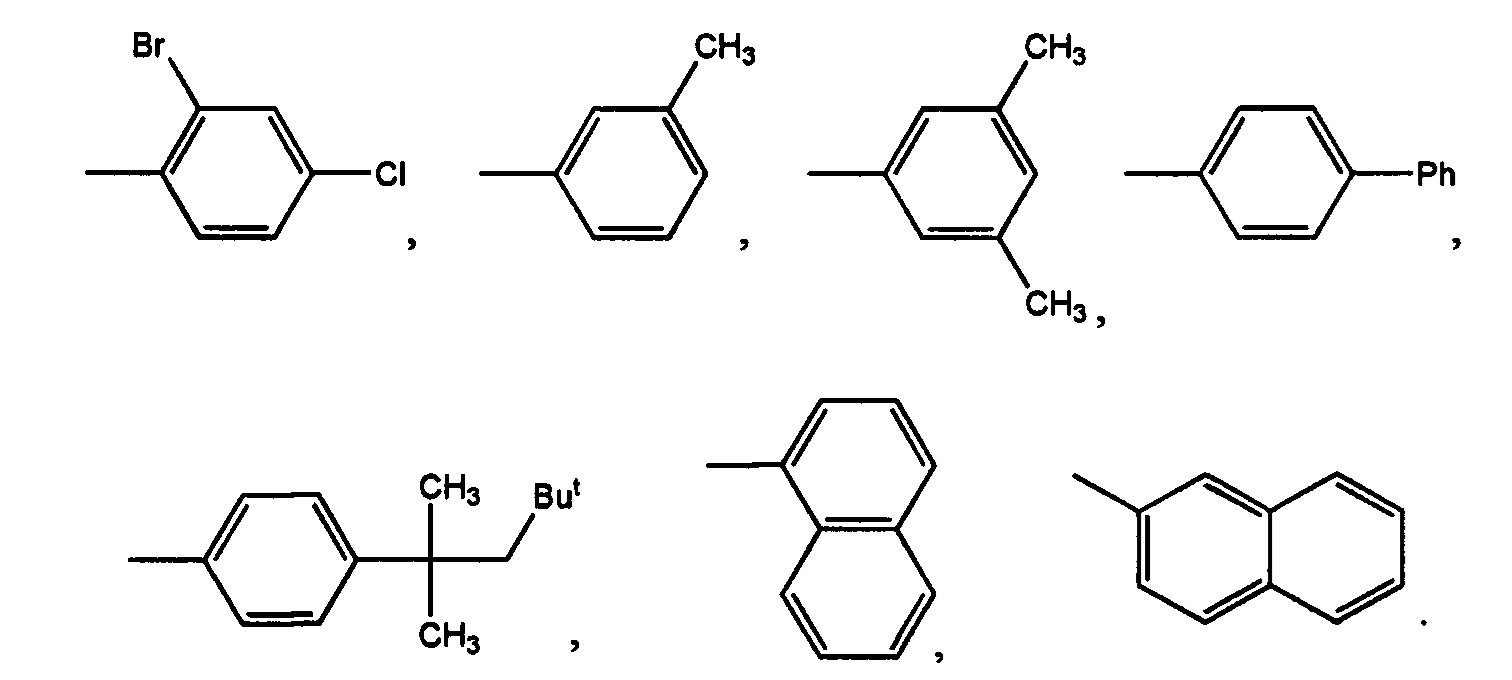
Поскольку сульфокислоты характеризуются низким значением pKa<1, такие соединения в биологических системах будут находиться в виде солей при любом молекулярном окружении. Инвариантным структурным элементом, обуславливающим базовую ингибиторную активность данных соединений, является фурансульфонат с присоединенным к нему гидразидным линкером. Вторым концом линкер присоединен к вариабельному гидрофобному фрагменту на основе бензольного кольца. Варьирование гидрофобной части приводит к модуляции ингибиторного эффекта в отношении транскетолазы из Mycobacterium tuberculosis. Структура нескольких соединений данного класса известна из баз данных коммерчески доступных низкомолекулярных веществ Vitas-M (http://www.vitasmlab.biz) и ZINC (http://zinc.docking.org). В базе данных Vitas-M соединения имеют уникальные идентификационные номера STK106769, STK394513, STK045765, STK105664, STK028127, STK376560 и STK045579, в их структуре R представляет собой следующие группы:
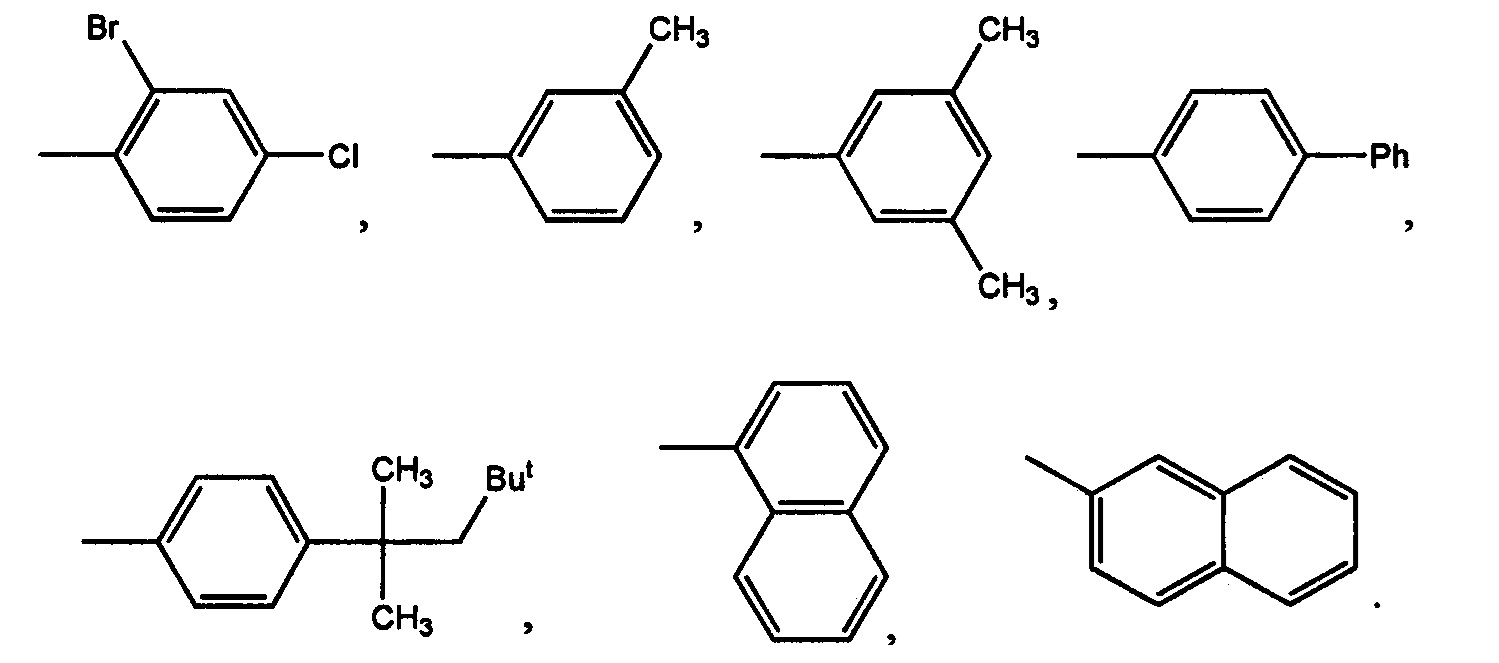
Краткое описание чертежей
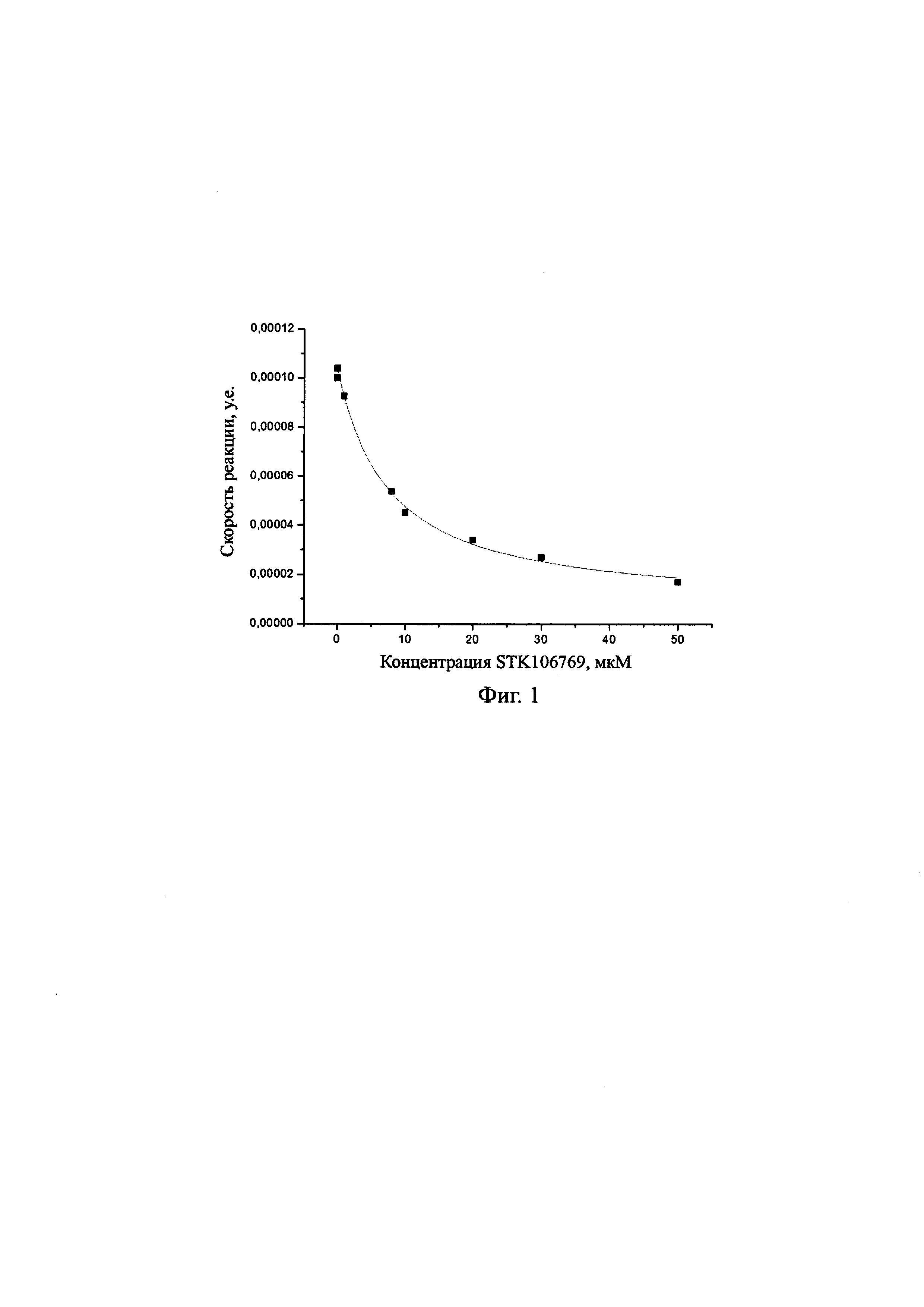
На Фиг. 1 представлена зависимость активности транскетолазы из Mycobacterium tuberculosis от концентрации ингибитора STK106769, измеренная по методике А.
Осуществление изобретения
Ниже представлено более подробное описание заявляемого изобретения. Настоящее изобретение может подвергаться различным изменениям и модификациям, понятным специалисту на основе прочтения данного описания. Такие изменения не ограничивают объем притязаний.
Для исследования ингибиторных свойств указанных соединений использовали следующие методики:
Методика А. Тестирование ингибиторной активности соединений проводили в отношении рекомбинантной транскетолазы из Mycobacterium tuberculosis. Для экспрессии транскетолазы из Mycobacterium tuberculosis использовали коммерчески доступную плазмиду рЕТ-19b (Евроген, Россия), несущую ген Rv1449с, а также ген устойчивости к ампициллину Amp. Культивирование, экспрессию, выделение и очистку фермента проводили по методике, известной из литературы [Fullam Е., Pojer F., Bergfors Т., Jones Т.А., Cole S.T. (2012) Open Biol., 2, 110026]. Для удаления кофакторов и получения апоформы фермента также использовали ранее описанную методику [Мешалкина Л.Е., Соловьева О.Н., Ходак Ю.А., Друца В.Л., Кочетов Г.А. (2010) Биохимия, 75, 992-1000]. Измерение активности транскетолазы в присутствии ингибиторов проводили по сопряженной реакции восстановления NAD+, катализируемой глицеральдегид-3-фосфатдегидрогеназой из мышц кролика [Kochetov G.A. (1982) Methods Enzymol., 90, 209-223]. Система для измерения активности содержала следующие компоненты: 50 мМ глицил-глицин, 3,2 мМ дитиотреитол, 10 мМ арсенат натрия, 2,5 мМ хлорид магния, 5 мкМ тиаминдифосфат, 70 мкМ ксилулозо-5-фосфат, 390 мкМ рибозо-5-фосфат, 370 мкМ NAD+, 2 Е глицеральдегид-3-фосфатдегидрогеназы, 0-1000 мкМ ингибитора (Vitas-M Laboratory), рН 7,4, 25°С. Реакцию начинали добавлением раствора апоформы транскетолазы в глицил-глициновом буфере. Скорость реакции регистрировали по увеличению оптической плотности раствора при 340 нм с помощью спектрофотометра Shimadzu UV-1800.
Методика Б. Тестирование противобактериальной активности ингибиторов транскетолазы из Mycobacterium tuberculosis проводили по стандартной методике [Sosunov V., Mischenko V., Eruslanov В., Svetoch E., Shakina Y., Stern N., Majorov K., Sorokoumova G., Selishcheva A., Apt A. (2007) J. Antimicrob. Chemother., 59, 919-925; Lyadova I., Yeremeev V., Majorov K., Nikonenko В., Khaidukov S., Kondratieva Т., Kobets N., Apt A. (1998) Infect. Immun., 66, 4981-4988]. Суспензии бактерий Mycobacterium tuberculosis штамм H37Rv из коллекции ЦНИИ туберкулеза РАН в среде RPMI-1640 с добавлением 2% эмбриональной телячьей сыворотки культивировали в лунках планшета. Ингибиторы (Vitas-M Laboratory) добавляли в лунки через 24 часа после начала культивирования до конечной концентрации 5 мМ. Затем бактерии инкубировали дополнительно 65 ч, при этом последние 18 ч в присутствии [3Н]-урацила (2 мкКи). Жизнеспособность микобактерий оценивали по уровню включения радиоактивной метки на сцинтилляционном счетчике.
В методиках А и Б для растворения ингибиторов могут быть использованы смешивающиеся с водой растворители, не оказывающие в конечной концентрации ингибирующего действия на транскетолазу из Mycobacterium tuberculosis.
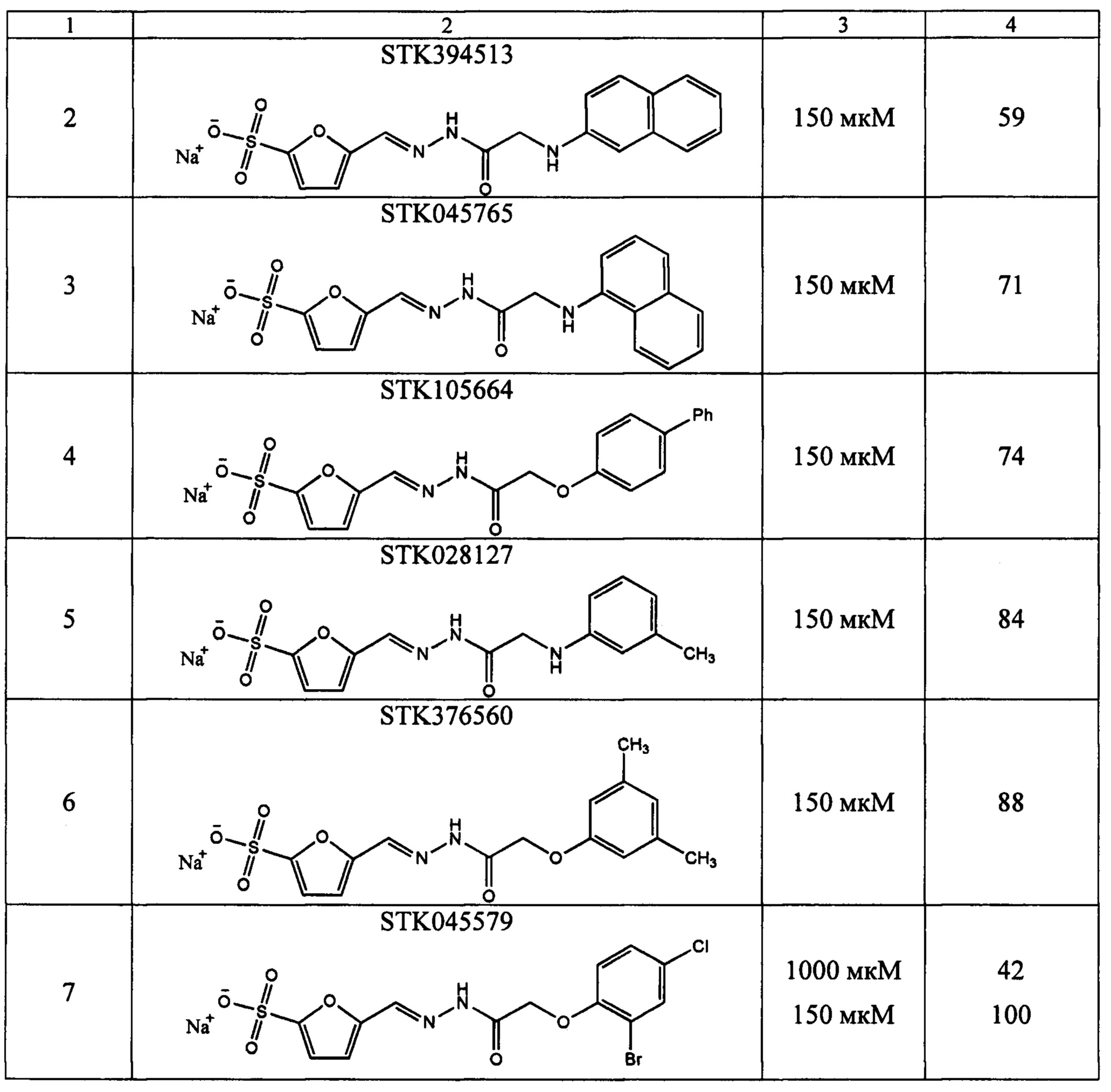
Результаты тестирования ингибиторных свойств соединений в отношении очищенного фермента из Mycobacterium tuberculosis (примеры 1-7) приведены в таблице 1.
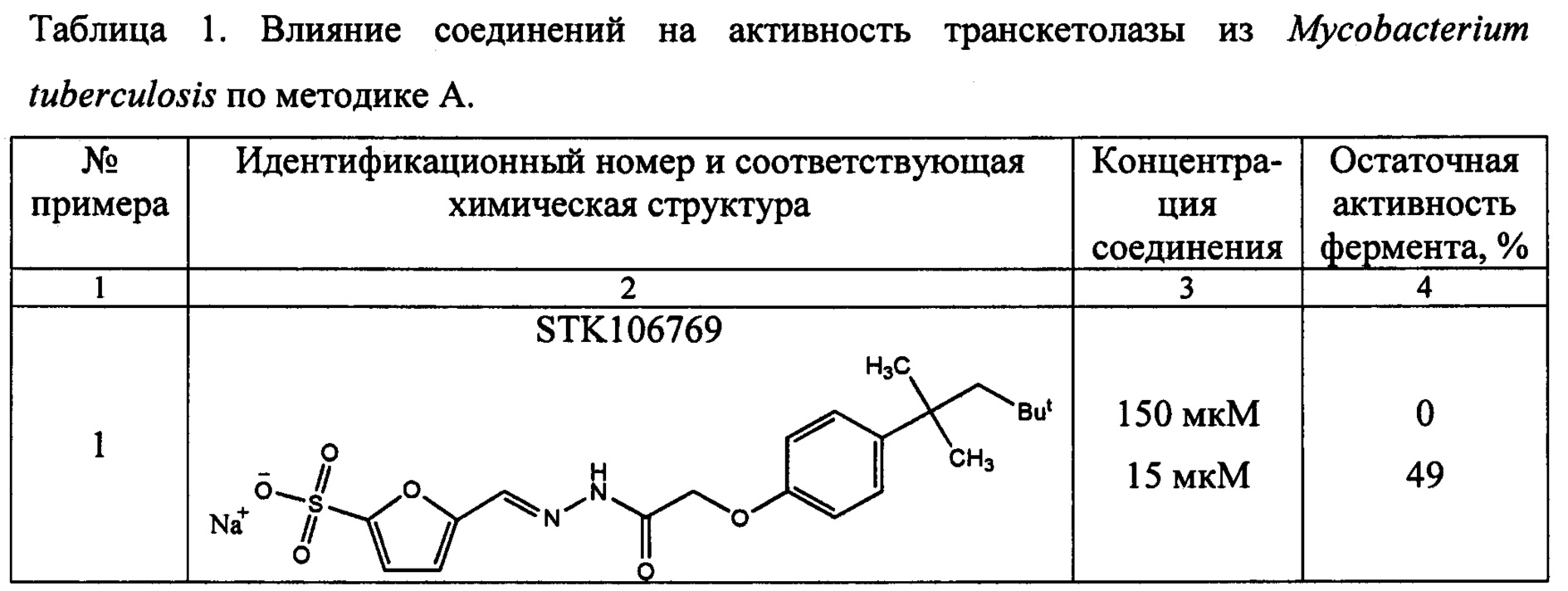
Пример 8. Значение IC50 для эффективного ингибитора STK106769 было определено по методике А путем варьирования его концентрации (см. фиг. 1) и составило 7 мкМ.
Пример 9. Раствор ингибитора STK106769 использовали для определения противотуберкулезной активности по методике Б. Подавление роста Mycobacterium tuberculosis, штамм H37Rv в присутствии ингибитора в концентрации 5 мМ составило 92%.
Пример 10. Раствор ингибитора STK394513 использовали для определения противотуберкулезной активности по методике Б. Подавление роста Mycobacterium tuberculosis, штамм H37Rv в присутствии ингибитора в концентрации 5 мМ составило 97%.
Пример 11. Раствор ингибитора STK045765 использовали для определения противотуберкулезной активности по методике Б. Подавление роста Mycobacterium tuberculosis, штамм H37Rv в присутствии ингибитора в концентрации 5 мМ составило 97%.
Представленные примеры свидетельствуют о том, что испытанные соединения способны подавлять активность транскетолазы из Mycobacterium tuberculosis в микромолярном диапазоне концентраций, а также тормозить рост данной патогенной бактерии.