Результат интеллектуальной деятельности: Способ количественного определения действующих веществ в лекарственных препаратах методом ИК-спектроскопии
Вид РИД
Изобретение
Заявлен способ, позволяющий определить количественное содержание сразу двух действующих веществ по построенной калибровочной модели, используя только одну серию препарата, предварительно проанализированную методом высокоэффективной жидкостной хроматографии, далее ВЭЖХ. С помощью данного подхода разработаны калибровочные модели для спектральных данных полученных в средней и ближней ИК-области, а также для метода комбинационного рассеяния. Проведено количественное сравнение полученных калибровочных моделей и подтверждена их применимость с помощью нормативного метода.
Известные аналоги с недостатками.
А) Для построения калибровки при количественном определении действующих веществ (ДВ) методом ИК-спектроскопии используют смеси стандартных (СО) образцов с бромидом калия, который выступает в качестве матрицы или разбавителя. Таким образом меняя соотношение СО и бромида калия можно получить набор калибровочных смесей с различным содержанием ДВ в требуемом диапазоне. На основе этих смесей строится калибровочная модель для количественного определения. [Sherazi, S.T.H. Application of Fourier transform infrared (FT-IR) transmission spectroscopy for the estimation of roxithromycin in pharmaceutical formulations / S.T.H. Sherazi, M. Ali, S.A. Mahesar // Vibrational Spectroscopy. – 2011. – Vol. 55, №1. – P. 115–118]. Недостатком данного метода является замена вспомогательных компонентов, входящих в состав препарата, на бромид калия, что может искажать спектр образца вследствие отсутствия положительной или отрицательной интерференции ДВ и вспомогательных компонентов препарата. Кроме этого вспомогательные компоненты могут иметь довольно интенсивные полосы поглощения — это может привести к ошибке в выборе спектрального диапазона при построении калибровочной модели и как следствие к получению недостоверных результатов анализа. В данной работе проведен сравнительный анализ качества калибровочной модели и достоверности полученных результатов, полученных методом разведения ДВ бромидом калия и предложенной методики.
Б) Известен метод калибровки в котором для построения модели в качестве калибровочных стандартов используются препараты с известным содержанием ДВ, которое определяется альтернативными методами (ВЭЖХ, титрование, УФ-спектрометрия и т.д.). Данный подход позволяет избежать потери спектральных данных присущих методу А, но он существенно сложнее в практическом применении. Это связано с необходимостью наличия большого количества образцов препарата с разной концентрацией, измеренной альтернативным способом. Так в зависимости от метода обработки данных необходимо от 3n+1 до 10n+1 и более образцов препарата, где n это количество определяемых компонентов (ДВ). Второй трудностью является степень охвата допустимого диапазона концентраций стандартными образцами. Сложность обусловлена тем, что методы количественного определения не поддерживают экстраполяцию калибровочной модели, иными словами, калибровочная модель работает только в области, ограниченной крайними точками калибровочного графика [Государственная фармакопея Российской Федерации, XIII издание, Москва (2015)]. На практике сложно сделать выборку препаратов для построения калибровочной модели, которые бы охватывали весь допустимый для данного действующего вещества диапазон концентраций. Естественно, ситуация значительно усложняется в случае многокомпонентных препаратов.
Задачи.
1. Предложенный метод построения калибровки позволяет учесть влияние вспомогательных компонентов препарата на спектр образца, что позволяет провести статистически достоверный анализ содержания сразу двух действующих веществ методом ИК-спектроскопии, например, на примере трех серий препарата «Каниквантел плюс».
2. Для построения калибровочной модели достаточно одной серии препарата с известным содержанием ДВ, полученным альтернативным методом (например, методом высокоэффективной жидкостной хроматографии - ВЭЖХ).
Технический результат – повышение точности и скорости измерений сразу двух действующих веществ препарата.
Технический результат достигается тем, что способ количественного определения действующих веществ в лекарственных препаратах методом ИК-спектроскопии включает:
- измельчение и перемешивание оригинального лекарственного препарата, содержащего действующие вещества А и Б, до получения однородной смеси 1;
- анализ полученной однородной смеси 1 методом ИК-спектроскопии с получением спектрограммы 1;
- смешивание и перемешивание до 50% полученной однородной смеси 1 с действующим веществом А, в количестве (2,3–2,6)% от массы однородной смеси 1 с получением однородной смеси 2,
- анализ полученной однородной смеси 2 методом ИК-спектроскопии с получением спектрограммы 2;
- смешивание и перемешивание однородной смеси 2 с действующим веществом А, в количестве (2,3–2,6)% от массы однородной смеси 2 с получением однородной смеси 3,
- анализ полученной однородной смеси 3 методом ИК-спектроскопии с получением спектрограммы 3;
- смешивание и перемешивание однородной смеси 3 с действующим веществом А, в количестве (2,3–2,6)% от массы однородной смеси 3 с получением однородной смеси 4,
- анализ полученной однородной смеси 4 методом ИК-спектроскопии с получением спектрограммы 4;
- смешивание и перемешивание однородной смеси 4 с действующим веществом А, в количестве (2,3–2,6)% от массы однородной смеси 4 с получением однородной смеси 5,
- анализ полученной однородной смеси 5 методом ИК-спектроскопии с получением спектрограммы 5;
- смешивание и перемешивание однородной смеси 5 с действующим веществом А, в количестве (2,3–2,6)% от массы однородной смеси 5 с получением однородной смеси 6,
- анализ полученной однородной смеси 6 методом ИК-спектроскопии с получением спектрограммы 6;
- смешивание и перемешивание оставшейся полученной однородной смеси 1 с действующим веществом Б, в количестве (14,7–55,9)% от массы однородной смеси 1 с получением однородной смеси 7,
- анализ полученной однородной смеси 7 методом ИК-спектроскопии с получением спектрограммы 7;
- смешивание и перемешивание однородной смеси 7 с действующим веществом Б, в количестве (14,7–55,9)% от массы однородной смеси 7 с получением однородной смеси 8,
- анализ полученной однородной смеси 8 методом ИК-спектроскопии с получением спектрограммы 8;
- смешивание и перемешивание однородной смеси 8 с действующим веществом Б, в количестве (14,7–55,9)% от массы однородной смеси 8 с получением однородной смеси 9,
- анализ полученной однородной смеси 9 методом ИК-спектроскопии с получением спектрограммы 9;
- смешивание и перемешивание однородной смеси 9 с действующим веществом Б, в количестве (14,7–55,9)% от массы однородной смеси 9 с получением однородной смеси 10,
- анализ полученной однородной смеси 10 методом ИК-спектроскопии с получением спектрограммы 10;
- смешивание и перемешивание однородной смеси 10 с действующим веществом Б, в количестве (14,7–55,9)% от массы однородной смеси 10 с получением однородной смеси 11,
- анализ полученной однородной смеси 11 методом ИК-спектроскопии с получением спектрограммы 11;
- получение калибровочной модели оригинального лекарственного препарата из полученных спектрограмм 1-11: выделение участков спектров, соответствующих веществам А и Б, и регистрация изменения высоты пиков в зависимости от концентрации вещества А или Б с получением калибровочной модели,
- измельчение и перемешивание исследуемого лекарственного препарата, содержащего действующие вещества А и Б, до получения однородной смеси 12,
- анализ полученной однородной смеси 12 методом ИК-спектроскопии с получением спектрограммы 12 и
- определение концентраций веществ А и Б исследуемого лекарственного препарата, с помощью полученной калибровочной модели по известным математическим методам, например был использован статистический метод Stepwise Multiple Linear Regression (множественная линейная регрессия).
При этом на каждом этапе анализа полученной однородной смеси методом ИК-спектроскопии получают 3 спектрограммы, с последующим усреднением полученных значений интенсивности на выбранных спектральных диапазонах.
Предпочтительно лекарственным препаратом является Каниквантел Плюс (производитель фирма «Euracon Pharma GmbH», Германия) содержащий действующие вещества Празиквантел и Фенбендазол.
Заявленное изобретение поясняется Фиг. 1 и Фиг. 2.
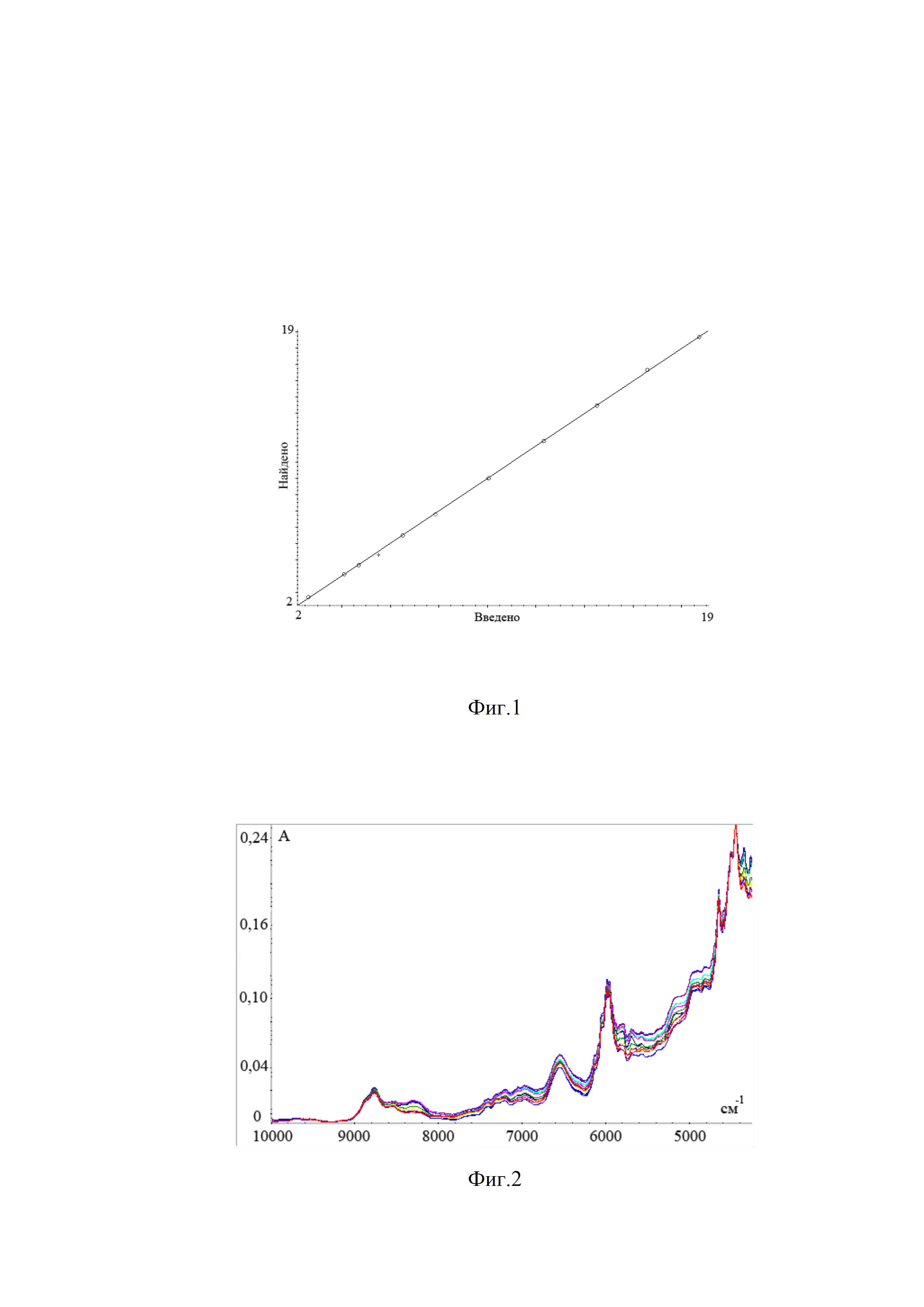
Фиг. 1. График соответствия истинной и вычисленной по спектральным данным концентрации Празиквантела, полученным на оптоволоконном зонде.
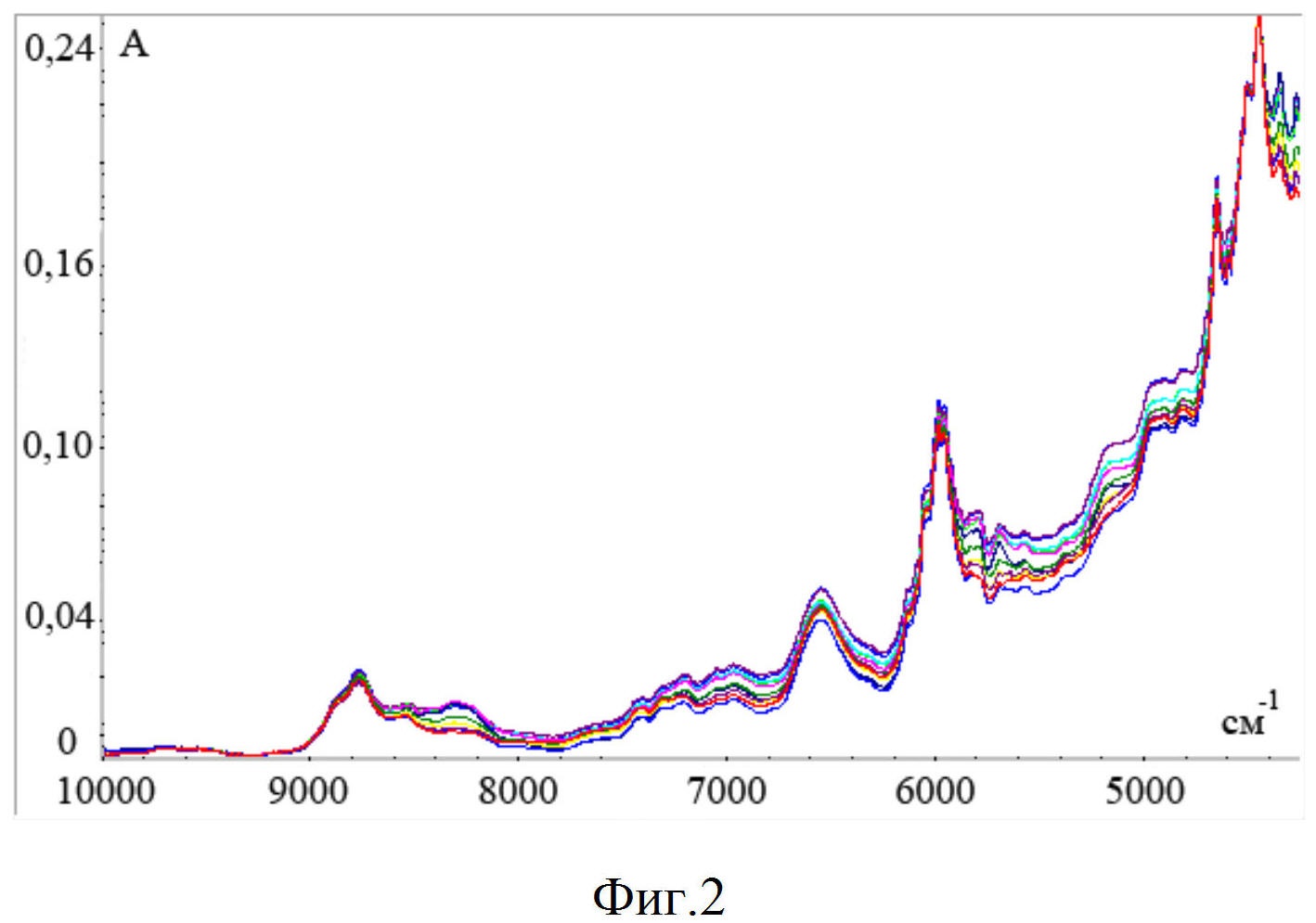
Фиг. 2. Спектры калибровочных смесей препарата Каниквантел Плюс зарегистрированные с помощью оптоволоконного зонда.
Экспериментальная часть
Для проведения исследования в качестве модельного препарата был использован лекарственный препарат для ветеринарии Каниквантел Плюс (фирма «Euracon Pharma GmbH», Германия). В качестве действующих веществ в 1 таблетке Каниквантела Плюс содержится 500 мг фенбендазола и 50 мг празиквантела, а также вспомогательные вещества: натрия лаурилсульфат - 10 мг, поливидон - 20 мг, ароматизатор со вкусом мяса - 12 мг, магния стеарат - до 0,6 г.
Для работы использовался ИК-Фурье спектрометр с Фурье-Раман модулем и блоком для ближней ИК-спектроскопии Thermo Scientific Nicolet iS50, США. Спектры в среднем ИК-диапазоне регистрировали методом нарушенного полного внутреннего отражения (далее - НПВО) с алмазным монолитным кристаллом. Работы в ближнем ИК-диапазоне проводили в режиме диффузного отражения с использованием интегрирующей сферы, а также с помощью оптоволоконного зонда.
Для анализа таблетку извлекали из упаковки и растирали в агатовой ступке. Затем порошок анализировали методом ИК-спектроскопии и комбинационного рассеяния света согласно стандартной методологии, описанной в инструкции по применению прибора. Для увеличения соотношения сигнал-шум каждый спектр был получен усреднением 32х сканов. Разрешение и прочие характеристики приведены в таблице 1 Параметры регистрации спектров.
Стандарты для построения калибровочной модели готовили исходя из одной серии препарата (Серия №16I19B). Предварительно содержание действующих веществ было определено по методике, изложенной в нормативном документе на препарат Каниквантел Плюс (ВЭЖХ).
Поскольку для построения калибровочной модели необходимо иметь весь диапазон концентраций действующих веществ в пределах заложенного производителем диапазона, недостающие соотношения действующих веществ получали смешиванием порошка препарата со стандартными образцами (СО) Празиквантел и Фенбендазол. После добавления навески стандартного образца Празиквантел смесь тщательно растирали в агатовой ступке и затем регистрировали спектры не менее 3 раз. Для подтверждения гомогенности смеси использовали программные методы анализа степени соответствия спектров. Затем к полученной смеси добавляли следующую навеску СО Празиквантела и все операции повторяли. Вес празиквантела выбирали такой, чтобы его содержание в полученных смесях равномерно перекрывало калибровочный график в требуемом диапазоне. Навеску СО Фенбендазол добавляли к исходному порошку препарата и проводили аналогичные процедуры. Вес фенбендазола выбирали такой, чтобы его содержание в полученных смесях равномерно перекрывало калибровочный график в требуемом диапазоне. Таким образом для каждого действующего вещества было получено по 5 смесей с известной концентрацией компонентов, что позволило использовать для построения калибровочной модели 11 калибровочных точек (исходный препарат, 5 смесей с Празиквантелом и 5 смесей с Фенбендазолом). Диапазон концентраций, охватываемый калибровочным графиком, составил для Празиквантела от 2,63% до 18,71%, а для Фенбендазола от 68,45% до 92,47%. Соотношения концентраций действующих веществ представлены в таблице 2.
Для количественного определения действующих веществ использовали статистический метод Stepwise Multiple Linear Regression (множественная линейная регрессия), представляющий концентрацию как функцию поглощения при разных частотах. Постобработка спектральных данных состояла в коррекции длины оптического пути методом Standard Normal Variate (стандартное отклонение случайной величины с нормальным распределением), коррекции базовой линии инструментом Spline Correction. Для расчета использовали вторые производные спектров ближнего ИК-диапазона и первые производные для спектров среднего ИК-диапазона и комбинационного рассеяния. Для устранения артефактов преобразования использовали фильтр Норриса.
Для калибровки по празиквантелу в среднем ИК-диапазоне использовали линии колебания циклогексанового кольца (2787 см-1) и третичного амида (1676 см см-1). В ближнем ИК-диапазоне использовали линии на 4351 см-1 и 8547 см-1 (оптоволоконный зонд), 4266 см см-1, 7243 см см-1 (интегрирующая сфера). В спектрах комбинационного рассеяния света использовали линии колебания карбонильной группы (2832 см-1) и линию 2230 см-1.
Для калибровки по фенбендазолу в среднем ИК-диапазоне использовали линии сульфидной связи (806 см см-1 и 485 см-1). В ближнем ИК-диапазоне использовали линии на 5627 см-1, 4652 см-1 (оптоволоконный зонд), 4493 см-1, 6626 см-1 (интегрирующая сфера). В спектрах комбинационного рассеяния света использовали линии колебания карбонильной группы (2832 см-1) и линии колебания валентных связей С=С в ароматическом кольце (1562 см-1).
На основе 11 спектрограмм строится калибровочный график зависимости интенсивности пиков Фиг. 2, соответствующих каждому компоненту от концентрации этого компонента в смеси. Полученному графику соответствует уравнение регрессии. Далее из уравнения регрессии, построенного на значениях интенсивности пиков, вычисляли концентрацию неизвестного вещества.
Оценку правильности и воспроизводимости полученной калибровки проводили методом перекрестной валидации (Таблица 3). Диагностическая процедура перекрестной валидации показывает, насколько хорошо прошедший калибровку количественный метод способен проанализировать калибровочные стандарты, как если бы они были валидационными стандартами. Для оценки качества калибровочной модели использовали значение средней величины модуля относительной ошибки калибровки (Md) которое вычисляется по формуле:
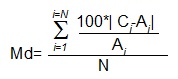
Где С – рассчитанное значение концентрации,
А – истинное значение концентрации,
N – число точек калибровочной модели.
Для подтверждения правильности получаемых результатов было проведено сравнение с результатами, полученными с помощью нормативного метода – ВЭЖХ (Таблица 5). Относительную ошибку рассчитывали по формуле:
Относительная ошибка = 100*|IR-HPLC|/HPLC,
где IR – результат измерения концентрации методом ИК-спектрометрии,
HPLC - результат измерения концентрации нормативным методом ВЭЖХ.
Результаты и их обсуждение.
По результатам перекрестной валидации наименьшее расхождение между вычисленным и истинным значением концентрации стандартных смесей показал метод спектрометрии в ближней инфракрасной области (далее – метод БИК) с применением оптоволоконного зонда Фиг. 1. Метод с использованием интегрирующей сферы также показал хорошее качество калибровочной модели для обоих действующих компонентов препарата. Комбинационное рассеяние и НПВО-метод в среднем ИК-диапазоне показали ошибку калибровочной модели более 4% для минорного компонента препарата – Празиквантела преимущественно в области низких концентраций (Таблица 3) Однако содержание действующего вещества Фенбендазол этими методами определяется с хорошей достоверностью во всем диапазоне концентраций.
Значения коэффициентов корреляции между истинными и вычисленными на основе спектральных данных значениями концентрациями действующих веществ также было более высоким для методов БИК (Таблица 4 Коэффициенты корреляции и точность калибровки).
В качестве основного критерия применимости в практике разработанных методик является соответствие результатов анализа данным, полученным с помощью валидированного нормативного метода (ВЭЖХ). В таблице 5 приведены результаты измерения концентрации действующих веществ нормативным и спектральными методами во всех 3 сериях препарата. Видно, что расхождения данных для методов БИК составило около 2%, что не превышает допустимую ошибку определения, установленную для нормативного метода - 4%. При этом результаты, полученные по спектрам комбинационного рассеяния, а также в среднем ИК-диапазоне, имеют большее расхождение с нормативным методом – до 3,98% и 8,01% соответственно. При этом максимальная ошибка также наблюдалась при определении минорного компонента – Празиквантела.
Воспроизводимость результатов анализа оценивали по величине среднеквадратического отклонения (RSD). Так для методов БИК-спектрометрии значение RSD не превышало 2% в 3 параллельных измерениях. RSD для метода НПВО составило около 4%. Максимальное расхождение в результатах параллельных измерений было зафиксировано в методе комбинационного рассеяния (RSD=5%).
Из приведенных данных видно, что ошибка калибровки, относительная ошибка определения и воспроизводимость для Празиквантела хуже, чем для Фенбендазола, что, очевидно, связано с 10-кратной разницей их содержания в препарате.
Для сравнения предложенной методики и известными аналогами были приготовлены калибровочные смеси на основе бромида калия в качестве матрицы. К навеске бромида калия добавляли известное количество СО Празиквантела и Фенбендазола в таком соотношении, чтобы воспроизвести соотношения концентраций действующих веществ в первом эксперименте. Результаты анализа трех серий препарата «Каниквантел Плюс» с использованием калибровки на основе матрицы из бромида калия представлены в таблице 6.
Из представленных данных видно, что предложенная методика построения калибровки имеет явное преимущество перед известными аналогами для определения содержания двух действующих веществ на примере измерения концентрации Празиквантела и Фенбендазола в препарате «Каниквантел Плюс». Ошибка определения содержания действующих веществ предложенным способом в среднем была менее 2% (Кроме метода комбинационного рассеяния света), в то время как ранее предложенный метод на основе матрицы из бромида калия не позволяет получить достоверный результат измерения концентрации действующих веществ.
Разработанная методика экспресс-анализа может быть использована, как в лабораториях контроля качества на производстве, так и в организациях, контролирующих качество лекарственных препаратов.
Способ количественного определения действующих веществ в лекарственных препаратах методом ИК-спектроскопии
|
* Для комбинационного рассеяния использовали лазер мощность 0,1Вт (λ=1064нм).
Таблица 1
|
Таблица 2
|
Таблица 3 Таблица показателей качества калибровочной модели по данным перекрестной валидации.
|
Таблица 4 Коэффициенты корреляции и точность калибровки.
|
Таблица 5 Результаты определения содержания Празиквантела и Фенбендазола в препарате Каниквантел Плюс спектральными методами и нормативным методом – ВЭЖХ.
|
Таблица 6 Результаты определения содержания Празиквантела и Фенбендазола в препарате Каниквантел Плюс спектральными методами с использованием калибровки на основе матрицы из бромида калия и нормативным методом – ВЭЖХ.