Результат интеллектуальной деятельности: Способ получения керамических гранул для регенерации костной ткани
Вид РИД
Изобретение
Область техники
Изобретение относится к способу изготовления керамического материала для замещения дефектов костных тканей в области ортопедии, стоматологии, травматологии, реконструктивно-восстановительной, челюстно-лицевой хирургии, нейрохирургии, онкологии и в качестве матриксов-носителей для генных конструкций (в частности, плазмидной ДНК), клеток, факторов роста и других биологически активных веществ.
Уровень техники
Для восстановления костной ткани в последнее десятилетие разработаны методы тканевой инженерии, основанные на имплантировании в место костного дефекта биоконструкции, состоящей из пористого матрикса и культивированных в нем остеообразующих клеток. Наиболее перспективными материалами матрикса являются фосфаты кальция. Обычно для этой цели используют гидроксиапатит (ГА), трикальцийфосфат (ТКФ), карбонат-содержащий ГА или их сочетания. Однако применение этих материалов связанно с определенными недостатками, в частности плохо согласующейся кинетикой биологической деградации с кинетикой остеогенеза и низкими остеокондуктивными потенциями. В самое последнее время усилия исследователей направлены на создание материалов матриксов из прекурсоров формирования биологического апатита в организме человека. Одним из возможных прекурсоров является октакальциевый фосфат (ОКФ), который, как полагают, проявляет не только остеокондуктивность, но и остеоиндуктивные качества - способность индуцировать формирование костной ткани. Однако ОКФ - термически нестабильное соединение, разлагающееся при температуре выше 150°С, из которого невозможно изготовить керамику посредством традиционной керамической технологии с использованием конечной стадии спекания. Поэтому актуальной задачей является разработка альтернативных методов формирования пористых матриксов из термически нестабильных фосфатов кальция, таких как ОКФ, с заданной микроструктурой и архитектоникой.
Наиболее близким по техническому решению и достигаемому результату является работа по получению гранул ОКФ (B.C. Комлев, А.Ю. Федотов. Патент на изобретение №2596504 Способ получения керамики на основе октакальциевого фосфата). В данной работе использовали гранулы α-трикальцийфосфата (α-ТКФ) размером 150-2000 мкм как исходный материал. Трансформацию гранул осуществляли следующим образом:
- трансформация гранул α-трикальцийфосфата в дикальцийфосфат дигидрат в растворе 1,5 М раствор ацетата натрия и 0,15±0,02 М глутаминовой аминокислоты, доведенный ортофосфорной кислотой до значения рН 5,5 (раствор АП), с соотношением гранул α-трикальцийфосфата и раствора АП 1:100 в течение 7 суток при температуре 35±1°С;
- трансформация дикальцийфосфат дигидрата в растворе БП с рН 8,7±0,1, с соотношением дикальцийфосфат дигидрата и 1,5 М раствора ацетата натрия со значением рН 8,7 (раствор БП) 1:100 в течение 7 суток при температуре 35±1°С;
- термическая обработка полученных гранул при 130°С в течение двух часов.
В настоящем техническом решении предложен способ трансформации керамики на основе карбоната кальция (КК, СаСО3) в ОКФ при физиологических температурах. Данный способ позволяет проводить трансформацию с изменением фазового состава керамики, морфологии поверхности и, как следствие, увеличением удельной поверхности и значений рН материала.
Раскрытие изобретения
Задачей и техническим результатом настоящего изобретения является получение керамических гранул октакальциевого фосфата (ОКФ) на основе гранул КК заданного размера с развитой микроструктурой, высокой удельной поверхностью и повышенным значениями рН для формирования пористых матриксов.
Такие гранулы обладают оптимальной кинетикой резорбции, могут обеспечить эффективное восстановление и реконструкцию поврежденных костных тканей и могут использоваться в качестве матриксов-носителей для генных конструкций (в частности, плазмидной ДНК), клеток, факторов роста и других биологически активных веществ.
Поставленная задача решается путем разработки способа изготовления керамических гранул с взаимосвязанной пористостью 40-70% на основе частиц октакальциевого фосфата пластинчатой формы, имеющих следующий фазовый состав:
- 85-95 масс. % октакальциевого фосфата,
- 0-5% масс. % гидроксиапатита,
- 5-10% масс. % карбоната кальция,
включающего следующие этапы:
- трансформация гранул карбоната кальция в дикальцийфосфат дигидрат в растворе А с рН 4,1±0,1, с соотношением карбоната кальция и раствора А 1:100 в течение 7 суток при температуре 40±1°С, понижение рН раствора со значения 5,5 в прототипе до 4,1 обусловлено тем, что гранулы КК создают щелочную среду и для обеспечения трансформации гранул в полном объеме, необходимо понижение значения рН процесса;
- трансформация дикальцийфосфат дигидрата в растворе Б с рН 9±0,1, с соотношением дикальцийфосфат дигидрата и раствора Б 1:100 в течение 7 суток при температуре 40±1°С, повышение значений рН с 8,7 до 9 позволяет получить более чистый конечный продукт;
- термическая обработка полученных гранул при 130°С в течение двух часов;
где раствор А - водный 2 М раствор дигидроортофосфата аммония при значении рН 4,1±0,1, раствор Б - водный 2 М раствор ацетата натрия со значением рН 9±0,1.
Размер получаемых гранул зависит от исходных размеров гранул карбоната кальция. Таким образом, размер получаемых гранул может быть задан путем выбора размера исходных гранул. Предпочтительными являются гранулы, размеры которых составляют 150-500, 500-1000 или 1000-2000 мкм.
Получаемые гранулы представляют собой частицы пластинчатой формы (размеры частиц - толщина 0,3±0,1 мкм, длина 15±5 мкм и ширина 8±2 мкм), которые формируют керамический каркас с взаимосвязанной пористостью 40-70% (доминирующая популяция пор относится к порам размером 1-500 мкм на поверхности и 20-300 мкм внутри), и имеют следующий фазовый состав: 85-95 масс. % октакальциевого фосфата, 0-5% масс. % гидроксиапатита, 5-10% масс. % КК. Атомное соотношение элементов получаемых гранул Са/Р составляет 1,33±0,25.
Проведенные эксперименты показали, что величина предельной адсорбционной способности получаемых гранул равна 1,1±0,05 ммоль/г.; величина удельной поверхности равна 40±1 м2/г (20±1 м2/г прототип); величина адсорбции растворов бычьего сывороточного альбумина и лизата тромбоцитов доноров на поверхности материала для исходной концентрации белка в растворе 1,2 мг/мл равна 86,5% и 59,7%, соответственно; значение рН равно 7,7.
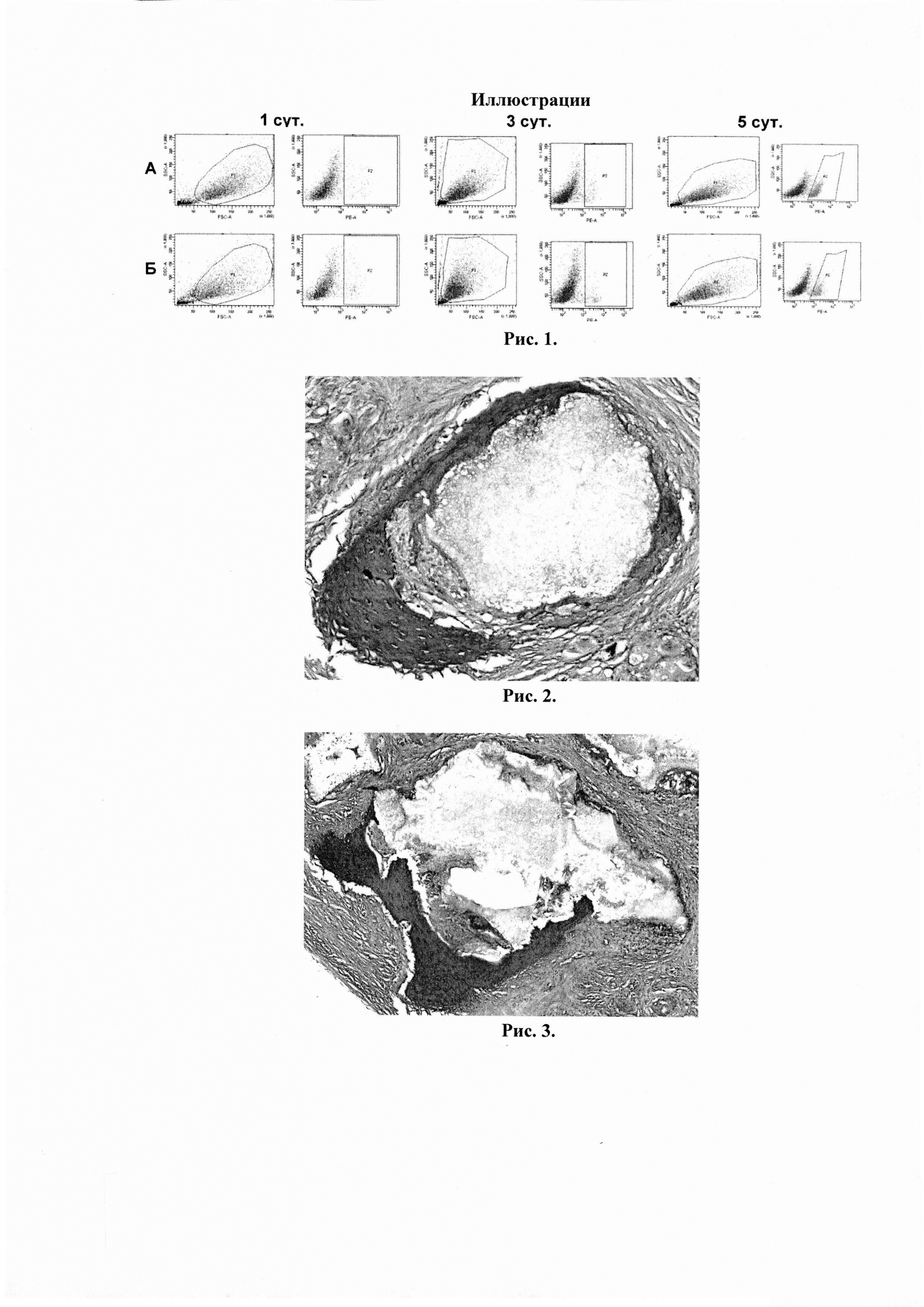
Биологические исследования ОКФ in vitro показали отсутствие цитотоксического действия материала на живые мезенхимальные стволовые клетки. В ходе оценки цитотоксического действия ОКФ с использованием проточной цитофлуориметрии определялось количество погибших и живых клеток в культуре. Гистограммы распределения клеток представлены на рисунке 1.
Не было выявлено статистически значимых различий в численности погибших клеток при сравнении экспериментальных групп с контрольной - интактной культурой ММСК.
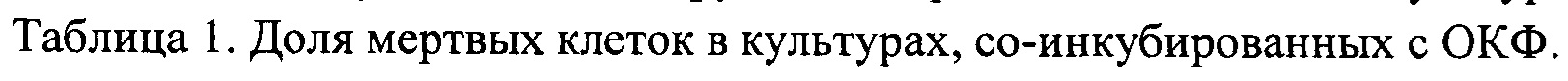
Полученные данные подтверждают отсутствие цитотоксичности ОКФ.
При оценке пролиферативной активности клеток было выявлено, что через 3 и 5 сут. после начала эксперимента количество клеток в культурах, со-инкубированных с ОКФ, было меньшим, а на сроке в 7 сут. даже большим, чем в контроле, однако различия не были статистически значимы.
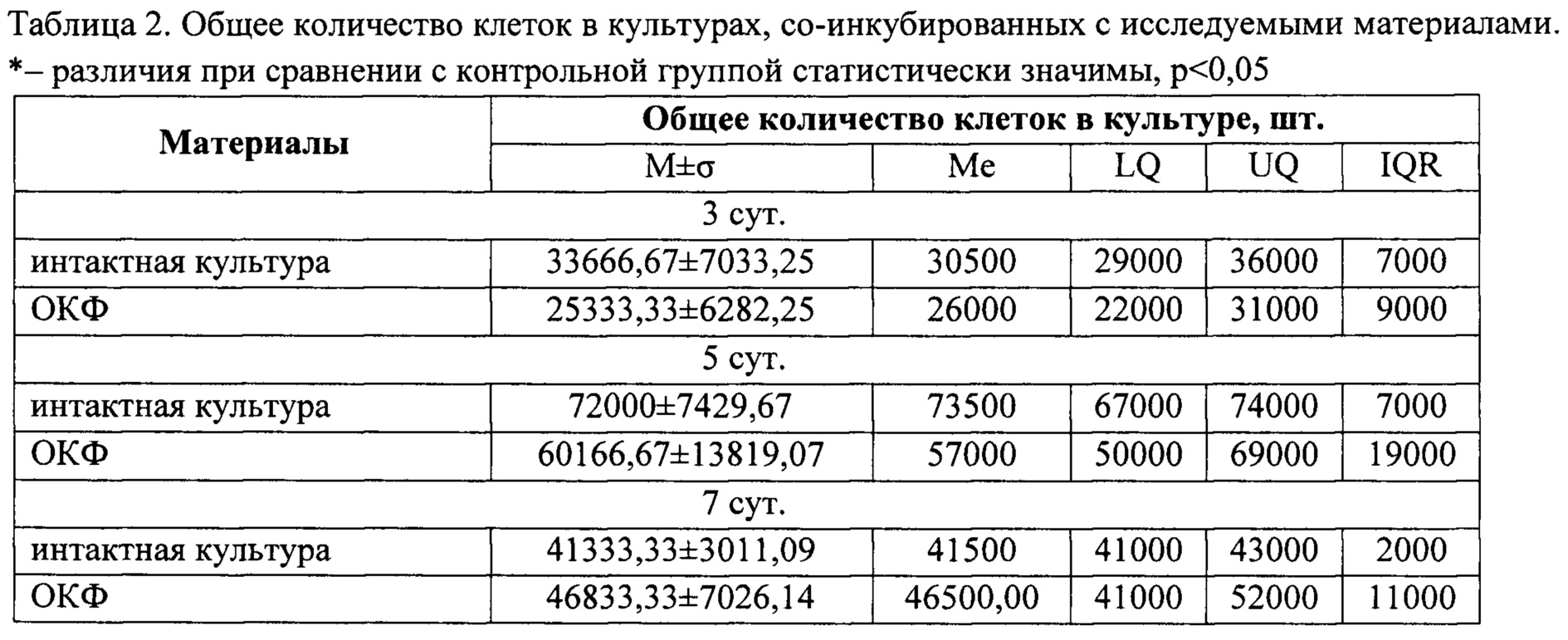
Средняя скорость удвоения интактных культур ММСК в исследовании составила 42,41±5,78 ч., а в случае со-инкубирования с ОКФ - 51±8,32, однако различия не были статистически значимыми.
Таким образом, ОКФ не обладает цитотоксическими свойствами и существенно не снижает пролиферативную активность клеток in vitro.
При имплантации ОКФ в краниальные дефекты кроликам, гистологические исследования на 30 сутки после имплантации показали, что большая часть костного дефекта замещена реактивно измененной рыхлой волокнистой соединительной тканью (РВСТ), окружающей гранулы ОКФ. Образование костной ткани наблюдалось, главным образом, со стороны опилов теменных костей: средняя протяженность костного регенерата составляла 1-1,5 мм. Важным показателем является то, что периферически расположенные гранулы материала непосредственно контактировали с костной тканью опилов теменных костей без формирования какой либо соединительнотканной прослойки, капсулы. Периферический костный регенерат окружал «приграничные» гранулы ОКФ, формируя своеобразные «мостики» от одной гранулы к другой, что служит прямым подтверждением оптимальных остеекондуктивных свойсв материала и крайне значимо для медицинских изделий, показанных для замещения костных дефектов. Кроме того, у некоторых гранул материала, расположенных на удалении от границ дефекта, определялись участки репаративного остеогистогенеза в виде «ободков» новообразованной ретикулофиброзной костной ткани толщиной от 10 до 105 мкм (рис. 2) Через 60 сут после имплантации ОКФ центральная часть дефекта длиной 6,5-7 мм была заполнена преимущественно РВСТ, протяженность костного регенерата из опилов теменных костей составила более 3 мм. При этом была выявлена характерная особенность -асимметрия новообразования костной ткани: большая выраженность регенерата с одной из сторон. По всей видимости, такая особенность обусловлена анатомическими предпосылками экспериментальной модели: при выполнении билатеральных дефектов теменных костей расстояние между дефектами составляет 2-3 мм по саггитальному шву, тогда как латерально дефекты ограничены большим объемом нативной кости (часть теменной и височная кости). Кроме того, крупные сосуды, кровоснабжающие кости черепа, также проходят с боковых сторон.
Важно отметить, что гранулы ОКФ, находящиеся на расстоянии 2,6-3 мм от одного из краев периферического костного регенерата были окружены новообразованной костной тканью, источником формирования которой, вероятно, являлись теменные кости. Иными словами, рост регенерата с периферии был поддержан гранулами ОКФ, выполняющими остеокондуктивную роль. На препарате же в виду специфики метода исследования (срез толщиной 10 мкм) костный регенерат, исходящий с периферии и переходящий от одной гранулы ОКФ к другой, выявлялся в виде не всегда связанных друг с другом «ободков», окружающих гранулы ОКФ. Более того, в ряде случаев даже в центральной части дефекта определялись единичные гранулы ОКФ, окруженные новообразованной костной тканью, которая либо являлась продолжением периферического костного регенерата, либо исходно сформировалась в центре дефекта под действием имплантированного материала, что можно рассматривать как остеоиндуктивное действие ОКФ (рис. 3).
Процесс биодеградации гранул на сроке в 60 сут. после операции был более выражен за счет большего количества визуализирующихся у поверхности имплантированного материала гигантских многоядерных клеток инородных тел и остеокластов. При этом резорбирующие гранулы клетки также определялись между поверхностью гранул и окружающим ее костным регенератом - в участках периваскулярной РВСТ. Иными словами, процесс биорезорбции ОКФ был «синхронен» формированию костной ткани.
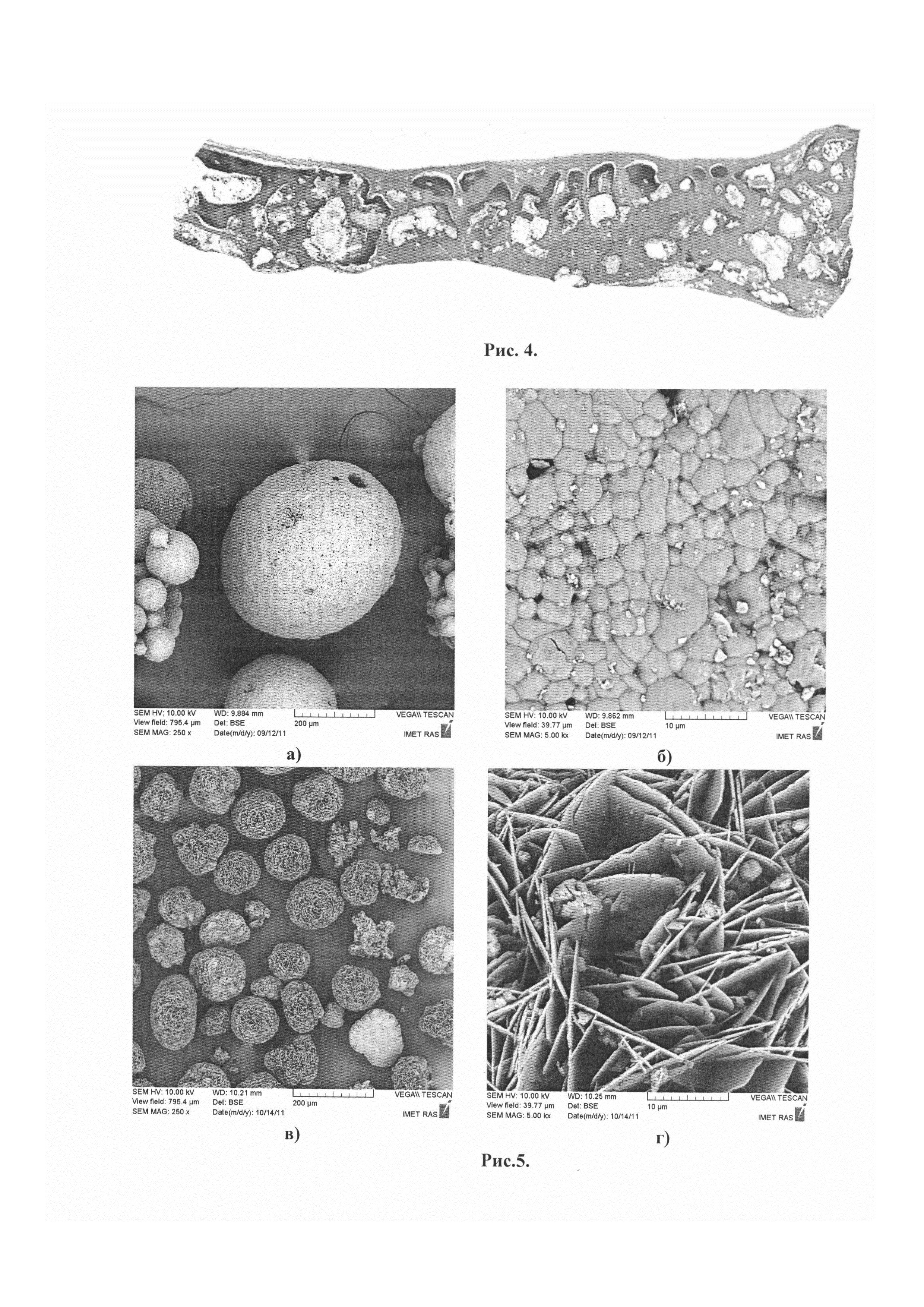
Через 90 сут. после выполнения операции костный регенерат прослеживался от одного опила теменной кости до другого. В периферических зонах новообразованная костная ткань была более объемной. В центральной части дефекта - прослеживалась, главным образом, вокруг гранул имплантированного материала. Участки дефекта, свободные от гранул, были выполнены РВСТ. Таким образом, к данному сроку наблюдения ОКФ обеспечивал восстановление целостности теменной кости (рис. 4).
Характерной особенностью репаративного остеогистогенеза на данном сроке наблюдения оказалось наличие костного регенерата как из ретикулофиброзной, так и из пластинчатой костной ткани. При этом участки, непосредственно контактирующие с гранулами ОКФ были представлены пластинчатой костной тканью, которая к периферии сменялась ретикулофиброзной костной тканью, переходящей далее в РВСТ. Таким образом, выявленные морфологические признаки можно расценивать как подтверждение продолжающегося репаративного остеогистогенеза: сформированный ранее вокруг гранул ОКФ костный регенерат к данному сроку подвергался ремоделированию в пластинчатую костную ткань, а формирующаяся позже костная ткань еще сохраняла ретикулофиброзное строение.
По результатам гистоморфометрического анализа было установлено, что уже к 60 суткам периферические зоны костного дефекта характеризуются долей костного регенерата, превышающей 30%, при нормализованном значении, рассчитанном по такой же гистоморфометрической методике, в 50-55%. При этом наиболее выраженная положительная динамика была выявлена именно в центральной части дефекта, где прирост доли костного регенерата при сравнении показателя на сроках 60 и 90 сут составил 13,9%.
Таким образом, ОКФ обладает оптимальными остеокондуктивными свойствами, за счет которых обеспечивает рост костного регенерата от стенок костного дефекта к центру. Также обнаружение единичных гранул в центре костных дефектов на сроке 60 сут., окруженных новообразованной костной тканью, может являться свидетельством некоторого остеоиндуктивного действия, которое, однако, требует более детального изучения.
Такой керамический материал обеспечивает оптимальные условия для культивирования генных конструкций (в частности, плазмидной ДНК), клеток, факторов роста и других биологически активных веществ за счет фазового состава керамики, морфологии поверхности и размера гранул, что в конечном итоге позволяет обеспечить оптимальную кинетику резорбции и эффективное восстановление и реконструкцию поврежденных костных тканей и делает их перспективным материалом для замещения дефектов костных тканей в таких областях, как ортопедия, стоматология, травматология, реконструктивно-восстановительной и челюстно-лицевая хирургия, нейрохирургия, онкология.
Подробное раскрытие изобретения
Для получения ОКФ керамики предлагается модифицировать керамические гранулы с развитой структурой и поверхностью на основе карбоната кальция. Для этого предварительно получают гранулы карбоната кальция, которые состоят из частиц размером от 4 до 15 мкм, неправильной анизотропной формы, из которых состоит керамический каркас с взаимосвязанной пористостью 40-70% (доминирующая популяция пор относится к порам размером 1-500 мкм на поверхности и 20-300 мкм внутри) и имеют следующий состав: 100 масс. % карбоната кальция (КК, СаСО3); величина удельной поверхности равна 0,1±0,05 м2/г. Такие гранулы КК могут быть получены по технологии несмешивающихся жидкостей [1], или методами трехмерного прототипирования [2, 3], или другими известными методами [4, 5].
Модификацию керамических гранул с развитой структурой и поверхностью на основе КК по изобретению осуществляют в специальных буферных растворах А и Б. Для получения раствора А готовят водный 2 М раствор дигидроортофосфата аммония со значением рН 4,1±0,1 раствора. Дигидроортофосфат аммония служит буфером и источником фосфора. Понижение рН раствора со значения 5,5 в прототипе до 4,1 обусловлено тем, что гранулы КК создают щелочную среду и для обеспечения трансформации гранул в полном объеме, необходимо понижение рН. Для получения раствора Б готовят водный 1,5 М раствор ацетата натрия со значением рН 9±0,1 раствора. Повышение значений рН с 8,7 до 9 позволяет получить более чистый конечный продукт.
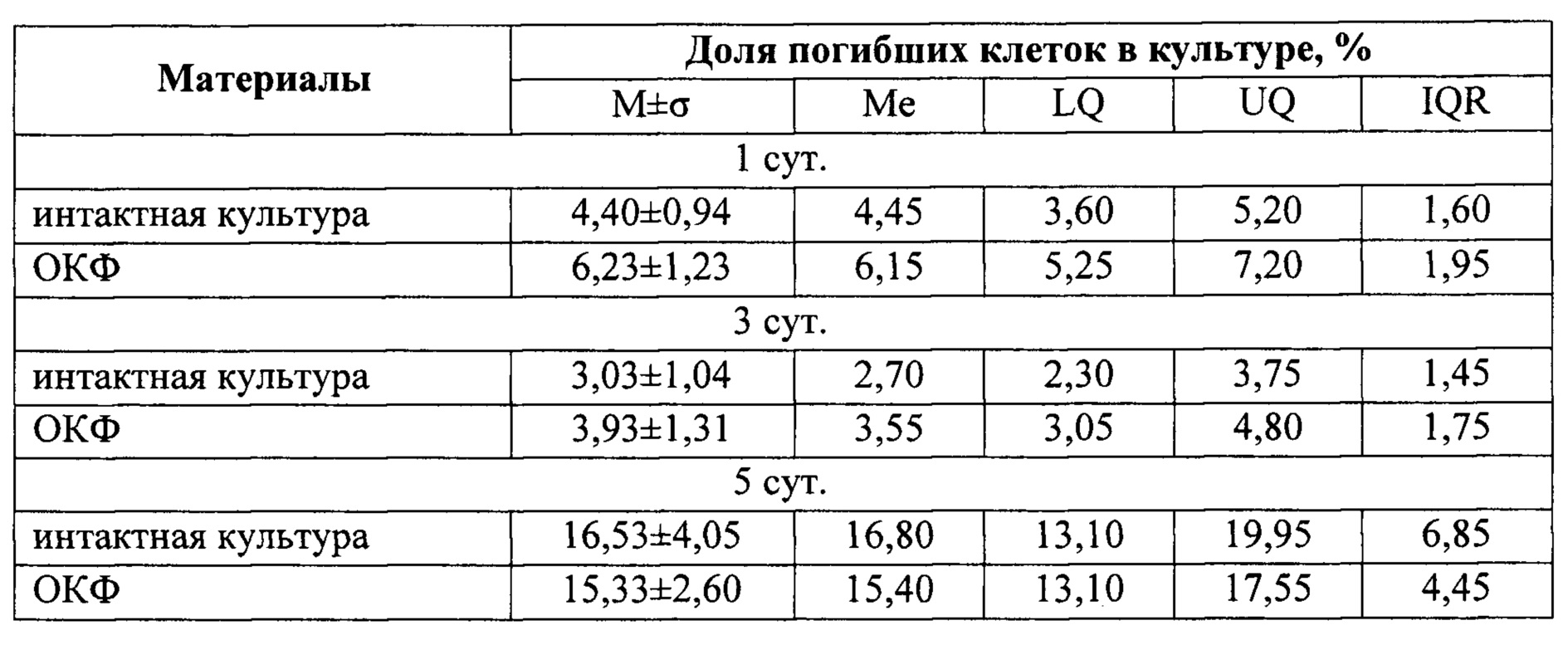
Раствор А предназначен для перевода КК в дикальцийфосфат дигидрат (ДКФД). Процесс ведут при 40±1°С. Соотношение керамики КК и раствора А составляет 1:100. Для гранул фракции 500-1000 мкм процесс максимально эффективно протекает к 7 суткам. При проведении процесса при температуре выше 40±1°С или значениях рН реакции выше 4,4 вместе с ДКФД начинает образовываться безводный дикальцийфосфат (ДКФ), который является цитотоксичным. При значениях рН ниже 4,1 также наблюдается образование ДКФ. При температуре менее 30°С реакция перехода замедляется, так что даже через месяц выдержки в растворе достигается значение менее 60% ДКФД (таблица 1). Далее полученные гранулы отмывают в дистиллированной воде до значения рН не ниже 6,8. Полученные гранулы сушат при температуре 40±1°С в течение суток.
Раствор Б служит для трансформации ДКФД в ОКФ. Химическую обработку ведут при 35±1°С. Соотношение ДКФД и раствора Б составляет 1:100. Для гранул фракции 1000-2000 мкм процесс максимально эффективно протекает к 7 суткам. При проведении процесса при температуре выше 35±1°С или значениях рН реакции более 9,1 образовавшийся ОКФ начинает начинает переходить в гидроксиапатит (ГА), что не желательно, поскольку процесс трансформации ОКФ в ГА должен проходить в организме in vivo. При значениях рН реакции ниже 8,8 или температуре менее 35°С в материале наблюдается не до конца трансформированный ДКФД (таблица 1). После чего полученные гранулы отмывают в дистиллированной воде до значения рН 7,6±0,5. Далее гранулы сушат при температуре 40±1°С в течение суток. Проводят рентгенофазовый анализ, и если в результате наблюдают отсутствие ДКФД, то проводят термическую обработку при 130°С в течение 2-х часов, если ДКФД присутствует, то еще раз проводиться химическая обработка в растворе Б.
Использование растворов А и Б позволяет проводить трансформацию гранул КК в гранулы ОКФ при физиологических температурах (не превышающих 40°С), что очень существенно при получении гранул ОКФ.
Склеившиеся гранулы ОКФ разбивают и выделяют нужные размеры фракций, например такие как 150-500, 500-1000, 1000-2000 мкм методом сепарации. Полученные фракции отмывают от пыли водным раствором и контролируют рН 7,6±0,5. Сушат при 80°С, упаковывают и стерилизуют при 130°С в течение 3 часов. Присутствие остаточного количества КК повышает значения рН в конечных гранулах, что значительно повышает адсорбционные и биологические свойства конечной керамики.
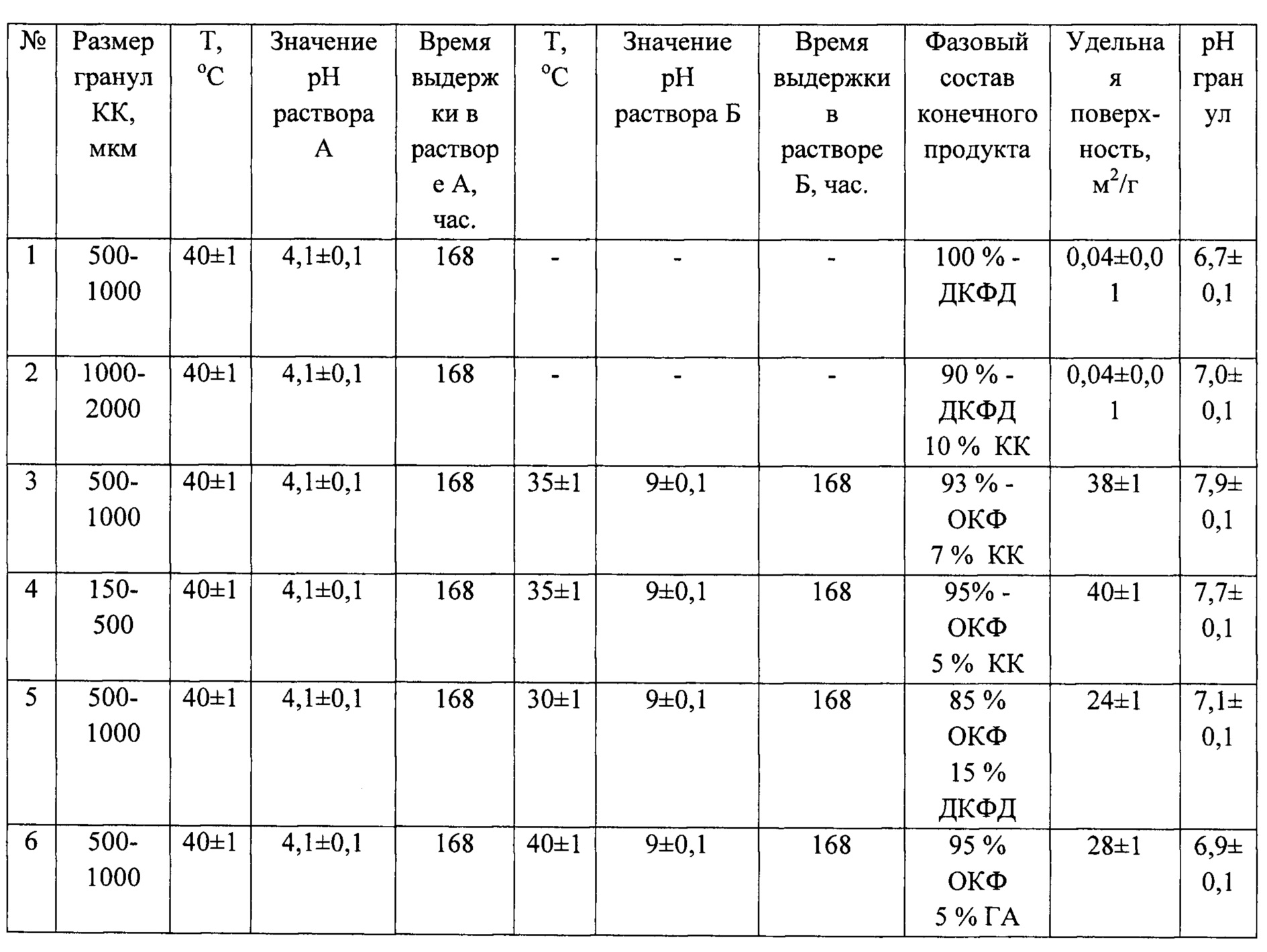
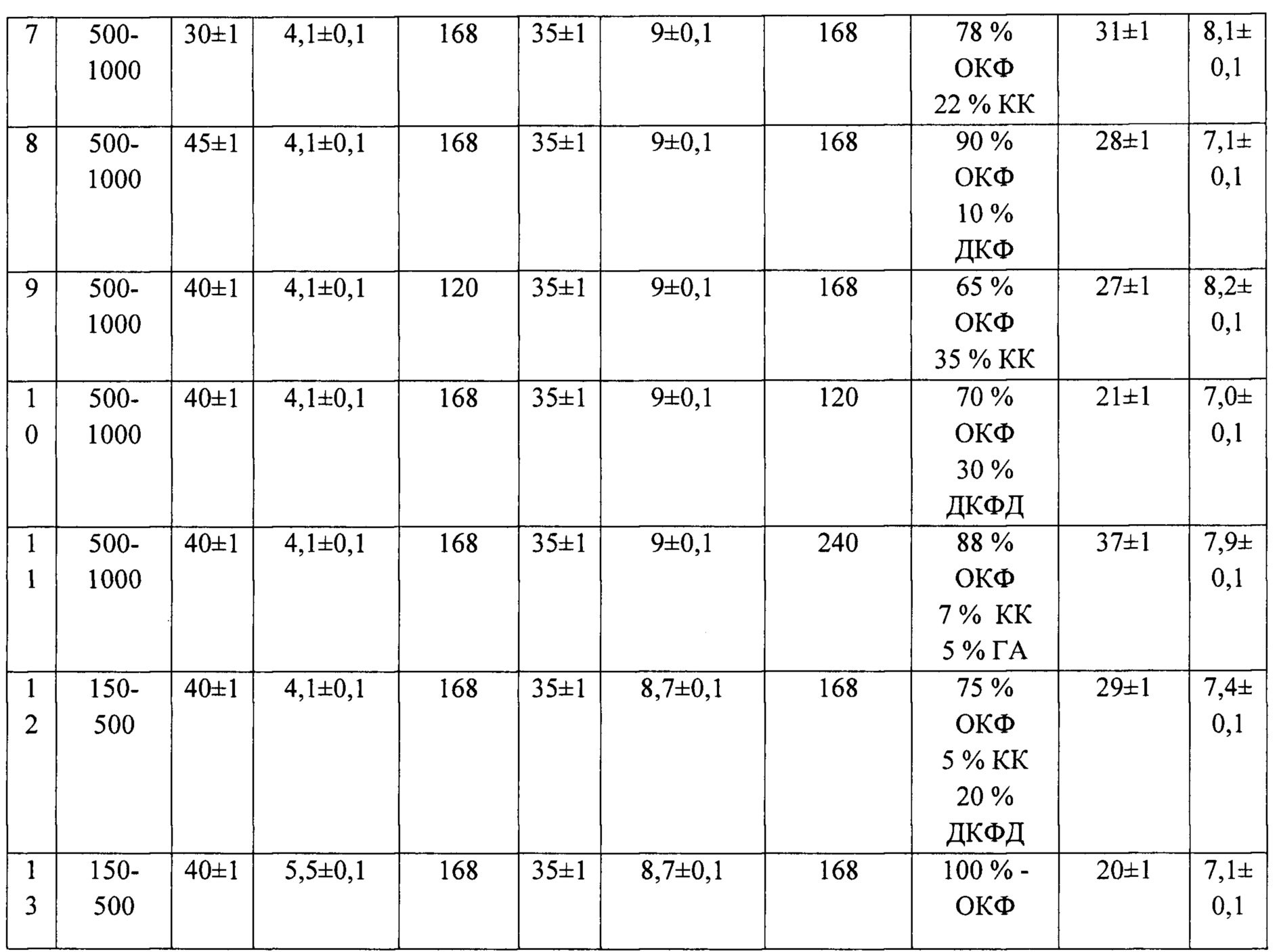
Таблица 3. Влияние условий проведения процесса получения гранул на фазовый состав гранул.
Изобретение иллюстрируется следующими рисунками:
Рисунок 1. Распределение живых и погибших клеток в культуре ММСК, со-инкубированных с исследуемыми материалами, на разных сроках наблюдения: А - интактная культура (контроль); Б - ОКФ. Проточная цитофлуориметрия. Красные точки - живые клетки, зеленые - погибшие.
Рисунок 2. Гранула ОКФ, расположенная в 3 мм от границы костного дефекта, окруженная новообразованной костной тканью; 30 сут. после имплантации.
Рисунок 3. Гранула ОКФ, расположенная в центре костного дефекта, с участком прилежащего костного регенерата.
Рисунок 4. Гистотопограмма дефекта теменной кости кролика, 90 сут. после имплантации остеопластического материала из ОКФ.
Рисунок 5. Микрофотографии поверхности гранул:
а, гранулы КК, с размером ~300 мкм, увеличение в 250 раз;
б) гранулы КК, с размером ~300 мкм, увеличение 5×103;
в гранулы ОКФ, полученные способом по изобретению, с размером ~150 мкм, увеличение в 250 раз;
г), гранулы ОКФ, полученные способом по изобретению, с размером ~150 мкм, увеличение 5×103;
Примеры осуществления изобретения.
Пример 1. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Согласно рентгенофазовому анализу состав конечного продукта соответствуем 100% ДКФД. Значения рН конечных гранул равно 6,7±0,1. Удельная поверхность гранул достигает 0,04±0,01 м2/г.
Пример 2. Гранулы КК размером 1000-2000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Согласно рентгенофазовому анализу состав конечного продукта соответствуем 90% ДКФД и 10% КК. Значения рН конечных гранул равно 7,0±0,1. Удельная поверхность гранул достигает 0,04±0,01 м2/г.
Пример 3. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 93% ОКФ, 7% КК. Значения рН конечных гранул равно 7,9±0,1. Удельная поверхность гранул достигает 38±1 м2/г.
Пример 4. Гранулы КК размером 150-500 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 95% ОКФ, 5% КК. Значения рН конечных гранул равно 7,7±0,1. Удельная поверхность гранул достигает 40±1 м2/г.
Пример 5. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 30±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 85% ОКФ, 15% ДКФД. Значения рН конечных гранул равно 7,1. Удельная поверхность гранул достигает 24±1 м2/г.
Пример 6. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 40±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 95% ОКФ, 5% ГА. Значения рН конечных гранул равно 6,9±0,1. Удельная поверхность гранул достигает 28±1 м2/г.
Пример 7. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 30±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 78% ОКФ, 22% КК. Значения рН конечных гранул равно 8,1±0,1. Удельная поверхность гранул достигает 31±1 м2/г.
Пример 8. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 45±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 90% ОКФ, 10% ДКФ. Значения рН конечных гранул равно 7,1±0,1. Удельная поверхность гранул достигает 28±1 м2/г.
Пример 9. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 5 суток (120 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 65% ОКФ, 35% КК. Значения рН конечных гранул равно 8,2±0,1. Удельная поверхность гранул достигает 27±1 м2/г.
Пример 10. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 5 суток (120 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 70% ОКФ, 30% ДКФД. Значения рН конечных гранул равно 7,0±0,1. Удельная поверхность гранул достигает 21±1 м2/г.
Пример 11. Гранулы КК размером 500-1000 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 9±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 10 суток (240 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 88% ОКФ, 5% ГА, 7% КК. Значения рН конечных гранул равно 7,9±0,1. Удельная поверхность гранул достигает 37±1 м2/г.
Пример 12 Гранулы КК размером 150-500 мкм помещали в шейкер-инкубатор при 40±1°С в количестве 5 гр. на 500 мл раствора А со значением рН 4,1±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7±0,5 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор Б объемом 500 мл со значением рН 8,7±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,6±0,6. Согласно рентгенофазовому анализу состав конечного продукта соответствует 75% ОКФ, 5% КК 20% ДКФД. Значения рН конечных гранул равно 7,4±0,1. Удельная поверхность гранул достигает 29±1 м2/г.
Пример 13 (по способу аналога). Гранулы α-ТКФ размером 150-500 мкм помещали в шейкер-инкубатор при 35±1°С в количестве 5 гр. на 500 мл раствора Ап со значением рН 5,5±0,1. Выдерживали в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 6,5±0,2 и сушили при температуре 35±1°С в течение суток. Затем полученные гранулы ДКФД в количестве 5 гр. погружали в раствор БП объемом 500 мл со значением рН 8,7±0,1. Процесс вели в шейкере-инкубаторе при 35±1°С в течение 7 суток (168 часов). Далее полученные гранулы отмывали в дистиллированной воде до значения рН 7,4±0,2. Согласно рентгенофазовому анализу состав конечного продукта соответствует 100% ОКФ. Значения рН конечных гранул равно 7,1±0,1. Удельная поверхность гранул достигает 20±1 м2/г.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования способа согласно настоящему изобретению, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
Библиографический список
1. Komlev, V.S., Barinov, S.M., Koplik, E.V. A method to fabricate porous spherical hydroxyapatite granules intended for time-controlled drug release // Biomaterials 2002. V. 23. P. 3449-3454.
2. Klammert U., Gbureck U., Vorndran E., Diger J.R., Meyer-Marcotty P., Bier A.C. 3D powder printed calcium phosphate implants for reconstruction of cranial and maxillofacial defects // Journal of Cranio-Maxillo-Facial Surgery. 2010. V. 38. P. 565-570.
3. Butscher A., Bohner M., Hofmann S., Gauckler L., Mbller R. Structural and material approaches to bone tissue engineering in powder-based three-dimensional printing // Acta Biomaterialia 2011. V. 7. P. 907-920.
4. Y.H. Hsu, I.G. Turner, A.W. Miles. Fabrication and mechanical testing of porous calcium phosphate bioceramic granules // J Mater Sci: Mater. Med. 2007. V. 18 P. 1931-1937.
5. Surmenev R.A. A review of plasma-assisted methods for calcium phosphate-based coatings fabrication // Surface & Coatings Technology. 2012. V. 206. P. 2035-2056.