Результат интеллектуальной деятельности: СОЧЕТАННАЯ ТЕРАПИЯ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к фармацевтическим комбинациям, например, к продуктам, включающим сочетание (i) ингибитора MET или его фармацевтически приемлемой соли или гидрата и (ii) ингибитора EGFR (ErbB-1), которые совместно активны при лечении пролиферативных заболеваний, к соответствующим фармацевтическим лекарственным формам, способам применения, методам, способам, коммерческим упаковкам и связанным с ними вариантам осуществления.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОМУ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Лекарственные средства, которые разработаны для действия против индивидуальных молекулярных мишеней, часто не подходят для борьбы с заболеваниями, имеющими в качестве причины более одной мишени (мультигенными заболеваниями), такими как рак или другие пролиферативные заболевания.
Для борьбы с такими заболеваниями один подход заключается в использовании отдельно взятых многоцелевых лекарств - однако, в этом случае требуется, чтобы мишени, являющиеся причиной, вызывающей манифестацию заболевания, все поражались рассматриваемым лекарством. С другой стороны, многоцелевые лекарственные средства могут привести к нежелательным побочным эффектам, поскольку они также могут действовать на мишени, не участвующие в манифестации заболевания.
Другой подход заключается в использовании сочетания лекарств в виде многоцелевых препаратов. В самом хорошем варианте это может привести к сочетанной эффективности, например, синергичному действию, таким образом, что даже создается возможность уменьшения побочных эффектов, вызываемых отдельно взятыми лекарствами при использовании по отдельности.
Иногда компоненты (сочетанные компоненты) таких препаратов могут влиять на отдельные мишени для создания сочетанного эффекта, и, таким образом, могут вызывать сочетанный эффект, выходящий за рамки эффекта, который может быть достигнут с помощью отдельных соединений и/или при рассмотрении их отдельных эффектов, соответственно, либо с помощью одного и того же пути, либо различных путей в пределах отдельной клетки или отдельных клеток в отдельных тканях. Альтернативно один компонент может изменить способность другого компонента в отношении достижения своей мишени, например, путем ингибирования выкачивающих насосов или тому подобного. В качестве еще одной альтернативы сочетанные компоненты могут связываться с отдельными участками одной и той же мишени. Эти варианты связанности мишеней препятствуют поиску соответствующих сочетаний в результате существенного увеличения возможных типов взаимодействий, которые могут быть полезны или нет для сочетания.
Однако желаемая кооперация или даже синергизм при использовании таких лекарств во многих случаях может быть не обнаружен. По мере увеличения числа парных (r=2) сочетаний лекарств в соответствии с формулой n!(r!(n-r)!) при количестве подвергаемых тестировании агентов n (например, при тестировании 2000 агентов уже будет генерироваться 1999000 уникальных парных сочетаний), требуется подходящий метод скрининга с высокой эффективностью.
Кроме того, до рассмотрения любого сочетания существует важная потребность в определении путей, ферментов, метаболических состояний или тому подобного, участвующих в качестве причины или в качестве пути поддержания манифестации заболевания.
Во многих случаях даже вообще неизвестно, что данное заболевание является мультигенным.
Таким образом, поиск подходящих сочетаний и количеств может быть описан должным образом, что соответствует поиску иголки в стоге сена.
Протоонкоген cMET (MET) кодирует белковый рецептор фактора роста гепатоцитов (HGFR), который обладает активностью тирозинкиназы и имеет большое значение для эмбрионального развития и заживления ран. При стимуляции фактором роста гепатоцитов (HGF) MET вызывает несколько биологических ответов, ведущих к инвазивному росту. Аномальная активация МЕТ индуцирует рост опухоли, образование новых кровеносных сосудов (ангиогенез) и метастазирование при различных типах злокачественных опухолей, включая рак почки, печени, желудка, молочной железы и мозга. Известен ряд ингибиторов киназы МЕТ и альтернативно ингибиторов индуцированной HGF активации MET (=HGFR). Биологические функции с-MET (или сигнального пути с-MET) в нормальных тканях и злокачественных опухолях человека, таких как рак, хорошо документированы (Christensen, J.G. et al., Cancer Lett. 2005, 225(1):1-26; Corso, S. et al., Trends in Mol. Med. 2005, 11(6):284-292).
Нарушение регуляции пути с-Met (с-МЕТ) играет важную, а иногда (в случае генетических изменений) причинную роль в образовании, росте, поддержании и прогрессии опухоли, (Birchmeier, C. et al., Nat. Rev. Mol. Cell. Biol. 2003, 4(12):915-925; Boccaccio, C. et al., Nat. Rev. Cancer 2006, 6(8):637-645; Christensen, J.G. et al., Cancer Lett. 2005, 225(1):1-26). HGF и/или c-Met избыточно экспрессируются в значительной части большинства злокачественных опухолей человека, и часто связаны с плохими клиническими исходами, такими как более агрессивное заболевание, прогрессия заболевания, метастазирование опухоли и укорочение выживаемости больных. Кроме того, больные с высокими уровнями белков HGF/c-Met более устойчивы к химиотерапии и лучевой терапии. В дополнение к аномальной экспрессии HGF/c-Met рецептор c-Met также может быть активирован у больных раком в результате генетических мутаций (как зародышевых, так и соматических) и амплификации гена. Хотя амплификация гена и мутации являются наиболее распространенными генетическими изменениями, которые были зарегистрированы у больных, рецептор также может быть активирован путем делеций, укорочений, перегруппировки генов.
Различные виды рака, в которые вовлечен с-МЕТ, включают, но не ограничиваются этим: карциномы (например, мочевого пузыря, молочной железы, шейки матки, холангиокарциному, колоректальную карциному, карциномы пищевода, желудка, головы и шеи, почки, печени, легких, носоглотки, яичников, поджелудочной железы, простаты, щитовидной железы); саркомы опорно-двигательного аппарата (например, остеосаркому, синовиальную саркому, рабдомиосаркому); саркомы мягких тканей (например, MFH/фибросаркому, леймиосаркому, саркому Капоши); гемопоэтические злокачественные опухоли (например, множественную миелому, лимфомы, лейкоз Т-клеток взрослых, острый миелобластный лейкоз, хронический миелоидный лейкоз); и другие новообразования (например, глиобластомы, астроцитомы, меланому, мезотелиому и опухоль Вильмса ((www.vai.org/met/; Christensen, J.G. et al., Cancer Lett. 2005, 225(1):1-26).
Представление о том, что активированный путь c-МЕТ способствует образованию и прогрессии опухоли и может быть хорошей мишенью для эффективного вмешательства в развитие рака, дополнительно подтверждается многочисленными доклиническими исследованиями (Birchmeier, C. et al., Nat. Rev. Mol. Cell Biol. 2003, 4(12):915-925; Christen sen, J.G. et al., Cancer Lett. 2005, 225(1):1-26; Corso, S. et al., Trends in Mol. Med. 2005, 11(6): 284-292). Например, исследования показали, что гибридный ген tpr-met, гиперэкспрессия c-Met и активирующие мутации c-Met (совместно обозначаемые в настоящем описании как Met), все вызывают онкогенную трансформацию различных модельных клеточных линий и приводят к образованию опухолей и метастазированию у мышей. Более важно, что значительная противоопухолевая активность (иногда с регрессией опухоли) и активность, направленная против метастазирования, продемонстрирована in vitro и in vivo с помощью агентов, которые специфически нарушают и/или блокируют сигнализацию HGF/с-МЕТ. Эти агенты включают антитела против HGF и против c-Met, пептидные антагонисты HGF, рецептор-манок c-Met, пептидные антагонисты c-Met, доминантные негативные мутации c-Met, специфические антисмысловые олигонуклеотиды и рибозимы c-Met и селективные низкомолекулярные ингибиторы киназы c-Met (Christen sen, J.G. et al., Cancer Lett. 2005, 225(1):1-26).
В дополнение к установленной роли в развитии рака, аномальная передача сигнала HGF/МЕТ также участвует в развитии атеросклероза, фиброза легких, фиброза и регенерации почек, заболеваний печени, аллергических заболеваний, воспалительных и аутоиммунных заболеваний, заболеваний сосудов головного мозга, сердечнососудистых заболеваний, состояний, связанных с трансплантацией органов (Ma, H. et al., Atherosclerosis. 2002, 164(1):79-87; Crestani, B. et al., Lab. Invest. 2002, 82(8):1015-1022; Sequra-Flores, A.A. et al., Rev. Gastroenterol. Mex. 2004, 69(4)243-250; Morishita, R. et al., Curr. Gene Ther. 2004, 4(2)199-206; Morishita, R. et al., Endocr. J. 2002, 49(3)273-284; Liu, Y., Curr. Opin. Nephrol. Hypertens. 2002, 11(1):23-30; Matsumoto, K. et al., Kidney Int. 2001, 59(6):2023-2038; Balkovetz, D.F. et al., Int. Rev. Cytol. 1999, 186:225-250; Miyazawa, T. et al., J. Cereb. Blood Flow Metab. 1998, 18(4)345-348; Koch, A.E. et al., Arthritis Rheum. 1996, 39(9):1566-1575; Futamatsu, H. et al., Circ. Res. 2005, 96(8)823-830; Eguchi, S. et al., Clin. Transplant. 1999, 13(6)536-544).
Рецептор эпидермального фактора роста (EGFR, также известный как ErbB-1; HER1 у человека) является рецептором лигандов семейства эпидермального фактора роста. Несколько типов рака, таких как рак легкого, типы рака анального канала, мультиформная глиобластома, и многие другие, главным образом, типы эпителиального рака, как известно, зависят от гиперактивности или гиперэкспрессии EGFR.
Рак часто зависит от генетического изменения рецепторных тирозинкиназ (RTK), например, в результате точечной мутации, амплификации гена или хромосомной транслокации, что приводит к неконтролируемой активности этих RTKs, которые таким образом становятся онкогенными. Клеточная пролиферация раковых клеток зависит от активности этих аберрантных RTKs.
При лечении возникающих в результате пролиферативных заболеваний часто используются ингибиторы вовлеченной онкогенной RTK. Тем не менее, часто после определенного времени лечения наблюдается устойчивость к используемому препарату. Один механизм устойчивости может включать RTK-мишень с нарушением связывания или активности терапевтического агента. Другой механизм заключается в компенсаторной активации альтернативной киназы, которая продолжает стимулировать рост ракового образования, когда первичная киназа ингибируется. Хорошо охарактеризованным примером участия обоих типов механизмов является приобретенная устойчивость к гефитинибу и эрлотинибу, направленных против рецептора эпидермального фактора роста (EGFR), при немелкоклеточном раке (NSCLC), несущем активирующие мутации EGFR (смотри Lynch, T. J., et al., N Engl J Med, 350: 2129-2139, 2004; or Paez, J. G., et al., Science, 304: 1497-1500, 2004). Например, активация MET может компенсировать потерю активности EGFR (путем ингибирования) в результате нижележащей активации сигнальных молекул, таких как HER3, например, амплификация MET может это компенсировать, или его лиганд - фактор роста гепатоцитов может активировать MET (смотри Engelman, J. A., et al., Science, 316: 1039-1043, 2007; Yano, S., et al., Cancer Res, 68: 9479-9487, 2008; and Turke, A. B., et al., Cancer Cell, 17: 77-88, 2010). Известно также, что MET-зависимые клеточные линии рака (пролиферация которых зависит от активности MET) могут уклоняться от ингибиторов MET с помощью индуцированной лигандом активации EGFR (Bachleitner-Hofmann, T., et al, Mol Cancer Ther, 7: 3499-3508, 2008).
В патенте WO2013/149581 описывается сочетание различных ингибиторов c-MET с различными ингибиторами EGFR. Он относится к фармацевтическим продуктам, включающим сочетание (i) ингибитора MET и (ii) ингибитора EGFR, или его фармацевтически приемлемой соли, или гидрата, соответственно, или к их пролекарствам, которые совместно активны при лечении пролиферативных заболеваний, к соответствующим фармацевтическим составам, применению, методам, способам, коммерческим упаковкам и к связанным с ними вариантам осуществления.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к фармацевтической комбинации, включающей
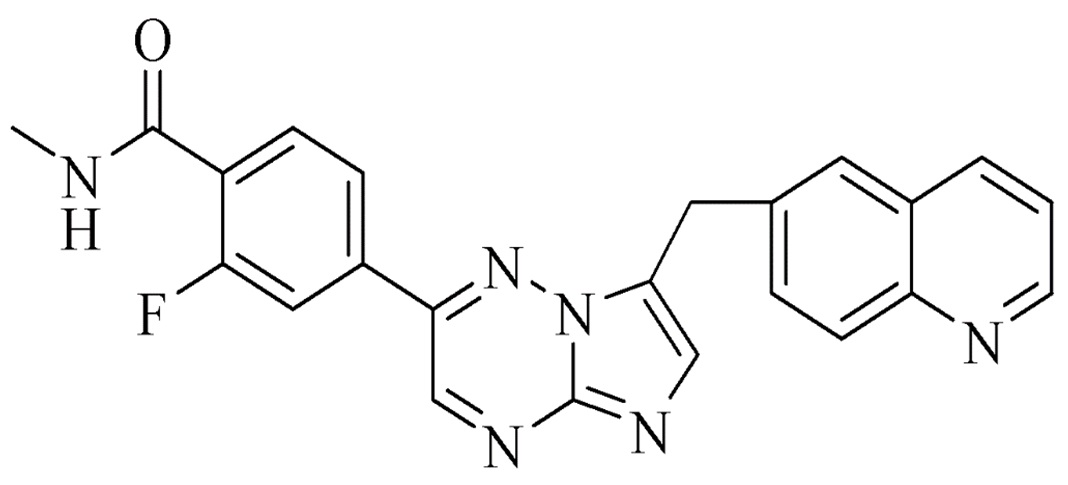
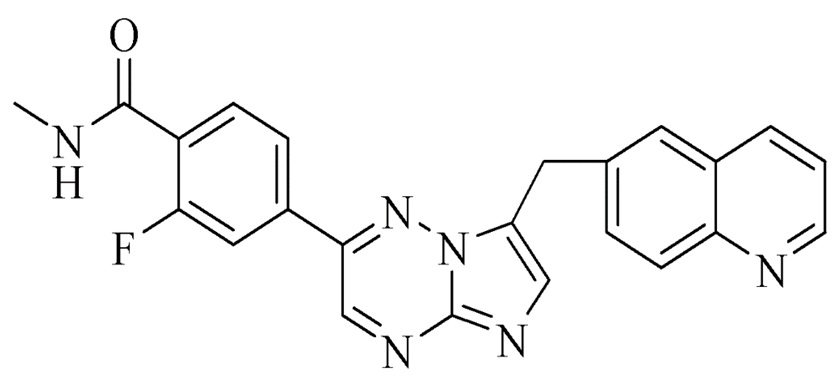
(i) ингибитор тирозинкиназы MET, который представляет собой соединение INC280, имеющее формулу
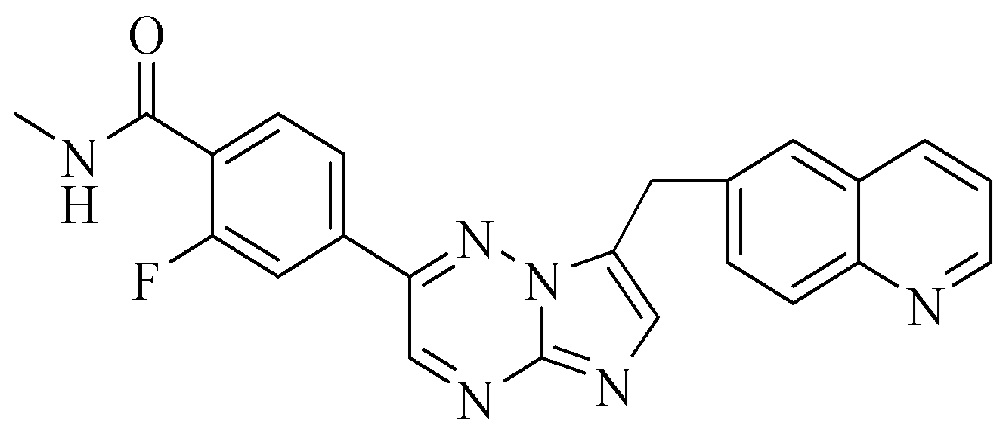
или его фармацевтически приемлемую соль или его гидрат,
(ii) ингибитор тирозинкиназы EGFR, который представляет собой соединение, имеющее формулу (X), или его таутомер: 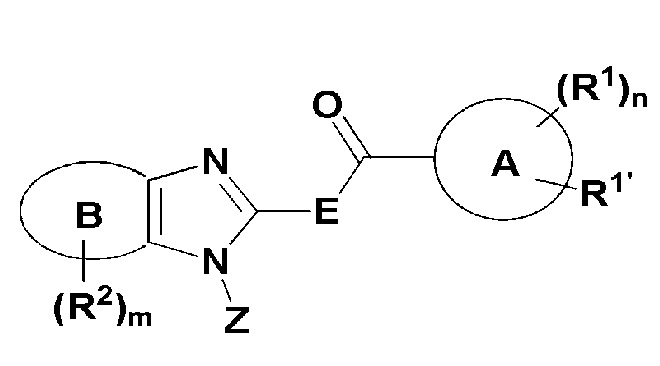
(X)
где кольцо A представляет собой 6-10-членный моноциклический или бициклический арил; 5-10-членный гетероарил, включающий 1-4 гетероатома, выбранных из N, O и S; или 4-12-членный моноциклический или бициклический гетероциклил, включающий 1-4 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо;
Кольцо B представляет собой фенил; 5-6-членный гетероарил, включающий 1-3 гетероатома, выбранных из N, O и S; или 5-6-членный гетероциклил, включающий 1-2 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо;
Е представляет собой NH или CH2;
R1, R1' и R2 независимо представляют собой водород; галоген; циано; С1-6-алкил; С1-6-галогеналкил; 5-6-членный гетероарил, включающий 1-4 гетероатома, выбранных из N, O и S; фенил, 5-6-членный гетероциклил, включающий 1-2 гетероатома, выбранных из N, O, S и P, и необязательно замещенный оксо; - X1-C(O)OR3; -X1-O-C(O)R3; -X1-C(O)R3; -X1-C(O)NR4R5; -X1-C(O)NR4-X3-C(O)OR3; -X1-C(O)NR4-X3-S(O)0-2 R6; -X1-NR4R5; -X1NR4-X2-C(O)R3; -X1-NR4-X2-C(O)OR3; -X1-NR4-X2-C(O)NR4R5; -X1-NR4-X3-S(O)0-2R6; -X1-NR4S(O)2R6; -X1-OS(O)2R6; -X1-OR3; -X1-O-X4-OR3; -X1-O-X4-S(O)0-2R6; -X1-O-X4-NR4R5; -X1-S(O)0-2R6; -X1-S(O)0-2-X3-NR4R5; -X1-C(O)NR4-X3-P(O)R6aR6b; -X1-NR4-X1-P(O)R6aR6b; -X1-O-X1-P(O)R6aR6b; -X1-P(O)R6a-X1-NR4R5; -X1-P(O)R6aR6b или -X1-S(O)2NR4R5; где каждый фенил, гетероарил или гетероциклил в R1 или R2 является незамещенным или замещен 1-3 группами, выбранными из ОН, галогена, С1-6-алкила; С1-6-галогеналкила; и С1-6-галогеналкокси;
R3, R4 и R5 независимо представляют собой водород, С1-6-алкил или С1-6-галогеналкил; или где R4 и R5 вместе с N в NR4R5 могут образовывать 4-7-членное кольцо, содержащее 1-2 гетероатома, выбранных из N, O, S и P, и необязательно замещенное 1-4 R7;
R6 представляет собой С1-6-алкил или С1-6-галогеналкил;
R6a и R6b независимо представляют собой гидрокси, С1-6-алкил, С1-6-галогеналкил, С1-6-алкокси, С1-6-галогеналкокси, 6-10-членный моноциклический или бициклический арил; 5-10-членный гетероарил, включающий 1-4 гетероатома, выбранных из N, O и S; или 4-12-членный моноциклический или бициклический гетероциклил, включающий 1-4 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо;
Z представляет собой
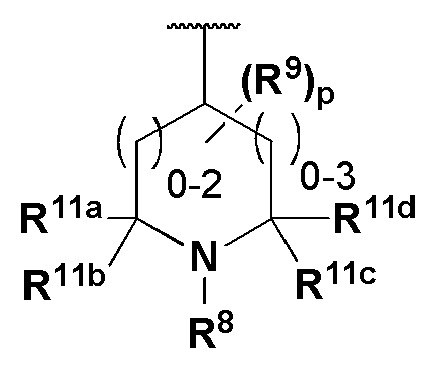 или
или 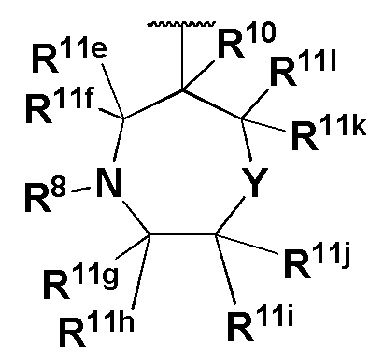
где Y представляет собой O или NR10;
R8 представляет собой
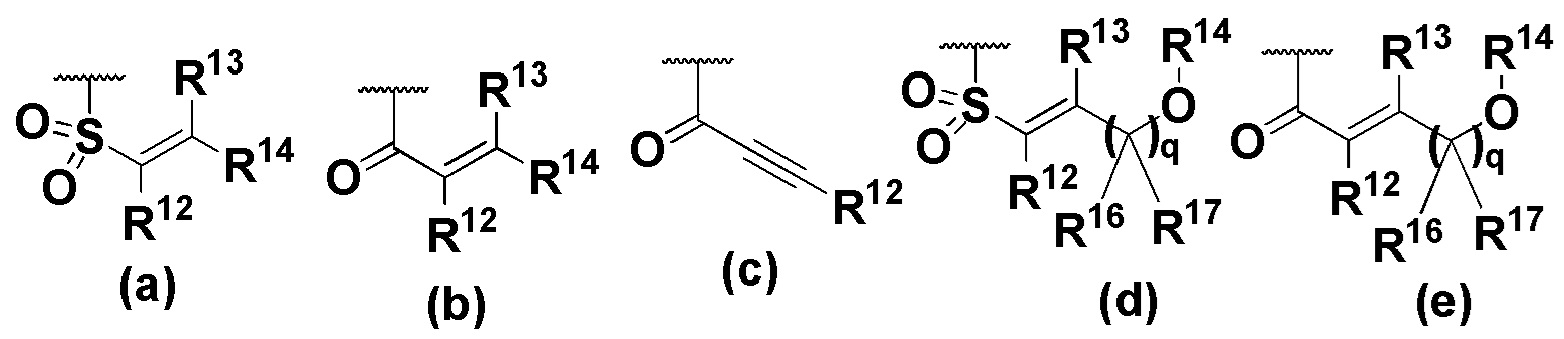
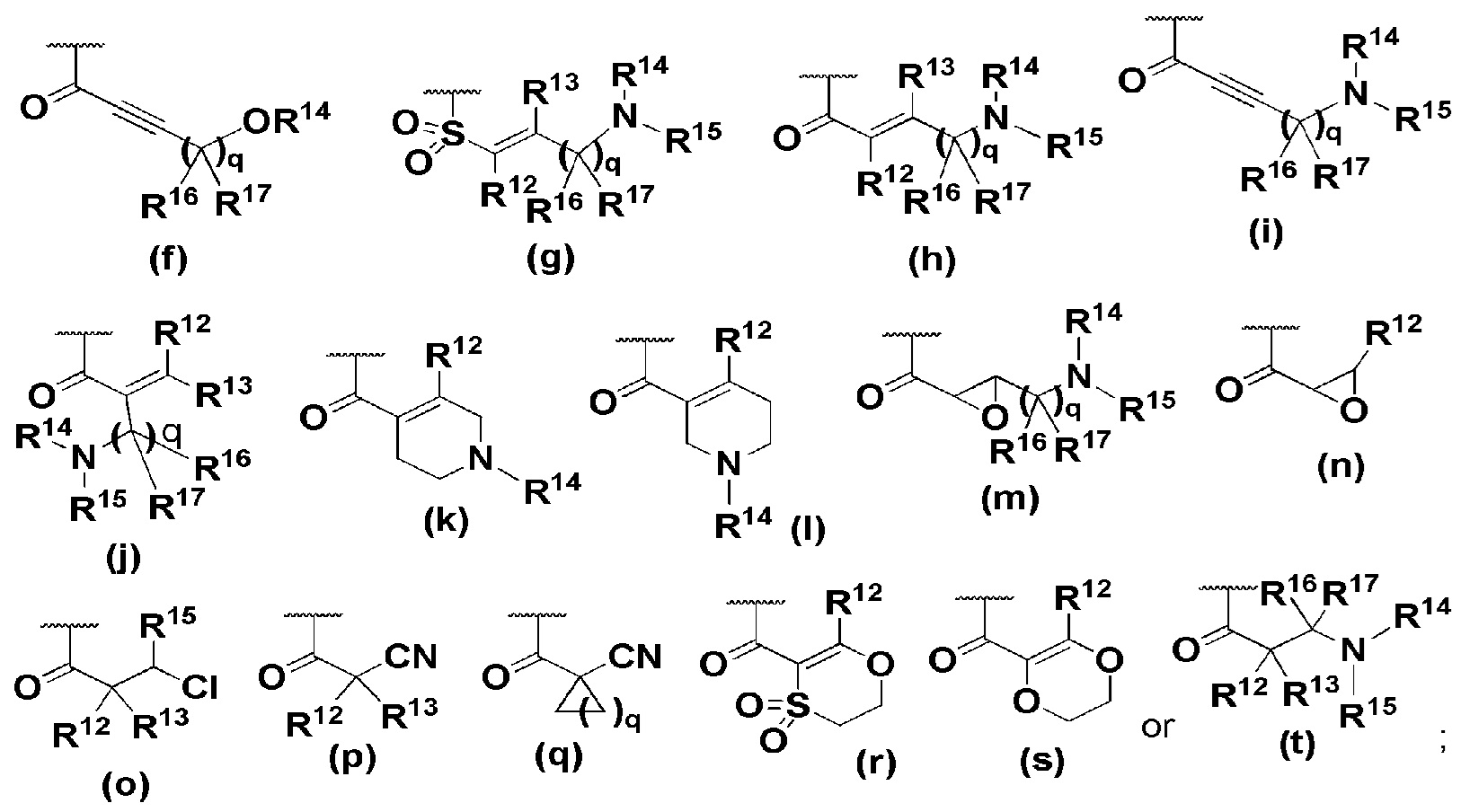
R9 и R10 независимо представляют собой водород, галоген, С1-6-алкил, С1-6-галогеналкил, ОН, циано, С1-6-алкокси, С1-6-галогеналкокси;
R11a, R11b, R11c, R11d, R11e, R11f, R11g, R11h, R11i, R11j, R11k и R11l независимо представляют собой водород, С1-6-алкил или С1-6-галогеналкил;
R12 и R13 независимо представляют собой водород, галоген, циано, С1-6-алкил или С1-6-галогеналкил;
R14 и R15 независимо представляют собой водород, C1-6-алкил, -L1-R23, -(CRaRb)2-3-Rc или -L2-Rd; или R14 и R15 совместно с N в NR14R15 могут образовывать 4-7-членное кольцо, содержащее 1-2 гетероатома, выбранных из N, O, S и P, и необязательно замещенное 1-4 группами R18;
R16 и R17 независимо представляют собой водород или C1-6-алкил; или R16 и R17 совместно с атомом углерода, к которому они присоединены, могут образовывать C3-6-циклоалкил;
X1 и X2 независимо представляют собой связь или C1-6-алкил;
X3 представляет собой C1-6-алкил;
X4 представляет собой C2-6-алкил;
R19 представляет собой водород, C1-6-алкил, COR20, COOR20, CONR20R21 или S(O)2R20;
R20 представляет собой C1-6-алкил, C1-6-галогеналкил или циклоалкил;
R21 представляет собой водород или C1-6-алкил; или R20 и R21 совместно с N в NR20R21 могут образовывать 4-7-членное кольцо, содержащее 1-2 гетероатома, выбранных из N, O, S, P, и необязательно замещенное 1-4 группами R22;
R7, R18 и R22 независимо представляют собой оксо, галоген, гидрокси, C1-6-алкил, C1-6-галогеналкил, C1-6-алкокси или C1-6-галогеналкокси;
R23 независимо представляет собой C3-7-циклоалкил или 4-10-членный гетероциклил, включающий 1-3 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо; и R23 не замещен или замещен C1-6-алкилом, C1-6-галогеналкилом, -L3-Re или -L4-Rf;
Rc и Re независимо представляют собой галоген, циано, гидрокси, -OR24, -NRR25, -NR-CO2R24, -NR-SO2-R26, -NR-COR26, -NR-C(O)-NRR25, -OC(O)-NRR25 или C1-6-алкил, замещенный галогеном, C1-6-алкокси, гидрокси или циано;
Rd и Rf независимо друг от друга представляют собой -SO2NRR25, -CONRR25, -C(O)OR24, -SO2R26 или C(O)R26;
R24 представляет собой C1-6-алкил, C1-6-галогеналкил, -L2-R23a или -(CRaRb)2-3-N(RaRb)2;
R25 представляет собой водород, C1-6-алкил, C1-6-галогеналкил, -L2-R23b или -(CR2)2-3-N(RaRb)2;
R26 представляет собой C1-6-алкил, C1-6-галогеналкил, -L2-R23c или -(CRaRb)1-3-N(RaRb)2;
R23a, R23b и R23c независимо выбраны из R23;
R, Ra и Rb независимо представляют собой водород или C1-6-алкил;
L1, L2, L3 и L4 независимо представляют собой связь или -(CRaRb)1-3; и
n и m независимо равны 1-3; и p и q равны 1-4;
или его фармацевтически приемлемую соль, и
(iii) по меньшей мере, один фармацевтически приемлемый носитель.
Настоящее изобретение также относится к фармацевтической комбинации, включающей
(i) ингибитор тирозинкиназы MET, который представляет собой соединение INC280, имеющее формулу
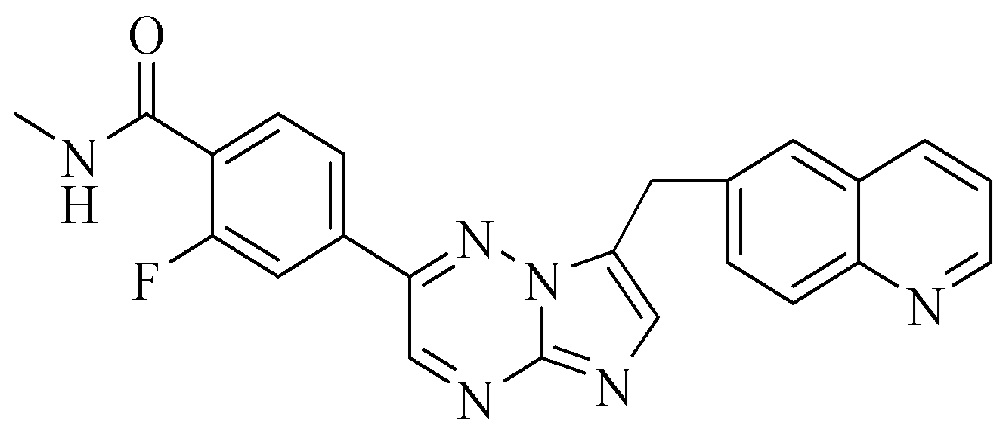
или его фармацевтически приемлемую соль или его гидрат,
(ii) ингибитор тирозинкиназы EGFR, который представляет собой соединение, имеющее формулу (X), или его таутомер: 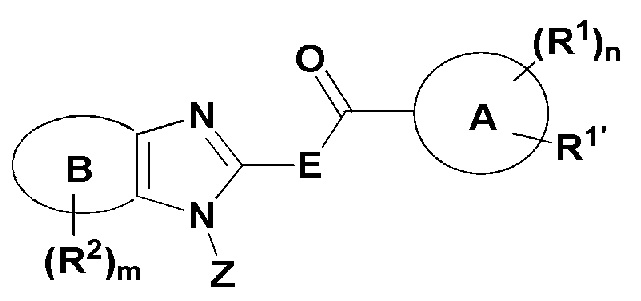
(X)
как описано выше, или его фармацевтически приемлемую соль.
В одном из вариантов осуществления сочетания, ингибитор тирозинкиназы EGFR представляет собой соединение А, которое имеет химическое название (R,E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1Н-бензо[d]имидазол-2-ил)-2-метилизоникотинамид и имеет структуру
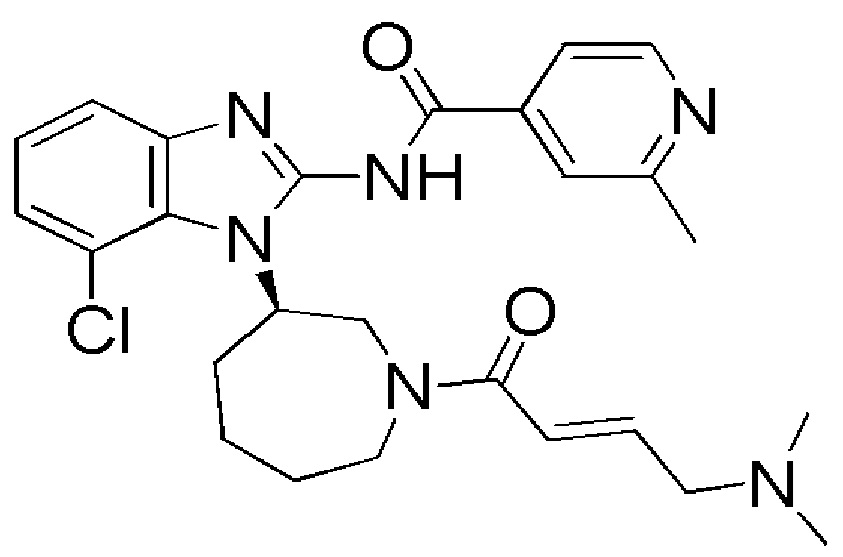 (Соединение А).
(Соединение А).
Ингибитор(ы) тирозинкиназы EGFR по настоящему изобретению подробно описаны в патенте WO2013/184757. В частности, соединение А описано как пример 5 патента WO2013/184757.
В одном из вариантов осуществления комбинации соединение INC280 находится в форме дигидрохлоридной соли кислоты.
В другом варианте осуществления соединение INC280 находится в форме моногидрата дигидрохлоридной соли.
В одном из вариантов осуществления комбинации ингибитор тирозинкиназы МЕТ и ингибитор тирозинкиназы EGFR вводят одновременно, раздельно или последовательно.
Настоящее изобретение также относится к способу лечения заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы MET, особенно рака, включающему введение фармацевтической комбинации, включающей
(i) ингибитор тирозинкиназы MET, который представляет собой соединение INC280, имеющее формулу
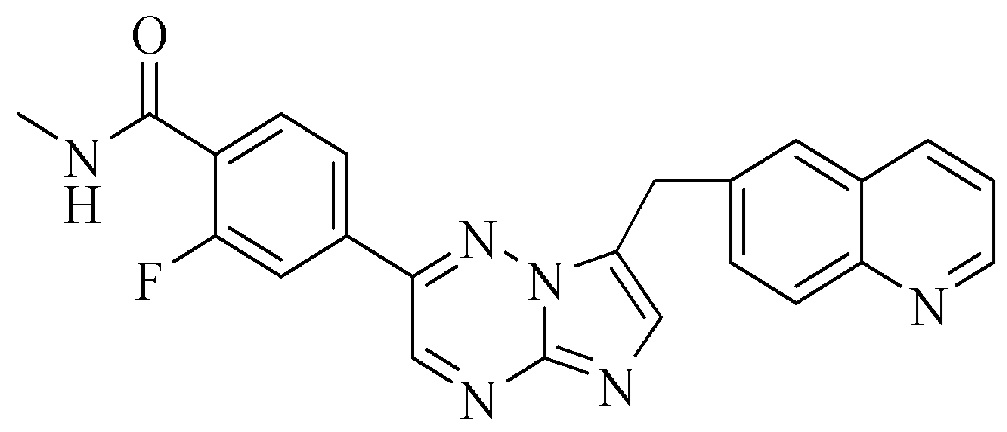
или его фармацевтически приемлемую соль или его гидрат,
(ii) ингибитор тирозинкиназы EGFR, который представляет собой соединение, имеющее формулу (X), или его таутомер: 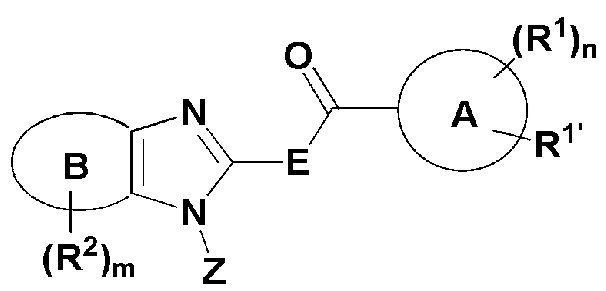
(X)
где кольцо A представляет собой 6-10-членный моноциклический или бициклический арил; 5-10-членный гетероарил, включающий 1-4 гетероатома, выбранных из N, O и S; или 4-12-членный моноциклический или бициклический гетероциклил, включающий 1-4 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо;
Кольцо B представляет собой фенил; 5-6-членный гетероарил, включающий 1-3 гетероатома, выбранных из N, O и S; или 5-6-членный гетероциклил, включающий 1-2 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо;
Е представляет собой NH или CH2;
R1, R1' и R2 независимо представляют собой водород; галоген; циано; С1-6-алкил; С1-6-галогеналкил; 5-6-членный гетероарил, включающий 1-4 гетероатома, выбранных из N, O и S; фенил, 5-6-членный гетероциклил, включающий 1-2 гетероатома, выбранных из N, O, S и P, и необязательно замещенный оксо; - X1-C(O)OR3; -X1-O-C(O)R3; -X1-C(O)R3; -X1-C(O)NR4R5; -X1-C(O)NR4-X3-C(O)OR3; -X1-C(O)NR4-X3-S(O)0-2 R6; -X1-NR4R5; -X1NR4-X2-C(O)R3; -X1-NR4-X2-C(O)OR3; -X1-NR4-X2-C(O)NR4R5; -X1-NR4-X3-S(O)0-2R6; -X1-NR4S(O)2R6; -X1-OS(O)2R6; -X1-OR3; -X1-O-X4-OR3; -X1-O-X4-S(O)0-2R6; -X1-O-X4-NR4R5; -X1-S(O)0-2R6; -X1-S(O)0-2-X3-NR4R5; -X1-C(O)NR4-X3-P(O)R6aR6b; -X1-NR4-X1-P(O)R6aR6b; -X1-O-X1-P(O)R6aR6b; -X1-P(O)R6a-X1-NR4R5; -X1-P(O)R6aR6b или -X1-S(O)2NR4R5; где каждый фенил, гетероарил или гетероциклил в R1 или R2 является незамещенным или замещен 1-3 группами, выбранными из ОН, галогена, С1-6-алкила; С1-6-галогеналкила; и С1-6-галогеналкокси;
R3, R4 и R5 независимо представляют собой водород, С1-6-алкил или С1-6-галогеналкил; или где R4 и R5 вместе с N в NR4R5 могут образовывать 4-7-членное кольцо, содержащее 1-2 гетероатома, выбранных из N, O, S и P, и необязательно замещенное 1-4 R7;
R6 представляет собой С1-6-алкил или С1-6-галогеналкил;
R6a и R6b независимо представляют собой гидрокси, С1-6-алкил, С1-6-галогеналкил, С1-6-алкокси, С1-6-галогеналкокси, 6-10-членный моноциклический или бициклический арил; 5-10-членный гетероарил, включающий 1-4 гетероатома, выбранных из N, O и S; или 4-12-членный моноциклический или бициклический гетероциклил, включающий 1-4 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо;
Z представляет собой
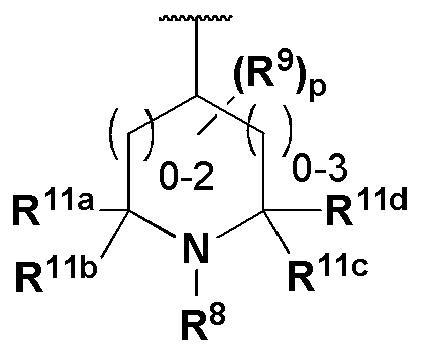 или
или 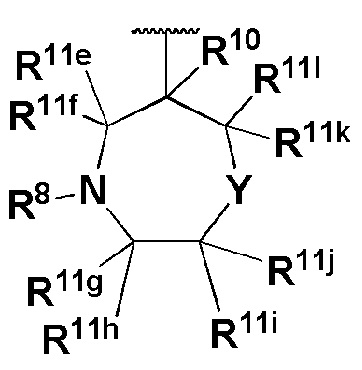
где Y представляет собой O или NR10;
R8 представляет собой
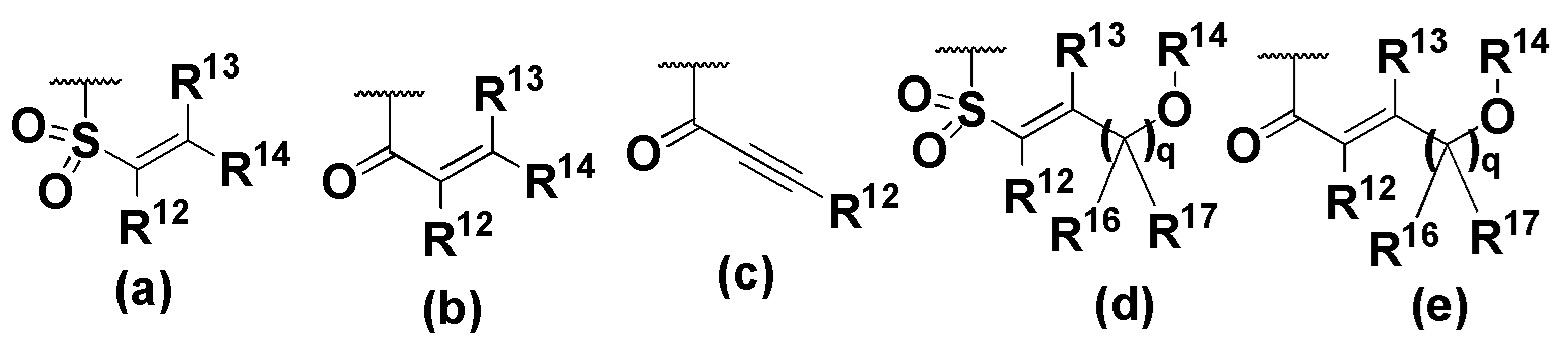
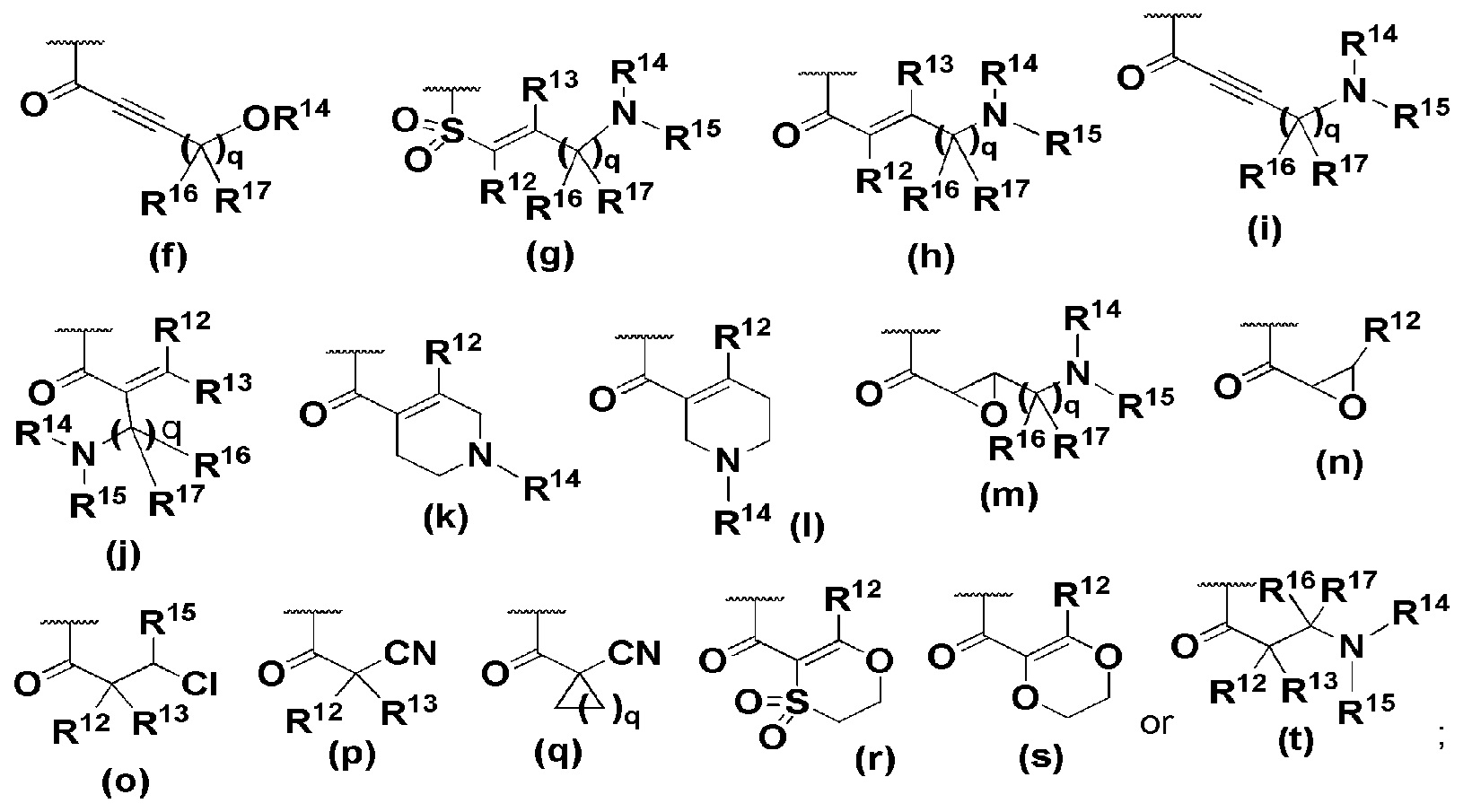
R9 и R10 независимо представляют собой водород, галоген, С1-6-алкил, С1-6-галогеналкил, ОН, циано, С1-6-алкокси, С1-6-галогеналкокси;
R11a, R11b, R11c, R11d, R11e, R11f, R11g, R11h, R11i, R11j, R11k и R11l независимо представляют собой водород, С1-6-алкил или С1-6-галогеналкил;
R12 и R13 независимо представляют собой водород, галоген, циано, С1-6-алкил или С1-6-галогеналкил;
R14 и R15 независимо представляют собой водород, C1-6-алкил, -L1-R23, -(CRaRb)2-3-Rc или -L2-Rd; или R14 и R15 совместно с N в NR14R15 могут образовывать 4-7-членное кольцо, содержащее 1-2 гетероатома, выбранных из N, O, S и P, и необязательно замещенное 1-4 группами R18;
R16 и R17 независимо представляют собой водород или C1-6-алкил; или R16 и R17 совместно с атомом углерода, к которому они присоединены, могут образовывать C3-6-циклоалкил;
X1 и X2 независимо представляют собой связь или C1-6-алкил;
X3 представляет собой C1-6-алкил;
X4 представляет собой C2-6-алкил;
R19 представляет собой водород, C1-6-алкил, COR20, COOR20, CONR20R21 или S(O)2R20;
R20 представляет собой C1-6-алкил, C1-6-галогеналкил или циклоалкил;
R21 представляет собой водород или C1-6-алкил; или R20 и R21 совместно с N в NR20R21 могут образовывать 4-7-членное кольцо, содержащее 1-2 гетероатома, выбранных из N, O, S, P и необязательно замещенное 1-4 группами R22;
R7, R18 и R22 независимо представляют собой оксо, галоген, гидрокси, C1-6-алкил, C1-6-галогеналкил, C1-6-алкокси или C1-6-галогеналкокси;
R23 независимо представляет собой C3-7-циклоалкил или 4-10-членный гетероциклил, включающий 1-3 гетероатома, выбранных из N, O и S, и необязательно замещенный оксо; и R23 не замещен или замещен C1-6-алкилом, C1-6-галогеналкилом, -L3-Re или -L4-Rf;
Rc и Re независимо представляют собой галоген, циано, гидрокси, -OR24, -NRR25, -NR-CO2R24, -NR-SO2-R26, -NR-COR26, -NR-C(O)-NRR25, -OC(O)-NRR25 или C1-6-алкил, замещенный галоген, C1-6-алкокси, гидрокси или циано;
Rd и Rf независимо друг от друга представляют собой -SO2NRR25, -CONRR25, -C(O)OR24, -SO2R26 или C(O)R26;
R24 представляет собой C1-6-алкил, C1-6-галогеналкил, -L2-R23a или -(CRaRb)2-3-N(RaRb)2;
R25 представляет собой водород, C1-6-алкил, C1-6-галогеналкил, -L2-R23b или -(CR2)2-3-N(RaRb)2;
R26 представляет собой C1-6-алкил, C1-6-галогеналкил, -L2-R23c или -(CRaRb)1-3-N(RaRb)2;
R23a, R23b и R23c независимо выбраны из R23;
R, Ra и Rb независимо представляют собой водород или C1-6-алкил;
L1, L2, L3 и L4 независимо представляют собой связь или -(CRaRb)1-3; и
n и m независимо равны 1-3; и p и q равны 1-4;
или его фармацевтически приемлемую соль, и
(iii) необязательно, по меньшей мере, один фармацевтически приемлемый носитель.
В одном из вариантов осуществления способа, ингибитор тирозинкиназы EGFR представляет собой соединение А, которое имеет химическое название (R,E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1Н-бензо[d]имидазол-2-ил)-2-метилизоникотинамид и имеет структуру
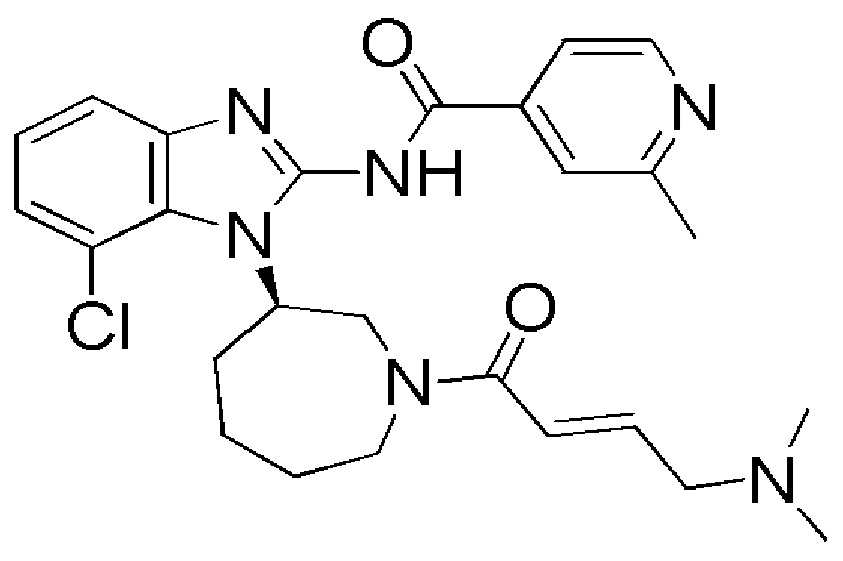 (Соединение А).
(Соединение А).
Соединение А может находиться в фармацевтически приемлемой форме, например, в виде соли хлористоводородной кислоты или в форме соли мезилата.
В одном из вариантов осуществления способа соединение INC280 находится в форме дигидрохлоридной соли кислоты.
В другом варианте осуществления INC280 находится в форме моногидрата дигидрохлоридной соли.
В одном из вариантов осуществления способа ингибитор тирозинкиназы МЕТ и ингибитор тирозинкиназы EGFR вводят одновременно, раздельно или последовательно.
В одном из вариантов осуществления способа рак выбран из группы, состоящей из карцином (например, мочевого пузыря, молочной железы, шейки матки, холангиокарциномы, колоректальной карциномы, карциномы пищевода, желудка, головы и шеи, почки, печени, легких, носоглотки, яичников, поджелудочной железы, простаты, щитовидной железы); сарком опорно-двигательного аппарата (например, остеосаркомы, синовиальной саркомы, рабдомиосаркомы); сарком мягких тканей (например, MFH/фибросаркомы, леймиосаркомы, саркомы Капоши); гемопоэтических злокачественных опухолей (например, множественной миеломы, лимфом, лейкоза Т-клеток взрослых, острого миелобластного лейкоза, хронического миелоидного лейкоза); и других новообразований (например, глиобластом, астроцитомы, меланомы, мезотелиомы и опухоли Вильмса.
В одном из вариантов осуществления способа рак представляет собой немелкоклеточный рак легкого (NSCLC).
В другом варианте осуществления способа рак представляет собой метастатический немелкоклеточный рак легкого.
В другом варианте осуществления способа рак представляет собой колоректальный рак (CRC).
В другом варианте осуществления способа рак представляет собой метастатический колоректальный рак (mCRC).
В другом варианте осуществления способа рак представляет собой рак головы и шеи.
В другом варианте осуществления способа рак представляет собой метастатический рак головы и шеи.
В еще одном варианте осуществления способа рак представляет собой плоскоклеточный рак головы и шеи (HNSCC).
ПОДРОБНОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
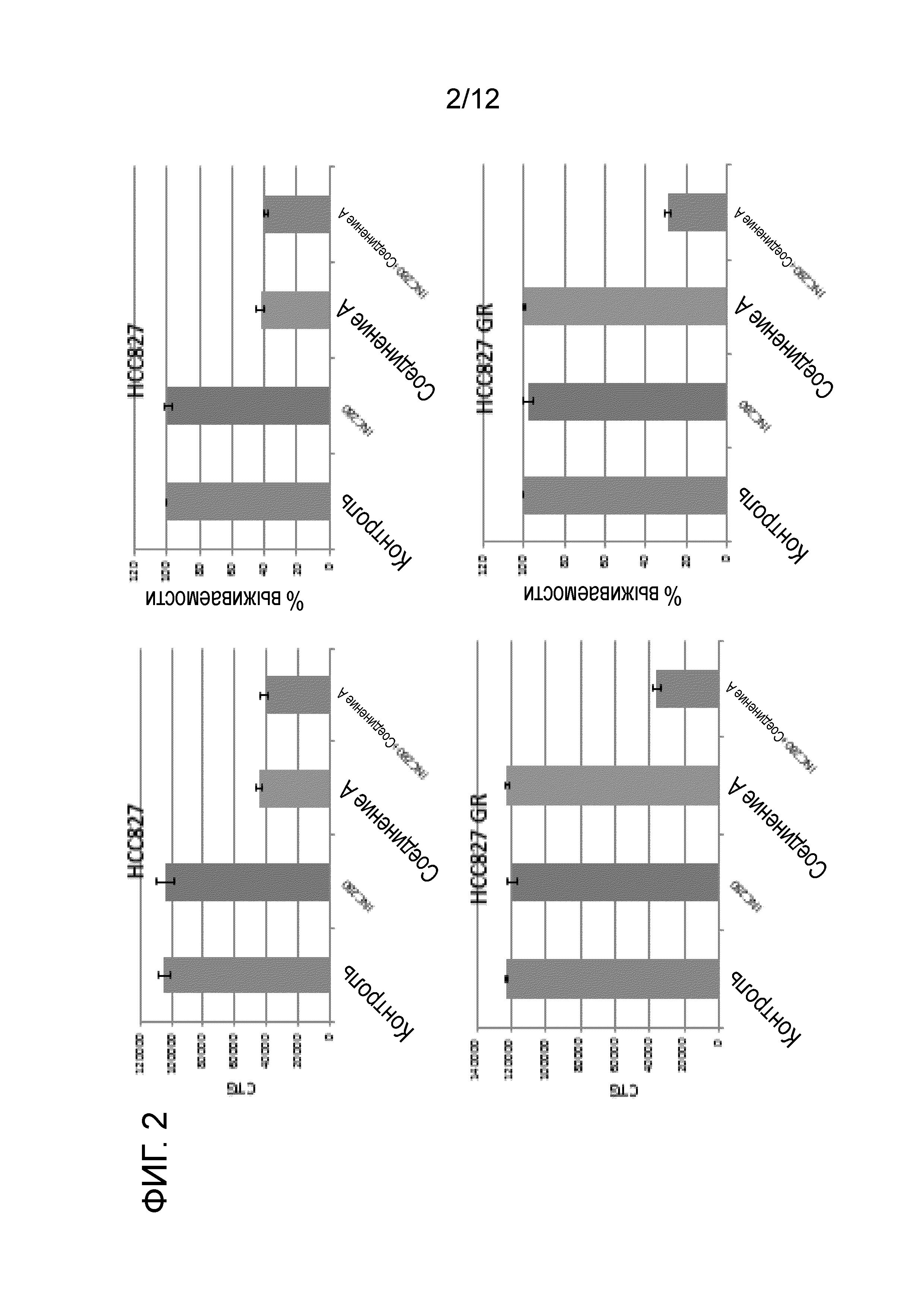
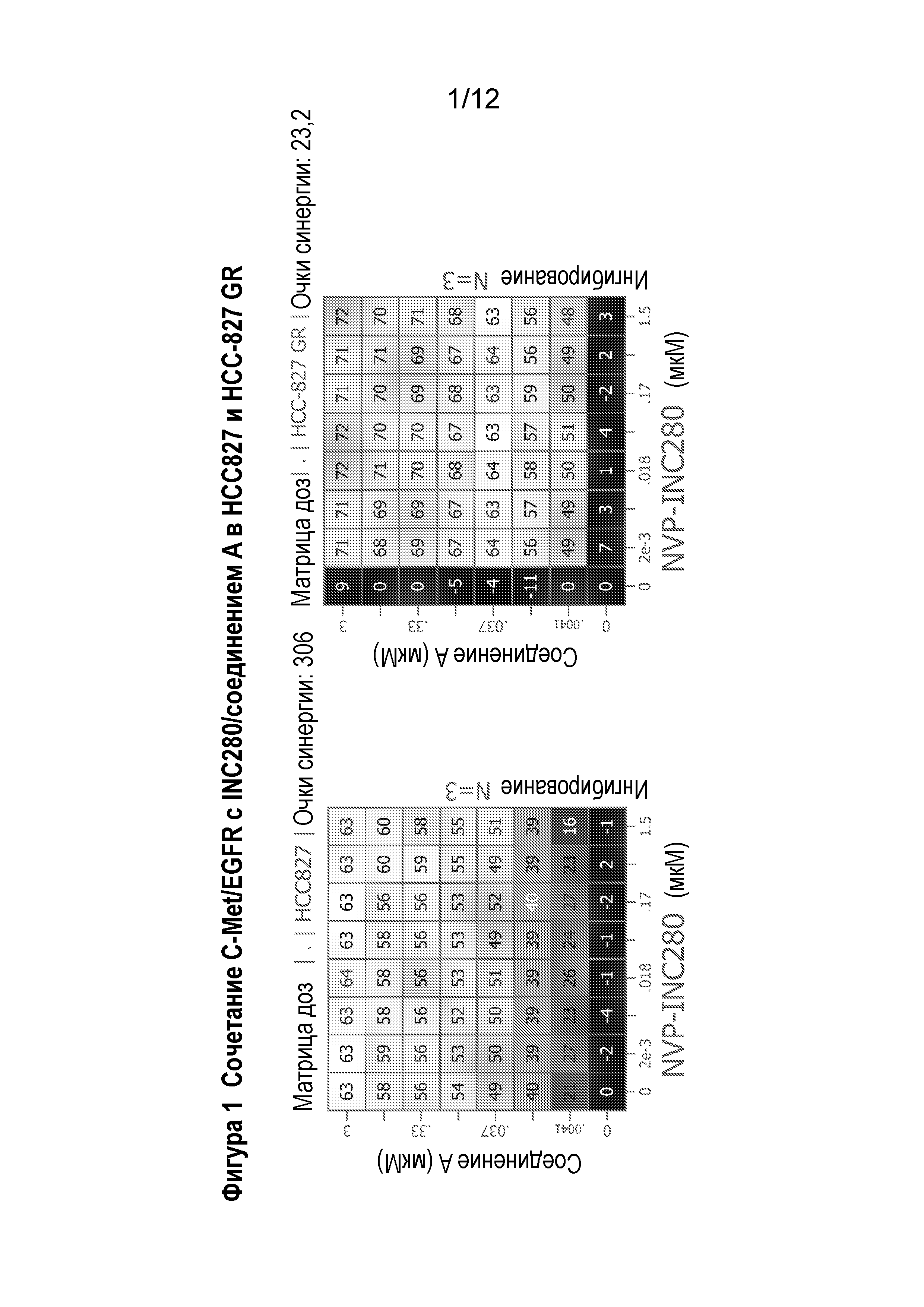
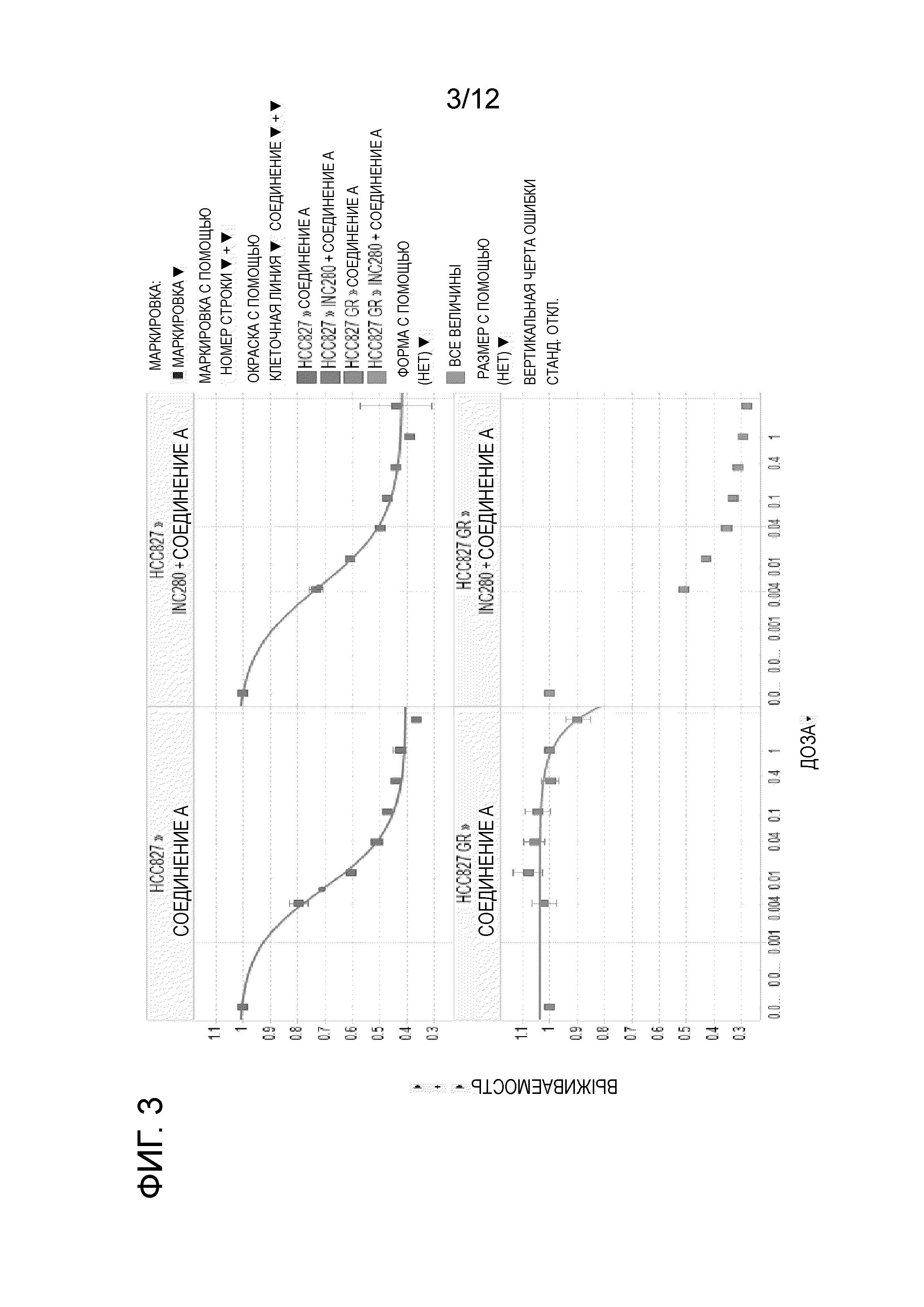
Фигуры 1-4 демонстрируют эффекты сочетания соединения А и соединения INC280.
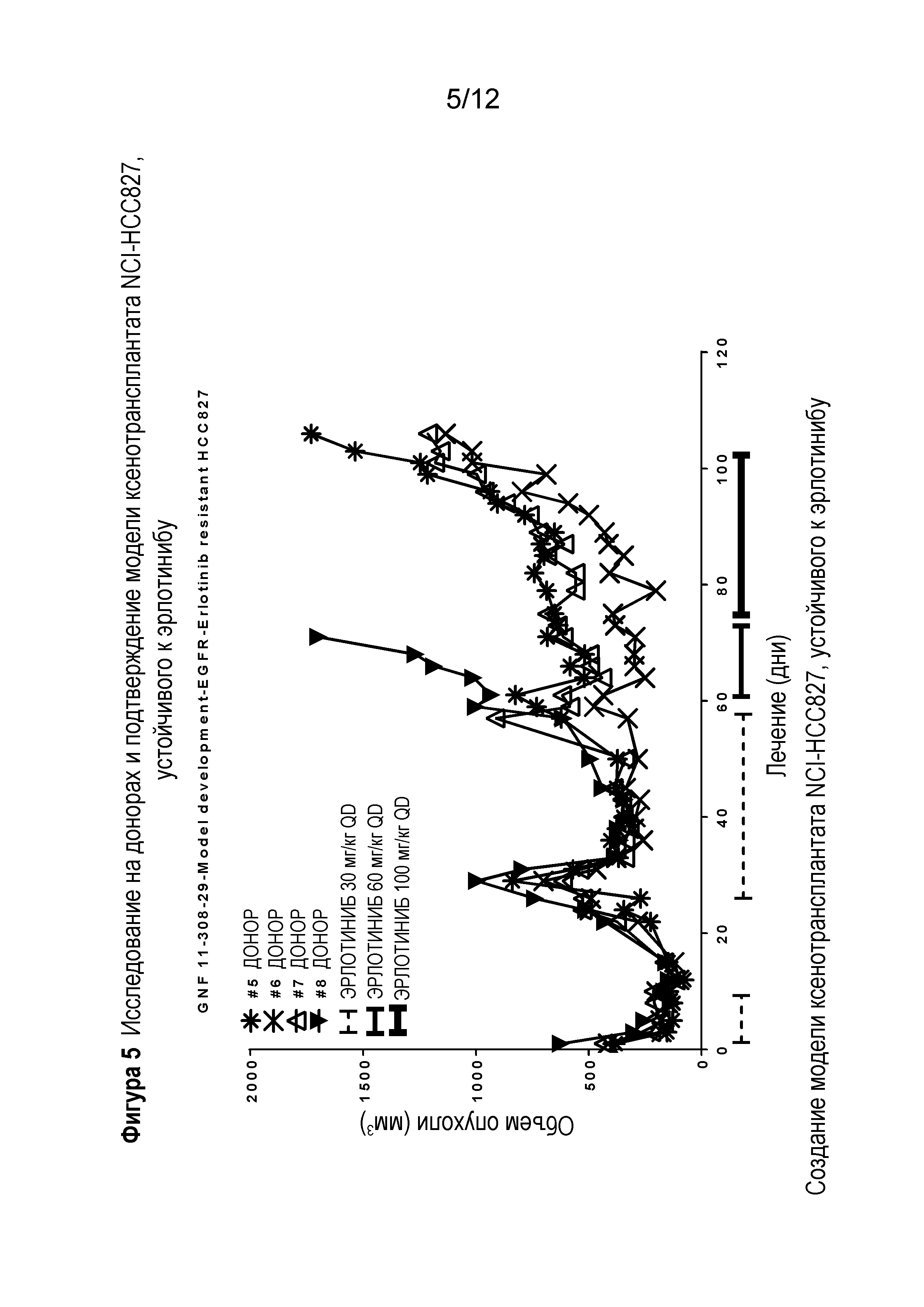
Фигура 5 иллюстрирует исследование доноров и подтверждение модели ксенотрансплантата NCI-HCC827, устойчивого к эрлотинибу.
Фигура 6 иллюстрирует подтверждение активности фосфо-MET с помощью анализа pRTK.
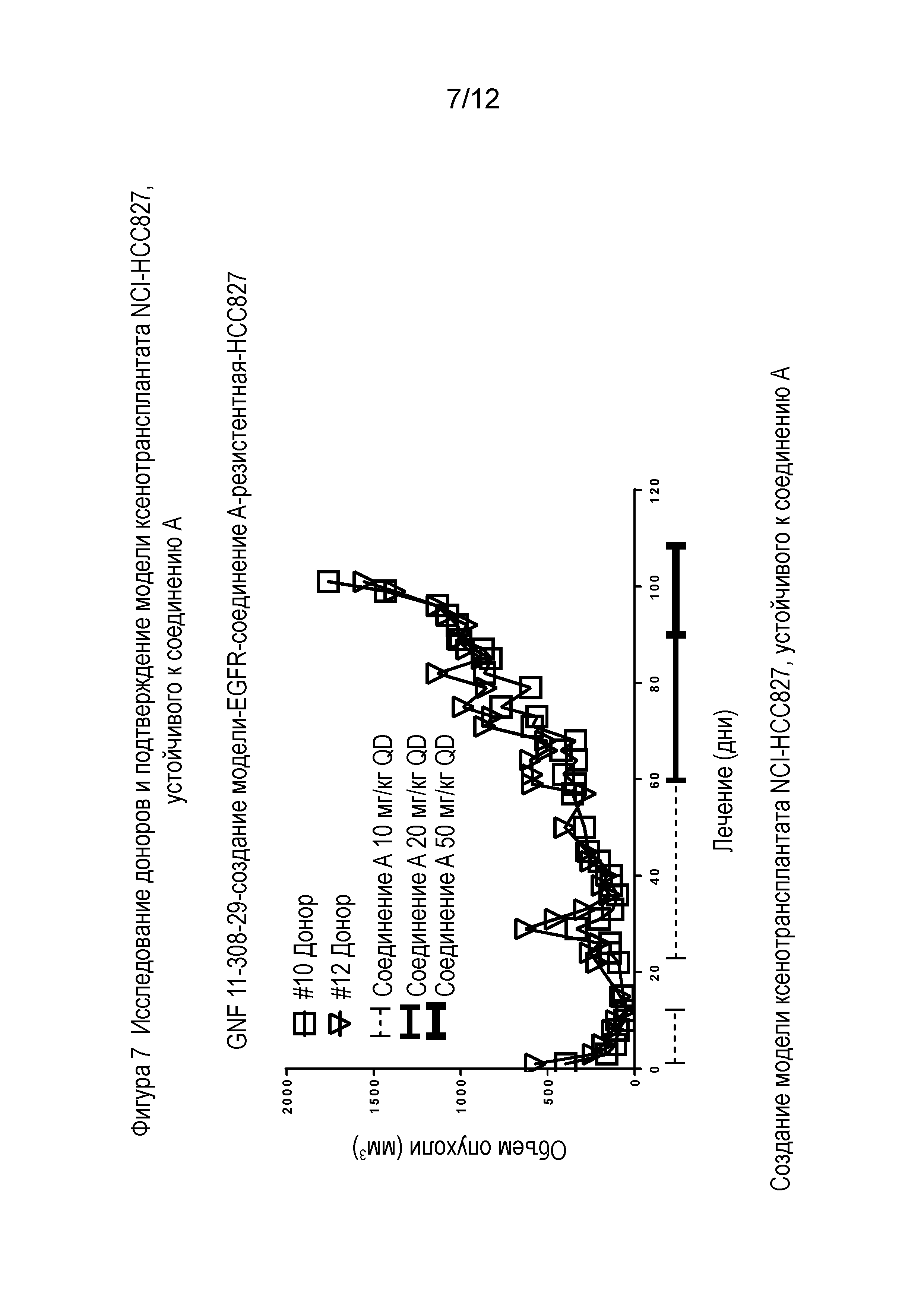
Фигура 7 иллюстрирует исследование доноров и подтверждение модели ксенотрансплантата NCI-HCC827, устойчивого к соединению А.
Фигура 8 иллюстрирует подтверждение активности фосфо-MET с помощью анализа pRTK.
Фигура 9 иллюстрирует результаты вестерн-блоттинга PD с использованием лизатов опухолей, демонстрирующие селективное снижение экспрессии pEGFR и pMET при использовании соединения А и/или соединения INC280.
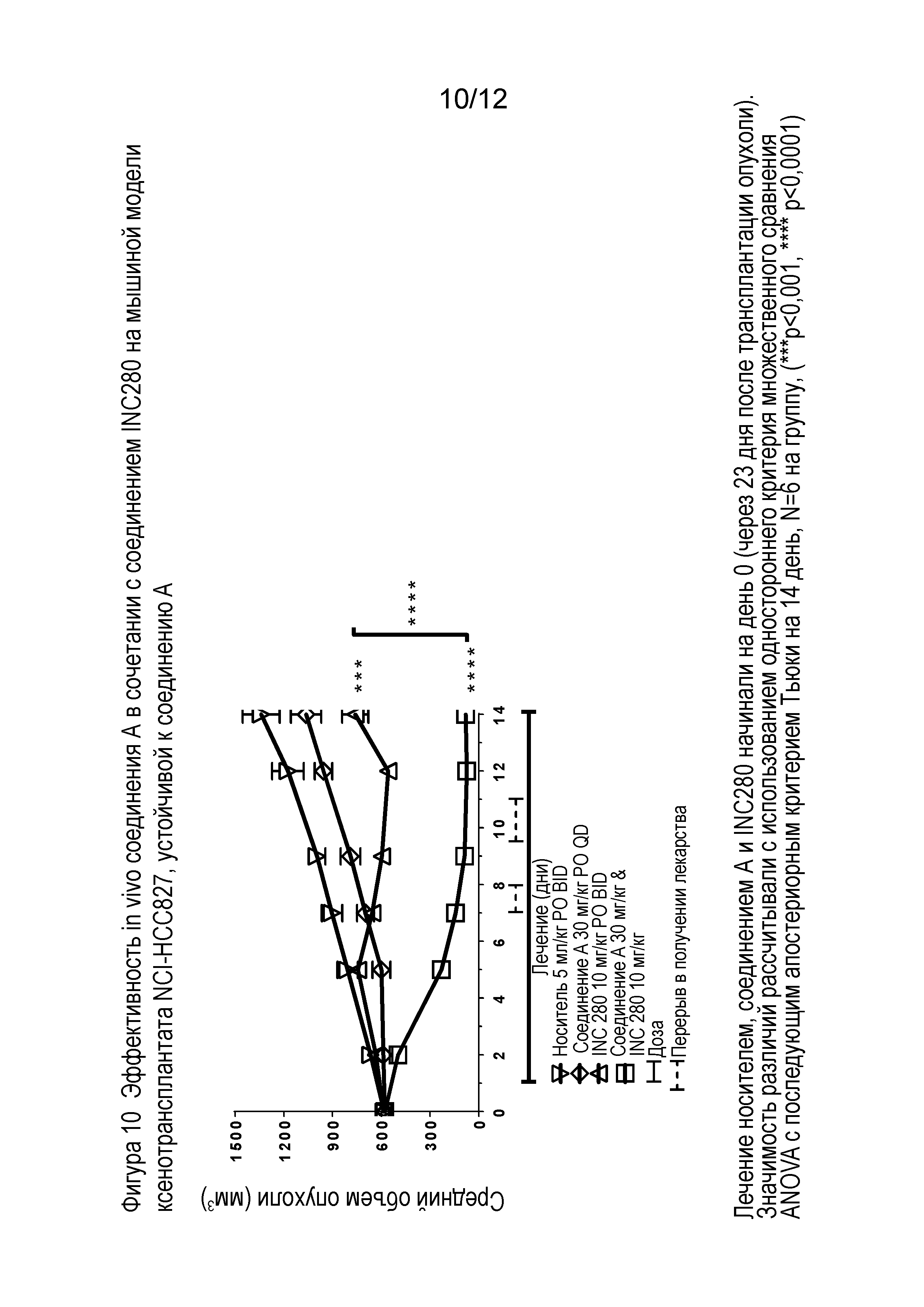
Фигура 10 иллюстрирует эффективность in vivo соединения А в сочетании с соединением INC280 на мышиной модели ксенотрансплантата NCI-HCC827, устойчивого к соединению A.
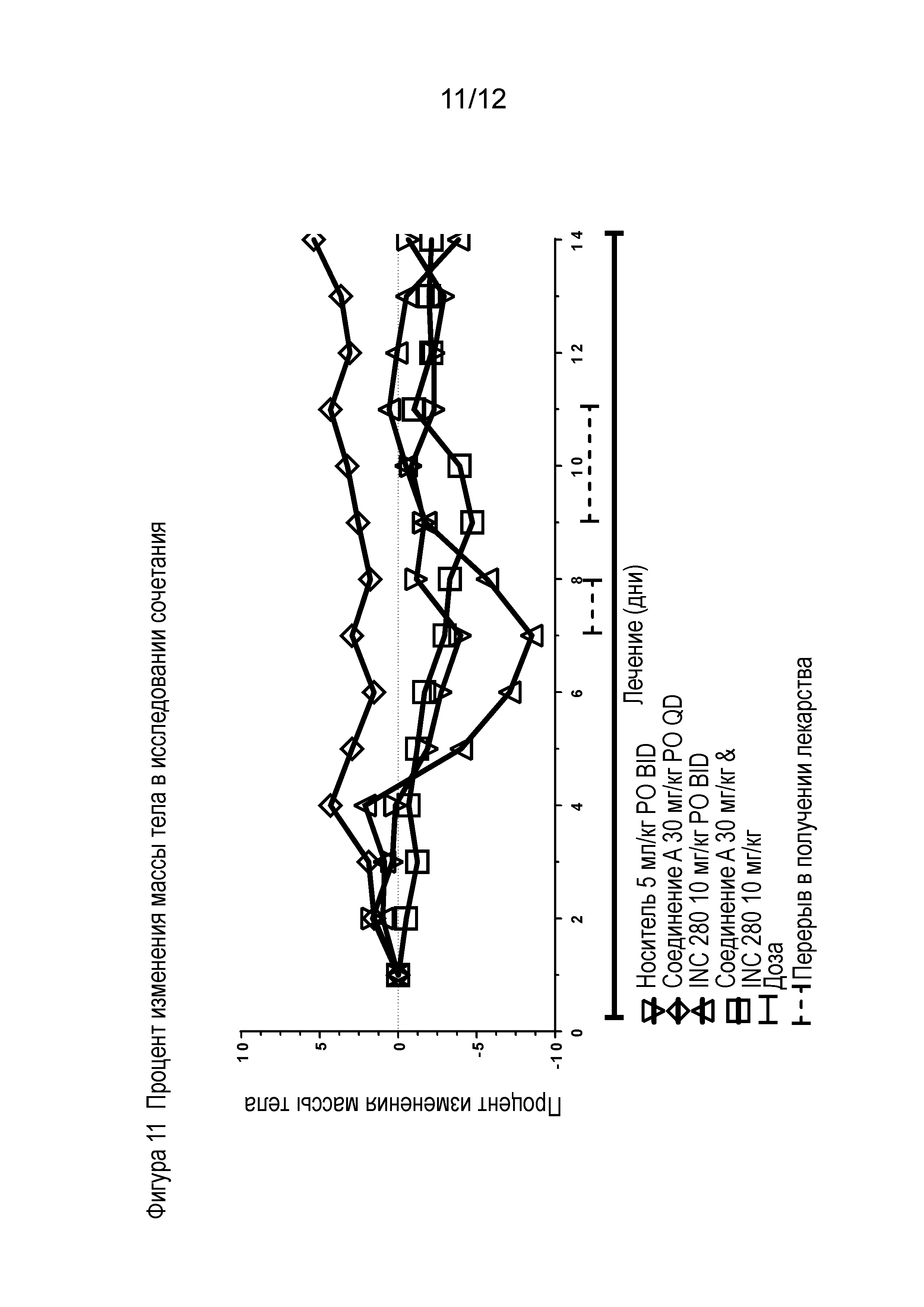
Фигура 11 показывает процент изменения массы тела в исследовании сочетания.
Фигура 12 иллюстрирует IHC и результаты гистологии.
ПОДРОБНОЕ ОПИСАНИЕ РАСКРЫТИЯ
Настоящее изобретение относится к фармацевтической комбинации, (например, к комбинированному продукту), включающей
(i) ингибитор MET, который представляет собой соединение INC280 или его фармацевтически приемлемую соль или гидрат, и (ii) ингибитор EGFR формулы (X), например, соединение А, как описано в настоящем документе.
Настоящее изобретение в соответствии с одним вариантом осуществления относится к фармацевтической комбинации, (например, к комбинированному продукту), включающей
(i) ингибитор МЕТ, который представляет собой соединение INC280 или его фармацевтически приемлемую соль и (ii) ингибитор EGFR формулы (X), описанный в данном документе, или его фармацевтически приемлемую соль и, по меньшей мере, один фармацевтически приемлемый носитель.
Предпочтительным ингибитором EGFR формулы (X) является соединение А или его фармацевтически приемлемая соль. Соединение А может быть в свободной форме (т.е. не в виде соли). В качестве альтернативы соединение А может присутствовать в виде соли. Соединение А может присутствовать в виде гидрохлоридной соли или соли мезилата (метилсульфоната), более предпочтительно в виде мономезилатной соли. Указанные мезилатные соли могут находиться в аморфном кристаллическом состоянии. Особенно пригодной формой соли соединения А является его мономезилатная тригидратная соль. Свободные формы и формы соли соединения А описаны в заявке РСТ PCT/IB2014/066475, которая опубликована как патент WO/2015/083059.
Химическим названием соединения INC280 является 2-фтор-N-метил-4-[(7-хинолин-6-ил-метил)-имидазо[1,2-b]триазин-2-ил]бензамид, который имеет формулу
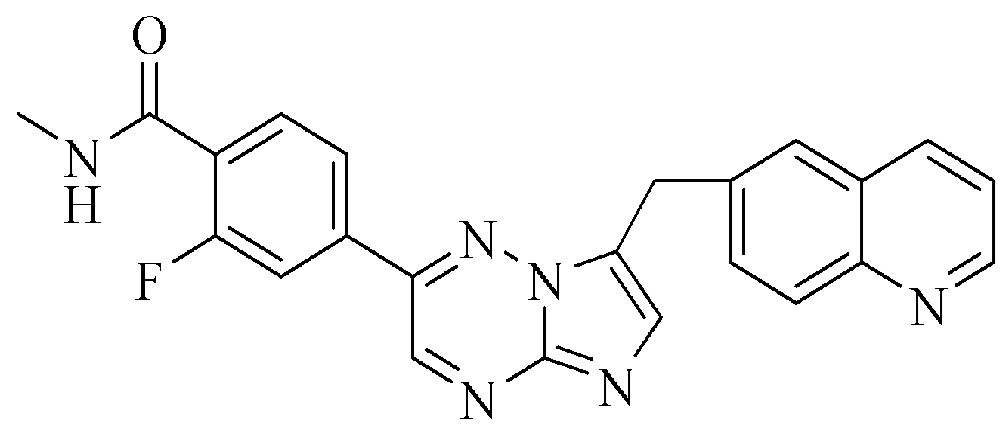
Соединение INC280 раскрыто в патенте WO 2008/064157, пример 7. Неограничивающие примеры солевых форм INC280 представляют собой формы дигидрохлоридных солей кислоты и соли дибензолсульфоновой кислоты. В частности, соединение INC280 может быть в солевой форме моногидрата дигидрохлорида (также описанного в патенте США No 8420645). Соединение INC280 также известно по своему INN, которое представляет собой капматиниб.
Еще в одном варианте осуществления настоящего изобретения предлагается комбинация (например, комбинироавнный продукт), включающая количество, которое совместно терапевтически эффективно против заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы MET, особенно рака, включающее сочетанные компоненты (i) ингибитор тирозинкиназы EGFR, который представляет собой соединение формулы (X), описанное в настоящем документе, или его фармацевтически приемлемую соль, и (ii) ингибитор тирозинкиназы MET, который представляет собой соединение INC280 или его фармацевтически приемлемую соль, и необязательно, по меньшей мере, один фармацевтически приемлемый носитель.
Еще один вариант осуществления изобретения относится к применению комбинации по изобретению (например, комбинированного продукта) для лечения заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы МЕТ, особенно рака.
Предлагается также комбинация, как описано в настоящем документе, для применения при лечении заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы МЕТ, особенно рака. Комбинация может представлять собой фиксированное сочетание или нефиксированное сочетание.
Еще один вариант осуществления изобретения относится к применению комбинации (i) ингибитора тирозинкиназы EGFR, который представляет собой соединение формулы (X), описанное в данном документе, например, соединение А, или его фармацевтически приемлемую соль, и (ii) ингибитора тирозинкиназы МЕТ, который представляет собой соединение INC280 или его фармацевтически приемлемую соль, для получения лекарства или фармацевтического продукта для лечения заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы MET, особенно рака.
Еще один вариант осуществления изобретения относится к способу лечения заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы МЕТ, особенно рака, с помощью сочетания (i) ингибитора тирозинкиназы EGFR, который представляет собой соединение формулы (Х), описанное в настоящем документе, например соединение А, или его фармацевтически приемлемую соль, и (ii) ингибитора тирозинкиназы МЕТ, который представляет собой соединение INC280 или его фармацевтически приемлемую соль.
Еще один вариант осуществления изобретения относится к способу лечения заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы МЕТ, особенно рака, причем указанный способ включает введение эффективного количества комбинации или комбинированного продукта, включающего (i) ингибитор тирозинкиназы EGFR, который представляет собой соединение формулы (X), описанное в данном документе, например, соединение А, или его фармацевтически приемлемую соль, и (ii) ингибитор тирозинкиназы МЕТ, который представляет собой соединение INC280 или его фармацевтически приемлемую соль, нуждающемуся в этом индивидууму, например, теплокровному животному, в частности человеку.
Еще один вариант осуществления настоящего изобретения относится к фармацевтическому продукту или коммерческой упаковке, включающей сочетанный продукт в соответствии с изобретением, описанный в настоящем документе, в частности, вместе с инструкциями для одновременного, раздельного или последовательного их применения (особенно для реализации совместной активности) при лечении заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы МЕТ, особенно рака, в частности, для применения при лечении заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы МЕТ, особенно рака.
Еще один вариант осуществления данного изобретения относится к применению (i) ингибитора тирозинкиназы EGFR, который представляет собой соединение формулы (X), описанное в данном документе, или его фармацевтически приемлемую соль, и (ii) ингибитора тирозинкиназы MET, который представляет собой соединение INC280 или его фармацевтически приемлемую соль, для получения сочетания (например, сочетанного продукта) в соответствии с настоящим изобретением.
Следующие определения показывают более конкретные варианты осуществления общих свойств или выражений, которые могут быть использованы для замены одного, более одного или всех общих свойств или выражений в вариантах осуществления, описанных выше и ниже, что ведет к более конкретным вариантам осуществления.
Определения
Термин «С1-6-алкил», используемый в данном описании, обозначает насыщенный или ненасыщенный алкильный радикал, имеющий от 1 до 6 атомов углерода, причем радикалы являются либо линейными, либо разветвленными с одним или несколькими разветвлениями; например, бутил, такой как н-бутил, втор-бутил, изобутил, трет-бутил; пропил, такой как н-пропил или изопропил; этил или метил. В конкретных вариантах осуществления С1-6-алкил представляет собой насыщенный алкильный радикал, и, где указано, может быть незамещенным или замещенным, например, галогеном (т.е. галогеналкил, такой как трифторметил и тому подобное), гидроксилом (гидроксиалкил, такой как гидроксиметил, гидроксиэтил, 2-гидрокси-2-пропил и тому подобное), или цианогруппой (цианоалкил, такой как цианометил, цианоэтил и тому подобное).
Термин «С1-6-алкокси», используемый в данном описании, относится к группе -ORa, где Ra представляет собой C1-6-алкильную группу, как определено в данном описании. Неограничивающие примеры алкоксигрупп, используемых в настоящем описании, включают метокси, этокси, н-пропокси, изопропокси, н-бутилокси, трет-бутилокси, пентилокси, гексилокси и тому подобное.
Термин «С1-6-галогеналкил» относится к С1-6-алкильной группе, как определено в данном описании, замещенной одной или более галогенными группами, которые могут быть одинаковыми или различными. Галогеналкил может представлять собой моногалогеналкил, дигалогеналкил или полигалогеналкил, включая пергалогеналкил. В некоторых вариантах осуществления галогеналкильная группа представляет собой трифторметил.
Термин «циклоалкил», используемый в данном описании, относится к насыщенной или ненасыщенной моноциклической углеводородной группе. Термины «С3-7-циклоалкил» или «С5-6 циклоалкил», используемые в данном описании, относятся к циклоалкилу, имеющему от 3 до 7 атомов углерода, или от 5 до 6 атомов углерода, соответственно; например, к циклопропилу, циклобутилу, циклопентилу, циклогексилу или циклогептилу.
Используемый в данном описании термин «арил» относится к ароматической углеводородной группе, имеющей 6-10 атомов углерода в структуре кольца, и оно может представлять собой одиночное или бициклическое ароматическое кольцо. Неограничивающие примеры включают фенил, нафтил или тетрагидронафтил.
Термин «гетероарил», используемый в данном описании, относится к 5-10-членному гетероароматическому кольцу, имеющему от 1 до 4 гетероатомов, независимо выбранных из азота, кислорода и серы, которое может представлять собой 5-6-членное моноциклическое кольцо или 8-10-членное конденсированное бициклическое кольцо, где, по меньшей мере, одно из колец является ароматическим. Такие бициклические системы могут быть конденсированы с одним или более арильными, циклоалкильными или гетероциклоалкильными кольцами. Неограничивающие примеры гетероарильных групп, используемых в настоящем описании, включают 2- или 3-фурил; 1-, 2-, 4- или 5-имидазолил; 3-, 4- или 5-тиазолил; 3-, 4- или 5-изоксазолил; 2-, 4- или 5-оксазолил; 4- или 5-1,2,3-оксадиазолил; 2- или 3-пиразинил; 1-, 3-, 4- или 5-пиразолил; 3-, 4-, 5- или 6-пиридазинил; 2-, 3- или 4-пиридил; 2-, 4-, 5- или 6-пиримидинил; 1-, 2- или 3-пирролил; 1- или 5-тетразолил; 2- или 5-1,3,4-тиадиазолил; 2-, 4- или 5-тиазолил; 2- или 3-тиенил; 2-, 4- или 6-1,3,5-триазинил; 1-, 3- или 5-1,2,4-триазолил; 1-, 4- или 5-1,2,3- триазолил; 2-, 4-, 5-, 6- или 7-бензоксазолил; 1-, 2-, 4-, 5-, 6- или 7-бензимидазолил; 2-, 4-, 5-, 6- или 7-бензотиазолил; 2-, 3-, 4-, 5-, 6-, 7-бензо[b]тиенил; 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9-бензо[b]оксепин; 2-, 4-, 5-, 6-, 7- или 8-бензоксазинил; 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8- или 9-карбазолил; 3-, 4-, 5-, 6-, 7- или 8-циннолинил; 2-, 4- или 5-4H-имидазо[4,5-d]тиазолил; 2-, 3-, 5- или 6-имидазо[2,1-b]тиазолил; 2-, 3-, 6- или 7-имидазо[1, 2-b][1,2,4]триазинил; 1-, 3-, 4-, 5-, 6- или 7-индазолил; 1-, 2-, 3-, 5-, 6-, 7- или 8-индолизинил; 1 -, 2-, 3-, 4-, 5-, 6- или 7-индолил; 1-, 2-, 3-, 4-, 5-, 6- или 7-изоиндолил; 1-, 3-, 4-, 5-, 6-, 7- или 8-изохинолил; 2-, 3-, 4-, 5-, 6- или 7-нафтиридинил; 1-, 4-, 5-, 6-, 7- или 8-фталазинил; 2-, 4-, 6- или 7-птеридинил; 2-, 6-, 7- или 8-пуринил; 2-, 3-, 5-, 6- или 7-фуро[3,2-b]-пиранил; 1-, 3- или 5-1Н-пиразоло[4,3-d]-оксазолил; 2-, 3-, 5- или 8-пиразино[2,3-d]пиридазинил; 1 -, 2-, 3-, 4-, 5- или 8-5H-пиридо[2,3-d]-о-оксазинил; 1-, 2-, 3-, 4-, 6-, 7-, 8- или 9-хинолизинил; 2-, 3-, 4-, 5-, 6-, 7- или 8-хинолинил; 2-, 3-, 4-, 5-, 6-, 7- или 8-хиназолинил; и 2-, 3-, 4- или 5-тиено[2,3-b]фуранил.
Используемые в настоящем описании термины «гетероциклил» или «гетероциклический» относятся к насыщенному или ненасыщенному неароматическому кольцу или кольцевой системе, например, которая представляет собой 4-, 5-, 6- или 7-членную моноциклическую, или 6, 7-, 8-, 9-, 10-, 11- или 12-членную бициклическую кольцевую систему, и содержит, по меньшей мере, один гетероатом, выбранный из O, S, P и N, где N, S и Р могут также быть необязательно окисленными до различных степеней окисления. Гетероциклическая группа может быть присоединена у гетероатома или атома углерода. Примеры гетероциклов включают тетрагидрофуран (ТГФ), дигидрофуран, 1,4-диоксан, морфолин, 1,4-дитиан, пиперазин, пиперидин, 1,3-диоксолан, имидазолидин, имидазолин, пирролин, пирролидин, азетидинил, тетрагидропиран, дигидропиран, оксатиолан, дитиолан, 1,3-диоксан, 1,3-дитиан, оксатиан, тиоморфолин и тому подобное. Там, где указано, термин «гетероциклил» дополнительно относится к гетероциклическим группам, которые замещены оксо; например, пирролидин-2-он, 1,6-дигидропиридин-2(3H)-он, пиридин-2-(3H)-он и тому подобное.
Термин «гетероатомы», используемый в данном описании, относится к атомам азота (N), кислорода (O), серы (S) или фосфора (P), где N, S и Р, необязательно могут быть окислены до различных степеней окисления.
Соединения, применяемые в соответствии с изобретением, могут также включать все изотопы атомов, присутствующих в промежуточных или конечных соединениях. Изотопы включают такие атомы, которые имеют одно и то же атомное число, но разные массовые числа. Примеры изотопов, которые могут быть включены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2H, 3H, 11C, 13C, 14C, 15N, 18F, 31P, 32P, 35S, 36Cl, 125I, соответственно. Включаются различные меченные изотопами соединения по настоящему изобретению, например, соединения, в которые включены радиоактивные изотопы, такие как 3H, 13C и 14C. Такие меченные изотопами соединения используются в метаболических исследованиях (предпочтительно 14C), исследованиях кинетических реакций (с помощью, например, 2H или 3H), методах обнаружения и визуализации [таких как позитронно-эмиссионная томография (PET) или однофотонная эмиссионная компьютерная томография (SPECT), включая анализы тканевого распределения лекарств или субстратов, или в лучевой терапии больных. В частности, 18F или меченое соединение может быть особенно предпочтительным для исследований PET или SPECT. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий (т.е. 2H), может давать определенные терапевтические преимущества в результате более высокой метаболической стабильности, например, повышенного периода полужизни in vivo или снижения требуемых дозировок. Меченные изотопами соединения по данному описанию, как правило, могут быть получены путем осуществления методов, раскрытых в схемах или в примерах и препаратах, описанных ниже, путем замены легкодоступными меченными изотопами реагентами немеченных изотопами реагентов.
Кроме того, замещение более тяжелыми изотопами, в частности дейтерием (т.е. 2H или D), может давать определенные терапевтические преимущества в результате более высокой метаболической стабильности, например, повышенного периода полужизни in vivo или снижения требуемых дозировок или улучшения терапевтического индекса. Понятно, что дейтерий в этом контексте рассматривается в качестве заместителя соединения формулы (X) и/или соединения А. Концентрация такого более тяжелого изотопа, в частности дейтерия, может быть определена с помощью коэффициента изотопного обогащения. Термин «коэффициент изотопного обогащения», используемый в настоящем описании, обозначает отношение между изотопным составом и естественным содержанием конкретного изотопа. Если заместитель в соединении по данному изобретению обозначается дейтерием, такое соединение имеет коэффициент изотопного обогащения для каждого указанного атома дейтерия, по меньшей мере, 3500 (52,5% включения дейтерия в каждом обозначенном атоме дейтерия), по меньшей мере, 4000 (60% включения дейтерия), по меньшей мере, 4500 (67,5% включения дейтерия), по меньшей мере, 5000 (75% включения дейтерия), по меньшей мере, 5500 (82,5% включения дейтерия), по меньшей мере, 6000 (90% включения дейтерия), по меньшей мере, 6333,3 (95% включения дейтерия), по меньшей мере,, 6466,7 (97% включения дейтерия), по меньшей мере, 6600 (99% включения дейтерия), или, по меньшей мере, 6633,3 (99,5% включения дейтерия). В соединениях по данному изобретению любой атом, специально не обозначенный как конкретный изотоп, предназначен для представления любого стабильного изотопа этого атома. Если не указано иное, когда положение обозначается конкретно как «H» или «водород», положение понимается как обозначающее водород в природной распространенности его изотопного состава. Соответственно, в соединениях по настоящему изобретению любой атом, конкретно обозначаемый как дейтерий (D), предназначен для представления дейтерия, например, в пределах, указанных выше.
Меченные изотопами соединения, ингибирующие тирозинкиназы MET и/или EGFR, образующие часть сочетанного продукта в соответствии с изобретением, обычно могут быть получены стандартными методами, известными специалистам в данной области техники, или способами, аналогичными способам, которые описаны в прилагаемых примерах и способах получения, с использованием подходящих меченных изотопами реагентов вместо использованных ранее немеченых реагентов.
Варианты осуществления настоящего раскрытия также включают фармацевтически приемлемые соли соединений, используемых в соответствии с изобретением, описанных в настоящем документе. Используемый в настоящем описании термин «фармацевтически приемлемые соли» относится к производным раскрытых соединений, где исходное соединение модифицируют путем превращения существующей кислотной или основной части в ее солевую форму. Примеры фармацевтически приемлемых солей включают, но не ограничиваются этим, соли минеральных или органических кислот остатков оснований, таких как амины; щелочные или органические соли остатков кислот, таких как карбоновые кислоты; и тому подобное. Фармацевтически приемлемые соли по настоящему изобретению включают обычные нетоксичные соли исходного соединения, образованные, например, из нетоксичных неорганических или органических кислот. Фармацевтически приемлемые соли по настоящему изобретению могут быть синтезированы из исходного соединения, которое содержит основную или кислотную группу, обычными химическими способами. Как правило, такие соли могут быть получены путем взаимодействия форм свободной кислоты или основания этих соединений со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе, или в смеси их двух; обычно предпочтительны неводные среды, такие как простой эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечень подходящих солей можно найти в работах Reming tonʹs Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., 1985, p. 1418 и Journal of Pharmaceutical Science, 66, 2 (1977), каждая из которых включена в настоящее описание в качестве ссылки в полном объеме.
Выражение «фармацевтически приемлемые» используется в настоящем описании для обозначения таких соединений, материалов, композиций и/или лекарственных форм, которые в пределах здравого медицинского суждения пригодны для использования в контакте с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, соразмерно с приемлемым соотношением пользы/риска.
Соединения, используемые в соответствии с изобретением (= включаемые в сочетание, особенно в сочетанный продукт, в соответствии с изобретением, соответственно, или используемые в соответствии с изобретением, необязательно включая также дополнительные сопутствующие агенты, как определено ниже, то есть все активные ингредиенты), а также их фармацевтически приемлемые соли, также могут присутствовать в виде таутомеров, N-оксидов или сольватов, например, гидратов. Все эти варианты, а также любой из них по одиночке или в сочетании двух или более до менее всех таких вариантов, охватываются и должны рассматриваться в настоящем описании, где упоминается соединение, включенное в сочетанные продукты по изобретению, например, ингибитор тирозинкиназы EGFR и/или ингибитор тирозинкиназы МЕТ.
Настоящее изобретение в соответствии с вариантом осуществления, представленным выше и ниже, относится к фармацевтической комбинации, особенно к фармацевтическому комбинированному продукту, включающему указанные компоненты сочетания и, по меньшей мере, один фармацевтически приемлемый носитель.
Настоящее изобретение также относится к фармацевтической комбинации, особенно к фармацевтическому комбинированному продукту, включающему указанные компоненты сочетания.
«Комбинация» относится к составам отдельных компонентов с или без инструкций для сочетанного использования или для комбинированных продуктов. Сочетанные компоненты могут, таким образом, представлять собой полностью отдельные фармацевтические лекарственные формы, или фармацевтические композиции, которые также продаются независимо друг от друга, и где только инструкции для их совместного применения предлагаются в приложении к упаковке, например в виде вкладыша или тому подобного, или в виде другой информации, например, предоставляемой в распоряжение врачей и медицинского персонала (например, в виде устных сообщений, сообщений в письменной форме или тому подобного), для одновременного или последовательного применения при совместной активности, особенно как это определено ниже.
«Комбирированный продукт» относится особенно к любому фиксированному сочетанию в одной единице дозированной лекарственной формы, или к набору частей для сочетанного введения, где ингибитор тирозинкиназы EGFR и ингибитор тирозинкиназы Met (и, необязательно, еще один дополнительный компонент сочетания (например, другое лекарство, как описано ниже, также обозначаемое как «сопутствующий агент»), может быть введено независимо в одно и то же время или по отдельности в течение интервалов времени, особенно, когда эти временные интервалы позволяют компонентам сочетания проявлять кооперативный (=совместный), например, синергичный эффект. Термины «совместное введение», или «сочетанное введение», или тому подобное, при использовании в данном описании, предназначены для охвата введения выбранного компонента сочетания одному индивидууму, нуждающемуся в этом (например, больному), и предназначены для включения схем лечения, при которых агенты необязательно вводят одним и тем же путем введения и/или в одно и то же время. Термин «сочетанный продукт», используемый в настоящем описании, таким образом, обозначает фармацевтический продукт, который образуется в результате смешивания или объединения более одного активного ингредиента и включает фиксированные и нефиксированные сочетания активных ингредиентов (которые также могут быть объединены).
Термин «фиксированное сочетание» обозначает, что активные ингредиенты, например, ингибитор тирозинкиназы EGFR и ингибитор тирозинкиназы МЕТ, оба вводятся больному одновременно в виде одного целого или дозированной лекарственной формы. Другими словами: активные ингредиенты присутствуют в одной лекарственной форме, например, в одной таблетке или в одной капсуле.
Термин «нефиксированное сочетание» означает, что активные ингредиенты, оба вводятся больному в виде отдельных частей, либо одновременно, совместно, либо последовательно без каких-либо конкретных ограничений по времени, причем такое введение обеспечивает терапевтически эффективные уровни двух соединений в организме больного. Последнее также применимо к лечению коктейлями, например, при введении трех или более активных ингредиентов. Термин «нефиксированное сочетание», таким образом, определяет в особенности «набор частей» в том смысле, что сочетание компонентов (i) ингибитора тирозинкиназы EGFR и (ii) ингибитора тирозинкиназы MET (и, если присутствуют, одного или более дополнительных сопутствующих агентов), как определено в данном описании, можно вводить независимо друг от друга, или путем использования различных фиксированных сочетаний с различными количествами ингредиентов композиции, т.е. одновременно или в различные моменты времени, когда ингредиенты сочетания могут быть также использованы в качестве полностью отдельных фармацевтических дозированных лекарственных форм или фармацевтических составов, которые также продаются независимо друг от друга, и только инструкции о возможности их совместного использования предлагаются в приложении к упаковке, например, в виде вкладыша или тому подобного, или в виде другой информации, например, предоставляемой в распоряжение врачей и медицинского персонала. Независимые композиции или части набора частей можно затем, например, вводить одновременно или в хронологически скользящем порядке, то есть в различные моменты времени и с одинаковыми или различными интервалами времени для любой части набора частей. Очень предпочтительно, чтобы интервалы времени выбирались таким образом, чтобы воздействие на подвергаемое лечению заболевание при сочетанном применении частей было более сильным, чем воздействие, которое было бы получено при использовании только любого одного из компонентов (i) и (ii) сочетания, таким образом, что они будут совместно активными. Отношение суммарных количеств компонента (i) сочетания к компоненту (ii) сочетания, подлежащих введению в объединенном препарате, может варьироваться, например, для того, чтобы справиться с потребностями субпопуляции больных, подлежащих лечению, или с потребностями конкретного больного, которые отличаются, что может быть обусловлено различиями возраста, пола, массы тела больных и т.д.
Настоящее изобретение также относится (i) к ингибитору MET, который представляет собой соединение INC280 или его фармацевтически приемлемую соль, и (ii) к ингибитору EGFR, который представляет собой соединение формулы (X), описанное в данном документе, или его фармацевтически приемлемую соль, для сочетанного применения в способе лечения заболевания, опосредованного активностью тирозинкиназы EGFR и/или активностью тирозинкиназы МЕТ, особенно рака.
Компоненты (i) и (ii) сочетания в любом варианте осуществления предпочтительно составляют или используют так, чтобы они были совместно (профилактически или особенно терапевтически) активными. Это означает, в частности, что существует, по меньшей мере, один полезный эффект, например, взаимное усиление эффекта компонентов (i) и (ii) сочетания, в частности синергизм, например, более чем аддитивный эффект, дополнительные благоприятные эффекты (например, дополнительный терапевтический эффект, не обнаруженный для любого из отдельных соединений), меньше побочных эффектов, сочетанный терапевтический эффект в неэффективном дозе одного или обоих компонентов (i) и (ii) сочетания, и очень предпочтительно четкий синергизм компонентов (i) и (ii) сочетания. Например, термин «совместно (терапевтически) активные» может означать, что соединения могут быть введены отдельно или последовательно (в хронологически скользящем порядке, особенно в конкретном последовательном порядке) в такие интервалы времени, что они предпочтительно, у теплокровного животного, особенно человека, подвергаемого лечению, все еще демонстрируют (предпочтительно синергичное) взаимодействие (совместный терапевтический эффект). Совместный терапевтический эффект может среди прочего определяться последующими уровнями в крови, показывающими, что оба соединения присутствуют в крови человека, подлежащего лечению, по меньшей мере, в течение определенных интервалов времени, но это не исключает случай, когда соединения являются совместно активными, хотя они не присутствуют в крови одновременно.
Таким образом, настоящее изобретение относится к сочетанному продукту для одновременного, раздельного или последовательного применения, такому как сочетанный препарат или фармацевтическое фиксированное сочетание, или сочетание такого препарата и такого сочетания.
В сочетанной терапии по изобретению соединения, используемые в соответствии с изобретением, могут быть получены и/или составлены одними и теми же или разными производителями. Кроме того, сочетанные компоненты могут быть объединены вместе в сочетанной терапии: (i) перед передачей сочетанного продукта врачам (например, в случае набора, включающего соединение по данному изобретению и другой терапевтической агент); (ii) самими врачами (или под руководством врача) незадолго до введения; (iii) самими больными, например, во время последовательного введения соединения по данному изобретению и другого терапевтического агента.
В некоторых вариантах осуществления любой из указанных выше способов включает дополнительное введение одного или более других (например, третьих) сопутствующих агентов, особенно химиотерапевтического агента.
Таким образом, в еще одном варианте осуществления изобретение относится к сочетанному продукту, в частности, к фармацевтической композиции, включающей терапевтически эффективное количество (i) ингибитора тирозинкиназы EGFR, который представляет собой соединение формулы (X), описанное в данном документе, или его фармацевтически приемлемой соли и (ii) ингибитора тирозинкиназы МЕТ, который представляет собой соединение INC280, или его фармацевтически приемлемой соли, и, по меньшей мере, одного третьего терапевтически активного агента (сопутствующего агента), например, другого соединения (i) и/или (ii) или другого сопутствующего агента. Дополнительный сопутствующий агент предпочтительно выбран из группы, состоящей из противоракового агента; противовоспалительного агента.
В этом случае также сочетанные компоненты, образующие соответствующий продукт в соответствии с изобретением, могут быть смешаны с образованием фиксированной фармацевтической композиции, или они могут быть введены по отдельности или попарно (т.е. перед, одновременно или после других лекарственных(ого) веществ(а)).
Сочетанный продукт в соответствии с изобретением кроме этого или дополнительно в особенности для лечения рака можно вводить в сочетании с химиотерапией, лучевой терапией, иммунотерапией, хирургическим вмешательством или их сочетаниями. Долгосрочная терапия в равной степени возможна, как и адъювантная терапия в контексте других стратегий лечения, как описано выше. Другие возможные методы лечения представляют собой терапию для поддержания состояния больных после регрессии опухоли или даже химиопрофилактическую терапию, например, у больных в состоянии риска.
Возможные противораковые агенты (например, для химиотерапии) в качестве сопутствующих агентов включают, но не ограничиваются этим, ингибиторы ароматазы; антиэстрогены; ингибиторы топоизомеразы I; ингибиторы топоизомеразы II; соединения, активные в отношении микротрубочек; алкилирующие соединения; ингибиторы гистондеацетилазы; соединения, которые индуцируют процессы дифференцировки клеток; ингибиторы циклооксигеназы; ингибиторы MMP; ингибиторы mTOR; противоопухолевые антиметаболиты; соединения платины; соединения, направленно действующие/снижающие белковый продукт или активность липидкиназы; антиангиогенные соединения; соединения, которые направленно действуют, снижают или ингибируют активность белка или фосфатазы липидов; агонисты гонадорелина; антиандрогены; ингибиторы метионинаминопептидазы; бисфосфонаты; модификаторы биологической реакции; антипролиферативные антитела; ингибиторы гепараназы; ингибиторы онкогенных изоформ Ras; ингибиторы теломеразы; ингибиторы протеасом; соединения, используемые при лечении гематологических злокачественных новообразований, соединения, которые направленно действуют, снижают или ингибируют активность Flt-3; ингибиторы Hsp90; ингибиторы белка веретена кинезина; ингибиторы МЕК; лейковорин; агенты, связывающие EDG; соединения, направленные против лейкоза; ингибиторы рибонуклеотидредуктазы; ингибиторы S-аденозилметиониндекарбоксилазы; ангиостатические стероиды; кортикостероиды; другие химиотерапевтические соединения (как определено ниже); фотосенсибилизирующие соединения.
Кроме того, альтернативно или дополнительно сочетанные продукты в соответствии с изобретением могут быть использованы в сочетании с другими подходами к лечению опухолей, включая хирургическое вмешательство, ионизирующее облучение, фотодинамическую терапию, имплантаты, например с кортикостероидами, гормоны, или же они могут быть использованы в качестве радиосенсибилизаторов.
Термин «ингибитор ароматазы», используемый в настоящем описании, относится к соединению, которое ингибирует продукцию эстрогенов, т.е. превращение субстратов андростендиона и тестостерона в эстрон и эстрадиол, соответственно. Этот термин включает, но не ограничивается этим, стероиды, особенно атаместан, экземестан и форместан и, в частности, нестероидные агенты, особенно аминоглутетимид, роглетимид, пиридоглутетимид, трилостан, тестолактон, кетоконазол, ворозол, фадрозол, анастрозол и летрозол.
Термин «антиэстроген», используемый в настоящем описании, относится к соединению, которое противодействует эффекту эстрогенов на уровне рецепторов эстрогенов. Этот термин включает, но не ограничивается этим, тамоксифен, фулвестрант, ралоксифен и ралоксифена гидрохлорид.
Термин «антиандроген», используемый в настоящем описании, относится к любому веществу, которое способно ингибировать биологические эффекты андрогенных гормонов, и включает, но не ограничивается этим, бикалутамид (CASODEX), который может быть составлен, например, как описано в патенте США 4636505.
Термин «агонист гонадорелина», используемый в настоящем описании, включает, но не ограничивается этим, абареликс, гозерелин и ацетат гозерелина. Термин «ингибитор топоизомеразы I», используемый в данном описании, включает, но не ограничивается этим топотекан, гиматекан, иринотекан, камптотекан и его аналоги, 9-нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148 (соединение А1 в патенте WO99/17804).
Термин «ингибитор топоизомеразы II», используемый в настоящем описании, включает, но не ограничивается этим, антрациклины, такие как доксорубицин (включая липосомную композицию, например, CAELYX), даунорубицин, эпирубицин, идаруцибин и неморубицин, антрахиноны - митоксантрон и лосоксантрон и подофиллотоксины - этопозид и тенипозид.
Термин «соединение, активное в отношении микротрубочек» относится к соединениям, стабилизирующим микротрубочки, дестабилизирующим микротрубочки, и к ингибиторам полимеризации микротубулина, включая, но, не ограничиваясь этим, таксаны, например, паклитаксел и доцетаксел, алкалоиды барвинка, например, винбластин, особенно винбластина сульфат, винкристин, особенно винкристина сульфат, и винорелбин, дискодермолиды, колхицин и эпотилоны и их производные, например, эпотилон В или D или их производные.
Термин «алкилирующие соединения», используемый в настоящем описании, включает, но не ограничивается этим, циклофосфамид, ифосфамид, мелфалан или нитрозомочевины (BCNU или глиадел).
Термин «ингибиторы гистондеацетилазы» или «ингибиторы HDAC» относится к соединениям, которые ингибируют гистондеацетилазу и которые обладают антипролиферативной активностью. Они включают соединения, описанные в патенте WO 02/22577, особенно N-гидрокси-3-[4-[[(2-гидроксиэтил)[2-(1Н-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид, N-гидрокси-3-[4-[[[2-(2-метил-1Н-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид и их фармацевтически приемлемые соли. Кроме того, они дополнительно особенно включают субероиланилид гидроксамовой кислоты (SAHA). Соединения, которые направленно действуют, снижают или ингибируют активность ингибиторов гистондеацетилазы (HDAC), такие как бутират натрия и субероиланилид гидроксамовой кислоты (SAHA), ингибируют активность ферментов, известных как гистондеацетилазы. Специфические ингибиторы HDAC включают MS275, SAHA, FK228 (ранее FR901228), трихостатин А и соединения, раскрытые в патенте США 6552065, в частности, N-гидрокси-3-[4- [[[2-(2-метил-1H-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид или его фармацевтически приемлемую соль и N-гидрокси-3-[4-[(2-гидроксиэтил){2-(1Н-индол-3-ил)этил]амино]метил]фенил]- 2E-2-пропенамид или его фармацевтически приемлемую соль, особенно соль молочной кислоты.
Термин «противоопухолевый антиметаболит» включает, но не ограничивается этим, 5-фторурацил или 5-FU, капецитабин, гемцитабин, соединения, деметилирующие ДНК, такие как 5-азацитидин и децитабин, метотрексат и эдатрексат и антагонисты фолиевой кислоты, такие как пеметрексед.
Термин «соединения платины», используемый в настоящем описании, включает, но не ограничивается этим, карбоплатин, цисплатин, цисплатин и оксалиплатин.
Термины «соединения, направленно действующие/снижающие белковый продукт или активность липидкиназы»; или «белковый продукт или активность липидфосфатазы»; или «дополнительные антиангиогенные соединения», используемые в данном описании, включают, но не ограничиваются этим, ингибиторы тирозинкиназы с-Met и/или ингибиторы серин- и/или треонинкиназ или ингибиторы липидкиназ, например,
а) соединения, направленно действующие, снижающие или ингибирующие активность рецепторов фактора роста из тромбоцитов (PDGFR), такие как соединения, которые направленно действуют, снижают или ингибируют активность PDGFR, особенно соединения, которые ингибируют рецептор PDGF, например, производное N-фенил-2-пиримидинамина, например, иматиниб, SU101, SU6668 и GFB-111;
b) соединения, направленно действующие, снижающие или ингибирующие активность рецептора инсулиноподобного фактора роста I (IGF-IR), такие как соединения, которые направленно действуют, снижают или ингибируют активность IGF-IR, особенно соединения, которые ингибируют киназную активность IGF-IR, такие как соединения, описанные в патенте WO 02/092599, или антитела, которые направлены на внеклеточный домен рецептора IGF-I или на действующие на него факторы роста;
c) соединения, направленно действующие, снижающие или ингибирующие активность семейства рецепторных тирозинкиназ Trk, или ингибиторы семейства киназ эфриновых рецепторов;
d) соединения, направленно действующие, снижающие или ингибирующие активность рецепторных тирозинкиназ семейства Axl;
e) соединения, направленно действующие, снижающие или ингибирующие активность рецепторной тирозинкиназы Ret;
f) соединения, направленно действующие, снижающие или ингибирующие активность рецепторной тирозинкиназы Kit/SCFR, например, иматиниб;
g) соединения, направленно действующие, снижающие или ингибирующие активность рецепторных тирозинкиназ C-Kit - (часть семейства PDGFR), такие как соединения, которые направленно действуют, снижают или ингибируют активность семейства рецепторных тирозинкиназ с-Kit, особенно соединения, которые ингибируют рецептор с-Kit, например, иматиниб;
h) соединения, направленно действующие, снижающие или ингибирующие активность членов семейства с-Abl, их гибридных генных продуктов (например, BCR-Abl-киназы) и мутантов, такие как соединения, которые направленно действуют, снижают или ингибируют активность членов семейства с-Abl и их гибридных генных продуктов, например, производное N-фенил-2-пиримидинамина, например, иматиниб или нилотиниб (AMN107); PD180970; AG957; NSC 680410; PD173955 от ParkeDavis; или дазатиниб (BMS-354825);
i) соединения, направленно действующие, снижающие или ингибирующие активность членов семейства протеинкиназы С (ПКС) и серин/треонинкиназ Raf, членов семейств MEK, SRC, JAK, FAK, PDK1, PKB/Akt и Ras/MAPK и/или членов семейства циклинзависимых киназ (CDK), и особенно те производные стауроспорина, которые раскрыты в патенте США 5093330, например, мидостаурин; примеры дополнительных соединений включают, например, UCN-01, сафингол, BAY 43-9006, бриостатин 1, перифозин; лимофозин; RO 318220 и RO 320432; GO 6976; Isis 3521; LY333531/LY379196; соединения изохинолина, такие как соединения, описанные в патенте WO 00/09495; FTIs; PD184352 или QAN697 (ингибитор P13K) или AT7519 (ингибитор CDK);
j) соединения, направленно действующие, снижающие или ингибирующие активность ингибиторов белковых тирозинкиназ, такие как соединения, которые направленно действуют, снижают или ингибируют активность ингибиторов белковых тирозинкиназ, включающие мезилат иматиниба (GLEEVEC) или тирфостин. Тирфостин предпочтительно представляет собой соединение с низкой молекулярной массой (М.м. <1500) или его фармацевтически приемлемую соль, особенно соединение, выбранное из класса бензилиденмалонитрила или S-арилбензолмалонитрила, или соединения класса бисубстратных хинолинов, более конкретно, любое соединение, выбранное из группы, состоящей из тирфостина A23/RG-50810; AG 99; тирфостина AG 213; тирфостина AG 1748; тирфостина AG 490; тирфостина B44; (+) энантиомера тирфостина В44; тирфостина AG 555; AG 494; тирфостина AG 556, AG957 и адафостина, адамантилового эфира (4-{[(2,5-дигидроксифенил)метил]амино}бензойной кислоты; NSC 680410, адафостина);
k) соединения, направленно действующие, снижающие или ингибирующие активность семейства рецепторных тирозинкиназ эпидермальных факторов роста (EGFR, ErbB2, ErbB3, ErbB4, как гомо- или гетеродимеров) и их мутантов, такие как соединения, которые направленно действуют, снижают или ингибируют активность семейства рецепторов эпидермального фактора роста, особенно представляют собой соединения, белки или антитела, которые ингибируют членов семейства рецепторных тирозинкиназ EGF, например, рецептор EGF, ErbB2, ErbB3 и ErbB4, или связываются с EGF или с лигандами, родственными EGF, и, в частности, представляют собой те соединения, белки или моноклональные антитела, в целом и конкретно раскрытые в патенте WO 97/02266, например, соединение примера 39, или в патентах ЕР 0564409, WO 99/03854, ЕР 0520722, ЕР 0566226, ЕР 0787722, ЕР 0837063, US 5747498, WO 98/10767, WO 97/30034, WO 97/49688, WO 97/38983 и, в частности, в патенте WO 96/30347 (например, соединение, известное, как СР 358774), патенте WO 96/33980 (например, соединение ZD 1839) и патенте WO 95/03283 (например, соединение ZM105180); например трастузумаб (герцептин™), цетуксимаб (эрбитукс™), иресса, тарцева, OSI-774, CI-1033, EKB-569, GW-2016, E1,1, E2.4, E2.5, E6.2, E6.4, E2.11, E6.3 или E7.6.3 и 7H-пирроло[2,3-d]пиримидиновые производные, которые раскрыты в патенте WO 03/013541; а также
l) соединения, направленно действующие, снижающие или ингибирующие активность рецептора с-Met, такие как соединения, которые направленно действуют, снижают или ингибируют активность с-Met, особенно соединения, которые ингибируют киназную активность рецептора с-Met, или антитела, которые направлены на внеклеточный домен с-Met или связываются с HGF;
m) соединения, направленно действующие, снижающие или ингибирующие активность рецепторной тирозинкиназы Ron.
Дополнительные антиангиогенные соединения включают соединения, имеющие другой механизм своей активности, например, не связанный с ингибированием белкового продукта или липидкиназы, например, талидомид (THALOMID) и TNP-470.
Термин «соединения, направленно действующие, снижающие или ингибирующие активность белкового продукта или липидфосфатазы» включает, но не ограничивается этим, ингибиторы фосфатазы 1, фосфатазы 2А, или CDC25, например, окадаевую кислоту или ее производное. Термин «соединения, которые индуцируют процессы клеточной дифференцировки» включает, но не ограничивается этим, например, ретиноевую кислоту, α-, γ- или δ-токоферол или α-, γ- или δ-токотриенол.
Термин «ингибитор циклооксигеназы», используемый в настоящем описании, включает, но не ограничивается этим, например, ингибиторы СОХ-2, 5-алкил-замещенную 2-ариламинофенилуксусную кислоту и производные, такие как целекоксиб (CELEBREX), рофекоксиб (VIOXX), эторикоксиб, валдекоксиб или 5-алкил-2-ариламинофенилуксусную кислоту, например, 5-метил-2-(2'-хлор-6'-фторанилино)фенилуксусную кислоту, лумиракоксиб. Термин «бисфосфонаты», используемый в настоящем описании, включает, но не ограничивается этим, этридоновую, клодроновую, тилудроновую, памидроновую, алендроновую, ибандроновую, ризедроновую и золедроновую кислоту.
Термин «ингибиторы mTOR» относится к соединениям, которые ингибируют мишень рапамицина млекопитающих (mTOR) и которые обладают антипролиферативным действием, такие как сиролимус (Rapamune®), эверолимус (Certican™), CCI-779 и АВТ578.
Термин «ингибитор гепараназы», используемый в данном описании, относится к соединениям, которые направленно действуют, снижают или ингибируют деградацию гепаринсульфата. Этот термин включает, но не ограничивается этим, PI-88.
Термин «модификатор биологического ответа», используемый в данном описании, относится к лимфокину или интерферонам, например, интерферону γ.
Термин «ингибитор онкогенных изоформ Ras», например, H-Ras, K-Ras или N-Ras, используемый в настоящем описании, относится к соединениям, которые направленно действуют, снижают или ингибируют онкогенную активность Ras, например, к «ингибитору фарнезилтрансферазы», например, L-744832, DK8G557 или R115777 (Zarnestra).
Термин «ингибитор теломеразы», используемый в данном описании, относится к соединениям, которые направленно действуют, снижают или ингибируют активность теломеразы. Соединения, которые направленно действуют, снижают или ингибируют теломеразы, особенно представляют собой соединения, которые ингибируют рецептор теломеразы, например, теломестатин.
Термин «ингибитор метионинаминопептидазы», используемый в настоящем описании, относится к соединениям, которые направленно действуют, снижают или ингибируют активность метионинаминопептидазы. Соединения, которые направленно действуют, снижают или ингибируют активность метионинаминопептидазы, представляют собой, например, бенгамид или его производное.
Термин «ингибитор протеасомы», используемый в данном описании, относится к соединениям, которые направленно действуют, снижают или ингибируют активность протеасомы. Соединения, которые направленно действуют, снижают или ингибируют активность протеасомы, включают, например, бортезомид (Velcade™) и MLN 341.
Термин «ингибитор металлопротеиназы матрикса» или (ингибитор «ММР»), используемый в настоящем описании, включает, но не ограничивается этим, ингибиторные пептидомиметики и непептидомиметики коллагена, производные тетрациклина, например, гидроксаматный ингибиторный пептидомиметик батимастат и его биодоступный перорально аналог маримастат (BB-2516), приномастат (AG3340), метастат (NSC 683551) BMS-279251, BAY 12-9566, TAA211, MMI270B или AAJ996.
Термин «соединения, используемые при лечении гематологических злокачественных новообразований», используемый в данном описании, включает, но не ограничивается этим, ингибиторы FMS-подобных тирозинкиназ, например, соединения, направленно действующие, снижающие или ингибирующие активность рецепторных FMS-подобных тирозинкиназ (FLT-3R); интерферон, 1-b-D-арабинофуранзилцитозин (ara-C) и бисульфан; и ингибиторы ALK, например, соединения, которые направленно действуют, снижают или ингибируют киназу анапластической лимфомы.
Термин «соединения, которые направленно действуют, снижают или ингибируют активность рецепторных FMS-подобных тирозинкиназ (Flt-3R)» особенно представляют собой соединения, белки или антитела, которые ингибируют членов семейства рецепторных киназ Flt-3R, например, РКС412, мидостаурин, производное стауроспорина, SU11248 и MLN518.
Термин «ингибиторы HSP90», используемый в данном документе, включает, но не ограничивается этим, соединения, которые направленно действуют, снижают или ингибируют присущую HSP90 АТФ-азную активность; вызывающие деградацию, направленно действующие, снижающие или ингибирующие клиентские белки HSP90 через убиквитин-протеасомный путь. Соединения, направленно действующие, снижающие или ингибирующие присущую HSP90 АТФ-азную активность, особенно представляют собой соединения, белки или антитела, которые ингибируют АТФ-азную активность HSP90, например, 17-аллиламино, 17-деметоксигелданамицин (17AAG, 17-DMAG), производное гелданамицина; другие соединения, родственные гельданамицину; радицикол и ингибиторы HDAC; IPI-504, CNF1010, CNF2024, CNF1010 от Conforma Therapeutics; темозоломид, AUY922 от Novartis.
Термин «антипролиферативные антитела», используемый в настоящем описании, включает, но не ограничивается этим, эрбитукс, бевацизумаб, ритуксимаб, PR064553 (анти-CD40) и антитело 2С4. Под антителами подразумеваются, например, интактные моноклональные антитела, поликлональные антитела, мультиспецифические антитела, образованные, по меньшей мере, из 2 интактных антител, и фрагменты антител, до тех пор, пока они проявляют желаемую биологическую активность.
Термин «агенты, связывающие EDG», используемый в настоящем описании, относится к классу иммунодепрессантов, который модулирует рециркуляцию лимфоцитов, например, к FTY720.
Термин «ингибиторы белка веретена кинезина» известен в данной области техники и включает SB715992 или SB743921 от GlaxoSmithKline, пентамидин/хлорпромазина от CombinatoRx.
Термин «ингибиторы MEK» известен в данной области техники и включает ARRY142886 от PioPharma, AZD6244 от AstraZeneca, PD181461 от компании Pfizer, лейковорин.
Термин «ингибиторы рибонуклеотидредуктазы» включает, но не ограничивается этим, нуклеозидные аналоги пиримидинов или пуринов, включая, но, не ограничиваясь этим, флударабин и/или цитозинарабинозид (ara-C), 6-тиогуанин, 5-фторурацил, кладрибин, 6-меркаптопкрин (особенно в сочетании с ara-C против ALL) и/или пентостатин. Ингибиторы рибонуклеотидредуктазы представляют собой в особенности гидроксимочевину или производные 2-гидрокси-1H-изоиндол-1,3-диона, такие как PL-1, PL-2, PL-3, PL-4, PL-5, PL-6, PL-7 или PL-8, описанные Nandy et al., Acta Oncologica, Vol. 33, No. 8, pp. 953-961 (1994).
Термин «ингибиторы S-аденозилметиониндекарбоксилазы», используемый в настоящем описании, включает, но не ограничивается этим, соединения, описанные в патенте США 5461076.
Кроме того, включены, в частности, те соединения, белки или моноклональные антитела к VEGF/VEGFR, раскрытые в патенте WO 98/35958, например, 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин или его фармацевтически приемлемая соль, например, сукцинат, или в патентах WO 00/09495, WO 00/27820, WO 00/59509, WO 98/11223, WO 00/27819 и ЕР 0 769 947; описанные Prewett et al, Cancer Res, Vol. 59, pp. 5209-5218 (1999); Yuan et al., Proc Natl Acad Sci U S A, Vol. 93, pp. 14765-14770 (1996); Zhu et al., Cancer Res, Vol. 58, pp. 3209-3214 (1998); и Mordenti et al., Toxicol Pathol, Vol. 27, No. 1, pp. 14-21 (1999); в патентах WO 00/37502 и WO 94/10202; ангиостатин, описанный OʹReilly et al., Cell, Vol. 79, pp. 315-328 (1994); эндостатин, описанный OʹReilly et al., Cell, Vol. 88, pp. 277-285 (1997); амиды антраниловой кислоты; ZD4190; ZD6474; SU5416; SU6668; бевацизумаб; или антитела против VEGF или антитела против рецептора VEGF, например, rhuMAb и RHUFab, аптамеры VEGF, например, макугон; ингибиторы FLT-4, ингибиторы FLT-3, антитело IgG1 против VEGFR-2, ангиозим (RPI 4610) и бевацизумаб.
Термин «фотодинамическая терапия», используемый в данном описании, относится к терапии, которая использует определенные химические вещества, известные как фотосенсибилизирующие соединения, для лечения или профилактики рака. Примеры фотодинамической терапии включают лечение соединениями, такими как, например, VISUDYNE и порфимер натрия.
Термин «ангиостатические стероиды», используемый в данном описании, относится к соединениям, которые блокируют или ингибируют ангиогенез, таким как, например, анекортав, триамцинолон, гидрокортизон, 11-α-эпигидрокортизол, кортексолон, 17α-гидроксипрогестерон, кортикостерон, дезоксикортикостерон, тестостерон, эстрон и дексаметазон.
«Кортикостероиды» при использовании в настоящем описании включают, но не ограничиваются этим, такие соединения как, например, флуоцинолон, дексаметазон; в частности, в виде имплантатов.
Другие химиотерапевтические соединения включают, но не ограничиваются этим, растительные алкалоиды, гормональные соединения и антагонисты; модификаторы биологического ответа, предпочтительно лимфокины или интерфероны; антисмысловые олигонуклеотиды или производные олигонуклеотидов; shRNA или миРНК; или смешанные соединения или соединения с другим или неизвестным механизмом действия.
Комбинированный продукт в соответствии с изобретением также может быть использован в сочетании или с включением одного или более дополнительных лекарственных средств, выбранных из группы противовоспалительных лекарственных средств; антигистаминных лекарственных средств; бронходилятаторных лекарственных средств, НПВС; антагонистов рецепторов хемокинов.
Подходящие противовоспалительные лекарственные средства включают стероиды, в частности глюкокортикоиды, такие как будесонид, бекламетазона дипропионат, флутиказона пропионат, циклезонида или мометазона фуроат, или стероиды, описанные в патенте WO 02/88167, WO 02/12266, WO 02/100879, WO 02/00679 (особенно стероиды из примеров 3, 11, 14, 17, 19, 26, 34, 37, 39, 51, 60, 67, 72, 73, 90, 99 и 101), WO 03/035668, WO 03/048181, WO 03/062259, WO 03/064445, WO 03/072592, нестероидные агонисты глюкокортикоидного рецептора, такие как соединения, описанные в патенте WO 00/00531, WO 02/10143, WO 03/082280, WO 03/082787, WO 03/104195 и WO 04/005229.
Антагонисты LTB4, такие LY293111, CGS025019C, CP-195543, SC-53228, BIIL 284, ONO 4057, SB 209247 и антагонисты, которые описаны в патенте США 5451700; антагонисты LTD4, такие как монтелукаст и зафирлукаст; ингибиторы PDE4, такие как циломиласт, рофлумистат (Byk Gulden), V-11294A (Napp), BAY19-8004 (Bayer), SCH-351591 (Schering-Plough), арофиллин (Almirall Prodesfarma), PD189659/PD168787 (Parke-Davis), AWD-12-281 (Asta Medica), CDC-801 (Celgene), SelCID (TM) СС-10004 (Celgene), VM554/UM565 (Vernalis), Т-440 (Tanabe), KW-4490 (Kyowa Hakko Kogyo), и ингибиторы, которые раскрыты в патентах WO 92/19594, WO 93/19749, WO 93/19750, WO 93/19751, WO 98/18796, WO 99/16766, WO 01/13953, WO 03/104204, WO 03/104205, WO 03/39544, WO 04/000814, WO 04/000839, WO 04/005258, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/018431, WO 04/018449, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/019944, WO 04/019945, WO 04/045607 и WO 04/037805; агонисты А2а, такие как описанные в патентах ЕР 409595A2, ЕР 1052264, ЕР 1241176, WO 94/17090, WO 96/02543, WO 96/02553, WO 98/28319, WO 99/24449, WO 99/24450, WO 99/24451, WO 99/38877, WO 99/41267, WO 99/67263, WO 99/67264, WO 99/67265, WO 99/67266, WO 00/23457, WO 00/77018, WO 00/78774, WO 01/23399, WO 01/27130, WO 01/27131, WO 01/60835, WO 01/94368, WO 02/00676, WO 02/22630, WO 02/96462, WO 03/086408, WO 04/039762, WO 04/039766, WO 04/045618 и WO 04/046083; антагонисты A2b, такие как соединения, описанные в патенте WO 02/42298; и агонисты бета-2-адренорецепторов, такие как альбутерол (сальбутамол), метапротеренол, тербуталин, салметерол, фенотерол, прокатерол и особенно, формотерол и их фармацевтически приемлемые соли и соединения (в свободной форме или в форме соли или сольвата) формулы I из патента WO 0075114, который включен в настоящее описание в качестве ссылки, предпочтительно соединения из примеров этого патента, особенно соединение формулы
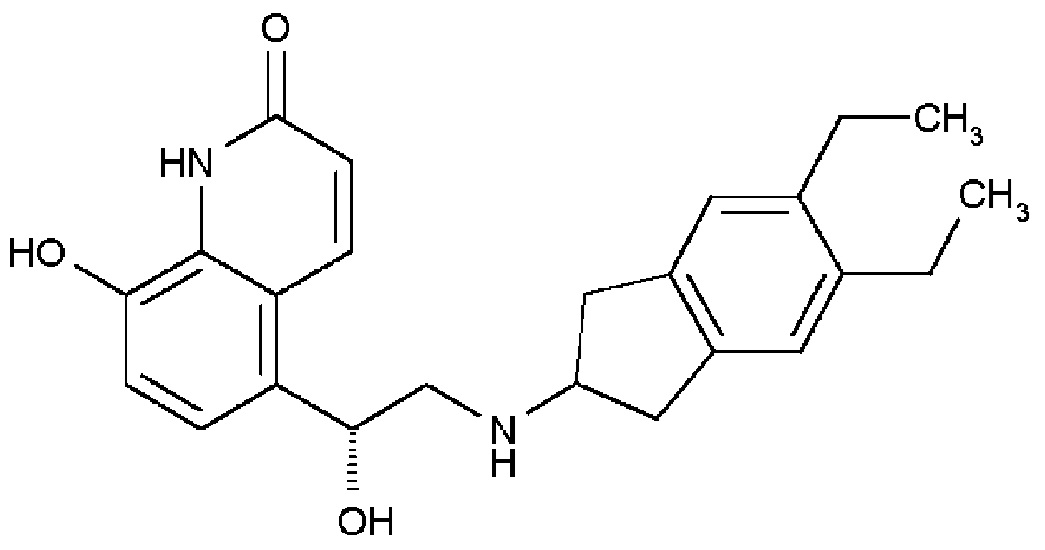
и его фармацевтически приемлемые соли, а также соединения (в свободной форме или в форме соли или сольвата) формулы I из патента WO 04/16601, а также соединения патента WO 04/033412.
Подходящие бронходилятаторные лекарственные средства включают антихолинергические или антимускариновые соединения, в частности бромид ипратропия, бромид окситропия, соли тиотропия и CHF 4226 (Chiesi) и гликопирролат, но также соединения, описанные в патентах WO 01/04118, WO 02/51841, WO 02/53564, WO 03/00840, WO 03/87094, WO 04/05285, WO 02/00652, WO 03/53966, ЕР 424021, US 5171744, US 3714357, WO 03/33495 и WO 04/018422.
Подходящие рецепторы хемокинов включают, например, CCR-1, CCR-2, CCR-3, CCR-4, CCR-5, CCR-6, CCR-7, CCR-8, CCR-9 и CCR10, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, особенно антагонисты CCR-5, такие как антагонисты SC-351125, SCH-55700 и SCH-D от Schering-Plough, антагонисты Takeda, такие как N-[[4-[[[6,7-дигидро-2- (4-метилфенил)-5Н-бензоциклогептен-8-ил]карбонил]амино]фенил]метил]тетрагидро-N,N-диметил-2Н-пиран-4-аминия хлорид (TAK-770), и антагонисты CCR-5, описанные в патентах США 6166037 (в частности, пункты 18 и 19 формулы изобретения), WO 00/66558 (в частности, пункт 8 формулы изобретения), WO 00/66559 (в частности, пункт 9 формулы изобретения), WO 04/018425 и WO 04/026873.
Подходящие антигистаминные лекарственные средства включают гидрохлорид цетиризина, ацетаминофен, клемастина фумарат, прометазин, лоратидин, дезлоратидин, дифенгидрамин и гидрохлорид фексофенадина, активастин, астемизол, азеластин, эбастин, эпинастин, мизоластин и тефенадин, а также соединения, которые раскрыты в патентах WO 03/099807, WO 04/026841 и JP 2004107299.
Структура активных агентов, идентифицированная по номерам кода, генетическим или торговым названиям, может быть взята из современного издания стандартного справочника «The Merck Index» или из баз данных, например, Patents International (например, IMS World Publications). Соответствующее их содержание включено в данное описание в качестве ссылки.
Термин «фармацевтически эффективное» предпочтительно относится к количеству, которое является терапевтически или в более широком смысле также профилактически эффективным против прогрессии заболевания или нарушения, как описано в настоящем документе.
Термин «коммерческая упаковка», используемый в настоящем описании, определяет в частности «набор частей» в том смысле, что компоненты (a) ингибитора тирозинкиназы MET и (b) ингибитора тирозинкиназы EGFR, как определено выше и ниже, и необязательно дополнительные сопутствующие агенты, могут дозироваться независимо друг от друга, или путем использования различных фиксированных сочетаний с различными количествами компонентов (a) и (b), т.е. одновременно или в различные моменты времени. Кроме того, эти термины включают коммерческую упаковку, включающую (особенно объединяющую) в виде активных ингредиентов компоненты (a) и (b), вместе с инструкциями для одновременного, последовательного (хронически в скользящем порядке, в конкретной последовательности по времени, что предпочтительно) или (что менее предпочтительно) раздельного их применения для задержки прогрессии или для лечения пролиферативного заболевания. Части набора частей можно затем, например, вводить одновременно или в хронологически скользящем порядке, то есть в различные моменты времени и с одинаковыми или различными интервалами времени для любой части набора частей. Очень предпочтительно, чтобы интервалы времени выбирались таким образом, чтобы воздействие на заболевание, подвергаемое лечению, при сочетанном применении частей было больше, чем эффект, который был бы получен при использовании только одного из любых компонентов сочетания (a) и (b), (как может быть определено в соответствии со стандартными методами). Отношение общих количеств компонента сочетания (a) к компоненту сочетания (b), предназначенных для введения, в сочетанном препарате, может варьироваться, например, для того, чтобы справиться с потребностями субпопуляции больных, подлежащих лечению, или с потребностями одного больного, причем различные потребности могут возникать из-за конкретного заболевания, возраста, пола, массы тела и т.д. больных. Предпочтительно индуцировать, по меньшей мере, один благоприятный эффект, например, взаимное усиление эффекта сочетания (a) и (b), в частности, более чем аддитивный эффект, который, следовательно, может быть достигнут при более низких дозах каждого из сочетанных лекарств, соответственно, чем переносимая доза в случае лечения только индивидуальными лекарствами без их сочетания, получение дополнительных благоприятных эффектов, например, снижение побочных эффектов, или сочетанный терапевтический эффект в неэффективной дозе одного или обоих участников (компонентов) сочетания (a) и (b), и очень предпочтительно сильный синергизм ингредиентов композиции (a) и (b).
Как в случае использования сочетания компонентов (a) и (b), так и коммерческой упаковки, любое сочетание одновременного, последовательного и раздельного применения также возможно, что означает, что компоненты (a) и (b) можно вводить одновременно в один момент времени, с последующим введением только одного компонента с более низкой токсичностью у хозяина также хронически, например, более 3-4 недель ежедневного приема, в более поздний момент времени, и в дальнейшем с введением другого компонента или сочетания обоих компонентов в еще более поздний момент времени (в последующих курсах лечения сочетанными лекарственными средствами для оптимального эффекта) или тому подобное.
Комбинированные продукты в соответствии с настоящим изобретением являются подходящими для лечения различных заболеваний, которые опосредуются, в частности зависят от активности тирозинкиназы EGFR и/или МЕТ, соответственно. Таким образом, они могут быть использованы при лечении любых заболеваний, которые можно лечить с помощью ингибиторов тирозинкиназы EGFR и ингибиторов тирозинкиназы MET.
Комбинация по настоящему изобретению может быть особенно полезной для лечения рака, где рак представляет собой опухоль, резистентную в отношении EGFR с активацией/амплификацией c-MET. Например, рак может представлять собой немелкоклеточный рак легкого (NSCLC) или метастатический немелкоклеточный рак легкого.
Комбинация по настоящему изобретению может быть особенно пригодной для лечения рака (например, NSCLC), когда рак перестает отвечать на предыдущее лечение, например, соединением А, с эрлотинибом, гефитинибом или афатинибом. Таким образом, рак, подлежащий лечению, как может быть установлено, становится резистентным к лечению терапевтическим агентом, который выбран из группы, состоящей из эрлотиниба, гефитиниба, афатиниба, соединения А или их сочетания.
Ингибиторы EGFR являются полезными, например, при лечении одного или более заболеваний, которые реагируют на ингибирование активности EGFR, особенно неопластического или опухолевого заболевания, особенно солидной опухоли, более конкретно тех видов рака, в развитие которых вовлечены киназы EGFR, включая рак молочной железы, рак желудка, рак легкого, рак предстательной железы, рак мочевого пузыря и рака эндометрия. Другие виды рака включают рак почки, печени, надпочечников, желудка, яичников, толстой кишки, прямой кишки, поджелудочной железы, влагалища или щитовидной железы, саркому, глиобластомы и многочисленные опухоли головы и шеи, а также лейкозы и множественную миелому. Особенно предпочтительны виды рака молочной железы или яичника; рак легкого, например, NSCLC или SCLC; головы и шеи, почек, колоректальный рак, рак поджелудочной железы, мочевого пузыря, желудка или рак предстательной железы; или глиома; в частности, должны быть упомянуты глиома или рак толстой кишки, прямой кишки или колоректальный рак или более конкретно рак легких. Также включаются заболевания, зависящие от лигандов EGFR, таких как EGF; TGF-α; HB-EGF; амфирегулин; эпирегулин; бетацеллюлин.
Ингибиторы MET являются полезными, например, при лечении заболеваний, связанных с МЕТ, особенно видов рака, при которых имеются доказательства одновременной активации MET и FGFR, включая амплификацию генов, активирующие мутации, экспрессию родственных лигандов RTK, фосфорилирование RTKs в остатках, свидетельствующих об активации, например, когда рак выбран из группы, состоящей из рака головного мозга, рака желудка, рака половых органов, мочевыделительной системы, рака предстательной железы, рака мочевого пузыря (мочевыделительной системы) (поверхностно расположенного и инвазивного в мышцы), рака молочной железы, рака шейки матки, рака толстой кишки, колоректального рака, глиомы (включая глиобластому, анапластическую астроцитому, олигоастроцитому, олигодендроглиому), рака пищевода, рака желудка, рака желудочно-кишечного тракта, рака печени, гепатоцеллюлярной карциномы (HCC), включая детскую HCC, рака головы и шеи (включая плоскоклеточную карциному головы и шеи, карциному носоглотки), карциномы клеток Гюртля, эпителиального рака, рака кожи, меланомы (включая злокачественную меланому), мезотелиомы, лимфомы, миеломы (включая множественную миелому), лейкозов, рака легких (включая немелкоклеточный рак легкого (включая все гистологические подтипы: аденокарциному, плоскоклеточный рак, бронхоальвеолярный рак, крупноклеточный рак, и аденосквамозный рак смешанного типа), мелкоклеточный рак легкого), рака яичников, рака поджелудочной железы, рака предстательной железы, рака почки (включая, но, не ограничиваясь этим, папиллярный тип почечно-клеточной карциномы), рака кишечника, почечно-клеточного рака (включая наследственный и спорадический папиллярный тип почечно-клеточного рака типа I и типа II, и светлоклеточный рак почки); сарком, в частности, остеосарком, светлоклеточных сарком и сарком мягких тканей (включая альвеолярные и (например, эмбриональные) рабдомиосаркомы, альвеолярные саркомы мягких тканей); рака щитовидной железы (папиллярного и других подтипов).
Ингибиторы MET также полезны, например, при лечении рака, где рак представляет собой рак желудка, толстой кишки, печени, половых органов, мочевыводящей системы, меланому или рак предстательной железы. В конкретном варианте осуществления рак представляет собой рак печени или пищевода.
Ингибиторы MET также полезны, например, при лечении рака толстой кишки, включая метастазы, например, в печень, а также немелкоклеточного рака легкого.
Ингибиторы MET также могут быть использованы, например, при лечении наследственного папиллярного рака почки (Schmidt, L. et al. Nat. Genet. 16, 68-73, 1997) и других пролиферативных заболеваний, при которых с-МЕТ гиперэкспрессируется или конститутивно активирован в результате мутаций (статья Jeffers and Vande Woude. Oncogene 18, 5120-5125, 1999; и цитируемые в ней ссылки) или хромосомных перестроек (например, TPR-MET; Cooper et al. Nature 311, 29-33, 1984; Park. et al. Cell 45, 895-904, 1986).
Ингибиторы MET дополнительно могут быть использованы, например, при лечении дополнительных видов рака и состояний, как это предусмотрено в данном описании или известно в данной области техники.
Ингибиторы MET также пригодны, например, для лечения одного или более воспалительных состояний.
В еще одном варианте осуществления изобретения воспалительное состояние обусловлено инфекцией. В одном варианте осуществления способ лечения должен заключаться в блокировании инфицирования патогеном. В конкретном варианте осуществления инфекция представляет собой бактериальную инфекцию, например, инфицирование Listeria. Смотри, например, Shen et al. Cell 103: 501-10, (2000), в результате чего бактериальный белок поверхности активирует киназу c-Met путем связывания с внеклеточным доменом рецептора, тем самым имитируя эффект родственного лиганда HGF/SF.
Сочетанный продукт по настоящему изобретению особенно подходит для лечения любого из видов рака, упомянутых выше, которые поддаются лечению ингибитором EGFR или Met, особенно видов рака, выбранных из аденокарциномы (особенно молочной железы или в первую очередь особенно легких), рабдомиосаркомы, остеосаркомы, рака мочевого пузыря, колоректального рака и глиомы.
Термин «терапевтически эффективное количество» соединения по настоящему изобретению относится к количеству соединения по настоящему изобретению, которое будет вызывать биологический или медицинский ответ у индивидуума, например, снижение или ингибирование активности фермента или белка, или ослаблять симптомы, облегчать состояние, замедлять или задерживать прогрессию заболевания, или предотвращать заболевание и т.д. В одном неограничивающем варианте осуществления изобретения термин «терапевтически эффективное количество» относится к количеству соединения по настоящему изобретению, которое при введении индивидууму, эффективно в отношении (1), по меньшей мере, частичного смягчения, ингибирования, предупреждения и/или облегчения состояния, или нарушения, или заболевания, (i) опосредованного активностью cMet (МЕТ) и/или опосредованного активностью EGFR, или (ii) характеризуемого активностью (нормальной или аномальной) cMet и/или EGFR; или (2) снижения или ингибирования активности cMet и/или EGFR; или (3) уменьшения или ингибирования экспрессии cMet и/или EGFR. В другом неограничивающем варианте осуществления изобретения термин «терапевтически эффективное количество» относится к количеству соединения по настоящему изобретению, которое при введении в клетку или ткань, или в бесклеточный биологический материал или в среду, эффективно в отношении, по меньшей мере, частичного снижения или ингибирования активности cMet и/или EGFR; или, по меньшей мере, частичного снижения или ингибирования экспрессии MET и/или EGFR.
Используемый в данном описании термин «индивидуум» относится к животному. Как правило, животное является млекопитающим. Индивидуум также относится, например, к приматам (например, к людям), коровам, овцам, козам, лошадям, собакам, кошкам, кроликам, крысам, мышам, рыбам, птицам и тому подобному. В некоторых вариантах осуществления индивидуумом является примат. В других вариантах осуществления индивидуумом является человек.
«И/или» означает, что каждый или оба, или все компоненты или функции списка представляют собой возможные варианты, особенно два или более из них альтернативно или в совокупности.
Используемый в данном описании термин «ингибировать», «ингибирование» или «ингибирующий» относится к снижению или подавлению данного состояния, симптома или нарушения, или заболевания, или к существенному снижению базальной активности биологической реакции или процесса.
Используемый в данном описании термин «лечить», «проводить лечение» или «лечение» любого заболевания или нарушения относится в одном из вариантов осуществления к облегчению заболевания или нарушения (т.е. к замедлению или прекращению, или ослаблению развития заболевания или, по меньшей мере, одного из его клинических симптомов). В другом варианте осуществления изобретения «лечить», «проводить лечение» или «лечение» относится к смягчению или облегчению, по меньшей мере, одного физического показателя, включая показатели, которые могут не ощущаться больным. В еще одном варианте осуществления «лечить», «проводить лечение» или «лечение» относится к модуляции заболевания или нарушения, либо физической (например, стабилизации ощутимого симптома), физиологической (например, стабилизации физического показателя), либо и к тому, и к другому. В еще одном варианте осуществления «лечить», «проводить лечение» или «лечение» относится к профилактике или задержке начала или развития или прогрессии заболевания или нарушения.
Термин «лечение» включает, например, профилактическое или особенно терапевтическое введение сочетанных компонентов теплокровному животному, предпочтительно человеку, нуждающемуся в таком лечении, с целью излечения заболевания или действия на регрессию заболевания или на замедление прогрессии заболевания.
Используемый в настоящем описании термин индивидуум, «нуждающийся» в лечении, применяется, если такой индивидуум получит выгоду с биологической, с медицинской точки зрения или в отношении качества жизни от такого лечения.
Используемый в данном описании термин «a», «an» и «the» и аналогичные термины, используемые в контексте настоящего изобретения (особенно в контексте формулы изобретения), должны толковаться как охватывающие как единственное, так и множественное число, если в настоящем документе не указано иначе или явно не противоречит контексту.
Комбинации в соответствии с изобретением могут быть получены способом, известным в чистом виде, и способами, которые пригодны для энтерального, такого как пероральное или ректальное, и парентерального введения млекопитающим (теплокровным животным), включая человека, включающие терапевтически эффективное количество, по меньшей мере, одного фармакологически активного компонента сочетания в отдельности или в сочетании с одним или более фармацевтически приемлемыми носителями, особенно подходящими для энтерального или парентерального применения. В одном из вариантов осуществления настоящего изобретения один или более активных ингредиентов вводят перорально.
Используемый в данном описании термин «носитель» или «фармацевтически приемлемый носитель» включает любые и все растворители, дисперсионные среды, покрытия, поверхностно-активные вещества, антиоксиданты, консерванты (например, антибактериальные агенты, противогрибковые агенты), изотонические агенты, замедляющие абсорбцию агенты, соли, консерванты, лекарственные средства, стабилизаторы лекарств, связующие вещества, наполнители, разрыхлители, смазывающие агенты, подсластители, ароматизаторы, красители и тому подобное, и их сочетания, как должно быть известно специалистам в данной области техники (смотри, например, Remington's Pharmaceutical Sciences, 18th Ed. Mack Printing Company, 1990, pp. 1289-1329). За исключением случаев, когда любой обычный носитель является несовместимым с активным ингредиентом, охватывается их использование в терапевтических или фармацевтических композициях.
Фармацевтический комбинирвоанный продукт в соответствии с изобретением (как фиксированное сочетание или в виде набора, например, в виде сочетания фиксированного сочетания и индивидуальных составов для одного или обоих компонентов сочетания или в виде набора индивидуальных составов компонентов сочетания) включает сочетание компонентов (по меньшей мере, одного ингибитора тирозинкиназы МЕТ, по меньшей мере, одного ингибитора тирозинкиназы EGFR и необязательно одного или более дополнительных сопутствующих агентов) по настоящему изобретению и один или более фармацевтически приемлемые материалы носителей (носителей, наполнителей). Комбинированные продукты или компоненты сочетания, составляющие их, могут быть составлены для конкретных путей введения, таких как пероральное введение, парентеральное введение, ректальное введение и т.д. Кроме того, сочетанные продукты по настоящему изобретению могут быть составлены в твердой форме (включая без ограничения капсулы, таблетки, пилюли, гранулы, порошки или суппозитории), или в жидкой форме (включая без ограничения растворы, суспензии или эмульсии). Комбинированные продукты и/или компоненты их сочетания могут быть подвергнуты обычным фармацевтическим методам обработки, таким как стерилизация, и/или могут содержать обычные инертные разбавители, смазывающие агенты, или буферирующие агенты, а также адъюванты, такие как консерванты, стабилизаторы, смачивающие агенты, эмульгаторы и буферы и т.д.
В одном варианте осуществления фармацевтические композиции представляют собой таблетки или желатиновые капсулы, включающие активный ингредиент совместно с одним или более широко известными носителями, например, с одним или более носителями, выбранными из группы, состоящей из
a) разбавителей, например, лактозы, декстрозы, сахарозы, маннита, сорбита, целлюлозы и/или глицина;
b) смазывающих агентов, например, диоксида кремния, талька, стеариновой кислоты, ее магниевой или кальциевой соли и/или полиэтиленгликоля; для таблеток также
с) связующих агентов, например, алюмосиликата магния, крахмального клейстера, желатина, трагаканта, метилцеллюлозы, натриевой соли карбоксиметилцеллюлозы и/или поливинилпирролидона; и при необходимости
d) дезинтегрирующих агентов, например, крахмалов, агара, альгиновой кислоты или ее натриевой соли, или шипучих смесей; и
e) абсорбентов, красителей, ароматизаторов и подсластителей.
Таблетки могут быть либо покрыты пленкой, либо покрыты оболочкой для всасывания в кишечнике в соответствии со способами, известными в данной области техники.
Подходящие композиции для перорального введения в особенности включают эффективное количество одного или более, или в случае составов с фиксированным сочетанием каждого из компонентов сочетания (активных ингредиентов) в виде таблеток, лепешек, водных или масляных суспензий, дисперсных порошков или гранул, эмульсии, твердых или мягких капсул, сиропов или эликсиров. Композиции, предназначенные для перорального применения, получают в соответствии с любым способом, известным в данной области техники для получения фармацевтических композиций, и такие композиции могут содержать один или более агентов, выбранных из группы, состоящей из подсластителей, отдушек, красителей и консервантов для того, чтобы обеспечить фармацевтически первоклассные и приятные на вкус препараты. Таблетки могут содержать активный ингредиент(ы) в смеси с нетоксичными фармацевтически приемлемыми наполнителями, которые пригодны для изготовления таблеток. Эти наполнители представляют собой, например, инертные разбавители, такие как карбонат кальция, карбонат натрия, лактозу, фосфат кальция или фосфат натрия; гранулирующие и дезинтегрирующие агенты, например, кукурузный крахмал или альгиновую кислоту; связующие агенты, например, крахмал, желатин или гуммиарабик; и смазывающие агенты, например стеарат магния, стеариновую кислоту или тальк. Таблетки не покрывают или покрывают с помощью известных методов с целью замедлить дезинтеграцию и абсорбцию в желудочно-кишечном тракте и тем самым обеспечить пролонгированное действие в течение более длительного периода. Например, может быть использовано вещество для замедления, такое как глицерилмоностеарат или глицерилдистеарат. Композиции для перорального применения могут быть представлены в виде твердых желатиновых капсул, в которых активный ингредиент смешан с инертным твердым разбавителем, например, карбонатом кальция, фосфатом кальция или каолином, или в виде мягких желатиновых капсул, в которых активный ингредиент смешан с водной или масляной средой, например, с арахисовым маслом, жидким парафином или оливковым маслом.
Некоторые композиции для инъекций (особенно пригодные, например, когда в качестве ингибиторов EGFR используются антитела) представляют собой водные изотонические растворы или суспензии, а суппозитории преимущественно получают из жирных эмульсий или суспензий. Указанные композиции могут быть стерилизованы и/или содержать адъюванты, такие как консерванты, стабилизаторы, смачивающие или эмульгирующие агенты, стимуляторы растворения, соли для регуляции осмотического давления и/или буферы. Кроме того, они могут также содержать другие терапевтически ценные вещества. Указанные композиции получают в соответствии с обычными способами смешивания, гранулирования или покрытия, соответственно, и они содержат приблизительно 0,1-75%, или содержат приблизительно 1-50% активного ингредиента.
Подходящие композиции для чрескожного применения включают эффективное количество одного или более активных ингредиентов с подходящим носителем. Носители, пригодные для чрескожной доставки, включают абсорбируемые фармакологически приемлемые растворители, способствующие проникновению через кожу хозяина. Например, средства для чрескожного введения находятся в виде бандажа, включающего поддерживающий слой, резервуар, содержащий соединение необязательно с носителями, необязательно контролирующий скорость барьер для доставки соединения в кожу хозяина с контролируемой и предварительно определенной скоростью в течение продолжительного периода времени, и средство для крепления устройства к коже.
Подходящие композиции для местного применения, например, на кожу и в глаза, включают водные растворы, суспензии, мази, кремы, гели или распыляемые составы, например, для доставки с помощью аэрозоля, или тому подобное. Такие местные системы доставки должны, в частности, подходить для кожного применения, например, для лечения рака кожи, например, для профилактического применения в солнцезащитных кремах, лосьонах, спреях и тому подобном. Таким образом, они особенно подходят для использования в местных составах, включая косметические, хорошо известных в данной области техники. Они могут содержать солюбилизаторы, стабилизаторы, повышающие тоничность агенты, буферы и консерванты.
Используемое в данном описании местное применение может также относиться к ингаляционному или к интраназальному применению. Они могут быть легко доставлены в форме сухого порошка (либо по отдельности в виде смеси, например, сухой смеси с лактозой, либо в виде частицы смешанных компонентов, например, с фосфолипидами) из ингалятора сухого порошка или при подаче аэрозольного спрея из контейнера с избыточным давлением, насоса, спрея, пульверизатора или небулайзера с использованием или без использования подходящего пропеллента.
Изобретение относится также к набору частей или фиксированной фармацевтической композиции, включающей эффективное количество, особенно количество, эффективное для лечения одного из указанных выше заболеваний, по меньшей мере, одного ингибитора тирозинкиназы Met, по меньшей мере, одного ингибитора тирозинкиназы EGFR или его фармацевтически приемлемой соли, соответственно, и необязательно, по меньшей мере, одного дополнительного сопутствующего агента или его фармацевтически приемлемой соли вместе с одним или несколькими фармацевтически приемлемыми носителями, которые пригодны для местного, энтерального, например, перорального или ректального, или парентерального введения и которые могут быть неорганическими или органическими, твердыми или жидкими.
Во всех составах, активный ингредиент(ы), образующий часть сочетанного продукта в соответствии с настоящим изобретением, каждый может присутствовать в относительном количестве от 0,5 до 95% от массы соответствующего состава (относительно состава как такового, то есть без упаковки и вкладыша), например, от 1 до 90, от 5 до 95, от 10 до 98 или от 10 до 60, или от 40 до 80% по массе, соответственно.
Дозировка активного ингредиента, которую следует применять у теплокровного животного, зависит от множества факторов, включая тип, вид, возраст, вес, пол и медицинское состояние больного; тяжесть состояния, подлежащего лечению; путь введения; функцию почек и печени больного; и конкретное используемое соединение. Врач, клиницист или ветеринар обычной квалификации может легко определить и прописать эффективное количество лекарственного средства, необходимое для предупреждения, противостояния или прекращения прогрессии состояния. Оптимальная точность в достижении концентрации лекарственного средства в диапазоне, который обеспечивает эффективность без токсичности, требует режима, основанного на кинетике доступности лекарственного средства для сайтов-мишеней. Это включает рассмотрение распределения, равновесия и элиминации лекарственного средства. Доза каждого из компонентов сочетания или его фармацевтически приемлемой соли для введения теплокровным животным, например, людям с массой тела приблизительно 70 кг, предпочтительно составляет от приблизительно 3 мг до приблизительно 5 г, более предпочтительно от приблизительно 10 мг до приблизительно 1,5 г на человека в день, например, разделенная предпочтительно на от 1 до 3 разовых доз, например, для использования один или два раза в день, которая может быть, например, одинакового размера. Как правило, дети получают половину взрослой дозы.
Фармацевтический сочетанный продукт по настоящему изобретению может находиться, например, в единице дозированной лекарственной формы приблизительно 1-1000 мг активного ингредиента(ов) для индивидуума массой приблизительно 50-70 кг, или приблизительно 1-500 мг, или приблизительно 1-250 мг, или приблизительно 1-150 мг, или приблизительно 0,5-100 мг, или приблизительно 1-50 мг для любого одного или, в частности, суммарных активных ингредиентов; или (особенно для ингибитора EGFR) от 50 до 900, от 60 до 850, от 75 до 800 или от 100 до 600 мг, соответственно, для любого одного или, в частности, суммарных активных ингредиентов. Терапевтически эффективная дозировка соединения, фармацевтической композиции или их сочетания, зависит от вида индивидуума, массы тела, возраста и индивидуального состояния, нарушения или заболевания, подлежащего лечению, или их тяжести. Врач, клиницист или ветеринар (при использовании животных) обычной квалификации может легко определить эффективное количество каждого из активных ингредиентов, необходимых для профилактики, лечения или ингибирования прогрессии нарушения или заболевания.
Конкретные варианты осуществления изобретения, которые включены в настоящее описание в качестве ссылки, приведены также в формуле изобретения, а также в примерах.
ПРИМЕРЫ:
В последующих примерах иллюстрируется раскрытие, и предлагаются конкретные варианты осуществления, однако, без ограничения объема изобретения.
Пример 1. Данные клеточных культур
Реагенты:
INC280 (НВП-INC280) и соединение А растворяли в ДМСО в концентрации 10 мМ и хранили в аликвотах при -20°C.
Культура клеток:
HCC827 получали из АТСС. HCC827 GR5 (устойчивую к гефитинибу) получали от Jeff Engleman lab в Massachusetts General Hospital. Оба типа клеток культивировали в RPMI-1640 (АТСС, #30-2001) с добавлением 10% FBS (Thermo Scientific, # SH30071.03) и поддерживали при 37°С, в 5% СO2-инкубаторе. Клетки пересевали два раза в неделю, используя TrypLE™ Express (Invitrogen, #12604-013), свободный рекомбинантный фермент животного происхождения использовали для диссоциации прикрепленных клеток млекопитающих вместо обычного трипсина.
Анализ клеточной пролиферации:
Жизнеспособность клеток определяли путем измерения содержания клеточного АТФ с использованием люминесцентного анализа жизнеспособности клеток CellTiter-Glo® (CTG) (Promega #G7573) в соответствии с протоколом производителя. Вкратце, клетки (3100 для обеих HCC827 и HCC827 GR5) высевали в 80 мкл ростовой среды на лунку в 96-луночные черные планшеты с прозрачным дном (Costar, #3904) в трех повторностях. Клеткам позволяли закрепляться в течение ночи перед 72-часовой обработкой указанными соединениями (серийно разведенными, где это применимо) для эксперимента с сочетаниями Chalice (+20 мкл соединения А +20 мкл соединения В). В конце обработки лекарствами в каждую лунку добавляли 100 мкл реагента CTG для лизиса клеток, и люминесцентные сигналы регистрировали в планшетном ридере Envision (Perkin Elmer).
Метод расчета влияния сочетаний:
Для того, чтобы оценить влияние сочетаний непредвзятым образом и идентифицировать синергичный эффект при всех возможных концентрациях, исследования сочетаний проводили с «матрицей доз», где сочетание тестировали при всех возможных комбинациях серийно разведенных соединений. Во всех комбинационных анализах соединения вносили одновременно. Эта «матрица доз», используемая в данном исследовании, заключалась в следующем: соединение А подвергали серийному разведению 7 доз 3× с самой высокой дозой 3 мкМ и самой низкой дозой приблизительно 1,37 нМ. Соединение INC280 подвергали серийному разведению 7 доз 3× с самой высокой дозой 1,5 мкМ и самой низкой дозой приблизительно 686 пкМ. Синергичное взаимодействие анализировали с использованием программного обеспечения Chalice (CombinatoRx, Cambridge MA). Синергию рассчитывали путем сравнения ответа сочетания относительно ответа его отдельных агентов на предмет соответствия с референсной моделью добавления собственной дозы лекарства. Отклонения от добавлений дозы могут быть оценены численно с помощью количественного определения комбинационного индекса общей силы эффектов сочетания, который по существу представляет собой показатель уровня VHSA=ΣX,YlnfXlnfY(Idata-IHSA), и он также рассчитывается между данными и самым высоким уровнем действия одиночного агента, нормализованным на коэффициенты разбавления одиночного агента fX,fY (Lehar et al, 2009).
Результаты:
На фигурах 1-4 продемонстрированы результаты действия сочетания. Соединение А и соединение INC280 благоприятно действуют друг на друга в резистентной к гефитинибу линии HCC-827 (амплификация cMet), в то время как родительская линия отвечает только на соединение A (без сочетанного эффекта).
Пример 2. In vivo исследование сочетания с использованием соединения А и соединения INC280 в модели ксенотрансплантата HCC827 NSCLC человека, устойчивого к эрлотинибу и соединению A, несущего активирующую мутацию EGFR Ex19Del
Список сокращений
|
Противоопухолевую активность in vivo соединения А в сочетании с соединением INC280 исследовали с использованием ксенотрансплантата HCC827 клеточной линии немелкоклеточного рака легкого (NSCLC) человека, устойчивого к соединению А, подкожно имплантированного бежевым мышам SCID. NCI-HCC827 несет активирующую и онкогенную мутацию Ex19Del EGFR. Соединение INC280 представляет собой перорально биодоступный, селективный ингибитор рецепторной тирозинкиназы c-MET.
Как подробно показано ниже, соединение А в сочетании с соединением INC280 обладало значительной противоопухолевой активностью у бежевых мышей SCID, несущих опухоль HCC827 NSCLC, устойчивую к соединению A. Ежедневное пероральное введение 30 мг/кг соединения А в сочетании с двукратными ежедневными пероральными дозами 10 мг/кг соединения INC280 в течение курса лечения приводило к значительной регрессии опухолей по сравнению с контрольным носителем (р<0,0001). Уровни регрессии опухолей, достигнутые при сочетанном лечении, были значительно лучше, чем при монотерапии либо только соединением INC280, либо только соединением А (р<0,0001). Кроме того, соединение А в одиночку хорошо переносилось с небольшой потерей массы тела или без существенной потери массы тела в тестируемой дозе. Соединение INC280 при монотерапии по схеме два раза в день в этом эксперименте не вводили на 7, 8 день, тогда как в группе сочетанной терапии его не вводили на 9, 10 и 11 день. Соединение А при дозировании в сочетании с соединением INC280 вызывало значительную регрессию опухолей в случае устойчивости EGFR с активацией/амплификацией c-MET.
Методы
Тестируемые соединения:
Соединение А (в форме соли HCl)
Эрлотиниб (используется для состояния резистентности), и
INC280 (в форме дигидрохлоридной соли)
Состав:
Соединение А (в форме HCl) в дозе 30 мг/кг в 0,5% МС (метилцеллюлозе), 0,5% твине-80, суспензия.
Эрлотиниб в дозе 30-100 мг/кг в 90% воде, 10% этаноле/кремофоре (1:1), суспензия.
INC280-АА-3 (в форме дигидрохлоридной соли) в дозе 10 мг/кг в 0,25% MC (метилцеллюлозе), 0,05% твине 80 в воде, мелкодисперсная суспензия.
Материалы:
Голых мышей женского пола Harlan Foxnl и бежевых мышей SCID, (возраст 6-8 недель) использовали в качестве экспериментальных животных. Линию клеток NCI-HCC827 приобретали у АТСС (American Type Culture Collection, Manassas, VA). Эрлотиниб (соль HCl) приобретали у LC Laboratories (Woburn, MA) Cat # E-4007, лот BBE-106. Нейтральный забуференный формалин, раствор Ponceau S #P7170, BSA, TBST, коктейль ингибиторов фосфатазы I и II приобретали у Sigma-Aldrich. Первичное антитело против фосфо-рецептора EGF (Tyr1173) (53A5) (кроличье, 1:1000, Cat # 4407, против общего EGFR (кроличье, 1:1000, Cat # 2232) фосфо-Akt (Ser473) (193H12), (кроличье, 1:1000, Cat # 4058) и против общей Akt, кроличье, 1:1000, Cat # 9272, фосфо-р44/42 МАРК (ERK1/2) (Thr202/Tyr204) (197G2), кроличье, 1:1000 Cat # 4377, против общей р44/42 МАРК (ERK1/2), кроличье, 1:1000, Cat # 9102, фосфо-МЕТ (Tyr1234/1235) (кроличье-XP mAb, 1:1000, Cell Signaling, Cat # 3077) и против общей MET (кроличье, 1:1000, Cell Signaling, Cat # 4560) приобретали у Cell Signaling Technology (Danvers, MA). Контрольное антитело - изотип IgG кролика приобретали у Jackson ImmunoResearch (West Grove, PA.). Хемилюминесцентный субстрат Super Signal West Pico приобретали у Thermo Scientific, Cat # 34087. Таблетки полных ингибиторов протеаз 3× приобретали у Roche (Кат. # 04693159001). RTK-блот приобретали у R&D Systems, матрицу протеомного профиля антител - у Human Phospho-Kinase Array cat. ARY003B и Human Phospho-RTK Array Kit cat. ARY001B.
Для всех экспериментов животных содержали при 12 час циклах дня и ночи, и они имели свободный доступ к пище и воде.
Все процедуры, связанные с животными, проводили в соответствии с протоколом, утвержденным GNF IACUC (P11-308-DD) в соответствии с правилами закона о защите животных и руководством по уходу и использованию лабораторных животных.
Создание опухолевой модели NCI-HCC827, резистентной к эрлотинибу/соединению А
Эта опухолевая линия первоначально была создана путем имплантации клеток, и затем последовательных пассажей (3 пассажа) опухолевой ткани бежевым мышам SCID для создания стабильной опухолевой линии. Эта стабильная опухолевая линия была использована для создания опухолевой линии, резистентной к эрлотинибу/соединению А, как описано ниже, фигуры 5 и 7.
Анализ фосфо-RTK показан для опухолевых лизатов исходной линии HCC827 и животного 8 (фигура 6). В исходной линии HCC827 выявлена позитивная регуляция pEGFR при негативной регуляции pMet. Блот RTK линии HCC827, резистентной к эрлотинибу, выявил небольшую негативную регуляцию pEGFR при позитивной регуляции pMet по сравнению с исходной линией HCC827.
Резистентная к эрлотинибу/соединению A опухолевая биомасса с амплификацией cMet
Биомассу опухолей доноров получали из исследования 11-308-29 от мыши # 8 для устойчивости к эрлотинибу и мышей # 10, # 12 для устойчивости к соединению A для исследования 11308-138. В исследовании 11-308-29 интактные опухоли обрабатывали дозами эрлотиниба, начиная с 30 мг/кг в течение 75 дней, дозу увеличивали до 100 мг/кг на 76 день и продолжали вводить в течение 32 дней. Соединение А в дозе 10 мг/кг вводили в течение двух недель подряд и с перерывом во введении лекарства с 14 по 30 день. Введение соединения А в дозе 10 мг/кг возобновляли с 30 дня до 60 дня. Дозу соединения А увеличивали до 20 мг/кг на 60-85 день, и дозу снова увеличивали до 50 мг/кг в день с 85 дня до 106 дня. Когда опухоли достигали 1700 мм3, их собирали. Для имплантации ткани мышей анестезировали непрерывным потоком 2-4% смеси изофлурана/кислорода с использованием портативной камеры индукции анестезии (Vetequip Inc., Pleasanton, CA), 2-3 участка ткани опухоли имплантировали подкожно 40 бежевым мышам SCID с матригелем (пассаж 2) для исследования 11-308-138 и, как описано на фигурах 5 и 7.
Блот RTK на фигуре 8 демонстрирует опухолевые лизаты из исследования 11-308-29 животных 10, 12 (животное # 10 исследования 11-308-29 является донорским источником для исследования 11-308-138), pEGFR регулировался слегка негативно, а pMET регулировался позитивно по сравнению с исходной линией HCC827, как показано ранее в разделе резистентности к эрлотинибу. Сходно с опухолями HCC827, резистентными к эрлотинибу, pEGFR регулировался слегка негативно, а pMET регулировался позитивно в опухоли HCC827, резистентной к соединению А, по сравнению с исходной линией HCC827.
Вестерн-блоттинг ранней PD с использованием эрлотиниба, соединения А и соединения INC280 в качестве монотерапии или в сочетании в резистентных опухолях NCI-HCC827
Бежевых мышей SCID, несущих резистентные к эрлотинибу опухоли (2-5 животных), n=1 на группу, в общей сложности 4 группы, рандомизировали через 50 дней после имплантации фрагментов опухоли со средним объемом опухоли 1236,18 мм3 и SD 316,57 мм3. (Животных 6-16) с резистентными к соединению А опухолями HCC827 рандомизировали на 4 группы (n=3 мыши на группу) через 24 дня после имплантации фрагментов опухоли со средним объемом опухоли 963,24 мм3 с SD 179,56 мм3. Животные в каждой группе получали один раз в день пероральное введение соединения А в дозе 30 мг/кг или два раза в день соединение INC280-AA-3 в дозе 10 мг/кг, отдельно или в сочетании.
Фармакодинамические измерения
Оценку направленного ингибирования pEGFR и pMET проводили с помощью анализа вестерн-блоттингом. 40 мкг белков опухолевых лизатов на пробу подвергали электрофорезу с использованием бис-Трис гелей 4-12% Criterion (Bio-Rad, Cat # 345-0124). После завершения переноса белков мембраны инкубировали с 5% BSA (Sigma) в TBST (25 мМ Трис, 150 мМ NaCl, 0,1% Tween-20) в течение 1 час при комнатной температуре для блокирования неспецифического связывания. Мембраны затем инкубировали с первичными антителами против фосфорилированного EGFR, разведенными в 5% BSA-TBST (EGFR, Y1 173) (кроличьи, 1:1000, Cell Signaling, Cat # 4407, Danvers, MA) и против общего EGFR (кроличьи, 1:1000, Cell Signaling, Cat # 2232); против фосфорилированного Met (Y1234/1235), (кроличьи-XP mAb, 1:1000, Cell Signaling, Cat # 3077) и против общего Met (кроличьи, 1:1000, Cell Signaling Cat # 4560) в течение ночи при 4°С на платформенной качалке-шейкере. После промывания 3 раза в TBST, каждое в течение 10 минут, мембраны инкубировали с вторичным антителом, конъюгированным с пероксидазой хрена, против Ig кролика (1:2000, Cell Signaling, Cat # 7074) в 5% BSA-TBST в течение 1 час при комнатной температуре. Мембраны затем промывали 5 раз в TBST, каждое промывание в течение 5 минут, и инкубировали с хемилюминесцентным субстратом Super Signal West Pico (Thermo Scientific Cat # 34087) в течение 2 минут при комнатной температуре. Хемилюминесцентные сигналы определяли при экспозиции пленки от 20 сек до 2 мин (пленка Thermo CL-Xposure Cat # 34091).
Исследование эффективности в мышиной модели ксенотрансплантата HCC827, резистентного к соединению A (GNF-11-308-138)
Бежевых мышей SCID женского пола, несущих резистентные к эрлотинибу опухоли HCC827, рандомизировали на 4 группы (n=6 мышей на группу) через 6 дней после имплантации опухолевых клеток со средним диапазоном объема опухолей 89,30-386,24 мм3 (таблица 1). Соединение А-АА-14 в составе суспензии разводили 0,5% MC, 0,5% твином 80. Готовили раствор INC280-AA-3 в 0,25% MC (метилцеллюлозы) 0,05% твине 80 в воде. Животные в каждой группе получили носитель, соединение А-АА-14 в дозе 30 мг/кг перорально один раз в день и соединение INC280-АА-3 в дозе 10 мг/кг перорально два раза в день при объеме дозирования 5 мл/кг массы тела животного в течение курса лечения. Животных взвешивали в дни получения доз, и дозы корректировали на массу тела. Объемы опухолей измеряли с помощью цифрового штангенциркуля 3 раза в неделю, и массу тела всех животных регистрировали в течение всего исследования.
Анализ данных
Измерение опухолей и массы тела:
Массу тела контролировали ежедневно и % изменения массы тела рассчитывали как (BWтекущая-BWначальная)×100. Данные представляли в виде процента изменения массы тела со дня начала лечения.
Размеры опухолей оценивали три раза в неделю, как только опухоли становились пальпируемыми. Размеры опухолей определяли с помощью измерения штангенциркулем. Объемы опухолей рассчитывали по следующей формуле: (длина × ширина × ширина)/2.
Процент величин лечение/контроль (Т/С) для опухоли рассчитывали по следующей формуле:
%T/C=100×ΔT/ΔC, если ΔT>0
% регрессии=100×ΔΤ/Tисходный, если ΔT<0
где:
Т=средний объем опухоли в группе, получавшей лекарство, в последний день исследования;
ΔΤ=средний объем опухоли в группе, получавшей лекарство, в последний день исследования - средний объем опухоли в группе, получавшей лекарство, в исходный день начала дозирования;
Tисходный=средний объем опухоли в группе, получавшей лекарство, в исходный день начала дозирования;
C=средний объем опухоли в контрольной группе в последний день исследования; и
ΔC=средний объем опухоли в контрольной группе в последний день исследования - средний объем опухоли в контрольной группе в исходный день начала дозирования.
Все данные выражали в виде среднего±стандартная ошибка среднего (SEM). Дельту объема опухоли и массы тела использовали для статистического анализа. Межгрупповые сравнения проводили с использованием одностороннего критерия ANOVA с последующим апостериорным критерием Тьюки или критерием Данна. Для всех статистических оценок уровень значимости устанавливали на уровне р<0,05. Представлена значимость по отношению к контрольной группе, если не указано иное.
Результаты
Противоопухолевую активность и переносимость соединения А и соединения INC280 исследовали в модели ксенотрансплантата HCC827 мыши, резистентного к EGFRi. Опухолевые модели, резистентные как к эрлотинибу, так и к соединению А, создавали своими силами. С помощью вестерн-блоттинга и анализа pRTK получено подтверждение того, что эти опухоли имели амплификацию/активацию c-MET. Оценка фармакодинамики (PD) однократной дозы соединения А, соединения INC280 в виде монотерапии или в виде сочетания предполагает, что сочетание является наиболее эффективным в ингибировании фосфорилирования как EGFR, так и cMET. Носитель и соединение А в дозе 30 мг/кг вводили перорально один раз в день и соединение INC280 в дозе 10 мг/кг вводили перорально дважды в день через пероральный зонд в течение 14 дней. Однако из-за снижения массы тела, происходящей при получении соединения INC280 по схеме два раза в день, делали перерыв в приеме лекарства на 7 и 8 день при монотерапии и на 9, 10 и 11 дни в группе сочетанной терапии при исследовании. Сочетание соединения А и соединения INC280 приводило к регрессии опухолей in vivo в отличие от каждого агента по отдельности.
Фосфорилирование EGFR и cMET выявлено при использовании опухолевых лизатов из исходной HCC827 и наблюдается в любой из опухолей, резистентных к эрлотинибу/соединению А (фигура 3-1), эрлотиниб в дозе 100 мг/кг, соединение А в дозе 30 мг/кг и соединение INC280 в дозе 10 мг/кг, все дозировались на эффективном уровне, опухоли выделяли через 6 часов после введения дозы.
Эффективность соединения А относительно ксенотрансплантата HCC827 мыши:
Как показано на фигуре 10, носитель или соединение А в дозе 30 мг/кг вводили перорально один раз в день, и соединение INC280 в дозе 10 мг/кг вводили перорально два раза в день. Соединение А также оценивали в сочетании с соединением INC280. На фигуре показано, что действие только соединения А значимо не отличалось от носителя (р>0,05) с T/C, равным 64%. Действие только соединения А значимо отличалось (р<0,001) с T/C, равным 23%. Действие соединения А в сочетании с соединением INC280 значимо отличалось от носителя (р<0,0001) и индуцировало статистически значимую регрессию опухоли (Т/С равно -86%). Кроме того, сочетание соединения А и соединения INC280 действовало значительно лучше, чем каждый из двух отдельных агентов, соединение А или соединение INC280 по отдельности (р<0,0001). Подробные измерения объемов опухолей и изменения объемов опухолей приведены в приложениях к таблицам 1 и 2.
Переносимость соединения А в мышиной модели ксенотрансплантата HCC827
Переносимость соединения контролировали по проценту изменения массы тела в группе, как показано на фигуре 11. Только соединение А хорошо переносилось, и масса тела поддерживалась в течение 14-дневного курса лечения. Однако соединение INC280 по отдельности необходимо было давать с перерывом введения агента на 7 и 8 день из-за изменения массы тела на -8,5% и -5,66%, соответственно, но введение дозы возобновляли на 9 день. Поскольку соединение INC280 также было частью состава в группе сочетанной терапии и демонстрировало тенденцию к снижению массы тела на 9 день, в группе сочетанной терапии также делали перерыв приема лекарства на 9, 10 и 11 дни на основе изменений массы тела в группе -4,72%, -3,91, и -1,0%, и дозирование возобновляли с 12 до 14 дня. Исходные и конечные измерения массы тела подробно представлены в таблице 3.
Иммуногистохимическая оценка pEGFR (400×) и pMET (200×) в исследовании сочетания
IHC и гистология представлены на фигуре 12, верхняя панель представляет собой IHC pEGFR (p-EGFR (D). MS, HU; Hystology Immunohistochemistry SOP 33) 100×, нижняя панель представляет собой IHC pMET (p-Met (D).HU; Histology Immunohistochemistry SOP 53) 100×. Слева направо носитель, соединение А, соединение INC280, сочетание соединения A/INC280.
Заключение и обсуждение
Достижения лечения с помощью молекулярной направленной терапии против мутаций EGFR являются важной стратегией лечения больных с NSCLC. Среди них приблизительно 5% опухолей, позитивных в отношении мутаций EGFR с приобретенной резистентностью к TKIs EGFR, как обнаружено, имеют амплификацию гена MET.
Соединение А предназначено для улучшения эффективности действия ингибиторов EGFR первого и второго поколения, в то же время характеризуется пониженной токсичностью, лимитирующей дозу, по сравнению с предшествующими TKIs EGFR. Соединение А характеризуется возможностью обеспечения эффективной терапией для лечения NSCLC в сочетании с соединением INC280 в популяции больных, которые имеют активацию/амплификацию Met.
Соединение А обладает значительной противоопухолевой активностью и активностью в отношении регрессии опухолей в сочетании с соединением INC280 в опухолях HCC827, резистентных к монотерапии соединением А. После 14-дневного перорального введения один раз в день соединения А в дозе 30 мг/кг в сочетании с соединением INC280 в дозе 10 мг/кг два раза в день достигалась значительная регрессии опухолей (Т/С равно -86%). Соединение А отдельно хорошо переносится с небольшой или без потери массы тела, наблюдаемой при дозе 30 мг/кг. Соединение INC280 отдельно вызывало небольшое снижение массы тела на 7 день на -8,5% и хорошо переносилось в остальной части исследования. В сочетании, даже если сочетание соединения А и соединения INC280 переносилось, действовал перерыв приема лекарства на 9, 10 и 11 дни из-за эффектов одного агента INC280. В заключение, соединение А в сочетании с соединением INC280 может обеспечивать клиническое преимущество у больных NSCLC, в развитии которого участвует также cMet.
Таблица 1. Измерение индивидуального объема опухолей после лечения мышей с ксенотрансплантатом HCC827 (исследование # GNF-11-308-138-Eff-EGFR-соединение А-INC280-соединение А-резистентная HCC827)
|
Таблица 1. Фрагменты опухоли HCC827 NSCLC человека, резистентной к соединению А, пересаживали подкожно в правый бок 6-8-недельных самок бежевых мышей SCID. Лечение начинали, когда средний объем опухоли достигал ~580 мм3. Носитель (0,5% MC, 0,5% твин 80) или соединение А в дозе 30 мг/кг вводили один раз в день и INC280-АА-3 в дозе 10 мг/кг два раза в день перорально через зонд в течение 14 последовательных дней. Объемы опухолей рассчитывали путем измерения штангенциркулем, (длина × ширина × ширина)/2, и регистрировали 3 раза в неделю.
Таблица 2. Средний исходный и конечный объем опухолей ксенотрансплантата HCC827 мыши и противоопухолевый эффект T/C (лечение относительно контроля в процентах), сводка данных на 14 день после перорального введения соединения А один раз в день и/или перорального введения соединения INC280 два раза в день (исследование # GNF-11-308-138-Eff-EGFR-соединение А-HCC827)
|
Таблица 2. Фрагменты опухоли HCC827 NSCLC человека, резистентной к соединению А, пересаживали подкожно в правый бок 6-8-недельных самок бежевых мышей SCID. Лечение начинали, когда средний объем опухоли достигал~580 мм3. Носитель (0,5% MC, 0,5% твин 80) или соединение А в дозе 30 мг/кг вводили один раз в день и INC280-АА-3 в дозе 10 мг/кг два раза в день перорально через зонд в течение 14 последовательных дней. Объемы опухолей рассчитывали путем измерения штангенциркулем, (длина × ширина × ширина)/2, и регистрировали 3 раза в неделю. SE: стандартная ошибка. Изменения объема опухоли для каждой тестируемой (Т) и контрольной (С) группы измеряли путем вычитания среднего объема опухоли в день первой обработки (день стадирования) из среднего объема опухоли в указанный день наблюдений. Эти значения использовали для расчета процента T/C следующим образом:
%T/C=(ΔT/ΔC)×100; когда ΔT>0
%T/C=(ΔT/Т1)×100; когда ΔT<0
T1 представляет собой среднюю массу опухоли в начале лечения.
Таблица 3. Средняя исходная и конечная масса тела и процент изменения массы тела мыши с ксенотрансплантатом HCC827, резистентным к соединению А, на 14 день после перорального введения соединения А или носителя один раз в день и перорального введения соединения INC280 два раза в день (исследование № 11-308-138)
|
Таблица 3. Фрагменты опухоли HCC827 NSCLC человека, резистентной к соединению А, пересаживали подкожно в правый бок 6-8-недельных самок бежевых мышей SCID. Лечение начинали, когда средний объем опухоли достигал ~580 мм3. Носитель (0,5% MC, 0,5% твин 80) или соединение А в дозе 30 мг/кг вводили один раз в день и соединение INC280 в дозе 10 мг/кг два раза в день перорально через зонд в течение 14 последовательных дней. Массу тела рассчитывали с использованием весов Mettler (в граммах) и регистрировали от 1 дня до 14 дня. SD: стандартное отклонение. Процентное изменение массы тела рассчитывали как (BWтекущая-BWисходная)/(BWисходная)×100. Данные представлены в виде процента изменения массы тела со дня начала лечения.
Пример 3. Соединение А в сочетании с соединением INC280 у взрослых больных немелкоклеточным раком легкого с мутацией EGFR
Больных с распространенным или метастатическим NSCLC с мутантным EGFR L858R или ex19del можно лечить с помощью сочетания соединения А и соединения INC280.
Соединение А вводили ежедневно в дозе 50 мг, 75 мг, 150 мг, 300 мг, 450 мг, 600 мг или 800 мг. INC280 вводили в дозе 100 мг дважды в день, 200 мг дважды в день, 400 мг дважды в день или 600 мг дважды в день.