Результат интеллектуальной деятельности: Способ получения антигена вируса бешенства для серологической диагностики
Вид РИД
Изобретение
Изобретение относится к ветеринарной вирусологии, иммунологии, в частности к способу получения антигена вируса бешенства из производственного штамма вируса бешенства «Овечий» ГНКИ для диагностики бешенства.
Распространение бешенства среди животных является одним из важнейших международных критериев оценки биологической и экологической безопасности среды обитания человека. В мире от бешенства ежегодно погибают от 55 до 70 тыс. человек, половина из которых приходится на детей, и до 6,5 млн. человек подвергаются постэкспозиционным антирабическим обработкам (Smith A. et al. Ecology in disease control and public health Front Ecol Environ 2005; 3(1): 29-37, «Ecological theory to enhance infectious disease control and public health policy» 2005). В России ежегодно регистрируется 250-450 тыс.случаев бешенства. (Онищенко Г.Г., 2012 Постановление Главного государственного санитарного врача Российской Федерации от 1 февраля 2012 г. N 13 г. Москва «Об усилении мероприятий, направленных на профилактику бешенства в Российской Федерации»). Бешенство относится к числу наиболее опасных вирусных болезней, по оценке ВОЗ, входит в пятерку инфекций, общих для человека и животных, наносящих наибольший социальный и экономический ущерб. С учетом исключительности бешенства с присущими ему характеристиками многих классических инфекционных болезней - мировой нозоареал, природная очаговость, чрезвычайная контагиозность, векторная трансмиссия плотоядными, восприимчивость большинства видов животных, социальная и экономическая значимость, данное заболевание включено в список особо опасных инфекционных болезней МЭБ (World Organization for Animal Health, 2015), а в России - в Перечень заразных, в том числе особо опасных, болезней животных, по которым могут устанавливаться ограничительные мероприятия (карантин) (приказ МСХ РФ от 19.12.2011 г., №476).
Россия занимает доминирующее положение как по числу неблагополучных пунктов (очагов), так и по заболеваемости животных. За последние 20 лет в России регистрируется самая высокая смертность населения от заболевания бешенством среди развитых стран. Несмотря на проводимые мероприятия, на территории России в последний период активизировались природные очаги бешенства, увеличилась заболеваемость диких плотоядных, в эпизоотический процесс интенсивно вовлекаются домашние животные, создавая угрозу населению, что предопределяет современные особенности течения эпизоотии и видовой состав заболевших животных. На сегодняшний день проблема борьбы с бешенством является одной из наиболее актуальных ввиду широкой распространенности заболевания и отсутствия специфического лечения [5].
Наиболее значимым средством контроля распространения бешенства наряду со специфической профилактикой является точная и достоверная лабораторная диагностика [7, 8]. Современные средства лабораторной диагностики располагают определенным набором «in vitro» тестов, таких как реакция непрямой гемагглютинации (РНГА), реакция нейтрализации (РН), реакция связывания комплимента (РСК), реакция непрямой иммунофлюоресценции (РНИФ), реакция диффузионной преципитации зада (РДП), однако в скрининговых исследованиях они имеют ряд недостатков ввиду своей длительности и трудоемкости [1, 9]. Для решения подобных задач разработаны методы иммуноферментного анализа (ИФА) и их различные варианты, отличаются достаточной чувствительностью и специфичностью, определяемых на основе которых сконструированы тест-системы для количественного определения антител к вирусу бешенства в сыворотках крови, однако не все из них отличаются достаточной чувствительностью и специфичностью, определяемыми биологическими свойствами используемых в них антигенов [2, 3, 4].
В связи с этим одной из важнейших задач профилактики бешенства является совершенствование и подбор технических решений выделения высокоочищенного антигена вируса бешенства для дальнейшего его использования при создании современных диагностических тестов и получения специфических антител. Решение этой проблемы имеет важное народно-хозяйственное значение и способствует расширению возможностей лабораторной диагностики, детекции вируса бешенства и определению напряженности иммунного ответа вакцинированных животных и людей.
Совершенствование способов очистки вирусов имеет своей целью поиск новых технических подходов, способствующих увеличению выхода вирусной массы, сохранению ее серологической активности, получению высокоочищенных дискретных и мономерных структур возбудителя без посторонних примесей иных сопутствующих биологических структур, тропных к вирусу бешенства, при постоянном контроле каждой стадии очистки методами аналитического электрофореза, иммуноблотинга и ИФА с использованием гипериммунных сывороток крови кроликов и овец.
Известен способ получения антигена для диагностики бешенства, основанный на интрацеребральном заражении новорожденных ослят вирусом бешенства, взятии мозговой ткани, приготовлении суспензии, дополнительной двукратной обработкой мозговой ткани ультразвуком при 15-20 кГц в течение 25-30 мин и отделении вируса бешенства в градиенте сахарозы (инновационный патент KZ№23848, А61К 39/205, опуб. 15. 04.2011 г. Бюл. №4).
Данный способ имеет существенный недостаток, заключающийся в большом количестве балластного материала (рис. 1), наличие которого снижает долю специфичного антигена в данном материале и приводит к снижению специфичности гипериммунной сыворотки. Дальнейшее ее использование в серологических тестах, таких как ИФА, МФА снижает эффективность их использования. Очевидно, что данное явление обусловлено, с одной стороны, длительностью обработки ультразвуком (25-30 мин), приводящим к нагреву диспергируемого материала, в результате чего возможны необратимые деструктивные изменения биологического материала (суспензии клеток и вируса), с другой стороны - длительное кавитационное воздействие приводит к полному разрушению клеток и, как следствие этого, увеличивается выход вируса.
Наличие огромного количества разрушенного материала имеет предположительно одинаковую плавучую плотность с вирусом, в связи с чем наблюдается присутствие белков мозговой ткани в зонах локализации вирусной массы после центрифугирования в градиенте плотности сахарозы.
Наиболее близким к предлагаемому изобретению является способ получения антигена бешенства для серологической диагностики, включающей получение суспензий из мозга белых мышей, экспериментально зараженных вирусом бешенства - штамм «Овечий» ГНКИ, дезинтеграцию на приборе FastPrep 24™ при скорости вибрации 6 мл/с в течение 60в присутствии однородных частиц карбида кремния, осаждение мозговой ткани низкоскоростным центрифугированием, концентрирование супернатанта ультрацентрифугированием при 25000 об/мин и отделение вируса бешенства в ступенчатом градиенте сахарозы (15-50%) (см. ст.Ефимова М.А. и др. «Выявление, очистка и оценка серологической активности антигенов вируса бешенства» / «Проблемы особо опасных инфекций». Научно-практический ж., Саратов, вып. 4, 2017 г., с. 27-31).
Однако недостатком данного способа является низкий выход антигена вируса бешенства и невысокая чувствительность и специфичность.
Технический результат, на достижение которого направлено изобретение, заключается в увеличении выхода мономерного антигена, повышении его чувствительности и специфичности.
Для достижения названного технического результата в предлагаемом способе, включающем получение суспензий из мозга белых мышей, экспериментально зараженных вирусом бешенства - штамм «Овечий» ГНКИ, дезинтеграции на приборе FastPrep 24™ при скорости вибрации 6 мл/с в присутствии однородных частиц карбида кремния, центрифугирования полученной надосадочной жидкости для удаления посторонних частиц, ультрацентрифугирования для осаждения вирусных частиц и отделения вируса бешенства в ступенчатом градиенте сахарозы, перед дезинтеграцией мозговую ткань дополнительно гомогенизируют в стеклянном гомогенизаторе не менее 3-5 минут в 0,1 М фосфатно-буферном растворе, рН 7,2-7,4, а дезинтеграцию проводят три раза в течение 30 с с интервалом между обработками 5 мин, затем полученную мозговую суспензию выдерживают в пробирках Blue Lysing Matrix В не менее 5 мин до полного осаждения шариков карбида кремния, супернатант отбирают в отдельную емкость, а в пробирки добавляют 0,1 М фосфатно-буферный раствор, встряхивают 3 раза на Vortex V1 в течение 30 с и выдерживают не менее 5 мин, полученный раствор отбирают и все полученные супернатанты объединяют, центрифугирование проводят в течение 50 мин при 5000 об/мин, супернатант отбирают в стерильную емкость, концентрируют ультрацентрифугированием при 37000 об/мин в течение 4 часов при температуре +4°С, супернатант удаляют, а к осадку добавляют 0,1 М фосфатно-буферного раствора, рН 7,2-7,4, в объеме, равном 1/10 от исходного элюата, 3 раза встряхивают в течение 30 с с интервалом между встряхиваниями 3 мин, затем ресуспендированный осадок наслаивают на ступенчатый градиент 10-60%-ной сахарозы и ультрацентрифугируют в течение 3 часов при 30000 об/мин при температуре +4°С, далее вирусный материал фракционируют при помощи гель-фильтрации и по результатам иммуноблотинга отбирают активные фракции, переосаждают их спиртом и получают антиген вируса бешенства.
Отличительными признаками предложенного способа являются дополнительная гомогенизация мозговой ткани перед дезинтеграцией в стеклянном гомогенизаторе не менее 3-5 мин в 0,1 М фосфатно-буферном растворе, рН 7,2-7,4, проведение 3разовой дезинтеграции в течение 30 с с интервалом между обработками 5 мин, выдерживание мозговой суспензии в пробирках Blue Lysing Matrix В не менее 5 мин до полного осаждения шариков карбида кремния, отбор супернатанта в отдельную емкость, 3разовое встряхивание на Vortex V1 в течение 30 с и выдержки не менее 5 мин, отбор полученного супернатанта, объединение всех полученных супернатантов, центрифугирование в течение 50 мин при 5000 об/мин, отбор супернатанта в отдельную стерильную емкость, концентрирование ультрацентрифугированием при 37000 об/мин в течение 4 часов при температуре +4°С, удаление супернатанта и добавление к осадку 0,1 М фосфатно-буферного раствора, рН 7,2-7,4, в объеме, составляющем 1/10 от исходного элюата, 3разовое встряхивание в течение 30 с с интервалом между встряхиваниями 3 мин, наслаивание ресуспендированного осадка на ступенчатый градиент 10-60%-ной сахарозы, ультрацентрифугирование в течение 3 часов при 30000 об/мин при температуре +4°С, фракционирование вирусного материала при помощи гель-фильтрации, отбор активных фракций по результатам иммуноблотинга, переосаждение их спиртом и получение антигена вируса бешенства, что позволяет получить мономерный, высокоочищенный и специфичный антиген вируса бешенства и увеличить выход антигена в 2 раза, повысить специфичность и чувствительность в 8 раз.
Предлагаемое изобретение поясняется рисунками, на которых изображены:
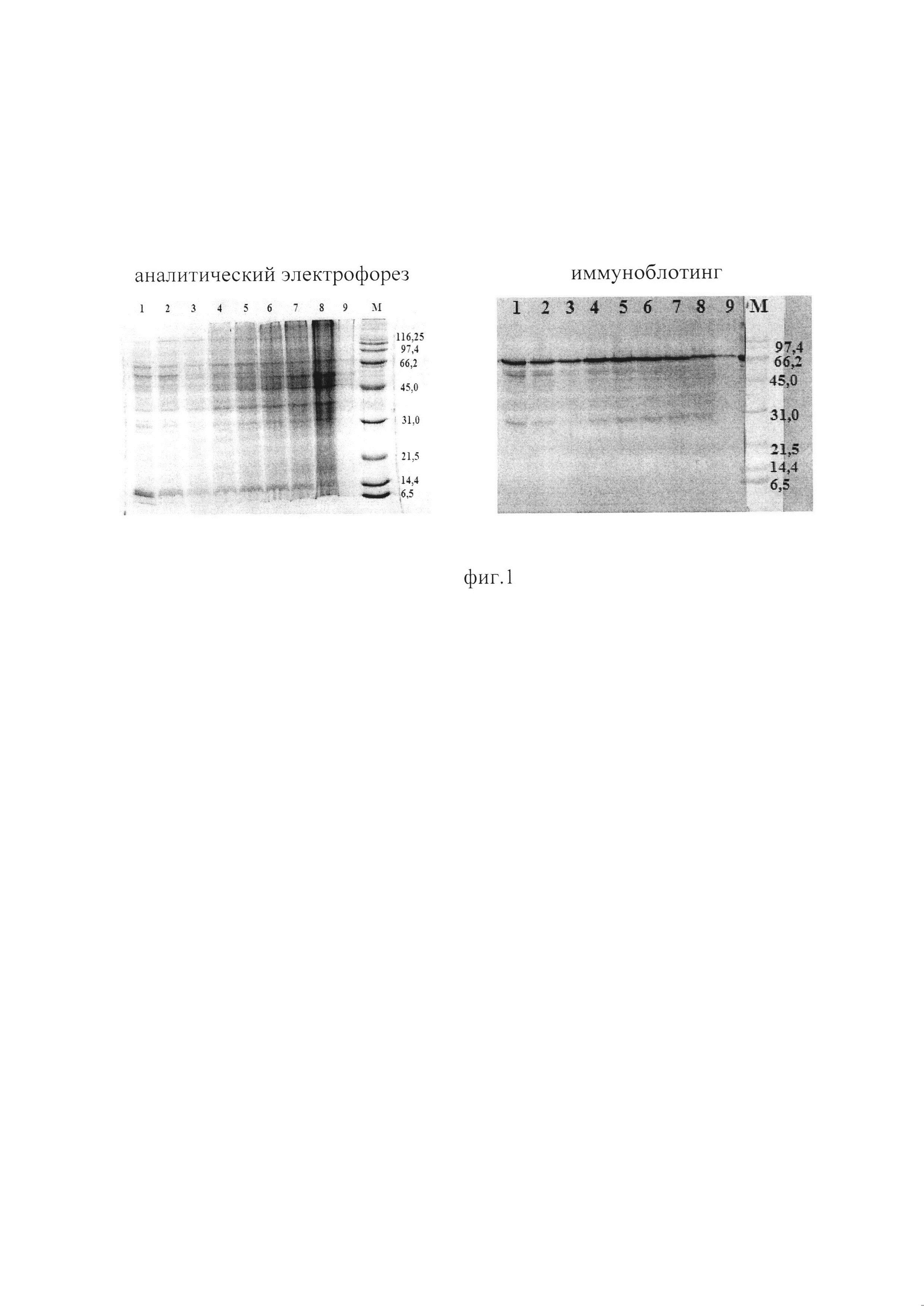
Фиг. 1. - Результаты аналитического электрофореза в 12,0% ПААГ и иммуноблота с кроличьей гипериммунной сывороткой осадка вирусного материала, разделенного по плавучей плотности, полученного после УЦФ при 37000 об/мин.
Фиг. 2. - Распределение по плавучей плотности осадка вирусного материала, полученного после УЦФ при 37000 об/мин в ступенчатом градиенте сахарозы (10-60%).
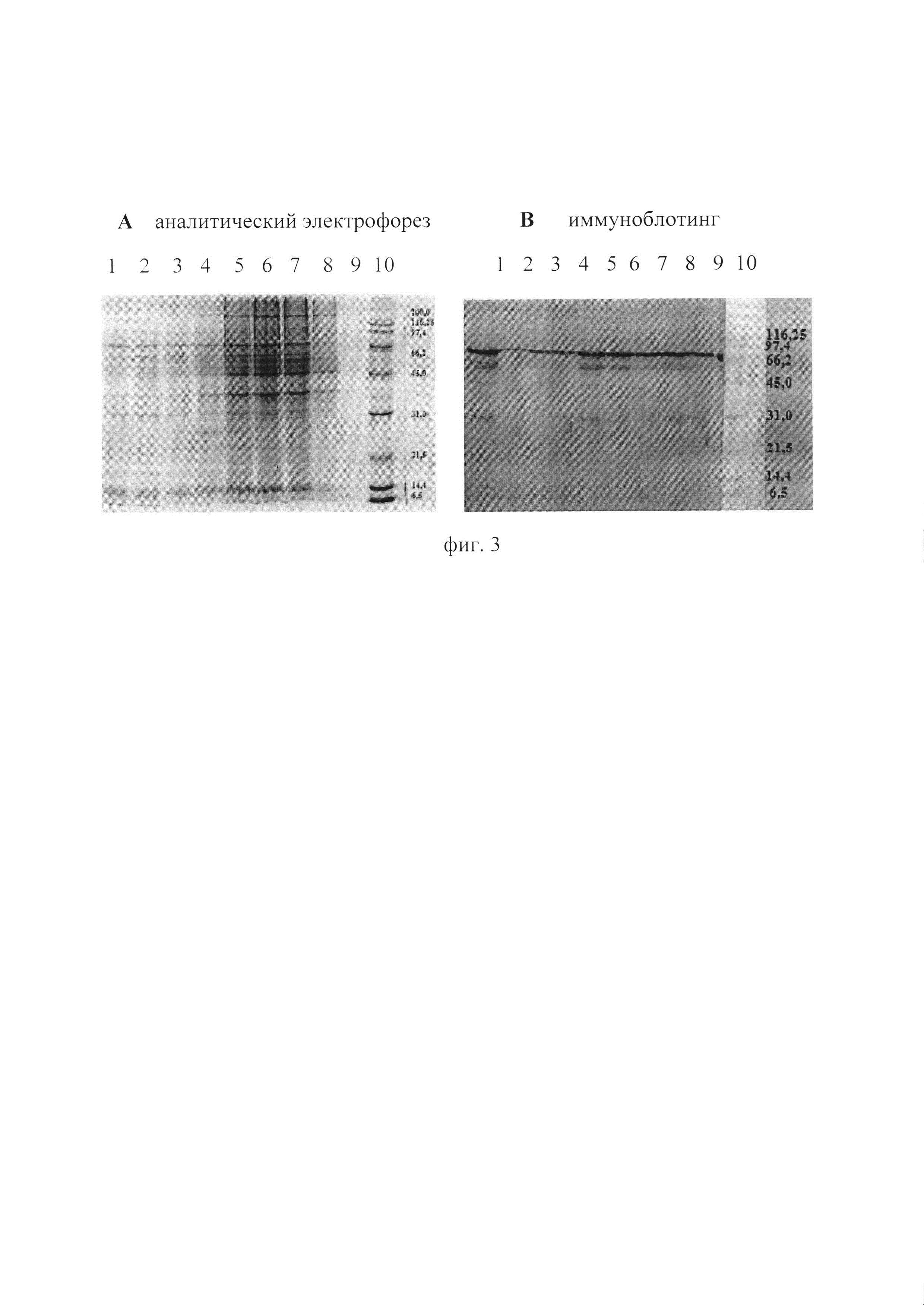
Фиг. 3. - Результаты аналитического электрофореза в 12,0% ПААГ и иммуноблотинга с кроличьей гипериммунной сывороткой осадка вирусного материала, разделенного по плавучей плотности в ступенчатом градиенте сахарозы (10-60%), полученного после УЦФ при 30000 об/мин.
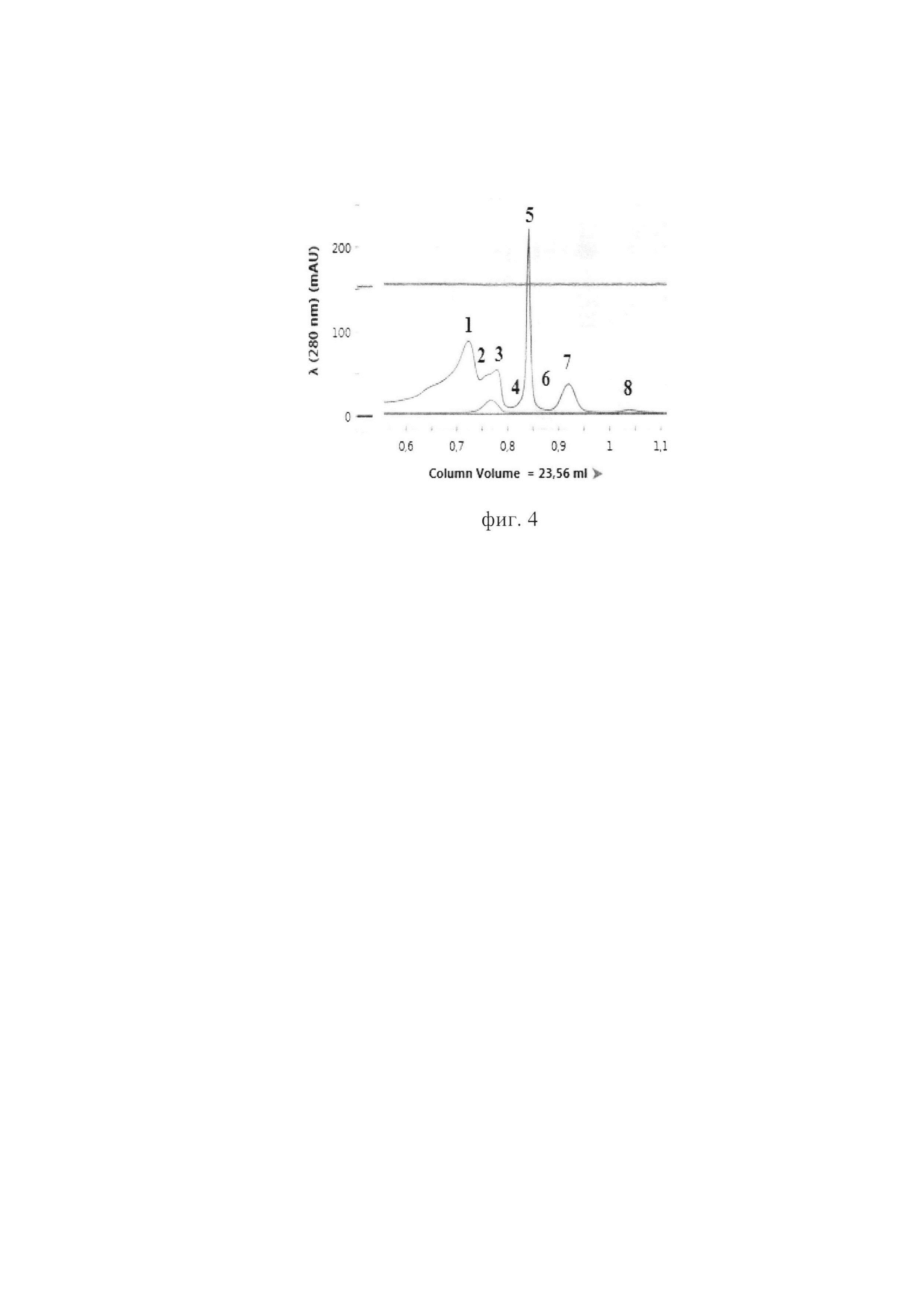
Фиг. 4. - Гистограмма фракционирования вирусного материала, отобранного по результатам иммуноблотинга после УЦФ в градиенте плотности сахарозы, полученного методом гель-фильтрации на колонке Enrich™SEC 70.
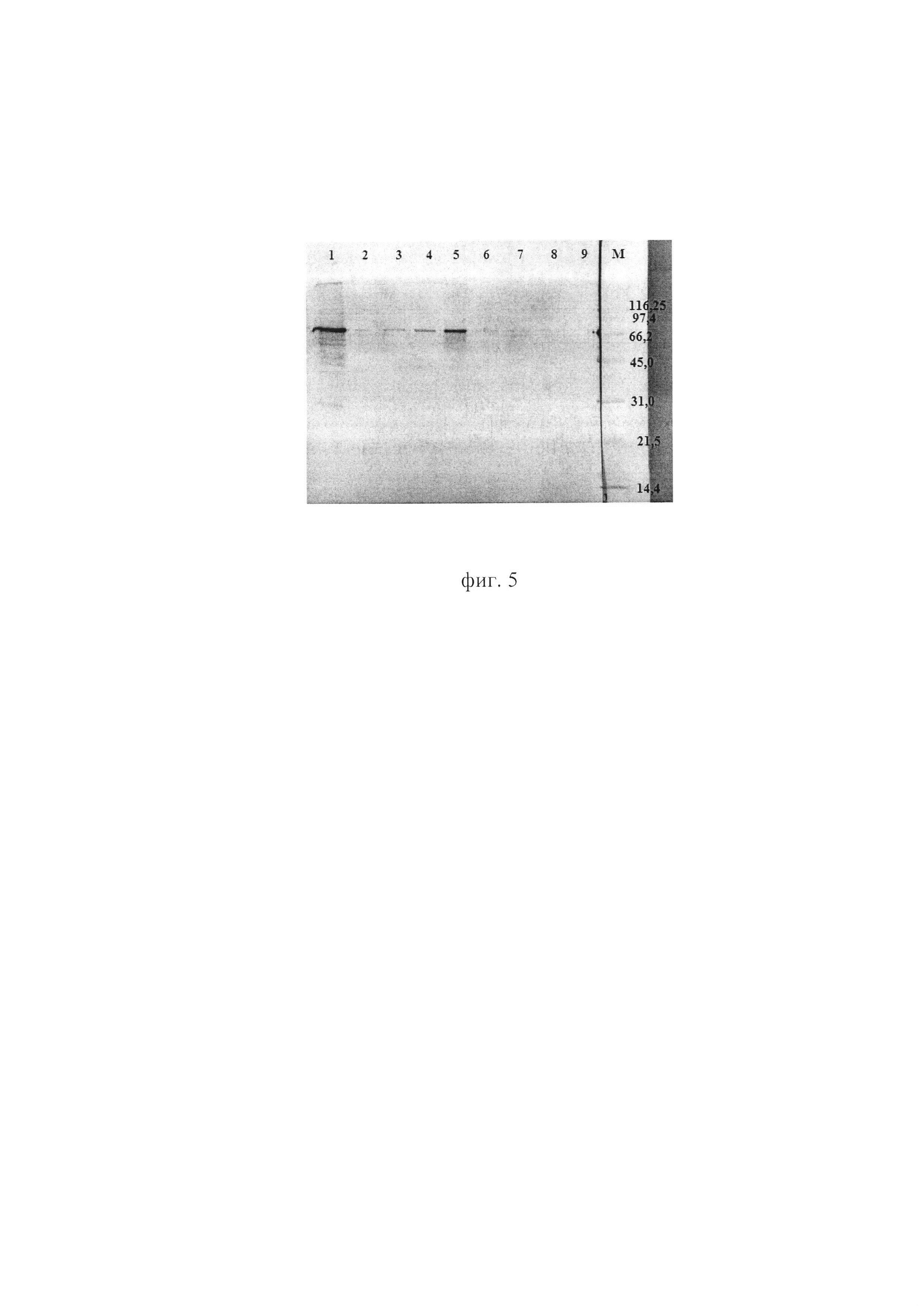
Фиг. 5. - Результаты иммуноблотинга вирусного материала после гель-фильтрациина колонке Enrich™SEC 70 с гипериммунной кроличьей сывороткой.
Фиг. 6. - Денситограмма иммуноблотинга исходного вирусного материала до хроматографии, фракция №5, и спиртовый осадок фракции №5.
Антиген для диагностики бешенства получают следующим образом:
Для получения использовали производственный штамм вируса бешенства «Овечий» ГНКИ (коллекция ФГБНУ «ФЦТРБ-ВНИВИ) органо-тканевого происхождения с инфекционным титром 5,25 lgLD50/0,03 мл. Предварительно вирус бешенства -штамм«Овечий» ГНКИ» освежали через мозг 12-14 суточных мышат, проводя 3-4 слепых пассажей. Затем брали ягнят 2-3 месячного возраста, полученных от серонегативных овец, под местной анестезиейинтрацеребрально заражали в дозе 0,5-2,0 см3 20%-ной суспензией мозга белых мышей, зараженных вирусом бешенства (штамм«Овечий» ГНКИ) после 4-го пассажа. На 7-14 сутки после заражения в период выраженных клинических симптомов - параличей ягнят убивали декапитированием, стерильно извлекали мозг. Мозговую ткань растирали в фарфоровой ступке и готовили 20%-ную мозговую суспензию в 0,1 М фосфатно-буферном растворе (ФБР). Далее мозговую ткань гомогенизировали в стеклянном гомогенизаторе не менее 3-5 мин для получения однородной массы в 0,1 М фосфатно-буферном растворе, рН 7,2-7,4. Затем гомогенат подвергали дезинтеграции на приборе FastPrep 24™ Classic Instrument (MP Biomedicals) для полного разрушения клеток мозговой ткани. Длямаксимального извлечения вируса использовали следующий режим обработки: скорость вибрации - 6 мл/с, время обработки - 30 с, количество обработок - 3 с интервалом между обработками 5 минут. Дезинтегрированную 20%-ную мозговую суспензию выдерживали в пробирках Blue Lysing Matrix В не менее 5 мин до полного осаждения шариков карбида кремния и после этого проводили отбор дезинтегрированного материала. Супернатант осторожно отбирали в отдельную емкость, а в пробирки Blue Lysing Matrix В вновь добавляли 0,1 М ФБР, рН 7,2-7,4, встряхивали на Vortex V1 в течение 30 с, затем выдерживали не менее 5 мин до полного осаждения шариков карбида кремния. Супернатант осторожно отбирали. Данную процедуру повторяли 3 раза. Все полученные дезинтегрированные супернатанты объединяли. Разрушенную на приборе FastPrep 24™ 20%-ную мозговую суспензию осаждали центрифугированием при 5000 об/мин в течение 50 мин при температуре +8-10°С на центрифуге Eppendorf 5804 R для удаления крупных посторонних частиц. Супернатант отбирали в отдельную емкость, а осадок удаляли. Отобранный супернатант концентрировали ультрацентрифугированием при 37000 об/мин в течение 4 часов при температуре +4°С на ультрацентрифуге Beckman L-7, ротор SW-41, для осаждения вирусных частиц. После концентрирования супернатант удаляли, а к осадку добавляли 0,1 М фосфатно-буферный раствор, рН 7,2-7,4, в объеме, равном 1/10 объема элюата, затем 3 раза встряхивали на Vortex V1 с интервалом между встряхиваниями 3 минуты. Далее ресуспендированный осадок наслаивали на ступенчатый градиент плотности сахарозы с концентрацией 10-60%. 1 мл концентрированной суспензии вируса наслаивали на 12 мл ступенчатого градиента сахарозы (10-60%-ный раствор сахарозы, приготовленный на физиологическом растворе, забуференном 0,01 М Na-фосфатным буфером, рН 7,5) (фиг. 1), где 1 - исходный вирусный материал (осадок), полученный после УЦФ при 37000 об/мин; 2 - вирусный материал, отобранный до 10% сахарозы; 3 - вирусный материал, отобранный с 10% до 20% сахарозы; 4 - вирусный материал, отобранный с 20% до 30% сахарозы; 5 - вирусный материал, отобранный с 30% до 40% сахарозы; 6 - вирусный материал, отобранный с 40% до 50% сахарозы; 7 - вирусный материал, отобранный с 50% до 60% сахарозы; 8 - вирусный материал, отобранный с 60% сахарозы до дна пробирки; 9 - визуально отсутствующий осадок на дне пробирки; 10 - маркер молекулярных масс Broad Range, «Bio-Rad», затем центрифугировали в течение 3 часов при 30000 об/мин при температуре +4°С на ультрацентрифуге Beckman L-7, ротор SW-41. После окончания центрифугирования дно пробирки прокалывали и отбирали фракции (всего фракций получено 5) по 2 мл по зонам опалесценции. Зона, содержащая вирус, располагалась на границе трети градиента (фиг. 2), где 1, 2, 3, 4, 5 - зоны визуальной опалесценции распределения по плавучей плотности осадка вирусного материала.
Отобранные фракции объединяли по результатам иммуноблотинга. Самые активные фракции располагались в зоне 10-20%-ной сахарозы, данную фракцию использовали для гель-фильтрации на колонке Enrich™SEC 70 (фиг. 3), где А - аналитический электрофорез, В - иммуноблотинг на фиг. 3А показан:
1 - вирусный материал, отобранный до 10% сахарозы; 2 - вирусный материал, отобранный с 10% до 20% сахарозы; 3 - вирусный материал, отобранный с 20% до 30% сахарозы; 4 - вирусный материал, отобранный с 30% до 35% сахарозы; 5 - вирусный материал, отобранный с 35% до 40% сахарозы; 6 - вирусный материал, отобранный с 40% до 45% сахарозы; 7 - вирусный материал, отобранный с 45% до 50% сахарозы; 8 - вирусный материал, отобранный с 50% до 60% сахарозы; 9 - вирусный материал, отобранный с 60% сахарозы до дна пробирки; 10 - маркер молекулярных масс Broad Range, производитель «Bio-Rad».
На фиг. 3В - иммуноблотинг фракций электрофореза вирусного материала, перенесенного после электрофореза на нитроцеллюлозную мембрану, разделенного по плавучей плотности с гипериммунной кроличьей сывороткой, полученной против производственного штамма вируса бешенства «Овечий» ГНКИ в разведении 1:100.
Белковый состав разделенных образцов изучали аналитическим электрофорезом в 12% ПААГ в присутствии 0,1%-ного додецилсульфата натрия по Laemmli U. K. [11] и переносили на нитроцеллюлозную мембрану (Suppoted nitrocellulose membrane 0,45 μm, «Bio-Rad») no Towbin H. [12], серологическую активность определяли в реакции иммуноблотинга с использованием гипериммунной сыворотки крови, полученной путем гипериммунизации кроликов производственным штаммом вируса бешенства «Овечий» ГНКИ (инфекционный титр5,25 lg LD50/0,03 мл) по методике [10].
На каждом этапе очистки вируса проводили контроль при помощи аналитического электрофореза и иммуноблотинга для выявления локализации полипептидов и их серологической активности. Концентрацию белка определяли на спектрофотометре UV5 (Mettler Toledo) при длине волны 280 нм согласно инструкции к прибору. Электрофоретический профиль вируса бешенства изучали по методу Laemmli U. K. [11]. Методом иммуноблотинга по Towbin Н. [12] определяли серологическую активность полученного материала с гипериммунной сывороткой овец против производственного штамма вируса бешенства «Овечий» ГНКИ и с сывороткой овец, вакцинированных антирабической вакциной - штамм «Щелково-51» (ФКП «Щелковский биокомбинат»).
Как показывали результаты иммуноблотинга, серологическая активность наблюдалась практически во всех зонах визуальной опалесценции, кроме зоны 60%-ной сахарозы. Наибольшая активность локализовалась в 10-30%-ной границе градиента сахарозы (фиг. 2 зоны 1 и 2).
Объединенный вирусный материал с зоны сахарозы 10-30% разделяли на хроматографе NGC Discovery (Bio-Rad) методом гель-фильтрации с использованием колонки Enrich ™SEC 70. Контроль разделения осуществляли с помощью одноволнового УФ-детектора при длине волны 280 нм. Фракции собирали по 1 мл, используя коллектор фракций BioFrac (Bio-Rad) (фиг. 4), где по оси абсцисс показано количество элюирующего буфера, прошедшего через колонку, по оси ординат - оптическая плотность, выраженная в единицах оптической плотности (ед.оп.) при длине волны 280 нм.
Активность фракционного материала анализировали методом иммуноблотинга с использованием гипериммунных сывороток кроликов. Кроликов иммунизировали 3-кратно, сначала с полным адъювантом Фрейнда в соотношении антигена и адъюванта 1:1 с внутрикожной инъекцией по 0,1 мл в 5 точек вдоль спины с каждой стороны, место инъекции предварительно выстригали, через 8-10 недель повторно иммунизировали в смеси с неполным адъювантом Фрейнда в дозе по 0,5 мл подкожно в области нижней трети шеи с каждой стороны, затем через 6 недель проводили последнюю процедуру. Отобранные сыворотки кроликов использовали в реакции иммуноблотинга (фиг. 5), где 1 - исходный вирусный материал до хроматографии (область 10-20% сахарозы); 2 - фракция №1; 3 - фракция №2; 4 - фракция №3; 5 - фракция №5; 6 - фракция №6; 7 - фракция №7; 8 - фракция №8; 9 - пустая лунка; 10 - маркер молекулярных масс Broad Range, «Bio-Rad».
Концентрацию белка определяли на спектрофотометре UV5 (Mettler Toledo) при длине волны 280 нм. Белковый состав фракционного материала изучали методом аналитического электрофореза в 12% ПААГ, а серологическую активность определяли в реакции иммуноблотинга и ИФА.
Наибольший интерес по результатам иммуноблотинга представляла фракция №5.
Результаты иммуноблотинга фиксировалина приборе GelDoc XR+ (Bio-Rad), а обрабатывали с использованием программы Image Lab Software 5.1. Результаты обработки представлены в виде денситограмм (фиг. 6), где по оси абсцисс показана длина пробега, по оси ординат - оптическая плотность, выраженная в единицах оптической плотности (ед.оп.) при длине волны 550-600 нм.
А - исходный вирусный материал до хроматографии (область 10-20% сахарозы зона);
В - фракция №5;
С - фракция №5, осажденная спиртом.
Как видно из фиг. 6, максимально очищенной является белковая фракция с молекулярной массой 65-67 кДа, отобранная с зоны сахарозы 10-30% (фиг. 6, позиция С). Высокая специфическая активность данной фракции подтверждена в ИФА и достигла 1:10240, что позволило увеличить выход антигена в 2 раза, повысить его специфичность и чувствительность в 8 раз по сравнению с прототипом [3].
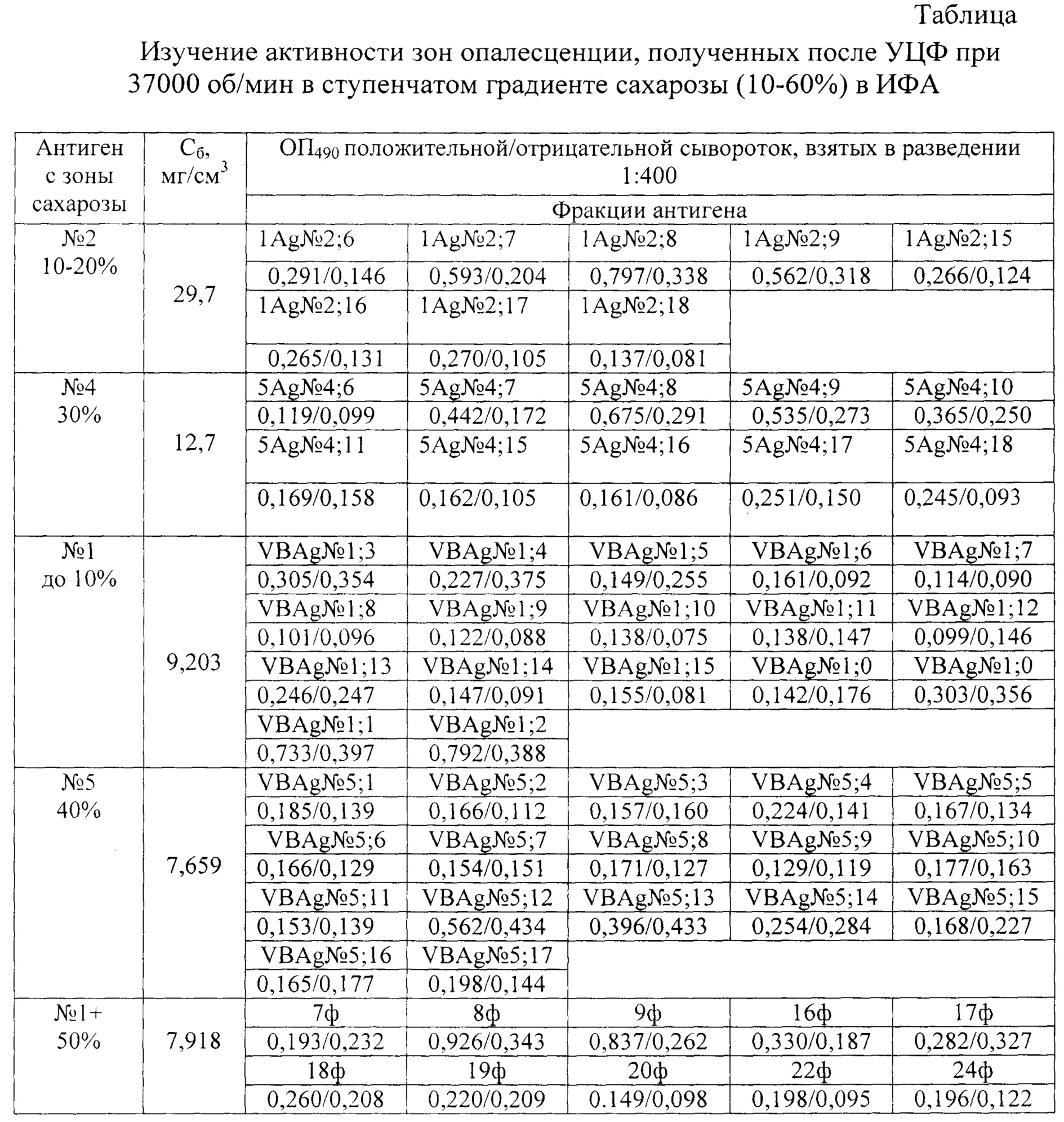
Максимально очищенную фракцию с 10-30%-ной зоны сахарозы дополнительно переосаждали спиртом в соотношении 1:2 и таким образом получали очищенную активную фракцию вируса бешенства, которую использовали в качестве рабического антигена для серологической диагностики бешенства. Осадок с концентрацией белка 20 мг/мл растворяли в 0,1 М ФБР, рН 7,2-7,4 в объеме, равном 1/10 от исходного. Данный материал использовали в дальнейшей работе в качестве антигена вируса бешенства для ИФА. Часть материала замораживалипри температуре -70°С для хранения и создания биобанка антигенов. Осажденный антиген представляет собой прозрачную, с небольшой опалесценцией жидкость. Серологическую активность очищенного антигена после гель-фильтрации и переосаждения спиртом определяли методом ИФА: в стрипованные лунки планшета ВНИИ «Медполимер» в объеме 120 мкл вносили очищенный антиген и выдерживали планшеты в течение 24 часов при комнатной температуре, затем 3 раза промывали дистиллированной водой и высушивали при комнатной температуре. Реакцию ИФА проводили с овечьей гипериммунной сывороткой крови, полученной к штамму вируса бешенства «Овечий» ГНКИ, а в качестве конъюгата использовали Anti-sheep IgG, меченные пероксидазой хрена, производства фирмы «Sigma». Полученные результаты приведены в таблице. Как видно из таблицы, активность распределялась в зависимости от зон концентрации сахарозы, достигая максимального значения в зоне 10-20% сахарозы(концентрация белка 29,9 мг/мл, соответствующая массе 65-67 кДа). Использование полученного антигена для иммунизации овец-продуцентов гипериммунной сыворотки позволило получить сыворотку с более высокой активностью в ИФА, которая достигала титра 1:12800.
Таким образом, полученный антиген вируса бешенства позволяет увеличить выход активного антигена в 2 раза повысить специфичность и чувствительность в 8 раз по сравнению с прототипом.
Список литературы
1. Абрамова Е.Г., Генералов С.В., Матвеева Ж.В., Жулидов И.М., Никифоров А.К., Комиссаров А.В. Экспериментальное обоснование внедрения культуральных технологий в производство антирабического иммуноглобулина. Проб. особо опасных инф. 2016; 2:95-101. DOI: 10.21055/03 70-1069-2016-2-95-101.
2. Дяченко С.А., Матвеева И.Н., Попова В.М., Кузнецов Д.П., Евглевский А.А. Сэндвич-вариант ИФА для выявления вируса бешенства в головном мозге животных и птицы // Вестник Курской государственной сельскохозяйственной академии. - 2015. - С. 201.
3. Ефимова М.А., Хаертынов К.С, Арсланова А.Ф., Ахмадеев P.M., Никитин А.И., Гумеров В.Г., Шуралев Э.А. Выделение, очистка и оценка серологической активности антигенов вируса бешенства //Пробл. особо опасных инф. - Научно-практический ж., Саратов - 2017. - №4. - С. 27-31.
4. Кондрахин И.П., Курилов Н.В., Малахов А.Г., Архипов А.В., Белов А.Д., Беляков И.М., Блинов Н.И., Коробов А.В., Фролова Л.А., Севастьянова
5. Макаров В.В. Бешенство // Российский ветеринарный журнал №1-2017. - С. 32.
6. Способ получения антигена для диагностики бешенства / Ахметсадыков Н.Н., Хусаинов Д.М., Батанова Ж.М., Икранбегийн Р., Кожаев А.Н., Абдикадырова A.M.; заявитель и патентообладатель ТОО «Научно-производственное предприятие «Антиген». - №(19) KZ (13) А4 (11) 23848 (51) А61К 39/205; заявл. 02.04.2010; опубл. 15.04.2011.
7. Тимиргалеев, Р.В. Усовершенствование методов идентификации вируса бешенства и выявления антирабических антител: автореф. дис.… канд. вет.наук: 16.00.03 и 03.00.07 / Руслан Владимирович Тимиргалеев. - Казань, 2006. - 24 с.
8. Хисматуллина Н.А., Гулюкин A.M., Шуралёв Э.А., Хаертынов К.С, Чернов А.Н., Филимонова М.Н., Авзалова А.Ф., Паршикова А.В., Иванов А.В. Ускоренный метод диагностики бешенства в культуре клеток невриномы Гассерова узла крысы (НГУК-1) // Журнал «Гены и клетки». -2014. - Т. 9, №3. - С. 276-280.
9. Янбарисова СР. Сравнение традиционных и экспресс-методов лабораторной диагностики бешенства // Известия Оренбургского государственного аграрного университета. - 2010. - С. 90-91.
10. Chacko K., Parakadavathu R.T., Al-Maslamani М., Nair А.Р., Chekura А.Р., Madhavan I. Diagnostic difficulties in human rabies: A case report and review of the literature. Qatar Med. J. 2017; 2016(2):15. DOI: 10.5339/qmj.2016.15.
11. Duong V., Tarantola A., Ong S., Mey C, Choeung R., Ly S., Bourhy H., Dussart P., Buchy P. Laboratory diagnostics in dog-mediated rabies: an overview of performance and a proposed strategy for various settings. Int. J. Infect. Dis. 2016; 46:107-4. DOI: 10.1016/j.ijid.2016.03.016.
12. Laemmli U.K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature. 1970; 227(5259):680-5.