Результат интеллектуальной деятельности: Фармацевтическая композиция для лечения заболеваний глаз, сопровождающихся окислительным стрессом, и способ ее применения
Вид РИД
Изобретение
Изобретение относится к лекарственным средствам местного применения для моно- и комплексной терапии заболеваний глаз, сопровождающихся окислительным стрессом, и содержащим в качестве действующего вещества фермент супероксиддисмутазу.
Под окислительным стрессом понимают усиление свободнорадикальных процессов на фоне ослабления собственной антиоксидантной системы с истощением пула эндогенных антиоксидантов, которое приводит к повреждению практически всех структурных и функциональных компонентов клеток [Зенков Н.К., Ланкин В.З., Меньщикова Е.Б. Окислительный стресс: Биохимический и патофизиологический аспекты. 2001, М.: МАИК «Наука/ Интерпериодика»]. При этом свободные радикалы инициируют перекисное окисление липидов, способствуют образованию токсических веществ, усугубляют нарушения микроциркуляции в тканях, приводящие к ишемизации тканей.
Развитие практически всех глазных патологий сопровождается развитием окислительного стресса. [Зиангирова Г.Г., Антонова О.В. Перекисное окисление липидов в патогенезе первичной открытоугольной глаукомы (2003) Вестн. Офтальмол., 4, 54-55; Yang X., Hondur G., Tezel G. Antioxidant treatment limits neuroinflammation in experimental glaucoma (2016); Бейшенова Г.А. Чеснокова Н.Б. Роль свободнорадикального окисления в патогенезе увеитов (Обзор литературы) (2015) РОЖ, 8, 99-106].
Для лечения заболеваний глаз, сопровождающихся окислительным стрессом, используют антиоксиданты, антигипоксанты, средства, оказывающие регенеративное действие и улучшающие микроциркуляцию [Рациональная фармакотерапия в офтальмологии (2006) (под ред. Е.А. Егорова), Изд-во Литтерра, Москва, с. 652-657; Морозов В.И., Яковлев А.А. (2009) Фармакотерапия глазных болезней, Изд-во МЕД пресс-информ, Москва, с. 169-179], в частности, препараты эмоксипина, пиридоксина, эхинохрома («Гистохром»).
Известен способ лечения заболеваний глаз, сопровождающихся окислительным стрессом (первичная открытоугольная глаукома, передний увеит, герпетическое и аденовирусное поражение глаз, вторичная кератопатия, травмы и ожоги глаз), предусматривающий инстилляции в конъюнктивальную полость антиоксидантного препарата на основе рекомбинантной супероксиддисмутазы (фармацевтический препарат «Рексод-ОФ», регистрационное удостоверение ЛСР-006689/10 от 15.07.10, и «Эрисод» [Патент RU 2144343 С1]). Однако известные лекарственные препараты супероксидисмутазы плохо проникают во внутренние структуры глаза.
Перспективным подходом к решению проблемы доставки лекарственного препарата к внутриглазным тканям является использование наночастиц в качестве систем доставки лекарственной субстанции, так как они значительно увеличивают биодоступность лекарства и позволяют создавать в тканях необходимые концентрации лекарственного вещества. [Патент RU 2508123; Патент RU 2577236; Чеснокова Н.Б., Галицкий В.А., Безнос О.В., Бейшенова Г.А., Кост О.А., Никольская И.И. Получение кальций-фосфатных частиц, содержащих супероксиддисмутазу, и их влияние на воспалительный процесс в глазу при экспериментальном увеите у кроликов (2015) РОЖ, 8, 31-36; Никольская И.И., Безнос О.В., Галицкий В.А., Чеснокова Н.Б., Кост О.А. Кальций-фосфатные частицы, содержащие супероксиддисмутазу - перспективный препарат для лечения заболеваний глаз, сопровождающихся окислительным стрессом (2016) Вестн. Моск. Унта. Сер. Хим., 57, 138-144; Kost О.А., Beznos O.V., Davydova N.G., Manickam D.S., Nikolskaya I.I., Guller A.E., Binevski P.V., Chesnokova N.B., Shekhter A.B., Klyachko N.L., Kabanov A.V. Superoxide dismutase I nanozyme for treatment of eye inflammation (2016) Oxidative Medicine and Cellular Longevity, 2016, 5194239doi].
Однако катионный полимер, использованный в качестве матрицы в [Патент RU 2508123], а именно метокси-поли(этиленгликоль)-поли(L-лизин) блок-сополимер, потенциально токсичен, а биодеградируемые и биосовместимые кальций-фосфатные частицы [Патент RU 2577236] обладают относительно большими гидродинамическими радиусами до 350 нм, в то время как для эффективного проникновения в ткани оптимальными считаются частицы радиусом до 100 нм.
Как указывалось выше, в настоящее время для лечения заболеваний глаз, сопровождающихся окислительным стрессом (первичная открытоугольная глаукома, передний увеит, герпетическое и аденовирусное поражение глаз, вторичная кератопатия, травмы и ожоги глаз применяются фармацевтические препараты, предусматривающие инстилляции их в конъюнктивальную полость, на основе супероксиддисмутазы - «Рексод-ОФ», (регистрационное удостоверение ЛСР-006689/10 от 15.07.10,) и «Эрисод» [Патент RU 2144343 С1]).
Препарат Рексод -ОФ и способ его применения выбран нами в качестве прототипа как в части «композиция», так и в части «способ». Препарат Рексод-ОФ выпускается в виде лиофилизата рекомбинантной супероксиддисмутазы человека. Перед употреблением содержимое флакона 0,8 млн ЕД разводят в 2 мл воды и полученный раствор (глазные капли) хранят в холодильнике при 4-10°С в течение не более 3 дней. Лечение указанным препаратом включает инсталляцию его в коньюнктивальную полость при первичной открытоугольной глаукоме по 6-7 раз в течение 30 минут дважды в сутки, при аденовирусных поражениях глаз 6-8 раз в сутки в течение не менее 10 дней.
Недостатком этого препарата и способа лечения с его помощью является плохое проникновение во внутренние структуры глаза. Известно, что в среднем только около 5% от вводимого лекарственного вещества способно проникнуть через роговую оболочку и достичь внутриглазных тканей [Ahmad I., Patton Т. Importance of the non and corneal absorption routes in topical ophthalmic drug delivery. (1985) Invest. Ophtalm. Vis. Sci., 26, 584-587]. В итоге, необходимую концентрацию лекарственной субстанции в препарате необходимо либо повышать, либо часто производить инсталляции препарата (до 8 раз в сутки), что усиливает нежелательные побочные эффекты (как локальные, так и системные), связанные с последующим попаданием этих препаратов в кровоток.
Техническим результатом заявленного изобретения как в части «композиция», так и в части «способ», является усиление антиокислительной активности супероксиддисмутазы и усиление противовоспалительного лечебного эффекта супероксиддисмутазы при заболеваниях глаза, сопровождающихся окислительным стрессом. Это выражается в уменьшении времени заживления воспаления, снижению проявлений воспалительного процесса как во внешних, так и внутренних отделах глаза. Кроме того, использование предлагаемой композиции позволяет снизить частоту введения препарата.
Этот технический результат в части «композиция» достигается тем, что фармацевтическая композиция для местного применения при воспалительных заболеваниях глаз, сопровождающихся окислительным стрессом, представляет собой суспензию в буфере, изотоническом физиологическому раствору с рН 7,4, действующего вещества в виде супероксиддисмутазы с активностью 50-500 кЕд/мл, включенной в наночастицы, сшитые глутаровым альдегидом, в которых фермент покрыт внутренней оболочкой из протамина и внешней оболочкой из блок-сополимера поли(глутаминовой кислоты) и полиэтиленгликоля (ПГ-ПЭГ), при этом гидродинамический радиус наночастиц фермента составляет 40-80 нм, а концентрация наночастиц в суспензии равна 0,5-5⋅1014 частиц/мл, композиция содержит также целевые добавки и/или лекарственные средства.
Композиция может быть выполнена в форме глазных капель или спрея.
Композиция может содержать в качестве целевой добавки консервант.
Композиция в качестве лекарственного средства может содержать антибиотики, и/или стероиды и/или адреноблокаторы.
Указываемый технический результат в части «способ» достигается тем, что производят инсталляции в конъюнктивальную полость глаза фармацевтической композиции по пп. 1-4, содержащей эффективное количество супероксиддисмутазы в дозе от 1,5 до 15 кЕД ежедневно 2-3 раза в день, длительностью от 1 недели до момента завершения воспалительного процесса.
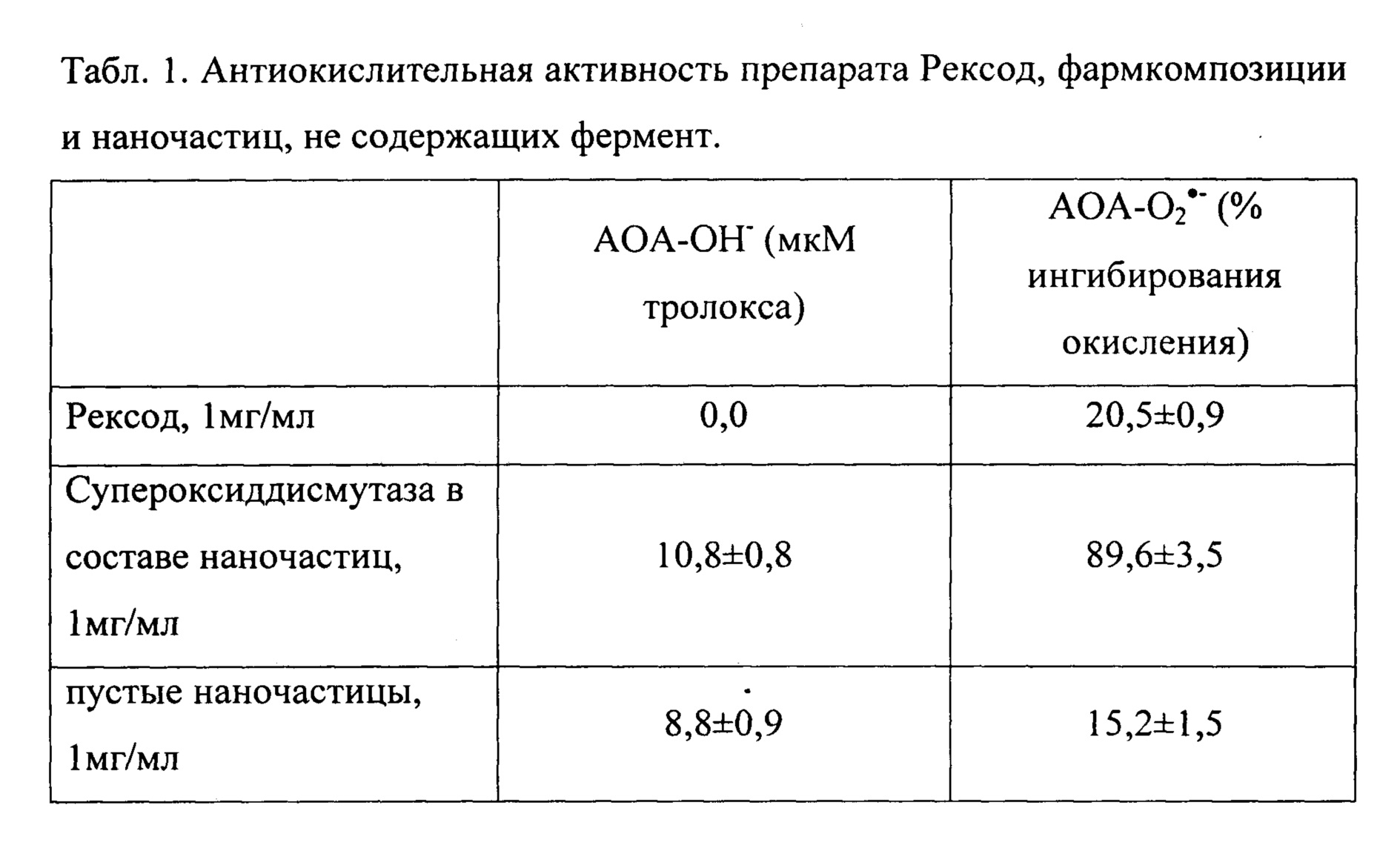
Изобретение поясняется табл. 1 «Антиокислительная активность препарата Рексод, фармкомпозиции и наночастиц, не содержащих фермент», в которой продемонстрировано, что, в то время как препарат Рексод обладал антиокислительной активностью только в отношении супероксид-анион радикала, супероксиддисмутаза в составе предложенной фармкомпозиции проявляет также активность по отношению к гидроксильному радикалу. Показано, что полимеры, образующие наночастицы, проявляют собственную антиокислительную активность по отношению к обоим активным формам кислорода. Однако антиокислительная активность фармкомпозиции даже выше, чем суммарная активность супероксиддисмутазы и пустых частиц. В таблице 1 также продемонстрировано, что антиокислительная активность заявляемой фармкомпозиции существенно выше, чем препарата «Рексод».
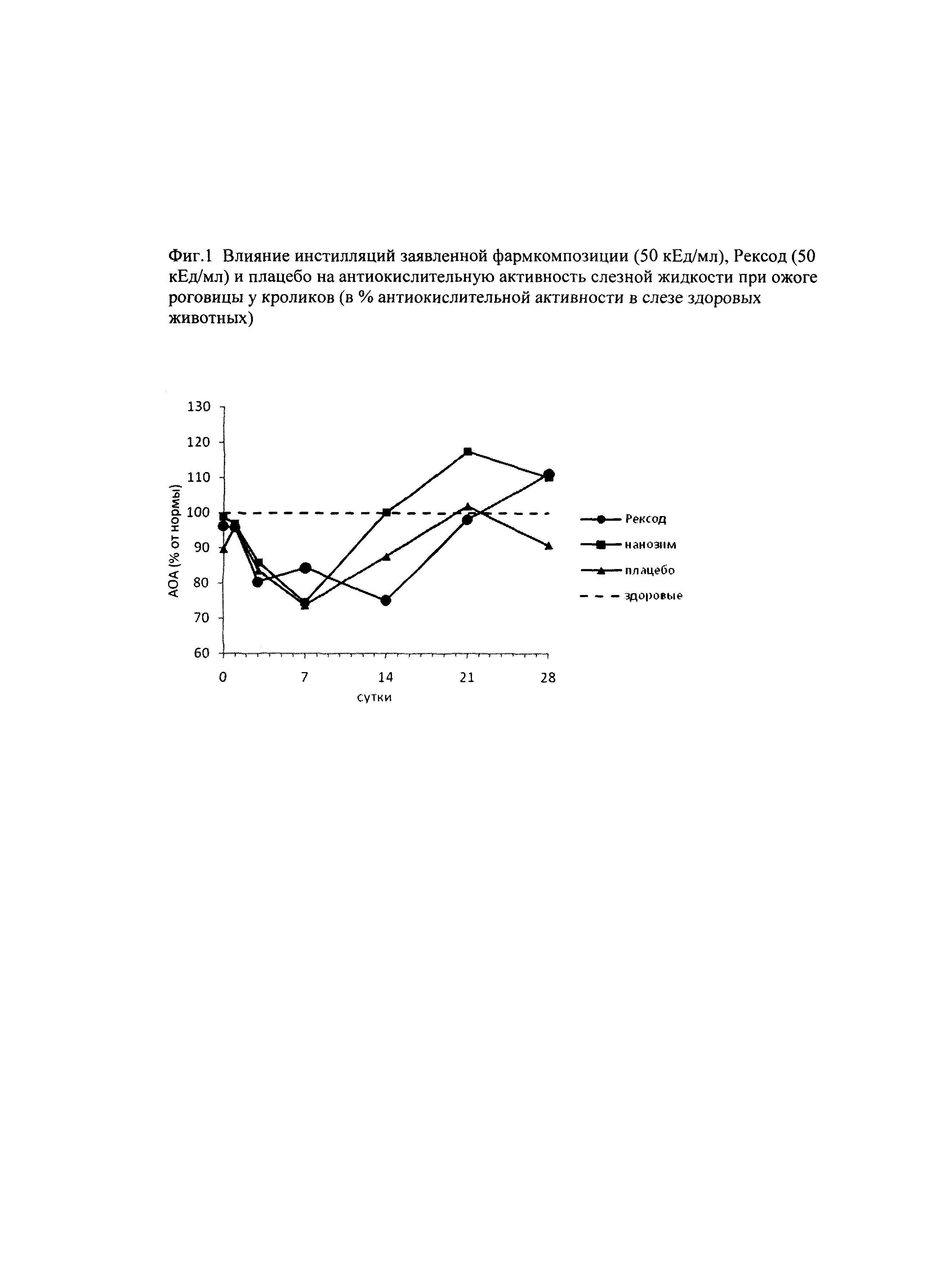
Изобретение поясняется также фиг. 1, на которой продемонстрировано влияние супероксиддисмутазы (препарата Рексод) и заявленной фармацевтической композиции на антиокислительную активность в слезной жидкости кроликов (кролик №2 - нелеченый; кролик №6 - леченый супероксиддисмутазой; кролик №12 - леченый заявленной фармкомпозицией) после щелочного ожога роговицы. Антиокислительную активность в слезе определяли хемилюминесцентным методом в модельной системе гемоглобин - перекись водорода - люминол, в которой в качестве субстрата окисления выступает люминол. Величину антиокислительной активности выражали в эквивалентах тролокса, для чего строили калибровочную кривую зависимости латентного периода хемилюминесценции от концентрации тролокса по [Владимиров Ю.А. Свободные радикалы и антиоксиданты (1998) Вестн. РАМН, №7, 43-51]. Статистическую обработку результатов производили с помощью U-критерия Манна-Уитни. Важно, что, в отличие от раствора супероксиддисмутазы, сниженный в острый период ожогового процесса антиоксидантный потенциал слезы восстанавливается под действием заявленной фармкомпозиции в более ранние сроки (14-е сутки против 21) и в дальнейшем остается выше, чем у нелеченых животных. Это свидетельствует о том, что супероксиддисмутаза в составе фармкомпозиции более эффективно подавляет окислительный стресс, который является причиной усиления образования провоспалительных метаболитов и повреждения структурных и функциональных компонентов тканей глаза.
Приготовление фармацевтической композиции по изобретению: Фармацевтическая композиция содержит в качестве действующего вещества эффективное количество супероксиддисмутазы, включенной в наночастицы на основе сшитых протамина и блок-сополимера поли(глутаминовой кислоты) и полиэтиленгликоля по методу [Патент RU 2575836; Заявка RU 2013 153 179] в виде суспензии в водном буферном растворе, изотоническом физиологическому раствору с рН 7,4, который может также содержать целевые добавки и лекарственные средства. Раствор имеет бесцветную окраску.
Глазные капли получали следующим образом: Переводили полученную суспензию наночастиц в необходимый водный раствор путем многократного разбавления и центрифугирования на мембранных системах 50 кДа, перед использованием проводили стерильную фильтрацию раствора через фильтры «Millipor» 0,22 мкм.
Соответствие состава проверяли по:
1. Активности супероксиддисмутазы, определяемой по методу [Костюк В.А., Потапович А.И., Ковалева Ж.В. Простой и чувствительный метод определения активности супероксиддисмутазы, основанный на реакции окисления кверцетина (1990) Вопр. Мед. Химии, 36, 88-91]. Метод основан на определении степени торможения реакции окисления кверцетина в присутствии супероксиддисмутазы. За единицу активности супероксиддисмутазы принимали такое количество фермента в 1 мл реакционной смеси, которое вызывает ингибирование реакции окисления кверцетина на 50%.
2. Значению рН раствора (7,4), которое проверяли с использованием рН-метра.
3. Электрофоретической подвижности препарата в условиях неденатурирующего электрофореза в 10% полиакриламидном геле по методу [Laemmli U.K. Cleavage of structural proteins during the assembly of the head of Bacteriophage T4 (1970) Nature, 227, 680-685]. Для окрашивания белков использовали Кумасси бриллиантовый синий R-250.
4. Наночастицы в композиции характеризовали методом анализа траектории наночастиц. Этот метод позволяет определять как размер, так и концентрацию частиц.
Сравнительное изучение терапевтического действия супероксиддисмутазы в растворе и супероксиддисмутазы в составе наночастиц проводили на моделях воспалительного процесса, сопровождающегося окислительным стрессом, во внутренних (иммуногенный увеит - воспаление сосудистой оболочки глаза) и внешних (ожог роговицы) структурах глаза кроликов. При увейте имеется высокая степень корреляции между выраженностью воспаления и окислительным стрессом. Показано, что супероксиддисмутаза в значительной степени снижает уровень окислительного стресса во внутренних средах глаза при увейте [Чеснокова Н.Б., Нероев В.В., Безнос О.В., Бейшенова Г.А., Никольская И.И., Кост О.А., Биневский П.В., Шехтер А.Б. Окислительный стресс при увейте и его коррекция антиоксидантным ферментом супероксиддисмутазой (2014) Вестн. Офтальмол., 30, 30-36]. При ожоге глаза развивается воспалительный процесс, сопровождающийся значительным снижением антиоксидантного потенциала, что свидетельствует об истощении собственной антиоксидантной системы при окислительном стрессе [Гулидова О.В., Любицкий О.Б., Клебанов Г.И., Чеснокова Н.Б. Изменение антиокислительной активности слезной жидкости при экспериментальной ожоговой болезни глаз (1999) Бюл. Эксп. Биол. Мед., 128, 571-574].
В эксперименте были задействованы 73 кролика породы шиншилла массой 2-2,5 кг. Работа с экспериментальными животными проводилась в соответствии с положениями Хельсинской декларации. Животные находились в стандартных условиях содержания. Лабораторные животные до начала исследования содержались 14 дней для адаптации. Во время этого периода у животных контролировали признаки отклонения от состояния здоровья. Каждому животному был присвоен индивидуальный номер (в соответствии с номером группы и порядковым номером). В экспериментальные группы случайным образом были отобраны животные без внешних отклонений.
Моделирование экспериментального увеита.
При исследовании заявленной фармкомпозиции на течение экспериментального увеита ожоговой болезни глаз у кроликов было задействовано 38 животных (76 глаз) У животных воспроизводили иммуногенный увеит по методике [Нероев В.В., Давыдова Г.А., Перова Т.С. Моделирование иммуногенного увеита у кроликов (2006) Бюлл. Эксперимент. Биол. Мед., 142, 598-600]. Каждому кролику двукратно вводили нормальную лошадиную сыворотку, сначала подкожно в количестве 5 мл, затем на 10 сутки после подкожной инъекции в оба глаза интравитреально вводили разрешающую дозу сыворотки в количестве 70 мкл.
Для лечения использовали препарат Рексод-ОФ (ООО "НПП Ферментные технологии", Россия), представляющий собой рекомбинантную супероксиддисмутазу 1 человека (400 кЕД в 1 мг), и заявленную фармкомпозицию с равной активностью фермента в качестве монотерапии. Первая группа получала инстилляции Рексод, вторая группа получала инстилляции заявленной фармкомпозиции, третья группа получала плацебо, четвертая группа - интактные кролики (для контроля показателей). Препараты вводили по 3 раза в день по 30 мкл в оба глаза в течение 8 дней.
Клинические признаки воспаления оценивали путем последовательного анализа данных наружного осмотра глаза, биомикроскопии с помощью щелевой лампы, офтальмоскопии. Оценку клинических проявлений увеита (гиперемия конъюнктивы, количество отделяемого, отек век, роговицы и радужки, содержание фибрина и общего белка во влаге передней камеры) проводили в условных баллах по четырехбалльной шкале: отсутствие признака - 0, проявления слабой степени - 1, средней - 2, сильной - 3.
Пример 1
Кроликам с иммуногенным увеитом проводили инстилляции растворов супероксиддисмутазы (препарат Рексод) в концентрации 50 кЕд/мл в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl, суспензии заявленной фармкомпозиции с концентрацией наночастиц 0,5⋅1014 частиц/мл и с такой же активностью фермента в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl, а также плацебо - фосфатный буфер, рН 7,4, содержащий 0,15 М NaCl.
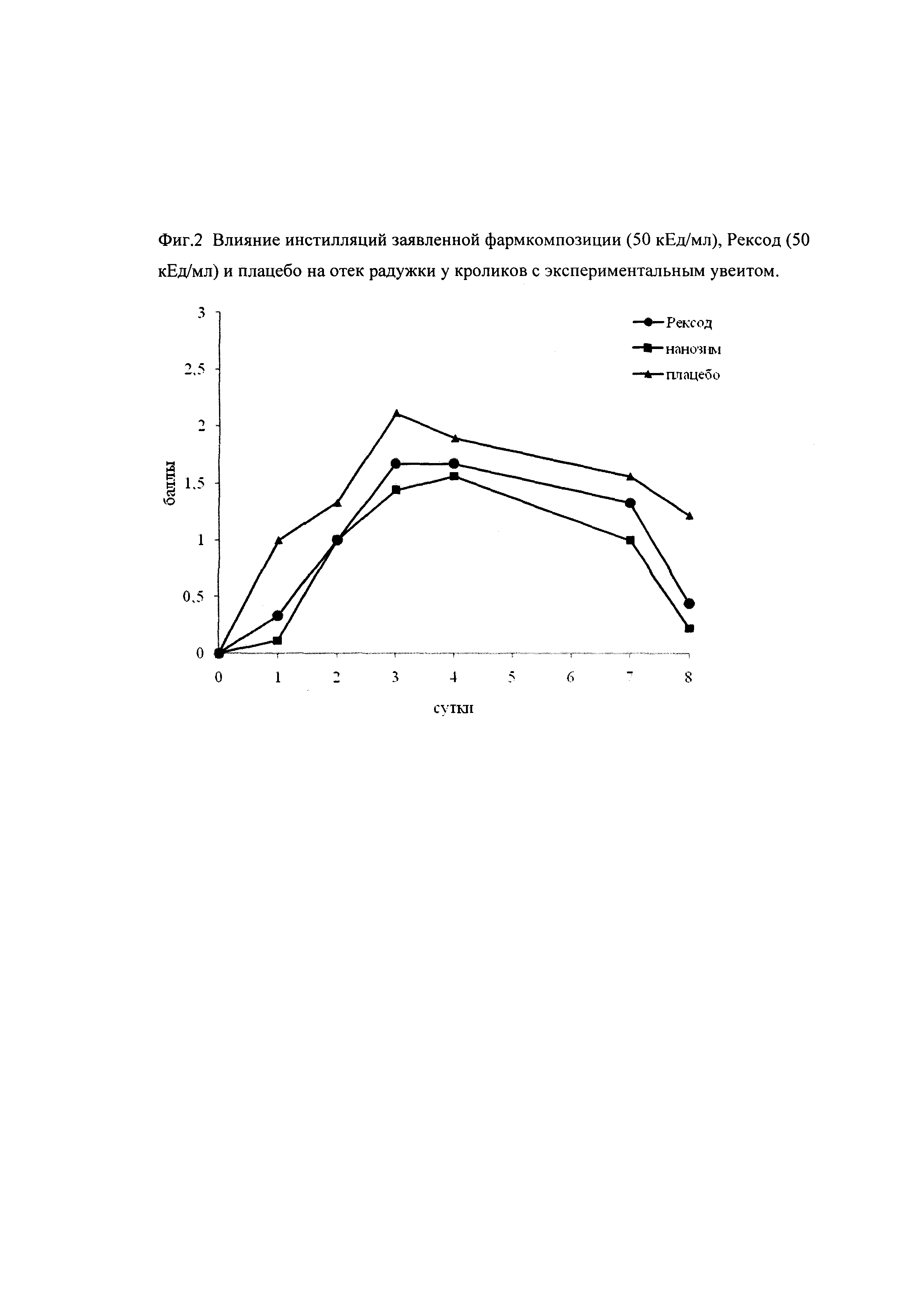
Оценивали отек радужки в разные дни после инициирования увеита.
Данные представлены на фиг. 2. Отек радужки в группе, получавшей инстилляции заявленной фармкомпозицией, снижался быстрее, чем в других группах.
Пример 2
Кроликам с иммуногенным увеитом проводили инстилляции растворов супероксиддисмутазы (препарат Рексод) в концентрации 50 кЕд/мл в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl и 0,3 мг/мл бензалконий хлорида, суспензии заявленной фармкомпозиции с концентрацией наночастиц 0,5⋅1014 частиц/мл и с такой же активностью фермента в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl и 0,3 мг/мл бензалконий хлорида, а также плацебо - фосфатный буфер, рН 7,4, содержащий 0,15 М NaCl и 0,3 мг/мл бензалконий хлорида.
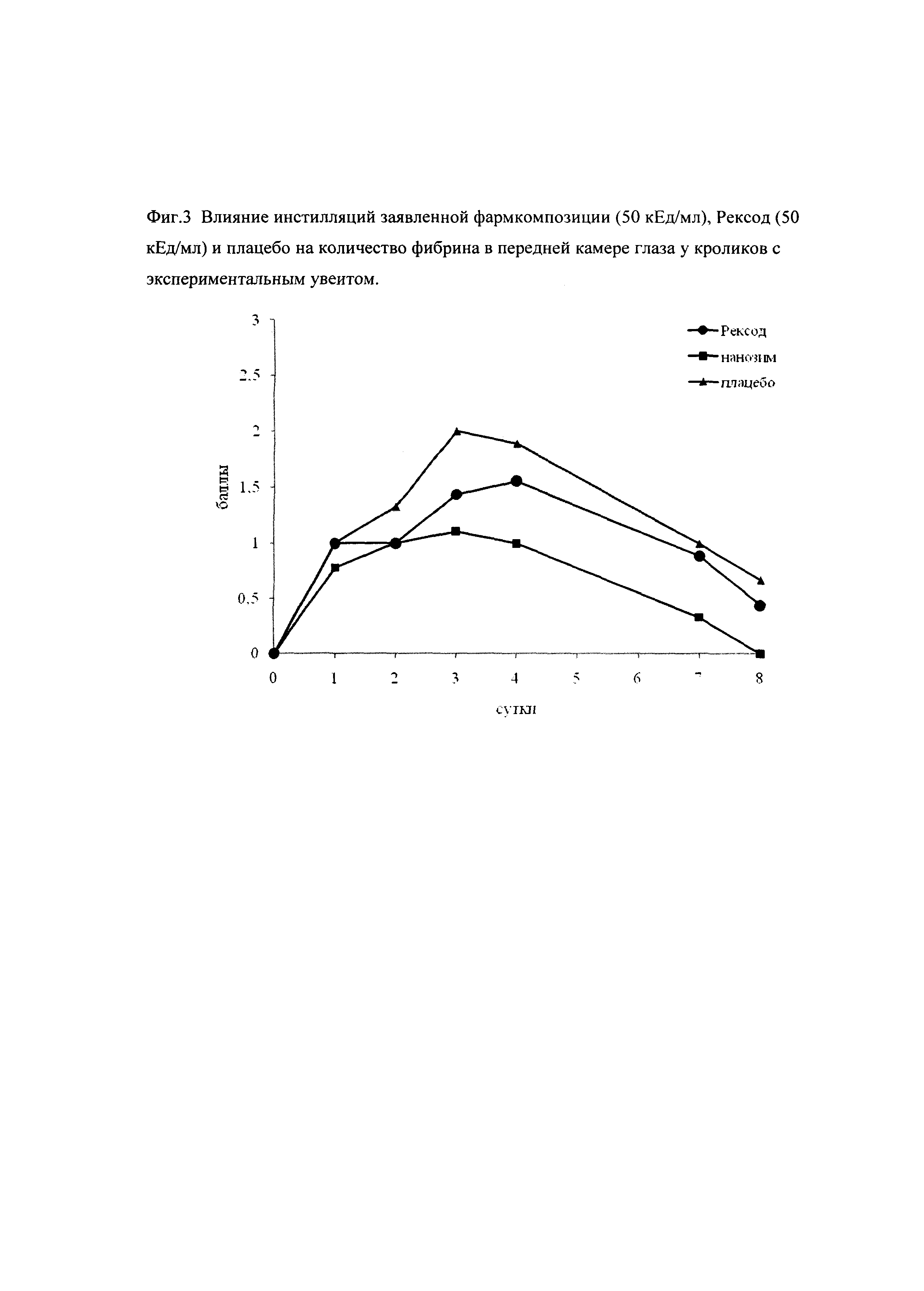
Оценивали содержание фибрина во внутренней камере глаза в разные дни после инициирования увеита.
Данные представлены на фиг. 3. Количество сгустков фибрина в передней камере у животных, получавших инстилляции заявленной композиции, было значительно меньше, чем у тех, что получали инстилляции раствора супероксиддисмутазы.
Пример 3
Кроликам с иммуногенным увеитом проводили инстилляции растворов супероксиддисмутазы (препарат Рексод) в концентрации 50 кЕд/мл в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl и 0,3 мг/мл бензалконий хлорида, суспензии заявленной фармкомпозиции с концентрацией наночастиц 0,5⋅1014 частиц/мл и с такой же активностью фермента в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl и 0,3 мг/мл бензалконий хлорида, а также плацебо - фосфатный буфер, рН 7,4, содержащий 0,15 M NaCl и 0,3 мг/мл бензалконий хлорида.
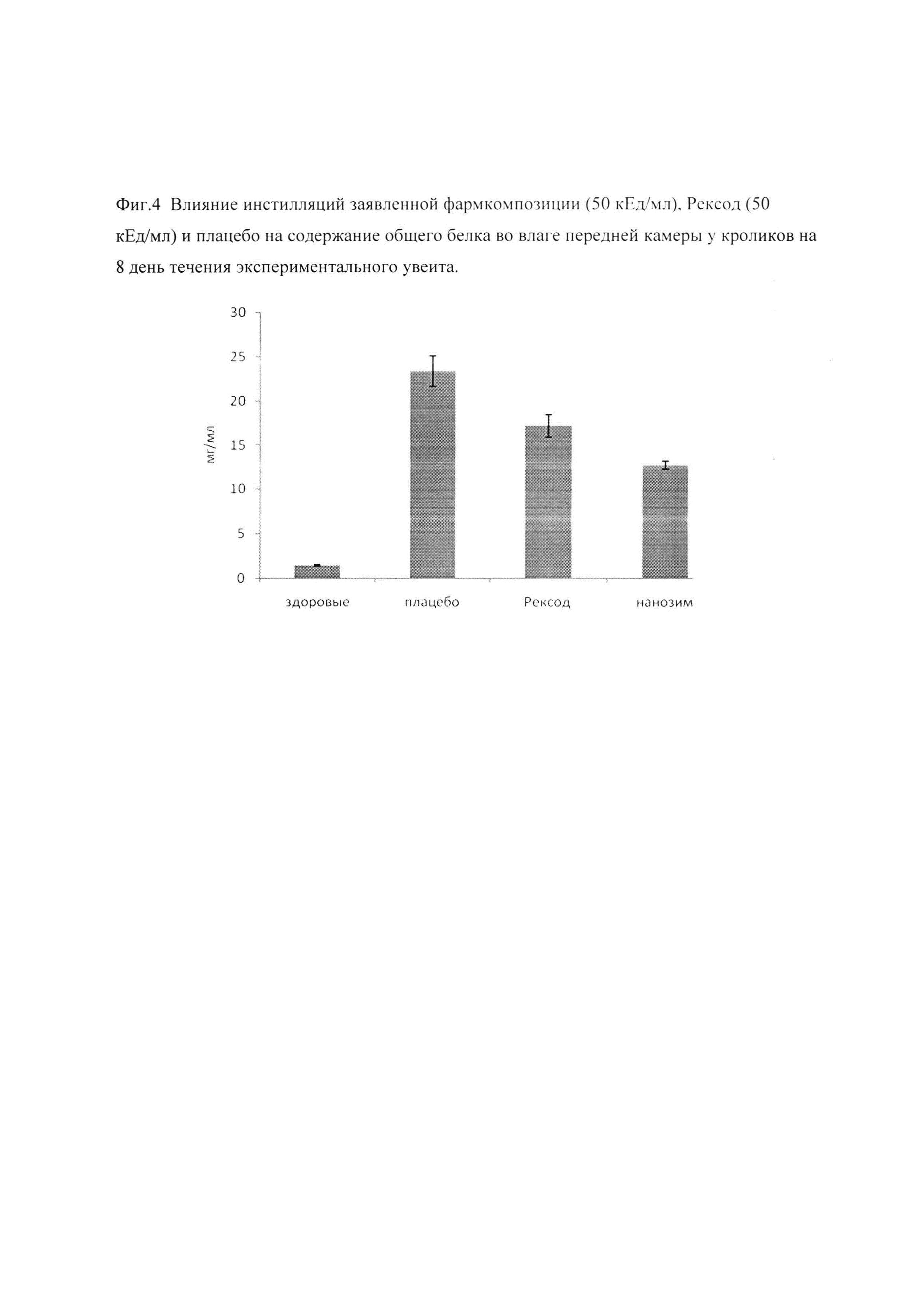
Оценивали общее содержание белка во внутренней камере глаза на 8 сутки течения увеита.
Данные представлены на фиг. 4. Общее содержание белка в острый период протекания увеита в передней камере у животных, получавших инстилляции заявленной композиции, было значительно меньше, чем у тех, что получали инстилляции раствора супероксиддисмутазы. Это свидетельствует о снижении проницаемости кровеносных сосудов увеального тракта и, следовательно, о меньшей выраженности воспаления
Моделирование ожога центральной части роговицы.
При моделировании дозированного по площади и глубине щелочного ожога роговицы использовали круги d=7 мм из тонкой хлопчатобумажной ткани, пропитанные 10% раствором NaOH, которые наносили на центральную область роговицы на 40 секунд, затем промывали глаза физиологическим раствором порциями по 20 мл. Для обезболивания использовали 2,5% раствор аминазина в сочетании с 0,5% раствором седуксена (1:1), который вводили подкожно (0,5 мл/кг веса). Одновременно проводили местную анестезию путем инстилляции на роговицу 0,5% раствора дикаина. В эксперименте использовали 35 кроликов (70 глаз).
Для лечения использовали препарат Рексод-ОФ и полученную нами фармкомпозицию на основе супероксиддисмутазы в составе наночастиц в качестве комплексной терапии с одновременным местным применением глазных капель на основе 2,5% раствора антибиотика левомицетина 5 раз в день. Первая группа получала инстилляции Рексод на фоне местного лечения левомицетином, вторая группа получала инстилляции заявленной фармкомпозиции на фоне местного лечения левомицетином, третья группа получала плацебо на фоне лечения левомицетином, четвертая группа - интактные кролики (для контроля показателей). Препараты вводили по 2 раза в день по 30 мкл в оба глаза в течение 21 дня.
Пример 4
Кроликам с щелочным ожогом роговицы проводили инстилляции растворов супероксиддисмутазы (препарат Рексод) в концентрации 500 кЕд/мл в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl, суспензии заявленной фармкомпозиции с концентрацией наночастиц 5⋅1014 частиц/мл и с такой же активностью фермента в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl, а также плацебо - фосфатный буфер, рН 7,4, содержащий 0,15 М NaCl. Все кролики получали также инстилляции раствора левомицетина.
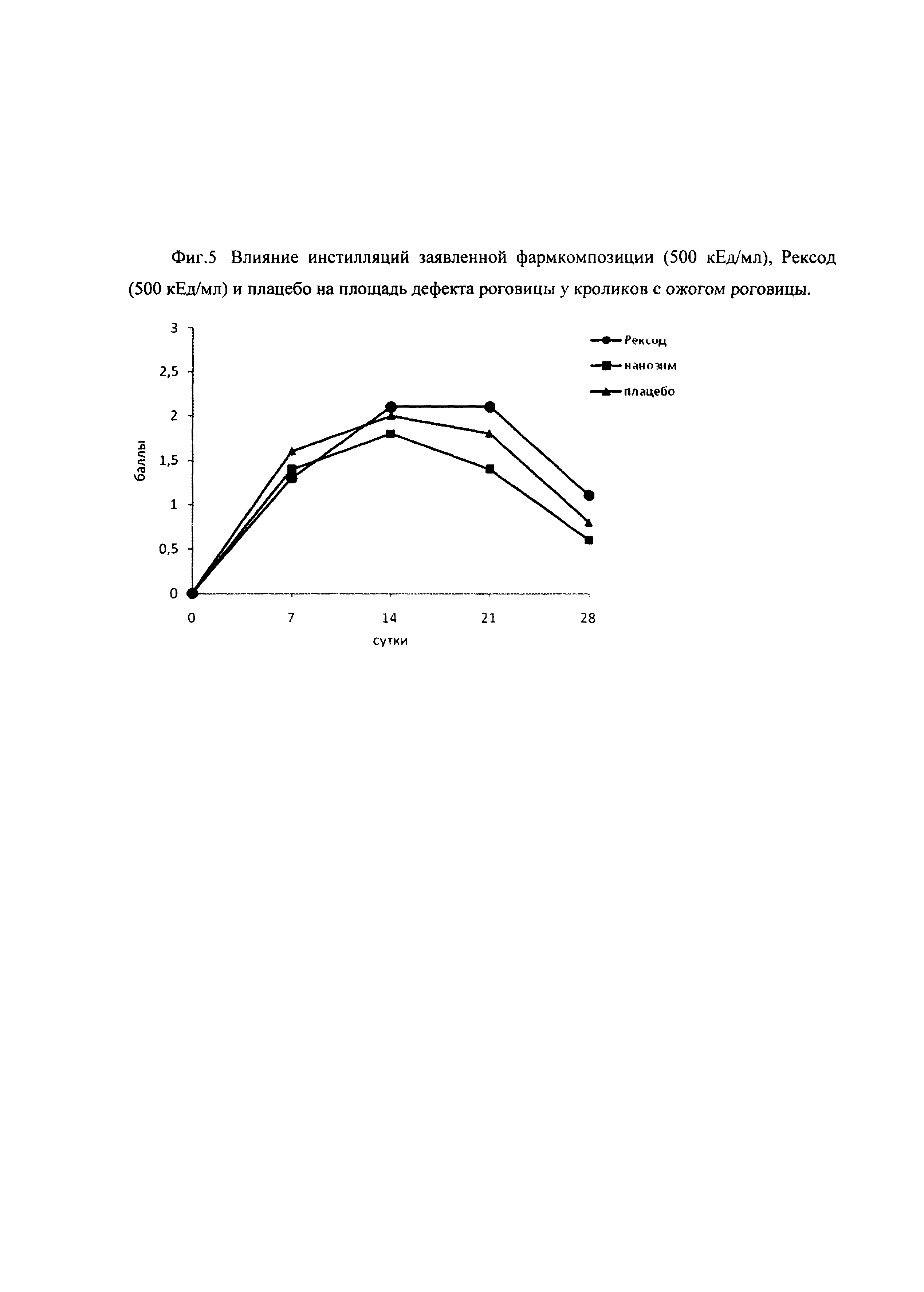
Оценивали площадь дефекта роговицы в разные дни после ожога.
Данные представлены на фиг. 5. Под действием заявленной фармкомпозиции площадь дефекта роговицы меньше и сокращается быстрее, чем при лечении раствором супероксиддисмутазы.
Пример 5
Кроликам с щелочным ожогом роговицы проводили инстилляции растворов супероксиддисмутазы (препарат Рексод) в концентрации 500 кЕд/мл в фосфатном буфере, рН 7,4, содержащем 0,15 М NaCl, суспензии заявленной фармкомпозиции с концентрацией наночастиц 5⋅1014 частиц/мл и с такой же активностью фермента в фосфатном буфере, рН 7,4, содержащем 0,15 M NaCl, а также плацебо - фосфатный буфер, рН 7,4, содержащий 0,15 М NaCl. Все кролики получали также инстилляции раствора левомицетина.
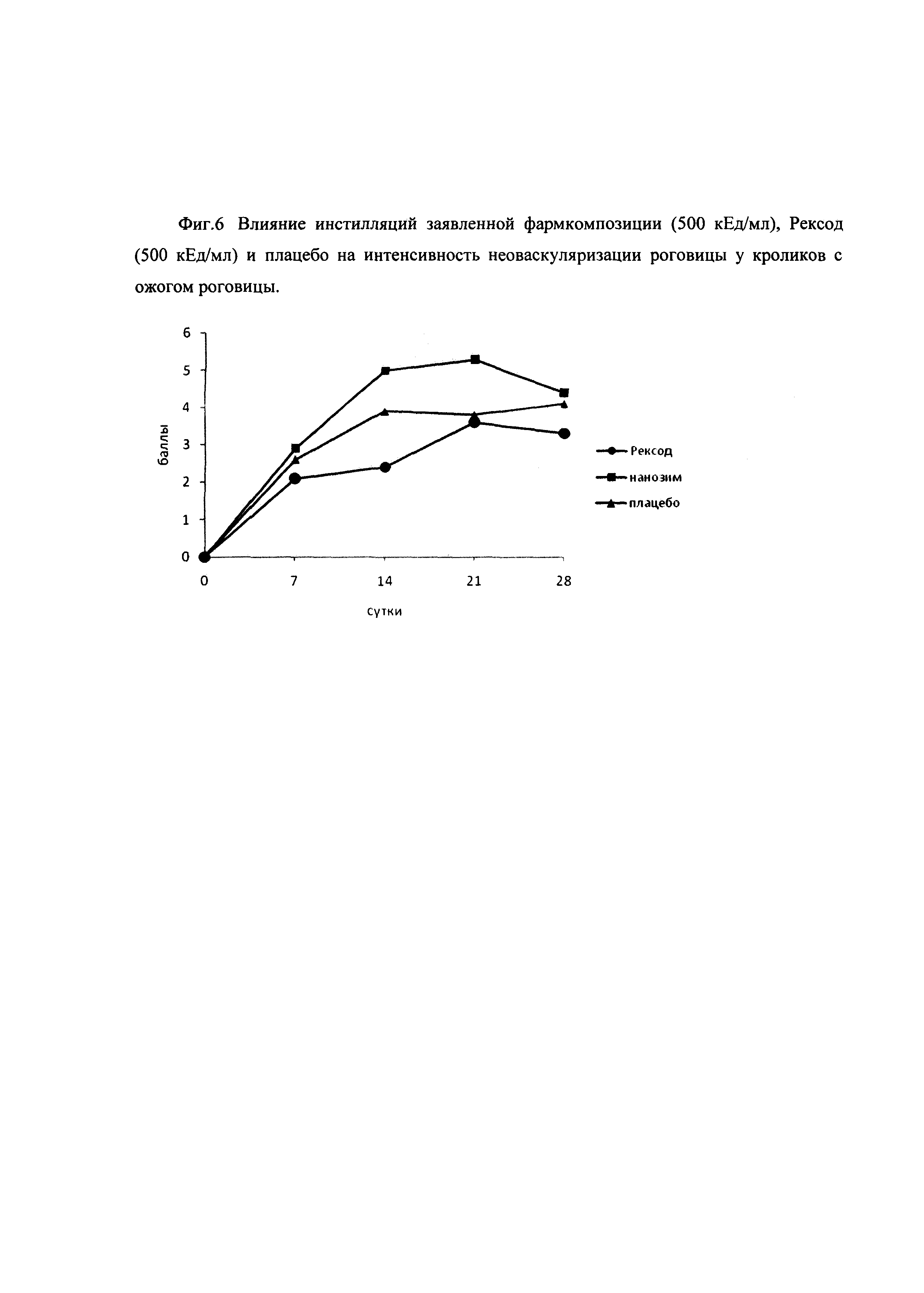
Оценивали интенсивность неоваскуляризации роговицы в разные дни после ожога.
Данные представлены на фиг. 6. Важно, что под действием предложенной фармкомпозиции происходит более быстрая и интенсивная неоваскуляризация роговицы в острой стадии процесса, что обеспечивает поступление в зону повреждения компонентов крови, необходимых для репарации ткани. Важно, что после отмены препарата происходит более быстрое запустевание новообразованных сосудов, что необходимо для образования менее грубой рубцовой ткани.
Таким образом, приведенные примеры свидетельствуют, что внедрение супероксиддисмутазы в наночастицы и местное применение заявленной фармацевтической композиции усиливает положительное действие фермента на течение воспалительного процесса как во внешних, так и во внутренних структурах глаза, а также более эффективно снижает количество свободных радикалов при воспалении.
Учитывая, что физиологические особенности глаза кролика и человека идентичны, данная фармацевтическая композиция может быть рекомендована к использованию как в ветеринарии, так и в клинике.
В данном исследовании мы сравнивали одинаковые режимы и дозы введения супероксиддисмутазы в растворе и супероксиддисмутазы в составе наночастиц. Полученные данные, свидетельствующие о большей терапевтической эффективности фермента в составе наночастиц, позволяют полагать, что его можно применять менее часто и в меньшей дозе, чем препарат в простом растворе. В то же время выбор дозы и режима применения должен зависеть от тяжести, локализации, характера течения патологии. Показанием к применению супероксиддисмутазы в составе предложенной фармкомпозиции является широкий круг глазных болезней, в патогенезе которых большую роль играет усиление процессов свободнорадикального окисления. Это воспалительные процессы любой этиологии и локализации, нейродегенеративные процессы в сетчатке, включая глаукому и возрастную дистрофию сетчатки, диабетическая ретинопатия, профилактика катаракты.