Результат интеллектуальной деятельности: Способ получения сорбентов для извлечения цезия из высокоминерализованных щелочных сред
Вид РИД
Изобретение
Изобретение относится к области радиохимии и радиоэкологии и может найти применение для получения сорбентов, предназначенных для дезактивации жидких щелочных сред.
Одним из наиболее опасных антропогенных радионуклидов является Cs-137 с периодом полураспада 30,17 лет. На его долю вместе со Sr-90 приходится около 97% проникающей радиации, при этом он обладает высокой миграционной способностью и с легкостью встраивается в биохимические циклы.
Очистка высокоминерализованных (Na+ 1,7-8,7 моль/дм3) и высокощелочных (pH 11,5-13,5) растворов от ионов Cs-137 требует от сорбентов высокой химической и механической стабильности в щелочной среде и одновременно высокой селективности к ионам Cs+ в присутствии значительной концентрации конкурирующих ионов (Na+, K+).
Известен описанный в патенте US 5441991, опубл. 1995.08.15, способ получения селективной к цезию катионообменной смолы, эффективно действующей в присутствии высоких концентраций ионов Na+, осуществляемый путем нейтрализации резорцина гидроксидом калия с последующей конденсацией/полимеризацией полученного промежуточного продукта с помощью формальдегида и термообработкой полученного полимера для формирования поперечных межмолекулярных связей, т.е. сшивки, и измельчением до частиц нужного размера. Однако известный способ является недостаточно технологичным, при этом полученный сорбент является ионитом с гелевой структурой. Такие иониты лишены свободного внутреннего объема в виде пор, поэтому ионный обмен возможен только в случае, когда полимер находится в набухшем состоянии. Изменение общего объема частиц ионита в процессе набухания приводит к их механическому разрушению. Кроме того, ионный обмен в отсутствии пор на ионитах гелевого типа лимитируется массопереносом внутри зерна смолы, что негативно сказывается на скорости сорбционного процесса с использованием сорбентов данного типа.
Известен также способ получения селективной резорцин-формальдегидной смолы, описанный в работе Egorin A.M. et al. «Effect of parameters of thermal treatment of resorcinol-formaldehyde resins on their chemical stability and Cs-137 uptake efficiency», Radioanal Nucl. Chem. 2015. P. 281-286, обеспечивающей эффективное извлечение радионуклида цезия в присутствии 3 моль/дм3 Na+ и химически устойчивого при pH 13. Синтез ионообменной резорцин-формальдегидной смолы проводят путем добавления 37% раствора формалина к водному раствору резорцина и гидроксида калия. В результате реакции полимеризации получают жесткий гель, который затем измельчают, отбирают фракцию 0,6-2,0 мм, промывают большим количеством дистиллированной воды, отфильтровывают, сушат до постоянного веса при 70-80°C и отверждают путем термообработки на воздухе в течение нескольких часов. Высокая температура отверждения (до 200°C) обеспечивает формирование высокосшитой полимерной матрицы, обладающей повышенной химической устойчивостью к воздействию щелочных растворов. Однако отсутствие свободного внутреннего порового пространства приводит к тому, что, во-первых, при набухании полимера происходит механическое разрушение зерна ионита, во-вторых за счет высокой сшивки полимерной сетки происходит снижение массопереноса внутри зерна смолы.
Наиболее близким к заявляемому является способ получения селективного сорбента для извлечения Cs-137 из щелочных растворов (RU 2551379, опубл. 2014.06.27), который предусматривает нейтрализацию резорцина раствором гидроксида щелочного металла, добавление формальдегида, введение в реакционную смесь мелкодисперсного карбоната кальция в количестве 10-40% в расчете на массу продукта с последующей олигомеризацией и поликонденсацией реакционной смеси, при этом процессы нейтрализации, олигомеризации и поликонденсации проводят в атмосфере инертного газа, поликонденсацию осуществляют диспергированием олигомерной смеси в слой несмешивающейся с ней жидкости, преимущественно трансформаторного масла, при температуре 105-120°C с получением продукта в виде сферических гранул. Готовый продукт отмывают от остатков трансформаторного масла бензолом в аппарате Сокслета. Затем удаляют карбонат кальция из полученных гранул кислотной обработкой, промывают и сушат полученный сорбент.
Известный способ обеспечивает получение устойчивого к окислению сорбента с наличием свободного внутреннего объема - порового пространства. Однако конденсация и отверждение смолы при температуре 105-120°C не обеспечивают достаточно высокой степени ее сшивки и, как результат, высокой осмотической стабильности, а также достаточно высокой химической и механической устойчивости и продолжительного срока службы в щелочной среде. Кроме того, проведение синтеза в атмосфере инертного газа, конденсация и гранулирование сорбента диспергированием в нагретом до температуры свыше 100°C трансформаторном масле с многоступенчатым отмыванием, требующим специального оборудования, усложняют известный способ и его аппаратурное оформление и удорожают получаемый сорбент.
Задачей изобретения является создание простого технологически и в аппаратурном оформлении способа получения селективного сорбента для извлечения цезия из высокосолевых щелочных растворов, характеризующегося высокой осмотической стабильностью, устойчивого к длительному воздействию щелочных сред.
Технический результат предлагаемого способа заключается в повышении осмотической стабильности, химической и механической устойчивости получаемых сорбентов при одновременном упрощении способа, его аппаратурного оформления и снижении стоимости производимой продукции.
Указанный технический результат достигают способом получения сорбентов для извлечения цезия из высокоминерализованных щелочных сред, включающим нейтрализацию резорцина раствором гидроксида щелочного металла, олигомеризацию путем добавления формальдегида, внесение в жидкую олигомерную массу тонкодисперсного карбоната кальция, поликонденсацию полученной олигомерной резорцин-формальдегидной массы при нагревании с получением жесткого геля, перевод последнего в дисперсную форму, отверждение, удаление карбоната кальция путем кислотной обработки, промывание и сушку, в котором, в отличие от известного, олигомеризацию проводят при температуре реакционной смеси 5-7°C и непрерывном перемешивании, олигомерную массу нагревают до температуры 50-55°C, обеспечивающей начало полимеризации и образования жесткого геля, после чего оставляют на 24 часа на воздухе при комнатной температуре, затем отверждают при температуре 190-210°C в течение 2-6 часов, отвержденный сорбент переводят в дисперсную форму путем механического измельчения с получением частиц размером 0,5-1,0 мм.
Наилучшим образом указанный технический результат достигают путем внесения в олигомерную массу карбоната кальция в количестве 8-12% по отношению к массе продукта поликонденсации.
Способ осуществляют следующим образом.
Резорцин переводят в солевую форму обработкой раствором гидроксида калия при молярном соотношении резорцина и KOH = 1:1. Затем осуществляют олигомеризацию полученного раствора резорцината калия добавлением избытка формальдегида (молярное соотношение резорцин: формальдегид = 1:4) при интенсивном перемешивании для равномерного протекания реакции и обязательном охлаждении реакционной смеси до 5-7°C для замедления процесса полимеризации. В полученную олигомерную массу при интенсивном перемешивании малыми порциями вносят тонкодисперсный порошок карбоната кальция CaCO3 в количестве 8-12% от массы продукта поликонденсации (ионообменной смолы). Не прекращая перемешивания, повышают температуру олигомерной массы до момента образования жесткого геля (50-55°C), который оставляют на 24 часа на воздухе при комнатной температуре.
После этого смолу отверждают на воздухе при 190-210°C в течение 2-6 часов, что обеспечивает протекание процесса поликонденсации с образованием высокосшитого полимера, а также удаление непрореагировавшего формальдегида.
Отвержденную смолу измельчают механическим способом, отбирают фракцию зернением 0,5-1,0 мм, которую последовательно промывают раствором кислоты (HNO3 c концентрацией не более 1 моль/л) для удаления частиц CaCO3 из объема смолы, затем раствором щелочи (0,5М NaOH) для отмывки ионита от непрореагировавших мономеров и олигомерных продуктов реакции. Обработка раствором HNO3 сопровождается выделением газообразного продукта в виде СО2, образующегося при растворении CaCO3, при этом нарушения фракционного состава смолы не происходит.
Перевод сорбента в рабочую H+-форму осуществляют путем обработки 1М раствором HNO3.
Величина поглощения Cs-137 из жидких щелочных сред резорцин-формальдегидными смолам (РФ-смолами) определяется двумя конкурирующими процессами: непосредственно ионным обменом и десорбцией, вызванной окислением и постепенным растворением полимера, которое визуально прослеживается по окрашиванию очищаемого раствора образующимися олигомерными продуктами. Поэтому эффективность извлечения Cs-137 из щелочных сред в значительной мере зависит от химической устойчивости получаемого сорбента и скорости его растворения, которые, в свою очередь, определяются способом его получения.
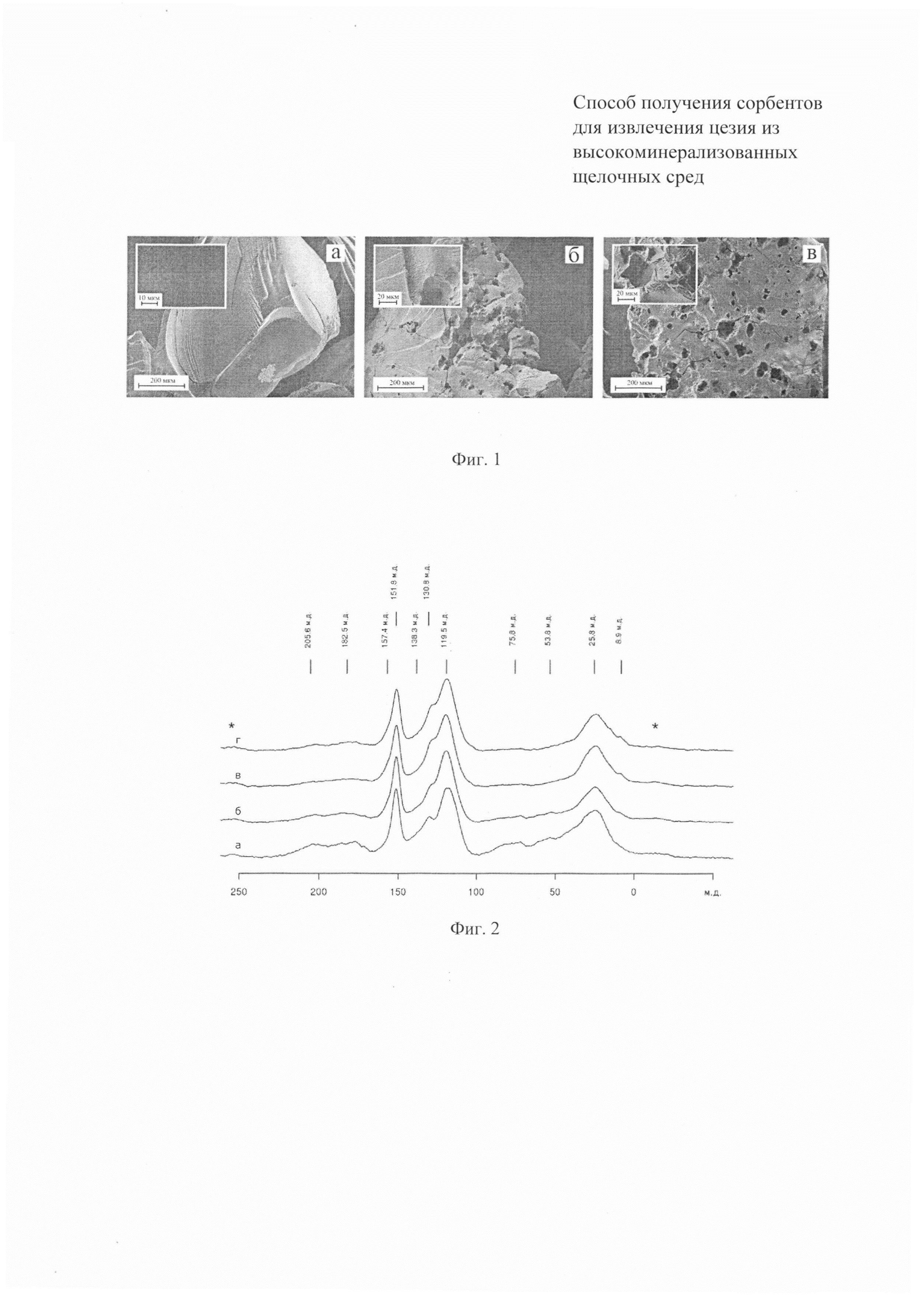
На фиг. 1 показаны СЭМ изображения поверхности сорбентов, полученных предлагаемым способом в различных условиях (а - образец получен без CaCO3; образцы б и в - при разном содержании CaCO3 в реакционной смеси, соответственно 10 и 25% по отношению к массе продукта поликонденсации). Четко видно различие в пористой структуре сорбента.
Эффективность извлечения Cs-137 РФ-смолами, а также их устойчивость в щелочных средах, зависят от полноты произошедшего в них процесса поликонденсации. Результаты испытания образцов показывают, что устойчивость и сорбционно-селективные характеристики РФ-смол изменяются в зависимости от температуры и продолжительности отверждения, при этом увеличение длительности и/или температуры отверждения приводит к протеканию более глубокого процесса поликонденсации.
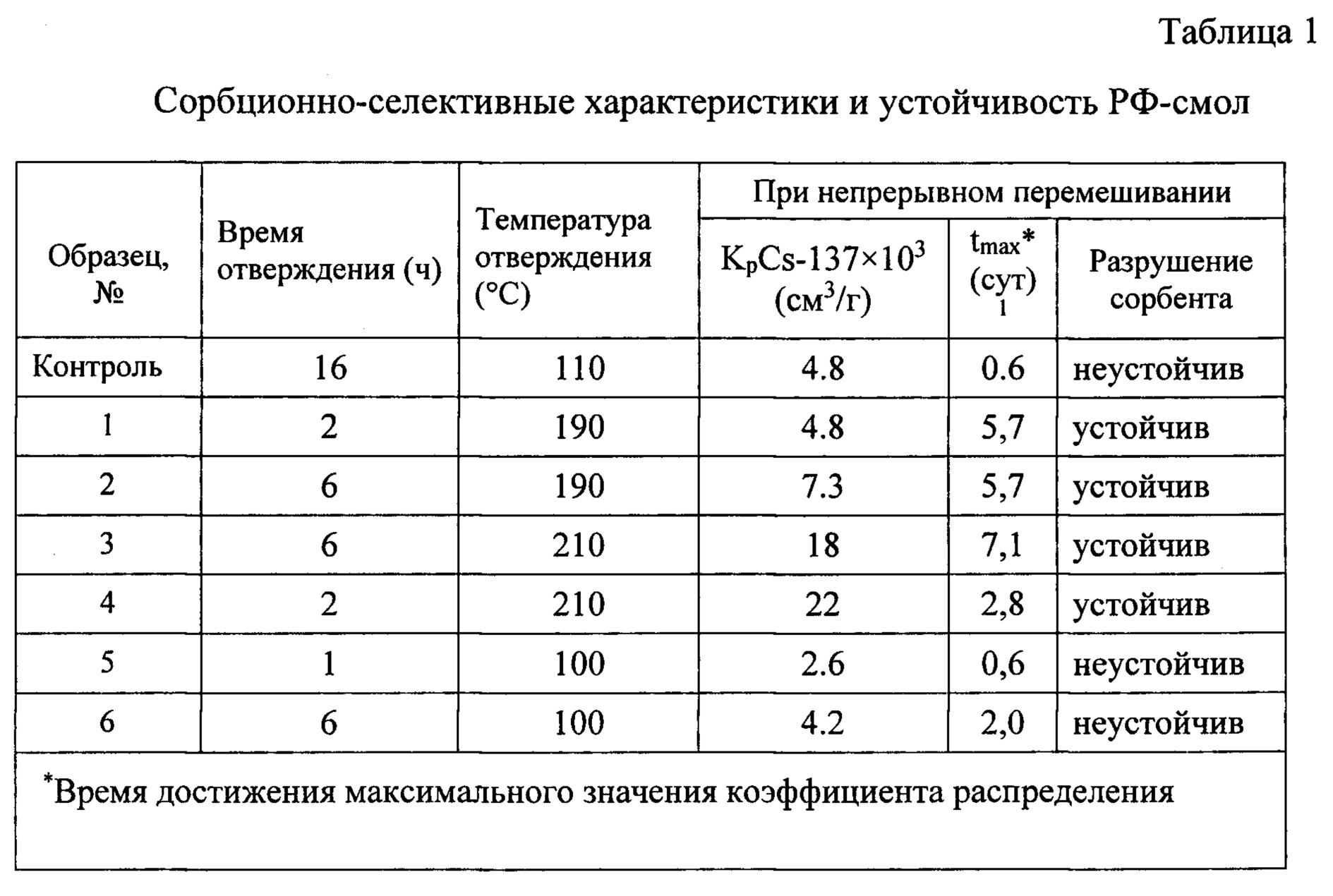
В таблице 1 представлены максимальные значения коэффициента распределения Cs-137, а также значения расчетной скорости разрушения некоторых образцов РФ-смол, свидетельствующие о том, что увеличение длительности и температуры отверждения приводит к увеличению химической стабильности и эффективности извлечения Cs-137.
Наибольшую химическую устойчивость при испытании в модельном щелочном растворе обнаруживают образцы, прогретые при температуре 190-210°C. Раствор, в который помещен обработанный таким образом сорбент, после 5-7 дней непрерывного перемешивания слегка окрашивается, однако десорбции Cs-137 не происходит.
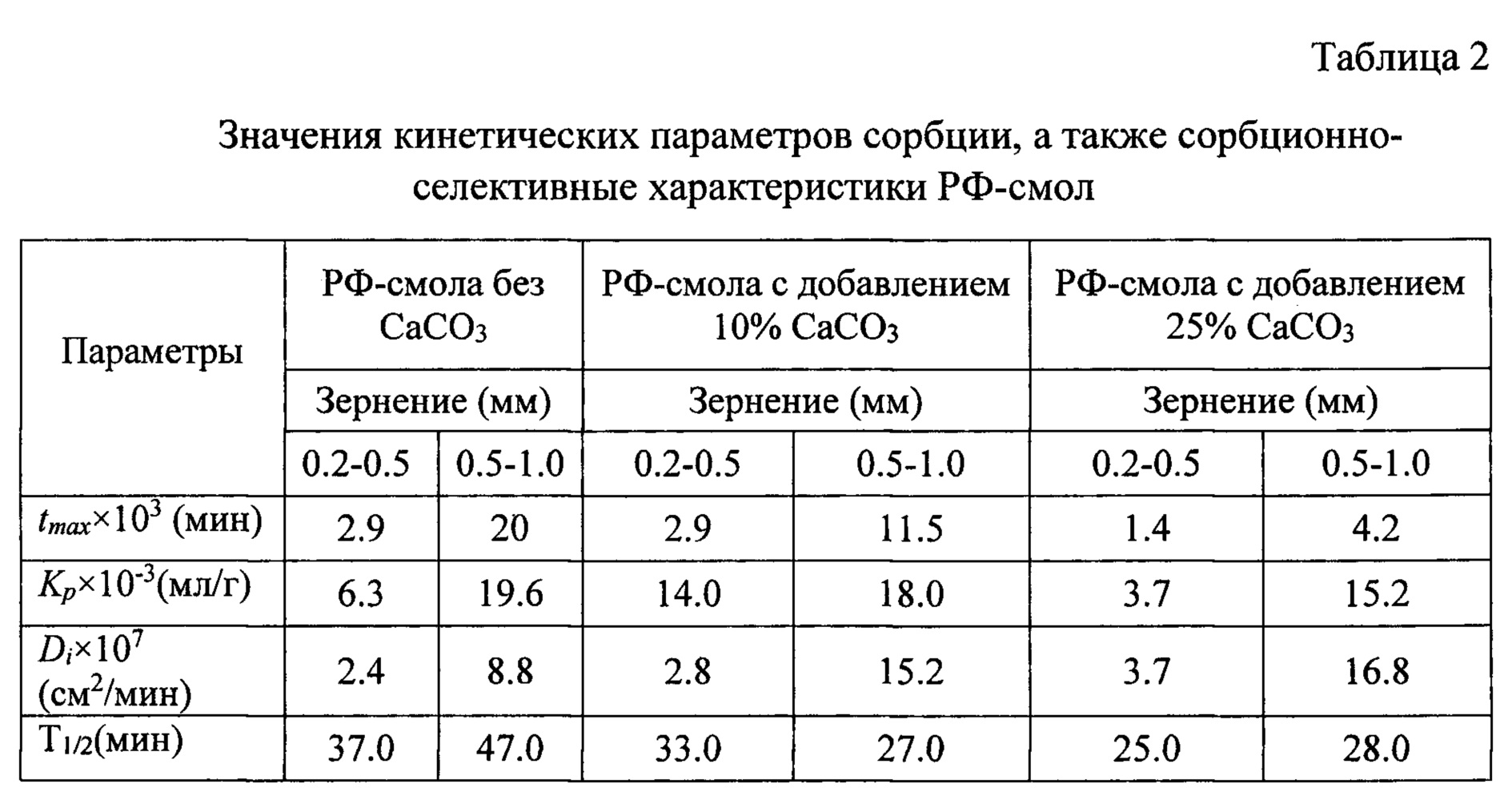
Рассчитанные на основании кинетических кривых сорбции Cs-137 в статических условиях коэффициенты внутренней диффузии (Di), величины времени полуобмена (t1/2), время достижения максимальной сорбции (tmax), после чего начинается разрушение сорбента, а также максимальные значения коэффициентов распределения Cs-137 приведены в Таблице 2.
Экспериментально подтверждено, что термообработка в заявленном интервале температур не приводит к заметному окислению резорцина до хиноновых структур и не вызывает термоокислительной деструкции полимера.
Полученные спектры ЯМР 13С синтезированных РФ-смол (фиг. 2) свидетельствуют, что с повышением температуры отверждения происходит снижение общего числа кислородсодержащих метилольных групп (ХС 53.8, 75.5 м.д.), при распаде которых образуются новые активные центры и формируются метиленовые мостиковые структуры. Увеличения интенсивности сигнала карбонильных групп (ХС 182.5 м.д.) при 190-210°C не происходит, что говорит об отсутствии окисления резорцинового кольца.
Таким образом, отверждение резорцин-формальдегидных смол в условиях предлагаемого способа приводит к более полному, в сравнении с известным способом, протеканию процесса поликонденсации с распадом кислородсодержащих метилольных групп.
Температура отверждения и продолжительность термообработки РФ-смолы в предлагаемом способе создают оптимальные условия для повышения степени сшивки полимерной сетки и обеспечивают увеличение устойчивости РФ-смолы к окислению растворенным кислородом при набухании в щелочных средах. При этом за счет повышения химической стабильности полученного сорбента увеличивается эффективность извлечения цезия-137 из высокоминерализованного щелочного раствора.
Изменение устойчивости полученных РФ-сорбентов связано также с различиями в их пористых характеристиках и дисперсности (крупности зернения).
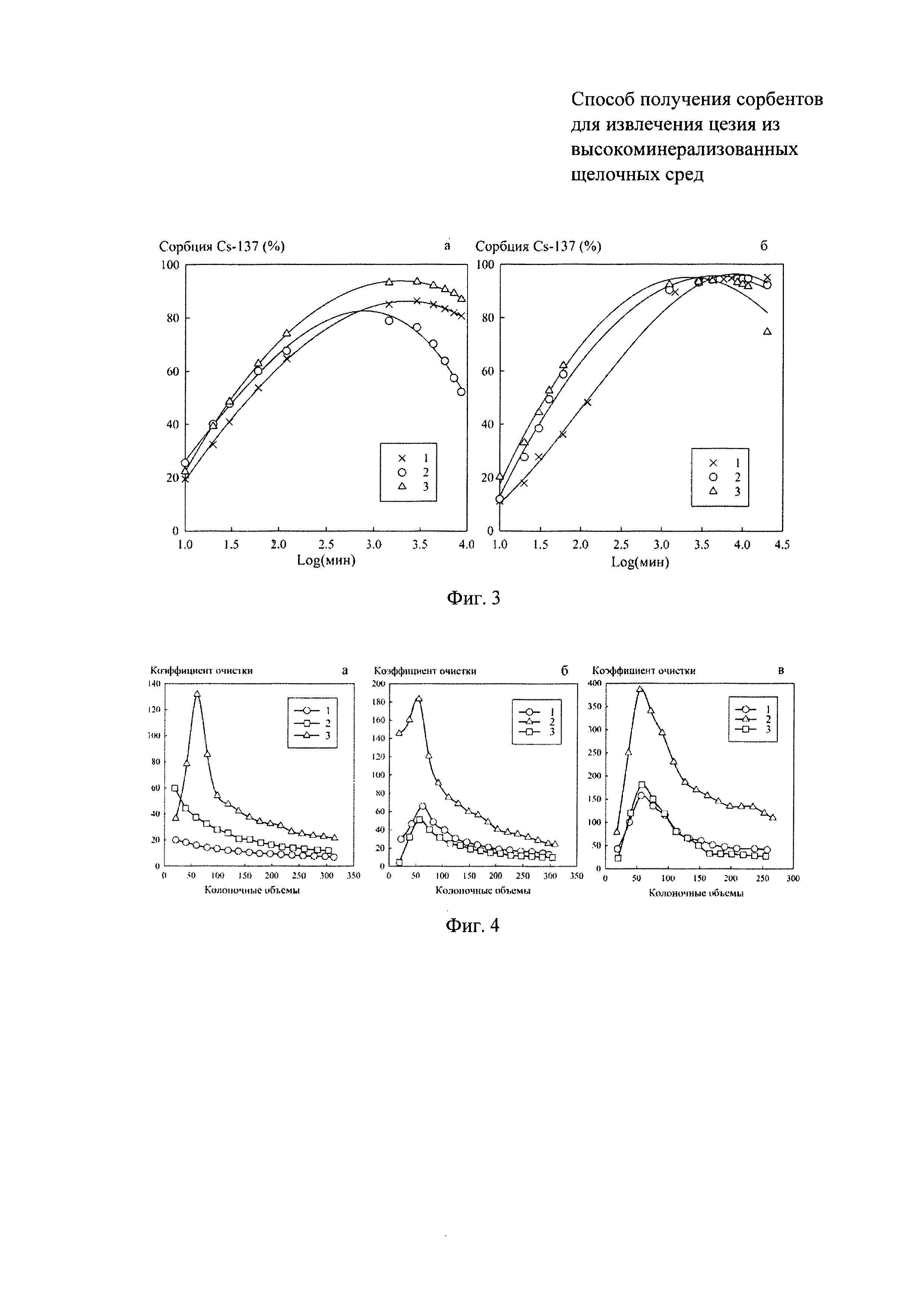
На фиг. 3 приведены кинетические кривые сорбции Cs-137 как функции зависимости сорбции Cs-137 (в %) от логарифма времени, полученные в статических условиях для сорбентов с различным зернением (3а - зернение 0,2-0,5 мм, 3б - зернение 0,5-1,0 мм) и различной пористостью (кривая 1 - РФ-смола без пор (CaCO3 не вносили); кривая 2 - РФ-смола, при синтезе которой было внесено 10% CaCO3 от массы продукта поликонденсации; кривая 3 - РФ-смола, при синтезе которой было внесено 25% CaCO3 от массы продукта поликонденсации).
Кривые на фиг. 3а достаточно быстро проходят через максимум, что свидетельствует о химической деструкции синтезированных смол в ходе сорбции Cs-137 из агрессивной щелочной среды. Химическая деструкция с мелкозернистых (0,2-0,5 мм) ионообменных смол подтверждается появлением интенсивного желто-коричневого окрашивания у контактирующих с ними модельных растворов. Иониты с зерном крупнее 0,5 мм являются химически устойчивыми (фиг. 3б - размер зерен 0,5-1,0 мм), что объясняется снижением скорости их растворения. Одновременно поведение кривых на фиг. 3 показывает, что наиболее устойчивыми к воздействию щелочных растворов являются пористые иониты, синтезированные из реакционной смеси, содержащей CaCO3 в количестве 10% от массы продукта поликонденсации (кривая 2 на фиг. 3б).
Повышение устойчивости ионитов с увеличением крупности зернения подтверждается значениями времени достижения максимальной сорбции (tmax), после которой начинается разрушение РФ-смолы (Таблица 2).
При длительном контакте с высокоминерализованным щелочным раствором РФ-сорбенты постепенно разрушаются, при этом скорость их разрушения напрямую связана с размером зерна, с уменьшением которого химическая стабильность сорбентов понижается и, в результате, ухудшаются их сорбционно-селективные характеристики,
Согласно предлагаемому способу, получают РФ-сорбент с зернением не менее 0,5 мм (0,5-1,0 мм); более мелкие фракции непригодны для использования в сильнощелочных средах в виду низкой химической стабильности.
Введение CaCO3 в состав ионообменных смол с последующим его удалением позволяет в значительной мере повысить кинетические характеристики синтезируемых сорбентов. Однако, экспериментально установленное оптимальное количество вносимого CaCO3 составляет 8-12% от массы продукта поликонденсации, при превышении которого вследствие избыточного увеличения поверхности зерен сорбента интенсифицируются процессы его растворения и снижается химическая устойчивость сорбента в щелочных средах.
Изменение коэффициента сорбции при извлечении Cs-137 из модельного раствора в динамических условиях с использованием РФ-сорбента с зернением 0,5-1,0 мм приведены на фиг. 4 (а, б, в - первый, второй и третий сорбционные циклы, соответственно). В каждом цикле кривая 1 соответствует беспористому сорбенту, синтезированному из состава, не содержащего CaCO3; кривая 2 - сорбенту, синтезированному из реакционной смеси, содержащей карбонат кальция в количестве 10% от массы продукта поликонденсации; кривая 3 - сорбенту, синтезированному из состава, содержащего 25 масс. % карбоната кальция. Во всех трех циклах наилучшие сорбционные характеристики показывает образец, обладающий оптимальной пористостью, который получен из состава, включающего 10 масс. % CaCO3. Наименьшей стабильностью обладает образец, полученный из состава, содержащего 25 масс. % CaCO3, характеризующийся избыточной пористостью.
Преимущества получаемых предлагаемым способом сорбентов четко проявляются при эксплуатации в динамических условиях, когда требуется высокая эффективность извлечения Cs-137 из жидких сред при повышенных скоростях перколяции очищаемого раствора через сорбент.
Примеры конкретного осуществления способа.
Оценку сорбционных характеристик полученных сорбентов проводили с использованием модельного раствора следующего состава: NaNO3 - 1,25 моль/л, NaOH - 0,75 моль/л. Кинетические характеристики ионообменного процесса оценивали по убыли гамма-активности модельного раствора, меченного радионуклидом Cs-137 (500-1000 Бк/мл).
Содержание Cs-137 в модельном растворе определяли на гамма-спектрометре МКС АТ-1315, производства фирмы «Атомтех», Республика Беларусь. Полученный сорбент приводили в контакт с модельным раствором при непрерывном перемешивании на орбитальном шейкере с амплитудой 10 мм и скоростью вращения 120 об/мин, m/V = 0,001 г/мл. Через определенные промежутки времени отбирали аликвоты раствора и определяли остаточную активность.
Спектры ЯМР 13С были записаны на многоядерном твердотельном спектрометре BrukerAvance AV-300.
Морфологию поверхности синтезированных сорбентов изучали с помощью сканирующей электронной микроскопии (SEM) на приборе Carl Zeiss Crossbeam 1540 ХВ (Германия).
Пример 1
Резорцин массой 5,5 г. (0,05 моль) и КОН массой 2,8 г. (0,05 моль) растворяли в 10 мл воды. К полученному раствору, при интенсивном перемешивании и охлаждении постепенно приливали 15 мл формалина. После чего в олигомерную смесь маленькими порциями вносили 3 тонкодисперсного CaCO3 (10 масс. %от массы продукта поликонденсации). Затем постепенно повышали температуру реакционной смеси до момента образования жесткого геля (50-55°C), который оставляли на воздухе. Спустя сутки смолу отверждали при 210°C в течение 2 часов в атмосфере воздуха (в сушильном шкафу). После отверждения смолу механически измельчали и отбирали фракцию зернением 0,5-1,0 мм, затем последовательно промывали 0,5М раствором HNO3 и 1М раствором NaOH. В рабочее состояние (Н+-форму) сорбент переводили путем обработки 1Н раствором HNO3.
Эффективность извлечения микроколичества радионуклида Cs-137 из модельного раствора в статических условиях оценивали по значению величины сорбции (в %), а также коэффициенту распределения (Кр).
Сравнение химической устойчивости непористой и пористых ионообменных смол оценивали по кривым зависимости величины сорбции от времени контакта с модельным раствором состава Na+ - 2 моль/л, NO3- - 1,25 моль/л, ОН- - 0,75 моль/л (фиг. 3). Максимум полученных кривых соответствует времени tmax, за которое достигается максимальное значение сорбции, после чего начинается разрушение ионита, сопровождающееся процессом десорбции радионуклида Cs-137 и снижением величины сорбции.
Величину сорбции Cs-137 из модельного раствора рассчитывали по формуле:
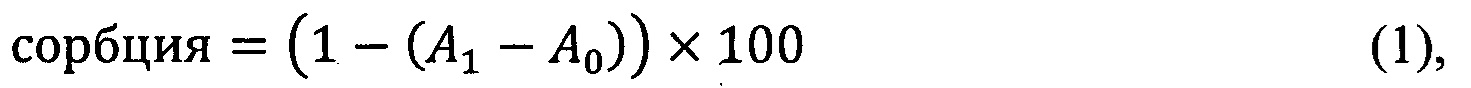
где А0 - начальная удельная активность модельного раствора (Бк/мл),
А1 - удельная активность раствора через интервал времени t (Бк/мл).
Устойчивость ионитов в зависимости от длительности и температуры отверждения оценивали по кривым зависимости величины сорбции от времени контакта с модельным раствором состава Na+ - 3,05 моль/л, NO3- - 2,95 моль/л, та ОН- - 0,1 моль/л. По полученным кривым оценивали стабильность сорбентов: если за установленное время (6 дней) десорбция Cs-137 с выходом значения сорбции на постоянный максимум не обнаруживалась, сорбент считали химически устойчивым, в противном случае его относили к химически неустойчивым. Для каждого значения tmax рассчитывали величину коэффициента распределения Кр (Таблица 1) по формуле:

где А0 - начальная удельная активность модельного раствора (Бк/мл),
A1 - удельная активность раствора через интервал времени t, (Бк/мл).
Для определения лимитирующей стадии и оценки кинетических параметров ионообменного процесса (Таблица 2) было использовано уравнение Бойда-Адамсона, позволяющее рассчитать эффективный коэффициент диффузии (Di):

где В - константа скорости диффузии (с-1), которая описывается уравнением:

где Di - эффективный коэффициент диффузии (см2/мин), r - радиус зерна ионита (см).
Зависимость Bt как математической функции от F описывается уравнением:
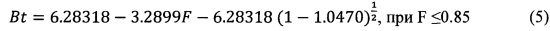
и приведена в виде в виде табличных значений в работе Е. Reichenberg D. Properties of Ion-Exchange Resins in Relation to their Structure. III. Kinetics of Exchange // Journal of the American Chemical Society. 1953. Vol. 75.
Величину В определяли, как тангенс угла наклона прямой, полученной при аппроксимации начальных значений кинетической кривой (при F<0.5) в координатах Bt=ƒ(t). Зная значения В, рассчитывали Di по уравнению (4).
Время полуобмена (Т1/2) рассчитывали по формуле:

Эффективности извлечения Cs-137 в динамических условиях оценивали, пропуская модельный раствор состава Na+ - 2 моль/л, NO3- - 1,25 моль/л, ОН- - 0,75 моль/л через колонку с внутренним диаметром 10 мм, содержащую 1 мл сорбента, при скорости пропускания 50 мл/ч. После пропускания 300-350 мл модельного раствора сорбент промывали 1М раствором HNO3, затем повторяли цикл сорбции. Эффективность извлечения Cs-137 в динамических условиях оценивали по коэффициенту очистки (Kоч), который рассчитывали по формуле:

где А0 - исходная активность раствора (Бк/мл);
Ai - активность фильтрата (Бк/мл).
Сорбционно-селективные характеристики синтезированных сорбентов (устойчивость сорбента в щелочной среде, значения tmax, скорости разрушения сорбента, KρCs-137×103 (см3/г), коэффициента внутренней диффузии Di×107 (см2/мин), времени полуобмена Т1/2 (мин) в зависимости от условий синтеза (температуры и продолжительности отверждения, количества введенного в олигомерную смесь CaCO3, крупности зернения) приведены в таблицах 1 и 2.
Пример 2
Сорбент получали аналогично примеру 1, при этом смолу отверждали при 190°C в течение 6 часов. CaCO3 вводили количестве 8 масс. %.
Пример 3
Сорбент получали аналогично примеру 1, при этом смолу отверждали при 210°C в течение 6 часов, CaCO3 вводили в количестве 12 масс. %.
Пример 4
Сорбент получали аналогично примеру 1, при этом смолу отверждали при 210°C в течение 1 часа.
Примеры 1-3 свидетельствуют о достижении заявленного технического результата способом, осуществляемым в описанных выше условиях.
В примере 4 указанное время термообработки 1 час оказывается недостаточным, несмотря на высокую температуру, для получения сорбента с высокой химической стабильностью и высокими сорбционно-селективными характеристиками.
Пример 5
Условия получения сорбента аналогичны условиям примера 1. Температура отверждения 100°C, время термообработки 1 час.
Пример 6
Условия получения сорбента аналогичны условиям примера 1. Температура отверждения 100°C, время термообработки - 6 часов.
Свойства сорбентов, синтезированных в условиях примеров 5-6, являются недостаточно высокими и не соответствуют заявленным.