Результат интеллектуальной деятельности: Штаммы гибридных клеток животных Mus. Musculus - продуценты моноклональных антител к белку GP вируса Эбола (subtype Zaire) и моноклональные антитела к белку GP вируса Эбола (subtype Zaire)
Вид РИД
Изобретение
Изобретение относится к области биотехнологии, в частности к гибридомной технологии, и касается получения моноклональных антител к белку GP вируса Эбола с помощью новых гибридных клонов клеток (гибридомы) животных. Изобретение может быть использовано для создания диагностикумов и иммунохимических тест-систем для определения наличия вируса Эбола в биологических образцах или антител к белку GP вируса Эбола. Изобретение может быть использовано для создания лекарственных препаратов против вируса Эбола.
Возбудитель геморрагической лихорадки Эбола относится к семейству Filoviridae, роду Ebolavirus. Заболевание, вызванное вирусами ZEBOV (Zaire ebolavirus) и SUDV (Sudan ebolavirus), сопровождается 53-90% летальностью [1]. Возбудитель впервые выделен осенью 1976 года во время обширных вспышек в Судане и Заире геморрагического заболевания с летальностью 50-90% [2, 3, 4, 14]. Позднее были выявлены вспышки в Кении [5], Габоне [6], Республике Конго [7], Уганде [8], Кот-д'Ивуаре [9]. Вариант вируса Рестон обнаружен у обезьян в Юго-Восточной Азии [5, 10]. Занос вируса Рестон с импортируемыми обезьянами выявлен в США [11].
Природный цикл вируса до сих пор неизвестен, но не вызывает сомнения возможность заражения в природных условиях человекообразных обезьян - шимпанзе и горилл, у которых наблюдается высокая смертность. Обсуждается возможная роль в качестве природного резервуара насекомоядных, летучих мышей, грызунов [12].
Вирус включен в список кандидатов для использования в качестве биологического оружия [13]. Легко осуществляется внутригоспитальная инфекция с передачей вируса от человека к человеку [1].
Инкубационный период составляет в среднем 6 суток. Клиническая картина сходна с лихорадкой Марбург, но протекает тяжелее [14]. Основная симптоматика включает астению, тошноту, рвоту, абдоминальную боль, атралгию, макулопапулезную сыпь на сгибательных поверхностях предплечий и верхних частях голени. У половины больных развивается геморрагический синдром. Причину гибели связывают с развитием ДВС-синдрома, отека легких и головного мозга [2, 4].
Спасение больных зависит от раннего применения иммунной плазмы и специфических противовирусных иммуноглобулинов [2, 14]. Разработка средств антителотерапии в отношении вируса Эбола проводится с 1990-х гг.Из восьми белков вируса ключевой мишенью для средств иммунотерапии является вирусный гликопротеин (GP), являющийся решающим фактором патогенности. Этот белок находится на поверхности вирусного капсида и служит для прикрепления вируса и слияния с мембраной [15].
Моноклональные антитела (МКА), обладающие высокой специфичностью к белку GP вируса Эбола, а также вируснейтрализующей активностью рассматриваются в качестве кандидатных высокоэффективных противовирусных препаратов [16].
Первым для лечения больных лихорадкой Эбола людей был использован препарат ZMapp™ на основе коктейля из трех химерных мышиных моноклональных антител, разработанный калифорнийской компанией Марр Biopharmaceutical Inc в 2014 году. Препарат продемонстрировал положительные результаты при лечении восьми обезьян. Лечение человека препаратом ZMapp началось в конце июля 2014 г. Первыми пациентами стали американский врач Кент Брэнтли и его жена, медсестра Нэнси Райтбол. Препарат вводился пациентам через девять дней после инфицирования. В ходе лечения удалось добиться полного выздоровления пациентов. Однако, дальнейшие исследования показали, что ZMapp специфически нейтрализует штамм Заир, и не действует на штамм Судан [16].
В настоящее время получены и охарактеризованы около 20 моноклональных антител, продемонстрировавших многообещающие результаты при исследовании их на животных моделях. Некоторые из них были рекомендованы для перехода к тестированию на приматах [17]. Например, МКА KZ52, изолированные от выжившего человека, успешно защищали мышей и морских свинок от летальной инфекции. Однако, в ходе тестирования данных антител на приматах было показано, что для полной защиты обезьян одних KZ52 недостаточно [18].
Наиболее перспективные препараты для лечения людей представляют собой коктейли из нескольких МКА.
МАb114 - человеческое моноклональное антитело, выделено от выжившего больного после вспышки лихорадки Эбола в 1995 году в Демократической Республика Конго. При исследовании МАb114 в экспериментах на приматах было показано, что данные МКА полностью защищали животных от летальной дозы вируса Эбола (3 животных в группе). Однако полностью добиться устранения всех клинических симптомов инфекции у животных удалось лишь в комбинации МАb114 с МАb100 [19].
Препараты МВ-003, ZMAb и MIL77E являются коктейлями моноклональных антител.
Препарат МВ-003 содержит три химерных мышиных моноклональных антитела: 13С6, 6D8 и 13F6. Были проведены исследования МВ-003 на высших приматах. Препарат вводился в концентрации 50 мг/кг через 24 и 48 часов после заражения животных вирусом Эбола. Выживаемость животных составила 67% [16].
ZMAb также содержит три МКА: 2G4, 4G7 и 1Н3, полученные от мышей, иммунизированных вирусом везикулярного стоматита (VSV) со встроенным геном GP вируса Эбола. При исследовании препарата на приматах установлено, что если вводить Zmab, через сутки после заражения вирусом Эбола (25 мг/кг, внутривенно, трехкратно) все животные в группе выживают. Если лечение начинается через 48 часов после заражения, выживаемость падает до 50% [16].
Препарат MIL77E, содержащий два МКА: 13С6 и 2G4, продемонстрировал полную защиту обезьян при введении через 3 дня после заражения летальной дозой EBOV. Соотношение МКА 13С6: 2G4 составляло 1:2, соответственно. Для всех других коктейлей антител (МВ-003, ZMAb, ZMapp), соотношение составляло 1:1:1 [16].
МКА также могут быть использованы для выявления антигена и специфических противовирусных антител. Чувствительность диагностикумов на основе МКА не ниже 95% при обнаружении антител (AT), а для определения антигена - 4,5 lgБOE/мл (БОЕ бляшкообразующая единица) [2, 20]. Известны МКА 4А2, продуцируемых гибридомой 4А2 (субкласс иммуноглобулинов IgGl) и МКА 1С1, продуцируемых гибридомой 1С1 (субкласс иммуноглобулинов IgGl), которые используют совместно в иммуноферментной системе формата "сэндвич" для выявления матриксного белка VP40 вируса вируса Эбола, субтип Заир (штамм Mainga) [21]. МКА 1В2, продуцируемые штаммом гибридных клеток животного Mus musculus L. 1В2 (субкласс иммуноглобулинов IgGl) и МКА 7В11, продуцируемые штаммом гибридных клеток животного Rattus Norvegicus 7В11 (субкласс иммуноглобулинов IgG) предложены для выявления нуклеопротеина вируса Эбола, субтип Заир (штамм Mainga) [22].
Известны мышиные гибридомы, продуцирующие МКА к белку GP вируса Эбола [23, 24, 25, 26]. Гибридому Э4/N-6G5, продуцирующую МКА а к структурному белку GP вируса Эбола, штамм Заир, относящиеся к изотипу Ig G, предложено использовать в качестве «индикаторных» антител в тест-системе на основе ИФА [27]. Еще 5 гибридом (GPE118, GPE274, GPE325, GPE463, GPE534) было получено при использовании в качестве антигена для иммунизации рекомбинантного белка EBOV rGPdTM, конъюгированного с белком теплового шока HSP65 из М. Tuberculosis. Проведен иммунохимический анализ эпитопной специфичности полученных антител, на основании которого отобрано 3 гибридомы (GPE 534, GPE 118 и GPE 325), продуцирующие МКА высокой аффинности и специфичные к разным антигенным детерминантам белка GP. Несмотря на то, что авторы рассматривают полученные МКА в качестве кандидатных компонентов комбинированного терапевтического средства для профилактики и лечения геморрагической лихорадки Эбола, данных по их вируснейтрализующей активности in vitro и in vivo не представлено [15]. Известна гибридома GPE 325, синтезирующая МКА класса IgM, селективно связывающая гликопротеин GP вируса Эбола с константой диссоциации 2,6 нМ [28].
Задачей изобретения является получение новых высокоактивных и продуктивных штаммов гибридных клонов клеток, секретирующих вируснейтрализующие МКА к различным эпитопам белка GP вируса Эбола, для последующего конструирования на их основе высокоспецифичных и стандартных отечественных тест-систем для определения антигена вируса Эбола или специфических антител к нему.
Технический результат изобретения заключается в расширении арсенала штаммов гибридом, продуцирующих МКА к антигенам вируса Эбола, обладающих высокой аффинностью, а также в расширении спектра групповой реактивности полученных МКА к белку GP вируса Эбола.
Указанный технический результат достигается путем получения новых гибридных клонов культивируемых клеток Mus. Musculus 6G3, 4В9, 5D9, 2С8, 8С2, 3A12 и 1А5, являющихся продуцентами МКА к белку GP вируса Эбола. Полученные МКА обладают специфичностью и сродством к вируснейтрализующим эпитопам белка GP, что, в свою очередь, дает возможность определять вирусный антиген в биологических жидкостях человека и животных. Нейтрализующие свойства МКА дают возможность рассматривать их в качестве кандидатных терапевтических препаратов для профилактики и лечения геморрагической лихорадки Эбола.
Краткое описание чертежей
На фигуре 1 в виде таблицы 1 представлены концентрации IgG (А280), выделенных из культуральной жидкости (КЖ).
На фигуре 2 в виде таблицы 2 представлены концентрации IgG (А280), выделенных из асцитической жидкости (АЖ) клонов 5D9, 4В9, 6G3 и 2С8.
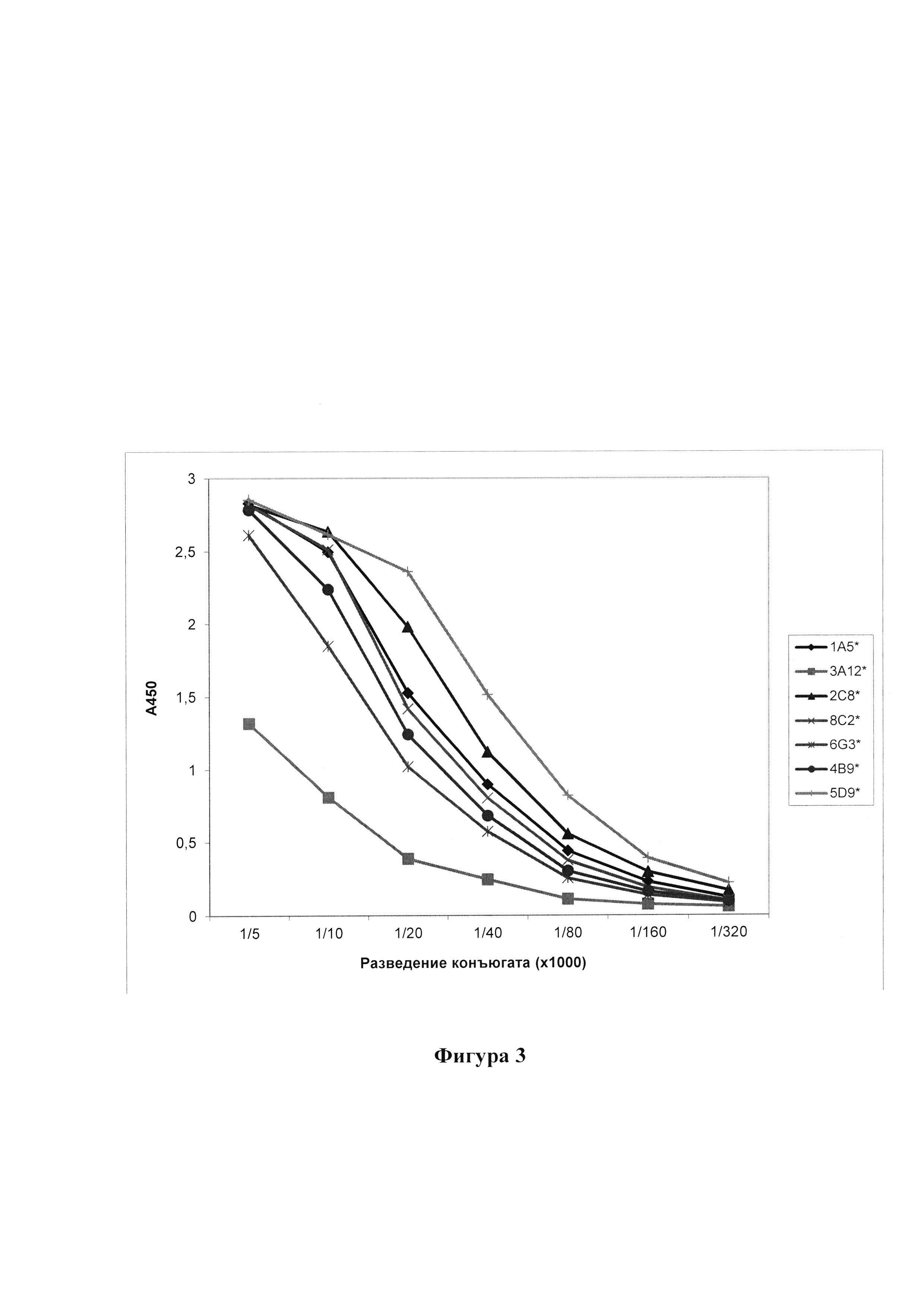
На фигуре 3 представлены графики титрования пероксидазных конъюгатов МКА на планшете с иммобилизованным рекомбинантным белком GP вируса Эбола. Звездочкой (*) помечены пероксидазные конъюгаты МКА (1А5*, 3А12*, 2С8*, 8С2*, 6G3* 4В9*, 5D9*).
На фигуре 4 в виде таблицы 3 представлены конкурентные отношения МКА исследованных клонов МКА. Цифрами указана степень подавления связывания конъюгатов МКА с рекомбинантным белком GP вируса Эбола, штамм Заир, Ebola virus/H.sapiens-wt/GIN/2014/Kissidougou-C15, выраженная в %. Звездочкой (*) помечены пероксидазные конъюгаты МКА.
На фигуре 5 представлены данные по детекции рекомбинантных белков GP вируса Эбола, экспрессированных в бакуловирусной системе (GP-B) и в клетках человека (GP-H) методом «сэндвич»-ИФА с применением МКА клонов 6G3, 4В9 или 2С8 в качестве «захватывающих» антител и пероксидазных конъюгатов этих же клонов (6G3*, 4В9*, 2С8*) в качестве детектирующих антител. GP-B - рекомбинантный белок GP вируса Эбола (subtype Zaire, strain H.sapiens-wt/GIN/2014/Kissidougou-C15), синтезированный в бакуловирусной системе экспрессии. GP-H - рекомбинантный белок GP вируса Эбола (subtype Zaire, strain H.sapiens-wt/GIN/2014/Kissidougou-C15), синтезированный в клетках человека.
На фигуре 6 в виде таблицы 4 представлены константы взаимодействия моноклональных антител (1А5, 5D9, 6G3, 4В9, 2С8) с указанием следующих параметров: ka (1/M*s) - параметр константа ассоциации, единицы измерения 1/M*s; kd (1/s) - параметр константа диссоциации, единицы измерения 1/s; KD (М) - параметр, измеряемый по формуле (ka/kd), единицы измерения М.
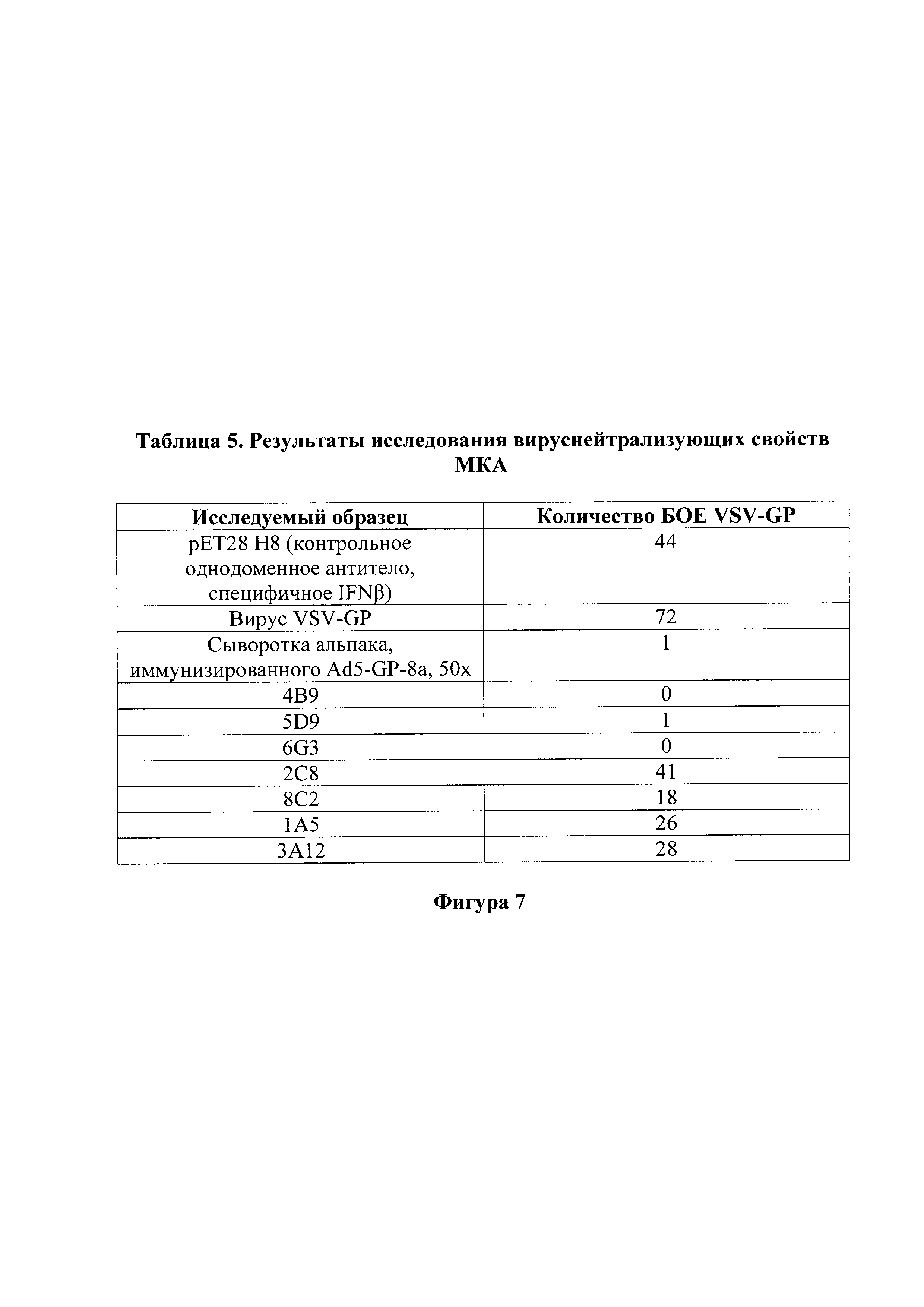
На фигуре 7 в виде таблицы 5 представлены результаты исследования вируснейтрализующих свойств МКА. рЕТ28 Н8 - контрольное однодоменное антитело, специфичное к интерферону бета человека и используемое в тесте на нейтрализацию для исключения ложноположительных результатов. Сыворотка альпака, иммунизированного Ad5-GP-8a, 50х - контрольная сыворотка, полученная при иммунизации альпака рекомбинантным аденовирусом, несущим ген белка GP вируса Эбола и обладающая нейтрализующим действием в отношении вируса Эбола. Используется в тесте на нейтрализацию в качестве положительного контроля.
На фигуре 8 в виде таблицы 6 представлена оценка вируснейтрализующих свойств МКА на примере нативного вируса Эбола. Контроль вируса - рабочая культура вируса Эбола, штамм Заир: биологическая активность - 5,2×10*8 БОЕ/мл). НК - негативные колонии, образованные вирусом Эбола в монослое клеток почки зеленой мартышки GMK-AH-1 (Д) под агаровым покрытием.
Созданные гибридные клоны культивируемых клеток Mus. Musculus: 6G3, 4В9, 5D9, 2С8, 8С2, 3A12 и 1А5 - характеризуются следующими свойствами.
Видовая принадлежность:
Mus. Musculus
Способ получения штаммов:
Штаммы получены путем слияния клеток мышиной миеломы Sp2/0-Ag-14 с клетками селезенки мышей линии Balb/c, иммунизированных введением внутримышечно аденовируса со встроенным геном белка GP вируса Эбола. Селекцию гибридом проводят на питательной среде RPMI-1640 («Sigma», США) с добавлением HAT Media Supplement (Hybri-Max®, «Sigma», США). Штаммы синтезируют МКА, специфически взаимодействующие в твердофазном иммуноферментном анализе с рекомбинантным белком GP вируса Эбола.
Культуральные свойства штаммов:
Гибридные клетки растут в виде суспензии in vitro или в виде асцитной опухоли в перитонеальной полости после введения сингенным мышам линии Balb/c.
Культивирование штаммов in vitro:
В качестве ростовой среды используют среду RPMI-1640 («Sigma», США), содержащую 20% фетальной сыворотки теленка (ФСТ), 4,5 г/л глюкозы, 3 мМ глутамина, 0,2 ед./мл инсулина, 60 мкг/мл гентамицина. Клетки культивируют при 37°С в атмосфере, содержащей 5% СO2. Для культивирования используют пластиковые планшеты или флаконы объемом 50 и 250 мл («Greiner», Германия). Характер роста - стационарная суспензия. Частота пассирования 2 суток. Кратность рассева 1:2-1:4.
Культивирование штаммов в организме животного in vivo:
За 14 суток до введения клеток гибридомы мышей линии Balb/c предварительно обрабатывают внутрибрюшинно 2,6,10,14-тетраметилпентадеканом (Pristane) («Sigma», США) в дозе 0,5 мл/животное. Далее праймированным животным вводят в брюшную полость гибридные клетки штамма в дозе 5-10×106 клеток. Асцитные жидкости, содержащие МКА, получают через 7-15 суток после введения.
Биотехнологическая характеристика штаммов (продуктивность):
- титр МКА в культуральной жидкости при выращивании in vitro -1:729 (в ИФА) (для каждого штамма);
- титр МКА в асцитной жидкости при выращивании in vivo -1:500000-1:1000000 (в ИФА) (для каждого штамма).
Условия хранения и поддержания жизнеспособности штаммов:
Штамм сохраняют посредством криоконсервации в жидком азоте. За 24 часа до замораживания клетки гибридомы пассируют с кратностью рассева 1:2. Осажденные центрифугированием клетки суспендируют в криозащитной среде (90% ФСТ, 10% диметилсульфоксида) и разливают по ампулам в концентрации 3-5 млн./мл., по 1 мл. Выдерживают 24 часа при минус 70°С, затем переносят в жидкий азот (минус 196°С).
Восстановление после размораживания:
Быстрое размораживание штамма проводят при 37°С. Гибридомные клетки разводят в 10 раз ростовой средой без сыворотки, осаждают центрифугированием в течении 10 мин. при 2000 об/мин. и ресуспендируют в ростовой среде, содержащей 20% эмбриональной сыворотки коров в концентрации 3-4×105 клеток/см3. Жизнеспособность восстановленных клеток составляет 70-80% и устанавливается по дифференциальной окраске клеток с использованием 0,4% раствора трипанового синего, рН=7,2-7,3.
Стабильность штаммов:
Стабильность продуцирования антител гибридными клетками сохраняется на протяжении 70 пассажей в культуре клеток и 5 пассажей на мышах линии BALB/c.
Контаминация:
Бактерии и грибы в культурах не обнаружены при длительном наблюдении и посевах на стандартные питательные среды (мясопептонный агар (МПА) - для выявления бактерий и агар Сабуро - для грибов). Заражение микоплазмой не выявлено (тест-система «Mycoplasma Stain Kit», фирмы Flow Lab.).
Кариотип гибридных клеток, модальное число хромосом не определялись.
Характеристика продуцируемых МКА к белку GP к вирусу Эбола:
- мишень - белок GP вируса Эбола;
- специфичность связывания с белком GP - 100%;
- константы диссоциации для полученных МКА составляют от 1,8 до 102 нМ.
- Изотип продуцируемых иммуноглобулинов - 6G3, 4В9, 3A12 и 8С2 - IgGl, 5D9 и 2С8 - IgG2a, 1А5 - IgG2b. (ИФА, тест-система «Моusе-Hybridoma-Subtyping Kit» («Sigma», США).
Изобретение иллюстрируется, но не ограничивается следующими примерами.
Пример 1. Получение штаммов гибридом.
Мышей линии Balb/c 8-недельного возраста массой 18-20 г. иммунизируют 3х-кратно с интервалом 2 недели. В качестве антигена для иммунизации используют аденовирус человека пятого серотипа, содержащего кассету со вставкой модифицированного гена GP вируса Эбола, штамм Заир (Ebola virus/H.sapiens-wt/SLE/2014/Makona-EM124.1; GenBank ID: КМ233045.1)[29]. Антиген с инфекционной множественностью 108 инф. частиц (100 мкл/мышь) вводят внутримышечно без адъюванта. Для бустерной иммунизации используют рекомбинантный белок GP вируса Эбола, штамм Заир, Ebola virus/H.sapiens-wt/GIN/2014/Kissidougou-C15, полученный в бакуловирусной системе экспрессии. Бустерная доза (50 мкг/мышь) вводится без адъюванта, внутрибрюшинно, за 4 суток до выделения селезенки.
Через 4 суток после введения бустерной дозы антигена получают суспензию клеток селезенки мыши стандартным методом в охлажденной ростовой среде без сыворотки.
Для слияния используют перевиваемую клеточную линию мышиной миеломы Sp2/0-Ag-14, дефектную по гену гипоксантин-гуанинфосфорибозилтрансфераза (ГГФРТ), не продуцирующую собственные иммуноглобулины. Гибридизацию проводят по методу, предложенному Kohler G. и Milstain С.[30]. Суспензию клеток селезенки и миеломные клетки смешивают в соотношении 5:1 соответственно. После слияния клетки ресуспендируют в селективной среде с HAT, вносят в 96-луночные панели с фидерным слоем из перитонеальных макрофагов мышей (5×106 кл/мл, по 50 мкл/лун) в концентрации 1,5×105 клеток в лунку в объеме 0,1 мл. Панели с клетками инкубируют при 37°С в атмосфере 5% СО2.
Замену среды в лунках с гибридомными клонами проводят каждые 2-3 суток, используя в течение 14 суток после слияния среду с HAT. Для селекции гибридом, продуцирующих МКА заданной специфичности, из лунок с растущими колониями отбирают культуральные жидкости и тестируют на наличие антител к белку GP вируса Эбола в твердофазном иммуноферментном анализе (ИФА), когда клоны гибридных клеток занимают не менее 50% поверхности лунки. Клоны, обнаружившие специфическую активность, реклонируют методом лимитирующих разведений в 96-луночных панелях с фидерным слоем из перитонеальных макрофагов мышей (5×106 кл/мл, по 50 мкл/лун). Супернатанты из лунок, содержащих реклонированные гибридомы, снова тестируют на наличие антител и их специфичность.
Пример 2. Получение МКА.
Скрининг МКА заданной специфичности и иммунологической активности проводят методом непрямого ИФА. Для этого в лунки иммунологических микропланшетов («Greiner», Германия) вносят 0,1 мл антигена в рабочем разведении в 0,1М карбонат-бикарбонатном буфере, рН 9,5. В качестве антигена используют рекомбинантный белок GP вируса Эбола, штамм Заир, Ebola virus/H.sapiens-wt/GIN/2014/Kissidougou-C15, полученный в бакуловирусной системе экспрессии. Микропланшеты инкубируют 18 часов при 4°С. Свободные участки пластика блокируют 1% Top Block («Yuro», Швейцария) в 0,01М фосфатно-солевом буфере (ФСБ). Инкубируют в течение 30 минут при 37°С и вносят в лунки 0,1 мл культуральной жидкости МКА в различных разведениях (без разведения, с 1:3 до 1:2187). Микропланшеты инкубируют 1 час при 37°С и добавляют пероксидазный конъюгат антител к IgG мыши («Sigma», США) в рабочем разведении. Инкубируют 1 час при 37°С. После каждого этапа не - связавшиеся реагенты отмывают ФСБ с добавлением 0,1% Tween-20 (ФСБТ). В качестве хромогена используют тетраметилбензидин (ТМБ). Интенсивность окраски в лунках определяют после остановки реакции 1М H2SO4 на спектрофотометре Multiscan MCC («Flow», Англия) при длине волны 450 нм.
Клоны, обнаружившие специфическую активность к белку GP вируса Эбола, реклонируют методом лимитирующих разведений в 96-луночных панелях с фидерным слоем из перитонеальных макрофагов мышей (5×106 кл/мл, по 50 мкл/лун). Супернатанты из лунок, содержащих реклонированные гибридомы, снова тестируют на наличие антител и их специфичность. Позитивные реклонированные гибридомы наращивают в культуральных флаконах размером 25 см3 и 75 см3 («Greiner»,Германия).
Выделение МКА из культуральных жидкостей (КЖ). Имуноглобулины (Ig) класса G осаждают из КЖ насыщенным раствором сульфата аммония (до 50% насыщения), инкубируют двое суток при 4°С, центрифугируют, осадок растворяют в ФСБ и очищают на колонке с Protein A-agarose. IgG элюируют с колонки 0.1М ацетатом Na с 0.1М NaCl (рН=2,2). Элюат нейтрализут карбонатным буфером (рН=9,5), осаждают насыщенным раствором сульфата аммония (до 50% насыщения), инкубируют двое суток при 4°С, центрифугируют, осадок растворяют в ФСБ и обессоливают в колонках с полусухим Сефадексом G-25 Medium в ФСБ. Объем каждого препарата - 0,2 мл. Концентрации IgG (A280) представлены в таблице 1 (фигура 1).
Выделение IgG из асцитной жидкости (АЖ) проводят осаждением белков при помощи каприловой кислоты ("Sigma", США). Для выделения МКА используют АЖ от 4-х клонов МКА (5D9, 4В9, 6G3, 2С8), которые разводят 0,06 М ацетатным буфером, рН=4,0, добавляют каприловую кислоту (3,3 мкл/мл АЖ), инкубируют 30 мин при 20°С, центрифугируют. Супернатант фильтруют через PVDF-фильтр (0,45 мкм) и диализуют в течение суток против ФСБ. Затем добавляют насыщенный раствор сульфата аммония (до 50% насыщения), инкубируют 18 часов при 4°С, центрифугируют, осадок растворяют в ФСБ и обессоливают в колонках с полусухим Сефадексом G-25 Medium в ФСБ. Оптическую плотность растворов Ig измеряют на спектрофотометре ("Eppendorf", Германия) при длине волны 280 нм. Концентрацию белка определяют по формуле:
C=D/1,4, где D - оптическая плотность, С - концентрация белка (мг/мл), 1,4 - оптическая плотность раствора IgG с концентрацией 1 мг/мл.
Характеристики полученных препаратов представлены в таблице 2 (фигура 2).
Пример 3. Синтез конъюгатов МКА с пероксидазой хрена и оценка эпитопной специфичности МКА методом конкурентного ИФА.
Для синтеза пероксидазных конъюгатов к 1,0 мл водного раствора пероксидазы (концентрация 4 мг/мл, RZ не менее 3) добавляют 200 мкл 0,1М водного раствора NaIO4 и перемешивают на шейкере 20 мин при комнатной температуре в темноте. Активированную таким образом пероксидазу диализуют в течение ночи против 0,001М ацетата натрия, рН=4,0. Затем к 1,0 мл полученного раствора пероксидазы добавляют 1,0 мл раствора очищенных МКА в 0,1М карбонатном буфере, рН=9,5, доводят рН до 9,5 0,4М карбонатным буфером и инкубируют 2 часа при комнатной температуре в темноте. После этого добавляют 0,1 мл водного раствора NaBH4 (концентрация 4 мг/мл), инкубируют 2 часа при комнатной температуре и диализуют против ФСБ в течение 18 часов. После диализа осаждают Ig сульфатом аммония до 50% насыщения, диализуют против ФСБ для удаления сульфата. Полученный конъюгат разводят в 2 раза глицерином и хранят при минус 20°С.
Активность полученных конъюгатов в системе прямого ИФА с использованием иммобилизованного рекомбинантного белка GP вируса Эбола, штамм Заир, Ebola virus/H.sapiens-wt/GIN/2014/Kissidougou-C15, полученного в бакуловирусной системе экспрессии, представлена на фигуре 3.
Постановка конкурентного ИФА.
В лунки 96-луночной микропанели, предварительно сенсибилизированные рекомбинантным белком GP вируса Эбола, штамм Заир, Ebola virus/H.sapiens-wt/GIN/2014/Kissidougou-C15 в рабочем разведении, вносят очищенные МКА в концентрации 0,1 мг/мл и инкубируют 1 час при 37°С. Затем вносят конъюгированные с пероксидазой хрена МКА в разведениях, позволяющих получить оптическую плотность в пределах 1-1,5 при взаимодействии с антигеном в отсутствии конкурирующих антител. Определение активности МКА проводят спектрофотометрически, при длине волны 450 нм. Конкурентные отношения между МКА (Кинг) вычисляют по формуле:
Кинг=100-(А450 пробы с конкурирующими МКА/А450 пробы без конкурирующих МКА)×100
Результаты представлены в таблице 3 (фигура 4).
Показано, что немеченые МКА клонов 2С8 и 8С2 блокируют связывание аналогичных конъюгатов на 57,8 и 80,1%, соответственно. Такие же результаты показаны для МКА клонов 6G3 и 4В9 (блокировка на 90,6 и 94,6%), т.е. пары МКА 2С8 - 8С2 и 6G3 - 4В9 узнают одинаковые эпитопы белка GP.
Таким образом, из полученных результатов следует, что общие эпитопы белка GP детектируют МКА группы клонов 2С8=8С2 и 6G3=4В9.
Пример 4. Использование МКА для детекции белка GP методом «сэндвич»-ИФА.
В лунки 96-луночной микропанели, предварительно сенсибилизированные очищенными МКА клонов 6G3, 4В9 или 2С8 (10 мкг/мл в 0,1М карбонатном буфере, рН=9,5) вносят антиген в концентрациях 0, 10, 20, 50, 100, 200 и 500 нг/мл и инкубируют 1 час при 37°С. В качестве антигена используют рекомбинантный белок GP, штамм Заир, полученный в бакуловирусной системе экспрессии (subtype Zaire, strain H.sapiens-wt/GIN/2014/Kissidougou-C15, GP-B) и рекомбинантный белок GP, штамм Заир, синтезированный в клетках человека (subtype Zaire, strain H.sapiens-wt/GIN/2014/Kissidougou-C15, GP-H). Панель промывают 4 раза ФСБТ и затем вносят конъюгированные с пероксидазой хрена МКА клонов 6G3, 4В9 или 2С8 в рабочих разведениях. Планшет промывают 4 раза ФСБТ и добавляют 100 мкл приготовленного хромоген-субстратного раствора с тетраметилбензидином (ТМБ). Инкубируют 15 мин при комнатной температуре в темноте и добавляют 100 мкл стоп-раствора для остановки реакции (1М H2SO4). Оптическую плотность при 450 нм (А450) измеряют на спектрофотометре с вертикальным лучом.
Из результатов, представленных на фигуре 5, видно, что присутствие в комбинации «сэндвич»-ИФА МКА клона 2С8 (в качестве захватывающего или детектирующего) позволяет выявлять белок GP вируса Эбола, экспрессированный в клетках человека (GP-H), а МКА клонов 6G3, 4В9 в различных комбинациях выявляют белок GP вируса Эбола, синтезированный в бакуловирусной системе экспрессии(GР-В).
Пример 5. Определение констант взаимодействия МКА.
Константы взаимодействия моноклональных антител определяют путем детекции изменения показателей поверхностного плазмонного резонанса на приборе Biacore 3000 («General Electric», Швеция). Для этого рекомбинантный белок GP EBOV ковалентно иммобилизуют на поверхности декстранового матрикса чипа СМ5 («General Electric», Швеция), а затем пропускают над поверхностью чипа различные концентрации полученных моноклональных антител. Обработку данных и вычисление констант проводят в автоматическом режиме при помощи программы Biaevaluation (General Electric, Швеция).
Из данных, представленных на фигуре 6, следует, что константы реакций МКА 1А5, 5D9, 6G3, 4В9 и 2С8 с белком GP EBOV составляют от 1,8 до 102 нМ.
Пример 6. Оценка вируснейтрализующих свойств полученных МКА.
Для проведения реакции вирусной нейтрализации используют псевдотипированный вирус везикулярного стоматита, содержащий в своем составе белок GP вируса Эбола (VSV-GP). Разведения препарата VSV-GP готовят на буфере (10 мМ Трис-HCl рН=7,5, 1 мМ ЭДТА, 10% сахароза) десятикратными разведениями. В приготовленном разведении концентрация вируса VSV-GP составляет 1000 БОЕ/мл.
Смесь равных объемов МКА и вируса инкубируют в течение 90 мин при температуре 37°С и вносят по 200 мкл на однодневный монослой клеток Vero Е6, предварительно слив ростовую среду. После адсорбции комплекса антиген-антитело на клетках в течение 120 мин при температуре 37°С, наносят агаровое покрытие. Через 48 часов производят учет.
Результаты исследования вируснейтрализующих свойств полученных МКА представлены на фигуре 7. Из этих данных следует, что наиболее эффективно нейтрализуют вирус VSV-GP МКА 4В9, 6G3 и 5D9.
Пример 7. Оценка вируснейтрализующих свойств полученных МКА на примере нативного вируса Эбола.
Вируснейтрализующие свойства МКА определяют в реакции нейтрализации на культуре клеток почки зеленой мартышки GMK-AH-1(Д). Разведения вируссодержащей суспензии на основе вируса Эбола, штамм Заир («антиген»), готовят на разводящей жидкости десятикратным шагом. В приготовленном рабочем разведении концентрация вируса Эбола составляет 120 БОЕ/мл.
Смесь равных объемов МКА и «антигена» вируса Эбола инкубируют в течение 60 мин при температуре от 36,5° до 37,5°С, затем вносят по 0,5 мл на 3-х суточный монослой клеток GMK-АН-1(Д), предварительно сливая ростовую среду, и, после адсорбции комплекса антиген+антитело на клетках в течение 60 мин при температуре от 36,5° до 37,5°С декантируют, затем наносят первичное агаровое покрытие.
Для исключения ложноположительных результатов использовали однодоменное антитело рЕТ28 Н8, специфичное к интерферону бета человека. В качестве положительного контроля использовали обладающую нейтрализующим действием в отношении вируса Эбола сыворотку альпака, иммунизированного рекомбинантным аденовирусом, несущим ген белка GP вируса Эбола (Ad5-GP-8a, 50х).
Через 7 суток инфицированный монослой клеток окрашивают 0,1% нейтральным красным и инкубируют в течение 48 часов при температуре от 36,5° до 37,5°С, затем производят учет негативных колоний во флаконах.
За титр антител исследуемого препарата принимают его высшее разведение, которое подавляет на 50% и более (по сравнению с контрольной сывороткой) негативные колонии, образованные вирусом Эбола на культуре клеток под агаровым покрытием.
Полученные данные представлены в таблице 6 (фигура 8). Титр нейтрализации вируса Эболы для МКА 6G3, 4В9 и 2С8 составил 1:2500. Полученные на основе мышиной миеломы Sp2/0-Ag-14 штаммы Mus musculus L. 6G3, 4В9, 5D9, 2С8, 3A12, 8С2 и 1А5 отличаются от всех описанных ранее гибридом, продуцирующих МКА к белкам вируса Эбола.
Предлагаемые в настоящем изобретении гибридомы: 6G3, 4В9, 5D9, 2С8, 3A12, 8С2, 1А5 - продуценты МКА, специфически взаимодействующих в ИФА с рекомбинантным белком GP вируса Эбола, обладают вируснейтрализующей активностью в отношении псевдотипированного вируса везикулярного стоматита, содержащего в своем составе белок GP вируса Эбола, а также в отношении нативного вируса Эбола (штамм Заир). Гибридомы 6G3, 4В9, 3А12 и 8С2 синтезируют МКА класса IgGl, гибридомы 2С8 и 5D9 - МКА класса IgG2a, гибридома 1А5 - МКА класса IgG2b. Нейтрализующие свойства МКА дают возможность в дальнейшем рассматривать их в качестве кандидатных терапевтических препаратов для профилактики и лечения геморрагической лихорадки Эбола.
Источники информации:
1. Руководство по вирусологии: Вирусы и вирусные инфекции человека и животных / Под ред. Академика РАН Д.К. Львова. - М.: ООО «Издательство «Медицинское информационное агентство», 2013. - 1200 с: ил.
2. Борисевич И.В., Маркин В.А., Фирсова И.В. и др. Эпидемиология, профилактика, клиника и лечение геморрагических лихорадок (Марбург, Эбола, Ласса и боливийской) // Вопр. вирусол. - 2006. - №5. - С. 8-16.
3. Львов Д.К., Клименко С.С, Гайдамович С.Я. Арбовирусы и арбовирусные инфекции. - М.:Медицина, 1989. - 336 с.
4. Leroy Е.М., Baize S., Lu C.Y. et al. Diagnosis of Ebola hemorrhagic fever by RT-PCR in an epidemic setting //J. Med. Virol. - 2000. - V. 60. - P. 463-472.
5. Peters C.J., Sanchez A., Feldman H. et al. Filoviruses as emerging pathogens // Semin. Virol. - 1994. - V.5. - P. 147-154.
6. Georges A.J., Leroy E.M., Renat A.F. et al. Ebola hemorrhagic fever // J. Infect. Dis.- 1999. -V. 179.-Suppl. 1. - P. 65-75.
7. Peterson A.T., Carroll D.S., Mills J.N. et al. Pottential mammalian Flavivirus reservoirs // Emerg/ Infect. Dis. - 2004. - V. 10. - №12. - P. 2073-2081.
8. Francesconi P., Yoti Z., Declich S. et al. Ebola hemorrhagic fever transmission and risk factors of contacs, Uganda // Emerg. Infect. Dis. - 2003. - V.9. - №11. - P. 1430-1437.
9. Formenty P., Boesch C, Wyers M. et al. Ebola virus outbreakamong wild chimpanzees living in a rain forest of Cote d'lvoire // J. Infect. Dis. - 1999. - V.179.-Suppl. 1. - P.120-126.
10. Viral hemorrhagic fevers. Report of WHO Expert Сотр. Tehn. Rep. - №721. - Geneva: WHO, 1985. - 126 p.
11. Morikawa S., Saijo M., Kurane I. Current knowledge on lower virulence of Reston Ebola virus (in French: Connaissances actuelles sur la moindre virulence du virus Ebola Reston) // соmр. Immunol. Microbiol. Infect. Dis. - 2007. - V.30. - №5-6. - P. 391-398.
12. Peterson A., Bauer J.T., Mills J.N. Ecologic and geographic distribution of Filovirus disease // Emerg. Infect. Dis. - 2004. - V.10. - №1. - P. 40-47.
13. Borio L., Inglesby Т., Peters C.J. et al. Hemorrhagic fever viruses as biological weapons // JAMA. - 2003. - V. 287. - P. 2391-2405.
14. Swanepoel R., Leman P.A., Burt F.J. et al. Experimental inoculation of plants and animals wits Ebola virus // Emerg. Infect. Dis. - 1996. - V. 2. - P. 321-325.
15. Шемчукова О.Б., Дементьева И.Г., Варламов H.E., Позднякова Л.П., Боков М.Н., Алиев Т.К., Панина А.А., Долгих Д.А., Кирпичников М.П., Свешников П.Г. Получение и характеристика моноклональных антител против гликопротеина вируса Эболы // Вест. Моск. Ун-та. Сер 16. Биология. - 2016. - №1. - С. 29-34.
16. Moekotte A.L., Huson М.А., van der Ende A.J., Agnandji S.T., Huizenga E., Goorhuis A., Grobusch M.P. Monoclonal antibodies for the treatment of Ebola virus disease. // Expert Opin Investig Drugs. - 2016. - Vol. 25 (11). - P. 1325-1335.
17.  E, Alvarez MM,
E, Alvarez MM,  AR, et al. Anti-Ebola therapies based on monoclonal antibodies: current state and challenges ahead // Crit Rev Biotechnol. - 2015 - Vol. 26 - p. 1-16.
AR, et al. Anti-Ebola therapies based on monoclonal antibodies: current state and challenges ahead // Crit Rev Biotechnol. - 2015 - Vol. 26 - p. 1-16.
18. Murin CD, Fusco ML, Bornholdt ZA, et al. Structures of protective antibodies reveal sites of vulnerability on Ebola virus // Proc Natl Acad Sci USA. - 2014 - Vol. 111 - p. 17182-17187.
19. Corti D, Misasi J, Mulangu S, et al. Protective monotherapy against lethal Ebola virus infection by a potently neutralizing antibody // Science. - 2016 - Vol. 351 - p. 1339-1342.
20. Борисевич И.В., Михайлов В.В., Потрываева Н.В. Разработка иммуноферментной тест-системы для определения антигена вируса Эбола // Вопр. Вирусол. - 1996. - №5. - С. 232-234.
21. Патент RU №2395577. Штамм гибридных клеток животного Mus musculus L. 1B2 - продуцент моноклональных антител для выявления белка vp40 вируса Эбола, субтип Заир (штамм Mainga) (варианты), моноклональное антитело, продуцируемое штаммом (варианты), и набор для иммуноферментной тест-системы формата "сэндвич" для выявления белка vp40 вируса Эбола, субтип Заир (штамм Mainga)./ Авторы: Казачинская Е.И. и др., заявка №2008150265/13, приоритет 18.12.2008.
22. Патент RU №2395576 штамм гибридных клеток животного Mus musculus L.1B2 - продуцент моноклональных антител для выявления нуклеопротеина вируса Эбола, субтип Заир (штамм Mainga) (варианты), моноклональное антитело, продуцируемое штаммом (варианты), набор для иммуноферментной тест-системы формата "сэндвич" для выявления нуклеопротеина вируса Эбола, субтип Заир (штамм Mainga)./Aвторы: Казачинская Е.И. и др., заявка №2008149653/13, приоритет 16.12.2008
23. Reynard О., Volchkov V.E. Characterization of a Novel Neutralizing Monoclonal Antibody Against Ebola Virus GP. // J Infect Dis. - 2015. - Vol. 212, Suppl 2. - P. 372-378.;
24. Lucht A., Grunow R., Otterbein C, Feldmann H., Becker S. Production of monoclonal antibodies and development of an antigen capture ELISA directed against the envelope glycoprotein GP of Ebola virus.// Med Microbiol Immunol. - 2004. - Vol. 193 (4). - P. 181-187.;
25. Shahhosseini S., Das D., Qiu X., Feldmann H., Jones S.M., Suresh M.R. Production and characterization of monoclonal antibodies against different epitopes of Ebola virus antigens // J Virol Methods. - 2007. - Vol. 143 (1). - P. 29-37.
26. Marceau C.D., Negi S.S., Hernandez H., et al. Novel neutralizing monoclonal antibodies protect rodents against lethal filovirus challenges.// Trials Vaccinology. - 2014. - Vol. 3. - P. 89-94.
27. Патент RU №2186106. Штамм гибридных клеток Э4/N-6G5 животных Mus Musculus L., продуцирующих моноклональные антитела к вирусу Эбола./Авторы: Ручко С.В. и др., заявка №2001108229/13, приоритет 29.03.2001.
28. Патент RU №2630304. Моноклональное антитело, связывающееся с гликопротеином вируса Эбола, фрагменты ДНК, кодирующие указанное антитело, и антигенсвязывающий фрагмент./Авторы: Алиев Т.К. и др., заявка №2015157142, приоритет 31.12.2015.
29. Патент RU №2578160. Иммунобиологическое средство и способ его использования для индукции специфического иммунитета против вируса эбола (варианты)./Авторы: Логунов Д.Ю. и др., заявка №2015111368/10, приоритет 31.03.2015.
30. Kohler G., Milstain С. Continuous cultures of fused cells secreting antibody of predefined specificity // Nature. - 1976. - Vol. 256. - P. 495-497.