Результат интеллектуальной деятельности: Способ получения высокомощного катодного материала на основе твердого раствора LiFe1-x-yMnxCoyPO4 со структурой оливина для литий-ионных аккумуляторов
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к электродным материалам на основе сложных фосфатов переходных металлов и лития и может быть использовано для получения катодного активного материала для литий-ионных аккумуляторов и батарей на основе такого материала.
Уровень техники
Литий-ионные аккумуляторы являются широко распространенным типом электрохимических накопителей энергии. Прогресс во многих областях науки и технологии приводит к постоянному увеличению потребности общества в автономных источниках электроэнергии. Это связано, в первую очередь, с массовым внедрением высокотехнологичных устройств, таких как электротранспорт (электромобили, электровелосипеды, промышленные погрузчики, автобусы и т.д.), беспилотные летательные аппараты, робототехника. Стоит отметить, что аккумуляторы для данных устройств должны демонстрировать не только высокую энергоемкость, но и иметь улучшенные мощностные характеристики. Известно, что удельные энергетические и мощностные параметры литий-ионного аккумулятора лимитируются, в первую очередь, материалом катода.
В настоящее время в качестве катодов литий-ионных аккумуляторов используются различные классы материалов, при этом наиболее распространены слоистые оксиды с общей формулой LiMO2 (M = Mn, Co, Ni), в том числе смешанного состава. Они демонстрируют высокую энергоемкость (~520-660 Вт*ч/кг относительно Li/Li+), однако в связи с особенностями кристаллической структуры имеют ряд проблем, в частности, связанных с эксплуатацией на высоких плотностях тока. Это ограничивает возможность их использования в массовом производстве высокомощных потребительских устройств. Кроме того, известна литий-марганцевая шпинель LiMn2O4 и твердые растворы на ее основе. Этот материал более дешев и безопасен в эксплуатации. Основные недостатки данного материала связаны с относительно невысокой энергоемкостью (~540 Вт*ч/кг) и потерей емкости в процессе циклирования, особенно при повышенных температурах и мощностях нагрузки.
Наиболее распространен в крупногабаритных и/или высокомощных устройствах катодный материал на основе LiFePO4 со структурой оливина, экспериментальная удельная энергоемкость которого составляет ~540 Втч/кг. Основными преимуществами этого материала являются высокий уровень безопасности при повышенных нагрузках, низкая стоимость и отличная циклическая устойчивость. Главный недостаток этого соединения – относительно низкая энергоемкость, связанная с невысоким потенциалом перехода Fe2+/Fe3+. Для решения данной проблемы можно использовать твердые растворы на основе структуры оливина с другими d-металлами: Mn, Co. Это позволяет повысить рабочий потенциал, и, следовательно, энергоемкость, а также улучшить мощностные характеристики, благодаря изменению механизма (де)интеркаляции Li+ (Drozhzhin O.A., Sumanov V.D., Karakulina O.M., Abakumov A.M., Hadermann J., Baranov A.N., Stevenson K.J., Antipov E.V., Switching between solid solution and two-phase regimes in the Li1-xFe1-yMnyPO4 cathode materials during lithium (de)insertion: Combined PITT, in situ XRPD and electron diffraction tomography study, Electrochimica Acta, 191 (2016) pp. 149-157). Стоит отметить, что характеристики LiFePO4 и твердых растворов на его основе в значительной степени зависят от наличия или отсутствия дефектов в кристаллической структуре, размера и формы частиц материала, однородности распределения катионов d-металлов (в случае твердых растворов) в объеме частицы, качества углеродного покрытия и других особенностей. В связи с этим, ключевым моментом достижения привлекательных электрохимических характеристик является не только формула соединения, но также и качество материала на микро- и макроуровне. Другим важным требованием к материалу, кроме непосредственно рабочих характеристик, является возможность простого и экономичного производства этого материала, масштабируемость метода синтеза. Такими характеристиками (простота, легкость в масштабировании, экономичность) обладает гидро- и сольвотермальный синтез, позволяющий получать высокодисперсные однородные материалы с нужной морфологией при невысокой (190-200оС) температуре.
Наиболее близким к настоящему изобретению является техническое решение, раскрытое в документе US 2015/0349343 A1. Приведенный в этом документе катодный материал синтезирован гидро- и сольвотермальным методом и имеет в основе твердый раствор оливина LiFe1-xMnxPO4 (0<x<1). Лучший изученный в этом документе образец обладает показателями энергоемкости на низких скоростях циклирования (от 0,1C до 1C), сравнимыми с таковыми показателями катодных материалов, полученных с использованием способа по настоящему изобретению. Однако на высокой скорости разряда (т.е. при повышенных мощностных нагрузках), такой как 5С и 10C, материал, описанный в документе US 2015/0349343, демонстрирует существенное снижение электрохимической емкости и, как следствие, энергоемкости, что ставит под сомнение возможность использования данного материала в высокомощных устройствах. Данных о циклировании на режимах с более высокой плотностью тока в US 2015/0349343 не приведено.
Из близких по тематике документов также можно отметить документы WO 2014/098933 и US 2015/303473 A1. В первом из них предлагается использовать широкий спектр допантов в подрешетке железа и марганца, а также пониженные температуры сольвотермального синтеза (вплоть до 100оС). Во втором используется другая последовательность смешения реагентов: растворы солей d-металлов сначала смешиваются с фосфорной кислотой, а затем к полученному раствору добавляется гидроксид лития. Катодные материалы, полученные по описанным в приведенных патентах методикам, также характеризуются существенным снижением энергоемкости при высоких плотностях тока.
Раскрытие изобретения
Задачей настоящего изобретения является создание экономичного и масштабируемого способа получения катодного материала на основе структуры оливина, отличающегося высокой удельной энергоемкостью при циклировании на средних и высоких скоростях циклирования (более 1С) и стабильностью рабочих характеристик при длительной эксплуатации и ориентированного на использование в высокомощных источниках тока с повышенной удельной энергией.
Авторы изобретения обнаружили, что данная техническая задача может быть решена с использованием способа получения твердых растворов состава LiFe1-x-yMnxCoyPO4 (0≤x≤1, 0≤y≤1 и сумма x и y не превышает 1), характеризующихся структурой оливина, включающего стадии, на которых:
a) получают частицы Li3PO4 путем внесения источников ионов Li+ и PO43- в водный растворитель;
б) выдерживают осадок, образовавшийся в реакционной смеси на стадии a), в течение по меньшей мере 1 часа;
в) в реакционную смесь, полученную на стадии б) вносят:
- по меньшей мере одно соединение, которое является источником одного или нескольких катионов Fe2+, Mn2+ и Co2+, где сумма мольных количеств катионов Fe, Mn и Co приблизительно равна мольному количеству Li3PO4; и
- по меньшей мере один органический сорастворитель, представляющий собой одноатомный или многоатомный органический спирт или смесь таких спиртов, в таком количестве, чтобы массовое содержание сорастворителя в реакционной смеси составляло от 20% до 80%;
г) реакционную смесь, полученную на стадии в), нагревают при перемешивании в атмосфере инертного газа в автоклаве при температуре в диапазоне 190-210оC в течение по меньшей мере 1 часа.
Такой способ представляет собой первый вариант осуществления настоящего изобретения.
Способ по изобретению характеризуется последовательностью стадий, ранее не использовавшейся для получения твердых растворов данного состава, и позволяет получать однородные высокодисперсные порошки с ориентацией частиц по наименьшему измерению вдоль направления диффузии лития, высоким уровнем кристалличности и однородным распределением катионов d-металлов (Fe, Mn, Co) в структуре материала.
В других вариантах осуществления способ может дополнительно включать нанесение электропроводного покрытия, позволяющее равномерно покрывать частицы слоем хорошо проводящего углеродного материала (например, сажи), что позволяет оптимизировать характеристики материала.
В частности, во втором варианте осуществления изобретения способ по изобретению используется для получения композитного материала, имеющего формулу LiFe1-x-yMnxCoyPO4/C, где 0≤x≤1, 0≤y≤1 и сумма x и y не превышает 1, характеризующегося структурой оливина, и включает стадии, на которых:
a) получают частицы Li3PO4 путем внесения источников ионов Li+ и PO43- в водный растворитель;
б) выдерживают осадок, образовавшийся в реакционной смеси на стадии a), в течение по меньшей мере 1 часа;
в) в реакционную смесь, полученную на стадии б) вносят:
- по меньшей мере одно соединение, которое является источником одного или нескольких катионов Fe2+, Mn2+ и Co2+, где сумма мольных количеств катионов Fe, Mn и Co приблизительно равна мольному количеству Li3PO4; и
- по меньшей мере один органический сорастворитель, представляющий собой одноатомный или многоатомный органический спирт или смесь таких спиртов, в таком количестве, чтобы массовое содержание сорастворителя в реакционной смеси составляло от 20% до 80%;
г) реакционную смесь, полученную на стадии в), нагревают при перемешивании в атмосфере инертного газа в автоклаве при температуре в диапазоне 190-210оC в течение по меньшей мере 1 часа;
д) вещество, полученное на стадии г), выделяют, смешивают с источником углерода и отжигают при 600-700оС в течение по меньшей мере 1 часа в атмосфере инертного газа.
В других вариантах осуществления настоящее изобретение также относится к электродному материалу для литий-ионного аккумулятора, полученному описанными выше способами. В частности, в третьем и четвертом вариантах осуществления настоящее изобретение относится к электродным материалам для литий-ионного аккумулятора, полученным способами по первому и второму вариантам осуществления изобретения, соответственно.
Изобретение также охватывает катод литий-ионного аккумулятора, содержащий материал, полученный способом по настоящему изобретению. В частности, в пятом и шестом вариантах осуществления настоящее изобретение относится к катодам, содержащим материал по третьему и четвертому вариантам осуществления изобретения, соответственно.
Другие варианты осуществления настоящего изобретения будут очевидны специалистам из нижеследующего описания и из прилагаемой формулы изобретения.
Технический результат настоящего изобретения заключается в экономичном и масштабируемом получении катодного материала, отличающегося высокой удельной энергоемкостью при циклировании на средних и высоких скоростях циклирования (более 1С) и стабильностью рабочих характеристик при длительной эксплуатации.
Не ограничивая себя какой-либо теорией, авторы изобретения полагают, что технический результат настоящего изобретения может быть связан с комбинацией факторов, позволяющих получать однородные по составу и морфологии субмикронные частицы с высокой степенью кристалличности (бездефектности), и в первую очередь обеспечивается синтезом Li3PO4 с последующим выдерживанием продукта для получения исходного прекурсора оптимальной морфологии (Фиг. 1) с последующим добавлением солей d-металлов совместно с органическим сорастворителем.
Краткое описание чертежей
На Фиг. 1 представлена зависимость морфологии свежеосажденного прекурсора Li3PO4 в зависимости от времени выдерживания осадка в растворе: 0 часов (а), 1 час (б) и 5 часов (в).
На Фиг. 2 представлена морфология катодного материала LiFe0,5Mn0,5PO4, полученного при различных временах выдерживания свежеосажденного прекурсора Li3PO4 в растворе: 0 часов (а), 1 час (б) и 5 часов (в).
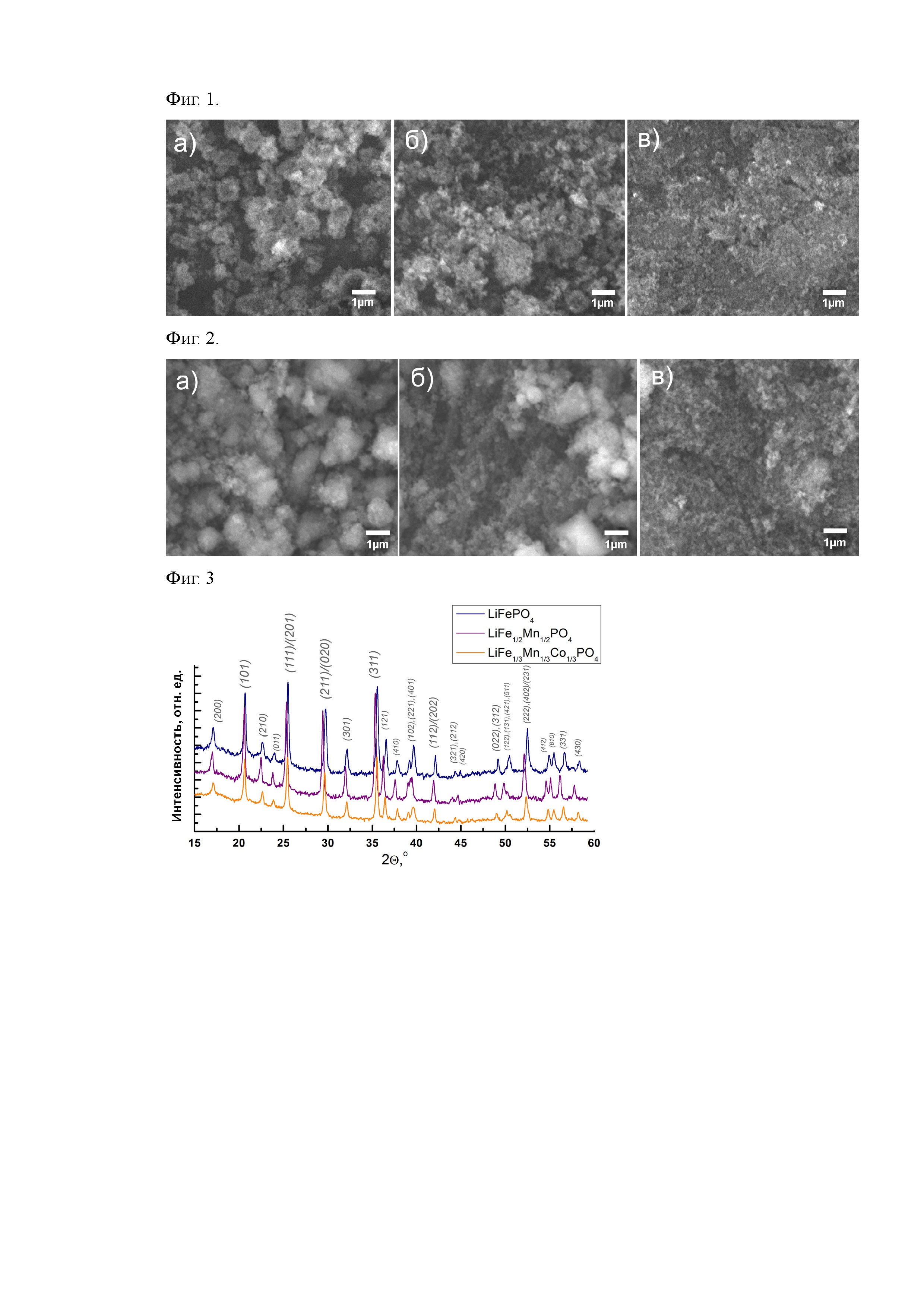
На Фиг. 3 представлены дифрактограммы материалов с одним, двумя и тремя d-катионами в структуре (LiFePO4, LiFe0,5Mn0,5PO4, LiFe1/3Mn1/3Co1/3PO4), полученных в соответствии с Примерами 2, 1 и 5, соответственно. Дифрактограммы проиндицированы в орторомбической сингонии (пространственная группа Pnma) в полном соответствии с структурным типом оливина. Индексы основных рефлексов элементарной ячейки оливина также приведены на фиг. 3.
На Фиг. 4 приведены микрофотографии частиц материала и результаты изучения образца LiFe0,5Mn0,5PO4 методом просвечивающей электронной микроскопии (TEM).
На Фиг. 5 приведены результаты изучения образца LiFe0,5Mn0,5PO4 методом сканирующей просвечивающей электронной микроскопии в электронах, рассеянных на большие углы (HAADF-STEM) и анализа поверхности частиц методом рентгеноспектрального локального микроанализа (РСЛМА, EDX) на пространственной шкале 1 микрон.
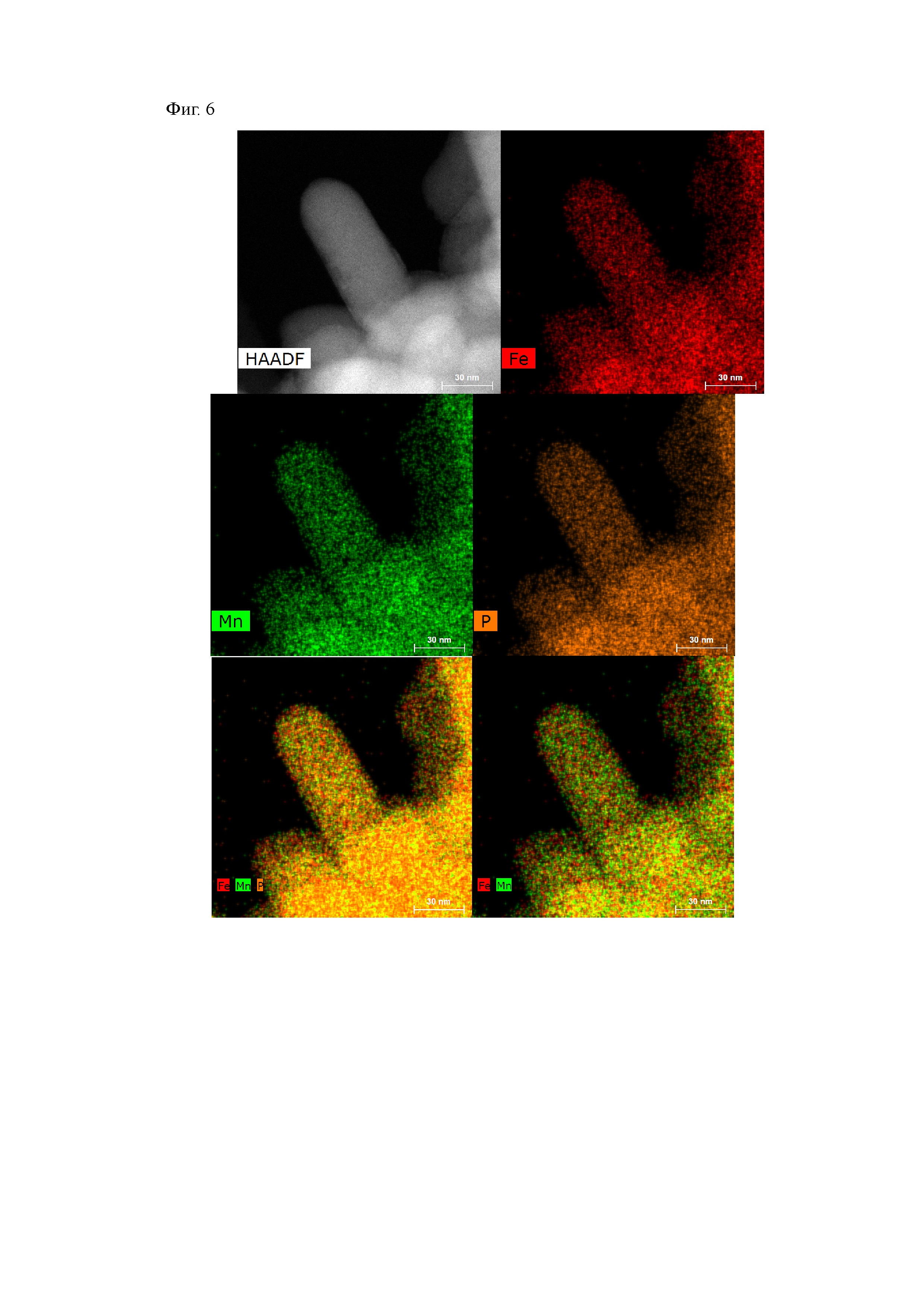
На Фиг. 6 приведены результаты изучения образца LiFe0,5Mn0,5PO4 методом сканирующей просвечивающей электронной микроскопии в электронах, рассеянных на большие углы (HAADF-STEM) и анализа поверхности частиц методом рентгеноспектрального локального микроанализа (РСЛМА, EDX) на пространственной шкале ~10 нанометров.
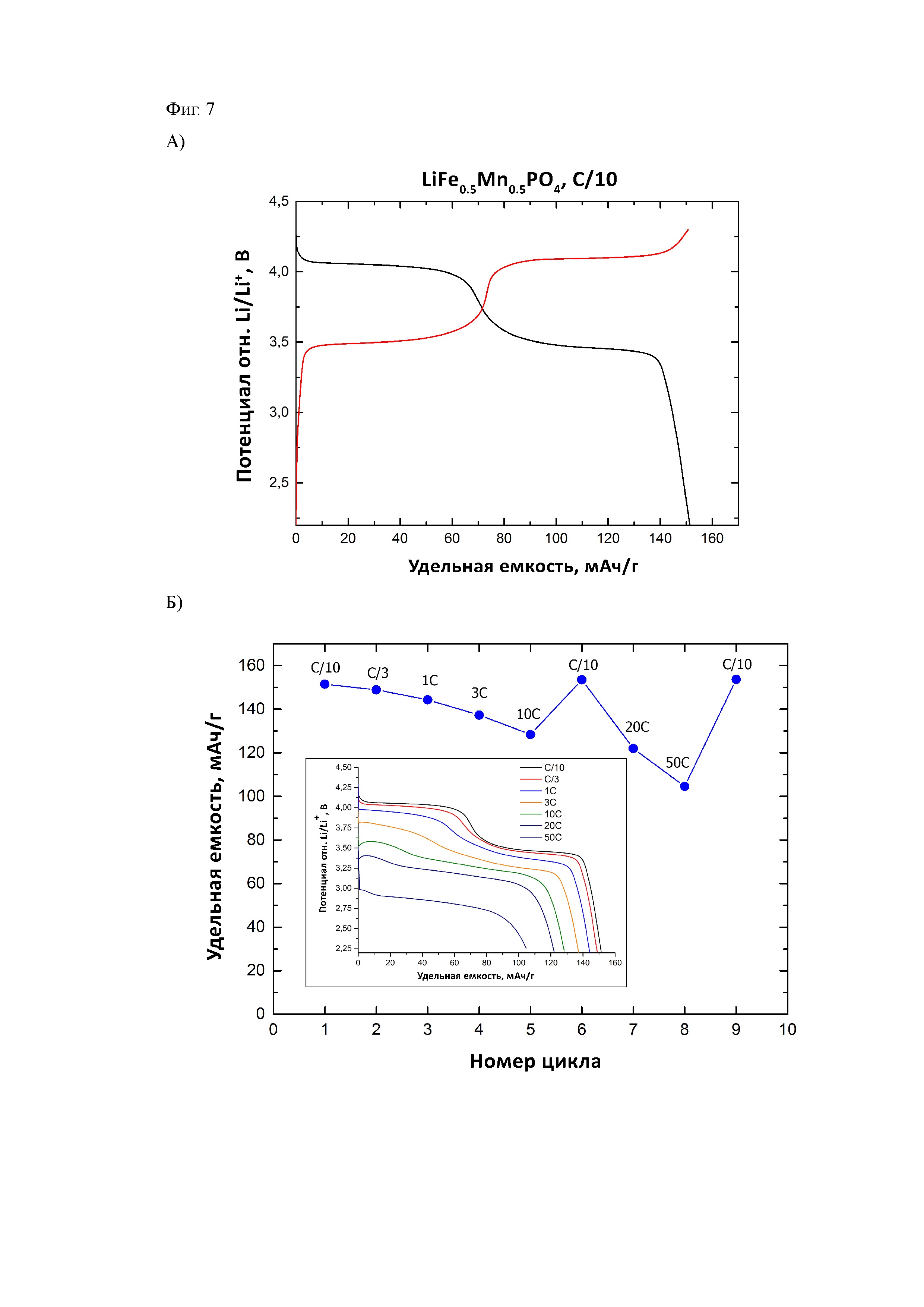
На Фиг. 7 приведены результаты электрохимического тестирования LiFe0,5Mn0,5PO4/С в литий-ионной полуячейке в интервале потенциалов 2,2-4,3 В отн. Li/Li+, при комнатной температуре:
А) кривые гальваностатического заряда-разряда при скорости С/10;
Б) зависимость удельной емкости от номера цикла при различных скоростях разряда и разрядные кривые при различных скоростях разряда.
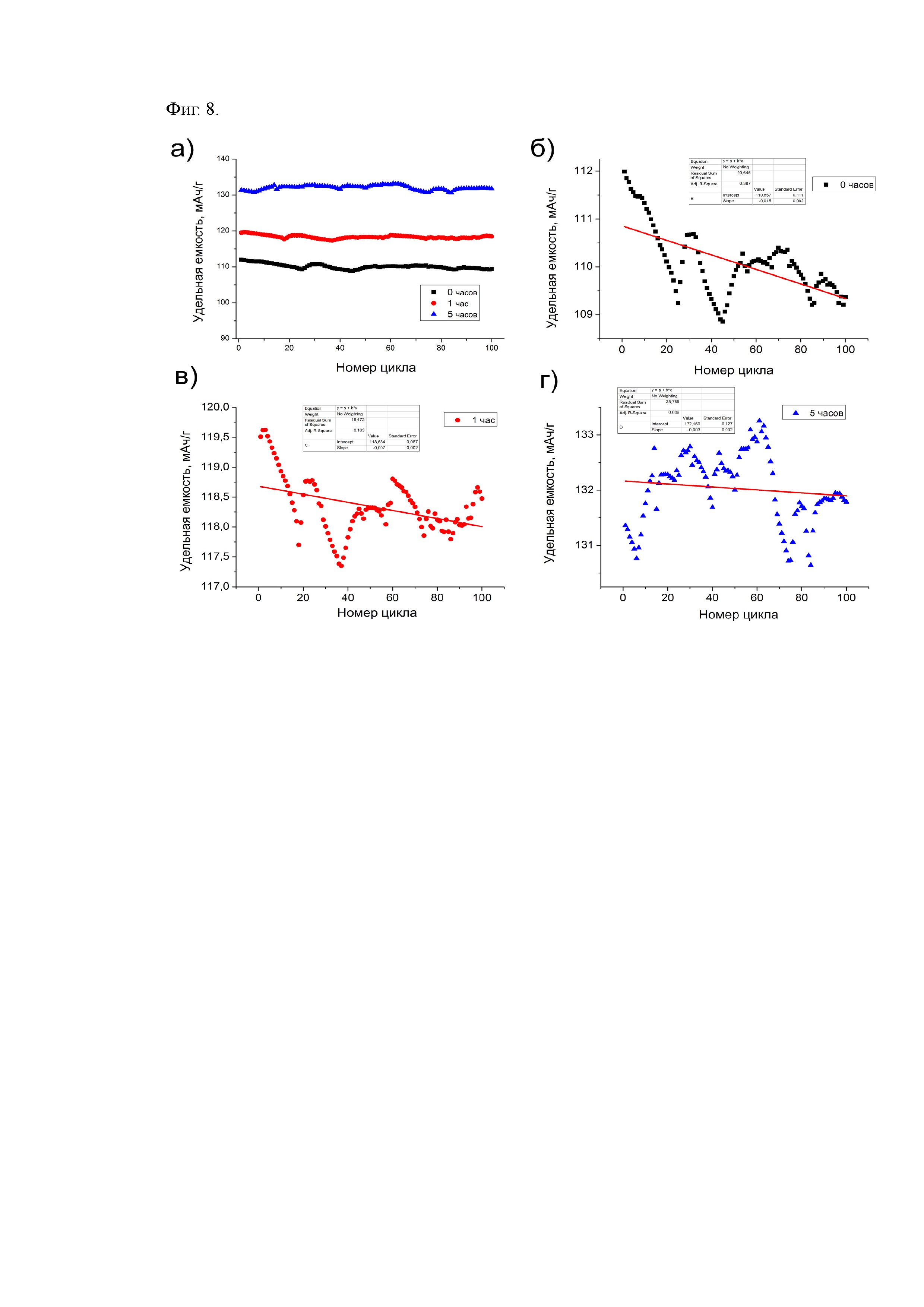
На Фиг. 8 приведены результаты циклирования (разрядная емкость) при скорости заряда/разряда 1С для катодного материала LiFe0,5Mn0,5PO4/С, полученного при различных временах выдерживания свежеосажденного прекурсора Li3PO4 в растворе: 0 часов, 1 час и 5 часов (а). Для каждого времени выдерживания приведен отдельный график значений разрядной емкости с линейной аппроксимацией среднего значения. Тангенс угла наклона в приведенных координатах составил -0,015 для t = 0 часов (б), -0,007 для t = 1 час (в) и -0,003 для t = 5 часов (г).
Осуществление изобретения
В настоящем изобретении выражения «содержит» и «включает» и их производные используются взаимозаменяемо и понимаются как неограничивающие, т.е. допускающие присутствие/использование других компонентов, стадий, условий и т.п., помимо тех, что перечислены в явном виде. Напротив, выражения «состоит из» и «составлен из» и их производные предназначены для указания на то, что перечисленные компоненты, стадии, условия и т.п. являются исчерпывающими.
В настоящем изобретении, когда для какой-либо величины приводится диапазон возможных значений, подразумевается, что граничные точки этого диапазона также включены в объем настоящего изобретения. Следует понимать, что все поддиапазоны, лежащие в приведенных диапазонах, также включены в объем настоящего изобретения, как если бы они были указаны в явном виде. В случае, когда для какой-либо величины приведены несколько диапазонов возможных значений, все диапазоны, получаемые путем комбинирования различных граничных точек из указанных диапазонов, также включены в настоящее изобретение, как если бы они были указаны в явном виде.
В случае, когда какие-то признаки изобретения раскрыты в настоящем документе для одного варианта осуществления, эти признаки также могут быть использованы и во всех других вариантах осуществления изобретения, при условии, что это не противоречит смыслу изобретения.
В рамках настоящего изобретения термины в единственном числе охватывают также и соответствующие термины во множественном числе, и наоборот, при условии, что из контекста явно не следует иное.
За исключением экспериментальной части описания, все численные значения, выражающие какие-либо количества и условия в настоящем изобретении, являются приближенными, и их следует читать, как предваряемые термином «приблизительно» или «около», даже если эти термины и не приводятся в явном виде. Напротив, в экспериментальной части описания все численные величины приведены настолько точно, насколько это возможно, однако следует понимать, что любая экспериментально определенная величина по природе своей несет в себе некоторую погрешность. Таким образом, все численные величины, приведенные в экспериментальной части описания, следует воспринимать с учетом существования указанной экспериментальной погрешности и, по меньшей мере, с учетом количества приведенных значащих цифр и стандартных методик округления.
В настоящем документе все проценты являются массовыми, если явно не указано иное.
Под «электродным материалом» в настоящем изобретении понимается активный материал, используемый в комбинации с электропроводящими добавками, связующими и, при необходимости, другими вспомогательными веществами для получения электродов литий-ионных аккумуляторов.
На стадии а) способа по настоящему изобретению получают осадок соли Li3PO4. Эту стадию осуществляют путем внесения необходимых количеств источников ионов Li+ и PO43- в водный растворитель.
В настоящем изобретении в качестве источника ионов Li+ могут быть использованы гидроксид лития (LiOH), гидрат LiOH (LiOH*H2O) или соли лития или их гидраты, в том числе водные растворы этих веществ. Соли лития могут быть выбраны из известных специалистам органических и неорганических солей лития, таких как хлорид лития, бромид лития, сульфат лития, нитрат лития, ацетат лития и т. п. Также одним из источников лития может выступать дигидрофосфат лития (LiH2PO4) или его водный раствор. В предпочтительном варианте осуществления в качестве источника ионов Li+ используют LiOH или LiOH*H2O .
В настоящем изобретении в качестве источника ионов PO43- могут быть использованы фосфорная кислота (H3PO4) или дигидрофосфат лития (LiH2PO4), в том числе их водные растворы.
Под водным растворителем в настоящем изобретении понимается растворитель, по существу состоящий из воды, т. е. содержащий по меньшей мере 80% мас. воды, предпочтительно по меньшей мере 90% мас. воды, более предпочтительно по меньшей мере 95% мас. воды, еще более предпочтительно по меньшей мере 99% мас. воды, наиболее предпочтительно состоящий из воды, например из дистиллированной или деионизированной воды.
На стадии б) заявляемых способов осадок Li3PO4, образовавшийся в реакционной смеси на стадии а), выдерживают в течение по меньшей мере 1 часа. В способах по изобретению особое внимание уделяется подготовке прекурсора, а именно времени выдерживания осадка Li3PO4 перед внесением в реакционную среду источника ионов переходных металлов. Как показано в Примере 1А и на Фиг. 8, эта стадия играет существенную роль при последующем получении катодного материала с привлекательными электрохимическими характеристиками: при увеличении времени выдержки от 0 до 5 часов возрастает как удельная емкость катодного материала, так и его циклическая устойчивость. Не ограничивая себя какой-либо теорией, авторы полагают, что это связано с повышением однородности материала и уменьшением количества дефектов в кристаллической структуре. Согласно настоящему изобретения, особенно предпочтительное время выдерживания осадка Li3PO4 (прекурсора) составляет 3-5 часов.
Как неожиданно обнаружили авторы изобретения, предварительное получение и выдерживание осадка Li3PO4 позволяет осуществлять сольвотермальный синтез однофазных образцов с кристаллической структурой оливина с получением однородных по составу и размеру частиц материала заданной формы (Фиг. 2-6). Однородность материала, как полагают авторы, выражается в а) равномерном распределении катионов переходных металлов в масштабе от 1 мкм (Фиг. 5) вплоть до ~10 нм, т.е. до размеров порядка одной частицы (Фиг. 6), и б) идентичности геометрических параметров частиц в объеме материала (Фиг. 2в).
На стадии в) заявляемых способов в реакционную смесь, полученную на стадии б), вносят:
- по меньшей мере одно соединение, которое является источником одного или нескольких из катионов Fe2+, Mn2+ и Co2+, где сумма мольных количеств катионов Fe, Mn и Co приблизительно равна мольному количеству Li3PO4; и
- по меньшей мере один органический сорастворитель, представляющий собой одноатомный или многоатомный органический спирт или смесь таких спиртов, в таком количестве, чтобы массовое содержание сорастворителя в реакционной смеси составляло от 20% до 80%.
В предпочтительном варианте осуществления указанные компоненты вносят в смесь, полученную на стадии б), при перемешивании.
В настоящем изобретении соединениями, являющимися источниками одного или нескольких из катионов Fe2+, Mn2+ и Co2+, являются известные специалистам соли железа, марганца и/или кобальта или гидраты таких солей, в том числе водные растворы этих веществ. В предпочтительном варианте осуществления соли железа, марганца и/или кобальта содержат Fe(II), Mn(II) и Co(II), однако возможно также использование солей этих металлов в других степенях окисления, при условии, что в раствор также добавляются восстановители, переводящие железо, марганец и/или кобальт в степень окисления +2. Более того, в предпочтительном варианте осуществления восстановитель может добавляться и к солям Fe(II), Mn(II) и/или Co(II) с целью поддержания катионов железа, марганца и/или кобальта в степени окисления +2. В качестве восстанавливающего агента в настоящем изобретении могут быть использованы различные известные специалистам восстанавливающие агенты, например аскорбиновая кислота, щавелевая кислота, сульфат гидразина и т.п.
В качестве примера подходящих соединений, являющихся источниками ионов Fe2+, можно привести сульфат железа (II), нитрат железа (II), хлорид железа (II), бромид железа (II), ацетат железа (II) и т. д., а также гидраты этих солей.
В качестве примера подходящих соединений, являющихся источниками ионов Mn2+, можно привести сульфат марганца (II), нитрат марганца (II), хлорид марганца (II), бромид марганца (II), ацетат марганца (II) и т. д.
В качестве примера подходящих соединений, являющихся источниками ионов Co2+, можно привести сульфат кобальта (II), нитрат кобальта (II), хлорид кобальта (II), бромид кобальта (II), ацетат кобальта (II) и т. д.
Особенно предпочтительные варианты источников катионов Fe2+, Mn2+ и Co2+ приведены в Таблице 1 ниже.
Таблица 1. Предпочтительные соединения переходных металлов, используемые в изобретении для получения LiFe1-x-yMnxCoyPO4 сольвотермальным методом
|
Количество соединения(й), являющегося(ихся) источником(ами) катионов Fe2+, Mn2+ и Co2+, выбирается таким образом, чтобы сумма мольных количеств катионов Fe, Mn и Co в смеси была приблизительно равна мольному количеству ионов PO43-. Например, отношение суммы мольных количеств катионов Fe, Mn и Co к мольному количеству Li3PO4 может лежать в диапазоне от 0,9:1 до 1,1:1, предпочтительно от 0,95:1 до 1,05:1, наиболее предпочтительно это отношение может быть равно 1:1.
Количество катионов Fe2+, Mn2+ и Co2+, добавляемых в реакционную смесь, предпочтительно выбирают таким образом, чтобы получить желаемые количества соответствующих катионов в продукте формулы LiFe1-x-yMnxCoyPO4. Например, в некоторых вариантах осуществления изобретения в получаемом продукте могут присутствовать все три катиона: Fe2+, Mn2+ и Co2+. В альтернативном варианте один или два из этих катионов могут отсутствовать, как, например, в случае отсутствия Co2+ или Mn2+ или в случает отсутствия как Co2+, так и Mn2+. В предпочтительном варианте осуществления катион Fe2+ обязательно присутствует в продукте, получаемом способами по изобретению, так что x+y меньше 1.
В качестве органического сорастворителя в настоящем изобретении можно использовать органические растворители, имеющие одну, две или более гидроксильных групп (т. е. одноатомные и многоатомные спирты), а также их смеси. Предпочтительными органическими растворителями являются одноатомные или многоатомные спирты, включающие от 2 до 8 атомов углерода, а также их смеси. Примерами органических растворителей, подходящих для использования в настоящем изобретении, являются этиловый спирт, бензиловый спирт, этиленгликоль, пропиленгликоль и т. п., а также их смеси.
Количество органического сорастворителя в настоящем изобретении выбирают таким образом, чтобы массовое содержание сорастворителя в реакционной смеси составляло от 20% до 80%. В предпочтительном варианте осуществления массовое содержание сорастворителя в реакционной смеси составляет от 30% до 70%, например от 40 до 60%.
На стадии г) заявляемых способов реакционную смесь, полученную на стадии в), нагревают при перемешивании в атмосфере инертного газа в автоклаве при температуре в диапазоне 190-210оC.
Под инертным газом в настоящем изобретении понимаются известные специалистам инертные газы, т. е. газы, не вступающие ни в какие в химические реакции в условиях, при которых осуществляются обсуждаемые способы. Примерами таких инертных газов могут быть азот, аргон и т. п.
Время нагрева реакционной смеси составляет по меньшей мере 1 час. В одном предпочтительном варианте осуществления нагрев осуществляют в течение по меньшей мере 2 часов, например в течение по меньшей мере 3 часов. Верхняя граница для диапазона подходящих времен нагрева в настоящем изобретении специально не ограничивается, но предпочтительно составляет менее 24 часов, более предпочтительно менее 6 часов, например менее 4 часов.
В настоящем изобретении в течение смешивания реагентов и в течение всей сольвотермальной обработки используется механическое перемешивание реакционной смеси, что позволяет добиться хорошей однородности получаемых порошков.
Кроме того, в некоторых вариантах осуществления настоящего изобретения с целью обеспечения привлекательных электрохимических характеристик синтезируемого электродного материала в способ получения может быть включена стадия отжига с источником углерода в качестве дополнительной стадии синтетического процесса. В ходе такой дополнительной стадии д) отжига вещество, полученное на стадии г) способа по изобретению, выделяют, смешивают с источником углерода и отжигают при 600-700оС в течение по меньшей мере 1 часа в атмосфере инертного газа, в результате чего получают композитный материал, описывающийся формулой LiFe1-x-yMnxCoyPO4/C, т. е. композитный материал, содержащий частицы LiFe1-x-yMnxCoyPO4 и углерод.
Источником углерода на стадии отжига способа по изобретению могут служить известные специалистам источники углерода, такие как сажа, графит, углеродные нанотрубки, графен, восстановленный оксид графита и/или органические соединения, такие как аскорбиновая кислота, лимонная кислота, уксусная кислота, глюкоза, сахароза и т. п.
Время отжига, как уже было указано, составляет по меньшей мере 1 час. В предпочтительно варианте осуществления время отжига составляет по меньшей мере 2 часа, например по меньшей мере 3 часа. Верхняя граница для диапазона подходящих времен отжига в настоящем изобретении специально не ограничивается, но предпочтительно составляет менее 10 часов, более предпочтительно менее 6 часов, например менее 4 часов.
Содержание углерода в композитном материале LiFe1-x-yMnxCoyPO4/C после отжига может составлять от 1 до 30% мас., предпочтительно от 1 до 20% мас., более предпочтительно от 1 до 10% мас., наиболее предпочтительно от 3 до 7% мас, например приблизительно 5% мас.
Для приготовления электродной композиции (катодной массы) электродный материал, полученный одним из способов по изобретению, смешивают с одной или несколькими электропроводящими добавками, одним или несколькими связующими и, при необходимости, с другими добавками, традиционно используемыми в данной области техники.
В качестве электропроводящей добавки могут использоваться, например, различные формы углерода, в т. ч. графит, сажа, углеродные нанотрубки и фуллерен, проводящие полимерные материалы (на основе полианилина, полипиролла, полиэтилендиокситиофена) и т.п. Содержание электропроводящих добавок в электродной композиции по изобретению может варьироваться от 1 до 20% мас.
В качестве связующего могут быть использованы, например, поливинилиденфторид в N-метилпирролидоне или суспензия перфторполиэтилена (фторопласт, тефлон) в воде.
Содержание связующего в электродной композиции может варьироваться от 1 до 20% мас.
Катод для литий-ионного аккумулятора может быть изготовлен из электродного материала по изобретению известными в данной области техники методами.
Далее настоящее изобретение будет описано более подробно с приведением конкретных примеров осуществления. Следует понимать, что данные примеры приведены исключительно для иллюстрации изобретения, и они не ограничивают объем изобретения.
Примеры
Общая методика
Материал LiFe1-x-yMnxCoyPO4 получают сольвотермальным синтезом с последующим отжигом для получения углерод-содержащего композита LiFe1-x-yMnxCoyPO4/C.
В рамках сольвотермального синтеза сначала готовят прекурсор (Li3PO4) смешением водных растворов LiOH и H3PO4 в мольном соотношении 3:1. Полученный прекурсор затем выдерживают в течение 1-5 часов при механическом перемешивании. К полученному прекурсору добавляют этиленгликоль с целью получения содержания спирта в смеси 20-80% мас. Затем в реакционную смесь добавляют соли Fe2+, Mn2+, Co2+ в необходимом количестве, а также восстанавливающий агент, например аскорбиновую кислоту, с целью поддержания степени окисления катионов железа +2 в ходе синтеза. Реактор продувают аргоном, помещают в гидротермальный реактор и выдерживают при температуре 190-210oС в течение 1-3 часов при интенсивном перемешивании на магнитной мешалке.
В результате проведения синтеза получают материал, представляющий собой соединение формулы LiFe1-x-yMnxCoyPO4, кристаллизующийся в орторомбической сингонии с параметрами элементарной ячейки, которые несколько варьируются в зависимости от элементного состава.
Для получения углерод-содержащего композита LiFe1-x-yMnxCoyPO4/C готовят смесь LiFe1-x-yMnxCoyPO4 и источника углерода. Полученную смесь тщательно перетирают и гомогенизируют в шаровой мельнице или ступке, а затем отжигают при 600-700°C в течение 1-10 часов в атмосфере аргона или азота. После осуществления отжига получают композит материала LiFe1-x-yMnxCoyPO4 с углеродом (доля углерода приблизительно 5%).
Образцы электродного материала LiFe1-x-yMnxCoyPO4 были охарактеризованы стандартным для данной области техники набором физико-химических методов исследования. Фазовый состав LiFe1-x-yMnxCoyPO4 был установлен методом рентгенофазового анализа (Bruker D8 Advance, CuKα1radiation, LynxEye PSD). Все полученные образцы LiFe1-x-yMnxCoyPO4 оказались однофазными. Химический состав образцов LiFe1-x-yMnxCoyPO4 был подтвержден методами атомно-эмиссионной спектроскопии с индуктивно связанной плазмой на масс-спектрометре фирмы «PerkinElmer SCIEX» и локальным рентгеноспектральным анализом на просвечивающем электронном микроскопе (JEOL JSM6490 LV, Wcathode, 20 kV, EDX spectrometer INCAX-Sight, Oxford Instruments). Морфология и ориентация частиц, а также локальный катионный состав образца LiFe0,5Mn0,5PO4, изучены с помощью просвечивающей электронной микроскопии (FEI Titan G3, 200 kV, Super-XEDX). Полученные частицы материала имеют форму пластин с линейными размерами 100-200 нм, толщиной 20-30 нм, ориентация частиц по наименьшему измерению в направлении [010]. Содержание углерода в образцах LiFe0,5Mn0,5PO4/C, установленное методом термогравиметрии (ТГ, термический анализатор TG-DSC STA-449, в атмосфере воздуха), не превышает 10% мас.
Для приготовления электродной композиции (катодной массы) полученный LiFe1-x-yMnxCoyPO4/C тщательно смешивают с одной или несколькими электропроводящими добавками и одним или несколькими связующими. Содержание электропроводящих добавок может варьироваться от 1 до 20% мас., связующего – также от 1 до 20% мас.
Электрохимические испытания образцов LiFe1-x-yMnxCoyPO4/С проводили методом гальваностатического циклирования в двухэлектродной ячейке относительно металлического лития c 1М раствором LiPF6 в этиленкарбонате:диметилкарбонате (1:1 об.) в качестве электролита. В качестве сепаратора использовалось борсиликатное стекловолокно, ячейка собиралась в боксе с атмосферой аргона MBraun. Катодную массу готовили смешением в ступке 75% электродного материала по изобретению, 12,5% поливинилидендифторида (ПВдФ) в N-метилпирролидоне и 12,5% ацетиленовой сажи (Timcal Super-C). Полученную пасту равномерно наносят на алюминиевую подложку (токосъемник), сушат и прокатывают на вальцах, затем вырезают электроды диаметром 16 мм, которые взвешивают и окончательно высушивают при пониженном давлении (10-2 атм) при 110°C в течение 12 часов для удаления остаточной воды и растворителя. Гальваностатические измерения полученных катодных материалов проводили на потенциостате Biologic VMP-3 (программное обеспечение EC-Lab) при комнатной температуре.
Пример 1.
Электродный материал LiFe0,5Mn0,5PO4 синтезируют сольвотермальным методом с последующим отжигом с источником углерода.
Первоначально получают Li3PO4. Для этого исходные реагенты 3,43 г LiOH*H2O и 3,06 г 87% H3PO4 растворяют в 15 мл дистиллированной H2O при постоянном перемешивании при 80°C. Образовавшийся осадок выдерживают в течение 3 часов. Далее, к осадку добавляют 15 мл этиленгликоля и 3,78 г FeSO4*7H2O, 2,30 г MnSO4*H2O, 0,14 г аскорбиновой кислоты. Автоклав продувается азотом и запечатывается. После запечатывания автоклав выдерживается в течение 3 часов при температуре 200oС и постоянном перемешивании.
По окончании процесса содержимое автоклава извлекают и центрифугируют 3 раза с дистиллированной водой для очистки от растворимых примесей. Полученный порошок сушат на воздухе. По данным EDX, катионный состав образца соответствует соотношению Fe:Mn = 0,49:0,51 c погрешностью ±3%.
Дифрактограмма полученного материала LiFe0,5Mn0,5PO4 показана на Фиг. 3.
На Фиг. 4 приведены микрофотографии частиц материала и результаты изучения образца LiFe0,5Mn0,5PO4 методом просвечивающей электронной микроскопии (TEM).
На Фиг. 5 приведены результаты изучения образца LiFe0,5Mn0,5PO4 методом сканирующей просвечивающей электронной микроскопии в электронах, рассеянных на большие углы (HAADF-STEM) и анализа поверхности частиц методом рентгеноспектрального локального микроанализа (РСЛМА, EDX) на пространственной шкале 1 микрон.
На Фиг. 6 приведены результаты изучения образца LiFe0,5Mn0,5PO4 методом сканирующей просвечивающей электронной микроскопии в электронах, рассеянных на большие углы (HAADF-STEM) и анализа поверхности частиц методом рентгеноспектрального локального микроанализа (РСЛМА, EDX) на пространственной шкале ~10 нанометров.
Для получения углерод-проводящего покрытия полученный LiFe0,5Mn0,5PO4 смешивают с глюкозой (в массовом соотношении 0,8:0,2) и тщательно перетирают в ступке под ацетоном или в планетарной мельнице. Полученную смесь отжигают в токе аргона в течение 3 часов при температуре 650oС. Количество сажи в полученном композите LiFe0,5Mn0,5PO4/C определяют методом термогравиметрии.
На Фиг. 7 приведены результаты электрохимического тестирования LiFe0,5Mn0,5PO4/C в литий-ионной полуячейке в интервале потенциалов 2,2-4,3 В отн. Li/Li+, при комнатной температуре при различных скоростях разряда. Электрохимическая разрядная емкость такого материала при плотности тока С/10 составляет 152 мАч/г, при плотности тока 10С – 128 мАч/г.
Пример 1А.
Электродный материал LiFe0,5Mn0,5PO4 синтезируют по схеме, описанной в примере 1, за исключением того, что осадок Li3PO4 выдерживали в течение 0, 1 и 5 часов, соответственно.
Морфология свежеосажденного прекурсора Li3PO4 в зависимости от времени выдерживания осадка в растворе показано на Фиг. 1: (а) выдерживание в течение 0 часов, (б) выдерживание в течение 1 часа, (в) выдерживание в течение 5 часов.
На Фиг. 2 проиллюстрирована морфология катодного материала LiFe0,5Mn0,5PO4, полученного при различных временах выдерживания свежеосажденного прекурсора Li3PO4 в растворе: 0 часов (а), 1 час (б) и 5 часов (в).
На Фиг. 8 приведены результаты циклирования (разрядная емкость) при скорости заряда/разряда 1С для катодного материала LiFe0,5Mn0,5PO4/C, полученного при различных временах выдерживания свежеосажденного прекурсора Li3PO4 в растворе: 0 часов, 1 час и 5 часов (а). Для каждого времени выдерживания приведен отдельный график значений разрядной емкости с линейной аппроксимацией среднего значения. Тангенс угла наклона в приведенных координатах составил -0,015 для t = 0 часов (б), -0,007 для t = 1 час (в) и -0,003 для t = 5 часов (г).
Как видно из представленных данных, в данном примере удалось убедительно показать, что время выдерживания осадка Li3PO4 чрезвычайно важно для достижения выгодных электрохимических характеристик электродного материала формулы LiFe1-x-yMnxCoyPO4.
Пример 2.
Электродный материал LiFePO4/C синтезируют по схеме, описанной в примере 1, только в качестве исходных компонентов используют FeSO4*7H2O в количестве, соответствующем количеству молей Li3PO4.
Дифрактограмма материала LiFePO4 приведена на Фиг. 3.
Электрохимическая разрядная емкость композита LiFePO4/C при плотности тока С/10 составляет 158 мАч/г, при плотности тока 10С – 124 мАч/г.
Пример 3.
Электродный материал LiFe0,25Mn0,75PO4/C синтезируют по схеме, описанной в примере 1, только мольное соотношение исходных компонентов FeSO4*7H2O и MnSO4*H2O соответствует 1:3, а в качестве сорастворителя выступает пропиленгликоль. По данным EDX, катионный состав получаемого образца соответствует соотношению Fe:Mn = 0,26:0,74 c погрешностью ±3%.
Электрохимическая разрядная емкость композита LiFe0,25Mn0,75PO4/C при плотности тока С/10 составляет 144 мАч/г, при плотности тока 10С – 120 мАч/г.
Пример 4
Электродный материал LiFe0,25Mn0,75PO4/C синтезируют по схеме, описанной в примере 1, но в качестве сорастворителя выступает бензиловый спирт. По данным EDX, катионный состав получаемого образца соответствует соотношению Fe:Mn = 0,23:0,77 c погрешностью ±3%.
Электрохимическая разрядная емкость композита LiFe0,25Mn0,75PO4/C при плотности тока С/10 составляет 130 мАч/г, при плотности тока 10С – 110 мАч/г.
Пример 5.
Электродный материал LiFe1/3Mn1/3Co1/3PO4/C синтезируют по схеме, описанной в примере 1, только в качестве исходных компонентов используют FeSO4*7H2O, MnSO4*H2O и CoSO4*7H2O в количестве, соответствующем 1/3 мольного количества Li3PO4 для каждого из сульфатов. По данным EDX, катионный состав получаемого образца соответствует соотношению Fe:Mn:Co = 0,34:0,31:0,35 c погрешностью ±3%.
Дифрактограмма материала LiFe1/3Mn1/3Co1/3PO4 приведена на Фиг. 3.
Электрохимическая разрядная емкость композита LiFe1/3Mn1/3Co1/3PO4/C при плотности тока С/10 составляет 145 мАч/г, при плотности тока 10С – 71 мАч/г.
Композиты LiFe1-x-yMnxCoyPO4/C, полученные способом по настоящему изобретению, обеспечивает стабильную разрядную емкость на высоких скоростях циклирования (3С-50C, время разряда 20 мин – 72 сек). Так, в Примере 1 удалось добиться сохранения более 69% от первоначальной удельной емкости (т. е. удельной емкости при скорости C/10) даже при плотности тока 50С (см. Фиг. 7). По величине энергоемкости, достигаемой на высоких плотностях тока, материалы, получаемые по предложенной в настоящем изобретении методике, превосходят катодные материалы, полученные гидро- и/или сольвотермальными методами синтеза, описанными в документах-аналогах из уровня техники (см. Таблицу 2):
Таблица 2. Сравнение характеристик образцов LiFe1-xMnxPO4/С со структурой оливина, полученных гидро- и сольвотермальным синтезом, по изобретению с лучшими известными аналогами. Приведены данные для тех аналогов, которые демонстрируют наибольшую разрядную емкость при плотности тока 10С.
|
Результаты разряда на плотности тока выше 10С в указанных в Таблице 2 документах уровня техники не приведены. В случае катодного материала LiFe0,5Mn0,5PO4/C, полученного способом по изобретению, при скорости циклирования 20С и 50С (т. е. при плотности тока в 2 и 5 раз выше, чем максимальная показанная в Таблице 2), емкость составила 81% и 69% от первоначальной, соответственно, что говорят о высокой работоспособности материала при повышенных нагрузках.
Материал по изобретению, соответствующий значениям x = y = 0, т.е. LiFePO4, также обладает улучшенными электрохимическими характеристиками при высоких плотностях тока разряда. Например, в документе RU 2402114 C1 приведены данные для разряда материала на основе LiFePO4 при плотностях тока С/10 и 10С – 140 и 80 мАч/г, соответственно. Материал на основе LiFePO4, полученный по предложенной в настоящем изобретении методике, в аналогичных условиях демонстрирует разрядную емкость 158 и 124 мАч/г, соответственно.