Результат интеллектуальной деятельности: Средство для стимулирования адаптации организма к экстремальным и стрессовым факторам и способ стимулирования адаптации организма к экстремальным и стрессовым факторам
Вид РИД
Изобретение
Изобретения относятся к фармацевтической промышленности и могут быть использованы для снижения последствий стрессовых ситуаций организма как при применении индивидуальной композиции алкил-глицериновых эфиров (АГЭ), так и в сочетании с другими веществами, обладающими биологическим действием.
Психические и неврологические расстройства, включая разные виды стресса, распространены во всех регионах мира. Они поражают каждое сообщество и каждую возрастную группу в странах с разными уровнями дохода. На эти расстройства приходится 14% глобального бремени болезней (Программа охраны психического здоровья Всемирной организации здравоохранения. Доступно: http://www.who.int/mental_health/mhgap/en/).
Социально-бытовая обстановка создаёт длительный, постоянный психоэмоциональный стресс у подавляющего большинства людей. Постоянное умственное и психоэмоциональное напряжение, нарушение режима труда, отдыха и питания часто приводят к срыву механизмов адаптации и развитию заболевания. Неспособность справиться с воздействием рабочих стрессоров эмпирически связана с рядом неблагоприятных состояний, таких как дисфункция желудочно-кишечного тракта, скелетно-мышечные проблемы, заболевания сердечно-сосудистой системы (Van der Doef M., Maes C. The job demand-control (-support) model and physical health outcomes: A review of the strain and buffer hypothesis // Psychology and health. 1998. 13, 909-936).
В мировой практике в качестве антистрессовых препаратов используют большую группу психотропных лекарственных средств (нейролептики, транквилизаторы, седативные средства, антидепрессанты, стимуляторы центральной нервной системы и пр.) (Машковский М.Д. «Лекарственные средства. Пособие для врачей». 16-е изд., 2012. М: Новая волна. С. 50-139). В эту группу входят преимущественно синтетические препараты, такие, как – аминазин, феназепам, амитриптилин, ацефен и др., наряду с природными – валерианой, зверобоем, женьшенем, элеутерококком, родиолой розовой и др. Однако, ограниченным количеством препаратов проблемы стрессовых ситуаций решены быть не могут – слишком многообразны вызовы, стоящие перед современным человеком и слишком вариабелен ответ организма каждого из нас на прием того или иного средства.
Так, известно использование для борьбы с последствиями сильного, особенно психологического стресса производных бензодиазепина, в частности диазепам (сибазон, седуксен, реланиум) (Машковский М.Д. «Лекарственные средства. Пособие для врачей». 16-е изд., 2012. М: Новая волна. С. 78-79). Однако его использование сопряжено с целым рядом отрицательных и побочных последствий. Возможны сонливость, лёгкое головокружение, неуверенность походки, кожный зуд, тошнота, запор, нарушения менструального цикла, понижение либидо. В отдельных случаях в начале лечения может наблюдаться возбуждение. Препарат противопоказан при острых заболеваниях печени и почек, при тяжёлой миастении. Не следует назначать женщинам во время беременности. Препарат не следует применять во время и накануне работы водителям транспорта и другим лицам, работа которых требует быстрой умственной и физической реакции. Во время приёма препаратов этой группы необходимо строго воздержаться от употребления спиртных напитков. Из-за возможного возникновения психологической зависимости длительность непрерывного лечения не должна превышать двух месяцев.
Всё это делает препарат абсолютно неприменимым для профилактического использования, особенно длительного.
Для стимулирования адаптации организма (профилактики) и устранения последствий стрессовых ситуаций применяется экстракт элеутерококка (Машковский М.Д. «Лекарственные средства. Пособие для врачей». 16-е изд., 2012. М: Новая волна. С. 134). Экстракт оказывает адаптогенное действие, повышает неспецифическую резистентность организма, обладает стимулирующим действием на центральную нервную систему, устраняет переутомление, раздражительность, восстанавливает и повышает физическую и умственную работоспособность, защищает от неблагоприятных факторов внешней среды. Побочное действие – аллергические реакции, бессонница, гипогликемия. Противопоказаниями являются гиперчувствительность, артериальная гипертензия, повышенная возбудимость, острые инфекционные заболевания, инфаркт миокарда, аритмии, бессонница, церебрально-сосудистая патология, беременность и период лактации, возраст до 12 лет (ViDAL. Справочник лекарственных средств https://www.vidal.ru/).
Известно использование для лечения при стрессовых ситуациях женьшеня, как в виде настойки, так и в виде других лекарственных форм (Машковский М.Д. «Лекарственные средства. Пособие для врачей». 16-е изд., 2012. М: Новая волна. С. 133-134).
Препараты женьшеня оказывают стимулирующее воздействие на центральную нервную систему, повышают умственную и физическую работоспособность, регулируют работу желёз внутренней секреции, незначительно снижают артериальное давление, а также уровень холестерина и глюкозы в сыворотке крови. У женьшеня чётко выражена сезонность действия: применение осенью и зимой наиболее эффективно (ViDAL. Справочник лекарственных средств https://www.vidal.ru/).
Однако эти препараты также обладают довольно большим спектром побочных действий. К ним относятся тахикардия, повышение артериального давления, носовое кровотечение, нарушение сна, головная боль, нервозность, возбуждение, тошнота, рвота, диарея, гипогликемия, кожные аллергические реакции. Они противопоказаны при артериальной гипертензии, эпилепсии, судорожных состояниях, повышенной возбудимости, расстройствах сна (бессонница), кровоточивости, острых инфекционных заболеваниях, детям до 12 лет, в период беременности и лактации. Во избежание нарушений сна препараты женьшеня не рекомендуется применять во второй половине дня. Их следует применять с осторожностью у пациентов с сердечно-сосудистыми заболеваниями и сахарным диабетом (Машковский М.Д. «Лекарственные средства. Пособие для врачей». 16-е изд., 2012. М: Новая волна. С. 133-134; ViDAL. Справочник лекарственных средств https://www.vidal.ru/).
Техническая проблема, на решение которой направлена заявляемая группа изобретений, является расширение арсенала средств, обладающих антистрессовым действием и используемых для стимулирования адаптации организма к экстремальным и стрессовым факторам, а также не имеющих побочных действий.
Поставленная техническая проблема решается тем, что в качестве средства для стимулирования адаптации организма к экстремальным и стрессовым факторам, предлагается использовать морские алкил-глицериновые эфиры (АГЭ).
Сведений о проявлении морскими алкил-глицериновыми эфирами антистрессового воздействия на организм человека (и животных) из уровня техники заявителем не найдено. К морским алкил-глицериновым эфирам относятся батиловый, селахиловый и химиловый спирт, структурные формулы этих соединений представлены на фиг.1.
Заявителем впервые обнаружено, что применение морских алкил-глицериновых эфиров в качестве средства стимулирования адаптации организма к экстремальным и стрессовым факторам, продемонстрировало неожиданный для этих соединений результат, а именно снижение негативного воздействия стресса на организм.
Источником для получения природных алкил-глицериновых эфиров являются морские гидробионты. Значительные количества липидов с простой эфирной связью обнаружены в морских гидробионтах – хрящевых рыбах (акулах, скатах, химерах) (Bakes M.J., Nichols P.D. Lipid, fatty acid and squalene composition of liver oil from six species of deep-sea sharks collected in southern Australian waters // Comp. Biochem. Physiol. B. 1995. 110, 267-275; Magnusson C.D., Haraldsson G.G. Ether lipids // Chem. Phys. Lipids. 2011. 164, 315-340), моллюсках (Hayashi, K.; Kishimura H. Amount and composition of diacyl glyceryl ethers in various tissue lipids of the deep-sea squid Berryteuthis magister // Journal of Oleo Science. 2002. 51, 523-529), морских звездах (Hayashi K., Kishimura H. Content and composition of diacyl glyceryl ethers in the pyloric ceca and ovaries of the asteroids Solaster paxillatus and Asterias amurensis // Fisheries Science. 1997. 63, 945-949), зоопланктоне (Phleger C.F. et al. Lipids and buoyancy in southern ocean pteropods // Lipids. 1997. 32, 1093-1100) и других объектах, что может способствовать созданию лекарств с широким спектром компенсаторного действия. Морские (природные) алкил-глицериновые эфиры, получаемые из сырья морского происхождения, в частности, из кальмара, краба, ската, акул, моллюсков, планктона, отличаются от синтетических тем, что имеет строгую пространственную структуру. Добиться такой селективности при химическом синтезе невозможно – изомеры продуктов составляют до 50%. Ни о какой биологической активности этих соединений говорить не приходится – это биологические яды.
Для решения заявленной технической проблемы заявителем разработан новый способ стимулирования адаптации организма к экстремальным и стрессовым факторам.
Известен способ повышения адаптационных возможностей организма в условиях теплового стресса, включающий ежедневное введение препарата Цитофлавин внутрибрюшинно в дозе 100 мг/кг массы в течение 14 дней (патент РФ №2553374, МПК A61K 31/194, A61P 43/00, опубл. 30.12.2015 г.).
Недостатками известного способа является использование лекарственного средства, имеющего ряд побочных эффектов. Абсолютными медицинскими противопоказаниями для приема таблеток Цитофлавин являются возраст пациента до 18-ти лет (нет достаточных данных о безопасности и эффективности препарата для детей) и индивидуальная непереносимость любого из компонентов препарата. С осторожностью данное лекарственное средство применяется при сопутствующей хронической патологии органов системы пищеварения (эрозии, язвы желудка или двенадцатиперстной кишки, гастрит, дуоденит) в стадии обострения, артериальной гипертонии (повышенное артериальное давление), нефролитиазе (формирование нерастворимых конкрементов в почках), подагре и повышенном уровне мочевой кислоты в крови (гиперурикемия).
При приеме препарата Цитофлавин возможно развитие негативных патологических реакций со стороны нескольких органов и систем:
1) система пищеварения – болевые ощущения, дискомфорт в области желудка (эпигастрий);
2) нервная система – головная боль;
3) метаболизм – снижение уровня глюкозы в крови (гипогликемия);
4) повышение концентрации мочевой кислоты (гиперурикемия);
5) обострение подагры; 6) аллергические реакции – покраснение (гиперемия) кожи, зуд.
Перед назначением препарата Цитофлавин врач должен обязательно обращать внимание на несколько особых указаний и мер предосторожности:
1) на фоне приема данного лекарственного средства при сопутствующей артериальной гипертонии может понадобиться коррекция антигипертензивных препаратов (лекарственные средства, снижающие артериальное давление);
2) у пациентов с сопутствующим сахарным диабетом на фоне приема таблеток Цитофлавин может понадобиться коррекция дозировки инсулина или препаратов, снижающих уровень сахара в крови.
3) рибофлавин, который входит в состав препарата, может снижать активность некоторых антибактериальных средств (тетрациклин, линкомицин, эритромицин), поэтому об их возможном применении следует предупредить лечащего врача;
4) данных о достаточной эффективности и безопасности данного лекарственного средства для беременных и кормящих грудью женщин на сегодняшний день нет, поэтому применение таблеток Цитофлавин для данных категорий пациентов не рекомендуется.
Даже в аптечной сети таблетки Цитофлавин отпускаются по рецепту врача. Исключается их самостоятельный прием, так как это может стать причиной негативных последствий для организма. Таким образом, основным недостатком известного способа является использование в качестве активного начала препарата, имеющего слишком много побочных действий.
Наиболее близким к заявляемому изобретению является способ стимулирования и адаптации организма к экстремальным и стрессовым факторам путем введения водного раствора активного начала, в котором в качестве активного начала используют композицию, содержащую высокодисперсное металлическое серебро и поли-N-винилпирролидон при соотношении компонентов (массовые части): поли-N-винилпирролидон – 1; Серебро - 0,01 - 2,33, при этом поли-N-винилпирролидон берут с молекулярной массой от 6000 до 40000 ед., активное начало вводят внутрижелудочно или внутримышечно в дозах от 1 до 300 мг/кг массы тела (патент РФ №2108789, А61К 31/79, опубл. 20.04.1998).
Авторы данного изобретения заявляют о высокой эффективности защиты от гипоксии, шока, боли и др. Однако авторы не приводят никаких возможных негативных явлений такой стимуляции на организм. Хотя широко известно о высоком токсическом действии атомарного серебра. Это одно из соединений, ничтожные концентрации которого являются смертельными для множества микроорганизмов и бактерий, а также для различных видов клеток, с которыми оно контактирует. Если внутрижелудочный прием будет способствовать снижению общего числа патогенных микроорганизмов, то механизм внутримыщечного действия, можно рассмотреть при данной стимуляции, как «от обратного». То есть локальная гибель клеток из-за нарушения метаболизма, первично вызывает в организме внутренний стресс и организм мобилизует все имеющиеся у него резервы для восстановления нормальной деятельности. Именно эта вспышка обеспечивает происходящую стимуляцию. Но продолжительность такого действия не может быть значительной, так как резервы организма истощаются. Исследований авторов недостаточно, чтобы говорить о безопасности таких процедур. Авторы не пишут, что они вкладывают в понятие «высокодисперсное серебро». Если это наноструктуры или хотя бы их часть (что авторами не показано и не опровергнуто), то известно, что в этом случае серебро оказывает генотоксический эффект, разрушая целостность ДНК, вызывая перестройки в хромосомах и повреждая геномы в сперматозоидах; негативно воздействует на сердечный ритм, частоту дыхания и координацию тела; накапливаясь в тканях наночастицы провоцируют отеки и некрозы. К тому же, длительный прием препаратов серебра может вызвать аргирию с необратимой пигментацией кожи и слизистых оболочек; Роспотребнадзор относит серебро, наряду со свинцом, ко 2 классу опасности – высокоопасное химическое вещество.
Необходимы серьезные биологические испытания, чтобы предлагать данный вид стимуляции. В отношении второго компонента - поли-N-винилпироллидона, выступающего носителем дисперсного серебра, можно сказать следующее. Как правило, поли-N-винилпирролидон считается безопасным и не вызывает серьезных побочных эффектов, однако были зафиксированы случаи аллергических реакций на поли-N-винилпирролидон, особенно в отношении его подкожного применения и ситуаций, когда поли-N-винилпирролидон вступает в контакт с аутологичной сывороткой и слизистыми оболочками.
Основным недостатком данного способа является использование в качестве активного начала 2-х компонентной композиции, содержащей вещества с неоднозначным биологическим действием, что может привести, сразу или в дальнейшем, к серьезным проблемам для организма, вследствие чего, рекомендовать его к широкому применению преждевременно.
Поставленная техническая проблема решается также тем, что в известном способе стимулирования адаптации организма к экстремальным и стрессовым факторам путем введения активного начала, согласно изобретению, в качестве активного начала используют морские алкил-глицериновые эфиры в дозах от 15 до 157 мг/кг массы не менее одного месяца.
Экспериментально установлено, что введение морских АГЭ в количестве менее 15 мг/кг массы не оказывает положительного эффекта на стрессированный организм, т.е. не обеспечивает достижение заявленного результата. В то же время введение морских АГЭ в количестве 157 мг/кг массы, практически восстанавливает все системы организма к прежнему уровню, т.е. обеспечивает стимулирование адаптации организма к экстремальным и стрессовым факторам, поэтому повышение дозы морских АГЭ нецелесообразно.
С целью достижения заявленного технического эффекта препарат морских АГЭ следует принимать не менее 1 месяца.
Способ легко осуществим, так как предполагает только пероральный прием морских АГЭ. К тому же в мировой практике при использовании препаратов морских АГЭ не наблюдали никаких побочных эффектов и противопоказаний. Заявитель также при проведении экспериментов не выявил никаких побочных эффектов.
Изобретения осуществляют следующим образом.
В исследовании использовались препараты морских алкил-глицериновых эфиров, полученные известными методами из дальневосточных промысловых гидробионтов.
Приготовление препарата морских алкил-глицериновых эфиров
Кальмар Berryteuthis magister был выловлен в Беринговом море в сентябре 2017 г. Камчатский краб Paralithodes camtschaticus добыт в Татарском проливе в ноябре 2017 г. Скат Bathyraja parmifera выловлен в июле 2017 г. в заливе Петра Великого Японского моря. После переработки отделенную печень (пищеварительную железу) хранили в течение 3 мес. при −18°C. Все химические реактивы и растворители для хроматографии были аналитической чистоты (Sigma–Aldrich, USA).
Экстракцию общих липидов проводили по методу Блай и Дайера (Bligh E.G., Dyer W.J. A rapid method of total lipid extraction and purification // Can. J. Biochem. Physiol. 1959. 37, 911–917), гидролиз липидов – методом Кристи (Christie W.W. Lipid Analysis: Isolation, separation, identification and structural analysis of lipids. The oily Press, Bridgwater (UK), 2003. 415 р.).
Осаждение АГЭ из омыленных липидов проведено двойной кристаллизацией из ацетона при различных температурах (Ermolenko E. et al. Technological approach of 1-O-alkyl-sn-glycerols separation from Berryteuthis magister squid liver oil // J. Food. Sci. Technol. DOI 10.1007/s13197-015-2148-x).
Определение состава АГЭ
Состав АГЭ в виде их триметилсилильных производных TMS-АГЭ был определен газожидкостной хроматографией (ГХ) и газожидкостной хроматографией с масс-спектрометрией (ГХ-MС).
TMS-АГЭ были приготовлены следующим образом: 50 мкл N,Oбис(триметилсилил)трифтороацетамид (N,OBis(trimethylsilyl)trifluoroacetamide (BSTFA)) было добавлено к 5 мг АГЭ; смесь нагревали до 80°C в течение 1 ч. После добавления 200 мкл гексана, 1 мкл каждой силилированной фракции был введен в хроматограф. Состав TMS-АГЭ определяли методом ГХ, используя хроматограф «Shimadzu GC-2010» (Япония) с пламенно-ионизационным детектором и капиллярной колонкой «Supelco SLB™-5», 30 м× 0.25 мм (США). Разделение смеси компонентов проводили при следующих условиях: начальная температура 200°C, нагрев - 2 °C/мин до 290°C, выдержка при этой температуре в течение 35 мин. Температура инжектора - 270°C, детектора - 250°C. АГЭ идентифицировали сравнением с известными стандартами. ГХ-МС была использована для идентификации структуры TMS-АГЭ. Спектр электронных ударов регистрировали, используя прибор «Shimadzu TQ-8040» (Япония) с колонкой «Supelco SLB™-5» при 70 eV с теми же температурами, как при ГХ.
Выделенные фракции АГЭ содержат смесь батилового, химилового и селахилового спиртов, с преобладанием химилового спирта. Структурные формулы АГЭ представлены на фиг.1, где А- химическая структура батилового спирта; Б - химическая структура селахилового спирта; В – химическая структура химилового спирта.
Общее содержание морских АГЭ во фракциях, выделенных из различных видов сырья морского происхождения приведено в таблице 1.
Полученный препарат морских АГЭ, содержащий смесь батилового, селахилового и химилового спиртов, представляет собой белый рассыпчатый порошок без запаха.
Для подтверждения эффективности воздействия морских АГЭ при стрессовой ситуации были проведены эксперименты на животных. При этом в качестве показателей, отражающих положительное защитное действие морских АГЭ при стрессе на организм, регистрировались уровень гемоглобина, активность каталазы, содержание малонового диальдегида, степень поражения слизистой оболочки желудка, измеряли массу тела животных, массу надпочечников, селезёнки и тимуса, проводили гистологическое исследование гиппокампа.
Изобретения иллюстрируются следующими фигурами и таблицами.
Фиг.1. Структурные формулы морских АГЭ, где А- химическая структура батилового спирта; Б - химическая структура селахилового спирта и В - химическая структура химилового спирта;
Фиг. 2. Активность каталазы;
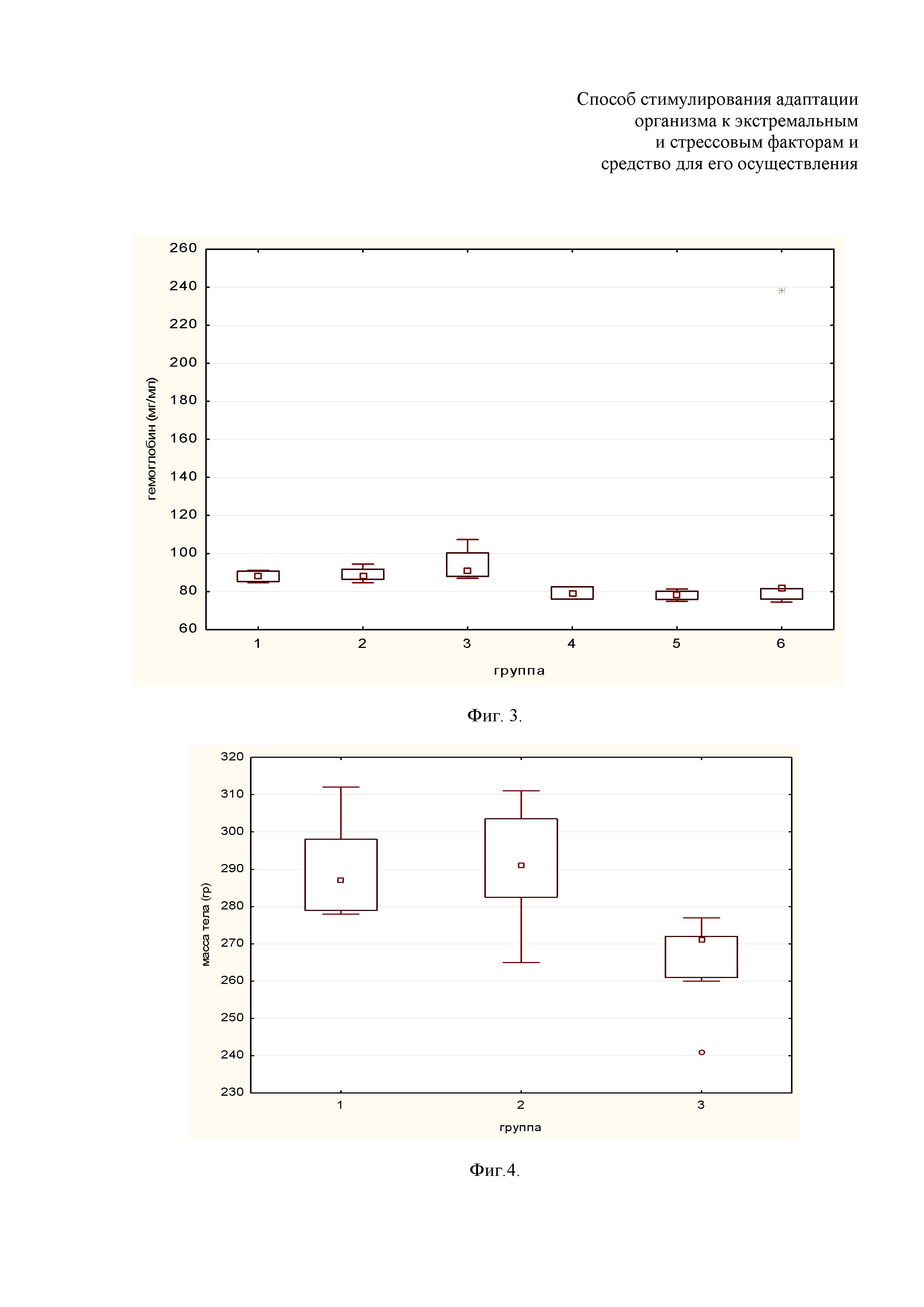
Фиг. 3. Уровень гемоглобина;
Фиг. 4. Масса тела;
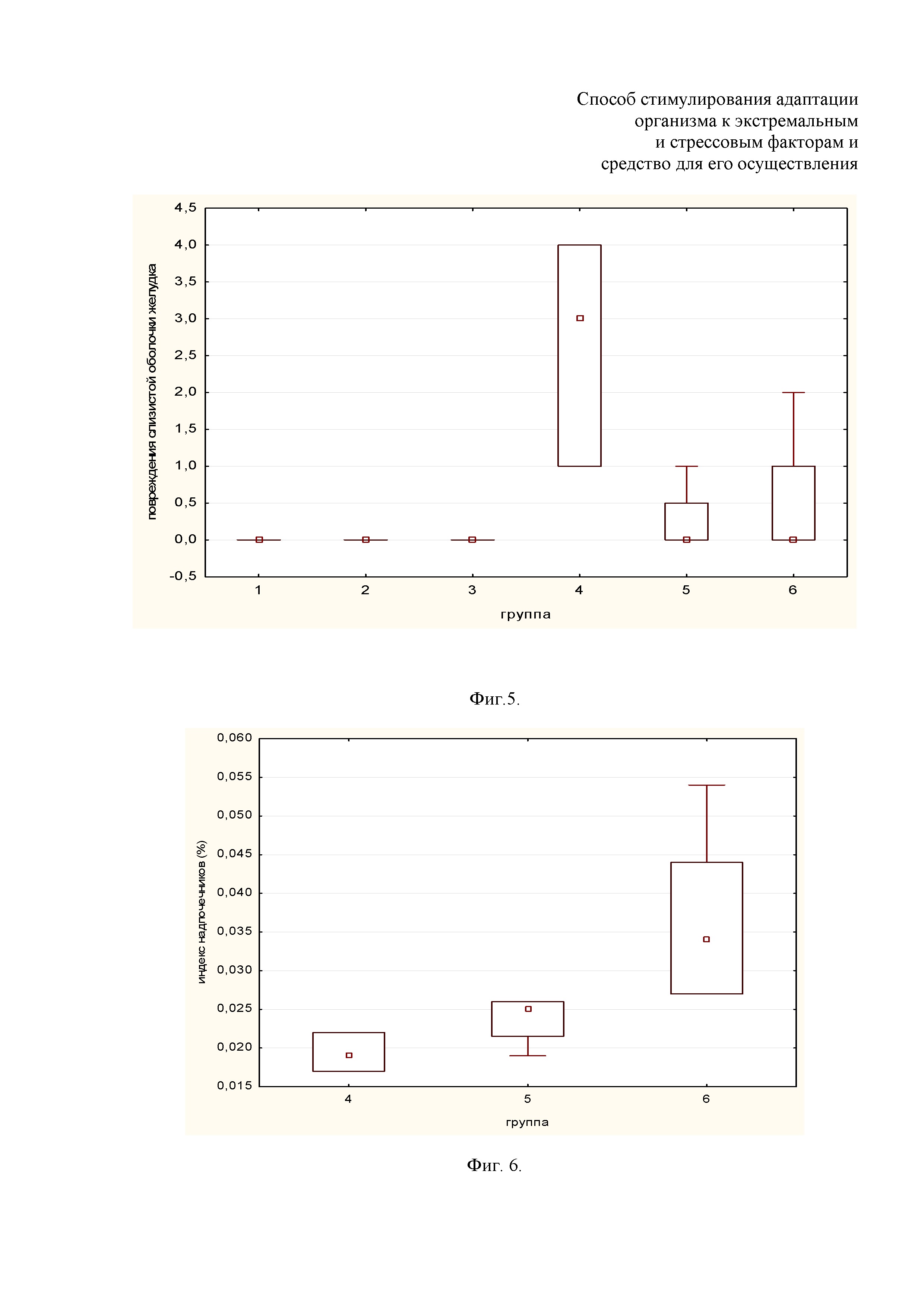
Фиг. 5. Эрозивные повреждения слизистой оболочки желудка;
Фиг. 6. Индекс надпочечников;
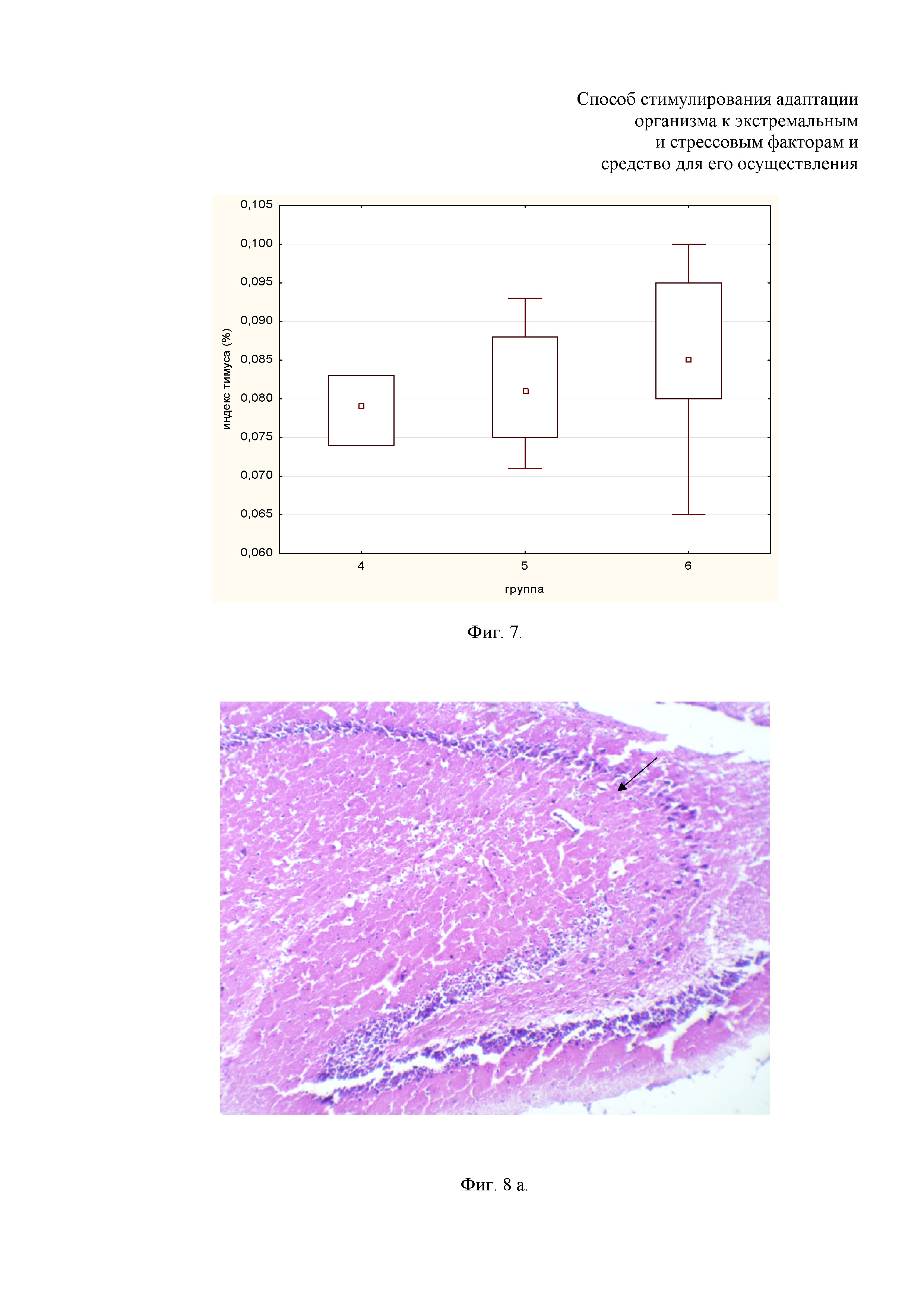
Фиг. 7. Индекс тимуса.
На представленных Фиг. 2.-7 малым квадратом обозначена медиана, большими прямоугольными столбцами данные 25-75% определений, вертикальными прямоугольными линиями – размах определений без выброса, кружком и звездочкой – выбросы и крайние точки, соответственно (если есть).
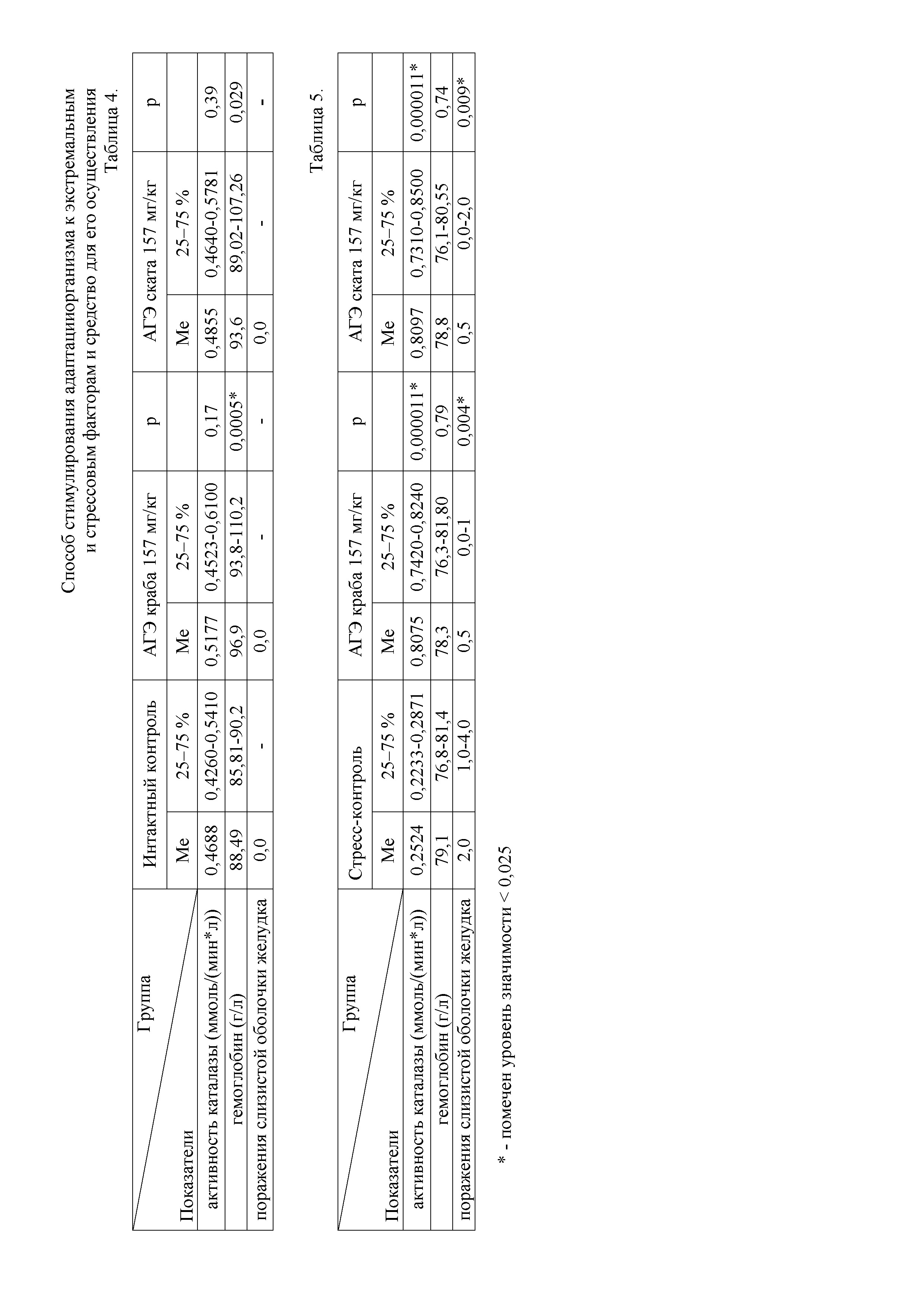
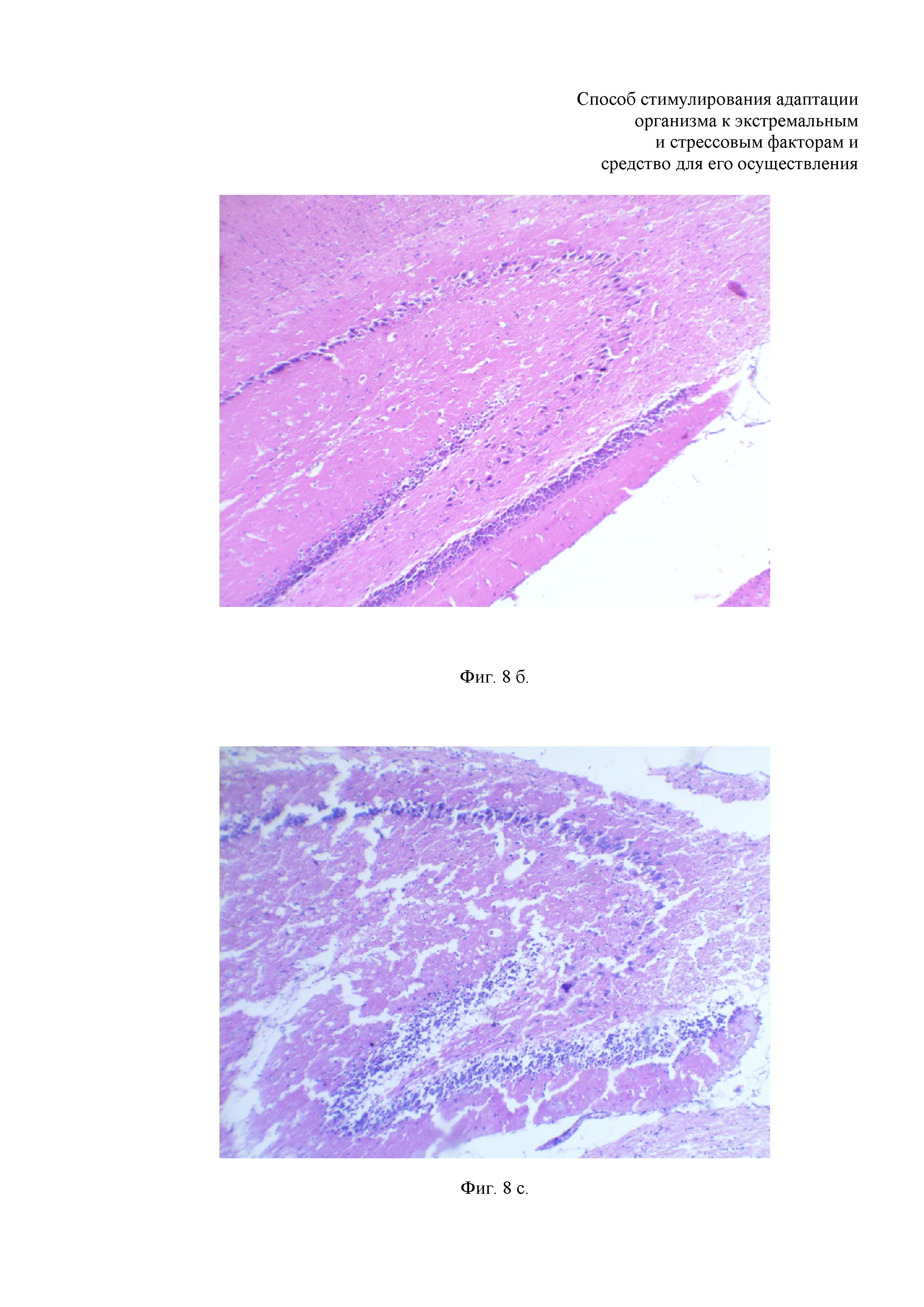
Фиг. 8. Зона СА3 гиппокампа, микрофото. ув. × 100, где на Фиг. 8а - стрелкой указана зона с уменьшенным количеством нейронов; на Фиг. 8б – показано уменьшение среднего числа клеток; на Фиг. 8в - контроль.
Таблица 1. Содержание морских АГЭ в препаратах;
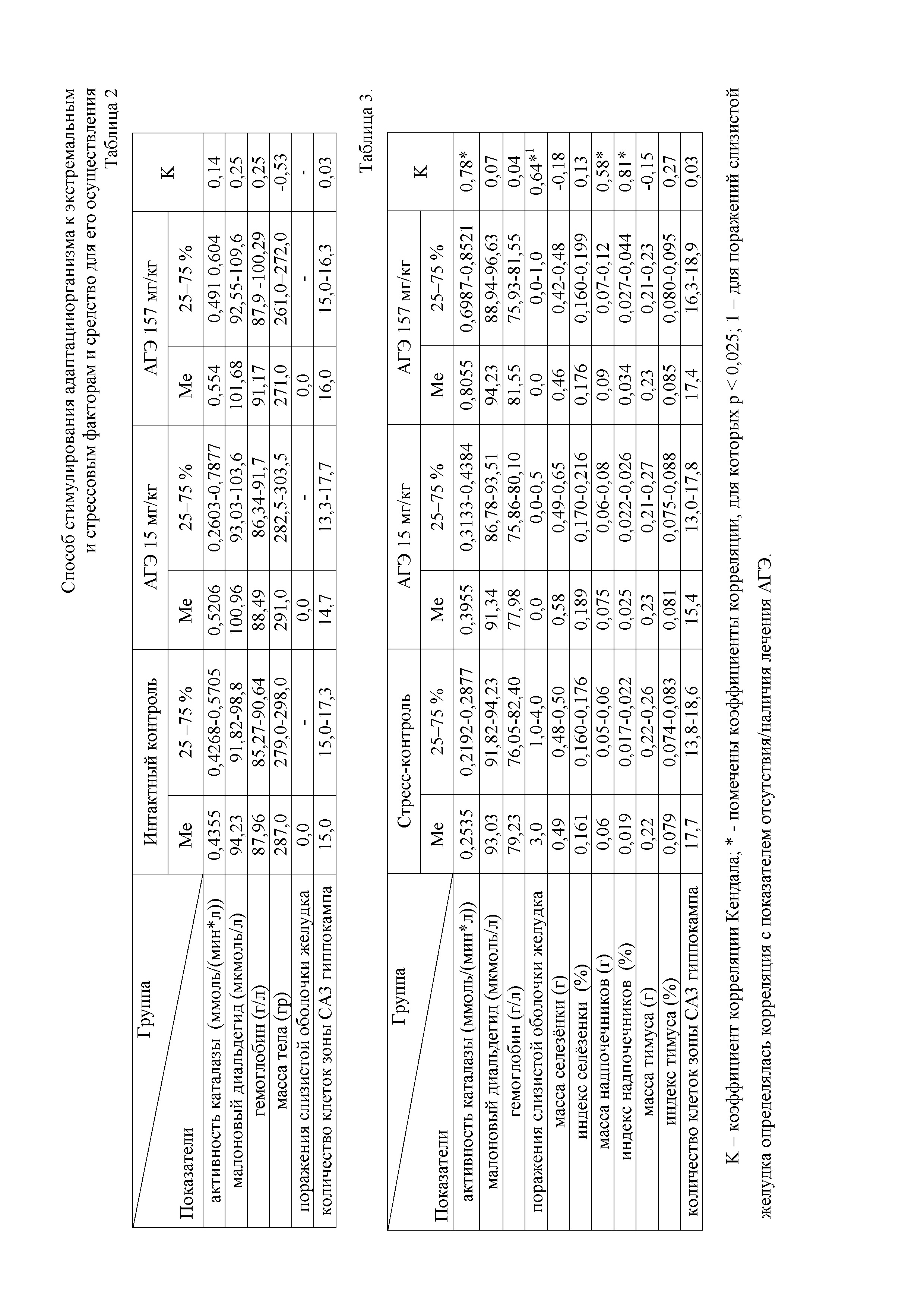
Таблица 2. Влияние различных доз морских АГЭ на состояние животных;
Таблица 3. Действие морских АГЭ при остром иммобилизационном стрессе;
Таблица 4. Действие морских АГЭ, выделенных из гепатопанкреаса краба и печени ската;
Таблица 5. Действие морских АГЭ, выделенных из гепатопанкреаса краба и печени ската, при остром иммобилизационном стрессе.
Пример 1. Способ лечения острого стресса морскими алкил-глицериновыми эфирами, получаемыми из сырья морского происхождения.
Животные
Исследование проводилось на 60 самцах крыс линии Wistar, содержащихся в условиях вивария при свободном доступе к пище и воде, одинаковом рацион питания. Все процедуры были одобрены Комитетом по этике работы с животными при «Национальном научном центре морской биологии» Дальневосточного отделения Российской академии наук (ННЦМБ ДВО РАН) в соответствии с рекомендациями Лаборатории по охране животных.
Биологический эксперимент (тестирование на животных)
В эксперименте использовали препарат из пищеварительной железы кальмара, содержащий 99% морских АГЭ с преимущественным содержанием химилового спирта (Фиг. 1). Перед использованием на животных, препарат АГЭ диспергировали в воде.
Крысы опытных групп в течение месяца получали морских АГЭ перорально через зонд в дозе 15 и 157 мг/кг.
Животные были разбиты на группы, в каждой из которых было по 10 животных:
группа 1 – интактный контроль;
группа 2 – животные, получавшие морских АГЭ в дозе 15 мг/кг;
группа 3 – животные, получавшие морских АГЭ в дозе 157 мг/кг;
группа 4 – стресс – контроль;
группа 5 - животные, получавшие морских АГЭ в дозе 15 мг/кг, а затем подвергнутые острому стрессу;
группа 6 животные, получавшие морских АГЭ в дозе 157 мг/кг, а затем подвергнутые острому стрессу.
Модель стресса
Острый иммобилизационный стресс моделировали фиксацией в специальном пенале, снабжённом отверстиями для прохождения воздуха, который подгонялся под размер животного в положении на спине на 16 часов однократно.
Подготовка образцов
Перед окончанием эксперимента до воздействия стресса определяли массу тела животных. Крыс декапитировали под эфирным наркозом, брали кровь для биохимических исследований, фиксировали мозг для гистологического анализа, подсчитывали количество поражений слизистой оболочки желудка. У животных, подвергнутых стрессу, определяли массу надпочечников (GA), селезёнки, вилочковой железы. Для взвешенных органов была рассчитана относительная масса органа на 100 г массы тела по формуле:
масса органа (г)/ масса тела животного (г)*100.
Биохимический анализ
Изучались активность каталазы и концентрация малонового диальдегида в эритроцитах, а также количество гемоглобина в эритроцитарной массе. Определение гематологических показателей проведено на приборе «Abacus» (США).
Гистологические исследования
Гистологические препараты изготавливались по стандартной схеме. Использовались методы окрашивания гематоксилином и эозином, а также по Нислю. Препараты изучались с помощью светового микроскопа «ImejerZ2 Zeiss», снабжённого камерой «AxioCam HRc Zeise» (Германия).
Фотографии зоны СА3 гиппокампа в дальнейшем обрабатывались с помощью программы «ImageJ» (версия 1.51 j1.8.0_112) с целью увеличить чёткость и контрастность изображения. Результаты обработки визуально контролировались сравнением с первоначальным изображением. Производился подсчёт клеток на площади 150*100 мкм. Исследовалось не менее 3 срезов для каждого животного.
Статистический анализ
Статистическая обработка проводилась с использованием программы Statistica 10.0. При описании данных приводятся среднее (М), медиана (Ме), верхняя и нижняя квартиль (интервал 25-75%).
Корреляционный анализ
Для выявления закономерностей был проведён корреляционный анализ. Использовался коэффициент корреляции Кендала-b, реализованный как коэффициент корреляции Кендала, тау-корреляции в программе Statistica, как рекомендованный для оценки связи двух порядковых или порядкового и количественного признака.
Результаты испытаний
При помощи корреляционного анализа в эксперименте проверялись две гипотезы:
1) влияют ли морские АГЭ на исследуемые показатели. Это влияние изучалось на двух разных выборках – животных, находившихся в стандартных условиях, и животных, подвергшихся действию острого иммобилизационного стресса;
2) влияет ли стресс на изучаемые показатели.
Так как для проверки двух гипотез использовались одни и те же данные, то необходимый уровень значимости должен быть не менее р = 0,025.
Количественное описание полученных результатов представлено в таблицах 2 и 3.
Каталаза
Выявлена значимая умеренная отрицательная корреляция активности каталазы с воздействием острого иммобилизационного стресса (K= -0,46). Под воздействием стресса активность каталазы показывает значимую сильную положительную корреляцию с применяемой дозой морских АГЭ (табл. 3). Тогда как среди животных, не подвергавшихся воздействию острого стресса, корреляция не является значимой (табл. 2). Фиг. 2 наглядно демонстрирует выявленные закономерности. Видно, что активность каталазы снижается при стрессе и значительно повышается у животных, которые предварительно получали морские АГЭ в дозе 157 мг/кг и затем подверглись действию стресса.
Малоновый диальдегид
Концентрация малонового диальдегида в эритроцитах значимо не зависит ни от стресса (K= -0,3), ни от приёма АГЭ (Табл. 2, 3), что может свидетельствовать об усилении антиоксидантной защиты самого организма при остром стрессе.
Баланс оксиданты / антиоксиданты
Каталаза – хромопротеид с молекулярной массой около 240кД, состоит из 4-х субъединиц, имеющих по одной группе гема. Это фермент, относящийся к классу оксидоредуктаз, который катализирует гетеролитическое расщепление О-О-связи в перекиси водорода. Каталаза всегда присутствует в системах, где осуществляется транспорт электронов с участием цитохромов, т.е. там, где образуется токсичный для клетки пероксид водорода. Она локализована преимущественно в пероксисомах клетки, частично в микросомах и, в меньшей мере, в цитозоле. У человека высокое содержание каталазы обнаружено в эритроцитах, а также в печени и почках.
Известно, что антиоксидантное состояние периферических тканей подвержено влиянию иммобилизационного стресса и что у крыс существуют тканеспецифические механизмы регуляции антиоксидантных ферментов.
Первичные продукты перекисного окисления липидов (гидроперекиси липидов), довольно скоро разрушаются с образованием вторичных продуктов перекисного окисления липидов – альдегидов, кетонов, спиртов, эпоксидов. Среди них наиболее известен малоновый диальдегид. При взаимодействии малонового диальдегида с аминогруппами фосфолипидов образуются конечные продукты перекисного окисления липидов – основания Шиффа.
Значительное снижение активности каталазы в эритроцитах в ответ на иммобилизационный стресс свидетельствует о том, что увеличивается скорость перекисного окисления липидов. В группах, предварительно получавших морские АГЭ в дозе 157 мг/кг, мы наблюдали восстановление активности каталазы до значений контрольной группы и выше, что подтверждает антиоксидантную активность морских АГЭ.
Известно, что диетарные морские АГЭ являются предшественниками в биосинтезе плазмалогенов, которые позволяют миновать стадию образования простой эфирной связи, проходящей при участии пероксисомальных ферментов. Ранее было показано, что диета с морскими АГЭ приводит к увеличению уровня плазмалогенов в эритроцитах, почках, печени и сердце у мышей с дефицитом фосфолипидов с простой эфирной связью. Вероятно, именно плазмалогены являются антиоксидантами и участвуют в связывании активных форм кислорода. Механизм антиоксидантного действия плазмалогенов, по-видимому, связан с тем, что винильная простая эфирная связь имеет относительно низкую энергию диссоциации и предпочтительнее окисляется под действием различных свободных радикалов и активных форм кислорода. Таким образом, морские АГЭ опосредованно, через увеличение уровня плазмалогенов способствуют защите клеток от перекисного окисления липидов.
Уровень гемоглобина
Обнаружена значимая умеренная отрицательная корреляция уровня гемоглобина с воздействием острого иммобилизационного стресса (К= -0,59). На фиг. 3. видно, что он снижается. Снижение уровня гемоглобина при стрессе может объясняться кровотечением, сопровождающим повреждения слизистой оболочки желудочно-кишечного тракта при стрессе и/или гемолизом.
Также график отражает чёткую тенденцию к повышению уровня гемоглобина после приёма препарата, что проявляется при дозе морских АГЭ 157 мг/кг. По полученным результатам можно сделать вывод о дозозависимом характере эффекта или необходимости большего времени для накопления препарата в организме. Так как уровень эритроцитов и гемоглобина являются важным компонентом адаптации к гипоксии, данный эффект препарата следует считать адаптогенным (антисрессовым).
Масса тела
Масса тела показывает значимую умеренную отрицательную корреляцию с дозой препарата (таб. 2). На фиг. 4. видно, что масса тела снижена в группе, получавшей морские АГЭ в дозе 157 мг/кг.
Поражения слизистой оболочки желудка
Применение выбранной модели острого иммобилизационного стресса вызвало у животных образование эрозий слизистой оболочки желудка, что хорошо известно по литературным данным (Selye H. Stress and disease // Science. 1955. 122, 625-631).
График, отражающий количество эрозивных повреждений слизистой оболочки желудка приведён на Фиг. 5.
Появление поражений слизистой желудка говорит об адекватности выбранной модели стресса. Количество повреждений слизистой оболочки желудка показывает значимую сильную положительную корреляцию с острым иммобилизационным стрессом (К= 0,96) и значимую умеренную отрицательную корреляцию с фактом лечения морскими АГЭ до воздействия стресса (табл. 3). Корреляция с фактом лечения морскими АГЭ, а не с их дозой была выбрана после визуального сравнения групп (Фиг.5.). Можно сделать вывод, что уже в дозе 15 мг/кг морских АГЭ проявляют противоязвенный эффект.
Надпочечники
Под воздействием стресса масса надпочечников (как относительная, так и абсолютная) показывает значимую положительную корреляцию с дозой препарата (табл. 3). Для индекса надпочечников эта связь была сильной. Относительная масса надпочечников (фиг. 6) выше у животных, получавших морские АГЭ и затем подвергнутых острому иммобилизационному стрессу.
Лимфоидные органы
В проведенном исследовании статистически значимых влияний дозы морских АГЭ на массу тимуса и селезёнки животных, подвергшимися острому иммобилизационному стрессу, не выявлено (табл. 3). Однако наблюдается тенденция к восстановлению индекса тимуса (фиг. 7).
Классические маркеры стресса
Ганс Селье выявил следующие признаки стресса, ставшие классическими: (1) увеличение и повышенную активность коры надпочечников, (2) сморщивание (или атрофию) вилочковой железы и лимфатических узлов, (3) появление язвочек желудочно-кишечного тракта (Selye, 1955). В современной литературе много примеров использования этих признаков для тестирования потенциальных адаптогенов, как на модели однократного иммобилизационного стресса (длительностью 8–18 часов), так и повторного.
В проведенном эксперименте ответ надпочечников на стрессовое воздействие был сильнее у крыс, получавших морские АГЭ в дозе 157 мг/кг и затем подвергнутых стрессу.
Можно предположить, что морские АГЭ влияют на снижение массы тела опосредованно, воздействуя на надпочечники, или вызывают перераспределение липидов в зависимости от текущего состояния метаболизма.
В.П. Казначеев выделил три стратегии адаптации (Казначеев В.П. Современные аспекты адаптации. М.: Наука, 1980. 192 с.). Первый тип стратегии (стратегия типа «спринтер»): организм обладает способностью мощных физиологических реакций с высокой степенью надежности в ответ на значительные, но кратковременные колебания во внешней среде. Имеет преимущества при чрезвычайной изменчивости среды, выраженных колебаниях неадекватных условий. Однако такой высокий уровень физиологических реакций может поддерживаться относительно короткий срок. К длительным физиологическим перегрузкам со стороны внешних факторов, даже если они средней величины, такие организмы мало приспособлены. Второй тип (стратегия типа «стайер»): организм менее устойчив к кратковременным значительным колебаниям среды, но обладает свойством выдерживать продолжительное время физиологические нагрузки. Третий тип – промежуточный.
Можно предположить, что под действием морских АГЭ организм переключается на стратегию адаптации типа «спринтер», о чём свидетельствуют следующие эффекты морских АГЭ:
1) мобилизация ресурсов организма за счёт глюкокортикоидов, на которую указывает повышение массы надпочечников;
2) антиоксидантная активность, подтверждённая в настоящем исследовании;
3) противоязвенный эффект, выявленный впервые;
4) усиление гемопоэза и стимуляция иммунитета.
Таким образом, организм находится в состоянии повышенной готовности к ответу на сильные стимулы, при этом отрицательные воздействия стресса (нарушение окислительно-восстановительного состояния, образование язв) снижаются.
Таким образом, морские АГЭ можно рассматривать как препарат, направленный на реализацию определенной антистрессовой (адаптационной) стратегии. Адаптогенный эффект морских АГЭ многогранен и проявляется в:
1. в мобилизации ресурсов организма при остром стрессе;
2. ограничении отрицательных эффектов острого стресса;
3. повышении адаптации к физическим нагрузкам и гипоксии, теоретически вытекающей из повышения уровня гемоглобина.
Гиппокамп
По литературным данным, под влиянием хронического иммобилизационного стресса в области гипокампа СА3 выявлены потери клеточного состава. Выявленные морфометрические изменения, вероятно, отражают снижение функциональной активности нейронов гиппокампа под влиянием иммобилизационного стресса.
По нашим данным, количество клеток в зоне СА3 значимо не зависит ни от стресса (K=0,3), ни от дозы препарата. Однако в группе стресс-контроля выявлено животное со сниженным количеством клеток (≤ 10) на двух срезах (фиг. 8а). У этого животного наблюдалась область, где количество клеток было визуально снижено и среднее количество клеток было 13,8. В группе животных, получавших морские АГЭ в дозе 15 мг/кг, а затем подвергнутых стрессу было выявлено, что у одной из крыс количество клеток колеблется от 12 до 14, среднее число клеток – 13 (фиг. 8б). Для сравнения приведено фото зоны СА3 животного из группы интактного контроля (фиг. 8в).
Пример 2. Способ лечения острого стресса алкил-глицериновыми эфирами, получаемыми из сырья морского происхождения.
Исследование проводилось на 60 самцах крыс линии Wistar. Условия содержания и обращения с животными, как в Примере 1.
В эксперименте использовали препараты АГЭ из гепатопанкреаса камчатского краба Paralithodes camtschaticus и печени ската Bathyraja parmifera, содержащие 99% АГЭ с преимущественным содержанием химилового спирта (Табл. 1, Пример 1). Перед использованием на животных препараты АГЭ диспергировали в воде.
Крысы опытных групп в течение месяца получали морские АГЭ перорально через зонд в дозе 157 мг/кг.
Животные были разбиты на группы, в каждой из которых было по 10 животных:
группа 1 – интактный контроль;
группа 2 – животные, получавшие морские АГЭ краба в дозе 157 мг/кг;
группа 3 – животные, получавшие морские АГЭ ската в дозе 157 мг/кг;
группа 4 – стресс – контроль;
группа 5 - животные, получавшие морские АГЭ краба в дозе 157 мг/кг, а затем подвергнутые острому стрессу;
группа 6 животные, получавшие морские АГЭ ската в дозе 157 мг/кг, а затем подвергнутые острому стрессу.
Модель стресса, все манипуляции и методы анализа были как в Примере 1.
Различия между группами определялись с помощью теста Манна-Уитни. Опытные группы, не подвергавшиеся стрессу, сравнивались с интактным контролем, животные, подвергшиеся воздействию стресса – с группой стресс-контроля. Так как, нужно было выполнить два сравнения необходимый уровень значимости составил 0,025.
Учитывая данные ранее проведенного эксперимента (Пример 1), заявителем были использованы только бόльшие дозы препаратов (157 мг/кг) и контролировались только наиболее значимые показатели – активность каталазы, уровень гемоглобина, степень поражения слизистой оболочки желудка.
Полученные данные приведены в таблицах 4 и 5. Как видно, все положительные тенденции, зафиксированные в примере 1, продемонстрированы и в этом опыте с соответствующей результативностью.
Препараты природных алкил-глицериновых эфиров, вне зависимости от используемого морского объекта, проявляли выраженный защитный эффект на организм при стрессе.
Причём при применении в течение 1 месяца действие морских АГЭ имеет выраженный дозозависимый эффект:
1. защитный эффект на слизистую оболочку желудка они оказывают уже в дозе 15 мг/кг;
2. в дозе 157 мг/кг морских АГЭ вызывают повышение активности каталазы и массы надпочечников при стрессе.
Результаты экспериментов показывают, что доза 15 мг/кг является нижним пределом для проявления защитных эффектов – достоверно подтверждается только уменьшение эрозии желудка. Поэтому уменьшение дозы ниже указанного предела, не даст никакого эффекта на стрессированный организм. Доза в количестве 157 мг/кг, наоборот, демонстрирует, что практически все системы организма восстанавливаются к прежнему уровню. Фактически наблюдается выход регистрируемых показателей на исходное плато.
Исходя из экспериментальных данных рекомендованной дозой морских АГЭ для получения адекватного адаптогенного эффекта, т.е. для стимулирования адаптации организма к экстремальным и стрессовым факторам является доза в количестве 15-157 мг/кг массы при минимальном сроке приема препарата в течение 1 месяца.
Таким образом, представленные данные свидетельствуют о том, что морские алкил-глицериновые эфиры способствуют активации надпочечников при остром стрессе. В то же время они нивелируют многие негативные эффекты стрессовых состояний – восстанавливают окислительно-восстановительный баланс, снижают образование язв, стимулируют синтез гемоглобина. Их можно считать препаратами, запускающими антистрессовую (адаптационную) стратегию, направленную на борьбу с сильными, но кратковременными стрессовыми воздействиями. Также они могут быть полезны в комплексной терапии язвенной болезни желудка и двенадцатиперстной кишки и язв другой этиологии.