Результат интеллектуальной деятельности: Способ получения полифункциональных O- и S-содержащих макрогетероциклов
Вид РИД
Изобретение
Изобретение относится к органической химии, конкретно к получению полифункциональных О- и S-содержащих макрогетероциклов, которые имеют широкий потенциал в качестве: биоактивных препаратов (в фармакологии), инсектицидов (в сельском хозяйстве) и комплексообразователей - экстрагентов благородных металлов (в промышленных флотационных процессах) (Хабибуллина Г.Р., Федотова Е.С., Абдуллин М.Ф., Тюмкина Т.В., Ахметова В.Р., Ибрагимов А.Г. Эффективный синтез N-(карбоксиметил)замещенных дитиаза- и диоксадитиазациклоалканов циклоконденсацией аминокислот с формальдегидом и α,ω-дитиолами // Журнал органической химии. - 2017. - Т. 53. - №2. - С. 277-281).
Известен способ получения шестичленных О- и S-содержащих гетероциклов взаимодействием 2-(l-метилциклопропил)пропан-1,3-дитиола с 4-этенилбензаледегидом в среде муравьиной кислоты при 0°С в течение 1 часа (Christopher J. Palmer, John E. Casida. Insecticidal 1,3-Dithianes and 1,3-Dithiane 1,1-Dioxides. // J. Agric. Food Chem. 1992. T. 40. P. 492-496).
Недостатками известного способа являются многостадйиность и дороговизна получения исходного 1,3-дитиола, а также ограниченность размера кольца получаемого конечного гетероцикла (только 6-членные кольца).
Задача, решение которой предлагается в настоящем изобретении, заключается в разработке способа получения макрогетероциклов, отличающегося увеличением выхода целевого продукта.
Указанная задача решается тем, что способ получения полифункциональных макрогетероциклов, каталитической реакцией, согласно изобретению, проводят взаимодействием этил-2-диазо-3-оксобутирата с 1,3-дитианами в бензоле в качестве растворителя в присутствии трифлата меди (II) Cu(OTf)2 при температуре 80°С в течение 4 часов.
Реакцию этил-2-диазо-3-оксобутирата с 1,3-дитианом проводят при следующем соотношении компонентов, мас. %: 1,3-дитиан 58; этил-2-диазо-3-оксобутират 40,4; трифлат меди 1,6.
Способ осуществляется следующим образом.
Этил-2-диазо-3-оксобутират получали по методике (Peace B.W., Carman F., Wulfman D.S. TheSolubleCopper(I)-CatalyzedDecompositionofDimethylDiazomalonateandDi-t-butylDiazomalonateinthePresenceofSomeCycloalkenes // Synthesis. - 1971. - V. 1971. - N. 12. - P. 658-661.).
Катализатор - трифлат меди (II) и исходный реагент - 1,3-дитиан- используются торговые реагенты.
Исходные реагенты должны соответствовать следующим требованиям:
- Бензол - ГОСТ 5955-75;
- Силикагель - mesh 60-100, «Lancaster».
К бензольному раствору 1,3-дитиана и катализатора трифлата мели Cu(OSO2CF3)2 при интенсивном перемешивании и температуре 80°С добавляют в течение 15 минутэтил-2-диазо-3-оксобутират в бензоле. Реакционную смесь перемешивают при температуре 80°С в течение 4 часов. Мольное соотношение 1,3-дитиан : этил-2-диазо-3-оксобутират : трифлат меди = 100:50:1. По окончании реакции реакционную смесь охлаждают до комнатной температуры и пропускают через тонкий слой силикагеля, растворитель удаляют в слабом вакууме и остаток хроматографируют на силикагеле.
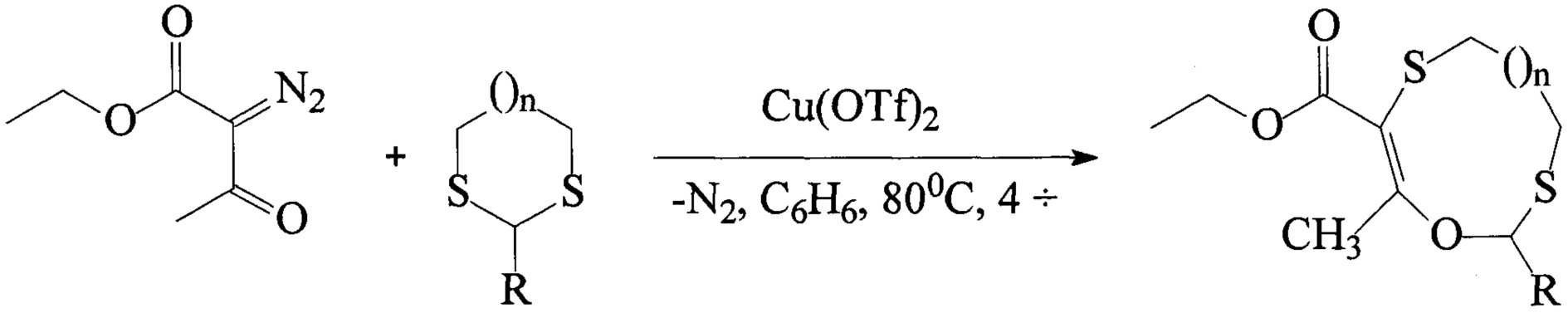
Пример 1.
К бензольному раствору 1,2 ммоль (144 мг) 1,3-дитиана и 1,2⋅10-5 моль (4 мг) катализатора трифлата меди Cu(OSO2CF3)2 при интенсивном перемешивании и температуре 80°С добавляли в течение 15 минут раствор 0.6 ммоль (100 мг) этил-2-диазо-3-оксобутирата в 10 мл бензола. Реакционную массу перемешивали при нагревании 4 часа. По окончании реакции (контроль по ГЖХ) реакционную смесь охлаждали до комнатной температуры и пропускали через тонкий слой силикагеля, растворитель удаляли в слабом вакууме и остаток хроматографировали на силикагеле.
Выход этил-(8Z)-9-метил-5,6-дигидро-4H-3,7-дитио-1-оксонин-8-карбоксилата - 85%. Светло-желтое маслообразное вещество, Rf 0.23 (бензол - этилацетат, 9.5:0.5). Спектр ЯМР 1Н (в CDCl3, в δ, м.д.): 1.30 т (3Н, СН3СН2, J=7.1), 1.88-1.97 м (2Н, СН2СН2), 2.35 с (3Н, СН3С), 2.65-2.80 м (2Н, СН2СН2), 3.32-3.51 м (2Н, CH2S), 4.25 к (2Н, CH2O, 3J=7.1), 3.78 с (2Н, CH2O), спектр ЯМР 13С (в CDCl3, в δ, м.д.): 13.9 (СН3СН2), 26.3 (CH3C), 28.5 (CH2S), 33.8 (СН2СН2), 34.9 (СН2СН2), 61.2 (СН2О), 62.7 (CH2O), 134.8 (C-S), 154.3 (C-S), 165.7 (С=O). Масс-спектр (ХИ), m/z: 217 [М+Н]+, (вычислено m/z: 216 для C10H16O3S2).
Приведенный пример не исчерпывает возможности способа в отношении других О- и S-содержащихмакрогетероциклов (5-, 6-, 7-членных), содержащих алкильные и арильные радикалы.
Из примера видно, что предлагаемый способ позволяет достигнуть выхода О- и S-содержащих макрогетероциклов 85% по сравнению с прототипом, что обеспечит широкое использование этих соединений в различных отраслях народного хозяйства.

