Результат интеллектуальной деятельности: Средство, сохраняющее популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии
Вид РИД
Изобретение
Изобретение относится к фармацевтической промышленности и медицине и касается производных гамма-аминомасляной кислоты (ГАМК), сохраняющих популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии.
Гамма-аминомасляная кислота (ГАМК) является важнейшим тормозным нейромедиатором в головном мозге млекопитающих. Она синтезируется в нервных клетках путем декарбоксилирования главного возбуждающего медиатора глутамата под действием фермента глутамат-декарбоксилазы (GAD) [Roberts Е., Frankel S. Gamma-aminobutyric acid in brain: its formation from glutamic acid // J. Biol. Chem. 1950. Vol. 187. №1. P. 55-63]. ГАМК улучшает кровообращение и обменные процессы в головном мозге. Стимулируя выработку соматотропного гормона, ГАМК регулирует рост и развитие ребенка [Fine R., Zhang J., Stevens H.E. Prenatal stress and inhibitory neuron systems: implications for neuropsychiatric disorders // Molecular Psychiatry. 2014 Jun. Vol. 19. №6. P. 641-651; Kahle K.T. The GABA excitatory/inhibitory shift in brain maturation and neurological disorders // Neuroscientist. 2012. Oct. Vol. 18. №5. P. 467-486].
ГАМК является действующим веществом лекарственного средства аминалон. Он применяется для лечения некоторых заболеваний головного мозга и относится к ноотропным средствам [Машковский М.Д. Лекарственные средства. М. «Новая волна». 2012. С. 17; Ковалев Г.В. Ноотропные средства. Волгоград. Нижне-Волжское книжное издательство. 1990. 368 с]. ГАМК не используется для лечения патологических состояний и нервно-психических заболеваний обусловленных перинатальной патологией. Ее свойства сохранять популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии также неизвестны.
Известно средство, обладающее антиишемической, гипотензивной, противоаритмической и ноотропной активностью, включающее производное ГАМК 4-амино-3-фенилбутановую кислоту и глутаминовую или никотиновую кислоты. Полученные средства имеют меньшую токсичность, чем исходные вещества, оказывают более выраженное антиангинальное и противоаритмическое действие, снижают артериальное давление [RU №2216322]. Свойство указанных в патенте композиций, сохранять популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии не описано. Кроме этого, свойства 4-амино-3-фенилбутановой кислоты сохранять популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии в литературных источниках не описаны. 4-Амино-3-фенилбутановая кислота в медицине вообще не используется.
Известно, что салициловая кислота обладает слабыми антисептическими, раздражающими и кератолитическими (в больших концентрациях) свойствами. Она применяется в медицине наружно [Машковский М.Д. Лекарственные средства. М. «Новая волна». 2012. С. 940]. Свойства салициловой кислоты защищать популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии не описаны.
Гипоксия - одна из основных причин возникновения патологии головного мозга у новорожденных, что часто приводит к младенческой смертности и инвалидности. Неонатальная гипоксия является одним из наиболее мощных и наиболее частых факторов возникновения патологии головного мозга у новорожденных, отрицательно влияющих на последующее развитие ребенка. [Моргун А.В., Кувачева Н.В., Таранушенко Т.Е., Хилажева Е.Д. и др. Современные представления о патогенезе перинатального ишемического повреждения клеток нейроваскулярной единицы головного мозга: молекулы-мишени для нейропротекции. Вестник РАМН. 2013. Т. 12. С. 26-35].
В последнее время в клинических и экспериментальных исследованиях значительное внимание уделяется изучению механизмов гипоксических поражений головного мозга новорожденных, а также механизмов формирования перинатальной патологии мозга, что позволяет разрабатывать эффективные способы предупреждения перинатальной патологии, проявляющейся в последующем онтогенезе [Fan X., Kavalaars F., Heijen C.J. et all. Fharmacological neuroprotection after perinatal hypoxic-ishemic brain injury. // Curr. Neuropharmacol. 2010. Vol. 8. №4. P. 324-334; Herrera-Marschitz M., Neira Pefia Т., Rojas-Mancilla E., Morales P. et all. Short- and long-term consequens of perinatal asphyxia: looking for neuroprotective strategies. // Adv. Neurobiol. 2015. №10. P. 169-198].
Перинатальная гипоксия, как правило, приводит к изменению цитоархитектоники неокортекса, задержке нейроногенеза, пролонгированной гибели части нейронов. В результате чего, численность популяций разных типов нейронов в различных областях коры головного мозга сокращается [Northigton F.J., Chavez-Valdez R., Martin L.J. Neuronal cell death in neonatal hypoxia - ischemia. // Ann. Neuroll. 2011. V. 69. №5. P. 743-758; Отеллин В.A., Хожай Л.И., Ватаева Л.А. Влияние гипоксии в раннем перинатальном онтогенезе на поведение и структурные характеристики головного мозга. // Журнал эволюционной биохимии и физиологии им. И.М. Сеченова. 2012. Т. 48. №5. С. 467-473]. Известно, что гипоксия в раннем перинатальном онтогенезе приводит к основным неврологическим нарушениям деятельности центральной нервной системы (ЦНС) и занимает первое место в ряду всех заболеваний нервной системы в детском возрасте [Рогаткин С.О. Актуальные проблемы перинатальной неврологии на современном этапе. // Журн. неврол. психиатр. 2001. №7. С. 4-8; Моргун А.В., Кувачева Н.В., Таранушенко Т.Е., Хилажева Е.Д., Малиновская Н.А., Горина Я.В., Пожиленкова Е.А., Фролова О.В., Салмина А.Б. Современные представления о патогенезе перинатального ишемического повреждения клеток нейроваскулярной единицы головного мозга: молекулы-мишени для нейропротекции. // Вестник РАМН. 2013. №12. С. 26-35]. Перинатальные гипоксические поражения нервной системы почти у 40% детей приводят к инвалидности (детский церебральный паралич, симптоматическая эпилепсия, задержка умственного развития, нарушения в когнитивной и эмоциональной сферах) [Власюк В.В. Родовая травма и перинатальные нарушения мозгового кровообращения. СПб. Нестор-История. 2009. 252 с.]. Особенно остро неблагоприятное воздействие гипоксии-ишемии проявляется у недоношенных детей, органы и системы которых еще не сформированы для полноценного функционирования.
В настоящее время в реестре лекарственных препаратов отсутствуют средства для фармакологической коррекции структурных повреждений мозга, являющихся последствием воздействия гипоксии в ранний послеродовой период. Также неизвестны фармакологически активные вещества-субстанции, обладающие свойством сохранять популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии.
Эта медицинская и социальная проблема определяет актуальность проведения экспериментальных исследований, направленных на поиск и разработку новых веществ-субстанций, обладающих свойством сохранять популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии, применение которых базируется на данных исследований о механизмах и мишенях воздействия перинатальной гипоксии на мозг.
Задача изобретения - получить высокоэффективное и малотоксичное вещество-субстанцию производное ГАМК, сохраняющее популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии. Применение средства будет основано на данных о механизмах и мишенях его действия.
Поставленная задача реализуется предлагаемым средством, включающим 4-амино-3-фенилбутановую кислоту и салициловую кислоту. Причем, соотношение 4-амино-3-фенилбутановая кислота : салициловая кислота как (1-3):1. При этом получают средство, сохраняющее популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии.
Лекарственное средство содержит эффективную дозу композиции 4-амино-3-фенилбутановой кислоты с салициловой кислотой, фармакологически приемлемые носители и целевые добавки.
Технический результат изобретения заключается в том, что предлагаемое средство малотоксично и способно сохранять популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии.
Изобретение иллюстрируется следующими примерами: Получение композиции 4-амино-3-фенилбутановой кислоты с салициловой кислотой (КАФС).
В шаровую мельницу загружают соответствующие количества 4-амино-3-фенилбутановой и салициловой кислот. Количества компонентов приведены в таблице А. Смесь компонентов тщательно перемешивают в течение 0,5-1 часа, затем выгружают полученный продукт. Выход количественный.
Далее приводятся примеры, иллюстрирующие специфическую активность композиции 4-амино-3-фенилбутановой кислоты с салициловой кислотой (КАФС) в условиях острой перинатальной гипоксии.
Острая токсичность КАФС оценивалась по выживаемости белых мышей через 24 часа после парентерального (внутрибрюшинного) и энтерального (внутрижелудочного) введения вещества. Усредненные значения показателей ЛД50: при парентеральном введении - 1080 мг/кг, при энтеральном - более 1700 мг/кг. Вещество относится к малотоксичным, что позволяет классифицировать его как малоопасное.
Для изучения специфической активности КАФС защищать ГАМК-ергические нейроны в условиях острой перинатальной гипоксии были применены стандартные экспериментальные методы исследования, основанные на применении глутамат-декарбоксилазы (GAD-67) в качестве маркера ГАМК-ергических нейронов.
В работе были использованы новорожденные животные лабораторных крыс линии Wistar, содержавшиеся в условиях лабораторного вивария, в течение двух недель до начала эксперимента, на стандартном пищевом рационе, при свободном доступе к воде, при естественном световом режиме. Эксперименты проводились в одно и то же время суток. Приводимые в таблицах значения показателей представляют собой среднестатистическую оценку результатов измерения параметров с учетом принятых уровней достоверности (р<0.05).
Острая перинатальная гипоксия моделировалась на вторые постнатальные сутки в барокамере с проточной газовой смесью: кислород - 7.6-7.8%; углекислый газ - 0.15-0.21% и азот - 91.8% в течение одного часа, при температуре 21.3°С-23°С и нормальном общем давлении.
Для проведения эксперимента были сформированы следующие группы животных ювенильного (на 20 сутки жизни) и препубертатного (на 40 сутки жизни) возраста: контрольная группа 1 - новорожденные крысята (интактные животные), получавшие перорально физиологический раствор - позитивный контроль, (n=8-10); контрольная группа 2 - животные, подвергавшиеся воздействию гипоксии и получавшие физиологический раствор - негативный контроль, (n=8-10); опытная группа 3 - новорожденные крысята с гипоксией, получавшие КАФС, (n=8-10). Исследуемую композицию - КАФС в дозе 15 мг/кг вводили подкожно, один раз в день, ежедневно в течение 14 суток.
Для проведения гистологических исследований мозг крысят фиксировали в течение 24 часов в цинк-этанол-формальдегиде на фосфатно-солевом буфере (рН=7.4). Фиксированный материал обезвоживали и заливали в парафин по общепринятой гистологической методике.
Иммуноцитохимическую реакцию проводили на серийных фронтальных парафиновых срезах толщиной 4-5 мкм, окрашенных метиленовым синим (Sigma, США) в синтетической среде Permaunt (Termo, США) по методу Ниссля.
Для выявления ГАМК-ергических нейронов использовали кроличьи поликлональные антитела (Spring Bioscience, США); в качестве вторичных реагентов для GAD-67 использовали реактивы из набора EnVision + System-HRP Labelled Polymer Anti-Rabbit (DakoCytomation, США). Для визуализации продукта иммуноцитохимической реакции применяли стандартную тест-систему в качестве хромогена использовали 3,3'-диаминобензидин (DAB+) (Dako, Дания). После проведения иммуноцитохимической реакции часть срезов докрашивали гематоксилином Джилла и заключали в синтетическую заливочную среду Permaunt (Termo, США). При проведении иммуноцитохимической реакции все процедуры были стандартизированы и осуществлялись одновременно для гистологических срезов, полученных от животных контрольных и опытной групп.
Количественный подсчет ГАМК-ергических нейронов проводили на цифровых изображениях серийных срезов, полученных при помощи светового микроскопа Leica DME (Leica, Германия) и цифровой камеры Leica ЕС3 (Leica, Германия). Подсчитывали число ГАМК-ергических нейронов в соматосенсорной области неокортекса на стандартной площади 1,06 мм2 при увеличении: окуляр × 10; объектив × 10 или 0,1 μkμ2 при увеличении: окуляр × 10; объектив × 40. Подсчитывали среднее число ГАМК-ергических нейронов на площади фрагментов неокортекса и стандартную ошибку среднего значения. Для подсчета использовали прикладные компьютерные программы Statistica 6.0, ImageScope Color и ORIGIN50. Приводимые в таблицах значения показателей представляют собой среднестатистическую оценку результатов измерения параметров с учетом принятых уровней достоверности (р<0.05).
Влияние КАФС на число ГАМК-ергических нейронов в соматосенсорной области неокортекса (ювенильный и препубертатный периоды развития животных) (табл. 1).
Результаты исследования показали, что у интактных животных ювенильного возраста (контрольная группа 1) ГАМК-ергические нейроны присутствуют во всех слоях неокортекса, они диффузно равномерно рассеяны по всему неокортексу (табл. 1). У животных контрольной группы 2 после острой перинатальной гипоксии наблюдалось существенное снижение (на 22%) общего числа ГАМК-ергических нейронов, в соматосенсорной области неокортекса, по сравнению с таковым у крыс контрольной группы 1 (табл. 1). Такой результат свидетельствует о значительной гибели ГАМК-ергических нейронов у животных, перенесших перинатальную гипоксию. Исследование влияния КАФС на количество ГАМК-ергических нейронов показало, что у крысят ювенильного возраста опытной группы 3 наблюдалось незначительное снижение общего числа ГАМК-ергических нейронов по сравнению с исходными показателями (контрольная группа 1) и было значительно выше (на 21,7%), чем у животных контрольной группы 2 (табл. 1).
Таким образом, предлагаемая композиция КАФС обладает выраженным свойством защищать ГАМК-ергические нейроны мозга крыс ювенильного возраста после острой перинатальной гипоксии, о чем свидетельствует практически равное количество ГАМК-ергических нейронов во всех слоях исследуемой области коры мозга у животных группы 3 с таковым у крысят контрольной группы 1. Существенно, что у животных негативного контроля, не получавших КАФС, в постнатальном периоде после гипоксии численность популяции ГАМК-ергических нейронов значительно снизилась (табл. 1).
Исследование влияния предлагаемого КАФС на животных, достигших препубертатного возраста, показало, что у крыс контрольной группы 1 также присутствует значительная численность популяции ГАМК-ергических нейронов во всех слоях коры (табл. 1). У крыс после острой перинатальной гипоксии (контрольная группа 2) наблюдается существенное снижение (на 39.5%) общего числа ГАМК-ергических нейронов, по сравнению с таковым у животных контрольной группы 1, что свидетельствует о прогрессирующем снижении числа ГАМК-ергических нейронов в слоях соматосенсорной области неокортекса после гипоксии (табл. 1). Результаты экспериментов показали, что у крыс препубертатного возраста опытной группы 3 общее число ГАМК-ергических нейронов во всех слоях неокортекса значительно больше (на 62.4%), чем у животных контрольной группы 2. Такой результат свидетельствует о выраженном свойстве КАФС предотвращать повреждение и гибель ГАМК-ергических нейронов (сохранять их популяцию), а также увеличивать их миграцию в неокортексе у крыс, перенесших на второй день жизни острую перинатальную гипоксию (табл. 1).
Влияние КАФС на число тормозных ГАМК-ергических нейронов в соматосенсорной области неокортекса (ювенильный и препубертатный периоды развития животных) (табл. 2, 3)
Изучение влияния КАФС на состояние ГАМК-ергической тормозной системы в разных слоях соматосенсорной области неокортекса животных ювенильного возраста (на 20 сутки жизни) показало, что у крысят контрольной группы 2 наблюдалось значительное снижение числа тормозных ГАМК-ергических нейронов во всех, но особенно в V и VI слоях неокортекса (табл. 2). В эксперименте на крысятах опытной группы 3, получавших КАФС в дозе 15 мг/кг установлено, что число ГАМК-ергических нейронов у этих животных превосходило в 1.3-1.7 раза таковое у крыс контрольной группы 2 (табл. 2).
Исследование неокортекса крыс препубертатного возраста (на 40 постнатальные сутки) показало, что у животных контрольной группы 2 после перинатальной гипоксии сохраняется тенденция к снижению численности тормозных нейронов в неокортексе (табл. 3). У животных опытной группы 3, получавших КАФС, число тормозных ГАМК-ергических нейронов в разных слоях неокортекса практически соответствует значениям интактных крыс (группа 1) и превосходит в 1.7-2.5 раза таковые у крыс негативного контроля (группа 2) (табл. 3).
Результаты проведенного эксперимента показали, что композиция КАФС в условиях острой перинатальной гипоксии обладает выраженным свойством сохранять популяцию ГАМК-ергических нейронов на 20-е и на 40-е сутки постнатального развития.
Лекарственное средство, содержащее в качестве действующего вещества, композицию 4-амино-3-фенилбутановой и салициловой кислот, в зависимости от выбранных носителей и целевых добавок, может быть изготовлено в любой твердой или жидкой лекарственной форме.
Таким образом, предлагаемое средство КАФС обладает выраженным свойством сохранять популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии, имеет низкую токсичность, что предполагает возможность его длительного использования для фармакологической коррекции повреждений ЦНС у детей с перинатальной гипоксией.


Примечания * - в процентах по сравнению с контрольной группой 1; ** - в процентах по сравнению с контрольной группой 2

Примечания * - в процентах по сравнению с контрольной группой 1; ** - в процентах по сравнению с контрольной группой 2
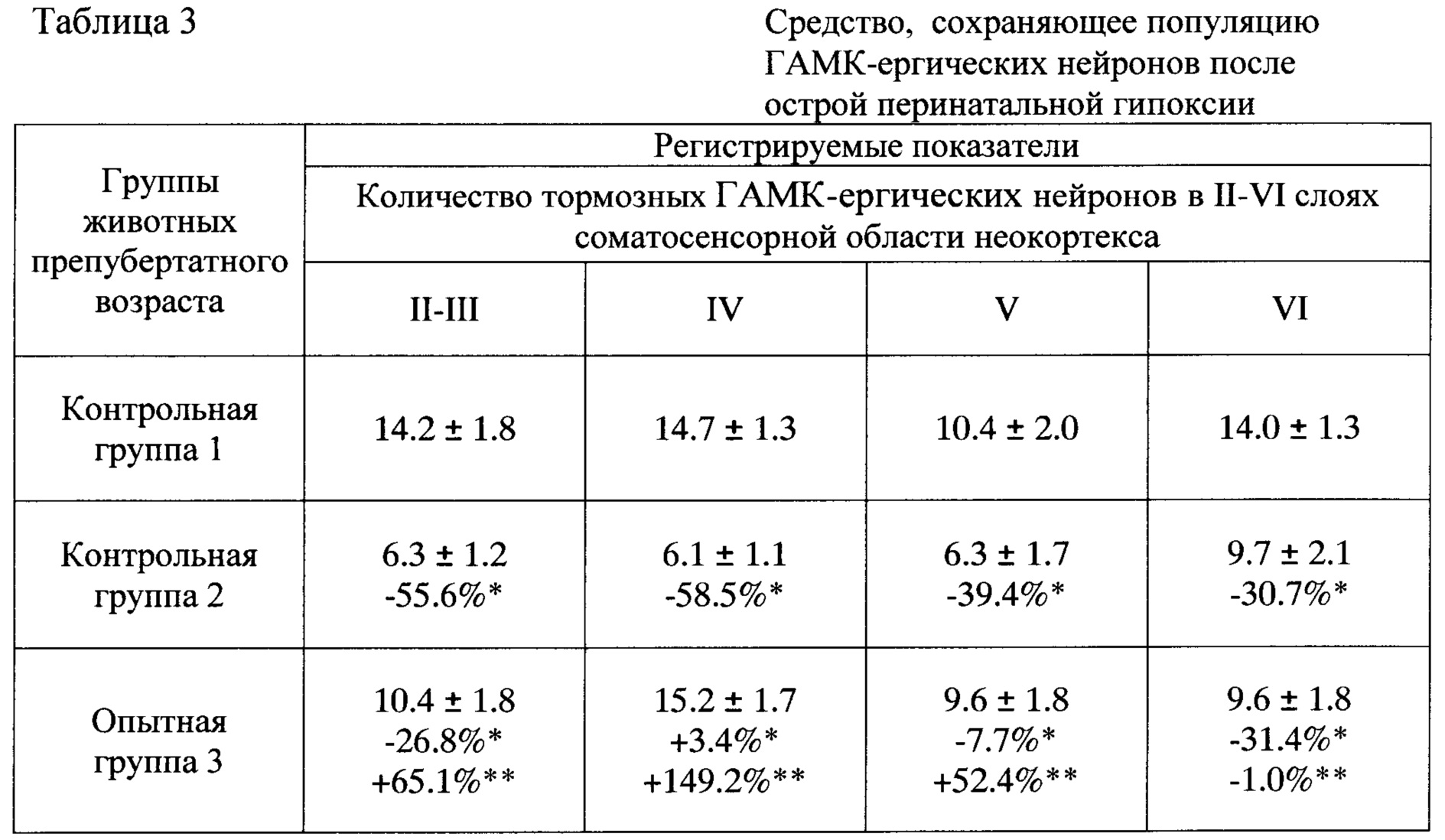
Примечания * - в процентах по сравнению с контрольной группой 1; ** - в процентах по сравнению с контрольной группой 2
Средство, сохраняющее популяцию ГАМК-ергических нейронов после острой перинатальной гипоксии, характеризующееся тем, что оно включает 4-амино-3-фенилбутановую кислоту и салициловую кислоту, при этом мольное соотношение 4-амино-3-фенилбутановой кислоты и салициловой кислоты составляет (1-3): 1.
