Результат интеллектуальной деятельности: Способ дифференциальной диагностики бактериальных и вирусных кишечных инфекций у детей раннего возраста
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно педиатрии, в частности, к разделу детских инфекционных болезней, и может быть использовано для дифференциальной диагностики бактериальных и вирусных кишечных инфекций у детей раннего возраста.
В настоящее время изучены многие аспекты диагностики и клинических проявлений острых кишечных инфекций у детей, вместе с тем, остаются во многом нерешенными проблемы ранней дифференциальной диагностики бактериальных и вирусных кишечных инфекций у детей раннего возраста.
Общепринятым в клинической практике методами дифференциального диагноза бактериальной и вирусной кишечной инфекции является оценка результатов гемограммы, копрограммы, бактериологического посева кала, в некоторых случаях серологических методов исследования, в сопоставлении с клиническими данными. В периферической крови определяют содержание лейкоцитов, лейкоцитарную формулу и СОЭ, при оценке степени дегидратации организма - показатели красной формулы, гематокрит. По копрограмме судят об уровне вовлечения желудочно-кишечного тракта в патологический процесс, отмечают признаки амилореи, стеатореи, креатореи, наличие патологических примесей (кровь, слизь), количество лейкоцитов в поле зрения.
Специфические методы исследования помогают точно установить этиологию заболевания. Золотым стандартом, при подозрении на кишечную инфекцию бактериальной этиологии является мазок на дизентерийную группу и сальмонеллы. Так, бактериологический посев определяет рост патогенных или условно-патогенных микроорганизмов. Кроме того, бактериологическому исследованию подлежат рвотные массы, кровь, моча, ликвор при генерализованных формах ОКИ. Недостатками данного метода является трудность забора биоматериала, поскольку необходимо использовать стерильную посуду, материал должен быть доставлен в лабораторию не позднее 8 часов с момента взятия, кроме того сам посев требует 5-7 дней для выявления возбудителя. Серологические методы исследования, также, уточняют этиологию кишечной инфекции. Диагностическим считается нарастание титра антител в 4 и более раз при двукратном исследовании с интервалом в 7-10 дней, что является недостатком данного метода. По этим показателям, в совокупности с данными клинического обследования, дифференцируют бактериальную и вирусную кишечные инфекции.
Известен способ экспресс-диагностики острых кишечных инфекций (ОКИ) - патент RU 2536243 С1 от 20.12.2014, включающий выявление маркеров-индикаторов этиологии ОКИ, с использованием иммунологического лабораторного исследования, отличается тем, что этиологию ОКИ устанавливают у детей ранней возрастной категории, предпочтительно у новорожденных, при этом определяют концентрацию в копрофильтрате цитокина - интерлейкина 1L-10 и наличие хронической фетоплацентарной недостаточности (ХФПН), после чего рассчитывают вероятность (Р) бактериальной этиологии ОКИ, причем значение Р больше 50% свидетельствует о бактериальной этиологии ОКИ, а меньше 50% свидетельствует об отсутствии бактериальной этиологии ОКИ, и необходимости проведения второго этапа диагностики, на котором определяют концентрацию в копрофильтрате цитокина - интерлейкина IL-4, выявляют срок прикладывания к груди, а также вид вскармливания, при этом рассчитывают вероятность (Р) вирусной либо вирусно-бактериальной этиологии ОКИ, причем значение Р больше 50% свидетельствует о вирусной этиологии ОКИ, а меньше 50% свидетельствует о вирусно-бактериальной ОКИ. Копрофильтрат готовили известным образом: пробу кала помещают в предварительно взвешенную, стерильную, вместимостью 10 мл пробирку, далее 100 мг кала интенсивно встряхивали с 5,0 мл физиологического раствора (NaCl 0,09%) до образования гомогенной взвеси или гомогенизировали образцы на многопробирочном вортексе, энергично шейкируя (на самой высокой скорости) в течение 30 мин, далее переносили гомогенат в 2 мл микроцентрифужную пробирку и центрифугировали 5 мин на микроцентрифуге со скоростью 3000 об/мин, отбирали супернатант в чистую помеченную пробирку. Концентрацию цитокинов в копрофильтрате, интерлейкина IL-10 и IL-4, определяли известным образом, путем иммуноферментного анализа с использованием реактивов R&D Diagnostics Inc. (USA), согласно прилагаемой инструкции, на анализаторе Multiscan (Финляндия). Расчеты количества цитокинов IL-10, IL-4 проводили путем построения калибровочной кривой с помощью компьютерной программы. Количество выражали в пикограммах на миллилитр (пг/мл). Анализ уровней цитокинов проводят в максимально короткие сроки после начала заболевания (фактически сразу после доставки ребенка в медучреждение).
Недостатками способа являются: необходимость проведения двухэтапного исследования больных, что требует большего количества биологического материала и времени для постановки реакций. Кроме того, необходимо уточнять дополнительный анамнез (наличие ХФПН, вида вскармливания, срока прикладывания к груди). Вместе с тем, предложенный способ не уточняет конкретный диапазон значений, соответствующий бактериальной или вирусной этиологии заболевания.
Известен способ экспресс - диагностики острых бактериальных кишечных инфекций - патент RU 2329507 от 20.07.2008. Этот результат достигается тем, что антиген возбудителя ОКИ определяют непрямым иммунопероксидазным методом и согласно изобретению клетки крови (лимфоцитарную взвесь в объеме 0,05 мл), полученные путем центрифугирования, наносят на предметное стекло (мазок), высушивают при комнатной температуре, фиксируют в чистом ацетоне - 3-5 мин, затем обрабатывают в 3% H2O2 20 минут, инкубируют с нормальной блокирующей сывороткой (10 минут), инкубируют с поли- или моноклональными антителами к искомым антигенам при температуре 37°С в течение 45 минут, инкубируют с полимерной системой детекции (Super Enhacer в течение 20 мин в темной камере при комнатной температуре, инкубируют с SS Label в течение 30 мин в темной камере при комнатной температуре), далее обрабатывают 3,3-диаминобензидин тетрахлоридом (ДАБ) и наличие коричневых гранул в лимфоцитах и моноцитах свидетельствует о выявлении искомого антигена возбудителя (диагностике инфекции).
Также известен способ идентификации острых кишечных инфекций -патент RU 2509804 С2 от 20.03.2014, включающий набор дифференцирующих олигонуклеотидов (зондов), обеспечивающий возможность определения в биологическом образце ДНК патогенных микроорганизмов, вызывающих ОКИ, и их видовой идентификации, где указанные микроорганизмы относятся к группе, включающей Shigella spp. и Enteroinvasive E. coli (EIEC), Salmonella spp., Campylobacter jejuni, Proteus mirabilis, Klebsiella pneumoniae. Описано конструирование биочипа с иммобилизованным на нем набором зондов по изобретению, предназначенного для проведения экспресс-анализа возбудителей ОКИ в клинических образцах и материале, полученном из объектов окружающей среды.
Кроме того, существует способ дифференциальной диагностики иерсиниоза путем иммуноферментной (ИФА) диагностики кишечного иерсиниоза, вызванного различными серовариантами Yersinia enterocolitica, и наборам для диагностики иерсиниоза (патент RU 2345365 С1 от 27.01.2009). Сущность способа: в качестве антигена используется видоспецифический порообразующий белок (порин) наружной мембраны Y. enterocolitica который обеспечивает определение специфических антител к порину из Y. enterocolitica в сыворотке крови человека независимо от серологического варианта возбудителя. В качестве реагента для предотвращения неспецифического связывания используется 0,1%-ный раствор твина-20 или твина-80. Диагностическим титром является разведение сыворотки крови больного 1:800-1:1600. Способ диагностики и предлагаемый набор для его осуществления повышают эффективность диагностики кишечного иерсиниоза, так как позволяют определять в сыворотке крови человека специфические антитела к Y. enterocolitica всех серовариантов как в ранние (на 1-й неделе заболевания), так и в более поздние сроки заболевания (на 2-й и 3-4-й неделях).
Однако, недостатками данных методов является выявление только определенных бактериальных возбудителей, без возможности проведения дифференциальной диагностики вирусных и бактериальных кишечных инфекций.
Наиболее близким к предлагаемому методу является способ ранней дифференциальной диагностики бактериальных и вирусных кишечных инфекций с использованием фекального кальпротектина [Кессаева И.К., Калоева З.Д., Барычева Л.Ю., Голубева М.В. Информативность фекального кальпротектина в диагностике острых кишечных инфекций у детей // Фундаментальные исследования. - 2015. - №1. - С. 87-91]. Фекальный кальпротектин определяли в образцах кала, взятых во время одной дефекации, при поступлении ребенка в стационар, что соответствовало 1-3 суткам заболевания. Собранные образцы кала хранили в холодильнике при температуре 2-8°С в течение 2-6 дней. Для определения ФК применяли стандартные наборы фирмы Buchlmann (Швейцария), исследование проводили в соответствие с рекомендациями фирмы-производителя. В пустую полипропиленовую пробирку помещали 50-100 мг образца стула и 2,5-5,0 мл буферного раствора для экстракции. Смесь в течение 30 мин энергично встряхивали на вортексе, затем 1,5 мл гомогенизированного образца переносили в чистую пробирку и центрифугировали в течение 5 мин при 10000 g. Полученный супернатант помещали в чистую пробирку и хранили при температуре 2°С до проведения ИФА. Определение кальпротектина проводили с помощью метода ИФА, результаты регистрировали на микропланшетном фотометре при длине волны 450 нм. Расчет концентрации кальпротектина осуществляли с помощью калибровочной кривой. Концентрацию фекального кальпротектина выражали в мкг кальпротектина на 1 г фекалий.
Авторами установлено умеренное повышение фекального кальпротектина до 95,3 плюс/минус 5,15 мкг/г у пациентов с вирусными диареями и существенное увеличение ФК до 5 13,27 плюс/минус 42,19 мкг/г у детей с бактериальными диареями, превышающее референтные значения (64,8 плюс/минус 5,72) более чем в 5 раз.
Установлена умеренная прямая взаимосвязь показателей ФК и уровня С-реактивного белка (rs равно 0,36, р равно 0,016), а также положительная корреляция показателей ФК и количества лейкоцитов в образцах стула (rs равно 0,49, р равно 0,0007). При проведении анализа шансов показана высокая предсказательная ценность всех трех показателей - уровня CRB, количества лейкоцитов в образцах стула, концентрации фекального кальпротектина для диагностики бактериальных диарей. Максимальная вероятность развития бактериальной диареи у госпитализированных детей отмечалась при значениях CRB более 5 мг/л, лейкоцитов в копрограмме более 10 кл/поле зрения, концентрации ФК более 340 мкг/г. Таким образом, определение фекального кальпротектина является объективным и неинвазивным тестом, который может быть использован в качестве скрининга для дифференциальной диагностики бактериальных и вирусных диарей на раннем докультуральном этапе диагностического поиска.
Недостаткам данного метода являются отсутствие точных диапазонов, указывающих на бактериальную и вирусную этиологию заболевания; необходимость определения дополнительных лабораторных критериев (СРБ), не входящих в обязательный минимум при обследовании детей больных ОКИ.
Острые кишечные инфекции (ОКИ) остаются одной из актуальных проблем детской инфекционной патологии. Однако, согласно данным официальной статистики, почти 60% всех ОКИ остаются этиологически нерасшифрованными, что указывает на актуальность дифференциальной диагностики на уровне верификации вирусных или бактериальных причин этих заболеваний.
В современной литературе нами отмечены публикации о возможности использования неоптерина, как дифференциально-диагностического маркера при вирусных и бактериальных инфекциях [Дудина К.Р., Кутателадзе М.М., Знойко О.О. и др. Неоптерин - потенциальный диагностический и прогностический маркер при инфекционных заболеваниях // Казанский медицинский журнал. - 2014.- Т. 95. - №6. - С. 938-943; Katarzyna Plata-Nazar,  Luczak, Anna Liberek, Julita Dudzinska-Gehrmann et al. Evaluation of clinical usefulness of serum neopterin determination in children with bacterial infections // Acta Biochim Pol. - 2015. - №62(1). - P. 133-137; Timothy H. Rainer, Cangel P.Y. Chan, Man Fai Leung et al. Diagnostic utility of CRP to neopterin ratio in patients with acute respiratory tract infections // Journal of infections. - 2009. - V. 58(2). - P. 123-130; M. Ip, Т.H. Rainer, N. Lee et al. Value of serum procalcitonin, neopterin, and C-reactive protein in differentiating bacterial from viral etiologies in patients presenting with lower respiratory tract infections // Diagnostic Microbiology and Infectious Disease. - 2007. - V. 59, №.2. - P. 131-136].
Luczak, Anna Liberek, Julita Dudzinska-Gehrmann et al. Evaluation of clinical usefulness of serum neopterin determination in children with bacterial infections // Acta Biochim Pol. - 2015. - №62(1). - P. 133-137; Timothy H. Rainer, Cangel P.Y. Chan, Man Fai Leung et al. Diagnostic utility of CRP to neopterin ratio in patients with acute respiratory tract infections // Journal of infections. - 2009. - V. 58(2). - P. 123-130; M. Ip, Т.H. Rainer, N. Lee et al. Value of serum procalcitonin, neopterin, and C-reactive protein in differentiating bacterial from viral etiologies in patients presenting with lower respiratory tract infections // Diagnostic Microbiology and Infectious Disease. - 2007. - V. 59, №.2. - P. 131-136].
Неоптерин [2-амино-4-гидрокси-6-(D-эритро-1',2',3'-тригидроксипропил)] - низкомолекулярное производное гуанозинтрифосфата, относящееся к классу птеридинов. Продуцируется макрофагами при активации последних интерфероном -γ или фактором некроза опухолей -αа и может быть обнаружено в моче и плазме (сыворотке) крови человека при различной патологии, связанной с активацией клеточного иммунитета [Фукс Д., Самсонов М.Ю., Вейс Г. Клиническое значение неоптерина при заболеваниях человека // Тер. архив. - 1993. - №5. - С. 80-87; Шевченко О., Олефиренко Г., Орлова О. Неоптерин // Лабораторная медицина. - 2001. - №4. - С. 55-61; Murr С. Neopterin as a marker for immune system activation // Curr. Drug Metabol. - 2002. - V. 3. - P. 175-187; Van der Poll, T. Effects on leukocytes after injection of tumor necrosis factor into healthy humans // Blood. - 1992. - V. 79. - P. 693-698; Fuchs, D. Interferon-gamma concentrations are increased in sera from individuals infected with human immunodeficiency virus type 1 // J. Acquired Immune Defic. Syndr. - 1989. - V. 2. - 158-162; Michael Eisenhut. Neopterin in Diagnosis and Monitoring of Infectious Diseases // Journal of Biomarkers. - 2013. - P. 1-10]. Доказана и роль других цитокинов в стимуляции (интерферон - α и β, ИЛ-2), либо ингибировании (ИЛ-4, ИЛ-10) синтеза неоптерина [Bitterlich G. Selective induction of mononuclear phagocytes to produce neopterin by interferons // Immunobiology. - 1988. - V. 176, №.3. - P. 228-235; Weiss, G. Modulation of neopterin formation and tryptophan degradation by Th1- and Th2 - derived cytokines in human monocytic cells // Clin. Exp. Immunol. - 1999. - V. 116. - P. 435-440; Ziegler, K. Control of tetrahydrobiopterin synthesis in T lymphocytes by synergistic action of interferon-γ and interleukin-2 // J Biol Chem. - 1990. - V. 265. - P. 17026-17030].
В настоящее время повышение уровня неоптерина в крови отмечено при онкологических заболеваниях [Sucher, R. Neopterin, a prognostic marker in human malignancies // Cancer Lett. - 2010. - V. 287. - P 13-22], аутоиммунных процессах [Mones, M. Association of neopterin as a marker of immune system activation and juvenile rheumatoid arthritis activity // JPediatr (RioJ). - 2015. - V. 91(4). - P. 352-357], заболеваниях сердца [Дегтярева О.В. Маркеры иммунного воспаления и сывороточный неоптерин у больных с острым коронарным синдромом // Украинский терапевтический журнал. - 2007. - №3. - С 28], в реакциях отторжения трансплантированных органов [Шевченко О.П. Неоптерин при трансплантации печени детям с врожденными заболеваниями печени и желчевыводящих путей // Вестник трансплантологии и искусственных органов. - 2011. - Т. 13, №2. - С. 58-62], при ожоговой травме [Лебедев М.Ю. Динамика изменений содержания неоптерина и интерфрона - гамма в сыворотке крови у пациентов с ожоговой травмой // Fundamental Research. - 2012. - №12. - С. 294-297].
Определена роль неоптерина и при инфекционных заболеваниях, на что указывают многие зарубежные и отечественные источники. Так, отмечено увеличение уровня неоптерина при вирусных заболеваниях [Дудина К.Р. Неоптерин-потенциальный диагностический и прогностический маркер при инфекционных заболеваниях // Казанский медицинский журнал. - 2014. - Т. 95, №6. - С. 938-943; BellmannWeiler R. IFN-gamma mediated pathways in patients with fatigue and chronic active Epstein Barr virus-infection // J. Affect Disord. - 2008. - V. 108, №1-2. - P. 171-176], ВИЧ-инфекции [Priyesh Bipathl. A non-specific biomarker of disease activity in HIV/AIDS patients from resource-limited environments // AfricanHealthSciences. - 2015. - V. 15. - P. 338-343]. Определено повышение концентрации неоптерина в крови у больных туберкулезом [Бердюгина О.В. Исследование уровня неоптерина при разных формах туберкулезного воспалительного процесса // Медицинский альянс. - 2015. - №4. - С. 68-72], бруцеллезом [G. Cakan, F.В. Bezirci, А. Kacka et al. Assessment of diagnostic enzyme-linked immunosorbent assay kit and serological markers in human brucellosis // Japanese Journal of Infectious Diseases. - 2008. - V. 61, №.5. - P. 366-370]. Уровень неоптерина среди умерших больных от сепсиса оказался в 3 раза выше, чем среди выживших больных, что позволило авторам рассматривать его как неблагоприятный прогностический маркер при данном заболевании [Nuriye Tasdelen Fisgin. The Value of Neopterin and Procalcitonin in Patients with Sepsis // SMJ. - 2010. - V. 103(3). - P. 210-216; T. Baydar, O. Yuksel, Т.T. Sahin et al. Neopterin as a prognostic biomarker in intensive care unit patients // Journal of Critical Care. - 2009. - V. 24, №3. - P. 318-321]. Кроме того, отмечено увеличение уровня неоптерина и при бактериальных менингитах [L. Hagberg, L. Dotevall, G. Norkrans, M. Larsson, H. Wachter, and D. Fuchs. Cerebrospinal fluid neopterin concentrations in central nervous system infection // Journal of Infectious Diseases. - 1993. - V. 168, №.5. - P. 1285-1288]. Сведений об уровне неоптерина в сыворотке крови больных, вирусными и бактериальными кишечными инфекциями в сравнении, в доступной нам литературе найдено не было.
Задача изобретения - предложить способ дифференциальной диагностики бактериальных и вирусных кишечных инфекций у детей раннего возраста.
Технический результат состоит в обеспечении возможности определения острой кишечной инфекции у детей раннего возраста с выявлением как бактериальной, так и вирусной этиологии заболевания.
Технический результат достигается изучением уровня неоптерина в сыворотке крови детей, больных бактериальными и вирусными кишечными инфекциями, с использованием иммуноферментного анализа (ИФА) с помощью набора реагентов «Neopterin, ELISA» Гамбург, Германия.
Для подтверждения объективности способа нами обследовано 79 детей раннего возраста с острыми кишечными инфекциями. Из них 38 детей были с бактериальными кишечными инфекциями (I группа). 41 ребенок был с вирусной кишечной инфекцией (II группа). Для установления бактериальной этиологии заболевания все больные были обследованы бактериологически (посев кала на шигеллы, сальмонеллы, УПФ, посев промывных вод желудка) и серологически (РИГА с дизентерийным, сальмонеллезным, иерсиниозным и псевдотуберкулезным диагностикумами). Случаи ОКИ, вызванные УПФ, учитывались при количестве выделенной флоры из фекалий, превышающей 104 КОЕ. Для диагностики вирусной этиологии заболевания использовался иммуноферментный анализ кала для выявления антигена ротавируса (Ротавирус-антиген, ИФА, “Вектор-БЕСТ”, Россия). На ротавирусы также были обследованы фекалии всех 79 наблюдавшихся нами больных. III группу (сравнения) составили 40 условно-здоровых ребенка, поступивших на плановое хирургическое лечение. Все обследованные нами больные - дети раннего возраста (от 2 месяцев до 3 лет включительно).
По результатам проведенного анализа, в острый период заболевания отмечено достоверное увеличение уровня неоптерина у детей больных кишечными инфекциями как вирусной (13,34 плюс/минус 1,46, р менее 0,01), так и бактериальной этиологии (29,03 плюс/минус 3,24, р менее 0,001), по сравнению с группой условно-здоровых детей (8,3 плюс/минус 0,61). Кроме того, разница показателей между группами бактериальных и вирусных кишечных инфекций также оказалась достоверной (р менее 0,001). Так, при бактериальных диареях уровень неоптерина в 2,2 раза выше, чем при вирусных.
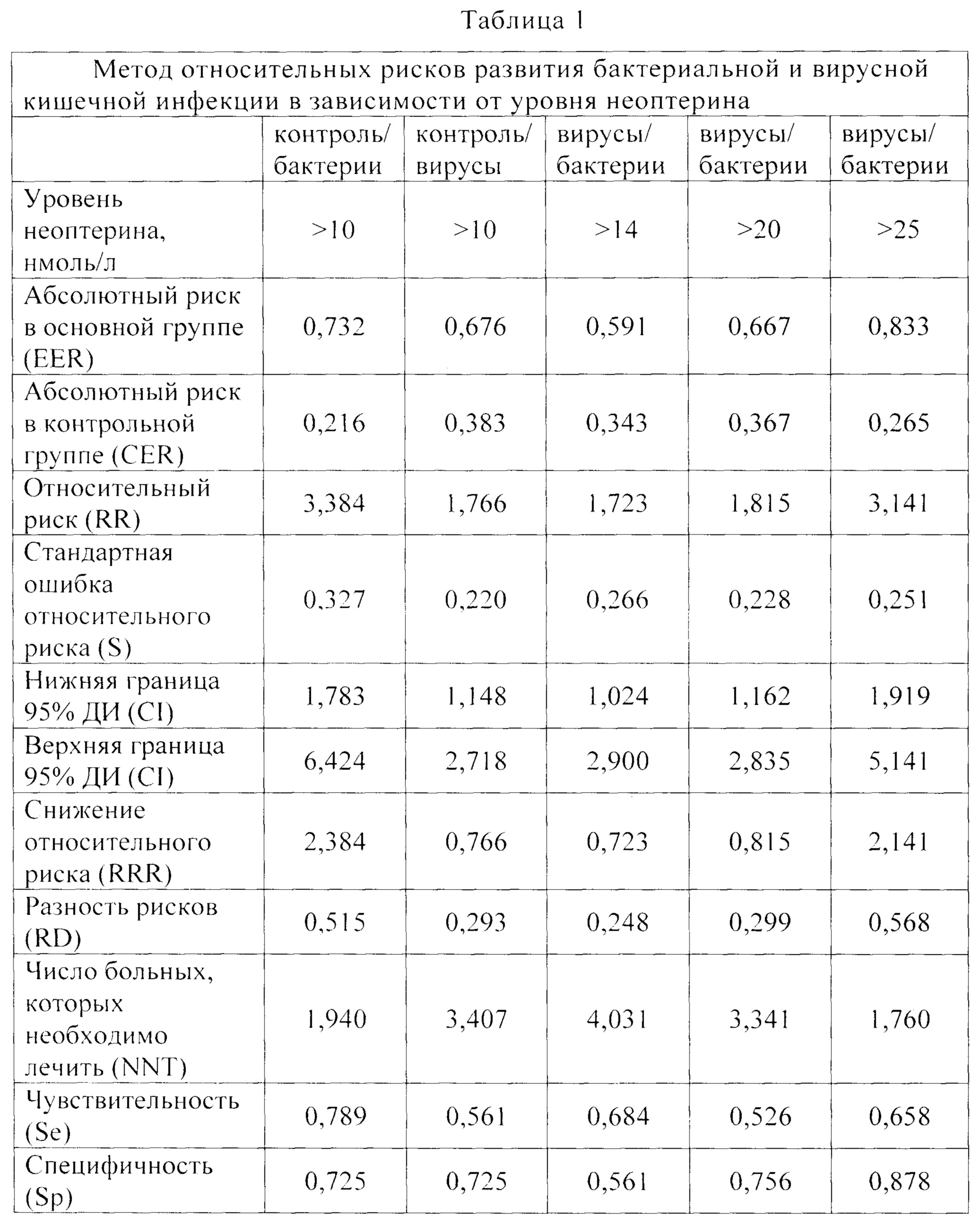
Методом относительных рисков, было выяснено, что значение неоптерина выше 10 нмоль/л повышает риск развития острых вирусных кишечных инфекций в 1,7 раз (чувствительность - 56,1%, специфичность - 72,5%), бактериальных - в 3,4 раза (чувствительность - 78,9%, специфичность - 72,5%). При этом, уровень неоптерина выше 14 нмоль/л повышает риск развития бактериальных кишечных инфекций в 1,7 раз (чувствительность - 68,4%, специфичность - 56,1%), чем вирусных инфекций. Уровень неоптерина выше 20 нмоль/л увеличивают риск бактериальной этиологии заболевания в 1,8 раз относительно вирусной природы заболевания (чувствительность - 52,6%, специфичность - 75,6%). Наиболее показательным является повышение уровня неоптерина выше 25 нмоль/л, когда относительный риск развития бактериальной диареи в 3,1 раз выше, чем вирусной (чувствительность - 65,8%, специфичность - 87,8%). Табл. 1.
Методом доверительных интервалов, были получены диапазоны значений уровня неоптерина, соответствующих бактериальной и вирусной этиологии заболевания. Так, при значении неоптерина в сыворотке крови детей раннего возраста в пределах 10,49-16,2 нмоль/л диагностируют вирусную этиологию заболевания, в диапазоне 22,54-35,52 нмоль/л бактериальную кишечную инфекцию. Табл. 2.
Полученные данные делают возможным использование неоптерина, как дополнительного дифференциально-диагностического маркера бактериальных и вирусных кишечных инфекций у детей раннего возраста.
Предложенный нами способ является более экономичным в использовании биологического материала (на анализ требуется 20 мкл сыворотки крови), что немаловажно в педиатрической практике. Способ является достаточно оперативным, дающим возможность получения результата в день забора материала, постановка реакции занимает в среднем 4 часа, что позволяет своевременно установить бактериальный или вирусный характер кишечной инфекции и назначить адекватную терапию больным. Кроме того, отличительной особенностью является определение уровня неоптерина сыворотки крови у детей раннего возраста, наиболее подверженных тяжелому и осложненному течению кишечных инфекций (Ершова И.Б., Мочалова А.А., Осипова Т.Ф. и др. Препараты, восстанавливающие микробиоценоз, как этиотропная терапия острых кишечных инфекций у детей // Актуальная инфектология. - 2015. - №2(7). - С. 45-50).
Преимущества предлагаемого способа:
- достаточная чувствительность для дифференциальной диагностики бактериальных и вирусных кишечных инфекций;
- возможность определения уровня неоптерина сыворотки крови в ранние сроки заболевания;
- требуется небольшой объем забираемого биологического материала (для анализа требуется 20 мкл сыворотки крови);
- возможность получения результата в день взятия крови, что особенно важно для ранней дифференциальной диагностики бактериальных и вирусных кишечных инфекций.
В качестве примера использования предлагаемого метода в клинико-лабораторном обследовании больных кишечными инфекциями приводим выписки из историй болезни.
Пример 1.
История болезни №1159. Больная Б. Геля, 1 год 10 месяцев, поступила в клинику декабре 2016 года на вторые сутки от начала заболевания. Заболела остро, когда температура тела повысилась до 39,5°С, появилась рвота 2 раза в день, жидкий стул до 3 раз в день с патологическими примесями (со слизью). Ребенок был доставлен в стационар врачом скорой помощи с предварительным диагнозом: «Кишечная инфекция неустановленной этиологии».
При поступлении в стационар состояние расценено как среднетяжелое за счет интоксикационного и кишечного синдромов. Ребенок в сознании. Отмечается слабость, вялость. Аппетит снижен. Кожные покровы бледные, чистые. В ротоглотке патологических изменений нет. Тоны сердца громкие, ритмичные, ЧСС 134 в 1 мин. Дыхание пуэрильное, хрипов нет. ЧД - 30 в 1 мин. Живот мягкий, умеренно болезненный, урчащий по ходу петель кишечника.
В общем анализе крови - лейкоцитоз до 15,1*109/л, токсический сдвиг лейкоцитарной формулы влево до 10% палочкоядерных нейтрофилов, нейтрофилез (69%). В копрограмме - признаки амилореи (+++), лейкоциты - до 20 в поле зрения, слизь ++, бактерии +.
При исследовании уровня неоптерина получен следующий результат: 20,264 нмоль/л, что позволило диагностировать бактериальную кишечную инфекцию.
Клинический диагноз: Кишечная инфекция, вызванная Pseudomona aeruginosae, гастроэнетрит, средней степени тяжести (выделение Pseudomona aeruginosae при бактериальном посеве кала).
Пример 2.
История болезни №3096. Больная Л. Софья, 1 год 5 месяцев поступила в стационар в апреле 2016 года, на 3 сутки от начала заболевания. Заболевание началось с подъема температуры до 39,6°С, рвоты до 10 раз в сутки, жидкого водянистого стула до 20 раз в сутки.
При поступлении в стационар состояние было расценено как среднетяжелое за счет умеренного интоксикационного и кишечного синдромов. Ребенок был вялым. Кожные покровы бледные, сыпи нет. Слизистые ротоглотки бледно-розовые, чистые. Язык сухой, обложен белесоватым налетом, запах ацетона изо рта. Тоны сердца громкие, ритмичные, ЧСС - 138 в 1 мин. Дыхание пуэрильное, хрипов нет. ЧД - 29 в 1 мин. Живот мягкий, безболезненный при пальпации, незначительно урчащий по ходу петель тонкого кишечника.
В общем анализе крови - лейкопения (до 4,7*109/л), токсический сдвиг лейкоцитарной формулы влево до 9% палочкоядерных нейтрофилов, нейтрофилез (77%). В копрограмме - слизь (+++), лейкоциты - большое количество в поле зрения, бактерии +.
Уровень неоптерина сыворотки крови составил 15,461 нмоль/л, свидетельствующий в пользу вирусной этиологии заболевания, которая была подтверждена положительным результатом ИФА кала на антиген ротавируса.
Клинический диагноз: Ротавирусная инфекция, гастроэнтерит, средней степени тяжести. Токсикоз с эксикозом 1 степени.