Аморфный аллисартан изопроксил, способ его получения и фармацевтическая композиция, содержащая аморфный аллисартан изопроксил
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к области фармацевтической химии, и в частности, относится к аморфному аллисартану изопроксилу (allisartan isoproxil), способу его получения и к фармацевтической композиции, содержащей аморфный аллисартан изопроксил.
Предшествующий уровень техники
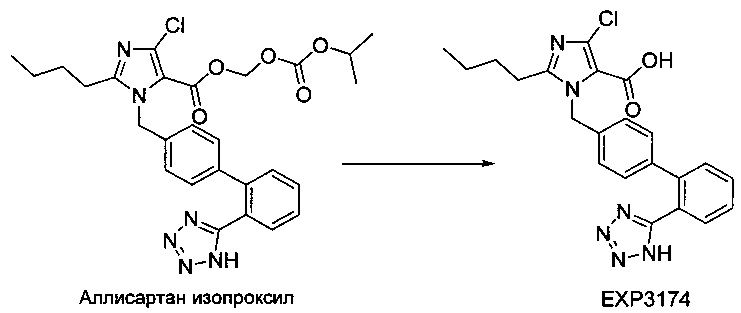
Аллисартан изопроксил (CAS: 947331-05-7) с химическим названием 1-[(изопропокси)-карбонилокси]метиловый эфир 2-бутил-4-хлор-1-[2'-(1Н-тетразол-5-ил)-1,1'-бифенил-метил]-имидазол-5-карбоновой кислоты представляет собой новый антагонист ангиотензиновых рецепторов II. В китайском патенте CN 200680000397.8 раскрыта структурная формула аллисартана изопроксила. Аллисартан изопроксил показывает низкую токсичность и лучшую антигипертензивную эффективность по сравнению с подобными продуктами (например лозартаном). Аллисартан изопроксил оказывает свое антигипертензивное действие посредством образования активного метаболита (ЕХР3174) in vivo.
Согласно известному уровню техники, аллисартан изопроксил показывает недостаточную текучесть, малую объемную плотность и заметные электростатические явления. В китайском патенте CN 200710094131.0 раскрыта кристаллическая форма аллисартана изопроксила и способ ее получения. Кристалл аллисартана изопроксила, полученный этим способом, показывает высокую стабильность, но относительно малую объемную плотность, недостаточную текучесть и заметные электростатические явления после сушки. Это вызывает загрязнение воздуха пылью во время пульверизации, субупаковки и использования этого кристалла, что, с одной стороны, вызывает затруднения для уборки и охраны труда в месте проведения работы и, с другой стороны, вызывает затруднения в отношении точности взвешивания и упаковки.
В китайских патентах, как в CN 200710094021.4, так и CN 201110289695.6 раскрыты способы получения аллисартана изопроксила, и как повторяется автором изобретения, полученные кристаллические формы согласуются с теми, что раскрыты в CN 200710094131.0.
Принимая во внимание вышеупомянутые недостатки аллисартана изопроксила, раскрытые в известном уровне техники, можно видеть, что техническая задача, подлежащая решению в настоящем изобретении прежде всего, заключается в получении аллисартана изопроксила с текучестью, подходящей для последующей обработки, с подходящей объемной плотностью и без заметных электростатических явлений.
Краткое изложение сущности изобретения
Для решения недостатков известного уровня техники автор изобретения посредством множества экспериментов получил улучшенную нерасфасованную лекарственную форму аллисартана изопроксила, которая показывает лучшую текучесть, чем кристалл аллисартана изопроксила, раскрытый в известном уровне техники, а, кроме того, объемная плотность заметно больше, чем у кристалла аллисартана изопроксила, раскрытого в известном уровне техники, и не наблюдается никаких заметных электростатических явлений. Посредством дополнительного анализа обнаружили, что полученный аллисартан изопроксил существует в аморфной форме, которая не была раскрыта в известном уровне техники, и, в больше степени неожиданно, полученный аморфный аллисартан изопроксил может стабильно существовать в фармацевтической композиции. Аморфный аллисартан изопроксил по настоящему изобретению не только решает недостатки кристалла аллисартана изопроксила известного уровня техники, но обеспечивает удобство в изготовлении препарата аллисартана изопроксила, а также дает больше возможностей для оптимизации изготовления препарата аллисартана изопроксила.
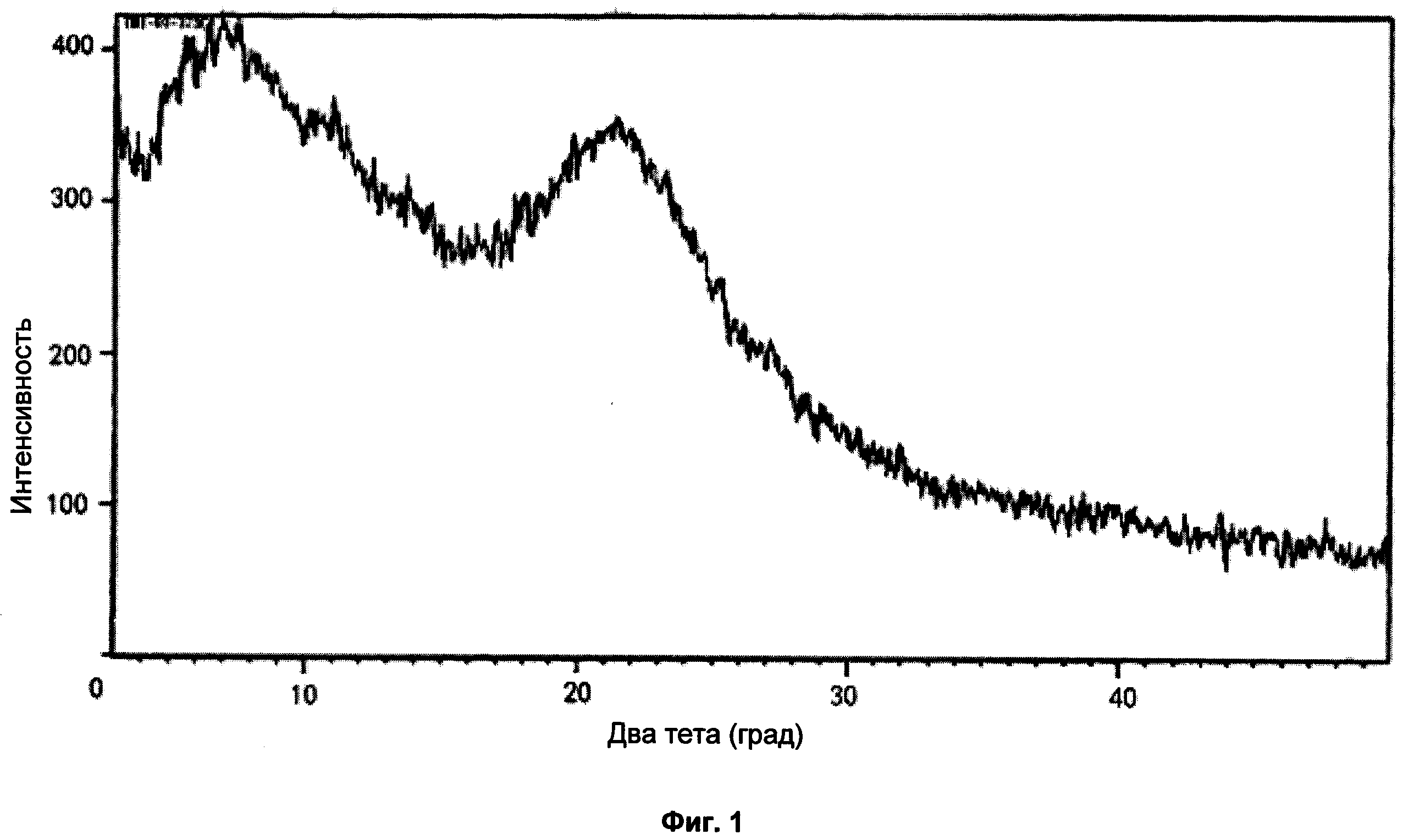
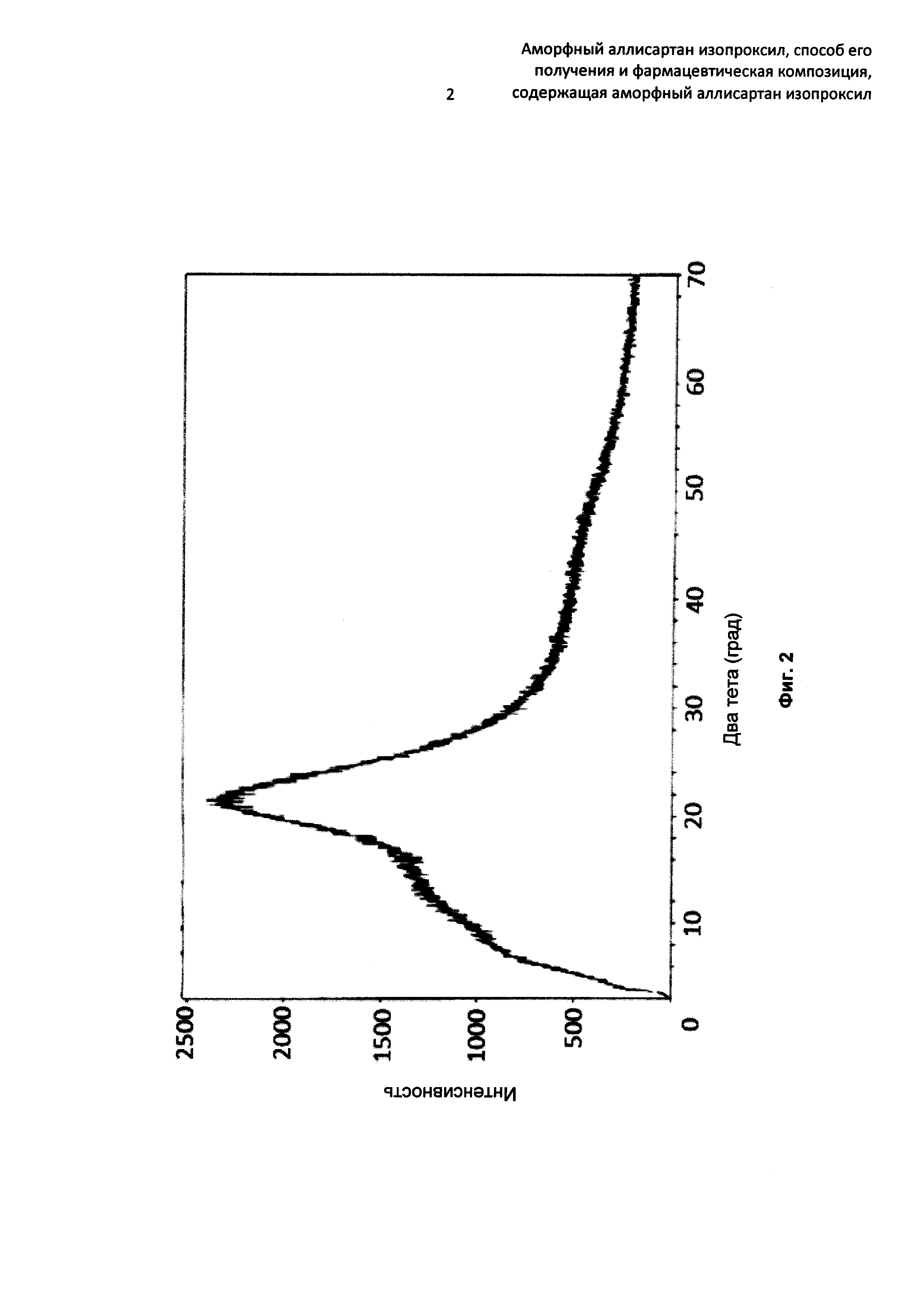
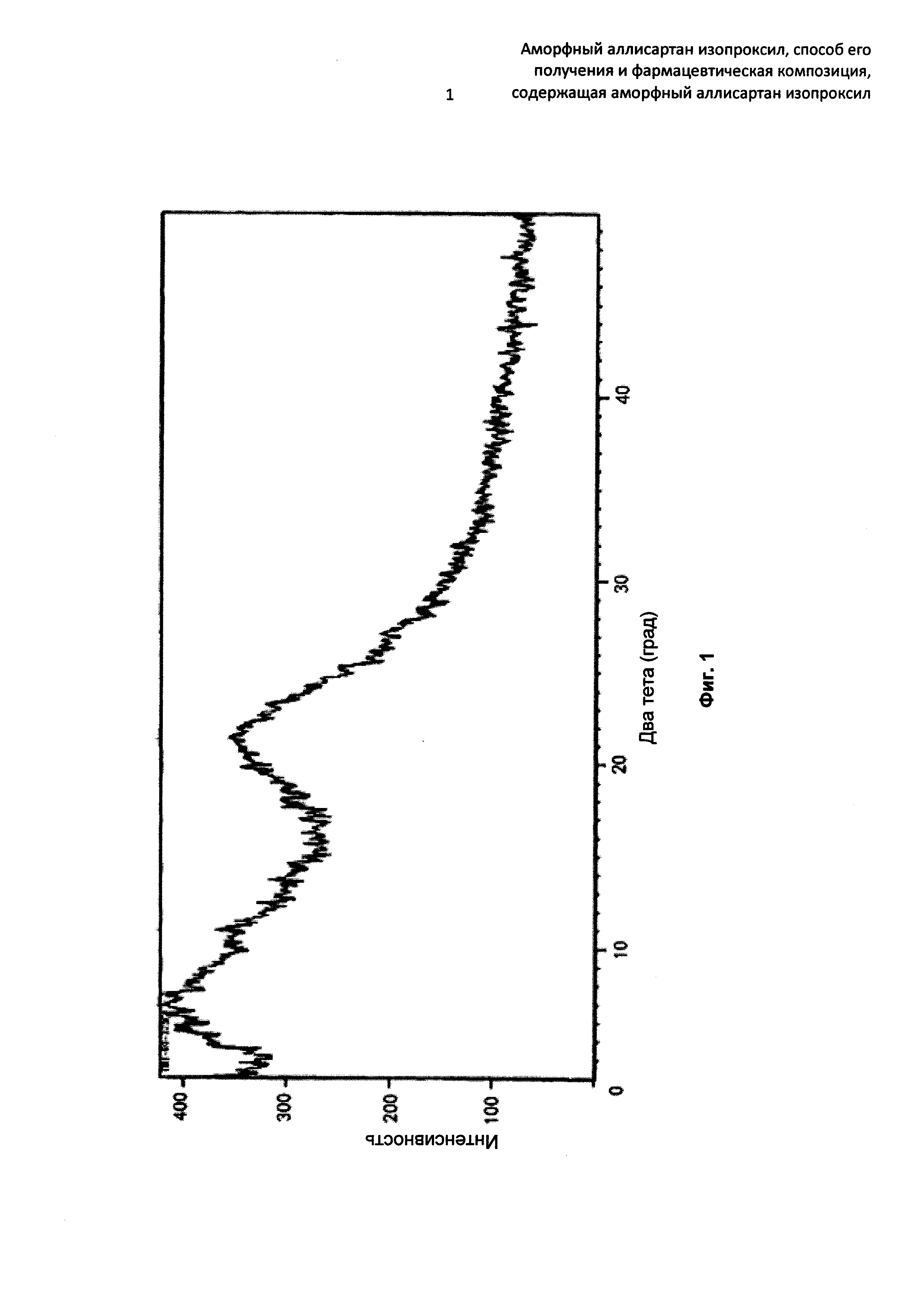
Аморфное твердое вещество по настоящему изобретению не имеет заметного и острого дифракционного пика в спектре дифракции рентгеновских лучей на порошке (XRD). Как хорошо известно в данной области техники, соединение в аморфной форме обладает термодинамической нестабильностью, что означает, что молекулы полностью разупорядочены, и поэтому не наблюдается никакого дифракционного пика или наблюдается неострый дифракционный пик/пики в спектре XRD аморфной формы. В заключение, соединение без острого дифракционного пика в спектре XRD может быть определено как существующее в виде аморфной формы. В одном воплощении настоящего изобретения аморфный аллисартан изопроксил не имеет ни одного заметного и острого дифракционного пика в спектре XRD, что может быть определено как аморфная форма. В одном воплощении настоящего изобретения аморфный аллисартан изопроксил имеет неострый(е) дифракционный(е) пик/пики в спектре XRD. В одном воплощении, как показано на Фиг. 1, спектр XRD аморфного аллисартана изопроксила имеет два широких и слабых неострых дифракционных пика при значении 2θ от 0° до 30°; в одном воплощении, как показано на Фиг. 2, спектр XRD аморфного аллисартана изопроксила имеет один широкий и слабый неострый пик при значении 2θ от 0° до 30° в спектре XRD. Кроме того, для Фиг. 1, существует два широких и слабых дифракционных пика, соответственно, при значении 2θ от 0° до 15° и при значении 2θ от 15° до 30° в спектре XRD. Обе Фиг. 1 и 2 демонстрируют, что аллисартан изопроксил, предлагаемый в настоящем изобретении, существует в аморфной форме.
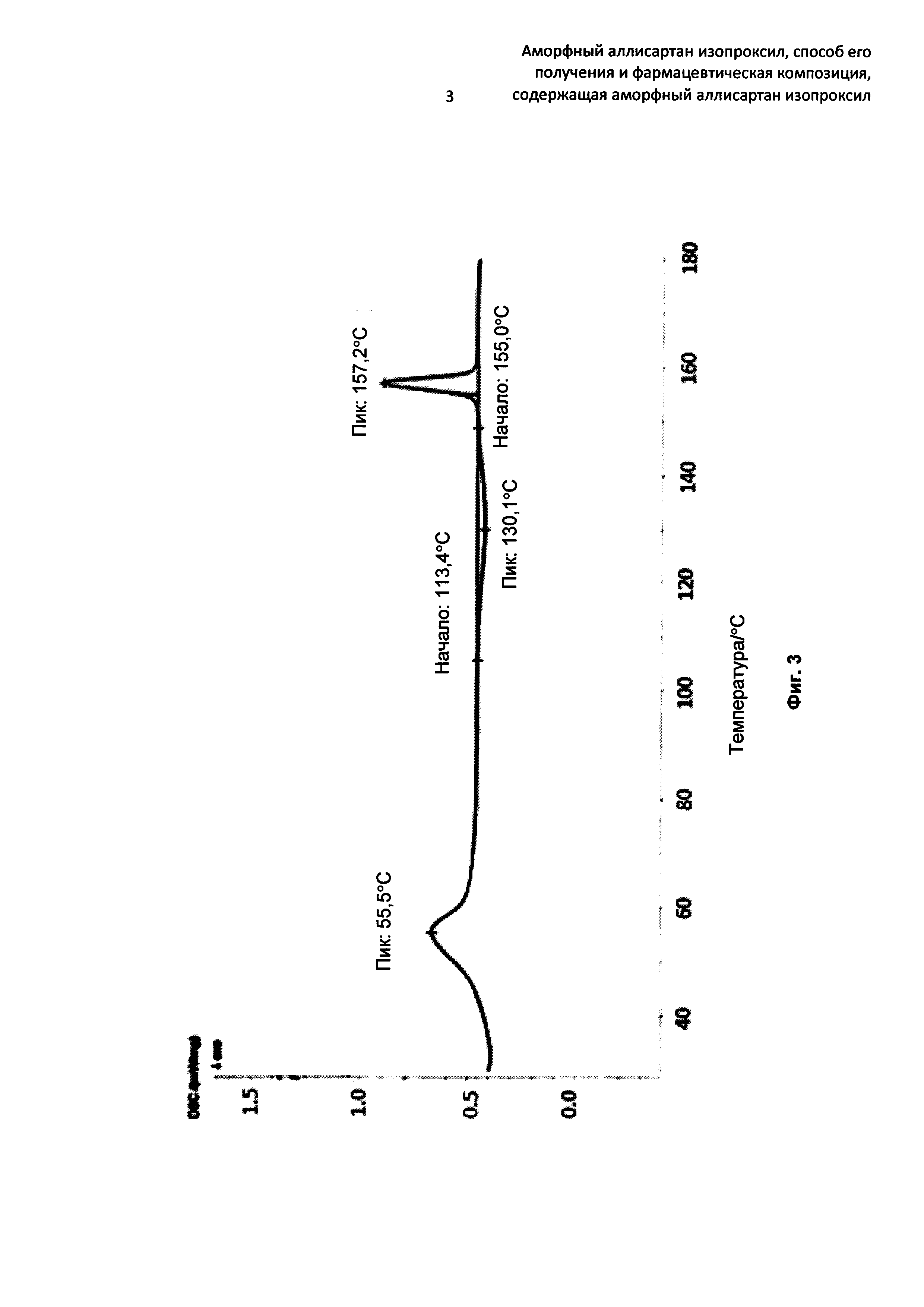
Спектр дифференциальной сканирующей калориметрии (DSC) аморфного аллисартана изопроксила является таким, как показано на Фиг. 3. В частности, данный спектр показывает, что: аморфная форма имеет эндотермический пик при 56±3°С, экзотермический пик при 130±3°С и эндотермический пик при 157±3°С.
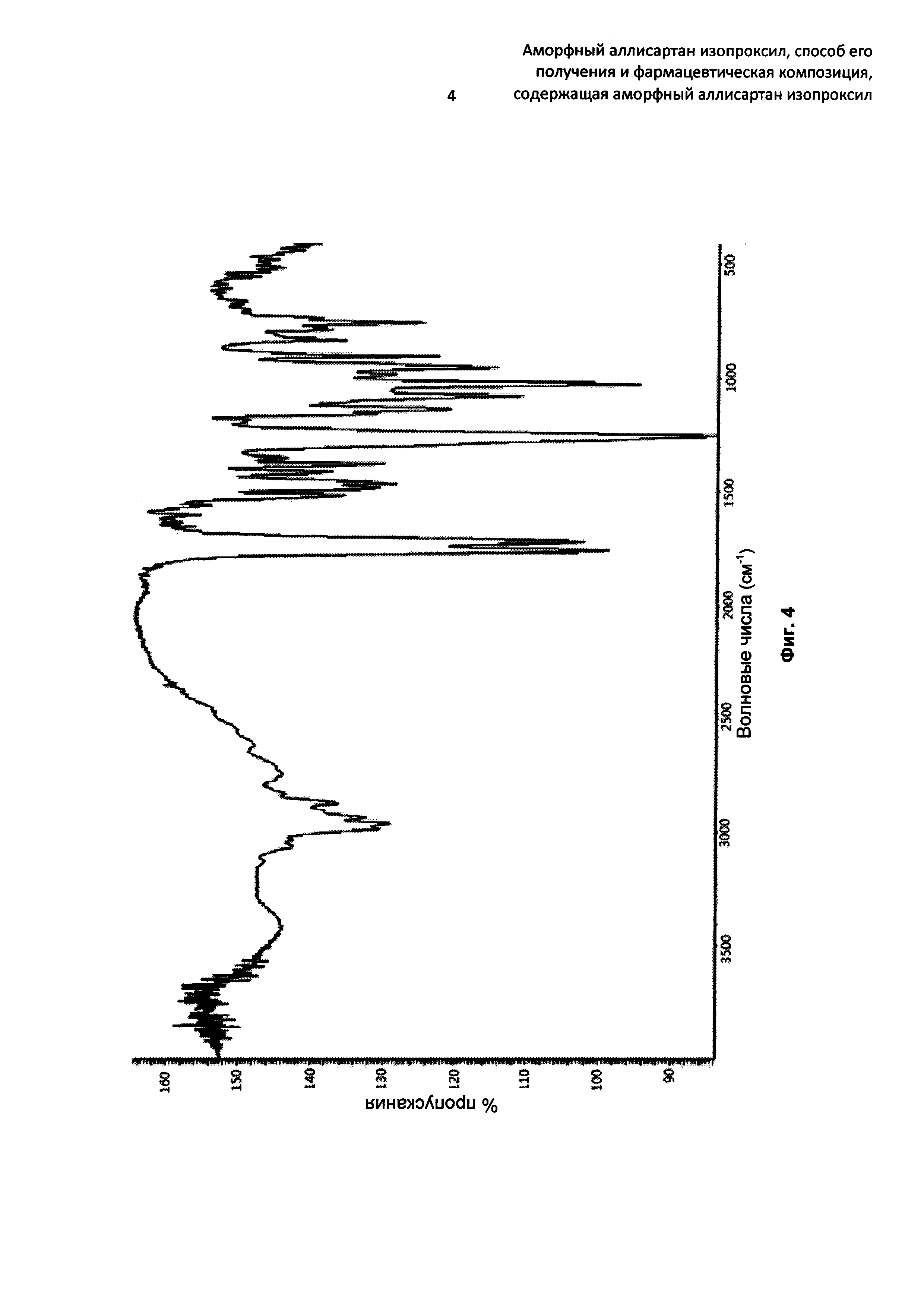
Инфракрасный (ИФ) спектр аморфного аллисартана изопроксила является таким, как показано на Фиг. 4. В частности, аморфный аллисартан изопроксил имеет пики поглощения около 2961, 1759, 1720, 1466, 1378, 1255, 1138, 1080, 1027, 955, 906 и 760 см-1.
Еще одна задача настоящего изобретения заключается в том, чтобы предложить способ, способный стабильно получать аморфный аллисартан изопроксил по настоящему изобретению, включающий следующие стадии:
1) растворение кристалла аллисартана изопроксила в органическом растворителе при комнатной температуре или при нагревании; и
2) концентрирование полученного раствора при пониженном давлении до сухого состояния, затем сушка в вакууме до постоянной массы и охлаждение до комнатной температуры, с получением аморфного аллисартана изопроксила.
На стадии 1) кристалл аллисартана изопроксила предпочтительно представляет собой кристалл, полученный способом из патента CN 200710094131.0, органический растворитель представляет собой дихлорметан или смешанный растворитель дихлорметан-метанол, где соотношение Vдихлорметан к Vметанол составляет 100 к 0-5, и соотношение объем-масса органического растворителя к аллисартану изопроксилу контролируют при 1,5-2 мл/г; если необходимо, добавляют для обесцвечивания подходящее количество активированного угля; на стадии 2) относительное давление, применяемое для концентрирования при пониженном давлении, равно или меньше -0,05 МПа (≤-0,05 МПа), и температуру регулируют при 0-40°С; и относительное давление сушки в вакууме равно или меньше -0,09 МПа (≤-0,09 МПа), и температура составляет 30-50°С. Более конкретно, если ожидают аморфный аллисартан изопроксил как показано на Фиг. 1, то во время концентрирования требуется более низкая температура суспензии или более низкое относительное давление, в одном воплощении при относительном давлении -0,05 МПа и температуре 25°С, в другом воплощении при относительном давлении -0,09 МПа и температуре 40°С. Если ожидают аморфный аллисартан изопроксил как показано на Фиг. 2, во время концентрирования требуется более высокое относительное давление и более высокая температура суспензии, в одном воплощении относительное давление -0,05 МПа и температура 40°С.
Различные технические параметры способа получения (например, количественное соотношение растворителей, температура, относительное давление и так далее) обусловливают получение стабильного аморфного аллисартана изопроксила по настоящему изобретению, и изменения технических параметров могут приводить к другим результатам эксперимента. Например, посредством сравнительных экспериментов обнаружено, что: исходя из допущения, что другие условия не изменяются, при использовании смешанного растворителя дихлорметан-метанол с соотношением Vдихлорметан к Vметанол равном 100 к 10 полученный аллисартан изопроксил находится в кристаллической форме, раскрытой в известном уровне техники.
Посредством экспериментов автор изобретения обнаружил, что объемная плотность порошка аморфного аллисартана изопроксила по настоящему изобретению значительно больше, чем объемная плотность кристаллического порошка в известном уровне техники, и также обнаружил, что электростатические явления аморфного порошка значительно уменьшаются. Кроме того, текучесть аморфного порошка также значительно лучше, чем текучесть кристаллического порошка, раскрытого в известном уровне техники. Применение аморфного аллисартана изопроксила может не только значительно снизить загрязнение воздуха пылью во время изготовления, но также обеспечить удобства для последующих процессов изготовления аллисартана изопроксила.
Еще одна задача настоящего изобретения заключается в том, чтобы предложить фармацевтическую композицию, содержащую аморфный аллисартан изопроксил по настоящему изобретению.
Фармацевтическая композиция состоит из аморфного аллисартана изопроксила по настоящему изобретению и фармацевтических эксципиентов. В частности, фармацевтические эксципиенты включают, без ограничения, наполнители, связывающие вещества, разрыхлители и смазывающие вещества.
Фармацевтическая композиция может быть получена в виде препаратов, которые включают, без ограничения, таблетки, капсулы, гранулы, порошки, суппозитории и тому подобное. Предпочтительно, фармацевтическая композиция может быть получена в виде таблеток.
Фармацевтические эксципиенты представляют собой эксципиенты, обычно применяемые в данной области техники. В частности, наполнители включают, без ограничения, крахмал, лактозу, маннит, сахарозу, микрокристаллическую целлюлозу и тому подобное; связывающие вещества включают, без ограничения, гидроксиметилцеллюлозу, карбоксиметилцеллюлозу натрия, крахмальную суспензию, желатин и тому подобное; разрыхлители включают, без ограничения, кроссповидон, карбонат кальция, карбонат натрия, картофельный крахмал или крахмал тапиоки, силикатное соединение, альгиновую кислоту и тому подобное; и смазывающие вещества включают, без ограничения, аэросил, порошок талька, стеарат магния, твердый полиэтиленгликоль, лаурилсульфат натрия и тому подобное; и, если желательно, дополнительно может быть включен процесс нанесения на композицию покрытия с помощью покрывающих веществ в данной области техники.
Аморфный аллисартан изопроксил по настоящему изобретению может стабильно существовать в фармацевтической композиции. В частности, благодаря анализу таблетки, изготовленной обычными способами в данной области техники, посредством XRD-детекции обнаружили, что после хранения в течение 6 месяцев в условиях ускоренного исследования стабильности (40°C/75%RH) аллисартан изопроксил по-прежнему существует в той же самой аморфной форме и по существу с постоянным содержанием, тем самым демонстрируется, что качество композиции может быть надежно обеспечено.
В одном воплощении ингредиенты фармацевтической композиции аллисартана изопроксила представляют собой:
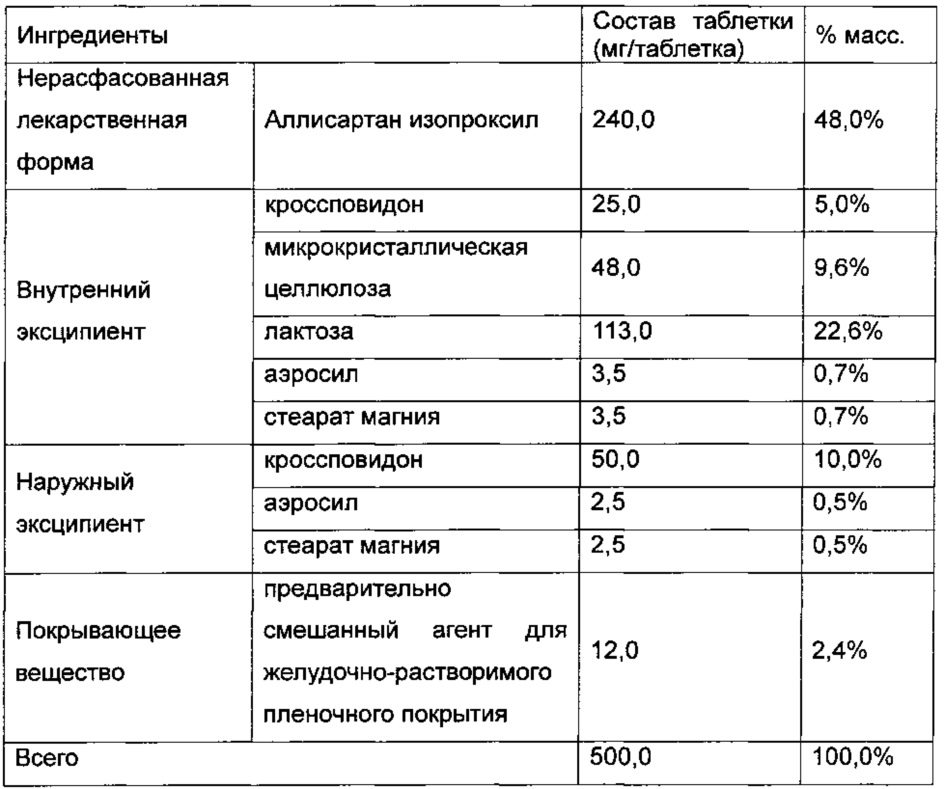
Смешивание нерасфасованной лекарственной формы и внутренних эксципиентов равномерно, в последовательности согласно количественным соотношениям, перечисленным выше, затем гранулирование посредством способа сухого гранулирования с получением гранул внутренней фазы; добавление и смешивание наружных эксципиентов последовательно, согласно перечисленным выше количественным соотношениям, с получением фармацевтической композиции; прессование полученной фармацевтической композиции и нанесение покрытия на полученные таблетки.
Посредством анализа обнаружили, что аморфный аллисартан изопроксил может стабильно существовать в таблетках, полученных выше. В частности, из спектра дифракции рентгеновских лучей на порошке полученных таблеток обнаружили, что аллисартан изопроксил по-прежнему существует в виде аморфной формы и остается стабильным в виде той же самой аморфной формы после хранения в течение длительного периода времени.
Посредством экспериментов автором изобретения обнаружено, что аморфный аллисартан изопроксил, предлагаемый в настоящем изобретении, может стабильно существовать в фармацевтической композиции и, таким образом, если способами детекции продемонстрировано, что активный ингредиент существует в виде аморфной формы в композиционном продукте, то следует считать, что использован аморфный аллисартан изопроксил, предлагаемый в настоящем изобретении. В дополнение к дифракции рентгеновских лучей на порошке (XRD), способы детекции дополнительно включают дифференциальную сканирующую калориметрию (DSC), инфракрасную (ИФ) спектрометрию, рамановскую спектроскопию (Raman), спектроскопию ядерного магнитного резонанса твердого тела (ттЯМР) и другие способы детекции, которые могут демонстрировать форму, в которой аллисартан изопроксил существует в фармацевтической композиции.
По сравнению с известным уровнем техники, настоящее изобретение показывает следующие преимущества и благоприятные эффекты:
1. Предложение аморфного аллисартана изопроксила, не раскрытого в известном уровне техники, объемная плотность которого больше, чем объемная плотность кристалла, раскрытого в известном уровне техники, электростатические явления не заметны, и текучесть заметно лучше, чем у кристалла, раскрытого в известном уровне техники.
2. Предложение способа получения аллисартана изопроксила, в соответствии с которым можно стабильно получать целевой аморфный аллисартан изопроксил.
3. Предложение фармацевтической композиции, содержащей аморфный аллисартан изопроксил по настоящему изобретению.
Краткое описание графических материалов
Фиг. 1 представляет собой спектр XRD аморфного аллисартана изопроксила, полученного по Примеру 1;
Фиг. 2 представляет собой спектр XRD аморфного аллисартана изопроксила, полученного по Примеру 3;
Фиг. 3 представляет собой спектр DSC аморфного аллисартана изопроксила, полученного по Примеру 1;
Фиг. 4 представляет собой инфракрасный спектр аморфного аллисартана изопроксила, полученного по Примеру 1;
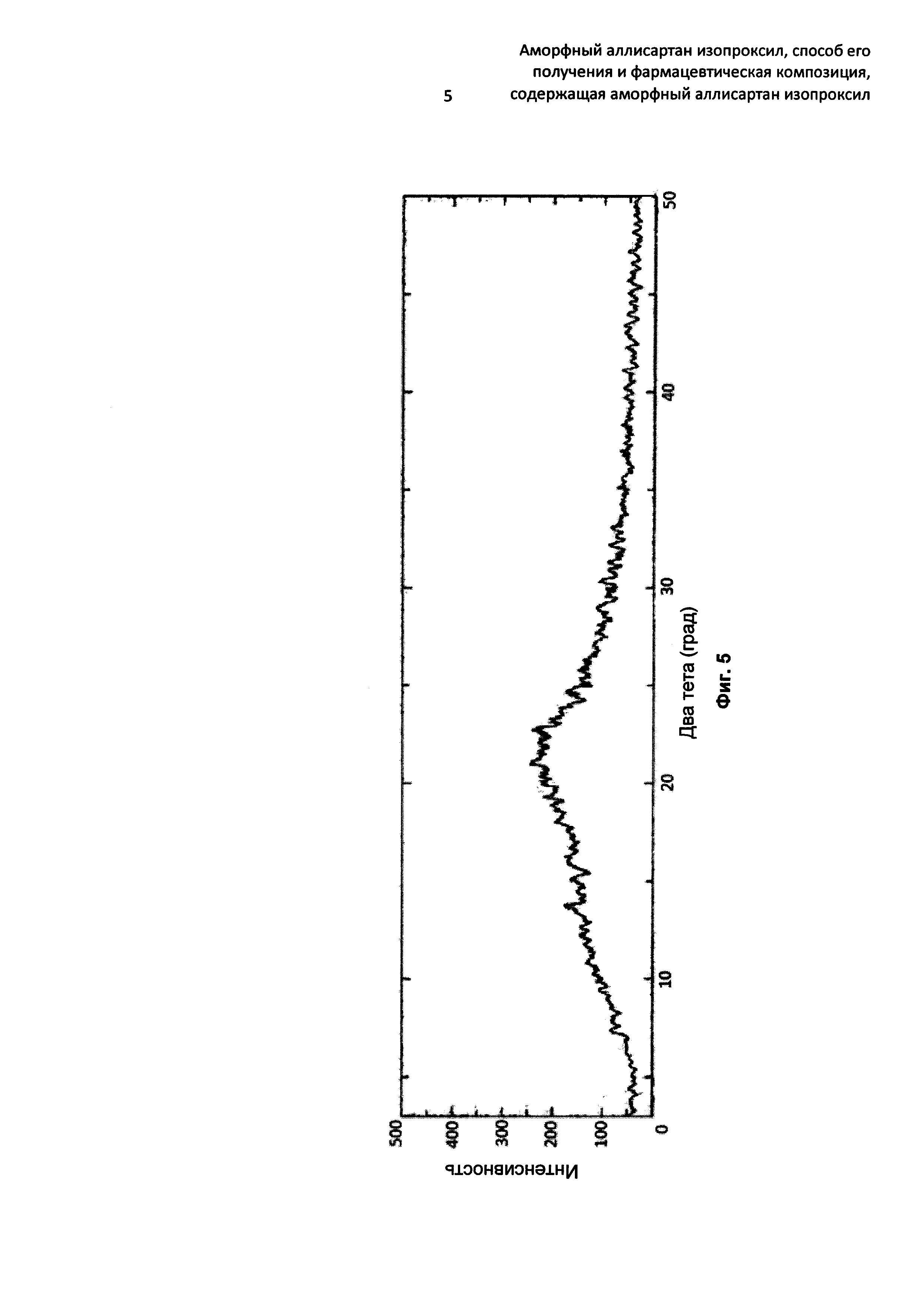
Фиг. 5 представляет собой спектр XRD фармацевтической композиции, полученной по Примеру 5.
Подробное описание Примеров
Все данные детекции и спектры по настоящему изобретению получены посредством обычных аналитических приборов в обычных методиках при обычных условиях детекции в данной области техники. Настоящее изобретение дополнительно в качестве примера описано более подробно в сочетании с примерами и фигурами, хотя осуществление настоящего изобретения не ограничивается этим.
Спектр XRD, как показано на Фиг. 1 настоящего изобретения, получен посредством детекции с помощью рентгеновского дифрактометра Empyrean в следующих условиях детекции: Cu Kα1, напряжение 40 кВ, ток 40 мА, щель расходимости 1/32°, щель рассеивания 1/16°, антирассеивающая щель 7,5 мм, диапазон 2θ 3-50°, размер шага 0,02° и время на стадию 40 секунд.
Спектр XRD, как показано на Фиг. 2 настоящего изобретения, получен посредством детекции с помощью рентгеновского дифрактометра Rigaku MiniFlex 600 в следующих условиях детекции: Cu Kα1, напряжение 40 кВ; ток 15 мА; щель Соллера (регистр.) 2,5 град., IHS 10,0 мм, DS 0,625 град., SS 13,0 мм и Соллер (рег.) 2,5 град.; щель рассеивания 1/16°, антирассеивающая щель 7,5 мм, диапазон 2θ 3-70°, размер шага 0,02° и 5 стадий/мин.
Спектр DSC по настоящему изобретению получен посредством детекции с помощью дифференциального сканирующего калориметра DSC 204F1 от Netzsch Corporation в атмосфере N2 (с чистотой больше или равной 99,99%, 20 мл/мин), причем кривую нагревания регистрируют от комнатной температуры до 180°С, со скоростью роста температуры 10°С/мин.
Инфракрасный спектр по настоящему изобретению получен с использованием методики с пластинкой KBr (бромида калия).
Пример 1
16,5 мл дихлорметана добавляли в колбу, содержащую 10 г кристаллов аллисартана изопроксила, и колбу нагревали при температуре дефлегмации до тех пор, пока раствор не становился прозрачным. После удаления растворителя посредством концентрирования раствора при относительном давлении -0,05 МПа и 25°С полученное твердое вещество сушили в вакууме при относительном давлении -0,09 МПа и 40°С до тех пор, пока его масса не стала постоянной, и затем охлаждали до комнатной температуры с получением аморфного аллисартана изопроксила. Полученный аморфный аллисартан изопроксил не показывал заметных электростатических явлений. Спектр XRD показан на Фиг. 1, спектр DSC показан на Фиг. 3, и ИФ-спектр показан на Фиг. 4.
Пример 2
20 мл смешанного раствора дихлорметан/метанол (соотношение Vдихлорметан к Vметанол равно 100 к 5) добавляли в колбу, содержащую 10 г кристаллов аллисартана изопроксила, и колбу нагревали при температуре дефлегмации до тех пор, пока раствор не становился прозрачным. После удаления растворителя посредством концентрирования раствора на водяной бане при относительном давлении -0,09 МПа и 40°С полученное твердое вещество сушили в вакууме при относительном давлении -0,095 МПа и 50°С до тех пор, пока его масса не стала постоянной, и затем охлаждали до комнатной температуры с получением такого же аморфного аллисартана изопроксила, как в Примере 1. Полученный аморфный аллисартан изопроксил не показывал заметных электростатических явлений.
Пример 3
16,5 мл дихлорметана добавляли в колбу, содержащую 10 г кристаллов аллисартана изопроксила, и колбу нагревали при температуре дефлегмации до тех пор, пока раствор не становился прозрачным. После удаления растворителя посредством концентрирования раствора при относительном давлении -0,05 МПа и 40°С полученное твердое вещество сушили в вакууме при относительном давлении -0,09 МПа и 50°С до тех пор, пока его масса не стала постоянной, и затем охлаждали до комнатной температуры с получением аморфного аллисартана изопроксила. Спектр XRD показан на Фиг. 2, и ИФ-спектр показан на Фиг. 4. Полученный аморфный аллисартан изопроксил не показывал заметных электростатических явлений.
Пример 4
20 мл смешанного раствора дихлорметан/метанол (соотношение Vдихлорметан к Vметанол равно 100 к 10) добавляли в колбу, содержащую 10 г кристаллов аллисартана изопроксила, и колбу нагревали при температуре дефлегмации до тех пор, пока раствор не становился прозрачным. Затем получали твердое вещество посредством действий в соответствии с условиями Примера 2 так, чтобы получить кристаллы аллисартана изопроксила с точкой плавления 156-157°С.
Пример 5
Тонкоизмельченные и сыпучие кристаллические порошки (названные «кристаллом по патенту») были получены в соответствии со способом, раскрытым в патенте CN 200710094131.0, и они показали заметные электростатические явления после сушки. Порошки Примеров 1 и 3 распыляли и затем просеивали через сито с размером ячеек 100-меш для получения порошков с размером частиц, аналогичным кристаллическому порошку. Затем детектировали углы естественного откоса порошков, соответственно, с использованием метода с фиксированной воронкой; и объемные плотности порошков детектировали соответственно с использованием измерения в градуированном цилиндре (Method I of Bulk Density, раскрытый в Ph. Eur (Европейской фармакопее)), и результаты показаны в таблице ниже:

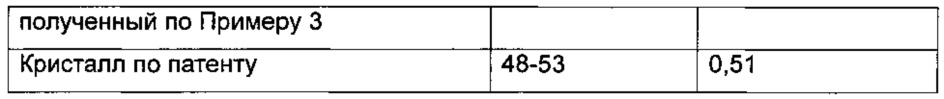
Из представленных выше данных можно видеть, что в сравнении с кристаллами, полученными согласно патенту CN 200710094131.0, аморфный аллисартан изопроксил, полученный согласно настоящему изобретению, показывал меньший угол естественного откоса и более высокую объемную плотность, и, таким образом, аморфный аллисартан изопроксил, предлагаемый настоящим изобретением, показывал лучшую текучесть.
Пример 6
Фармацевтическую композицию получали с использованием аморфного аллисартана изопроксила, полученного согласно способу Примера 1 в виде нерасфасованной лекарственной формы, и затем изготавливали в виде таблеток с ингредиентами, как изложено ниже:
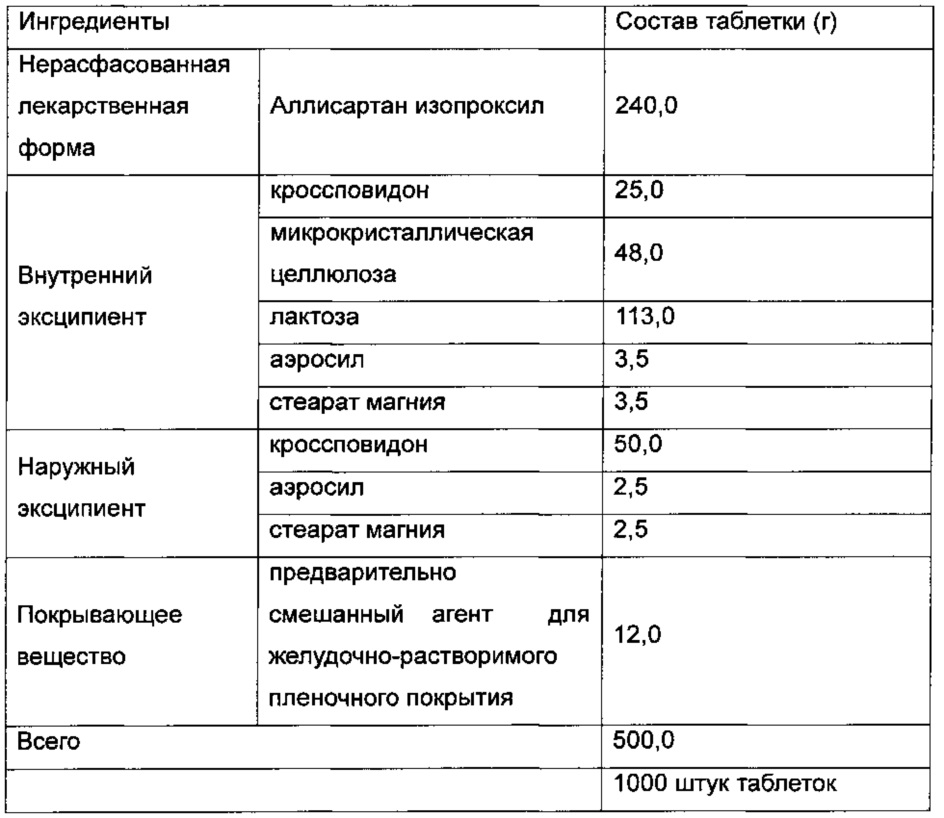
Смешивание нерасфасованной лекарственной формы и внутренних эксципиентов равномерно, в последовательности согласно перечисленным выше количественным соотношениям, затем гранулирование посредством способа сухого гранулирования с получением гранул внутренней фазы; добавление и смешивание наружных эксципиентов последовательно, согласно перечисленным выше количественным соотношениям, с получением фармацевтической композиции; прессование полученной фармацевтической композиции и нанесение покрытия на полученные таблетки.
При детекции полученных в результате таблеток полученный спектр XRD представлял собой такой, как показано на Фиг. 5, что показывает, что активный ингредиент по-прежнему существует в таблетках в виде аморфной формы. После хранения в условиях 40°C/75%RH в течение 6 месяцев обнаружили посредством XRD, что активный ингредиент существует в той же самой аморфной форме по существу с постоянным содержанием.
Подобным образом изготовили фармацевтическую композицию, используя аморфный аллисартан изопроксил, полученный согласно способу Примера 3 в виде нерасфасованной лекарственной формы, и затем изготовили в виде таблеток, в которых содержащийся активный ингредиент показал стабильность, согласующуюся со стабильностью вышеупомянутых таблеток.
Вышеприведенные примеры являются предпочтительными осуществлениями настоящего изобретения, хотя осуществление настоящего изобретения не ограничивается ими. Любое другое изменение, модификация, замена, комбинация или упрощение без отклонения от сущности и принципа настоящего изобретения считаются эквивалентными способами, которые входят в охраняемый объем настоящего изобретения.