Результат интеллектуальной деятельности: ПРОТИВООПУХОЛЕВЫЙ АГЕНТ, ВКЛЮЧАЮЩИЙ ГИДРАТ ГИДРОХЛОРИДА ИРИНОТЕКАНА
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001]
Настоящее изобретение относится к противоопухолевому средству, в котором использована комбинация лекарственных средств трифлуридин/типирацила гидрохлорид в комбинации с гидратом гидрохлорида иринотекана, и к усилителю противоопухолевого эффекта гидрата гидрохлорида иринотекана.
ИЗВЕСТНЫЙ УРОВЕНЬ ТЕХНИКИ
[0002]
Трифлуридин (называемый также: α,α,α-трифторотимидином. Здесь и далее именуемый также как “FTD”) проявляет противоопухолевый эффект, связанный с ингибированием образования тимидилата и с ингибированием синтеза ДНК путем включения его в ДНК. С другой стороны, типирацилгидрохлорид (химическое наименование: 5-хлор-6-[(2-иминопирролидин-1-ил)метил]пиримидин-2,4(1H,3H)диона гидрохлорид. Здесь и далее именуемый также как “TPI”) вызывает ингибирование тимидинфосфорилазы. Известно, что противоопухолевый эффект FTD усиливается за счет подавления TPI разложения FTD in vivo, вызываемого тимидинфосфорилазой (патентная литература 1). В настоящее время противоопухолевое средство, содержащее FTD и TPI в молярном отношении 1:0,5 (здесь и далее именуемый как “комбинированное лекарственное средство FTD/TPI”) находится в разработке как терапевтическое средство для лечения солидного рака, например рака толстой и прямой кишки (непатентная литература 1 и 2).
[0003]
Далее, гидрат гидрохлорида иринотекана (здесь и далее, также именуемый как “CPT-11”) представляет собой производное камптотецина, активным метаболитом которого является SN-38, и который подавляет синтез и транскрипцию ДНК путем ингибирования топоизомеразы I, и тем самым, проявляет противоопухолевый эффект. CPT-11 клинически используют в качестве терапевтического средства для лечения широкого круга типов раков, включая, например, мелкоклеточный рак легких, немелкоклеточный рак легких, рак шейки матки, рак яичников, рак желудка, рак толстой и прямой кишки, рак груди, карциному сквамозных клеток и злокачественную лимфому (непатентная литература 3).
Далее, если FTD и SN-38 воздействуют на клеточную линию рака толстой и прямой кишки, наблюдается синергическая цитотоксичность, и таким образом, ожидалась комбинированная терапия с использованием комбинации FTD/TPI лекарственных средств и CPT-11 (непатентная литература 4).
Список цитирования
Патентная литература
[0004]
Патентная литература 1: WO 96/30346
Непатентная литература
[0005]
Непатентная литература 1: Invest New Drugs 26 (5): 445-54, 2008.
Непатентная литература 2: Lancet Oncol. 13 (10): 993-1001, 2012.
Непатентная литература 3: Oncologist. 6(1): 66-80, 2001.
Непатентная литература 4: Eur J Cancer. 43(1): 175-83, 2007.
Сущность изобретения
Техническая проблема
[0006]
Целью настоящего изобретения является создание новой комбинационной терапии для лечения солидных раков, с использованием комбинированного лекарственного средства FTD/TPI, которое проявляет заметные противоопухолевые эффекты, и имеет мало побочных эффектов.
Решение проблемы
[0007]
С учетом сложившейся ситуации, если комбинационную терапию, включающая повторяющийся 28-дневный цикл, состоящий из двукратного 5-дневного введения FTD/TPI комбинированного лекарственного средства с 2-дневным отдыхом, с последующим отдыхом от введения в течение 2 недель, и введением CPT-11 один раз в 2 недели, осуществляют для пациента с раком толстой и прямой кишки на основе схемы введения, в которой эффекты каждого из лекарственных средств были ранее указаны в сравнительном примере, который будет раскрыт далее, только около 30% определенного ранее количества CPT-11 можно вводить из-за возникновения сильных побочных эффектов. Так как противоопухолевый эффект обычно пропорционален полной дозе, авторы настоящего изобретения провели исследования схемы введения, которая могла бы подавить возникновение таких побочных эффектов, и при которой можно было бы вводить заранее определенное количество. В результате авторы настоящего изобретения обнаружили, что комбинированная терапия, включающая схему повторного введения одного цикла, в котором, за период в 14 дней комбинированное лекарственное средство FTD/TPI вводят пациенту с солидным раком (в частности пациенту с раком толстой и прямой кишки) в течение 5 дней, с последующим отдыхом от введения в течение 9 дней, и CPT-11 вводят один раз в 2 недели, может подавить возникновение побочных эффектов, например, нейтропению, диарею и потерю массы, обеспечивает возможность введения заранее определенного количества, и проявляет превосходные противоопухолевые эффекты.
[0008]
Таким образом, в настоящем изобретении предложены следующие изобретения [1]-[26].
[0009]
[1] Противоопухолевое средство для лечения солидных раков, где один цикл схемы введения, в котором, за период в 14 дней комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[2] Противоопухолевое средство по п. [1], где комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 40 до 70 мг/м2/день, используя уменьшенное количество трифлуридина.
[3] Противоопухолевое средство по любому одному из пп. [1] или [2], где гидрат гидрохлорида иринотекана вводят в дозе от 100 до 180 мг/м2/день.
[4] Противоопухолевое средство по любому одному из пп. с [1] до [3], где указанный твердый рак представляет собой рак толстой и прямой кишки, рак легких, рак груди, рак поджелудочной железы или рак желудка.
[5] Усилитель противоопухолевого эффекта, включающий комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для усиления противоопухолевого эффекта гидрата гидрохлорида иринотекана у пациента с солидным раком, где один цикл схемы введения, в котором за период в 14 дней, комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[6] Противоопухолевое средство, включающее комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для лечения пациента с солидным раком, которому вводят гидрат гидрохлорида иринотекана, где один цикл схемы введения, в котором за период в 14 дней, комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[7] Набор препаратов, включающий противоопухолевое средство, содержащий комбинированное лекарственное средство трифлуридина и типирацилгидрохлорида в молярном отношении 1:0,5, и инструкцию по применению, где в инструкции по применению описан один цикл схемы введения пациенту с солидным раком, в котором за период в 14 дней, комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1.
[8] Комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для лечения твердого рака, где один цикл схемы введения, в котором за период в 14 дней, комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[9] Комбинированное лекарственное средство по п. [8], где комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 40 до 70 мг/м2/день, используя уменьшенное количество трифлуридина.
[10] Комбинированное лекарственное средство по любому одному из пп. [8] или [9], где гидрат гидрохлорида иринотекана вводят в дозе от 100 до 180 мг/м2/день.
[11] Комбинированное лекарственное средство по любому одному из пп. с [8] до [10], где солидный рак представляет собой рак толстой и прямой кишки, рак легких, рак груди, рак поджелудочной железы или рак желудка.
[12] Комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для усиления противоопухолевого эффекта гидрата гидрохлорида иринотекана у пациента с солидным раком, где один цикл схемы введения, в котором за период в 14 дней, указанное комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[13] Комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для лечения пациента с солидным раком, которому вводят гидрат гидрохлорида иринотекана, где один цикл схемы введения, в котором за период в 14 дней, комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[14] Применение комбинированного лекарственного средства, включающего трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для изготовления противоопухолевого средства против солидных раков, где один цикл схемы введения, в котором за период в 14 дней, указанное комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[15] Применение по п. [14], где комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 40 до 70 мг/м2/день, используя уменьшенное количество трифлуридина.
[16] Применение по любому одному из пп. [14] или [15], где гидрат гидрохлорида иринотекана вводят в дозе от 100 до 180 мг/м2/день.
[17] Применение по любому одному из пп. с [14] по [16], где солидный рак представляет собой рак толстой и прямой кишки, рак легких, рак груди, рак поджелудочной железы или рак желудка.
[18] Применение для изготовления усилителя противоопухолевого эффекта, включающего комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для усиления противоопухолевого эффекта гидрата гидрохлорида иринотекана у пациента с солидным раком, где один цикл схемы введения, в котором за период в 14 дней, указанное комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[19] Применение для изготовления противоопухолевого средства, включающего комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, для лечения пациента с солидным раком, который получает гидрат гидрохлорида иринотекана, где один цикл схемы введения, в котором за период в 14 дней, указанное комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1, повторяют один или два или большее количество раз.
[20] Терапевтический способ лечения солидных раков, включающий повторение одного цикла схемы введения пациенту с солидным раком один или два или большее количество раз, где за период в 14 дней, комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1.
[21] Способ по п. [20], где комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 40 до 70 мг/м2/день, используя уменьшенное количество трифлуридина.
[22] Способ по любому из пп. [20] или [21], где гидрат гидрохлорида иринотекана вводят в дозе от 100 до 180 мг/м2/день.
[23] Способ по любому одному из пп. с [20] до [22], где солидный рак представляет собой рак толстой и прямой кишки, рак легких, рак груди, рак поджелудочной железы или рак желудка.
[24] Способ усиления противоопухолевого эффекта гидрата гидрохлорида иринотекана у пациента с солидным раком, включающий повторение одного цикла схемы введения один или два или большее количество раз, где за период в 14 дней, комбинированное лекарственное средство, содержащее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1.
[25] Способ лечения пациента с солидным раком, которому вводят гидрат гидрохлорида иринотекана, включающий введение комбинированного лекарственного средства, содержащего трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, в дозе от 20 до 80 мг/м2/день, используя уменьшенное количество трифлуридина в дни с 1 по 5, и повторение одного цикла схемы введения один или два или большее количество раз, где за период в 14 дней, гидрат гидрохлорида иринотекана вводят в дозе от 50 до 200 мг/м2/день в день 1.
[26] Противоопухолевый агент для лечения солидных раков, где один цикл схемы введения, в котором за период в 14 дней, комбинированное лекарственное средство, включающее трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, вводят в дни с 1 по 5, в рекомендованной в монотерапии дозе для комбинированного лекарственного средства, включающего трифлуридин и типирацилгидрохлорид в молярном отношении 1:0,5, и гидрат гидрохлорида иринотекана вводят в день 1, в рекомендованной в монотерапии дозе для гидрата гидрохлорида иринотекана, повторяют один или два или большее количество раз.
Благоприятные эффекты настоящего изобретения
[0010]
В соответствии с противоопухолевым агентом настоящего изобретения, возможно проводить лечение рака, демонстрируя высокий противоопухолевый эффект, при этом подавляя возникновение побочных эффектов, тем самым, обеспечивая длительное выживание пациентов.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0011]
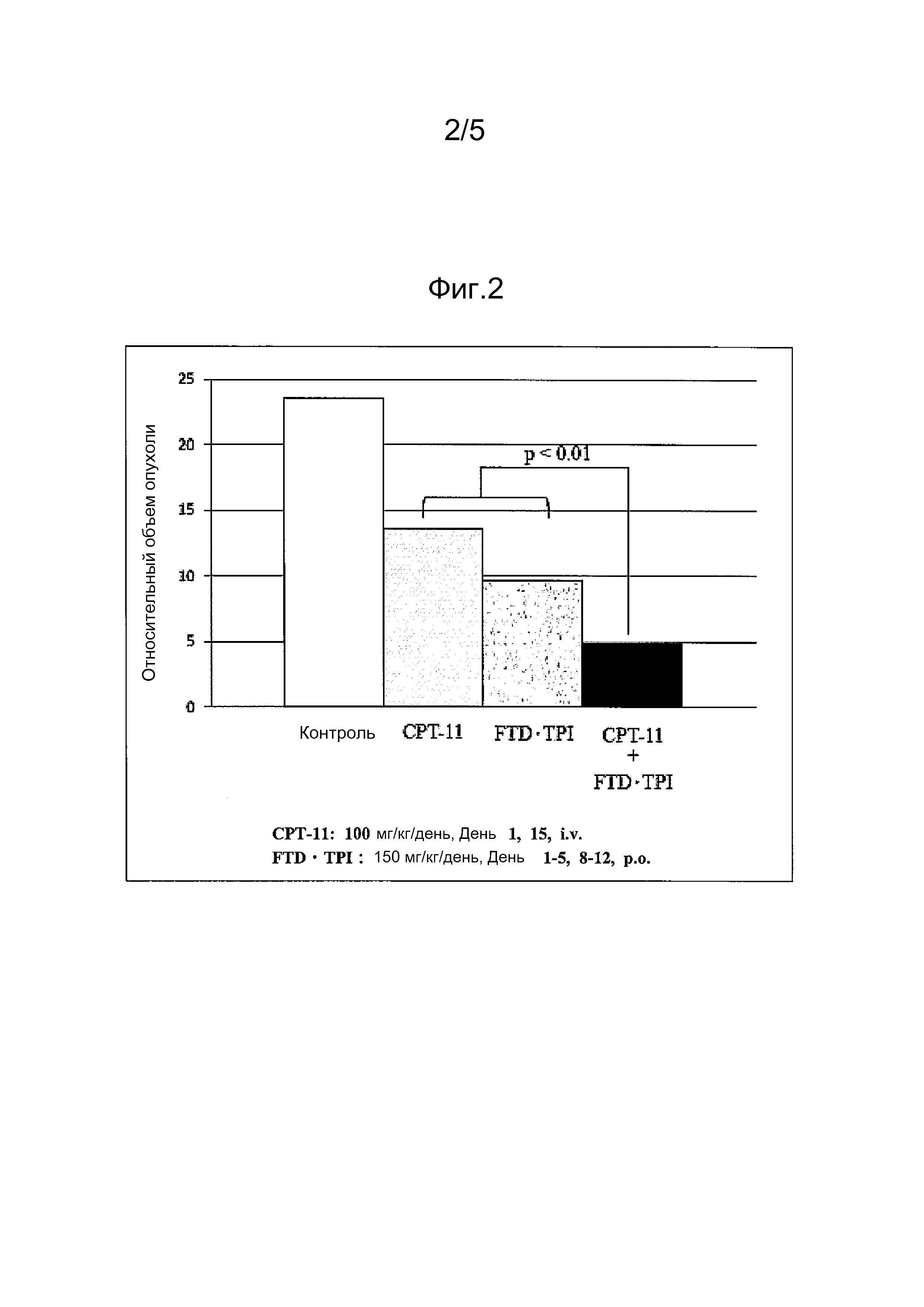
ФИГ. 1 представляет собой диаграмму, иллюстрирующую схемы введения схемы (1) и (2). Зачерненный кружок обозначает день введения.
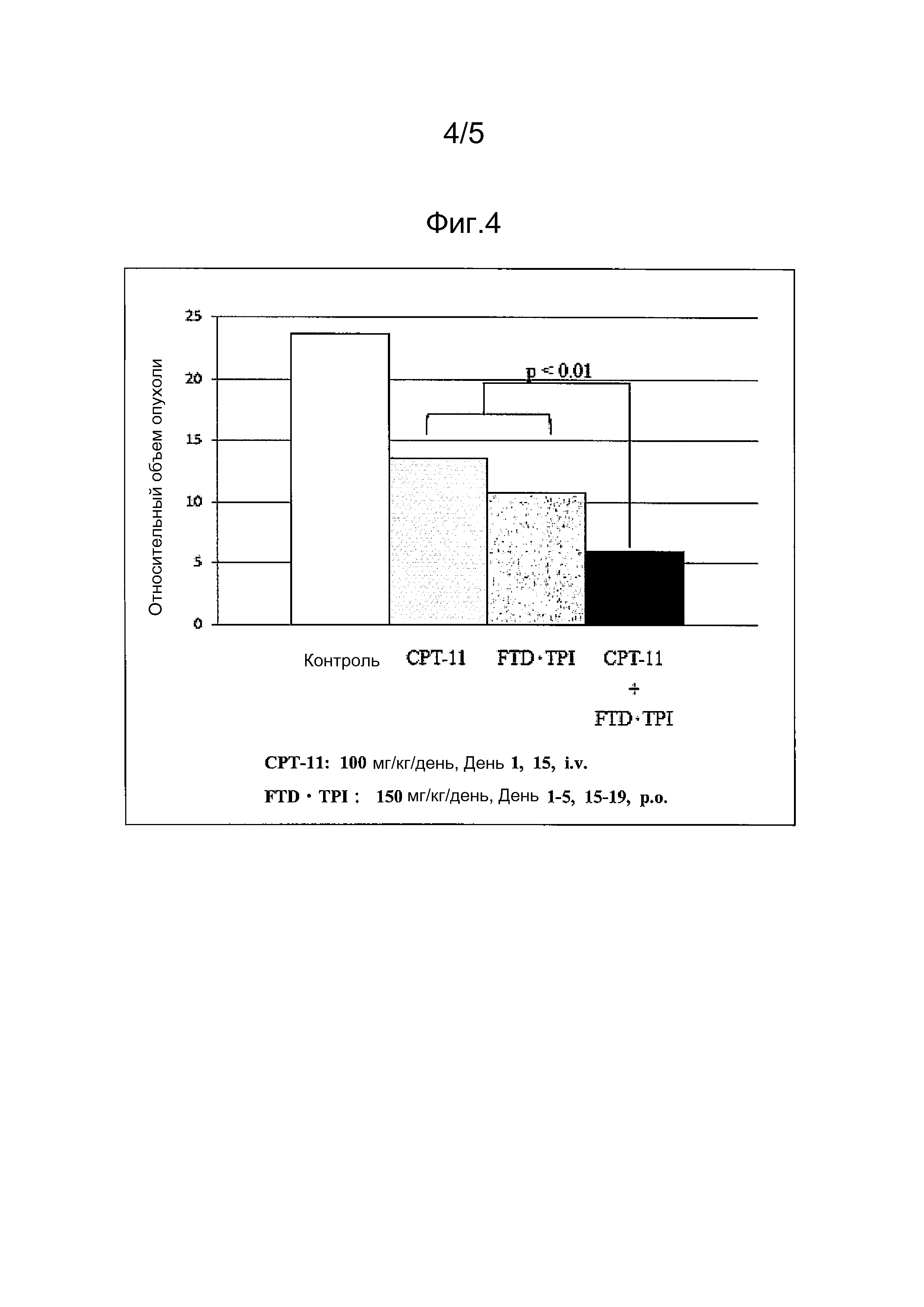
ФИГ. 2 представляет собой график, иллюстрирующий противоопухолевый эффект в соответствии со схемой введения (1).
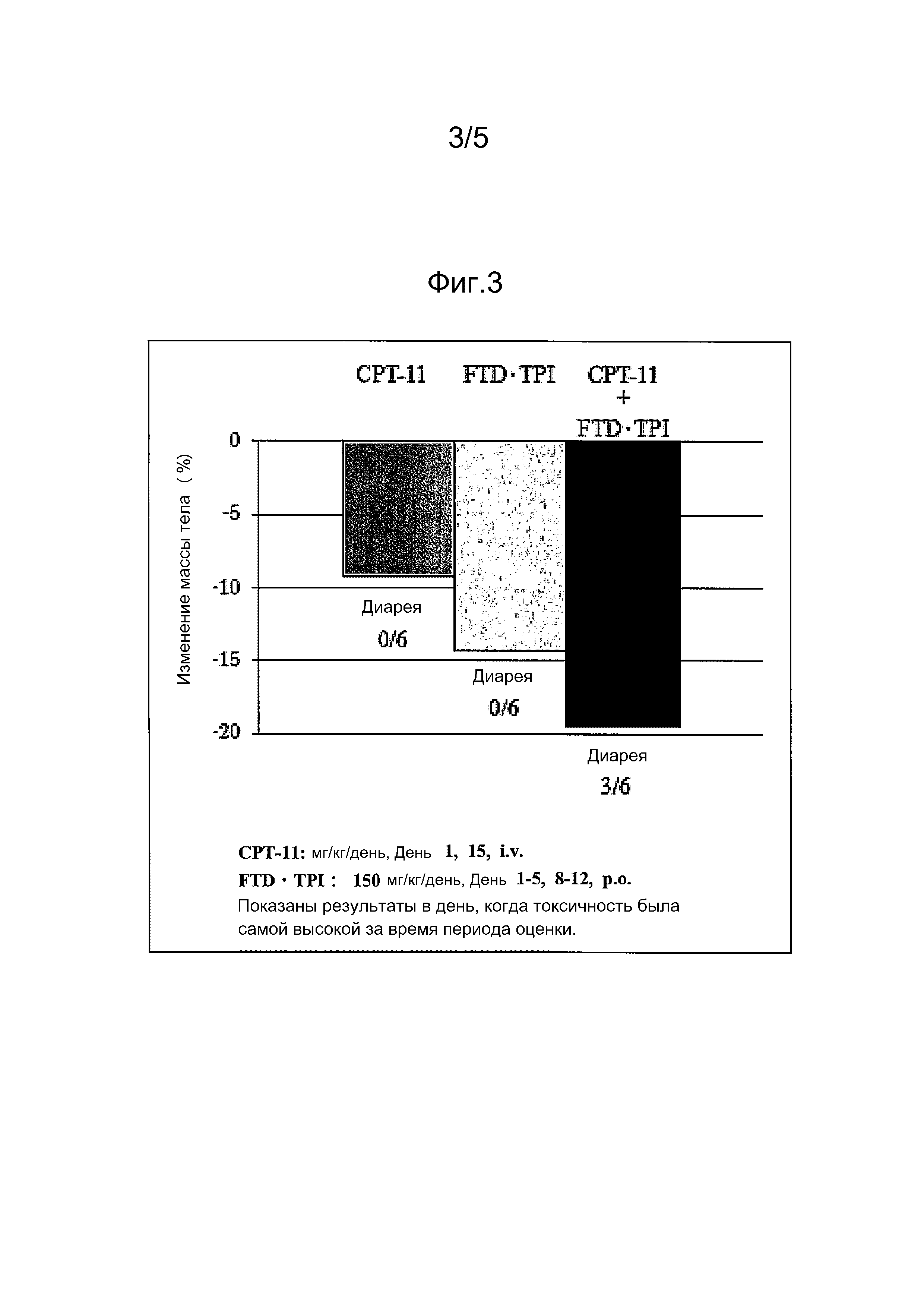
ФИГ. 3 представляет собой график, иллюстрирующий изменение массы тела и случаи диареи в соответствии со схемой введения (1).
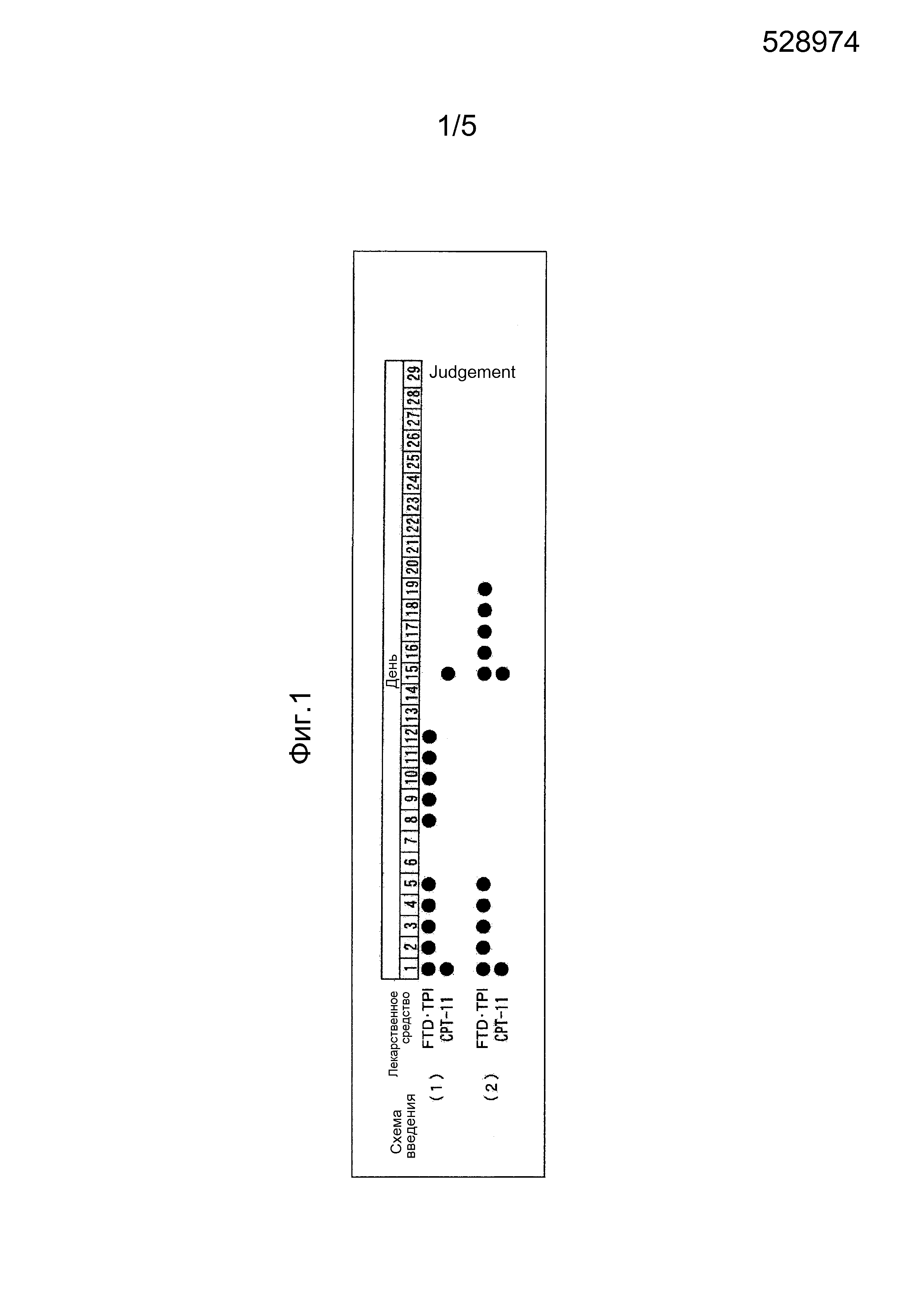
ФИГ. 4 представляет собой график, иллюстрирующий противоопухолевый эффект в соответствии со схемой введения (2).
ФИГ. 5 представляет собой график, иллюстрирующий изменения массы тела и случаи диареи в соответствии со схемой введения (2).
Описание предпочтительного варианта воплощения настоящего изобретения
[0012]
FTD и TPI настоящего изобретения оба представляют собой известные соединения, и их можно синтезировать, например, способом, раскрытым в WO 96/30346. Комбинированное лекарственное средство, содержащее FTD и TPI в молярном отношении 1:0,5, также известно (непатентная литература 1 и 2).
CPT-11 настоящего изобретения представляет собой известное соединение, и его можно синтезировать способом, раскрытым в Японском патенте № 3004077. Также можно использовать коммерчески доступный продукт, например, CAMPTO (зарегистрированная торговая марка, Yakult Honsha Co., Ltd.).
[0013]
Противоопухолевый агент настоящего изобретения отличается тем, что один цикл схемы введения, в котором за период в 14 дней, комбинированное лекарственное средство, включающее FTD и TPI в молярном отношении 1:0,5, вводят в дни с 1 по 5, и гидрат гидрохлорида иринотекана вводят в день 1, повторяют один или два или большее количество раз.
Как показано в представленных далее сравнительном примере и в примерах, если рекомендованную в монотерапии дозу комбинированного лекарственного средства FTD/TPI для мышей и рекомендованную в монротерапии дозу CPT-11 для мышей вводят в комбинации мышам в соответствии со схемой введения, можно достичь превосходных противоопухолевых эффектов, также как и подавления побочных эффектов. Таким образом, очевидно, что доза комбинированного лекарственного средства FTD/TPI и CPT-11 для человека в соответствии со схемой введения настоящего изобретения, эквивалентна рекомендованной дозе комбинированного лекарственного средства FTD/TPI и CPT-11 для человека в монотерапии.
Другими словами, доза FTD в дни с 1 по 5, составляет от 20 до 80 мг/м2/день, и с точки зрения баланса между противоопухолевыми эффектами и побочными эффектами, более предпочтительна доза FTD от 40 до 70 мг/м2/день, особенно предпочтительно 70 мг/м2/день.
Доза CPT-11 в день 1, составляет от 50 до 200 мг/м2/день, при использовании уменьшенного количества гидрата гидрохлорида иринотекана, и с точки зрения баланса между противоопухолевыми эффектами и побочными эффектами, доза CPT-11 предпочтительно составляет от 100 до 180 мг/м2/день, более предпочтительно от 150 до 180 мг/м2/день, особенно предпочтительно 180 мг/м2/день.
[0014]
Мишенями противоопухолевого агента настоящего изобретения являются солидные опухоли, включая конкретно рак головы и шеи, рак желудочно-кишечного тракта (эзофагеальный рак, рак желудка, дуоденальный рак, рак печени, рак желчевыводящих путей (рак желчного пузыря/желчных протоков), рак поджелудочной железы, рак тонкого кишечника, рак толстого кишечника (рак толстой и прямой кишки, рак толстой кишки, ректальный рак) и т.д.), рак легких, рак груди, рак яичников, рак матки (рак шейки матки, эндометриальный рак), рак почки, рак мочевого пузыря, рак простаты и т.д. Из них, с точки зрения противоопухолевых эффектов и побочных эффектов, мишенью противоопухолевого агента настоящего изобретения предпочтителен желудочно-кишечный рак, рак легких, или рак груди, более предпочтителен рак толстой и прямой кишки, рак поджелудочной железы рак желудка, рак легких, или рак груди, более предпочтителен рак толстой и прямой кишки и рак желудка, и особенно предпочтителен рак толстой и прямой кишки. Итак, твердый рак включает не только первичные опухоли, но также опухоли, причиной которых является солидный рак, который метастазирует в другие органы (такие как печень). Также, противоопухолевый агент настоящего изобретения может быть агентом, который используют для постоперационной вспомогательной химиотерапии, которую проводят для предотвращения рецидивов после хирургического удаления опухоли.
[0015]
Так как схема введения отличается для каждого активного ингредиента, все активные ингредиенты нельзя приготовить в одной дозовой форме. Так, противоопухолевый агент настоящего изобретения отдельно приготавливают во множестве дозовых форм для каждого активного ингредиента. Предпочтительно, чтобы FTD и TPI приготавливали как комбинированное лекарственное средство и CPT-11 приготавливали как отдельный агент.
[0016]
Кроме того, если каждый активный ингредиент вводят в соответствии со схемой введения настоящего изобретения, каждый препарат можно изготавливать и продавать вместе в единой упаковке, подходящей для комбинированного введения, или каждый препарат можно изготавливать и продавать после расфасовки в отдельные упаковки.
[0017]
Не существует конкретных ограничений относительно дозовых форм противоопухолевого агента настоящего изобретения, и их можно соответствующим образом выбрать в зависимости от терапевтических целей и они включают конкретные формы пероральных препаратов (таблетки, таблетки с покрытием, порошки, гранулы, капсулы, растворы, и т.д.), растворы для инъекций, суппозитории, пластыри, мази и т.д. Пероральные препараты предпочтительны для комбинированного лекарственного средства, включающего FTD и TPI, и препараты для инъекций предпочтительны для CPT-11.
[0018]
В зависимости от дозовой формы, противоопухолевый агент настоящего изобретения обычно можно приготовить обычными способами, используя фармацевтически приемлемый носитель. Такие носители включают различные носители, которые обычно используют для лекарственных средств, такие, как эксципиенты, связующие, разрыхлители, смазывающие вещества, разбавители, солюбилизаторы, суспендирующие вещества, изотонические вещества, вещества, регулирующие рН, буферные вещества, стабилизаторы, красители, вкусовые вещества и отдушки.
[0019]
Настоящее изобретение также относится к усилителям противоопухолевого эффекта, включающим комбинированное лекарственное средство, содержащее FTD/TPI, для усиления противоопухолевого эффекта CPT-11 у пациента с солидным раком (особенно у пациента с раком толстой и прямой кишки), где комбинированное лекарственное средство FTD/TPI и CPT-11 вводят, основываясь на раскрытой выше схеме введения. Усилитель противоопухолевого эффекта имеет дозовую форму вышеуказанного противоопухолевого агента.
[0020]
Кроме того, настоящее изобретение относится к противоопухолевому агенту, включающему комбинированное лекарственное средство FTD/TPI для лечения рака у пациента (особенно у пациента с раком толстой и прямой кишки), которому вводят CPT-11, где комбинированное лекарственное средство FTD/TPI и CPT-11 вводят, основываясь на раскрытой выше схеме введения. Противоопухолевый агент имеет вышеуказанную дозовую форму.
[0021]
Далее, настоящее изобретение относится к набору препаратов, включающему комбинированное лекарственное средство FTD/TPI и инструкцию, в которой указано, что при использование комбинированного лекарственного средства FTD/TPI и CPT-11 их следует вводить, руководствуясь указанной схемой введения. Здесь “инструкция для использования” может быть любой, если только она описывает схему введения; однако, предпочтительна инструкция для использования, в которой рекомендуется схема введения, разрешенная законом.
Инструкция для использования включает специально включенный пакет, инструкцию, и т.д. Также, набор препаратов, включающий инструкцию для использования может быть таким, в котором инструкция для использования напечатана на, или прикреплена к упаковке набора препаратов, или может быть такой, в которой противоопухолевый агент вместе с инструкцией для использования заключен в упаковку набора препаратов.
ПРИМЕРЫ
[0022]
Далее настоящее изобретение разъясняется более подробно с помощью примеров.
[0023]
Сравнительный пример
Культивируемые клетки (1×107 клеток/мышь) человеческой клеточной линии рака прямой кишки (KM20C) внутрибрюшинно трансплантируют 5-6 недельным мышам штамма BALB/cA Jcl-nu, и мышей распределяют по группам таким образом, чтобы средняя масса тел каждой из групп оказалась одинаковой. Дату, когда осуществляют разделение на группы (n=10) принимают за день 0.
Приготавливают комбинированное лекарственное средство FTD/TPI (смесь FTD и TPI в молярном отношении 1:0,5) таким образом, чтобы получить 75, 100, 150, 300, и 450 мг/кг/день как FTD. Так как имеются сообщения о том, что смерть вызывает вливание гидрата гидрохлорида иринотекана (CPT-11: CAMPTO (зарегистрированная торговая марка), Yakult Honsha Co., Ltd.) в дозе 111 мг/кг/день (Kiso to Rinsho, (1990), Vol. 24, No. 14, 7-17), гидрат гидрохлорида иринотекана приготавливают таким образом, чтобы доза составляла 80 и 100 мг/кг/день. Начиная введение лекарственного средства с дня 3, 5-дневное ежедневное пероральное введение комбинированного лекарственного средства FTD/TPI с 2-дневными перерывами проводят в течение 6 недель, и CPT-11 вводят раз в неделю в хвостовую вену в течение 6 недель.
В качестве показателя противоопухолевого эффекта сравнивают количество выживших в каждой группе мышей и время выживания каждой группы. Результаты представлены в таблице 1.
[0024]
|
[0025]
Как следует из таблицы 1, так как в группе, которой вводили 100 мг/кг/день CPT-11 длительность выживания у мышей была выше, рекомендованная доза (RD) CPT-11 для мышей составляет 100 мг/кг/день. Так, доза в 100 мг/кг/день для мышей эквивалентна RD в 150-180 мг/м2/день для людей.
[0026]
Так как длительность выживания оказалась длительной в группе, которой вводили 150 мг/кг/день комбинированного лекарственного средства FTD/TPI, используя уменьшенное количество FTD, RD комбинированного лекарственного средства FTD/TPI для мышей составляет 150 мг/кг/день при использовании уменьшенного количества FTD. Таким образом, доза в 150 мг/кг/день (с использованием уменьшенного количества FTD) для мышей эквивалентна RD в 70 мг/м2/день для людей.
[0027]
Пример 1
Человеческие клеточные линии рака прямой кишки (KM20C) трансплантируют в правую грудь 5-6 недельных мышей штамма BALB/cA Jcl-nu. После трансплантации опухоли измеряют главную ось (мм) и меньшую ось (мм) опухоли, и рассчитывают объем опухоли (TV). Затем животных распределяют на группы, таким образом, чтобы, средний TV для каждой группы оказался одинаковым, и день распределения на группы (n=6) принимают за день 0.
Приготавливают комбинированное лекарственное средство FTD/TPI (смесь FTD и TPI в молярном отношении 1:0,5) таким образом, чтобы в нем было 150 мг/кг/день как FTD. Инъекцию гидрата гидрохлорида иринотекана (CPT-11: CAMPTO (зарегистрированная торговая марка) infusion, Yakult Honsha Co., Ltd.) приготавливают таким образом, чтобы получить 100 мг/кг/день, как гидрата гидрохлорида иринотекана. По схеме введения (1), комбинированное лекарственное средство FTD/TPI вводят перорально ежедневно в дни 1-5 и в дни 8-12, и CPT-11 вводят в хвостовую вену в дни 1 и 15. По схеме введения (2), комбинированное лекарственное средство FTD/TPI перорально вводят ежедневно в дни 1-5 и в дни 15-19, и CPT-11 вводят в хвостовую вену в дни 1 и 15. Комбинированное лекарственное средство FTD/TPI и CPT-11 группе монотерапии вводят в той же самой дозе, что и в соответствующей схеме как соответствующее лекарственное средство в соответствии со схемой введения группе комбинированной терапии (ФИГ. 1).
[0028]
Как показатель противоопухолевого эффекта, рассчитывают TV в день 29 в каждой группе и относительные объемы опухолей (RTV) в день 0 определяют, используя следующую формулу и сравнивая с RTV для необработанной группы (контроль). Оценочное суждение относительно комбинационных эффектов составляют как эффективное в случае, если средние RTV значения для объединенной группы, которую обрабатывали, были статистически значительно ниже (Welch's IUT, over all maximum p<0,05), чем mean RTV значения для группы с индивидуальной монотерапией. Результаты представлены на ФИГ. 2 и 4. Если p-значение равно 0,05 или меньше, видно, что статистически значимое различие наблюдается для группы с монотерапией.
[0029]
TV (мм3)=(длинная ось (короткая ось)2)/2
RTV=(TV в день 29)/(TV в день 0)
[0030]
Кроме того массу тела (BW) измеряют как показатель токсичности со временем, и среднее изменение массы тела [BWC (%)] в день n относительно массы тела в день 0 рассчитывают по следующее формуле (n указывает день, когда массу тела измеряют дважды в неделю и последний день измерений соответствует дню 29, который является последним оценочным днем), и диарею одновременно наблюдают у отдельных мышей за время периода тестирования. Полученные результаты представлены на ФИГ. 3 и 5.
[0031]
На основании результатов, представленных на ФИГ. 2-5, удалось выявить, что схема введения (2) резко снижает побочные эффекты, такие как потеря массы и диарея, сохраняя при этом противоопухолевые эффекты, по сравнению со схемой введения (1).
Пример 2
Тест на комбинированное введение комбинированного лекарственного средства FTD/TPI и CPT-11 осуществляют тем же способом, что и в примере 1, за исключением того, что клеточную линию заменяют на клеточную линию рака желудка cell line (SC-2). Комбинированное лекарственное средство FTD/TPI (смесь FTD и TPI в молярном отношении 1:0,5) приготавливают таким образом, чтобы доза составляла 75 и 150 мг/кг/день (рекомендуемая доза) как FTD, и CPT-11 приготавливают таким образом, чтобы доза составляла 100 мг/кг/день (рекомендуемая доза) как гидрат гидрохлорида иринотекана. Полученные результаты представлены в таблице 2.
[0032]
|
Как следует из таблицы 2, ее данные подтверждают тот факт, что противоопухолевый эффект против рака желудка также значительно усиливается при использовании схемы введения (2). Кроме того, потеря массы была в приемлемых пределах.