Результат интеллектуальной деятельности: Способ изготовления формолвакцины гидроокисьалюминиевой полиштаммной против стрептококковых заболеваний крупного рогатого скота
Вид РИД
Изобретение
Изобретение относится к биотехнологии и ветеринарной медицине и может быть использовано при промышленном производстве формолвакцины гидроокисьалюминиевой полиштаммной против стрептококковых заболеваний крупного рогатого скота. Вакцина содержит бактериальную массу штаммов Str.agalactiae 346, Str.zooepidemicus 2082, Ent.faecalis, смешанных в определенной концентрации. Вакцина обладает высокой иммуногенностью, обеспечивает надежную защиту взрослого крупного скота от стрептококковых заболеваний.
Выпускаемая в настоящее время коммерческая вакцина против энтерококковой инфекции телят, ягнят и поросят обладает невысокой эффективностью. Это объясняется тем, что указанная вакцина, содержащая антиген только из штаммов энтерококков серогруппы D, не предохраняет от стрептококков серологических групп В и С, которые наиболее часто являются этиологическим фактором заболевания коров.
Однако способ получения вакцины является лабораторным, малопроизводительным, трудоемким и непригодным для промышленного производства. Культивирование стрептококков осуществляется в мясо-пептонном бульоне с глюкозой в стеклянных баллонах в стационарных условиях. Длительность культивирования составляет 18-24 часа, накопление бакмассы не выше 4 млрд. м.т./мл. Способ культивирования - неуправляемый, в силу чего не позволяет получать стандартную полноценную в антигенном отношении культуру в больших количествах.
Известен способ изготовления вакцины, ассоциированной против стрептококкоза крупного рогатого скота [5].
Ближайшим аналогом заявленного изобретения является известный из документа US 2012128719 А1, 24.05.2012. Способ изготовления вакцины против заболеваний и инфекций, в том числе стрептококковых крупного рогатого скота. Вакцина может содержать несколько штаммов микроорганизмов, а также адъювант, например гидроокись алюминия. Способ изготовления вакцины включает культивирование в питательной среде микроорганизмов, Str. Agalactia, Str. Zooepidemicus, Ent. Faecalis, инактивацию микроорганизмов и добавление адъюванта, например гидроокиси алюминия [6]. Отличием заявленного в формуле изобретения от ближайшего аналога является то, что при изготовлении вакцины проводят: 1) раздельное культивирование микроорганизмов в ферментерах; 2) инактивацию формальдегидом при температуре 43-47°С в течение 3-5 суток, причем конечная концентрация формальдегида в культуре составляет 0,03-0,07%;3) смешивание инактивированных культур в равных объемах при исходных концентрациях 17,5-25,5 млрд.м.т./см3; 4) снижение окислительно-восстановительного потенциала культуральной жидкости до -200- -150 мВ; 5) до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 15-25% от насыщения кислородом воздуха; 6) рН культуральной жидкости регулируют на уровне 6,8-7,2; 7) дробную подачу глюкозы осуществляют дозами до концентрации 0,05-0,20%.
Способ изготовления гидроокисьалюминиевой вакцины, содержащей несколько штаммов бактерий против инфекционных заболеваний, в том числе вызванными стрептококками по известному документу (RU 2191598 С2. 27.10.2002) очевиден для свиней и нельзя гарантировать ее эффективность для вакцинации крупного рогатого скота, в том числе с тем набором штаммов, представленных в ее описании [1].
Задачей изобретения является повышение качества целевого продукта за счет увеличения резистентности организма животных к заболеванию стрептококковой этиологии. Заявляемая вакцина для крупного рогатого скота обладает высокой профилактической эффективностью.
Технический результат изобретения достигается в способе изготовления вакцины против стрептококковых заболеваний крупного рогатого скота путем включения в состав заявляемой вакцины в качестве микроорганизмов бактериальную массу штаммов Str. agalactiae 346 (серогруппа В), Str. zooepidemicus 2082 (серогруппа С), Ent. faecalis (серогруппа D), взятых в вакцине в равных объемах при исходных концентрациях микроорганизмов 17,5-25,5 млрд.м.т./см3, а раздельное культивирование культур штаммов стрептококков проводят в ферментерах при окислительно-восстановительном потенциале культуральной жидкости -200÷-150 мВ, после чего до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 15-25% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне 6,8-7,2, а дробную подачу глюкозы осуществляют дозами до концентрации 0,05-0,2% при лимитировании роста стрептококков глюкозой, инактивацию культур стрептококков проводят формальдегидом при температура 43-47°С в течение 3-5 суток, причем конечная концентрация формальдегида в культуре составляет 0,03-0,07%.
В патентной и научно-технической литературе не известны технические решения, содержащие режимы способа изготовления вакцины против стрептококковых заболеваний крупного рогатого скота аналогичное заявляемому, т.е. предложение соответствует критерию «новизны».
Все режимы способа осуществимы в промышленных условиях, направлены на решение реальной технической задачи, т.е. предложение «промышленно применимо».
Впервые предложен способ изготовления вакцины против стрептококковых заболеваний крупного рогатого скота, где повышается качество целевого продукта за счет увеличения резистентности организма крупного рогатого скота к заболеванию стрептококковой этиологиии; заявляемая вакцина для крупного рогатого скота обладает высокой профилактической эффективностью при определенных условиях, т.е. предложение соответствует критериям «новизна» и «изобретательский уровень».
Изобретение иллюстрируется на следующих примерах.
Целью заявляемого изобретения является создание высокоиммуногенной формолвакцины гидроокисьалюминиевой полиштаммной, обеспечивающей надежную защиту крупного рогатого скота от заболеваний стрептококковой этиологии.
Эта цель достигнута подбором и введением в состав вакцины неконкурирующих между собой антигенов производственных штаммов и оптимальным количественным их соотношением, осуществлением управляемого периодического процесса культивирования и щадящих режимов инактивации.
Способ осуществляется следующим образом.
В стерильный ферментер загружают жидкую питательную среду на основе перевара Хоттингера.
Питательную среду в ферментере засевают раздельно маточными культурами (Str.agalactiae 346, Str.zooepidemicus 2082, Ent.faecalis), выращенными в жидкой питательной среде аналогичного состава, культивируют при температуре (37±1)°С в течение 6-8 часов.
После засева ферментера окислительно-восстановительный потенциал культуральной жидкости снижают до (-150)÷(-200) мВ, после чего до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 15-25% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне 6,8-7,2 ед. рН, а дробную подачу глюкозы осуществляют дозами до концентрации 0,05-0,2% при лимитировании роста стрептококков глюкозой, характеризующемся резким повышением pO2 при неизменных расходе воздуха и оборотах мешалки и прекращением снижения рН культуральной жидкости. Выращивание стрептококков проводят в соответствии с патентом (1).
Полученные бактериальные массы производственных штаммов стрептококков с известной концентрацией бактерий перекачивают в отдельные заранее приготовленные стерильные реакторы (или стеклянные баллоны) и добавляют при постоянном перемешивании дробно формальдегид до его конечной концентрации 0,03-0,07%, доводят рН до 7,1-7,2 ед.рН добавлением 10%-ного раствора гидроокиси натрия, перемешивают 15-20 мин и выдерживают при температуре 43-47°С в течение 3-5 суток.
После проверки на стерильность и полноту инактивации к инактивированной формальдегидом культуре каждого штамма, содержащей известное количество микробных тел в 1 см3, добавляют 4%-ную взвесь гидрата окиси алюминия рН (7,2±0,1) из расчета 130 см3 на каждый 1 дм3 культуры, перемешивают 15-20 мин и выдерживают при температуре 43-47°С в течение 2 суток, ежедневно перемешивая 2-3 раза, а затем без перемешивания 2 суток. После отстоя адсорбированной на гидрате окиси алюминия культуры проводят декантирование прозрачной надосадочной жидкости с таким расчетом, чтобы получить в осадке концентрацию микробных тел (17,5-25,5)⋅109 м.т./см3.
Культуры стрептококков после инактивации и адсорбции на гидрате окиси алюминия подают в оснащенный перемешивающим устройством реактор-смеситель и смешивают в равных объемах.
Бактериальную массу из штаммов Str. agalactiae 346 серогруппы В, Str. zooepidemicus 20 серогруппы С, Ent.faecalis серогруппы D тщательно перемешивают и с соблюдением условий асептики при постоянном перемешивании расфасовывают в стерильную стеклотару.
Пример 1. Способ изготовления вакцины с минимальными значениями параметров
Для культивирования стрептококков используют жидкую питательную среду на основе перевара Хоттингера. Среду засевают культурой стрептококков, выращенной в жидкой питательной среде аналогичного состава. Культивируют при (37±1)°С в течение 6-8 ч. После засева ферментера окислительно-восстановительный потенциал культуральной жидкости снижают до (-200) мВ путем выдержки культуры без подачи воздуха, после чего до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 15% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне 6,8 ед.рН с помощью подачи 10%-ного раствора NaOH, а дробную подачу глюкозы осуществляют дозами до концентрации 0,05% при лимитировании роста стрептококков глюкозой, характеризующемся резким повышением pO2 при неизменных расходе воздуха и оборотах мешалки и прекращением снижения рН культуральной жидкости.
Процесс инактивации культур штаммов стрептококков проводят формальдегидом при температуре 43°С в течение 3 суток, причем конечная концентрация формальдегида в культуре составляет 0,03%. После инактивации, адсорбции культур на гидрате окиси алюминия и декантации надосадочной жидкости компоненты вакцины смешивают в равных объемах при следующих исходных концентрациях, млрд. м.т./см3:
|
Пример 2. Способ изготовления вакцины с оптимальными значениями параметров
Для культивирования стрептококков используют жидкую питательную среду на основе перевара Хоттингера.
Среду засевают культурой стрептококков, выращенной в жидкой питательной среде аналогичного состава. Культивируют при (37±1)°С в течение 6-8 ч. После засева ферментера окислительно-восстановительный потенциал культуральной жидкости снижают до (-175) мВ путем выдержки культуры без подачи воздуха, после чего до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 20% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне 7,0 ед. рН с помощью подачи 10%-ного раствора NaOH, а дробную подачу глюкозы осуществляют дозами до концентрации 0,125% при лимитировании роста стрептококков глюкозой, и характеризующимся резким повышением pO2 при неизменных расходе воздуха и оборотах мешалки и прекращением снижения рН культуральной жидкости.
Процесс инактивации штаммов стрептококков проводят формальдегидом при температуре 45,0°С в течение 4 суток, причем конечная концентрация формальдегида в культуре составляет 0,05%.
После инактивации, адсорбции культур на гидрате окиси алюминия и декантации надосадочной жидкости компоненты вакцины смешивают в равных объемах при следующих исходных концентрациях, млрд. м.т./см3:
|
Пример 3. Способ изготовления вакцины с максимальными значениями параметров
Для культивирования стрептококков используют жидкую питательную среду на основе перевара Хоттингера.
Среду засевают культурой стрептококков, выращенной в жидкой питательной среде аналогичного состава. Культивируют при (37±)1°С в течение 6-8 ч. После засева ферментера окислительно-восстановительный потенциал культуральной жидкости снижают до (-150) мВ путем выдержки культуры без подачи воздуха, после чего до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 25% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне 7,2 ед. рН с помощью подачи 10%-ного раствора NaOH, а дробную подачу глюкозы осуществляют дозами до концентрации 0,2% при лимитировании роста стрептококков глюкозой, характеризующимся резким повышением pO2 при неизменных расходе воздуха и оборотах мешалки и прекращением снижения рН культуральной жидкости.
Процесс инактивации штаммов стрептококков проводят формальдегидом при температуре 47°С в течение 5 суток, причем конечная концентрация формальдегида в культуре составляет 0,07%.
После инактивации, адсорбции культур на гидрате окиси алюминия и декантации надосадочной жидкости компоненты вакцины смешивают в равных объемах при следующих исходных концентрациях, млрд. м.т./см:
|
Пример 4. Способ изготовления вакцины с параметрами ниже минимальных значений
Для культивирования стрептококков используют жидкую питательную среду на основе перевара Хоттингера.
Среду засевают культурой стрептококков, выращенной в жидкой питательной среде аналогичного состава. Культивируют при (37±1)°С в течение 6-8 ч.
После засева ферментера окислительно-восстановительный потенциал культуральной жидкости снижают до (-225) мВ путем выдержки культуры без подачи воздуха, после чего до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 10% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне 6,6 ед. рН с помощью подачи 10%-ного раствора NaOH, а дробную подачу глюкозы не осуществляют.
Процесс инактивации штаммов стрептококков проводят формальдегидом при температуре 41,0°С в течение 2 суток, причем конечная концентрация формальдегида в культуре составляет 0,01%.
После инактивации, адсорбции культур на гидрате окиси алюминия и декантации надосадочной жидкости компоненты вакцины смешивают в равных объемах при следующих исходных концентрациях, млрд. м.т./см3:
|
Пример 5. Способ изготовления вакцины с параметрами выше максимальных значений
Для культивирования стрептококков используют жидкую питательную среду на основе перевара Хоттингера.
Среду засевают культурой стрептококков, выращенной в жидкой-питательной среде аналогичного состава. Культивируют при (37±1)°С в течение 6-8 ч.
После засева ферментера окислительно-восстановительный потенциал культуральной жидкости снижают до (-125) мВ путем выдержки культуры без подачи воздуха, после чего до окончания процесса культивирования поддерживают pO2 в культуральной жидкости на уровне 30% от насыщения кислородом воздуха, рН культуральной жидкости регулируют на уровне 7,4 ед. рН с помощью подачи 10%-ного раствора NaOH, а дробную подачу глюкозы осуществляют дозами до концентрации 0,275% при лимитировании роста стрептококков глюкозой, характеризующемся резким повышением pO2 при неизменных расходе воздуха и оборотах мешалки и прекращением снижения рН культуральной жидкости.
Процесс инактивации штаммов стрептококков проводят формальдегидом при температуре 49,0°С в течение 6 суток, причем конечная концентрация формальдегида в культуре составляет 0,09%.
После инактивации, адсорбции культур на гидрате окиси алюминия и декантации надосадочной жидкости компоненты вакцины смешивают в равных объемах при следующих исходных концентрациях, млрд. м.т./см3:
|
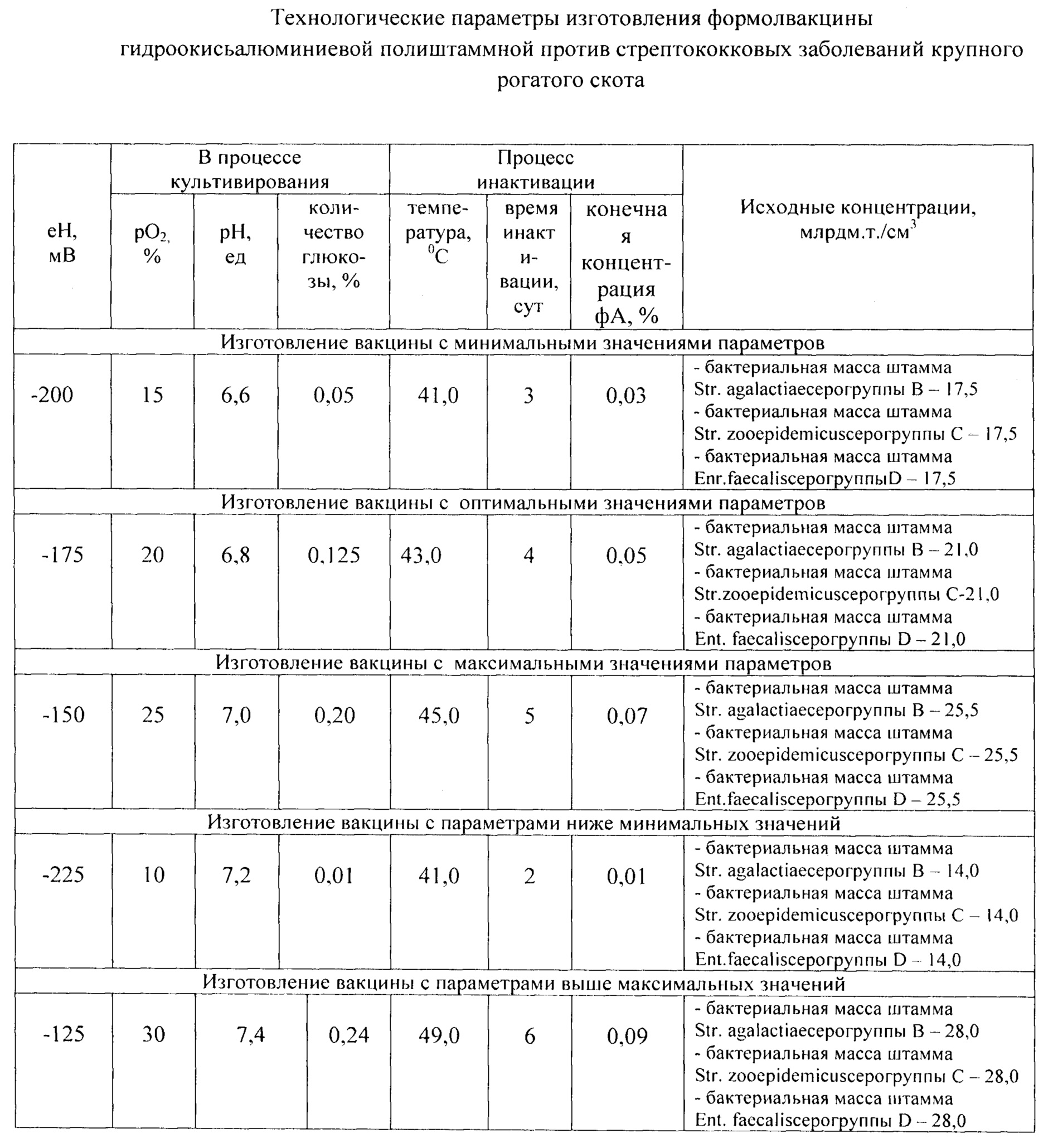
Технологические параметры изготовления формолвакцины гироокисьалюминиевой полиштаммной против стрептококковых заболеваний крупного рогатого скота, указанные в примерах, приведены в таблице.
Вакцина, приготовленная по примерам 1-3, обладает высокой иммуногенной активностью и соответствует требованиям технических условий, тогда как вакцина, приготовленная по примеру 4, не обладает достаточной иммунной активностью, а вакцина, приготовленная по примеру 5, обладает повышенной реактогенностью.
Источники информации
1. Патент РФ №2191598 С2 от 27 октября 2002 г. K 39/102 «Вакцина ассоциированная гидроокисьалюминиевая против инфекционных пневмоний свиней бактериальной этиологии и способ ее изготовления» (аналог).
2. Патент РФ №1566533 от 7 апреля 1993 г. А6 K 39/102 «Способ изготовления вакцины против пастереллеза птиц».
3. Патент РФ №2129016 от 20 апреля 1999 г. А61K 39/112 «Способ изготовления вакцины против сальмонеллеза сельскохозяйственных животных».
4. Титова М.Н. Усовершенствование лечебно-диагностических мероприятий при стрептококковом мастите коров // Автореферат диссертации кандидата ветеринарных наук. Новосибирск. 2013.
5. Патент РФ №2179861 от 27.02.2002 А61K 39/085. Вакцина ассоциированная против стрептококкоза крупного рогатого скота.
6. US 2012128719 А1, 24.05.2012 (прототип).