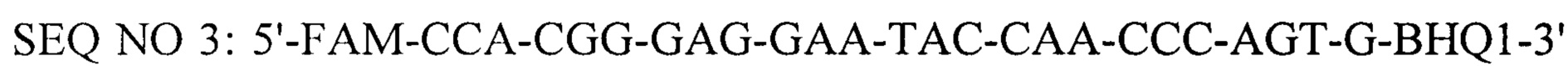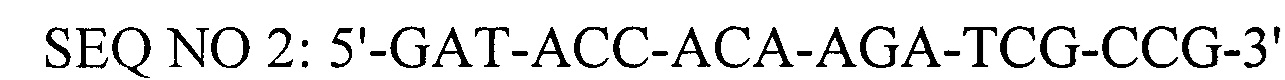Результат интеллектуальной деятельности: Тест-система для обнаружения ДНК вируса африканской чумы свиней с помощью полимеразной цепной реакции в режиме реального времени
Вид РИД
Изобретение
Изобретение относится к области ветеринарной вирусологии, в частности к тест-системе для обнаружения ДНК особо опасного возбудителя африканской чумы свиней (АЧС) в культуре инфицированных клеток и пробах патологических материалов от свиней, и может быть использовано при диагностике АЧС в научно-исследовательских учреждениях, региональных, областных ветеринарных лабораториях и на предприятиях биологической промышленности.
Известна тест-система (см. патент РФ №2360971, кл. C12Q 1/68, 2009 г.), включающая пластиковые флаконы и пробирки, термостабильный фермент Tag-полимеразу, ПЦР-смесь для постановки реакции со специфическими олигонуклеотидными праймерами, комплиментарными высококонсервативной области генома вируса АЧС района гена Р30, положительный и отрицательный контроли.
Также известна тест-система (см. патент РФ №2125089, кл. C12Q 1/68, 1999 г. - прототип), включающая пластиковые флаконы и пробирки, термостабильный фермент Tag-полимеразу, буфер для постановки реакции, смесь четырех дезоксинуклеотидтрифосфатов, положительный контроль - рекомбинантную плазмиду, содержащую фрагмент гена vp72 вируса африканской чумы свиней, синтетические олигонуклеотидные праймеры и зонд.
Недостатком прототипа является недостаточная степень специфичности и чувствительности тест-системы, а также длительность проведения диагностики, что не исключает вероятность технологических ошибок при лабораторных манипуляциях.
Техническим результатом является повышение степени специфичности и чувствительности тест-системы, а также сокращение времени проведения диагностики при снижении вероятности технологических ошибок во время лабораторных манипуляциях.
Технический результат достигается тем, что в тест-системе для обнаружения ДНК вируса африканской чумы свиней с помощью полимеразной цепной реакции в режиме реального времени, включающей пластиковые флаконы и пробирки, термостабильный фермент Tag-полимеразу, буфер для постановки реакции, смесь четырех дезоксинуклеотидтрифосфатов, положительный контроль - рекомбинантную плазмиду, содержащую фрагмент гена vp72 вируса африканской чумы свиней, синтетические олигонуклеотидные праймеры и зонд, согласно изобретению используют синтетические олигонуклеотидные праймеры и флуоресцирующий зонд, комплементарные консервативной области генома вируса африканской чумы свиней района гена vp72, имеющие следующий нуклеитидный состав:
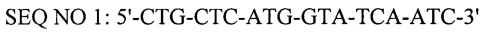 - прямой праймер,
- прямой праймер,
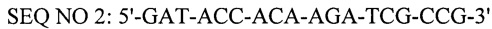 - обратный праймер,
- обратный праймер,
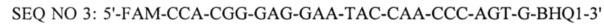 - флуоресцирующий зонд и взятые при соотношении 1:1:0,5, при этом BHQ1 - темновой гаситель флуоресценции присоединен к 3'-концевому нуклеотиду, а FAM - флуоресцентный краситель присоединен к нуклеотиду С, причем для постановка реакции используют 5-кратный буфер и в качестве отрицательного контроля используют дистиллированную воду.
- флуоресцирующий зонд и взятые при соотношении 1:1:0,5, при этом BHQ1 - темновой гаситель флуоресценции присоединен к 3'-концевому нуклеотиду, а FAM - флуоресцентный краситель присоединен к нуклеотиду С, причем для постановка реакции используют 5-кратный буфер и в качестве отрицательного контроля используют дистиллированную воду.
Существенными признаками, отличающими заявляемое техническое решение от прототипа, являются:
- нуклеотидные последовательности праймеров и зонда;
- формат амплификационной смеси;
- состав амплификационой смеси, в которой используют два внутренних контроля проведения полимеразной цепной реакции.
Новизна заявляемой тест-системы заключается в том, что она позволяет в биологических образцах, в качестве которых используют по выбору: плазму, сыворотку крови, мазки со слизистых от латентно инфицированных и больных животных; патологический материал от павших животных, в инфицированных культурах клеток, а также в продуктах свиноводства и изделиях свиного происхождения, выявлять специфическую последовательность консервативного участка генома вируса африканской чумы свиней без использования дополнительных методов детекции ампликонов, тем самым сокращая процент технологических ошибок. Формат и состав амплификационной смеси сокращает трудоемкость и продолжительность анализа, а также позволяют осуществлять эффективную наработку фрагментов нуклеиновой кислоты вируса африканской чумы свиней, содержащих выбранные функционально значимые консервативные локусы гена-мишени вируса.
Также тест-система отличается тем, что в ее составе используют синтетические олигонуклеотидные конструкции:
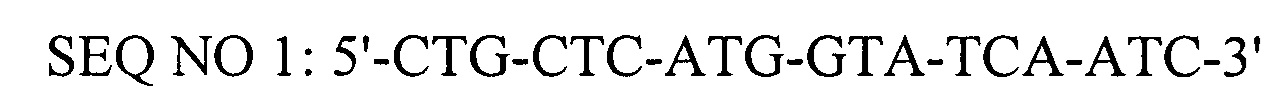 (прямой праймер),
(прямой праймер),
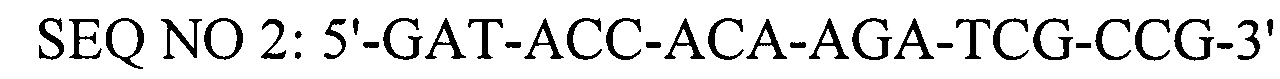 (обратный праймер),
(обратный праймер),
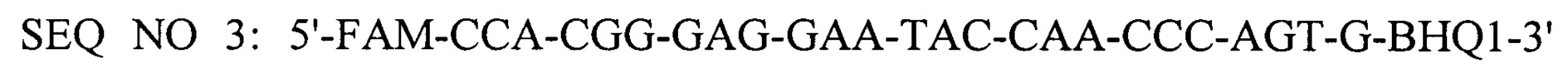 (флуоресцирующий зонд), где BHQ1 означает присоединенный к 3'-концевому нуклеотиду темновой гаситель флуоресценции, a FAM - флуоресцентный краситель FAM, присоединенный к нуклеотиду С.
(флуоресцирующий зонд), где BHQ1 означает присоединенный к 3'-концевому нуклеотиду темновой гаситель флуоресценции, a FAM - флуоресцентный краситель FAM, присоединенный к нуклеотиду С.
На основе синтетических олигонуклеотидных конструкций SEQ NO 1-3 готовят амплификационную смесь для проведения ПЦР в режиме реального времени; наличие в изучаемой пробе нуклеиновой кислоты искомого вируса определяют ростом сигнала флуоресценции красителя. Причем структура синтетических олигонуклеотидных конструкций обеспечивает связывание только с полностью комплементарными ДНК-мишенями, что обуславливает яркий флуоресцентный сигнал. Кроме того, физико-химические свойства олигонуклеотидных конструкций SEQ NO 1-3 препятствуют образованию между собой шпилек и дуплексов (высокоэнергетических внутренних структур), способствуют образованию необходимого количества продукта амплификации, а также подобраны с учетом одинаковой температуры отжига на ДНК-мишени (60-62°С). Для стабильной работы олигонуклеотидных конструкций в растворе тест-системы оптимизированы концентрация MgCl2 и самих конструкций, а также соотношение прямых, обратных праймеров и флуоресцентных зондов, количество циклов амплификации и их время на каждом этапе.
Сущность изобретения поясняется чертежом, где представлены графики из отчета работы прибора Rotor-Gene 6000 при использовании Real-time PCR:
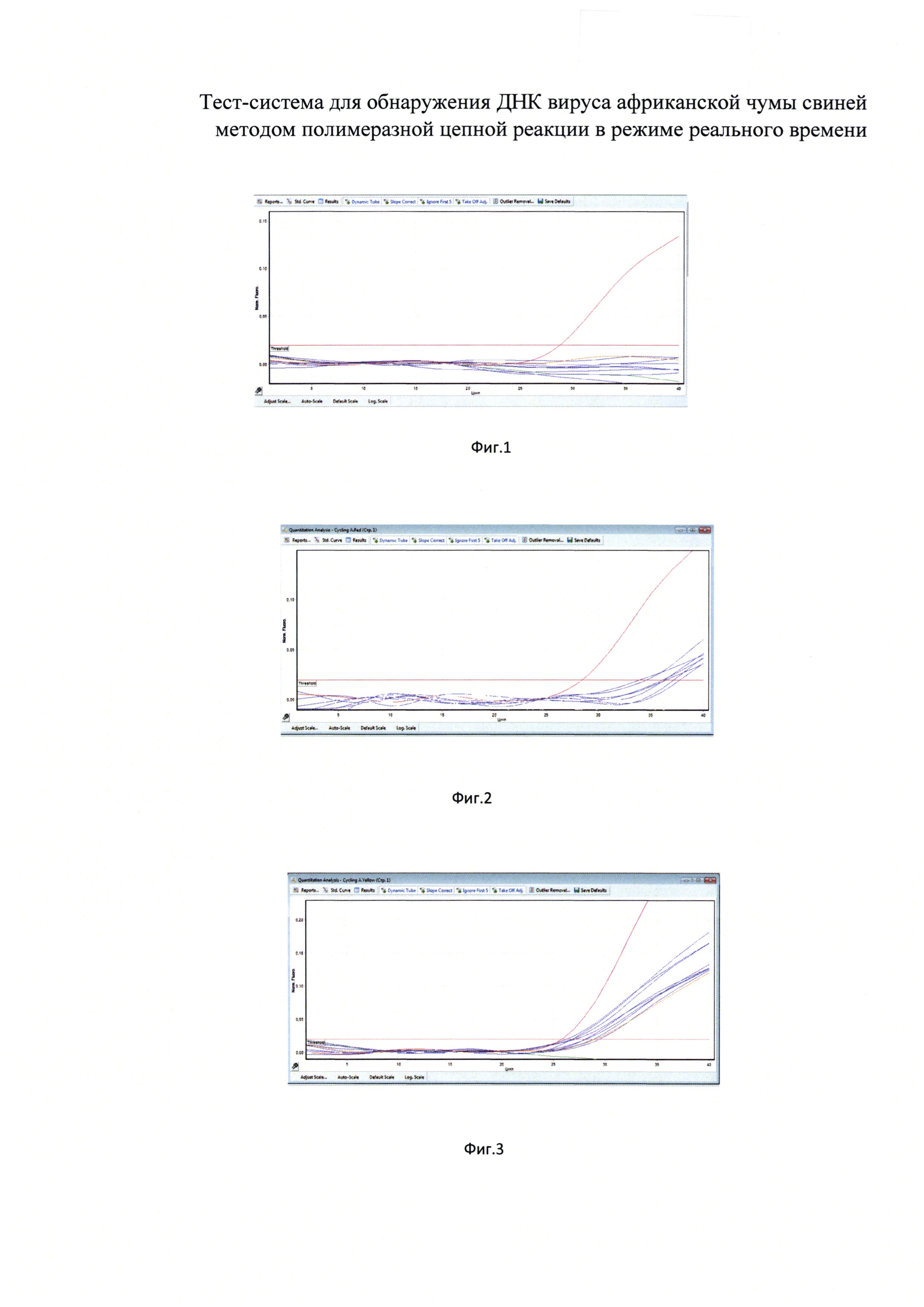
на фиг. 1 представлен график канала FAM - искомая ДНК АЧС для отрицательного образца;
на фиг. 2 представлен график канала Су5 - внутренний контрольный образец специфики - ДНК свиньи - отрицательный образец;
на фиг. 3 представлен график канала HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - отрицательный образец;
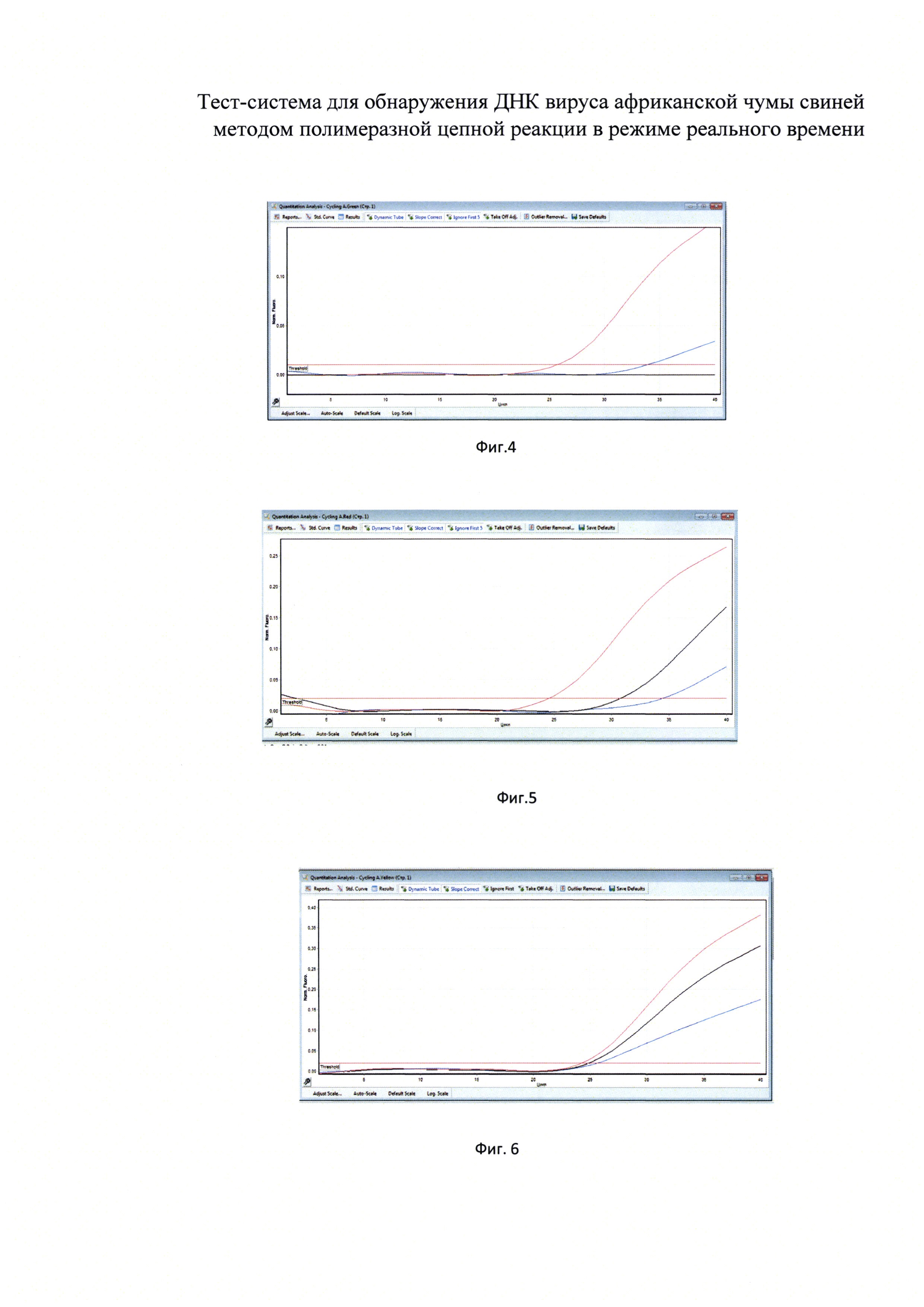
на фиг. 4 представлен график канала FAM - искомая ДНК АЧС для положительного образца;
на фиг. 5 представлен график канала Су5 - внутренний контрольный образец специфики - ДНК свиньи - положительный образец;
на фиг. 6 представлен график канала HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - положительный образец;
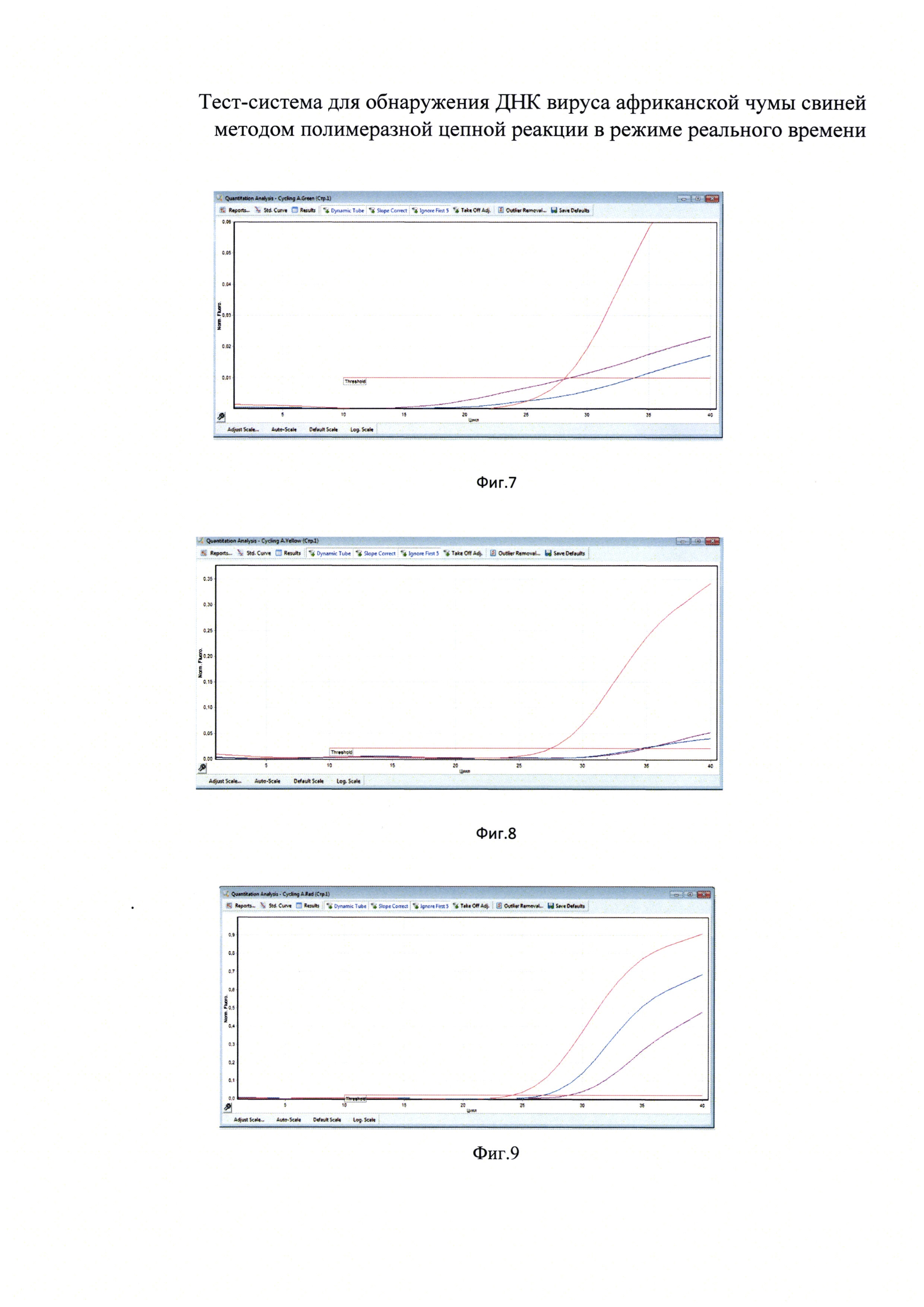
на фиг. 7 представлен график канала FAM - искомая ДНК АЧС для сомнительного образца;
на фиг. 8 представлен график канала Су5 - внутренний контрольный образец специфики - ДНК свиньи - сомнительный образец;
на фиг. 9 представлен график канала HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - сомнительный образец;
Сущность изобретения поясняется чертежом, где представлены графики из отчета работы прибора Rotor-Gene 6000 при использовании Real-time PCR:
на фиг. 1 представлен график канала FAM - искомая ДНК АЧС для отрицательного образца;
на фиг. 2 представлен график канала Су5 - внутренний контрольный образец специфики - ДНК свиньи - отрицательный образец;
на фиг. 3 представлен график канала HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - отрицательный образец;
на фиг. 4 представлен график канала FAM - искомая ДНК АЧС для положительного образца;
на фиг. 5 представлен график канала Су5 - внутренний контрольный образец специфики - ДНК свиньи - положительный образец;
на фиг. 6 представлен график канала HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - положительный образец;
на фиг. 7 представлен график канала FAM - искомая ДНК АЧС для сомнительного образца;
на фиг. 8 представлен график канала Су5 - внутренний контрольный образец специфики - ДНК свиньи - сомнительный образец;
на фиг. 9 представлен график канала HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - сомнительный образец;
Примеры конкретного использования тест-системы
Тест-система снабжена пластиковыми флаконами и пробирками, термостабильным ферментом Tag-полимеразой, 5-кратным буфером для постановки реакции, смесью четырех дезоксинуклеотидтрифосфатов, рекомбинантной плазмидой, содержащей фрагмент гена vp72 вируса африканской чумы свиней в качестве положительнго контроля, синтетическими олигонуклеотидными праймерами и зондом комплементарные консервативной области генома вируса африканской чумы свиней района гена vp72, имеющие следующий нуклеитидный состав:
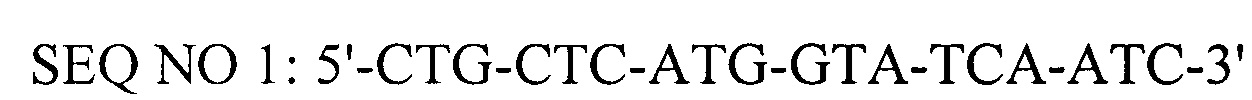 - прямой праймер,
- прямой праймер,
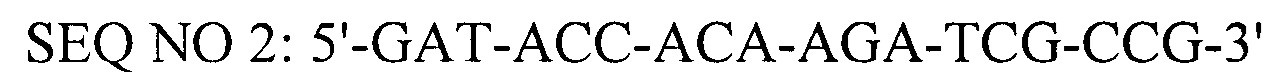 - обратный праймер,
- обратный праймер,
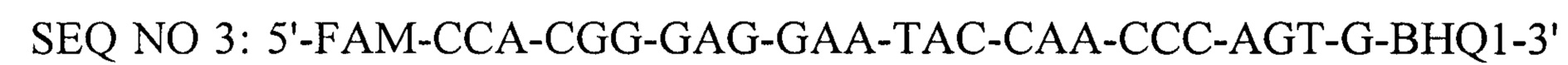 - флуоресцирующий зонд и взятые при соотношении 1:1:0,5 и отрицательным контролем в качестве которого используют дистиллированную воду.
- флуоресцирующий зонд и взятые при соотношении 1:1:0,5 и отрицательным контролем в качестве которого используют дистиллированную воду.
Пример 1. Проведение ПЦР анализа в формате «моноплексная ПЦР-РВ» для детекции вируса, выделенного из тканей свиней.
Для проведения ПЦР анализа проводили выделение вирусной ДНК из тканей селезенки свиньи. Выделение проводили по следующей методике с использованием коммерческого набора компании «ИДС» для экспресс-выделения «ДНК-экспресс».
Отбирают гомогенизат ткани селезенки и помещают его в пробирку на 1,5 мл с 300 мкл раствора «ДНК-экспресс». Добавляют в каждую пробирку по 10 мкл «ЭВК» (экзогенный внутренний контроль выделения, входит в состав коммерческого набора). Перемешивают на вортексе 5-10 сек. Осаждают капли с крышки пробирки коротким центрифугированием. Прогревают при 98°C в течение 15 минут. Центрифугируют 2 мин при максимальных оборотах (10-14,5 тыс.об/мин). Переносят надосадочную жидкость в чистую 1,5 мл пробирку. Перенесенную надосадочную жидкость используют для постановки ПЦР.
Для проведения самой ПЦР с использованием тест-системы требуется:
Подготовить необходимое количество пробирок с реакционной смесью, включая три пробирки для стандартных образцов ДНК и отрицательного контрольного образца. При конструировании праймеров и зонда основными требованиями являются: степень гомологии (комплементарность) с выбранным участком гена; отсутствие самокоплементарных участков внутри олигонуклеотидов и комплементарности друг другу, чтобы не допускать возникновения устойчивых вторичных структур (димеров); близость значений температуры отжига праймеров.
Разработанные олигонуклеотиды имеют оптимальные размер (24-25 пл.) и GC состав (45,8 и 48%), температуру отжига праймеров 55°C, температуру отжига зонда до 72°C.
Состав реакционной смеси был подобран таким образом, чтобы концентрация ионов MgCl2 была в пределах 2,0 - 2,5 мМ, что обеспечивает оптимальную скорость и точность работы фермента Taq-полимеразы, концентрация дНТФ - не более 2,5 мМ, концентрация каждого праймера -1,5 пмоль/мкл, зонда - 0,75 пмоль/мкл и объем пробы - 10 мкл.
Пробирки с амплификационной смесью расставляют в соответствии с заранее подготовленным протоколом, где указаны номера анализируемых проб, а также пробирки положительного и отрицательного контролей. Если реакцию проводят на анализаторе Rotor Gene 6000/Q (Corbett Research), то пробирки могут быть промаркированы.
Добавлят во все пробирки индивидуальными наконечниками с аэрозольными фильтрами по 7 мкл:
а) в амплификационную пробирку для постановки отрицательного контроля
- отрицательный контрольный образец (ОКО) из комплекта тест-системы;
б) в пробирки исследуемых образцов - исследуемые образцы ДНК;
в) в амплификационную пробирку для постановки положительного контроля
- положительный контрольный образец (ПКО) из комплекта тест-системы.
Для снижения риска контаминации образцы следует добавлять в указанном порядке.
Пробирку, в которую был внесен образец, следует по возможности немедленно закрыть крышкой и центрифугировать в течение 15 секунд на плашечной центрифуге или микроцентрифуге-вортексе. Затем переносят пробирки в прибор и проводят амплификацию.
Проводят амплификацию по программе для амплификатора Rotor-Gene Q или Rotor-Gene 6000 (Corbett Research), указанной в Таблице 1.
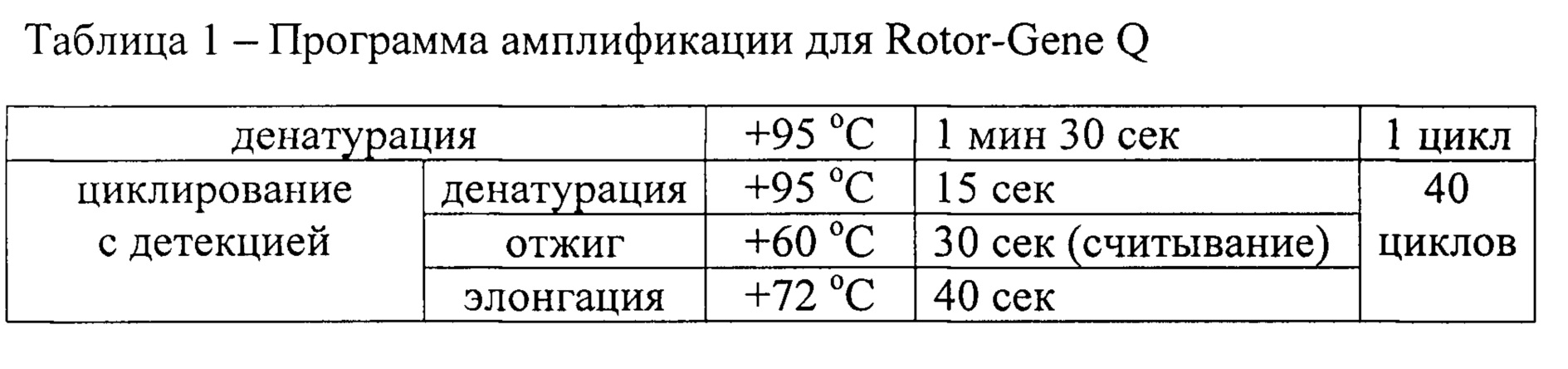
Детекция продуктов амплификации осуществляется прибором автоматически в каждом цикле амплификации. На основании этих данных управляющая программа строит кривые накопления флуоресцентного сигнала по каждому из заданных для образцов каналов.
Для работы с тест-системой используют каналы: FAM (специфический сигнал), HEX (сигнал внутреннего контроля), CY5 (сигнал экзогенного внутреннего контроля).
Оценка эффективности использования тест-системы осуществлялась по кривым накопления флуоресцентного сигнала по каждому из заданных для образцов каналов проводилась по графикам из отчета работы прибора Rotor-Gene 6000 при использовании Real-time PCR:
Для отрицательного образца
Фиг. 1. Канал FAM - искомая ДНК АЧС (фиолетовый цвет). Из исследуемых образцов не вышел. Регистрируется только сигнал контрольного образца (красный цвет).
Фиг. 2. Канал Су5 - внутренний контрольный образец специфики - ДНК АЧС (фиолетовый цвет) - выходят позже графика положительного контрольного образца (красный цвет), что говорит о незначительном ингибировании реакции.
Фиг. 3. Канал HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС (фиолетовый цвет). График экзогенного внутреннего контроля выделения и графики исследуемых образцов совпадают, что говорит, что реакция прошла успешно.
Для положительного образца
Фиг. 4. Канал FAM - искомая ДНК АЧС (синий цвет) - флуоресцентно сигнал начал накапливаться до 36 цикла, его можно считать положительным. Отрицательный контрольный образец не вышел - контаминации контроля нет.
Фиг. 5. Канал Су5 - внутренний контрольный образец специфики - ДНК АЧС (синий цвет) - накопление флуоресцентного сигнала достаточно, чтобы считать реакцию положительной. Черный график - отрицательный контрольный образец. Флуоресцирует благодаря наличию экзогенного контрольного образца, вносимого в пробирку на стадии выделения. Красный график - положительный контрольный образец.
Фиг. 6. Канал HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - накопления флуоресцентного сигнала достаточно, чтобы считать реакцию положительной. Черный график - отрицательный контрольный образец. Флуоресцирует благодаря наличию экзогенного контрольного образца, вносимого в пробирку на стадии выделения. Красный график – положительный.
Для сомнительного образца
Фиг. 7. Канал FAM - искомая ДНК АЧС (синий цвет) - по графику видно, что и отрицательный контрольный образец, и исследуемый образец вышли до 36 цикла, это говорит о возможной контаминации.
Фиг. 8. Канал Су5 - внутренний контрольный образец специфики - ДНК АЧС (синий цвет) - накопления флуоресцентного сигнала достаточно, чтобы считать реакцию положительной. Фиолетовый график - отрицательный контрольный образец. Флуоресцирует благодаря наличию экзогенного контрольного образца, вносимого в пробирку на стадии выделения. Красный график - положительный контрольный образец.
Фиг. 9. Канал HEX - внутренний контрольный образец выделения - синтетическая ДНК АЧС - накопления флуоресцентного сигнала достаточно, чтобы считать реакцию положительной. Фиолетовый график - отрицательный контрольный образец. Флуоресцирует благодаря наличию экзогенного контрольного образца, вносимого в пробирку на стадии выделения. Красный график - положительный контрольный образец.
При учете результата threshold (порог) устанавливали вручную на уровне 10% от максимального уровня флуоресценции в последнем цикле амплификации. Уровень threshold составил не более 0,02. Значения показателя «Ct» были на уровне 24-25. В положительных образцах кривая флуоресценции пересекает линию threshold и, в зависимости от интенсивности сигнала, возвышается над линией более или менее. В отрицательных образцах и отрицательном контроле флуоресценции не наблюдается, что отражается прямой детекции на уровне или ниже линии threshold.
Пример 1. Для анализа методом ПЦР были взяты 2 пробы тканей селезенки от свиней, признанных больными африканской чумой свиней, на основании ПЦР-исследований набором производства ГНУ ВНИИВВиМ, г. Покров. В процессе ПЦР в пробах были получены кривые флуоресценции, пересекающие линию threshold, при отсутствии таковой в отрицательном контроле. Это свидетельствует о воспроизводимости результатов проведенных опытов.
Пример 2. Применение реакции амплификации для выявления ДНК вируса африканской чумы свиней с использованием разработанных специфических олигонуклеотидных праймеров и зонда, входящих в тест-систему.
Для анализа методом ПЦР были взяты 6 проб тканей селезенки свиней. В процессе ПЦР во всех пробах были получены кривые флуоресценции, пересекающие линию threshold, при отсутствии таковой в отрицательном контроле. Значения показателя «Ct» составило от 32 до 36. Это свидетельствует о воспроизводимости результатов проведенных опытов.
Предложенная тест-система позволяет количественно выявлять на ранних стадиях высококонсервативную область гена VP72 вируса африканской чумы свиней. Применение олигонуклеотидного зонда позволяет повысить чувствительность и специфичность способа, исключить субъективность при оценке результатов. Использование предлагаемой модификации ПЦР позволяет значительно снизить возможность контаминации образцов, помещения, оборудования и реактивов, а также сократить сроки проведения анализа, что важно как для владельцев животных, так и для ветеринарных специалистов.
Предложенная тест-система апробирована с положительными результатами и регулярной воспроизводимостью этих результатов в 2016 году на 8 пробах тканей селезенки свиней, признанных больными африканской чумой свиней, на основании ПЦР-исследований набором производства ГНУ ВНИИВВиМ, г. Покров.
Работу проводили на базе ФГБОУ ВО «Краснодарский ГАУ».