Результат интеллектуальной деятельности: Катализатор и способ получения ацетальдегида с его использованием
Вид РИД
Изобретение
Изобретение относится к области гетерогенного катализа, а именно к катализатору и способу получения ацетальдегида (AA) в ходе газофазного неокислительного дегидрирования этанола, и может быть использовано на предприятиях химической и фармацевтической промышленности для получения ацетальдегида.
AA широко используется в промышленности в качестве полупродукта для получения уксусной кислоты, уксусного ангидрида, этилацетата, пиридина, бутанола и 2-этилгексанола (Химическая энциклопедия, Издательство БРЭ, Москва, 1998, т. 1, 224). На получение этих веществ расходуется до 95% производимого в мире ацетальдегида. Изначально в 50-60 годах ацетальдегид был получен окислительным дегидрированием этилового спирта, позднее использовали другие методы, такие как гидратация ацетилена, окисление этилена, дегидрирование этанола. Промышленным способом производства ацетальдегида является окисление этилена в присутствии катализатора, состоящего из растворов хлорида меди и хлорида палладия (RU 2454395, опубликован 27.06.2012). Однако способ имеет существенные недостатки, такие как высокая стоимость катализатора и сложное аппаратурное оформление и высокие энергозатраты.
Существуют различные катализаторы окислительного дегидрирования этанола с получением ацетальдегида. Так, в работе (V.I. Sobolev, K.Yu. Koltunov, О.A. Simakova, A.-R. Leino, D.Yu. Murzin // Low temperature gas-phase oxidation of ethanol over Au/TiO2 // Applied Catalysis A: General. 2012, V. 433-434. p. 88-95) окислительное дегидрирование этанола с получением ацетальдегида проводят с использованием золотосодержащих катализаторов, а в работе (E. Santacesaria, A. Sorrentino, R. Tesser, М. Di Serio, А. Ruggiero Oxidative dehydrogenation of ethanol to acetaldehyde on V2O5/TiO2-SiO2 catalysts obtained by grafting vanadium and titanium alkoxides on silica // Journal of Molecular Catalysis A: Chemical, 2003, V. 204-205. p. 617-627) на оксидно-ванадиевых катализаторах.
Общим недостатком этих катализаторов и способов окислительного дегидрирования этанола является низкая селективность по AA, связанная с образованием в качестве побочных продуктов этилена, оксидов углерода и таких оксигенатов, как диметиловый и диэтиловые эфиры (ДМЭ, ДЭЭ), уксусная кислота и др.
Процесс получения AA каталитическим неокислительным дегидрированием этилового спирта, широко применявшийся в 60-70-х годах прошлого столетия, не потерял практического значения. Этот метод имеет ряд преимуществ перед другими методами: отсутствие ядовитых отходов, достаточно мягкие условия проведения реакции и получения наряду с ацетальдегидом водорода, который молено использовать в других процессах (www.rccnews.ru). Исходным сырьем может являться этиловый спирт, получение которого из биомассы позволяет не использовать нефтяное сырье. Наиболее распространенным и эффективным катализатором процессов неокислительного дегидрирования спиртов является медь, главным образом, благодаря ее способности не разрывать связь C-C. Результаты исследований медных либо медьсодержащих катализаторов согласуются в том, что именно Cu°, образующаяся восстановлением из оксида CuO, является катализирующим агентом реакции дегидрирования. В литературе было предложено использовать другие металлы, включая Cd, Pd, Pt, Cr, Ni, Fe, Mn, Co, Zn, Ru (Morgenstern D.A., Fornango J.P. // Low-temperature reforming of ethanol over copper-plated raney nickel: A new route to sustainable hydrogen for transportation // Energy and Fuels, 2005, v. 19, p. 1708; Davidson J.M., McGregor C.M., Doraiswamy L.K. // Kinetics of the palladium-catalyzed vapor-phase thermal decomposition of ethanol // Industrial and Engineering Chemistry Research, 2001. v. 40, p. 101), однако все они уступают по селективности медьсодержащим катализаторам.
В связи с вышесказанным поиск эффективных катализаторов процесса является достаточно актуальным. Ряд работ посвящен исследованиям в реакции дегидрирования этанола серебросодержащих катализаторов. Так, в работе (Sushkevich V.L., Ivanova I.I., Taarning E. // Mechanistic study of ethanol dehydrogenation over silica-supported silver // Chem. Cat. Chem., 2013, V. 5. p. 2367) авторы исследовали катализатор 10% Ag/SiO2, полученный пропиткой силикагеля (340 м2/г) водным раствором нитрата серебра. Особенностью катализатора является то, что серебро находится в виде частиц 3±1 нм. Катализатор проявляет высокую активность в реакции дегидрирования этанола при температуре 300°C. Недостатками этого катализатора является то, что при 300°C конверсии этанола составила около 66%. а выход ацетальдегида не превышает 50%. При этом селективность по ацетальдегиду составляет ~76%, а в качестве побочных продуктов образуются этилацетат, этилметилкетон, бутаналь и бутанол-1. Таким образом, получаемый ацетальдегид необходимо подвергать трудоемкой очистке от получаемых соединений.
В патенте RU 2558368 (опубликован 10.08.2015) описан катализатор для получения ацетальдегида, который представляет из себя мезопористый силикагель (Sуд.=100-300 м2/г) с нанесенным на его поверхность серебром в количестве 1-8% от массы катализатора, находящимся в высокодисперсном (наноразмерном) состоянии со средним размером частиц 2-8 нм. При этом катализатор содержит один или несколько оксидов из CeO2, MnOx, ZrO2, FeOx при их суммарном содержании 0,5-8% от массы катализатора. Способ получения ацетальдегида из этанола заключается в пропускании через слой катализатора газовой смеси, содержащей 2% C2H5OH (остальное гелий), при нагревании и атмосферном давлении. Для повышения эффективности работы катализатора в реакционную смесь вводился кислород (до 21%). В примерах, проводимых в режиме неокислительного дегидрирования, газовую смесь, пропускали через слой катализатора (навеска 0,5 г) при скорости ее подачи 60 см3/мин. В режиме неокислительного дегидрирования ацетальдегид может быть получен с выходом более 50% в диапазоне температур 260-350°C. Так, в примере 3 для катализатора Ag/MnOx/SiO2 при температуре 345°C конверсия этанола составила 99,3%, а селективность по AA составила 84%. при этом максимально полученная производительность по AA составила всего 1.62 ммоль/г*ч.
Существенным недостатком способа является относительно высокая стоимость катализатора, поскольку он содержит серебро и модифицирующие добавки, а также низкая производительность по AA, поскольку все примеры осуществления реакции проведены при низкой массовой скорости подачи этанола (6 ммоль C2H5OH/г-Кт*ч).
Основное внимание в литературе для процесса получения AA в ходе реакции неокислительного дегидрирования этилового спирта сосредоточено на нанесенных медьсодержащих катализаторах. Так, в работе (Iwasa N., Takezawa N. // Reforming of ethanol - dehydrogenation to ethyl acetate and steam reforming to acetic acid over copper-based catalysts // Bulletin of the Chemical Society of Japan, 1991, №64, p. 2619) описаны каталитические свойства медных катализаторов на основе различных оксидов SiO2, ZrO2, Al2O3, MgO и ZnO. В продуктах, помимо AA наблюдали образование ряда побочных соединений. Так, оксиды ZrO2 и ZnO способствовали образованию этилацетата и ацетона соответственно, а Cu/ZrO2 и Cu/ZnO показали максимальную селективность в образовании этилацетата - 27,6% и 28,1%. Наибольшая селективность по ацетальдегиду 77.9% и 74,2% достигается в присутствии катализаторов Cu/SiO2 и Cu/MgO соответственно.
В работе (Chang F.W., Yang H.C., Roselm L.S., Kuo W.Y. // Ethanol dehydrogenation over copper catalysts on rice husk ash prepared by ion exchange // Applied Catalysis A: General - 2006, v. 304, p. 30) авторы пришли к выводу, что наиболее эффективными и селективными являются медьсодержащие катализаторы на основе SiO2. К преимуществам такого носителя относят большую площадь поверхности, высокое распределение частиц меди па поверхности носителя. Уже при 275°C конверсия этанола составила 77% при селективности но ацетальдегиду около 100%. Однако, эти катализаторы оказались нестабильными и деактивировались через 2-3 часа вследствие спекания частиц меди.
В работе (Raich В.А., Foley Henry С. // Ethanol dehydrogenation with a palladium membrane reactor: an alternative to Wacker chemistry // Ind. Eng. Chem. Res., 1998, v. 37, p. 3888) для приготовленных методом пропитки Cu/SiO2 катализаторов была измерена относительная скорость реакции дегидрирования, которая составила всего 7,8*10-2 ммоль C2H5OH/г-Кт*мин.
Наиболее близким к настоящему изобретению является способ получения ацетальдегида, описанный в работе (Р.С. Zonetti, J. Celnik, S. Letichevsky, А.В. Gaspar, L.G. Appel // Chemicals from ethanol - The clehydrogenative route of the ethyl acetate one-pot synthesis // Journal of Molecular Catalysis A: Chemical. 2011, V. 334, p. 29]. В качестве катализаторов использовали промышленный оксидный медь-цинк-алюминиевый катализатор марки CZA (состав и методика его приготовления не раскрываются), а также его механические смеси с оксидами ZrO2, CeO2, Al2O3 and SiO2. В предлагаемом способе получения ацетальдегида газовую смесь, содержащую 12 об. % этанола в азоте, пропускали при атмосферном давлении через слой нагретого до 150-200°C катализатора (навеска 0,1 г) при скорости подачи газовой смеси 20 см3/мин. В описанном способе конверсии этанола в AA селективность исходного катализатора CZA составляет 95%, при этом максимально достигнутая производительность по перерабатываемому этанолу составляет всего 37 мкмоль/г-Кт*мин. Для образцов катализаторов с добавлением в качестве промотирующих добавок различных оксидов производительность по перерабатываемому этанолу возрастает до 5,6 ммоль/г-Кт*ч, однако в продуктах реакции в значительных количествах (до 40%) появляется этилацетат.
Существенным недостатком способа является низкая производительность исходного катализатора по перерабатываемому этанолу. Для промотированных оксидными добавками катализаторов недостатком является низкая селективность процесса, связанная с образованием этилацетата, что ухудшает чистоту продукта.
Техническим результатом настоящего изобретения является создание высокоэффективного селективного катализатора и способа получения ацетальдегида по реакции неокислительного дегидрирования этанола, обеспечивающего повышенную производительность по AA.
Технический результат достигается использованием катализатора для получения ацетальдегида из этанола, который представляет собой смешанный металл оксидный катализатор, содержащий оксиды цинка, меди и алюминия, при этом на стадии его приготовления дополнительно добавляют нанопорошок карбида вольфрама (WC). Катализатор имеет состав ( мас.%): ZnO - 22.8; CuO - 58,9; Al2O3 - 9,2; WC - 9,1% и повышенную удельную поверхность 245 м2/г.
Технический результат достигается также использованием предлагаемого способа получения ацетальдегида, который заключается в пропускании чистого не разбавленного инертным газом (азотом) этанола через слой катализатора при температуре 150-250°C и массовой скорости подачи этанола 0,5-2 ч-1.
Осуществление изобретения
Катализатор для получения ацетальдегида из этанола имеет в своем составе оксиды цинка, меди и алюминия, так же как в традиционных катализаторах низкотемпературного синтеза метанола, при этом в настоящем изобретении его готовили так называемым «мокрым» способом в ходе добавления гидроксида алюминия и гидроксокарбоната меди к водной суспензии ZnO и WC. Добавление в катализатор карбида вольфрама (в виде нанопорошка со средним размером гранул 55 нм), казалось бы каталитически инертного материала с низкой удельной поверхностью (7 м2/г), приводит к увеличению общей удельной поверхности заявляемого в настоящем изобретении катализатора (245 м2/г - измерена методом БЭТ), по сравнению с поверхностью традиционных оксидных цинк-медных катализаторов синтеза метанола (не более 200 м2/г).
Отличительной особенностью предлагаемого способа получения ацетальдегида является то, что в качестве сырья используется чистый этанол, а не газовая смесь этанола в азоте, что при используемых в изобретении массовых скоростях подачи этанола 0,5-2 ч-1 позволяет повысить производительность по AA.
Изобретение иллюстрируется следующими примерами, не ограничивающими его объем.
Пример 1. Приготовление катализатора.
В металлический реактор, снабженный рубашкой для обогрева и мешалкой, заливали 200 см3 дистиллированной воды, и при включенной мешалке загружали 25,0 г оксида цинка (ZnO, производства "Pharma") и 10 г карбида вольфрама (WC в виде порошка с удельной поверхностью 7 м2/г и средним размером гранул 55 нм был получен методом плазмохимического синтеза в ИМЕТ РАН). Водную суспензию ZnO и WC перемешивали в течение 2 часов. Далее к водной суспензии добавляли порциями 34,5 г гидроксида алюминия (в виде псевдобемита). Суспензию перемешивали в течение 2 часов, после чего в нее порциями вводили 89,8 г измельченного гидроксокарбоната меди (II). Полученную массу разогревали в реакторе до температуры 90°C, после чего перемешивали при данной температуре в течение 2 часов и охлаждали до комнатной температуры.
Отделение готовой катализаторной массы проводили на центрифуге. Отделившуюся воду декантировали, а влажную катализаторную массу переносили на противень для последующей сушки при температуре 110°C в течение 12 часов, и далее прокаливали в муфеле в режиме ступенчатого подъема температуры (сначала с 20 до 150°C, а затем, через 50°C до 350°C, выдерживая заданный режим при каждой температуре в течение 1 часа).
Прокаленную массу смешивали с графитом марки "C2" и таблетировали, а далее размельчали гранулы и использовали фракцию катализатора 0,05-0,1 мм. Насыпная плотность полученного катализатора составила 1,23 г/см3.
В результате был получен образец металл-оксидного катализатора, содержащий, мас.%: ZnO - 22,8; CuO - 58,9; Al2O3 - 9,2 и WC - 9,1% (соотношение активных компонентов приведено без учета инертного связующего компонента - графита, который брали в количестве 5 мас.% по отношению к катализатору).
Примеры 2-4. Реакцию дегидрирования этанола проводили при атмосферном давлении в кварцевом реакторе (D=7 мм), помещенном в печь с электрообогревом. Контроль температуры осуществляли с помощью термопары, помещенной непосредственно в слой катализатора (загрузка катализатора 1 г, высота слоя 15 мм) и связанной с задатчиком - регулятором температуры "Термодат-17". Нагрев катализатора до необходимой температуры (150-250°C) осуществляли в токе азота, подаваемого из баллона через редуктор и вентиль тонкой регулировки. При достижении необходимой температуры выключали ток азота и включали подачу этанола (марки A). Этанол подавали шприцевым дозатором в верхнюю часть реактора, где на кварцевой насадке происходит его испарение и предварительный нагрев. Массовая скорость подачи C2H5OH составляла 0,5-2 ч-1. Жидкие продукты реакции охлаждали до -5°C в холодильнике на выходе из реактора и собирали в приемнике.
Анализ жидких продуктов реакции осуществляли хроматографическим методом на хроматографе модели "3700" производства НПО "Гранат" с использованием капиллярной колонки SE-54 (30 м) и пламенно-ионизационного (ПИД) детектора при температуре 60°C (газ носитель - гелий).
Показатели процесса конверсии этанола в AA с использованием заявленного в настоящем изобретении катализатора представлены в таблице.
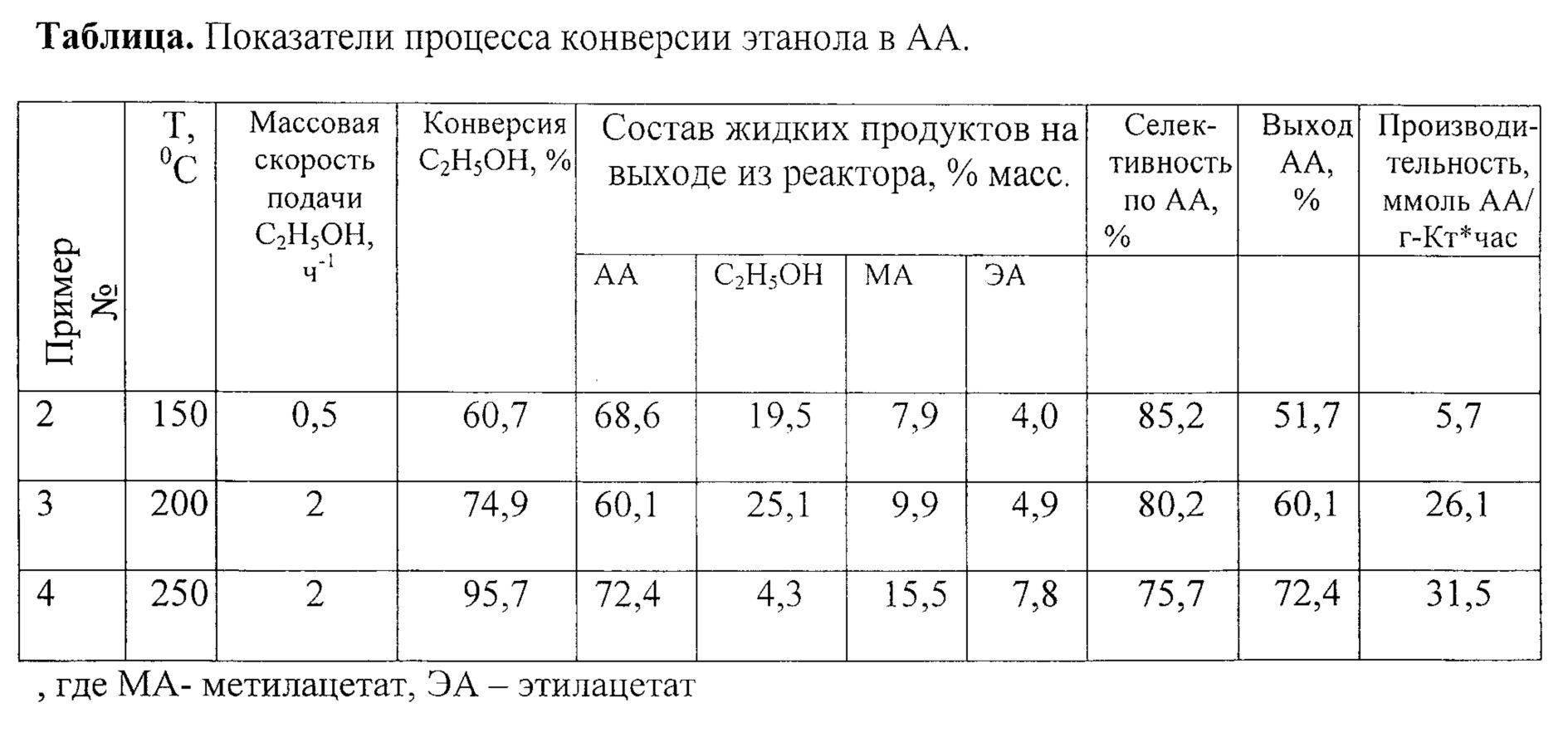
При сравнении каталитических свойств предлагаемого в настоящем изобретении катализатора с показателями процесса по изобретению-прототипу видно, что в настоящем изобретении ацетальдегид может быть получен из этанола при температурах 150-250°C с выходом до 72,4%. При этом производительность предлагаемого катализатора по образующемуся AA существенно превышает производительность катализатора по изобретению-прототипу. Так, при одинаковой температуре (150°C) производительность процесса с использованием предлагаемого в настоящем изобретении катализатора составляет 5,7 ммоль АА/г-Кт*час, что более чем в 2,5 раза выше, чем для исходного катализатора CZA в изобретении-прототипе. При более высоких температурах и массовой скорости подачи этанола (примеры 3 и 4) этот эффект еще более значителен. Это обусловлено тем, что в предлагаемом способе при сопоставимых с изобретением-прототипом конверсиях этанола массовая скорость подачи этанола существенно выше, при этом используется чистый этанол, а не его смеси с инертным газом.
Технический результат, получаемый при реализации настоящего изобретения, состоит в создании эффективного способа получения ацетальдегида, в котором используется высокоэффективный и селективный катализатор неокислительного дегидрирования этанола, обеспечивающий повышенную производительность по AA.
Существенным результатом предлагаемого изобретения является то, что в результате использования высокоселективного катализатора достигается более высокая чистота получаемого AA. Так, в примере 2 настоящего изобретения селективность по AA составляет 85,2%, в то время как для катализатора CZA с добавками ZrO2 и CeO2 в изобретении-прототипе она не превышает 53%.
Следует отметить, что предлагаемый способ может быть использован также для получения чистого водорода без его отделения от азота, поскольку в реактор подается чистый этанол, а не его смесь с азотом, как в способе по изобретению-прототипу, а в ходе реакции в стехиометрических количествах образуется водород.

