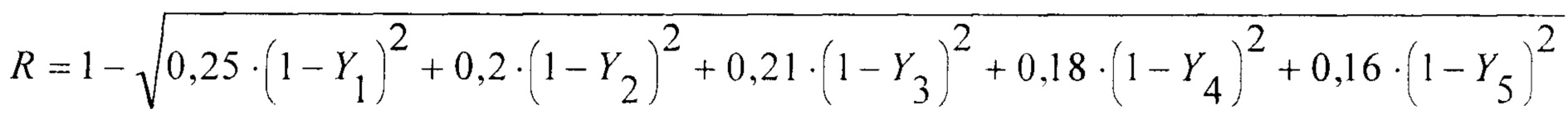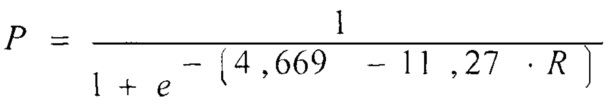Результат интеллектуальной деятельности: СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ОСЛОЖНЕНИЙ В РАННЕМ ГОСПИТАЛЬНОМ ПЕРИОДЕ У ПАЦИЕНТОВ ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно к кардиологии, сердечно-сосудистой хирургии, анестезиологии и реаниматологии, и может быть использовано для определения вероятного риска развития госпитальных осложнений у пациентов после кардиохирургического вмешательства в условия искусственного кровообращения.
Коронарное шунтирование (КШ) является эффективным методом лечения ишемической болезни сердца (ИБС). Однако, несмотря на достигнутые успехи как в технике выполнения КШ, так и в послеоперационном ведении пациентов, такие грозные осложнения, как инфаркт миокарда (ИМ), инсульт, острое повреждение почек с развитием почечной недостаточности являются лидирующими в причинах госпитальной летальности после КШ [Авалиани В.М. Особенности аортокоронарного шунтирования у больных системным атеросклерозом. Архангельск: 2007, 223]. Данный факт требует пересмотра ранее существовавших подходов к риск-стратификации пациентов, направляемых на КШ, и выявления наиболее чувствительных маркеров неблагоприятного прогноза.
В последние годы в связи с увеличением продолжительности жизни людей, возросла категория пациентов, имеющих сочетанное поражение органов и систем. При этом наиболее частым коморбидным фоном у пациентов с сердечно-сосудистыми заболеваниями являются сахарный диабет (СД), артериальная гипертензия (АГ), хроническая сердечная недостаточность (ХСН), мультифокальный атеросклероз (МФА).
Особое место среди сочетанных состояний занимает хроническая болезнь почек (ХБП), при которой риск сердечно-сосудистой смертности на 10-20% выше, чем у их сверстников без данной сопутствующей патологии [Белялов Ф.И. Диагностика и лечение ишемической болезни сердца при хронической болезни почек. 2010. Электронный ресурс [Текст]; Кардиосайт; Режим доступа свободный: http://therapy.irkutsk.ru]. В последние годы проведено множество исследований, которые показали, что нарушения функции почек и сердечно-сосудистой системы опосредованы рядом патофизиологических механизмов, объединенных понятием кардиоренальный синдром. Такая взаимосвязь приводит к неуклонно прогрессирующей дисфункции данных органов с формированием хронической почечной и сердечной недостаточности, влияющих на развитие неблагоприятных исходов у пациентов [Characteristics and outcomes of patients hospitalized for heart failure in the United States: Rationale, design, and preliminary observations from the first 100,000 cases in the Acute Decompensated Heart Failure National Registry (ADHERE) / K.F. Adams, G.C. Fonarow, C.L. Emerman et al. // Am. Heart J. - 2005. - Vol. 149. - P. 209-216.].
Нарушение функции почек ухудшает как ранний послеоперационный, так и отдаленный прогноз. Доказано, что снижение скорости клубочковой фильтрации (СКФ) до 60-90 мл/мин, 30-60 мл/мин и <30 мл/мин приводит к увеличению риска смерти в течение 5 лет после коронарного шунтирования в 1.2, 1.8 и 5.2 раза, соответственно, по сравнению с нормальной функцией почек (СКФ >90 мл/мин) [Holzmann М., Jernberg Т., Szummer K., Sartipy U. // Long-term Cardiovascular Outcomes in Patients With Chronic Kidney Disease Undergoing Coronary Artery Bypass Graft Surgery for Acute Coronary Syndromes // J Am Heart Assoc. 2014 Mar 4; 3 (2): е000707]. Выявление почечной дисфункции (ПД) в дооперационном периоде ассоциируется с наличием многососудистого поражения коронарного русла и некоронарных сосудистых бассейнов, приводит к увеличению сроков госпитализации после КШ и необходимости в диализе. Данные факты должны быть учтены при выборе стратегии реваскуляризации миокарда, объеме оперативного вмешательства и медикаментозного сопровождения.
Известен способ прогнозирования госпитальных осложнений при операциях на открытом сердце с использованием шкалы STS [The Society of Thoracic Surgeons National Adult Cardiac Surgery Database) (Online STS Risk Calculator [Электронный ресурс]: Risk Model and Variables - STS Adult Cardiac Surgery Database Version 2.81. - Режим доступа http://riskcalc.sts.org/stswebriskcalc/#/calculate, свободный, - загл. с экрана]. С помощью данного калькулятора определяют в процентах вероятность развития таких неблагоприятных событий, как госпитальная летальность, увеличениЕ срока госпитализации, развитие инсульта, продленная искусственная вентиляции легких, инфекционные осложнения, почечная недостаточность, проведение повторной операции. При этом используют широкий набор критериев: возраст, пол, рост, вес, расовая принадлежность, проявления сердечной недостаточности в течение последних 2-х недель, применение диализа, уровень креатинина крови, наличие стабильной/нестабильной стенокардии, ОКС с подъемом ST или без подъема ST (при поступлении в клинику или непосредственно перед операцией), перенесенный инфаркт миокарда, нарушения ритма, хронические заболевания легких, цереброваскулярные заболевания, признаки периферического атеросклероза, наличие сахарного диабета, артериальной гипертензии, инфекционного эндокардита, применение иммуносупрессивной терапии, срочность оперативного вмешательства (плановая, экстренная, отсроченная), количество пораженных коронарных артерий, проведение реанимационных мероприятий, кардиогенный шок, применение внутриаортальной баллонной поддержки (ВАБП), инотропных препаратов, поражение клапанного аппарата сердца, предшествующая операция на сердце.
Однако почечная дисфункция оценивается лишь по уровню креатинина крови, что недостаточно для определения истинного состояния функции почек. Известно, что показатель креатинина может варьировать в зависимости от возраста, пола и расы пациента, предпочтений в диете; приема некоторых лекарственных препаратов (например, циметидина и триметоприма); наличия соматической патологии. Кроме того, сывороточный креатинин зависит от уровня билирубина, кетонов и белка.
Известен способ прогнозирования осложнений в раннем послеоперационном периоде коронарного шунтирования, основанный на анализе показателей гомеостаза пациента [Пат. 2536278 Рос. Федерация, МПК А61В 5/00. Способ прогнозирования осложнений в раннем периоде после операций шунтирования коронарных артерий в условиях искусственного кровообращения / Семенова А.С., Шигаев М.Ю., Агапов В.В.; патентообладатель Семенова А.С. (RU), Шигаев М.Ю. (RU), Агапов В.В. (RU), № 2013152203/14, заявл. 25.11.13, опубл. 20.12.14., Бюл. №35. - 14 с.]. Способ включает измерение показателей центральной гемодинамики в диапазоне 25-35 минут с момента начала проведения процедуры искусственного кровообращения. Оценивают уровень артериального (АР) и центрального венозного давлений (CVP), показатели гомеостаза, включающие концентрацию лактата в крови (Lact), парциальное давление кислорода в венозной (pvO2) и артериальной крови (раO2), уровень гематокрита (Ht). Дополнительно определяют показатели длительности искусственного кровообращения (t1), времени пережатия аорты (t2) и возраста больного (age). После чего определяют значение дискриминантной функции по формуле: D=3,321+(0,006)*AP+(0,011)*CVP+(1,030)*Lact+(-0,009)*paO2+(0,005)*pvO2+(-0,124)*Ht+(-0,023)*age+(0,014)*t1+(-0,019)*t2. При значении D<-0,6 делают вывод о низком риске развития органных дисфункций в раннем периоде после проведения операции. При получении значений D>0,6 делают вывод о высоком риске развития органных дисфункций. Интервал значений -0,6<D<0,6 характеризуют как интервал неопределенности, и при получении значения D из данного интервала осуществляют контроль состояния пациента, включая более частое измерение стандартных параметров.
Недостатком способа является отсутствие при определении риска критериев исходной почечной дисфункции пациента и ее развития в послеоперационном периоде.
Известна шкала ASCERT Long-Term Survival Probability Calculator For Isolated CABG, позволяющая определить выживаемость пациентов, перенесших коронарное шунтирование в течение 7 лет [ASCERT Long-Term Survival Probability Calculator For Isolated CABG [Электронный ресурс]. - Электрон, текстовые дан. - Режим доступа к сайту, свободный: http://ascertcalc.sts.org/]. Калькулятор учитывает росто-весовые характеристики пациента, расу, фракцию выброса левого желудочка, уровень креатинина крови в мг/дл, значение градиента на аортальном клапане, применение диализа, наличие диабета (инсулинпотребный, на сахароснижающих препаратах или диетотерапия), хронические заболевания легких (умеренной степени выраженности или тяжелой), перенесенный инсульт или транзиторная ишемическая атака, наличие стеноза каротидных артерий более 75% или каротидная эндартерэктомия, применение иммуносупрессивной терапии, наличие периферического атеросклероза, курение, фибрилляция желудочков (постоянная или пароксизмальная) в течение предшествующих 2-х недель до операции, функциональный класс хронической сердечной недостаточности, количество предшествующих сердечно-сосудистых оперативных вмешательств, срочность операции, количество пораженных коронарных артерий более 50%, стеноз более 50% передней межжелудочковой артерии, давность перенесенного ИМ (более 6 часов, 6-24 часа, 1-7 дней, 8-21 день, более 21 дня), нестабильная стенокардия, проведение чрескожного коронарного вмешательства менее 6 часов до КШ, применение внутриаортального баллона или инотропной поддержки, наличие артериальной гипертензии, степени недостаточности клапанного аппарата сердца. Данная шкала позволяет определить процент выживаемости после изолированного коронарного шунтирования в течение от 1 до 7 лет.
Однако, несмотря на учет большого количества параметров, включенных в шкалу, она не получили широкого распространения в Российской Федерации, где наиболее используемой шкалой является EuroSCORE (ES) I и II.
Прогностическая шкала риска госпитальной летальности при коронарном шунтировании - EuroSCORE I учитывает умеренную (сывороточный креатинин >200 мкмоль/л) или терминальную стадию почечной дисфункции как одни из самых важных факторов, влияющих на летальность. [Nilsson J., Algotsson L.,  P. et al. Comparison of 19 pre-operative risk stratification models in open-heart surgery // Eur Heart. J. 2006. N 27. P. 867-874]. Недостатком данной шкалы является оценка степени выраженности мультифокального атеросклероза (МФА) по стенозам некоронарной локализации от 50% и выше, тогда как уже с 30% поражением чаще выявляется почечная дисфункция. Кроме того, способ не учитывает такой важный критерий почечной дисфункции, как скорость клубочковой фильтрации (СКФ), умеренное снижение которого является независимым предиктором в развитии ИМ и смерти у пациентов, подвергшихся КШ [Beddhu S., Allen-Brady K., Cheung A. et al. Impact of renal failure on the risk of myocardial infarction and death. Kidney Int. 2002; 62: 1776-83.].
P. et al. Comparison of 19 pre-operative risk stratification models in open-heart surgery // Eur Heart. J. 2006. N 27. P. 867-874]. Недостатком данной шкалы является оценка степени выраженности мультифокального атеросклероза (МФА) по стенозам некоронарной локализации от 50% и выше, тогда как уже с 30% поражением чаще выявляется почечная дисфункция. Кроме того, способ не учитывает такой важный критерий почечной дисфункции, как скорость клубочковой фильтрации (СКФ), умеренное снижение которого является независимым предиктором в развитии ИМ и смерти у пациентов, подвергшихся КШ [Beddhu S., Allen-Brady K., Cheung A. et al. Impact of renal failure on the risk of myocardial infarction and death. Kidney Int. 2002; 62: 1776-83.].
В шкале EuroSCORE II оценивают такие важные факторы, ассоциированные с неблагоприятным прогнозом, как сахарный диабет и потребность в инсулине, градация степени выраженности легочной гипертензии, нарушения подвижности пациента, объем оперативного вмешательства, включая операции на других сосудистых бассейнах, наличие периферического атеросклероза [The manuscript which supports the new model is being submitted for publication. The new model has been validated by the EuroSCORE Project Group and awaits validation by users worldwide. It was presented at EACTS in Lisbon on 3rd October 2011 http://euroscore.org/calc.html]. Эта шкала имеет недостатки, поскольку она оценивает почечную дисфункцию по формуле Кокрафта-Голта, которая была разработана для оценки клиренса креатинина (ККр). Показатель ККр всегда выше СКФ, следовательно, формулы, оценивающие ККр, могут недооценивать истинное состояние почечной функции. Кроме того, эта шкала не позволяет выделить группы риска госпитальной летальности, например низкий, средний или высокий, а дает лишь значение в процентах. С помощью этой шкалы невозможно определить риск развития несмертельных сердечно-сосудистых или внесердечных осложнений, а именно развитие почечной дисфункции.
Наиболее близким к заявляемому является способ прогнозирования неблагоприятного годового и трехлетнего прогноза летальности и несмертельных сердечно-сосудистых событий у больных с острым коронарным синдромом с подъемом сегмента ST, основанный на исследовании уровня биомаркеров повреждения почек [Быкова, И.С. Клиническая и прогностическая значимость маркеров дисфункции почек у больных острым коронарным синдромом с подъемом сегмента ST: Дис. …канд. Мед. наук: 14.01.05 / Быкова Ирина Сергеевна; Федеральное государственное бюджетное научное учреждение «Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний». - Кемерово, 2015. - 168 с. табл. - Библиогр.: с. 142-168 (235 назв.). В качестве прогностических критериев, значимо влияющих на трехлетний прогноз летальности оценивали уровень микроальбуминурии, цистатина С, нейтрофильного желатиназо-ассоциированного липокалина (NGAL), а также неспецифических маркеров воспаления, таких как С-реактивный белок (СРБ) и фактор некроза опухоли - α (ФНО- α). В результате проведенного исследования выявлено, что прогностически значимое повышение уровня NGAL и цистатина С в отношении развития неблагоприятных сердечнососудистых событий, в том числе смерти, в течение трехлетнего периода наблюдения, зарегистрировано на 12-14-е сутки госпитального периода. А основными факторами, суммарно влияющими на риск развития в течение 3 лет неблагоприятных исходов заболевания, явились: передняя локализация ИМ, систолическая дисфункция миокарда, трехсосудистое поражение коронарных артерий, а также повышение на 12-14-е сутки госпитализации уровня NGAL≥1,25 нг/мл и цистатина С до ≥1,9 нг/л.
Однако способ не учитывает влияние такого триггера, как коронарное шунтирование в условиях искусственного кровообращения, и позволяет лишь определить прогноз отдаленных сердечно-сосудистых осложнений и неблагоприятных исходов, не имеющих диагностической ценности в ранний постоперационный период.
Техническим результатом изобретения является повышение точности прогнозирования риска развития осложнений, в раннем госпитальном периоде у пациентов после коронарного шунтирования в условиях искусственного кровообращения, за счет построения математической модели, учитывающей изменения уровня маркеров почечного повреждения в предоперационном периоде с расчетом интегрального показателя функции почек.
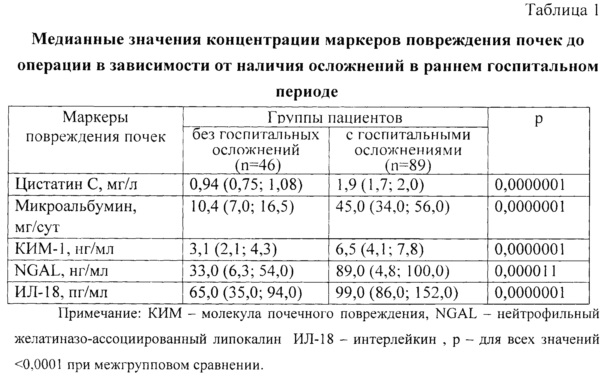
Способ основан на результатах исследования, выполненного на базе МБУЗ «Кемеровский кардиологический диспансер» и ФГБНУ НИИ КПССЗ г. Кемерово, включающего анализ анамнестических, социально-гигиенических, клинико-лабораторных и инструментальных показателей 630 пациентов с ИБС, подвергнутых коронарному шунтированию в условиях искусственного кровообращения. При этом в качестве основных прогностических факторов, влияющих на прогноз развития ранних госпитальных осложнений, оценивали значения таких биологических маркеров кардиоренального синдрома, как цистатин С, NGAL, микроальбмин, молекул почечного повреждения 1-го типа (kidney injury molecule, КИМ-1) и интерлейкина - 18 (ИЛ-18).
Первоначальный этап исследования включал анализ значений почечных маркеров в группах пациентов с осложнениями (ГО) в раннем госпитальном периоде коронарного шунтирования и без них (таблица 1).
Для определения граничных значений почечных маркеров и оценки их прогностической значимости в прогнозе ГО был проведен ROC-анализ и построена бинарная логистическая регрессия (таблица 2).
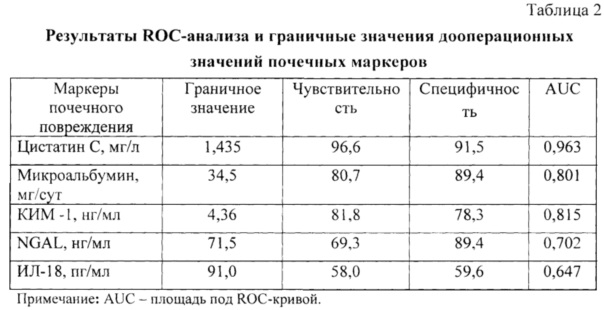
Анализ результатов, представленных в таблице 2, позволяет говорить о том, что наименьшей прогностической способностью в дооперационном периоде обладают ИЛ-18 и NGAL.
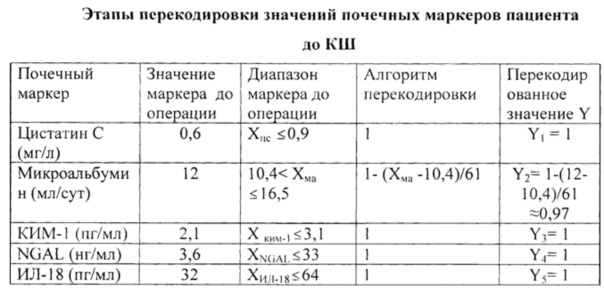
Далее осуществляли комплексную оценку почечной функции пациента в дооперационном периоде (до коронарного шунтирования), для чего был построен интегральный показатель. С этой целью после проведения сравнительного анализа распределения почечных маркеров в группах пациентов с ГО и без ГО была произведена перекодировка значений почечных маркеров путем кусочно-линейных приближений (таблица 3).
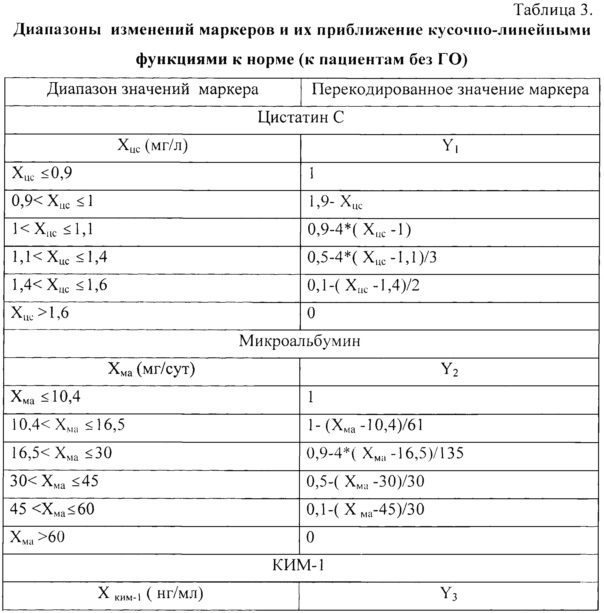

После перекодировки значений почечных маркеров интегральный показатель вычисляли по формуле:
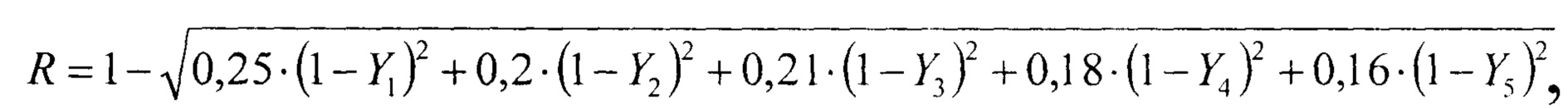
где Y1, Y2, Y3, Y4 и Y5 - перекодированные значения почечных маркеров, а 0,25; 0,2; 0,21; 0,18 и 0,16 - весовые коэффициенты значимости.
Для проверки работоспособности перекодированных показателей был проведен ROC-анализ, основные результаты которого представлены в таблице 4.
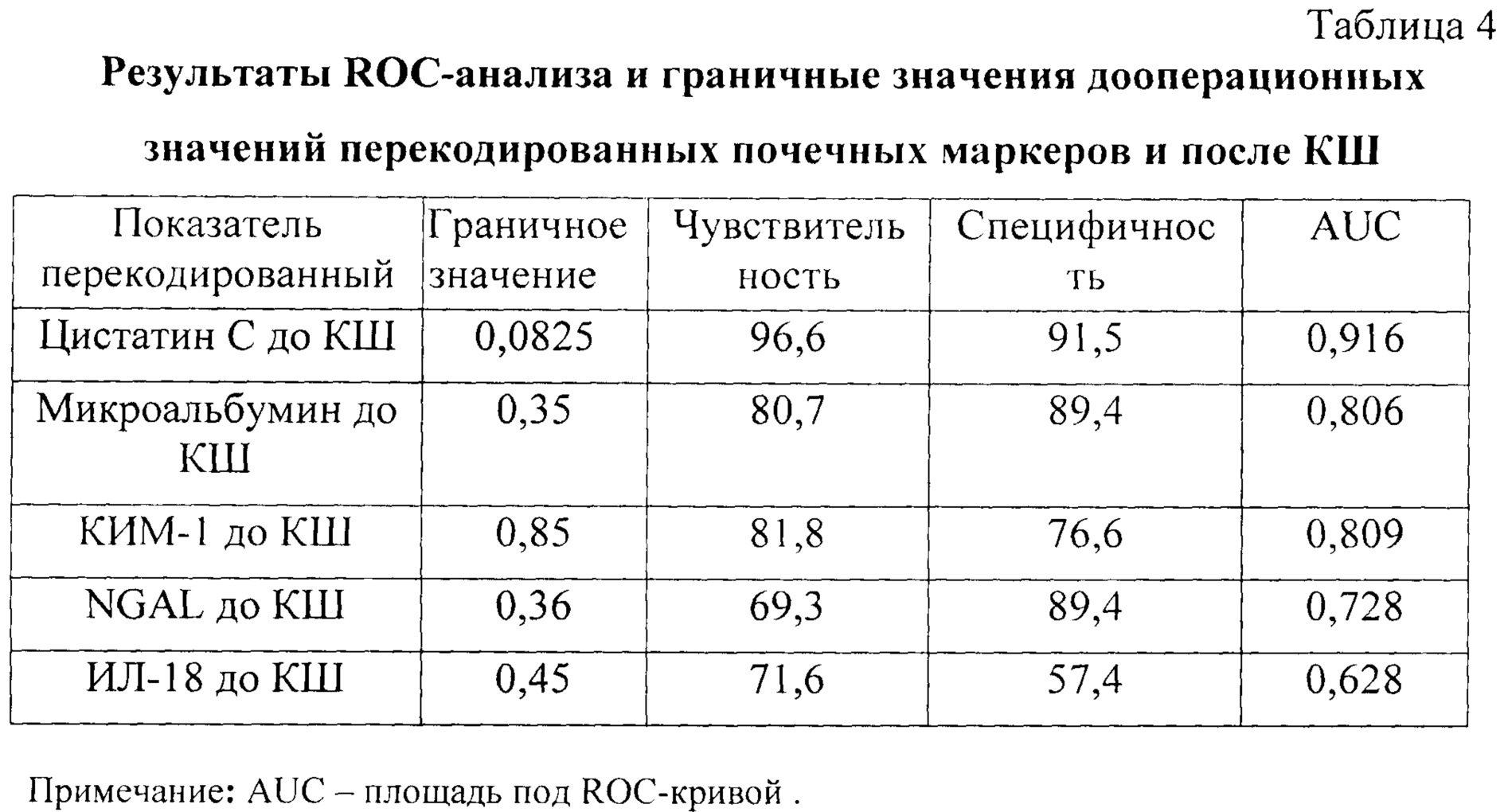
Для прогноза риска развития ближайших госпитальных осложнений по данным почечных маркеров, определяемым в предоперационном периоде и на основании рассчитанного интегрального показателя (R), характеризующего комплексную оценку функции почек до операции, была построена бинарная логистическая регрессия, основные результаты которой представлены в таблице 5.
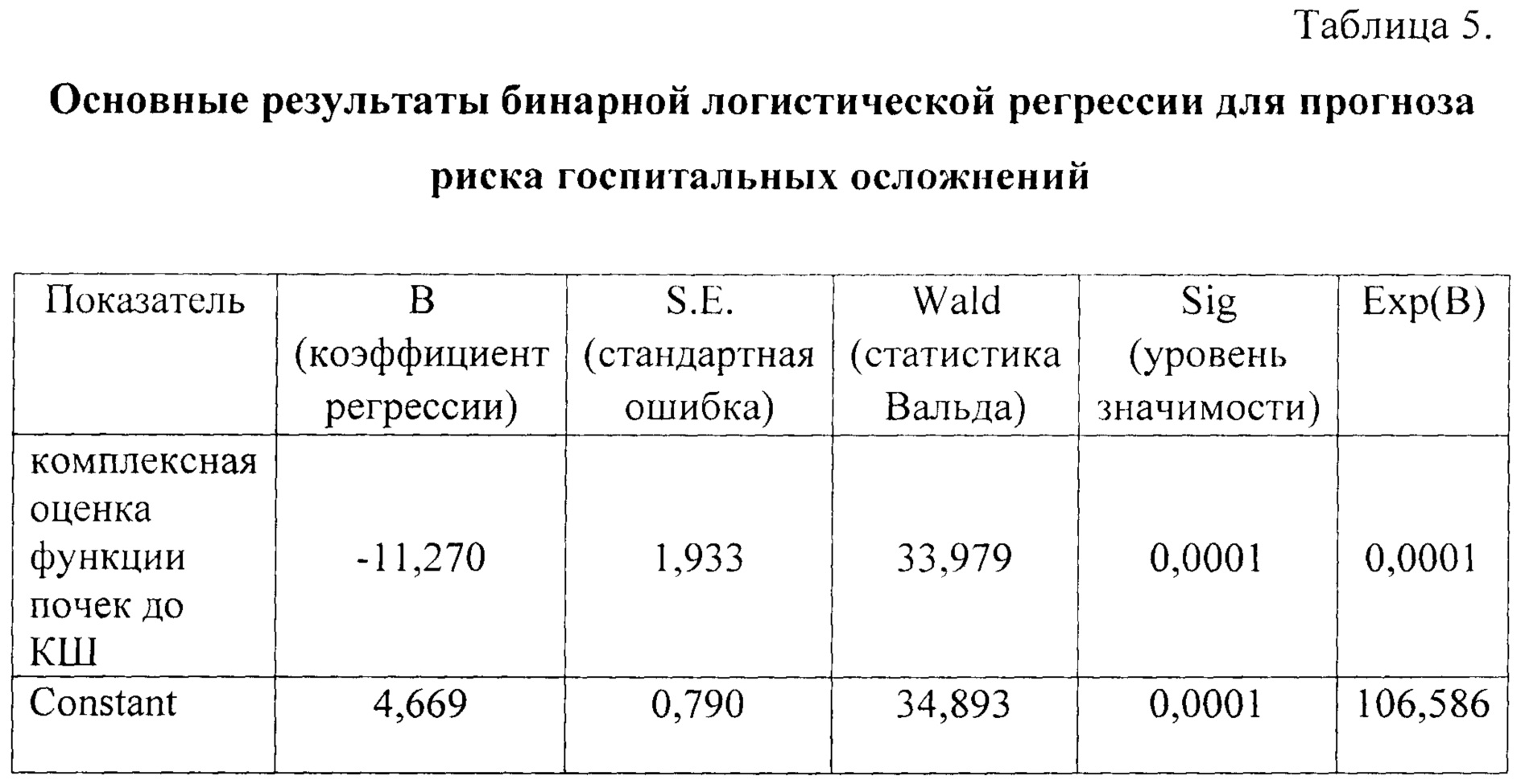
С учетом рассчитанных коэффициентов регрессии модель прогноза вероятности развития осложнений в раннем госпитальном периоде может быть рассчитана по формуле:
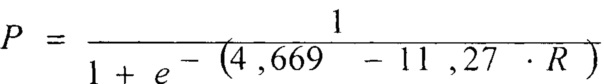
При пороге классификации, равном 0,5, чувствительность модели составила 88,6%, а специфичность 80,9%.
Для определения уровня вероятности развития осложнений в раннем госпитальном периоде были определены диапазоны значений показателя риска в сравниваемых группах пациентов.

Для проверки работоспособности модели был проведен ROC-анализ, при этом площадь под ROC-кривой равна 0,957, что говорит об очень высокой прогностической способности данной модели.
Ниже представлены примеры реализации предложенного способа прогнозирования риска развития ранних госпитальных осложнений у пациентов после коронарного шунтирования в условиях искусственного кровообращения.
Пример №1. Больной А., 53 лет, с диагнозом: ИБС. Стенокардия II ФК. ХСН I ФК II. Гипертоническая болезнь III ст, риск 4. По данным коронарографии выявлены стенозы ПНА 90%, I ДВ 85%, 100% ПКА, поступил для изолированного планового коронарного шунтирования с использованием ИК. Ранее заболеваний почек не имел, без атеросклеротического поражения периферических сосудов, сахарного диабета, инфаркта миокарда, инсульта. ФВ 65%. Оценка риска неблагоприятного исхода коронарного шунтирования по данным шкалы EuroSCORE II составила 0,5%, что соответствует низкому риску. По результатам анализов уровень креатинина крови до операции составил 80 мкмоль/л, СКФ по Кокрафту-Голту - 100 мл/мин, CKD-EPI - 97 мл/мин/1,73 м2.
До операции уровень цистатина С в сыворотке крови составил 0,6 мг/л, ИЛ-18 в сыворотке крови - 32 пг/мл микроальбуминурия - 12 мл/сут, КИМ-1 в моче - 2,1 нг/мл, NGAL в моче - 36 нг/мин.
Тогда интегральный показатель, характеризующий комплексную оценку функции почек в дооперационном периоде, будет равен:
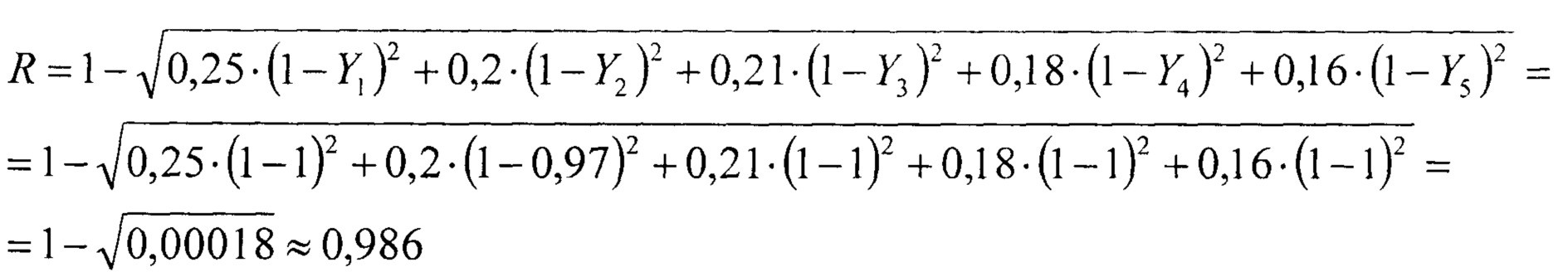
Вероятность развития госпитальных осложнений в раннем послеоперационном периоде КШ для данного пациента будет вычисляться по формуле:
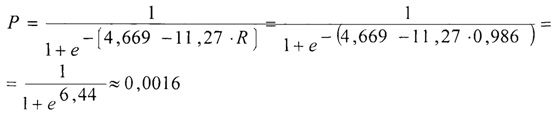
Показатель вероятного риска госпитальных осложнений в раннем послеоперационном периоде находится в диапазоне от 0 до 0,3 и соответствует низкому уровню. В послеоперационном периоде проведена стандартная терапия - минимальная инфузионная нагрузка поляризующей смесью, обезболивание ненаркотическими анальгетиками, дезагреганты. В раннем послеоперационном течении осложнений не зафиксировано, пациент выписан на 8-е сутки на амбулаторную реабилитацию.
Таким образом, предложенная модель расчета риска и стандартная шкала EuroSCORE II выявили низкий риск осложнений у данного пациента после коронарного шунтирования.
Пример №2. Больной Б., 58 лет, с диагнозом: ИБС. Стенокардия II ФК. Постинфарктный (2010) кардиосклероз. ХСН I ФК II. Гипертоническая болезнь III ст, риск 4. По данным коронарографии выявлены стенозы ПНА 95%, I ВТК 90%, ПКА 100%, поступил для изолированного планового коронарного шунтирования с использованием ИК. В анамнезе имеется указание на хронический пиелонефрит, в настоящее время вне обострения. ХПН 0. Сахарного диабета, инсульта не было. По ЦДС БЦА имеется стеноз ВСА справа 55%. ФВ 50%. Балл по EuroSCORE II составил 0,92%, что соответствует низкому риску неблагоприятных событий после предполагаемого вмешательства. По результатам анализов уровень креатинина крови до операции составил 101 мкмоль/л, СКФ по Кокрафту-Голту - 82 мл/мин, CKD-EPI - 70 мл/мин/1,73 м2.
Согласно предложенному способу перед оперативным вмешательством был оценен уровень маркеров почечного повреждения, так уровень цистатина С в сыворотке крови составил 1,1 мг/л, ИЛ-18 в сыворотке крови - 75 пг/мл микроальбуминурия - 50 мл/сут, КИМ-1 в моче - 6,2 нг/мл, NGAL в моче - 16 нг/мл. Полученные значения были перекодированы в соответствии с предложенным алгоритмом, результаты, которого представлены ниже.

Тогда интегральный показатель, характеризующий комплексную оценку функции почек в дооперационном периоде, будет равен:
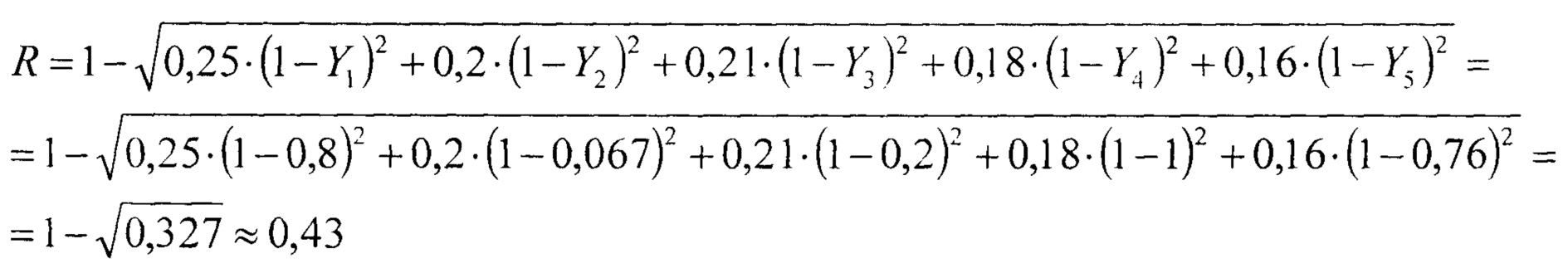
Вероятный риск развития осложнений в раннем госпитальном периоде коронарного шунтирования для данного пациента будет вычисляться по формуле:
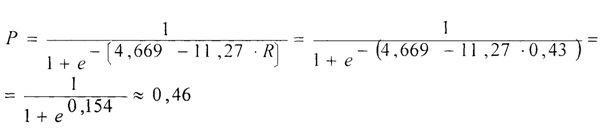
Таким образом, уровень риска средний - 0,46 и не соответствует низкому показателю шкалы EuroSCORE. Учитывая, прогноз для данного пациента была проведена коррекция лечения и интраоперационно проведена ультрафильтрация в объеме 700 мл до достижения нормоволемического гидробаланса при стабильном темпе диуреза без применения салуретиков, что позволило избежать неблагоприятных последствий. Пациент выписан на 9-е сутки на амбулаторную реабилитацию.
Пример №3. Больной В., 63 лет, с диагнозом: ИБС. Стенокардия III ФК. Постинфарктный (2011) кардиосклероз. ХСН I ФК II. Гипертоническая болезнь III ст, риск 4. По данным коронарографии выявлены стенозы ПНА 100%, I ВТК 95%, ПКА 100%, поступил для изолированного планового коронарного шунтирования с использованием ИК. В анамнезе не имеет заболеваний почек, сахарного диабета. В 2010 г перенес ОНМК по ишемическому типу в бассейне левой СМА. ФВ 50%. По ЦДС брахиоцефальных артерий стеноз левой ВСА 45%. Балл по EuroSCORE II составил 1,42% (низкий риск). По результатам анализов уровень креатинина крови до операции составил 101 мкмоль/л, СКФ по Кокрафту-Голту - 82 мл/мин, CKD-EPI - 70 мл/мин/1,73 м2. До операции уровень цистатина С в сыворотке крови составил 1,89 мг/л, ИЛ-18 в сыворотке крови - 113 пг/мл микроальбуминурия - 80 мл/сут, КИМ-1 в моче - 8,9 нг/мл, NGAL в моче -6,8 нг/мл.
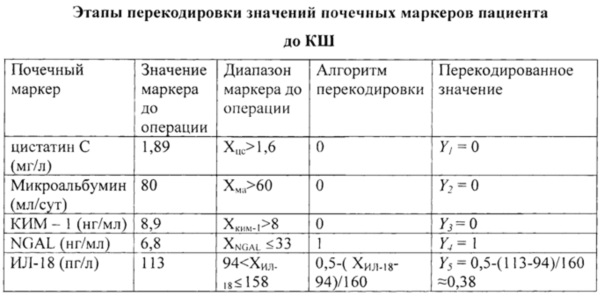
С учетом перекодированных значений маркеров почечного повреждения рассчитываем интегральный показатель:
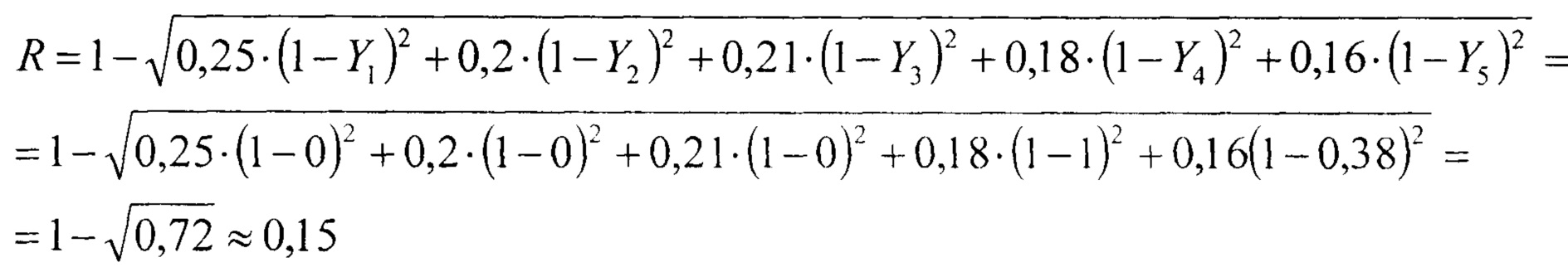
На основании интегрального показателя вероятность развития осложнений в раннем госпитальном периоде равна:
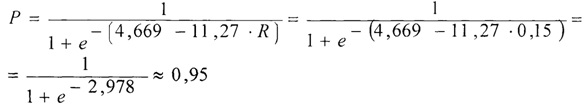
Таким образом, уровень риска высокий - 0,95, что не соответствует данным шкалы EuroSCORE II. Однако в первые сутки у пациента отмечено снижение темпа диуреза до 0,3 мл/кг/ч при повышении азотемии: кретаинин до 340 мкмоль/л, мочевина 24 ммоль/л. Для поддержания адекватного темпа диуреза при значимых дозировках вазопрессорной поддержки - иницация итермиттирующей почечно-заместительной терапии с переходом в программный диализ, всего 8 сеансов, восстановление почечной функции через полиурию.
Таким образом, использование шкалы EuroSCORE II не позволило выявить в предоперационном периоде высокий риск послеоперационных осложнений, что позволяет сделать вывод о большей прогностической ценности предложенного способа.