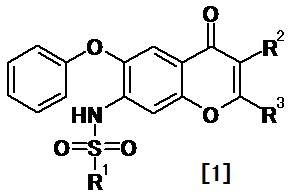
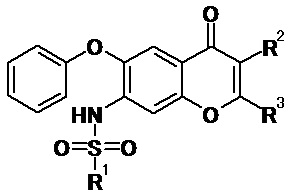
Результат интеллектуальной деятельности: ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЗАБОЛЕВАНИЙ НА ОСНОВЕ ИНГИБИРУЮЩЕГО ДЕЙСТВИЯ НА ФАКТОР ИНГИБИРОВАНИЯ МИГРАЦИИ МАКРОФАГОВ
Вид РИД
Изобретение
ОПИСАНИЕ
Область техники
Данное изобретение относится к способу применения производного бензопирана, обладающего ингибирующим действием на фактор ингибирования миграции макрофагов (далее обозначенный как МИФ) или его соли для терапевтического или профилактического лечения заболевания нервной системы, такого как невропатическая боль или рассеянный склероз. Кроме того, изобретение относится к фармацевтической композиции, содержащей производное бензопирана или его соль, применяемой для терапевтического или профилактического лечения заболевания нервной системы.
Уровень техники
Невропатическая боль (далее обозначенная как НБ) представляет собой тип хронической боли, вызванной расстройством периферийных и/или центральных нервов и функциональным расстройством из-за рака или физического повреждения. Такая боль потеряла свой первоначальный смысл предупреждения расстройства ткани, но является не более чем болью. Качество жизни (КЖ) пациента значительно снижается из-за такой боли.
Симптомом НБ является, кроме непрерывной спонтанной боли, в основном аллодиния, при которой тактильное раздражение воспринимается как резкая боль. Такая боль крайне устойчива к нестероидным противовоспалительным средствам (далее обозначенным как НСПВС), таким как ибупрофен, а также устойчива к морфину, то есть наркотическому обезболивающему (не патентный документ 1).
Патологическая физиология и причина НБ еще полностью не изучены, но представленные ниже выводы были доказаны в результате недавних фундаментальных исследований:
(1) НБ вызывается повреждением периферийных и/или центральных нервов.
(2) множество цитокинов и хемокинов выделяется из поврежденных нервных клеток.
(3) выделенные цитокины и подобные вызывают заметную активацию микроглии, известной как иммунокомпетентная клетка для центральной нервной системы.
НБ лечится в целях облегчения боли, повышения функциональных возможностей пациента и улучшения его/ее активности. Для этих целей, например, проводят введение антидепрессанта, наркотического обезболивающего средства или подобного, нервной блокады и акупунктуры и моксотерапии. Однако какой-либо превосходный терапевтический метод, основанный на механизме развития НБ, не известен, и превосходный терапевтический метод для НБ является желательным.
Рассеянный склероз (далее обозначенный как РС) является заболеванием, которое имеет фокус, генерированный в центральной нервной системе, такой как мозг или спинной мозг, и вызывает различные неврологические симптомы (такие как нарушения зрения, дискинезия, гипестезия, дизестезия, боль, нарушение равновесия, дрожание, дизурия, сексуальные дисфункции, усталость и эмоциональные расстройства). РС поделен, в зависимости от типа прогрессирования состояния пациента, на "возвратно-ремиттирующий тип", где возврат и ремиссия повторяются, и "хронический прогрессирующий тип", при котором симптомы постепенно ухудшаются. Хронический прогрессирующий тип также поделен на "вторичный прогрессирующий тип", при котором возвратно-ремиттирующий тип РС впоследствии показывает хроническое развитие, и "первичный прогрессирующий тип", при котором выраженный возврат не происходит, но симптом постепенно ухудшается от начальной стадии наступления.
Причины РС в настоящее время не объяснены. Существует доклад о причине РС, заключающейся в том, что Т клетки или макрофаги инфильтруются в нервные ткани и атакуют собственный миелин, покрывающий нейрит нервных клеток пациента в мозге или спинном мозге, и в результате воспаление вызывается в миелине и, следовательно, возникает демиелинирование, которое приводит к РС (не патентный документ 2).
Терапевтический метод для РС поделен на три категории, то есть ингибирование воспаления в острый период, ингибирование развития и облегчение симптомов.
При лечении в остром периоде, глюкокортикоид (стероидное противовоспалительное средство) применяют для ингибирования воспаления места, в котором поврежден миелин. РС является заболеванием, которое трудно восстановить полностью из-за постоянного чередования возврата и ремиссии. Были изучены различные иммунологические методы лечения на основе патогенетического механизма РС (не патентный документ 2), и полагают, что интерферон β и иммунодепрессивные агенты являются эффективными. Однако достаточно эффективный и безопасный метод не установлен. В частности, желателен превосходный терапевтический метод для РС во время возврата.
МИФ является цитокином, секретированным из активированных лимфоцитов и имеющим различную биологическую активность. Известно, что его активность направлена на, например, иммунную систему, эндокринную систему и пролиферацию или дифференциацию клеток. В частности, МИФ играет значительную роль в системном воспалении и иммунной реакции и является фактором, также имеющим отношение к отложенной реакции гиперчувствительности для ингибирования произвольной миграции макрофагов. Кроме того, МИФ обладает активностью в отношении допахром таутомеразы (не патентный документ 3).
С другой стороны, известно, что МИФ имеет гомологию с глутатион S-трансферазой, демонстрирует детоксикацию, секретируется из аденогипофиза во время эндотоксического шока, вызывается низким уровнем глюкокортикоида и противопоставляется его иммунодепрессивному действию (не патентный документ 4). Другими словами, МИФ ингибирует активность глюкокортикоида, антагонизирует противовоспалительному действию эндогенного или терапевтически вводимого глюкокортикоида и работает также как причина или усугубляющий фактор воспалительного заболевания и воспалительного состояния.
Кроме того, МИФ незаменим для активации T клеток, экспрессируется в различных клетках и сильно экспрессируется, в частности, в нервной системе.
В отношениях между МИФ и заболеваниями, например, ингибитор МИФ облегчает симптом аллодинии в животной модели НБ. С другой стороны, мышиная модель, показывающая реакцию чувствительности на стимул, обостренную стрессом, может быть получена впрыскиванием рекомбинантного МИФ нормальной мыши (не патентный документ 5). Кроме того, в животной модели для НБ, более конкретно, в модели аллодинии, вызванной лигированием седалищного нерва, МИФ в значительной степени экспрессируется в ипсилатеральном заднем роге спинного мозга, и сигнальные молекулы на низовой стороне от МИФ активируются (не патентный документ 6). Кроме того, у мышей с нокаутированным МИФ аллодиния, вызванная лигированием седалищного нерва, исключается (не патентные документы 5 и 6). Следовательно, подразумевается, что МИФ является нежелательным для экспрессии симптомов НБ.
С другой стороны, у пациента с РС концентрация МИФ в спинномозговой жидкости значительно повышается во время возврата, по сравнению со временем ремиссии (не патентный документ 7). Кроме того, возврат экспериментального аутоиммунного энцефаломиелита (далее обозначенного как ЭАЭ) у мышей, то есть в животной модели РС, может быть предотвращен нокаутированием МИФ генов (не патентный документ 8). Из данных фактов очевидно, что МИФ играет очень значительную роль в образовании НБ и РС.
ЭАЭ, то есть животная модель РС, включает модель для воспроизведения первичного наступления острого периода (монофазного) и модель воспроизведения хронического/повторяющегося состояния, и, в общем, крыс используют в первом случае, и мышей используют во втором случае для построения модели.
Было описано, например, что циклофосфамид иммунодепрессивного средства ингибирует наступление острого ЭАЭ у крыс, но является неэффективным для рецидивирующего типа или хронического прогрессирующего типа ЭАЭ у мышей (не патентный документ 9).
Также было описано, что анти-α4 интегриновое антитело крысы или мыши, эквивалентное терапевтическому средству для РС, натализумабу, замедляет наступление и снижает тяжесть заболевания в отношении острого ЭАЭ у крыс, и ингибирует наступление ЭАЭ у мышей при введении для профилактики ЭАЭ, но симптомы ухудшаются при терапевтическом введении (не патентные документы 10 и 11).
Производное бензопирана оказывает противоревматическое действие (патентный документ 1), ингибирующее действие на производство воспалительных цитокинов, таких как интерлейкин-1β и интерлейкин-6, и иммуномодулирующее действие (не патентные документы 12, 13 и 14), и, как известно, используется для лечения ревматоидного артрита и других артритов и аутоиммунных заболеваний (патентный документ 2). Кроме того, известно, что оно эффективно при остром ЭАЭ у крыс (не патентный документ 15).
Однако, вообще неизвестно, что производное бензопирана связывается с МИФ для ингибирования его биологического действия, как указано выше.
Кроме того, эффективность производного бензопирана в отношении НБ, как указано выше, не известна совсем, и его эффективность в отношении возвратно-ремиттирующего или вторичного прогрессирующего РС во время возврата также совсем не известно.
Документы известного уровня техники
Патентный документ
Патентный документ 1: JP 02-049778 A
Патентный документ 2: международная заявка № WO 94/23714
Не патентный документ
Не патентный документ 1: Lancet, 1999, vol. 353, pp. 1959-1964
Не патентный документ 2: N. Engl. J. Med., 2000, vol. 343, pp. 938-952
Не патентный документ 3: Nat. Rev. Drug Discov., 2006, vol. 5, pp. 399-410
Не патентный документ 4: Molecular Medicine, 1996, vol. 2, pp. 143-149
Не патентный документ 5: Exp. Neurol., 2012, vol. 236, pp. 351-362
Не патентный документ 6: Anesthesiology, 2011, vol. 114, pp. 643-659
Не патентный документ 7: J. Neurol. Sci., 2000, vol. 179, pp. 127-131
Не патентный документ 8: J. Immunol., 2005, vol. 175, pp. 5611-5614
Не патентный документ 9: Clin. Exp. Immunol., 2009, vol. 159, pp.159-168
Не патентный документ 10: J. Pharmacol. Exp. Ther., 2003, vol. 305, pp. 1150-62
Не патентный документ 11: J. Clin. Invest., 2001, vol. 107, pp. 995-1006
Не патентный документ 12: Chem. Pharm. Bull., 2000, vol. 48, pp. 131-139
Не патентный документ 13: J. Pharamcobiodyn., 1992, vol. 15, pp. 649-655
Не патентный документ 14: Int. J. Immunotherapy, 1993, vol. 9, pp. 69-78
Не патентный документ 15: J. Neuroimmunol., 1998, vol. 89, pp. 35-42
Сущность изобретения
Техническая задача
Заявляется лекарственное средство, применяемое для терапевтического или профилактического лечения заболеваний, таких как НБ и РС, и фармацевтическая композиция для ингибирования МИФ, то есть фактора, являющегося значимой причиной этих заболеваний.
В частности, заявляется фармацевтическая композиция, применяемая для терапевтического или профилактического лечения НБ, возвратного РС и подобных.
Решение задачи
В этих условиях, авторы данного изобретения обнаружили, что производное бензопирана, представленное общей формулой [1], или его соль связывается с МИФ, демонстрирует ингибирующее действие на МИФ и, следовательно, применяется для терапевтического или профилактического лечения заболевания, для которого ингибирование МИФ является эффективным, что и составляет данное изобретение:
Формула 1
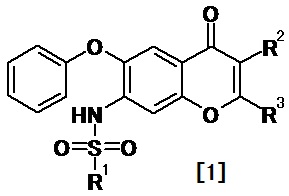 ,
,
где R1 является необязательно замещенной C1-6 алкильной группой; один из R2 и R3 является атомом водорода; и другой из R2 и R3 является атомом водорода, необязательно замещенной аминогруппой, необязательно замещенной ациламиногруппой, необязательно замещенной карбамоильной группой или необязательно замещенной арильной группой.
Преимущества данного изобретения
Производное бензопирана, представленное общей формулой [1], или его соль демонстрирует ингибирующее действие на МИФ и применяется для терапевтического или профилактического лечения заболеваний, для которых ингибирование МИФ является эффективным, таких как НБ и возвратно-ремиттирующий и вторичный прогрессирующий РС во время возврата.
Описание вариантов
Ниже данное изобретение описано более подробно.
Представленные здесь термины имеют следующие значения, если не указано иначе.
Атом галогена означает атом фтора, атом хлора, атом брома или атом йода.
C1-6 алкильная группа означает линейную или разветвленную C1-6 алкильную группу, такую как метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, втор-бутильную группу, изобутильную группу, трет-бутильную группу, пентильную группу, изопентильную группу и гексильную группу.
C1-6 алкоксигруппа означает линейную или разветвленную C1-6 алкилоксигруппу, такую как метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу, пентилоксигруппу и гексилоксигруппу.
C2-12 алканоильная группа означает линейную или разветвленную C2-12 алканоильную группу, такую как ацетильную группу, пропионильную группу, валерильную группу, изовалерильную группу и пивалоильную группу.
Ароильная группа означает бензаильную группу или нафтоильную группу.
Гетероциклическая группа означает никотиноильную группу, теноильную группу, пирролизинокарбонильную группу или фуроильную группу.
(α-Замещенная) аминоацетильная группа означает (α-замещенную) аминоацетильную группу, которая получена из аминокислоты (такой как глицин, аланин, валин, лейцин, изолейцин, серин, треонин, цистеин, метионин, аспарагиновая кислота, глутаминовая кислота, аспарагин, глутамин, аргинин, лизин, гистидин, гидроксилизин, фенилаланин, тирозин, триптофан, пролин и гидроксипролин) и которая может иметь защищенное N-окончание.
Ацильная группа означает формильную группу, сукцинильную группу, глутарильную группу, малеоильную группу, фталоильную группу, C2-12 алканоильную группу, ароильную группу, гетероциклическую карбонильную группу или (α-замещенную) аминоацетильную группу.
Ациламиногруппа означает аминогруппу, замещенную ацильной группой.
Арильная группа означает фенильную группу, нафтильную группу, инданильную группу инденильную группу, тетрагидронафтильную группу или подобные.
C1-6 алкильная группа из R1 может быть замещена одним или более атомами галогена.
Аминогруппа или карбамоильная группа из R2 и R3 могут быть замещена одной или более C1-6 алкильными группами.
Ациламиногруппа из R2 и R3 может быть замещена одним или более атомами галогена.
Арильная группа из R2 и R3 может быть замещена одной или более группами, выбранными из атома галогена, аминогруппы, гидроксильной группы, C1-6 алкильной группы, которая может быть замещена одним или более атомами галогена, и C1-6 алкоксигруппы, которая может быть замещена одним или более атомами галогена.
Предпочтительные примеры производных бензопирана, представленных общей формулой [1] в соответствии с данным изобретением, включают соединения, описанные ниже.
Соединение, в котором R1 является необязательно замещенной C1-6 алкильной группой; один из R2 и R3 является атомом водорода и другой из R2 и R3 является необязательно замещенной ациламиногруппой, является предпочтительным.
Более конкретно, предпочтительными являются N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]формамид, N-(3-амино-4-оксо-6-фенокси-4H-1-бензопиран-7-ил)метансульфонамид, N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]ацетамид, N-(4-оксо-6-фенокси-4H-1-бензопиран-7-ил)метансульфонамид, 7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-2-карбоксамид, N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-2-ил]ацетамид, 7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-карбоксамид, N-[7-[(этилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]формамид и N-(4-оксо-6-фенокси-2-фенил-4H-1-бензопиран-7-ил)метансульфонамид, и более предпочтительным является N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]формамид.
Производное бензопирана общей формулы [1], применяемое в соответствии с данным изобретением, получают сочетанием объединением общепризнанных методов, и оно может быть получено, например, методом, описанным в патентном документе 1.
Примеры соли производного бензопирана общей формулы [1] включают соль со щелочным металлом, таким как натрий или калий; соль с щелочноземельным металлом, таким как кальций и магний; аммониевая соль; и соль с азотсодержащим органическим основанием, таким как триметиламин, триэтиламин, трибутиламин, пиридин, N,N-диметиланилин, N-метилпиперидин, N-метилморфолин, диэтиламин, дициклогексиламин, прокаин, дибензиламин, N-бензил-β-фенилэтиламин, 1-эфенамин и N,N'-дибензилэтилендиамин.
Среди указанных выше солей предпочтительны фармакологически приемлемые соли.
МИФ имеет высокую гомологию с бактериальной таутомеразой и катализирует реакцию допахромтаутомеразы (Molecular Medicine, 1996, vol. 2, pp. 143-149). Поэтому биологическое действие МИФ может быть оценено с применением реакции таутомеразы с допахромом в качестве субстрата.
Производное бензопирана общей формулы [1] или его соль в соответствии с данным изобретением может ингибировать активность МИФ таутомеразы (а именно ингибирующее действие на МИФ), и лекарственное средство, содержащее производное бензопирана общей формулы [1], или его соль применяют для терапевтического или профилактического лечения заболеваний, для которых ингибирование МИФ является эффективным.
Примеры заболеваний, для которых ингибирование МИФ является эффективным, включают НБ и возвратно-ремиттирующий и вторичный прогрессирующий РС во время возврата и, предпочтительно, включают НБ.
Примеры НБ включают фибромиалгию, постгерпетическую боль, диабетическую невропатию, боль после повреждения спинного мозга, постинсультную боль, хроническую боль, рефлекторную симпатическую дистрофию, боль в спине, при которых НСПВС недостаточно эффективны, пояснично-крестцовый радикулит, боль в области таза, невралгию тройничного нерва, остеоартритную боль, для которой НСПВС недостаточно эффективны, деафферентационный болевой синдром, боль из-за миозита, боль из-за фасциита и боль из-за серонегативного артрита. Примеры деафферентационного болевого синдрома включают таламическую боль, боль из-за РС, боль после разрыва, фантомные боли конечностей и послеоперационный болевой синдром. Примеры боли из-за серонегативного артрита включают боль из-за расстройства осевого сустава, боль из-за болезни Бехтерева, боль из-за расстройства крестцово-подвздошного сочленения и боли из-за серонегативного спондилоартрита.
Предпочтительные примеры включают фибромиалгию, постгерпетическую боль, диабетическую невропатию, боль в спине, при которых НСПВС недостаточно эффективны, остеоартритную боль, для которой НСПВС недостаточно эффективны, боль из-за миозита, боль из-за фасциита и боль из-за серонегативного артрита, и более предпочтительные примеры включают постгерпетическую боль, диабетическую невропатию, боль в спине, при которых НСПВС недостаточно эффективны, остеоартритную боль, для которой НСПВС недостаточно эффективны, боль из-за миозита, боль из-за фасциита и боль из-за серонегативного артрита.
Возвратно-ремиттирующий РС отличается тем, что он облегчается через несколько недель или несколько месяцев после того, как остро проявившийся неврологический симптом достигает вершины четвертого желудочка мозга, и затем он возвращается с повторением или ухудшением неврологического симптома. За возвратом следует период ремиссии. Возврат происходит каждые несколько месяцев или лет и медленная или постепенная ремиссия повторяется.
Вторичный прогрессирующий РС отличается тем, что состояние ремиссии у пациента, у которого изначально развился возвратно-ремиттирующий РС, постепенно ухудшается, в то время как возврат и ремиссии повторяются.
Примеры симптомов возвратно-ремиттирующего и вторичного прогрессирующего РС во время возврата включают ухудшение зрения, двигательный паралич, сенсорные расстройства, полиопсию, дизурию и дизартрию.
Соединение в соответствии с данным изобретением может быть составлено в фармацевтические композиции, такие как пероральные препараты (включая таблетку, капсулу, порошок, гранулу, тонкоизмельченную гранулу, пилюлю, суспензию, эмульсию, жидкость и сироп), инъекции и глазные капли, смешиванием различных фармацевтических добавок, таких как наполнитель, связующий агент, разрыхлитель, ингибитор разложения, антикомкователь, смазывающий агент, носитель, растворитель, заместитель, агент для регулировки тоничности, солюбилизирующий агент, эмульгатор, суспендирующий агент, загуститель, покрывающий агент, улучшитель абсорбции, улучшитель гелеобразования, усилитель коагулирования, светостабилизатор, консервант, высушивающее вещество, стабилизатор эмульсии, стабилизатор суспензии, стабилизатор дисперсии, ингибитор окрашивания, поглотитель кислорода, антиоксидант, агент, маскирующий вкус, агент, маскирующий запах, краситель, пенообразователь, пеногаситель, успокаивающее средство, антистатик, разбавитель, pH буфер и pH корректор.
Описанные выше различные композиции составлены обычными методами.
Пероральные твердые композиции, такие как таблетки, порошок и гранулы, могут быть составлены обычным методом с применением фармацевтической добавки, например наполнителя, такого как лактоза, сахароза, хлорид натрия, глюкоза, крахмал, карбонат кальция, каолин, кристаллическая целлюлоза, безводный двухосновный фосфат кальция, частично прежелатинизированный крахмал, кукурузный крахмал и альгиновая кислота; связующего агента, такого как простой сироп, раствор глюкозы, раствор крахмала, раствор желатина, поливиниловый спирт, поливиниловый эфир, поливинилпирролидон, карбоксиметилцеллюлоза, шеллак, метилцеллюлоза, этилцеллюлоза, альгинат натрия, аравийская камедь, гидроксипропилметилцеллюлоза и гидроксипропилцеллюлоза; разрыхлитель, такой как сухой крахмал, альгиновая кислота, порошковый агар, крахмал, поперечно-сшитый поливинилпирролидон, поперечно-сшитая карбоксиметилцеллюлоза натрия, карбоксиметилцеллюлоза калия и натриевая соль гликолята крахмала; ингибитор разложения, такой как стеариловый спирт, стеариновая кислота, масло какао и гидрогенизированное масло; антикомкователь, такой как силикат алюминия, гидрофосфат кальция, оксид магния, тальк и кремневый ангидрид; смазывающее вещество, такое как карнаубский воск, легкая безводная кремниевая кислота, силикат алюминия, силикат магния, гидрированное масло, производное растительного гидрированного масла, кунжутное масло, белый пчелиный воск, оксид титана, сухой гель гидроксида алюминия, стеариновая кислота, стеарат кальция, стеарат магния, тальк, гидрофосфат кальция, лаурилсульфат натрия и полиэтиленгликоль; улучшитель абсорбции, такой как соли четвертичного аммония, лаурилсульфат натрия, мочевина и фермент; и носитель, такой как крахмал, лактоза, каолин, бентонит, ангидрид кремниевой кислоты, гидратированный диоксид кремния, алюмометасиликат магния и коллоидная кремниевая кислота.
Таблетка может быть сформирована, при необходимости, в виде таблетки с общим покрытием, такой как таблетка с сахарным покрытием, таблетка с желатиновым покрытием, таблетка с гастросолюбильным покрытием, таблетка с энтеросолюбильным покрытием и таблетка с водорастворимым пленочным покрытием.
Капсулу получают заполнением твердой желатиновой капсулы, мягкой капсулы и подобных любой из указанных выше фармацевтических добавок.
Альтернативно, фармацевтическая добавка, такая как растворитель, расширитель, агент для корректировки тоничности, солюбилизирующий агент, эмульгатор, суспендирующий агент и загуститель, может применяться для получения обычным методом с получением водной или масляной суспензии, раствора, сиропа и эликсира.
Инъекция может быть получена обычным методом с применением фармацевтической добавки, например разбавителя, такого как вода, этиловый спирт, макроголь, пропиленгликоль, лимонная кислота, уксусная кислота, фосфорная кислота, молочная кислота, лактат натрия, серная кислота и гидроксид натрия; буфера рН и регулятора рН, такого как цитрат натрия, ацетат натрия и фосфат натрия; стабилизатора эмульсии, стабилизатора суспензии и стабилизатора дисперсии, таких как пиросульфит натрия, этилендиаминтетрауксусная кислота, тиогликолевая кислота и тиомолочная кислота; агента, регулирующий тоничность, такой как поваренная соль, глюкоза, маннит и глицерин; солюбилизирующего агента, такого как карбоксиметилцеллюлоза натрия, пропиленгликоль, бензоат натрия, бензилбензоат, уретан, этаноламин и глицерин; успокаивающего средства, такого как глюконат кальция, хлорбутанол, глюкоза и бензиловый спирт; и местного анестетика.
Глазные капли могут быть получены обычным методом подходящим смешиванием с консервантом, таким как хлорбутанол, дегидроацетат натрия, хлорид бензалкония, хлорид цетилпиридиния, фенэтиловый спирт, метиловый параоксибензоат и хлорид бензэтония; буфером рН и регулятором рН, таким как бура, борная кислота и дигидрофосфат калия; загустителем, таким как метилцеллюлоза, гидроксиэтилцеллюлоза, карбоксиметилцеллюлоза, гидроксипропилметилцеллюлоза, поливиниловый спирт, карбоксиметилцеллюлоза натрия и хондроитинсульфат; солюбилизирующего агента, такого как полисорбат 80 и отвержденное полиоксиэтиленом касторовое масло 60; стабилизатора эмульсии, стабилизатора суспензии и стабилизатора дисперсии, таких как эдетат натрия и гидросульфит натрия; и агента, регулирующего тоничность, такого как хлорид натрия, хлорид калия и глицерин.
Способ введения композиции особенно не ограничен, и он подходящим образом определяется в соответствии с формой композиции, возрастом, полом и другими состояниями пациента, и степенью симптома пациента.
Доза активного ингредиента в соответствии с данным изобретением подходящим образом выбирается в соответствии с предполагаемым применением, возрастом и полом пациента, формой заболевания и другими состояниями, и обычно он может вводиться в дозе от 0,1 до 500 мг, предпочтительно от 10 до 200 мг в сутки один раз или несколько раз в сутки для взрослого человека.
ПРИМЕРЫ
Далее данное изобретение описано со ссылкой на экспериментальные примеры, и необходимо отметить, что данное изобретение не ограничено этими примерами.
Аббревиатуры, применяемые в соответствующих примерах, имеют следующие значения.
МЭС: 2-(N-морфолино)этансульфоновая кислота
ДМФ: N,N-диметилформамид
ЭДК: гидрохлорид 1-этил-3-(3-диметиламинопропи)карбодиимида
ЭДТК: этилендиаминтетрауксусная кислота
NHS: N-гидроксисукцинимид
ПЛБ: протеолипидный белок
TBST: содержащий Tween 20 трис-буферированный физиологический раствор
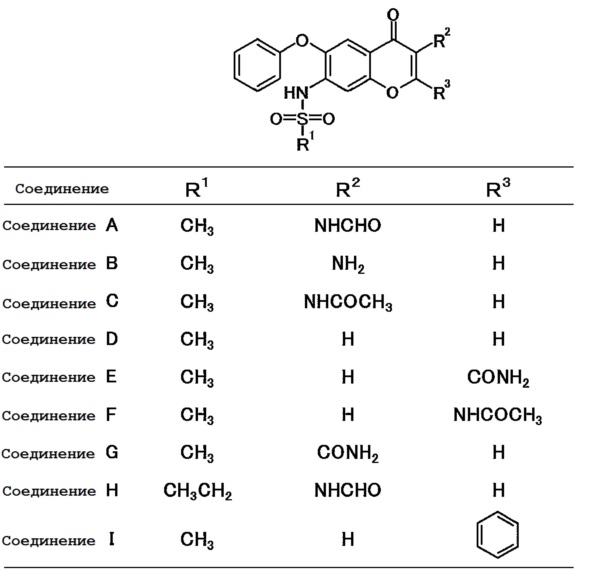
Следующие соединения применяют в качестве тестируемых соединений.
Таблица 1
Экспериментальный пример 1. Подтверждение связывания соединения А и МИФ
В качестве тестируемого вещества применяют соединение A (N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]формамид).
(1) Получение клеточного лизата
Клетки THP-1 культивируют в течение около 6 часов в среде PRMI 1640, содержащей 1% фетальной телячьей сыворотки и 50 мкмоль/л 2-меркаптоэтанола. Затем липополисахарид (E. coli 0127:B8, Sigma Aldrich) добавляют в культуральный планшет в конечной концентрации 1 мкг/мл и клетки культивируют в течение около 30 минут. Клетки собирают и промывают физиологическим раствором с фосфатным буфером и смешивают с около 2-кратным объемом буфера для клеточного лизиса (20 ммоль/л Tris, 150 ммоль/л хлорида натрия, 1 ммоль/л хлорида магния, 0,1% НБ-40, 1 ммоль/л дитиотреитола, 0,1% Triton X-100, pH 7,4). Полученную смесь помещают на лед при периодическом перемешивании в течение около 30 минут и центрифугируют (20000 × g, 4°C, 8 минут). Отделенную и добавленную надосадочную жидкость применяют в качестве клеточного лизата. Концентрацию белка в клеточном лизате измеряют с применением реагента для исследования BCA белка (Thermo Fisher Scientific K.K.) в соответствии с инструкцией по применению.
(2) Синтез гидрохлорида 4-амино-N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]бутанамида
К раствору 500 мг N-(3-амино-4-оксо-6-фенокси-4H-1-бензопиран-7-ил)метансульфонамида в 5,0 мл ДМФ добавляют 293 мг 4-(трет-бутоксикарбониламино)масляной кислоты и 304 мг ЭДК, затем перемешивают при комнатной температуре в течение 1 часа и 30 минут. К полученной реакционной смеси добавляют 111 мг ЭДК, затем перемешивают при комнатной температуре в течение 3 часов и 30 минут. Этилацетат и 10%-ный водный раствор лимонной кислоты добавляют к полученной реакционной смеси, смесь перемешивают при комнатной температуре в течение 30 минут и твердое вещество отфильтровывают. К полученному твердому веществу добавляют ДМФ, этилацетат и 10% водный раствор лимонной кислоты, затем перемешивают при комнатной температуре в течение 1 часа. Затем твердое вещество фильтруют с получением 397 мг трет-бутил [4-[[7-[(метилсульфонил)амино]-4-оксо-6-фонокси-4H-1-бензопиран-3-ил]амино]-4-оксобутил]карбамата в форме бледно-желтого твердого вещества. 300 мг полученного трет-бутил [4-[[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]амино]-4-оксобутил]карбамата суспендируют в 3,0 мл метиленхлорида, туда добавляют 0,60 мл трифторуксусной кислоты при охлаждении на льду, полученную смесь перемешивают при комнатной температуре в течение 40 минут и затем растворитель отгоняют при пониженном давлении. К полученному остатку добавляют 3 мл этилацетата и 0,25 мл 4 моль/л раствора гидрохлорида/этилацетата, и растворитель отгоняют при пониженном давлении. К полученному остатку добавляют 5,0 мл этилацетата и 0,50 мл 4 моль/л раствора гидрохлорида/этилацетата с последующим перемешиванием при комнатной температуре в течение 2 часов. Затем твердое вещество фильтруют с получением 232 мг гидрохлорида 4-амино-N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]бутанамида в виде бледно-желтого твердого вещества.
(3) Получение шариков
Иммобилизацию гидрохлорида 4-амино-N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]бутанамида на Dynabeads M-270 Carboxylic Acid (Life Technologies Corporation) проводят общим методом.
Коротко, после NHS эстерификации концевых COOH около 30 мг шариков (Dynabeads M-270 Carboxylic Acid, Life Technologies Corporation), туда добавляют 0,010 мл ДМФ, 0,90 мл 0,01 моль/л раствора гидрохлорида 4-амино-N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]бутанамида/ДМФ и 0,090 мл 1 моль/л раствора N,N-диизопропилэтиламина/ДМФ, и полученную смесь встряхивают при комнатной температуре в течение 70 минут. Шарики промывают 0,5 мл ДМФ дважды и затем туда добавляют 0,94 мл ДМФ и 0,060 мл 2-аминоэтанола, с последующим встряхиванием при комнатной температуре в течение 2 часов. Шарики промывают 0,5 мл ДМФ дважды и затем промывают 1 мл 0,05 моль/л фосфатным буфером (pH 6) четыре раза, и получают шарики, с которыми связано соединение A через линкер (далее обозначение как шарики с соединением). Кроме того, шарики, полученные похожей реакцией без добавления гидрохлорида 4-амино-N-[7-[(метилсульфонил)амино]-4-оксо-6-фенокси-4H-1-бензопиран-3-ил]бутанамида, используют в качестве контрольных шариков. Каждый тип шариков суспендируют в 1 мл 0,05 моль/л фосфатного буфера (pH 6) и хранят в холодильнике до использования. Непосредственно перед использованием часть шариков отделяют и промывают буфером для клеточного лизиса три раза.
(4) Реакция между клеточным экстрактом и шариками
0,1 мл клеточного лизата (2 мг/мл белка) и около 0,9 мг шариков с соединением или контрольных шариков тщательно смешивают в течение ночи при 4°C. Надосадочные жидкости отделяют от шариков с помощью магнита и собирают как проточную фракцию. Кроме того, шарики промывают буфером для клеточного лизиса и затем подвергают взаимодействию с 40 мкл буфера для клеточного лизиса, содержащего 0,5 ммоль/л соединения A при 4°C в течение около 8 часов при энергичном перемешивании. Надосадочные жидкости отделяют от шариков с помощью магнита и собирают как элюат соединения A. Кроме того, шарики слегка промывают буфером для клеточного лизиса, смешивают с 15 мкл буфера для образца SDS-PAGE (2ME+) (Wako Pure Chemical Industries, Ltd.), который разводят до 4 раз, и нагревают при около 95°C в течение 5 минут. Затем надосадочные жидкости отделяют от шариков с помощью магнита и собирают как элюированную теплом фракцию.
(5) Определение МИФ Вестерн-блоттингом
Вестерн-блоттинг проводят общим методом.
Часть проточной фракции и часть элюата соединения A, полученных как описано выше в (4), соответственно смешивают с буфером для образца SDS-PAGE (2ME+) и нагревают. Эти обработанные теплом образцы и элюированную теплом фракцию подвергают электрофорезу на геле SDS-PAGE (SuperSep Ace 15%, Wako Pure Chemical Industries, Ltd.) при 30-50 мА в течение около 80 минут и затем электрофоретически переносят на PVDF мембрану (Hybond-P, GE Healthcare Japan Corporation) при 100 мА в течение около 60 минут. Перенесенную белком мембрану погружают и осторожно встряхивают в TBST растворе (10 ммоль/л Tris, 100 ммоль/л хлорида натрия, 0,1% Tween-20, pH 7,5), содержащем 5% снятое молоко при комнатной температуре в течение около 1 часа. Затем мембрану погружают в TBST раствор, содержащий 1/50000 объема анти-МИФ антитела (Abcam Plc.) и 5% снятое молоко, и подвергают взаимодействию в течение ночи при 4°C при осторожном перемешивании. После трех легких промываний мембраны TBST раствором полученную мембрану погружают в TBST раствор, содержащий 1/5000 объема HRP-модифицированного козлиного антитела IgG (Santa Cruz Biotechnology Inc.) и 5% снятое молоко, и подвергают взаимодействию при комнатной температуре в течение 1 часа при осторожном перемешивании. После трех легких промываний мембраны TBST раствором, МИФ определяют с применением реагента ECL Prime (GE Healthcare Japan Corporation) в соответствии с инструкцией по применению.
На Фиг.1 показана фотография мембраны, на которой связывающие реагенты МИФ и антитела определены хемилюминесценцией.
Фракции, подвергнутые электрофорезу в соответствующих дорожках геля, следующие:
Дорожка 1: Проточная фракция шариков с соединением
Дорожка 2: Элюат соединения A шариков с соединением
Дорожка 3: Элюированная теплом фракция шариков с соединением
Дорожка 4: рекомбинантный МИФ (Abcam Plc.)
Дорожка 5: Проточная фракция контрольных шариков
Дорожка 6: Элюат соединения A контрольных шариков
Дорожка 7: Элюированная теплом фракция контрольных шариков
Элюат соединения A шариков с соединением содержит белки, которые обладают связующей способностью с шариками с соединением и могут быть выделены из шариков с соединением в присутствии избыточного количества соединения A. Полоса, определенная в элюате соединения A (т.е. Дорожка 2), оказалась МИФ, так как она связывается с анти-МИФ антителом и находится в положении, соответствующем той же молекулярной массе, что и у рекомбинантного МИФ.
Другими словами, было выявлено, что МИФ обладает связующей способностью с шариками с соединением.
С другой стороны, элюат соединения A контрольных шариков и элюированная теплом фракция контрольных шариков содержат белки, обладающие связующей способностью с контрольными шариками. Так как МИФ не был определен в этих фракциях (а именно Дорожки 6 и 7), было показано, что МИФ не обладает связующей способностью с контрольными шариками.
Следовательно, было доказано, что МИФ специфически связывается с соединением A.
Экспериментальный пример 2. Подтверждение ингибирования активности МИФ.
Соединения A-I применяют в качестве тестируемых соединений.
Ингибирующее действие тестируемых соединений на таутомеразную активность МИФ оценивают методом, описанным у Healy et al. (Cancer Epidemiology Biomarkers and Prevention, 2011, vol. 20, pp. 1516-1523).
В этом методе таутомерную реакцию из метилового эфира L-3,4-дигидроксифенилаланина (метилового эфира L-допахрома, окрашенного) до метилового эфира 5,6-гидроксииндол-2-карбоновой кислоты (бесцветной) измеряют как изменение абсорбции при 475 нм.
В качестве источника фермента применяют рекомбинантный МИФ производства Abcam Plc. или МИФ, полученный и очищенный по методу Lubetsky et al. (The Journal of Biological Chemistry, 2002, vol. 277, pp. 24976-24982). Метод очистки МИФ описан ниже.
Вектор pET15b (Merck), в который вставлена первичная нуклеотидная последовательность гена МИФ, трансфицируют штаммом E. coli BL21 Star (DE3) (Life Technologies Corporation). E. coli культивируют до тех пор, пока культуральная среда не покажет абсорбцию (при 600 нм) от 0,5 до 0,8, туда добавляют изопропил-β-тиогалактопиранозид (Wako Pure Chemical Industries, Ltd.) до конечной концентрации 0,1 ммоль/л, и экспрессию белка вызывают в течение 4 часов. E. coli повторно суспендируют в буфере (pH 7,5), содержащем 20 ммоль/л Tris (Wako Pure Chemical Industries, Ltd.), 20 ммоль/л хлорида натрия (Wako Pure Chemical Industries, Ltd.) и 1 ммоль/л дитиотреитола (Wako Pure Chemical Industries, Ltd.), и полученную смесь подвергают ультразвуковому лизису и центрифугированию при 15000 об/мин в течение 10 минут. Полученную надосадочную жидкость фильтруют с применением 0,20 мкм фильтра и пропускают через колонки HiTrap Q HP и HiTrap SP HP (GE Healthcare Japan Corporation) так, чтобы отделить проточные фракции по 5 мл каждая. Каждые 10 мкл отделенных фракций подвергают электрофорезу с применением 5-20% полиакриламидного геля (Wako Pure Chemical Industries, Ltd.), и все белки окрашивают реагентом кумасси бриллиантовым голубым (Bio-Rad Laboratories, Inc.). На основе полученных результатов фракцию, содержащую наибольшее количество МИФ, и фракцию, содержащую наименьшее количество других белков, выбирают в качестве очищенного МИФ. Концентрацию белка МИФ измеряют с помощью реагента для исследования белка BCA (Thermo Fisher Scientific K. K.).
Ингибирующее действие каждого тестируемого соединения на таутомеразную активность МИФ измеряют следующим образом.
Конечную концентрацию от 10 до 50 нмоль/л МИФ и конечную концентрацию 30 мкмоль/л каждого тестируемого соединения или 0,5% диметилсульфоксида (Wako Pure Chemical Industries, Ltd.) в качестве контроля добавляют в буфер (pH 6,2), содержащий 50 ммоль/л Bis-Tris (Dojindo Laboratories) и 1 ммоль/л ЭДТК (Dojindo Laboratories), и реакцию проводят при комнатной температуре в течение 15 минут с получением реакционного раствора 1.
С другой стороны, 1/20 объема 12 ммоль/л метилового эфира L-3,4-дигидроксифенилаланина (Sigma Aldrich) и 1/20 объема 24 ммоль/л периодата натрия (Wako Pure Chemical Industries, Ltd.) добавляют в буфер, имеющий такой же состав, как у буфера, применяемого для получения реакционного раствора 1, с получением реакционного раствора 2.
Затем реакционный раствор 1 и реакционный раствор 2 смешивают и сразу же измеряют временное изменение абсорбции при 475 нм полученной смеси.
Получают разницу абсорбции в моменты времени около 1 минуты после начала измерения и около 5 минут после начала измерения. Принимая за основу то, что изменение абсорбции контроля составляет 100%, рассчитывают степень ингибирования реакции таутомеразы в присутствии каждого тестируемого вещества.
Результаты показаны в таблице 2. В таблице 2, степень ингибирования реакции таутомеразы показана следующим образом. "-"; менее 50%, "+"; 50% или более и менее 75%, "++"; 75% или более.
Таблица 2
|
Все тестируемые вещества ингибируют таутомеразную активность МИФ.
Описанные выше результаты показали, что соединение общей формулы [1] или его соль демонстрирует ингибирующее действие в отношении МИФ и применяется в качестве ингибитора МИФ.
Экспериментальный пример 3. Действие соединения A на крысиную модель хронического повреждения перетяжкой нерва
Этот тест проводят по методу Bennett et al. (Pain, 1988, vol. 33, pp. 87-107).
Соединение A применяют в качестве тестируемого вещества, и целекоксиб, одно из НСПВС, используют в качестве ссылочного вещества. Соединение A вводят в дозе 30 мг/кг (группа соединения A). Целекоксиб вводят в дозе 30 мг/кг (группа целекоксиба). В контрольной группе вводят 0,5% водный раствор метилцеллюлозы, применяемый в качестве носителя.
Под анестезией Сомнопентилом (производства Kyoritsu Seiyaku Corporation, около 52 мг/кг, внутрибрюшинное введение) проводят операцию перетяжки нерва на левом седалищном нерве самцов крыс Sprague-Dawley (возраст 7 недель). Коротко, левую бедренную область каждой крысы рассекают, седалищный нерв отделяют от окружающих тканей, и нерв плотно перетягивают 4-0 шелковой хирургической нитью (производства Eticon Inc., хирургический шелк) так, чтобы получить узкие части в четырех положениях с интервалом около 1 мм. Мышечный слой и кожу соответственно сшивают, и область операции дезинфицируют. Носитель, тестируемое вещество или ссылочное вещество вводят перорально один раз в сутки непрерывно в течение 14 дней, начиная с 16 дня после операции.
С начала введения чувство боли (механическую аллодинию) подушечки стопы левой задней лапы оценивают с помощью теста фон Фрея. Коротко, нити фон Фрея, соответственно имеющие различную гибкость (Semmes-Weinstein Von Frey Anesthesiometer (производства Danmic Global, LCC)), вертикально прижимают к подушечке стопы левой задней лапы последовательно, начиная с нити с минимальной эластичностью, и силу упругости нити, к которой крыса показывает реакцию отдергивания, определяют как значение болевого порога.
Оценку чувства боли выражают как среднее значение болевого порога. Результаты показаны в таблице 3.
Таблица 3
|
Значение болевого порога группы соединения A повышается до 13,5 г через 14 дней после начала введения (на 30-й день после операции) и, таким образом, соединение A ингибирует симптом механической аллодинии по сравнению с контрольной группой.
С другой стороны, введение целекоксиба (30 мг/кг), НСПВС, не подавляет симптом механической аллодинии.
Описанные выше результаты показывают, что соединение A подавляет симптом механической аллодинии через механизм, отличный от механизма действия НСПВС.
Экспериментальный пример 4. Действие на модель хронического рецидивирующего ЭАЭ у мышей.
Соединение A выбирают в качестве тестируемого соединения, и салазосульфапиридин (далее обозначенный как САСП) выбирают в качестве сравнительного контрольного агента. Соединение A вводят в дозе 30 мг/кг (группа соединения A). САСП вводят в дозе 300 мг/кг (группа САСП). В контрольной группе и нормальной группе (группа не индукционного лечения) вводят 0,5% водный раствор метилцеллюлозы, применяемый в качестве носителя для введения жидкости.
Хронический рецидивирующий ЭАЭ вызывают у самок мышей SJL/J иммунизацией частичным ПЛБ пептидом. Коротко, эмульсию готовят смешиванием эквивалентных объемов физиологического раствора с фосфатным буфером, содержащего 1 мг/мл пептида, соответствующего остаткам 139-151 ПЛБ, и неполного адъюванта Фрейнда, содержащего 4 мг/мл убитых M. Tuberculosis H37Ra. Эмульсию вводят чрескожно (50 мкг ПЛБ на мышь) в четыре точки спины для иммунизации, и дополнительно в день иммунизации и через два дня после, коклюшный токсин вводят внутрибрюшинно в каждом количестве 150 нг на мышь, всего два раза. Носитель, тестируемое вещество или ссылочное вещество вводят перорально непрерывно в течение 44 дней один раз в сутки, начиная со дня иммунизации.
В данном эксперименте, развивающийся паралич достигает пика на 14-16 день после иммунизации, и симптом ослабевает один раз, но возвращается до пикового значения на 38 день.
Симптом оценивают в соответствии с докладом Weaver et al. (FASEB Journal, 2005, vol. 19, p. 1668). Коротко, паралич всех четырех конечностей и хвоста оценивают по шкале, включающей 4 уровня оценки, от 0 до 3, и 3 уровня оценки, от 0 до 2, соответственно, и сумму оценок определяют как оценку ЭАЭ (максимальная оценка 14).
Коэффициент заболеваемости (количество мышей, у которых развилось заболевание/количество использованных мышей) и среднюю оценку ЭАЭ для каждой группы измеряют в течение периода времени от изначального наступления (на 15-й день после иммунизации) до рецидива (на 38-й день после иммунизации). Результаты показаны в таблице 4.
Таблица 4
|
В группе соединения A коэффициент заболеваемости был низким как в период изначального наступления, так и в период рецидива, и оценка ЭАЭ также была низкой.
С другой стороны, в группе САСП ни коэффициент заболеваемости, ни оценка ЭАЭ не были снижены.
Описанные выше результаты показали, что соединение A подавляет наступление паралича при хроническом рецидивирующем ЭАЭ. Действие соединения A, очевидно, отличается от действия САСП, несмотря на то что оба эти лекарственных средства относятся к категории иммуномодуляторов.
Описанные выше результаты показывают, что соединение общей формулы [1] или его соль может применяться в качестве ингибитора МИФ, а также может применяться для терапевтического или профилактического лечения болезни, для которой ингибирование МИФ является эффективным, такой как НБ и период рецидива возвратно-ремиттирующего и вторичного прогрессирующего РС.
Краткое описание рисунков
На Фиг.1 представлена фотография мембраны, на которой связывающие реагенты МИФ и антитела определены хемилюминесценцией.
Промышленная применимость
Производное бензопирана, представленное общей формулой [1], или его соль связывается с МИФ, обладает ингибирующим действием на МИФ и применяется для терапевтического или профилактического лечения заболевания, для которого ингибирование МИФ является эффективным.