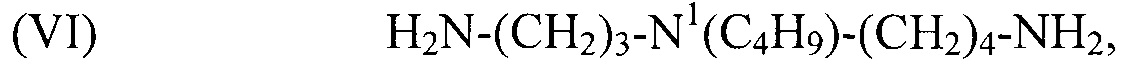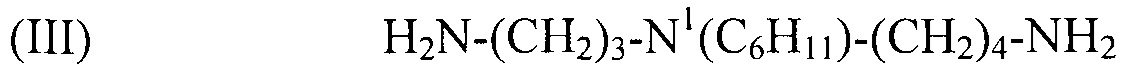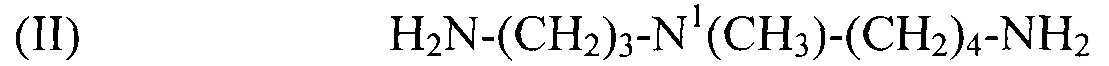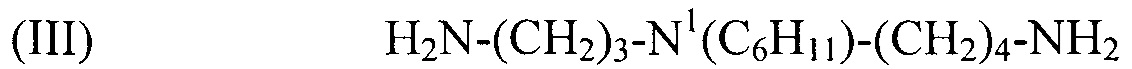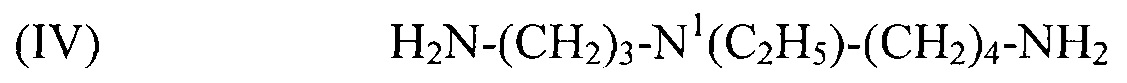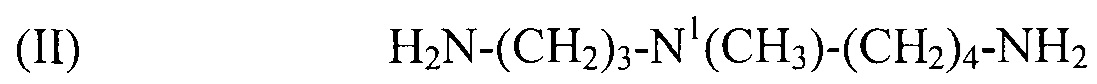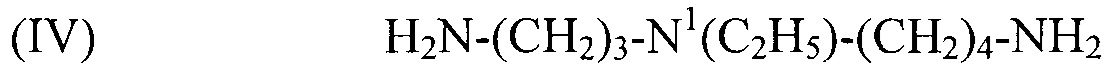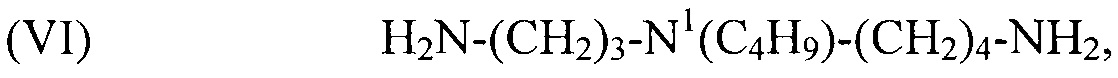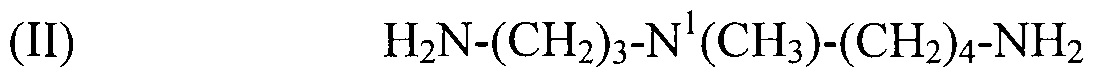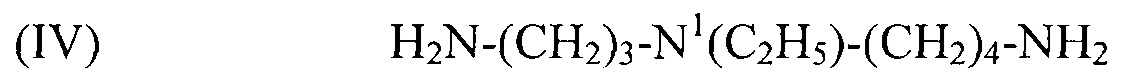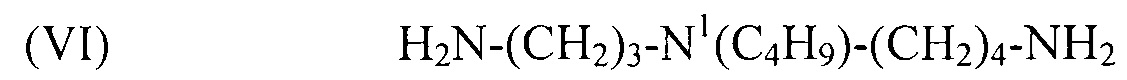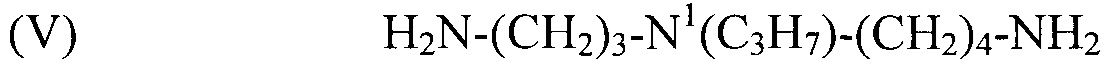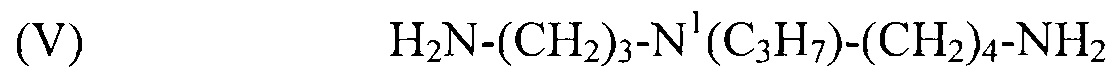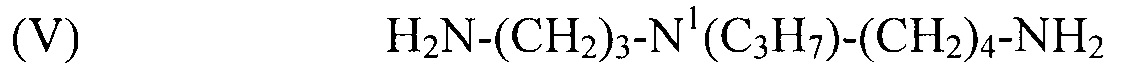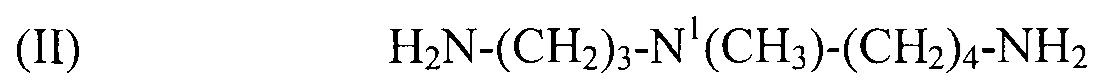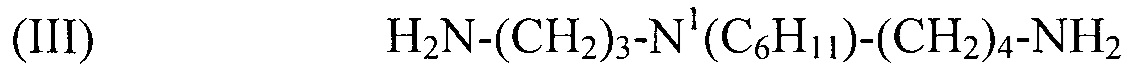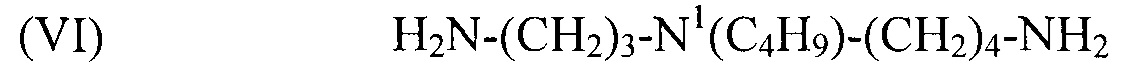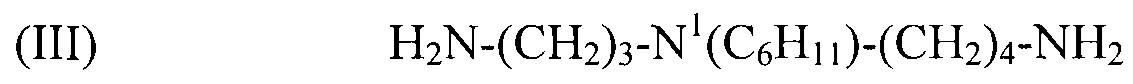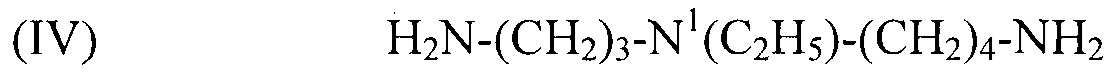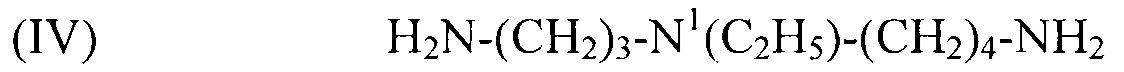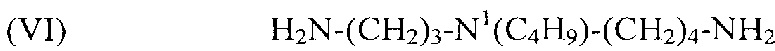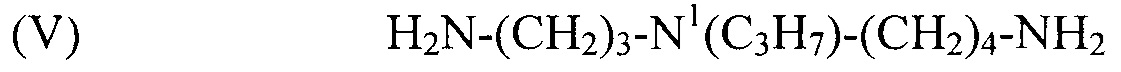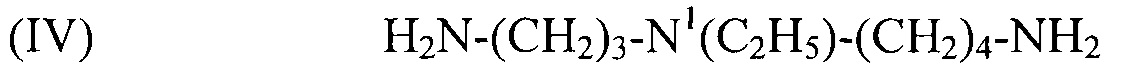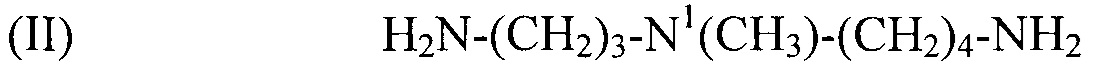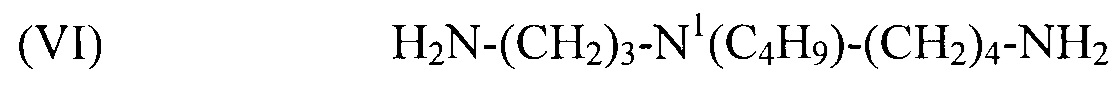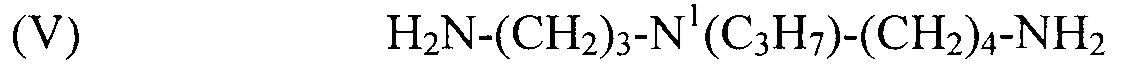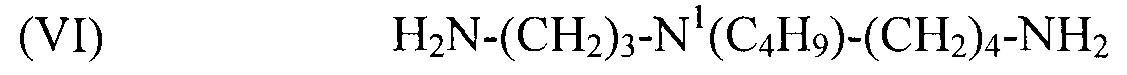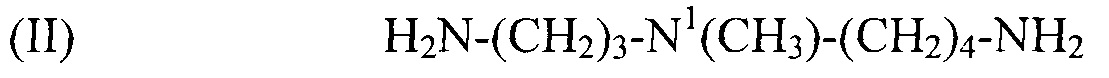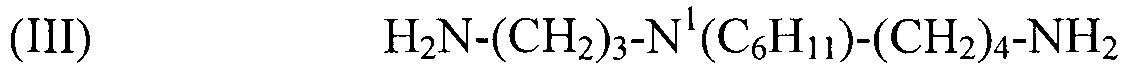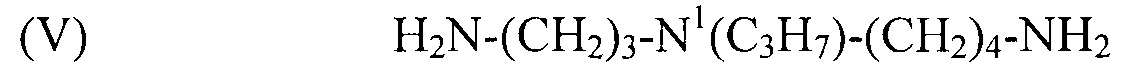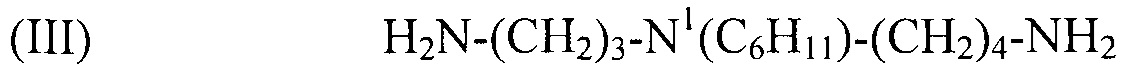Результат интеллектуальной деятельности: ФАРМАЦЕВТИЧЕСКАЯ ИЛИ КОСМЕТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ АЛОПЕЦИИ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Настоящее изобретение относится к фармацевтической или косметической композиции для лечения алопеции и в целом для борьбы с чрезмерным выпадением волос.
Уровень техники
Волосяной фолликул (HF) является одним из самых сложных мини-органов в теле человека, способным к регенерации. Цикл роста волос в послеродовой жизни описывает морфогистологические изменения волосяного стержня и фолликул во времени. Циклическая активность начинается с продуцирования волос с последующим быстрым ростом и удлинением волосяного стержня (фаза анагена). Фолликул и волос затем проходят регрессию, вызванную апоптозом (фаза катагена), затем фазу покоя (телоген) и, наконец, стадию выпадения волос (exogen).
Эти превращения включают быстрое ремоделирование эпителия и кожных компонентов на основе изменений в экспрессии и/или активности цитокинов, гормонов, ферментов, нейромедиаторов и их родственных рецепторов и транскрипционных факторов, которые признаны в качестве ключевых медиаторов цикла роста волос.
Все волосы на теле подчиняются аналогичным жизненным циклам, хотя рост, длительность фаз и длина волосяного стержня варьируются в зависимости от различных областей тела и между индивидуами в зависимости от их генетических факторов, возраста и состояния здоровья. Кроме того, многие регуляторы участвуют в биологии волос, влияя на морфогенез и регулируя инициирование фазы анагена и длительность.
Существуют различные гормоны, участвующие в регуляции цикла роста волос, включающие мелатонин, пролактин, меланоцитстимулирующий гормон (MSH), гормон щитовидной железы и эстроген. Например, было установлено, что пролактин участвует в регуляции роста волос у мышей и человека.
Многие из этих регуляторов могут быть объектом клинических процедур. Например, за исключением фолликулов лобка и подмышек, андрогенам требуется фермент 5а-редуктаза, который способен метаболизировать тестостерон в 5а-дигидротестостерон (DHT), более активный метаболит. Это фактический механизм, используемый как в клинической, так и косметической области борьбы с выпадением волос в случаях андрогенной алопеции.
В отличие от выпадения волос, чрезмерный рост волос может быть проблемой, особенно для женщин. В отличие от андрогенной алопеции, гирсутизм и гипертрихоз является результатом увеличенной фазы анагена, сопровождающейся патологическим ростом волосяных фолликулов.
Обычное лечение для борьбы с этим состоянием состоит в использовании крема и восков для удаления волос, которые только временно облегчают проблему, так как раздражение или разрыв быстро индуцирует фазу анагена волосяного фолликула и отрастание. Другими применяемыми системами являются электролиз и селективный фототермолиз, с использованием лазеров для разрушения волосяного стержня и дермального гребня волосяных фолликулов. Последние имеющиеся методики лечения являются очень агрессивными.
Для решения этих проблем необходимы новые и более эффективные способы. В последние десятилетия особый научный интерес направлен на роль орнитиндекарбоксилазы (ODC) и полиаминов в цикле роста волос. Этот интерес в первую очередь вызван тем, что фолликул является одним из наиболее пролиферативных органов. ODC, скорость определяющий фермент в биосинтезе полиаминов, является мишенью для ингибирующих препаратов (таких как эфлорнитин), что приводит к уменьшению скорости роста волос на лице in vivo и ингибированию роста волос человека в органной культуре.
Для клинических целей, для регулирования продуцируемого количества волос, одна стратегия состоит в изменении длительности анагена, сокращая его в случаях гирсутизма или увеличивая его в борьбе с алопецией. В целом, патология человеческого фолликула, такая как гирсутизм, седые волосы и алопеция имеют значительные негативные последствия для психики и самооценки больных.
В ЕР 1469843 того же заявителя описана композиция для фармацевтического, косметического или диетического применения для борьбы с потерей волос, в которой активным ингредиентом является полиамин, известный как спермидин или N'-(3-аминопропил)-1,4-диаминобутан, для перорального применения и для местного применения на коже головы. Формулой спермидина является: H2N-(CH2)3-NH-(CH2)4-NH2.
Этот патент представляет экспериментальные доказательства того, что композиция, содержащая спермидин, и отдельно спермидин и в сочетании с другими микробиогенными добавками может замедлить и остановить чрезмерное выпадение волос и в то же время повысить резистентность и общее состояние здоровья волос. Испытание на растяжение показали, что спермидин увеличивает предел прочности при растяжении волос, при этом трихограмма и промывочный тест показали улучшения, которые происходят в волосяной луковице. В дополнение к значительному уменьшению количества потерянных после мытья волос, количество потерянных волос в фазе телогена (патологическая потеря) также снижается по отношению к количеству волос, потерянных в фазе exogen (потеря для естественной замены). Лечение спермидином, таким образом, существенно улучшает цикл роста волос, нарушенный при болезни выпадения волос в фазе телогена, что приводит к нормальным физиологическим уровням. Поэтому спермидин является эффективным активным ингредиентом для борьбы с алопецией.
Однако спермидин, как и другие полиамины, подвержен окислению, особенно в случае местного применения на коже головы, при котором соединение остается в длительном контакте с воздухом в течение некоторого времени, прежде чем поглощается кожей и осуществляет свое действие. Любое окисление спермидина в течение этого времени до поглощения приведет к продуктам окисления, которые больше не являются активными, если не потенциально вредными.
Настоящее изобретение, прежде всего, направлено на нахождение решения этой проблемы. Теоретически, возможная химическая защита окисляющейся функциональной аминогруппы не появляется в целом пригодной на практике, особенно в свете известного уровня техники, кратко сформулированного следующими патентами.
WO 9937277 описывает замещенные полиамины для уменьшения роста волос у млекопитающих, выбором области кожи, где этот эффект должен быть получен, и нанесением на этом участке кожи дерматологически приемлемой композиции, включающей замещенный полиамин в качестве ингибитора биосинтеза гипузина, в количестве, которое эффективно снижает рост волос. Нежелательный рост волос у млекопитающих, включая человека, в частности, рост волос, стимулируемый андрогенами, таким образом может быть уменьшен или в случае нормального роста или аналогично в случаях увеличения в результате аномалий или расстройств (например, гирсутизм).
WO 02062341 относится к фармацевтической композиции, пригодной для местного применения человеком или другими млекопитающими, для борьбы с ростом волос в области, в которой он применяется, содержащей эффективное количество замещенного полиамина или его соли. В этом случае описан механизм ингибирования ODC (орнитин-декарбоксилаза) полиамином, который необратимо связывается с ODC присутствующим в клетке так, чтобы защитить ODC от катализа декарбоксилирования орнитина до путресцина. Согласно этому патенту, рост волос человека и отличных от человека млекопитающих можно регулировать применением определенных замещенных полиаминов, которые в основном предотвращают образование ODC в клетках, которыми они поглощаются. Таким образом, вместо того, чтобы действовать как настоящие ингибиторы ODC, считается, что указанные замещенные полиамины предотвращают синтез ODC. Экспериментальные примеры в данном документе, показывают, что применяемый полиамин, в этом случае диэтил-гомоспермидин, останавливает отрастание бритых волос у мышей.
Раскрытие изобретения
В любом случае, независимо от биологического механизма конечного эффекта предотвращения роста волос, известный уровень техники очевидно не предлагает в качестве гипотетического практического решения, в виде замещения спермидина функциональными группами так, чтобы получить противоположный эффект стимулирования роста в области применения на коже волосистой части головы, что является целью настоящего изобретения.
В то же время, другой целью настоящего изобретения является создание соединений, которые могут быть, по меньшей мере, в части некоторых свойств, даже более активными, чем спермидин в борьбе с потерей волос.
Осуществление изобретения
Вопреки тому, что можно предположить на основе известного уровня техники, кратко представленного выше, в соответствии с настоящим изобретением неожиданно было установлено, что следующие соединения формулы (I), R-N1-спермидин или N-(3-аминопропил)-N1-R-1,4-бутандиамин,
(I) H2N-(CH2)3-N1(R)-(CH2)4-NH2,
где R является заместителем, связанным с вторичной аминогруппой спермидина, выбранным из:
- насыщенной или ненасыщенной, линейной или разветвленной алкильной группы, состоящей из 1-6 атомов углерода, в которой необязательно один или несколько атомов углерода замещены фтором, такой как метил, этил, трифторметил, трифторэтил, пропил, изопропил, бутил, изобутил, пентил, гексил, этилен, винил, пропилен, бутилен;
- арильных или арилалкильных групп, таких как фенил, нафтил, бензил, толил, в которых необязательно один или несколько атомов углерода замещены фтором и в которых указанные арилалкильные группы включают насыщенные или ненасыщенные, линейные или разветвленные алкильные группы, состоящие из 1-6 атомов углерода, в которых необязательно один или несколько атомов углерода замещены фтором, такие как метил, этил, трифторметил, трифторэтил, пропил, изопропил, бутил, изобутил, пентил, гексил, этилен, винил, пропилен, бутилен;
- насыщенных или ненасыщенных циклоалкильных групп, включающих 3-8 атомов углерода, необязательно замещенных насыщенной или ненасыщенной, линейной или разветвленной алкильной группой, включающей 1-6 атомов углерода, в которой необязательно один или несколько атомов углерода замещены фтором, такой как метил, этил, трифторметил, трифторэтил, пропил, изопропил, бутил, изобутил, пентил, гексил, этилен, винил, пропилен, бутилен;
- или его фармацевтически приемлемой соли,
обладают активностью против потери волос по существу сопоставимой со спермидином, но без проблемы окисления в присутствии воздуха при местном применении на коже головы. Действительно, они настолько стабильны по отношению к воздуху, что позволяют эффективно применять для местного нанесения на кожу головы без превращения в окисленные побочные продукты, которые являются неактивными или неактивны для целей настоящего изобретения.
В частности, также неожиданно эти соединения по настоящему изобретению оказываются более активными, чем спермидин в борьбе с алопецией, по меньшей мере, относительно конкретных свойств, как описано выше.
Таким образом, настоящее изобретение относится к применению этих R-N1-спермидиновых соединений (I) для борьбы с потерей волос и к композициям для фармацевтического или косметического применения, которые включают их в качестве активных ингредиентов.
Предпочтительным соединением формулы (I) по настоящему изобретению является N1-метилспермидин, или N-(3-аминопропил)-N1-метил-1,4-бутандиамин (Регистрационный номер CAS 51460-23-2), формулы:
(II) H2N-(CH2)3-N1(CH3)-(CH2)4-NH2,
используемый в композиции по изобретению как таковой или в виде фармацевтически приемлемой соли, например тригидрохлорида (3HCl) или трималеата. Другим предпочтительным соединением формулы (I) в соответствии с настоящим изобретением является N1-циклогексилспермидин, или N-(3-аминопропил)-N1-циклогексил-1,4-бутандиамин (CAS регистрационный номер 183070-28-2), формулы:
(III) H2N-(CH2)3-N1(C6H11)-(CH2)4-NH2,
используемый в композиции по изобретению как таковой или в виде фармацевтически приемлемой соли, например тригидрохлорида (3HCl) или трималеата. Другим предпочтительным соединением формулы (I) в соответствии с настоящим изобретением является N1-этилспермидин, или N-(3-аминопропил)-N1-этил-1,4-бутандиамин (Регистрационный номер CAS 97141-36-1), формулы:
(IV) H2N-(CH2)3-N1(C2H5)-(CH2)4-NH2,
используемый в композиции по изобретению как таковой или в виде фармацевтически приемлемой соли, например тригидрохлорида (3HCl) или трималеата. Другим предпочтительным соединением формулы (I) в соответствии с настоящим изобретением является N1-пропилспермидин, или N-(3-аминопропил)-N1-пропил-1,4-бутандиамин (Регистрационный номер С AS 62659-14-7), формулы:
(V) H2N-(CH2)3-N1(C3H7)-(CH2)4-NH2,
используемый в композиции по изобретению как таковой или в виде фармацевтически приемлемой соли, например тригидрохлорида (3HCl) или трималеата. Другим предпочтительным соединением формулы (I) в соответствии с настоящим изобретением является N1-изобутилспермидин, или N-(3-аминопропил)-N1-изобутил-1,4-бутандиамин, формулы:
(VI) H2N-(CH2)3-N1(C4H9)-(CH2)4-NH2,
используемый в композиции по изобретению как таковой или в виде фармацевтически приемлемой соли, например тригидрохлорида (3HCl) или трималеата. Это соединение (VI) не описано в литературе. Поэтому способ синтеза описан ниже со ссылкой на следующую схему реакции, в которой соединение (VI) выделяют как соединение 4.
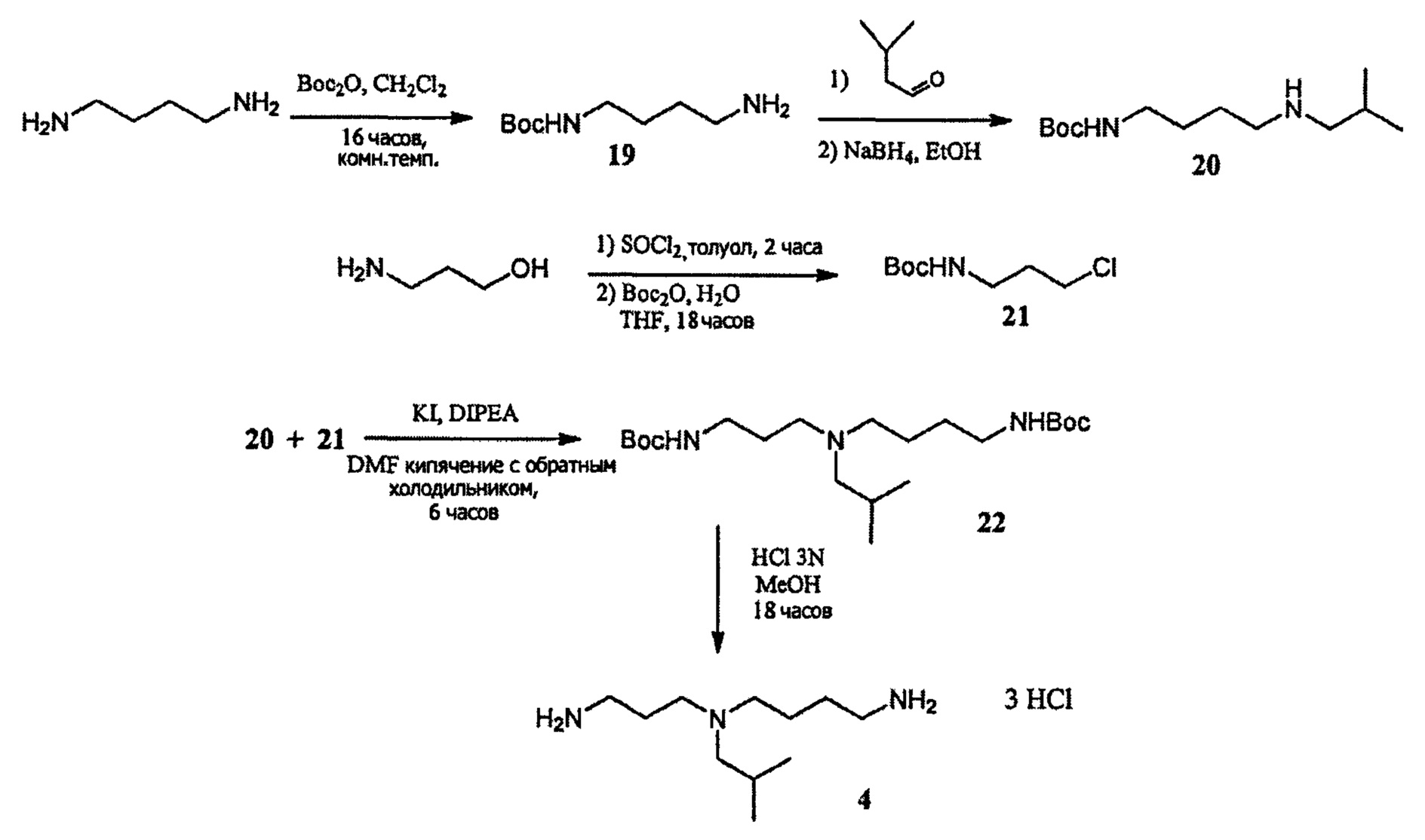
Синтез соединения 19: бутандиамин (1 г, 0,0113 моля, 5 экв.) растворяют в CH2Cl2 (15 мл). К раствору добавляют Boc2O (ди-третбутилдикарбонат) (0,619 г, 0,00283 моля, 1 экв.) растворенный в CH2Cl2 (15 мл). Реакционную смесь оставляют перемешиваться при комнатной температуре в течение 16 часов. Структуру продукта оценивают с помощью ТСХ CH2Cl2 8/МеОН 1/NH4OHводн. 33% 0,2. Полученную суспензию фильтруют и фильтрат сушат с помощью роторного испарителя. Маслянистый остаток элюируют EtOAc (15 мл) и промывают насыщенным раствором NaCl (3×10 мл), чтобы удалить избыток непрореагировавшего диамина. Органические экстракты сушат над сульфатом натрия и упаривают. Получают 0,520 г желтого масла. Выход 97,65%. 1Н-ЯМР (400 МГц, CDCl3) δ 1,38 (с, 9Н), 1,52-1,59 (ср, 4Н), 2,34 (шс, 2Н, D2O обм.), 2,72-2,79 (ср, 2Н), 3.19-3.24 (ср, 2Н), 5,95 (шс, Ш, D2O обм.).
Синтез соединения 20: вышеуказанное соединение 19 (0,358 г, 0,00190 моля, 1 экв.) растворяют в EtOH (5 мл). К раствору добавляют молекулярные сита 3А и изобутиральдегид (0,137 г, 0,00190 моля, 0,17 мл, 1 экв.). Реакционную смесь перемешивают при комнатной температуре в течение 18 часов. Добавляют NaBH4 (0,144 г, 0,0038 моля, 2 экв.) и смесь перемешивают при комнатной температуре в течение 16 ч. Структуру продукта оценивают с помощью ТСХ CH2Cl2 9/МеОН 1/NН4OНводн. 33% 0,1. Растворитель выпаривают и маслянистый остаток элюируют CH2Cl2 (10 мл) и промывают насыщенным раствором NaCl (5 мл). Органические экстракты сушат над сульфатом натрия и упаривают и полученный остаток очищали с помощью флэш-хроматографии с использованием смеси CH2Cl2 9/МеОН 1/NH4OНводн. 33% 0,1 в качестве фазы элюента. Получают 0,215 мг бесцветного масла. Выход 46,33% 1Н-ЯМР (400 МГц, CDCl3) δ 0,88 (д, 6Н, J=6,8 Гц), 1,41 (с, 9Н), 1.49-1.52 (ср, 4Н), 1,72-1,75 (ср, 1Н), 2,38 (д, 2Н, J=7,2 Гц), 2,59 (т, 2Н, J=6,6 Гц), 3,07-3,09 (ср, 2Н), 4,95 (шс, 1H, D2O обм.).
Синтез соединения 21: аминопропанол (0,49 г, 0,51 мл, 0,00652 моля, 1 экв.) растворяют в толуоле (5 мл). К раствору добавляют SOCl2 (3,10 г, 1,90 мл, 0,00261 моля, 4 экв.) в бане со льдом. Реакционную смесь перемешивают при кипячении с обратным холодильником в течение 2 часов. Структуру продукта оценивают с помощью ТСХ CH2Cl2 9/МеОН 1/NH4OНводн. 33% 0,1. Растворитель выпаривают и маслянистый остаток элюируют H2O (10 мл) и промывают CH2Cl2 (5 мл). Водную фазу используют без дальнейшей очистки на следующей стадии, Net3 (0,659 мг, 0,9 мл, 0,00652 моля, 1 экв.) добавляют к раствору и смесь перемешивают при комнатной температуре в течение 30 минут. Добавляют раствор Boc2O (1,42 г, 0,00652 моля, 1 экв.) в ТГФ (10 мл). Реакционную смесь перемешивают при комнатной температуре в течение 18 часов. Исчезновение исходного продукта оценивают с помощью ТСХ петролейный эфир 8/EtOAc 2. Растворители выпаривают и остаток элюируют EtOAc и промывают H2O. Органические экстракты сушат над сульфатом натрия и упаривают. Получают 1,23 г коричневого масла. Выход 97,70% 1Н-ЯМР (400 МГц, CDCl3) δ 1,43 (с, 9Н), 1,94-1,97 (ср, 2Н), 3,26 (т, 2Н, J=6,4 Гц), 3,58 (т, 2Н, J=6,4), 4,75 (шс, 1H, D2O обм.).
Синтез соединения 22: вышеуказанное соединение 20 (0,120 г, 0,00049 моля, 1 экв.) растворяют в ДМФА (3 мл). К раствору добавляют вышеуказанное соединение 21 (0,104 г, 0,00054 моля, 1,1 экв.) растворяют в ДМФА (2 мл). Реакционную смесь перемешивают с обратным холодильником в течение 6 часов. Структуру продукта оценивают с помощью ТСХ CH2Cl2 9/МеОН 1/NH4OНводн. 33% 0,03. Растворитель выпаривают и маслянистый остаток очищают флэш-хроматографией с использованием смеси CH2Cl2 9/МеОН 1/NH4OHводн. 33% 0,03 в качестве фазы элюента. Получают 0,084 мг желтого масла. Выход 42,71%. 1Н-ЯМР (400 МГц, CDCl3) δ 0,87 (д, 6Н, J=6,8 Гц), 1,43 (с, 18Н), 1,57-1,61 (ср, 7Н), 1,98-2,01 (ср, 2Н), 2,31-2,35 (ср, 2Н), 2,38-2,42 (ср, 2Н), 3,10-3,12 (ср, 2Н), 3,16-3,18 (ср, 2Н), 4,72 (шс, 1Н, обм D2O), 5,69 (шс, 1Н, D2O обм.).
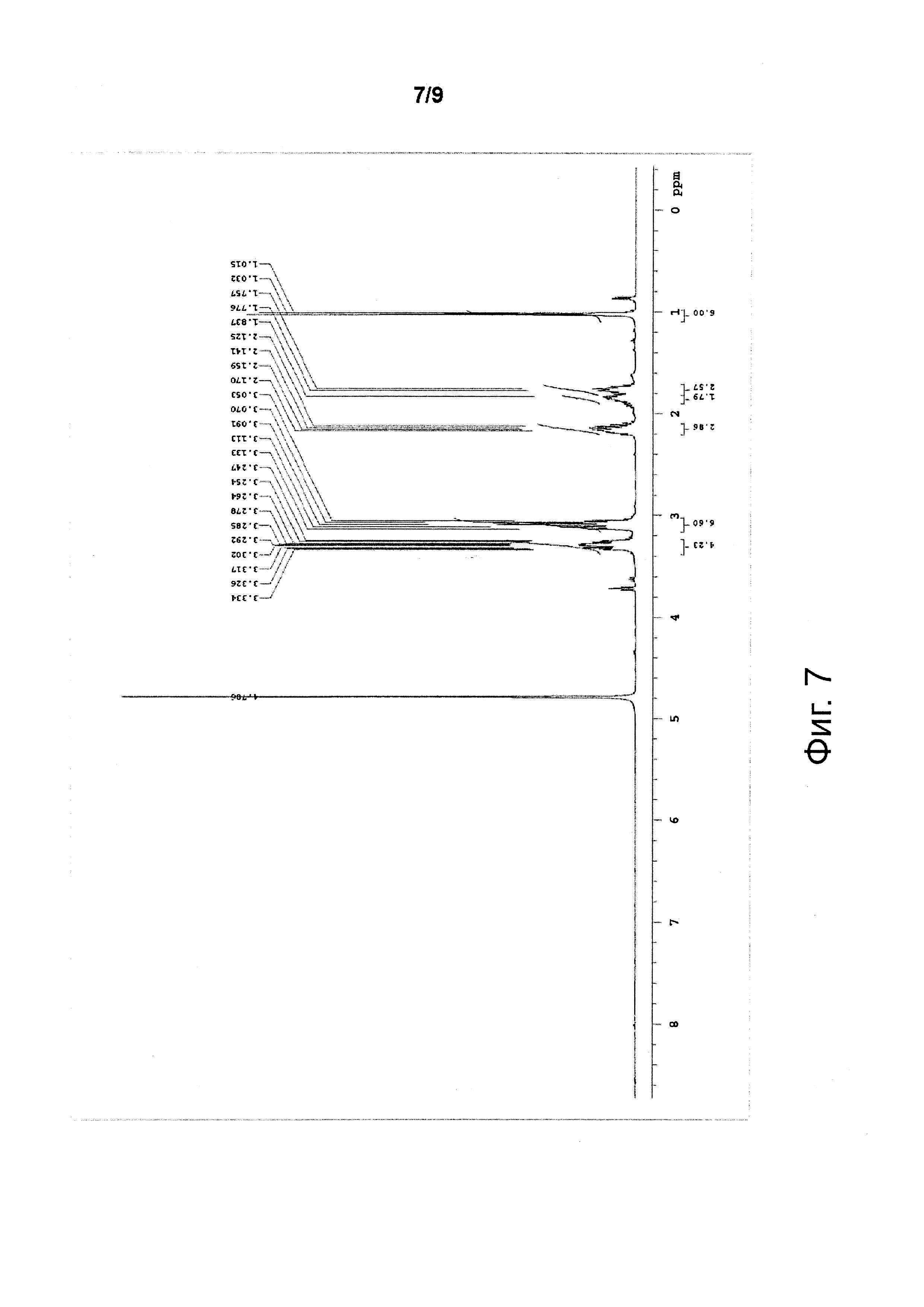
Синтез соединения 4: к указанному соединению 22 (0,084 г, 0,00021 моля, 1 экв.), растворенному в метаноле (2 мл) и находящемуся в бане со льдом, прикапывают HCl 3N (10 мл). Реакционную смесь перемешивают при комнатной температуре в течение 18 часов. Исчезновение исходного продукта оценивают с помощью ТСХ (CH2Cl2 9/МеОН 1/NH4OНводн. 0,03). МеОН выпаривают и водный остаток промывают диэтиловым эфиром (2×8 мл) и сушат. Получают 0,065 г соединения 4 в виде соли тригидрохлорида. Выход 100%. 1Н-ЯМР (400 МГц, D2O) δ 1,02 (д, 6Н, J=6,8 Гц), 1,76-1,78 (ср, 2Н), 1,79-1,84 (ср, 2Н), 2,14-2,17 (ср, 3Н), 3,06-3,25 (ср, 6Н), 3,26-3,33 (ср, 4Н); 13С ЯМР (100 МГц, D2O) δ 19,27, 20,15, 21,26, 23,83, 28,92, 36,52, 38,77, 50,18, 52,66, 58,88, 60,59. МС (ESI+) m/z=202 (М+Н)+
Фиг. 7, 8 и 9 прилагаемых чертежей представляют соответственно 1Н-ЯМР, 13С-ЯМР и масс-спектры соединения 4, то есть формулы (VI), как определено выше.
Примеры композиций
В дальнейшем, некоторые примеры композиций согласно изобретению для местного применения на коже головы описаны в качестве не ограничивающих примеров. В следующих примерах N1-метилспермидин обозначается соответствующим названием INCI, необходимым для использования в косметической продукции, а именно: N-метилспермидин. Это также относится к другим соединениям изобретения, приведенным в качестве примеров.
Пример 1
Шампунь для лечения выпадения волос
|
Пример 2
Лосьон для лечения для снижения выпадения волос
|
Пример 3
Бальзам-кондиционер, способствующий снижению выпадения волос
|
Пример 4
Бальзам для лечения выпадения волос
|
Пример 5
Высокоинтенсивная сыворотка для лечения волос
|
Пример 6
Высокоинтенсивная сыворотка для снижения выпадения волос
|
Пример 7
Шампунь для лечения выпадения волос
|
Пример 8
Лечебный лосьон для снижения выпадения волос
|
Пример 9
Укрепляющий гель для укладки
|
Пример 10
Лечебный лосьон для снижения выпадения волос
|
Пример 11
Высокоинтенсивная сыворотка для лечения волос
|
Экспериментальная часть и прилагаемые чертежи
Проводят следующие испытания активности N1-метилспермидина или N-(3-аминопропил)-N1-метил-1,4-бутандиамина, соединения формулы (II) в соответствии с изобретением или в виде свободного основания или в виде соли, тригидрохлорида (3HCl) или трималеата, по сравнению со спермидином (3HCl) в качестве контроля.
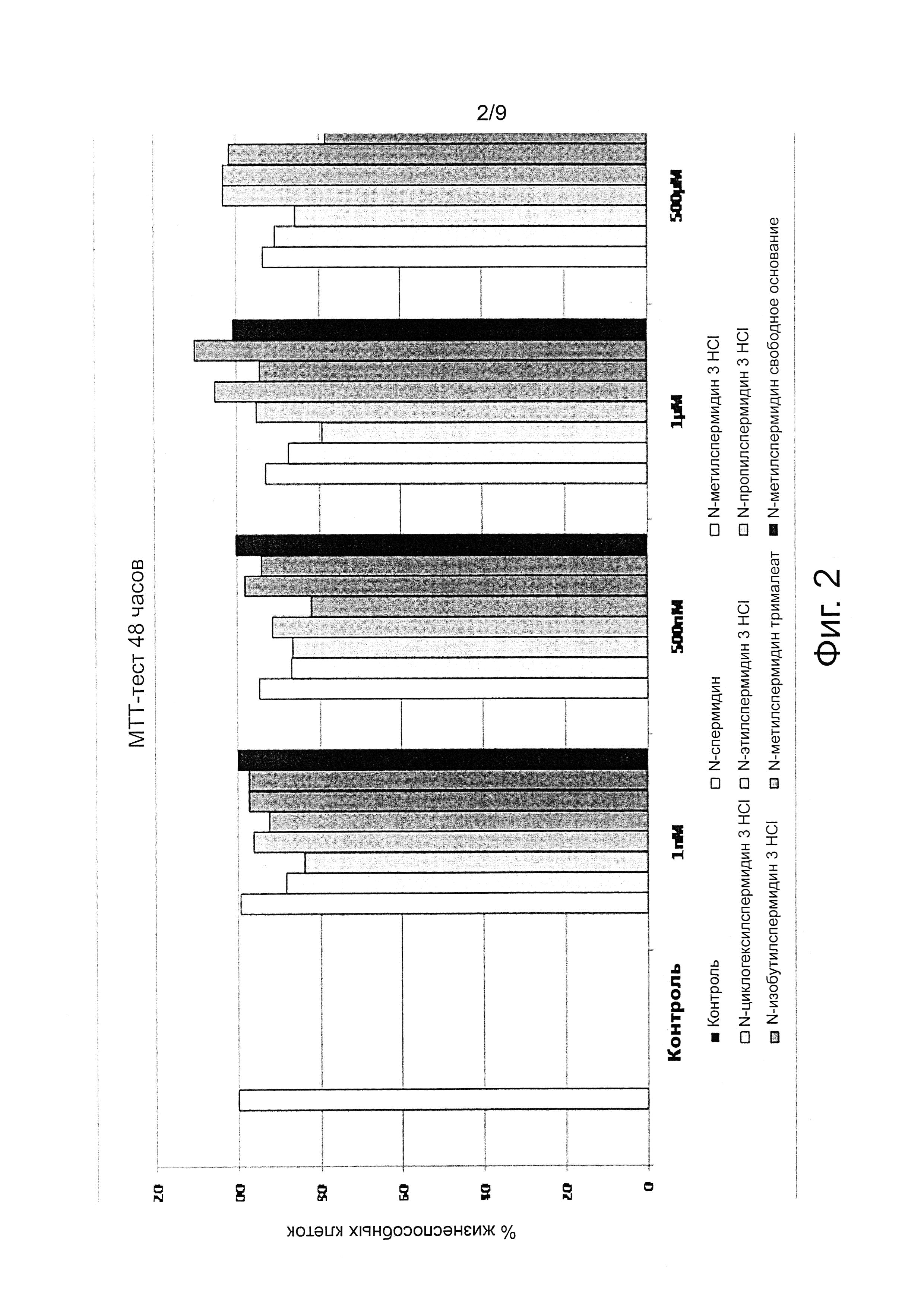
На фиг. 1 и 2 соответствующее испытание также распространяется на N1-циклогексилспермидин, N1-этилспермидин, N1-пропил спермидин и N1-изобутилспермидин, а именно соединения формулы (III), (IV), (V), (VI) в соответствии с изобретением в форме соли тригидрохлорида (3HCl).
В связи с этим, фиг. в соответствии со следующими фиг. прилагаются к настоящему описанию.
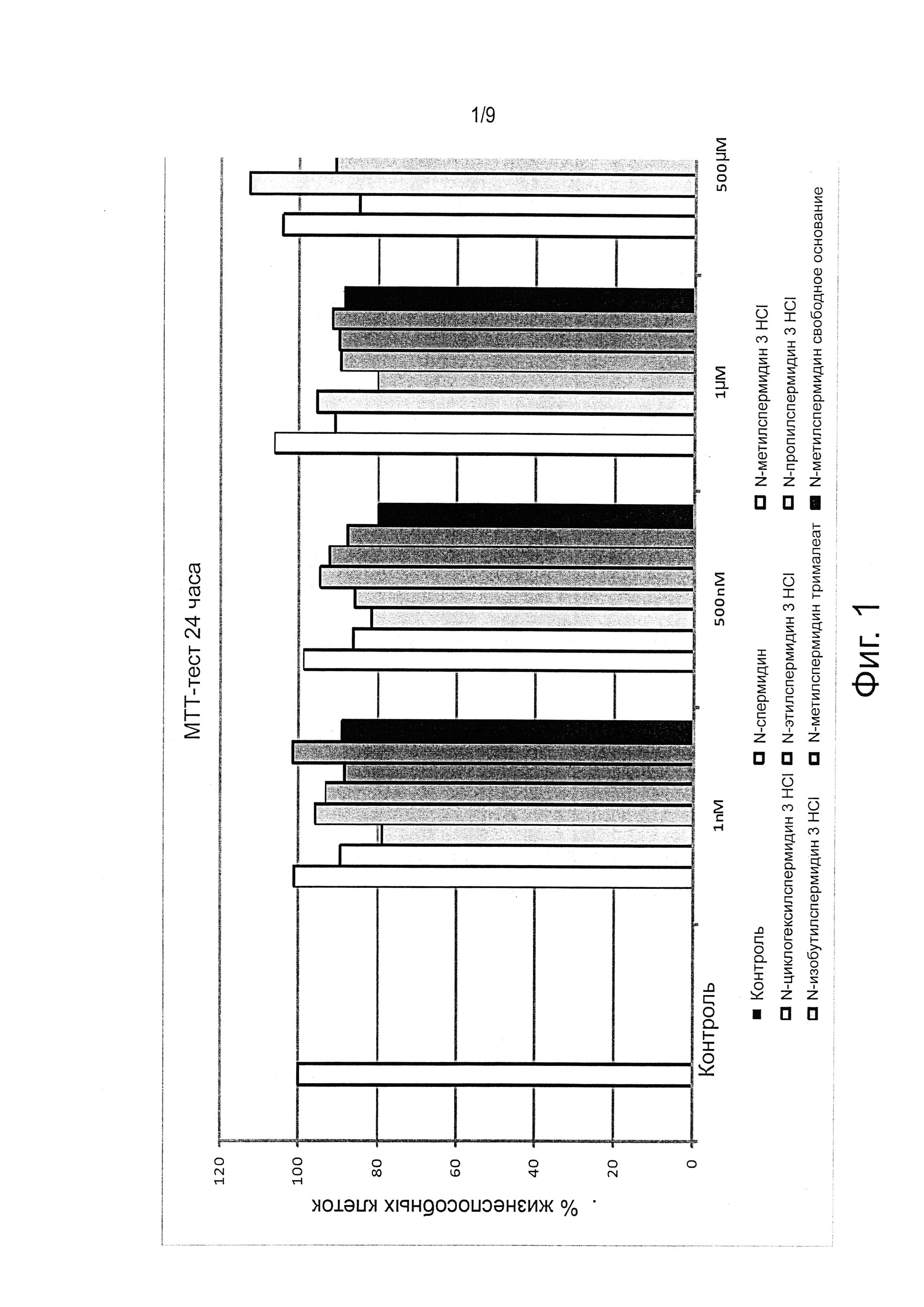
Фиг. 1 и 2 являются графиками результатов МТТ-теста.
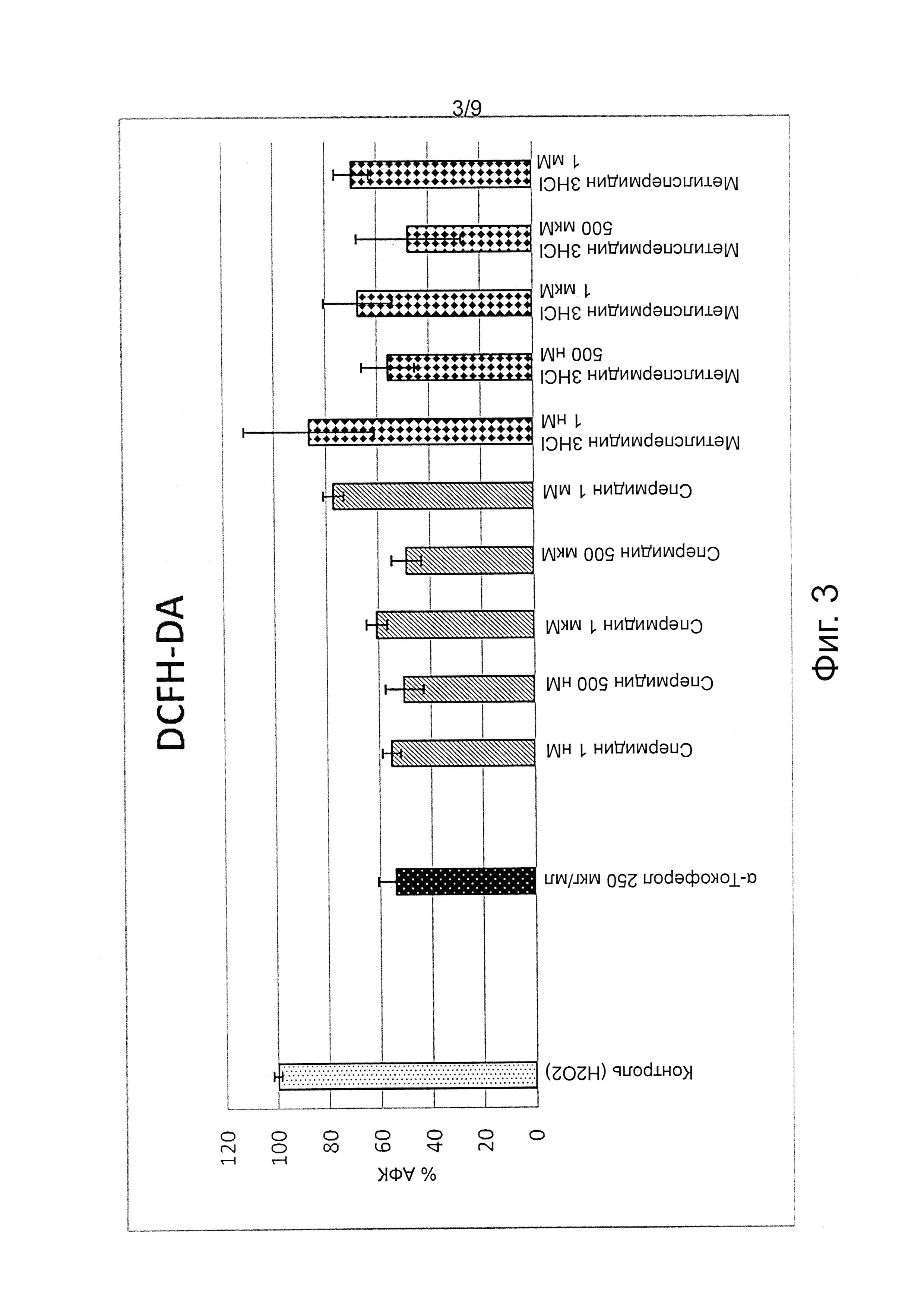
Фиг. 3 является графиком результатов испытаний стойкости к окислению.
Фиг. 4 является графиком результатов испытаний удлинения волос.
Фиг. 5 и 6 являются графиком результатов испытаний фиг. 4 в фазе анагена и катагена.
В результате, как указано выше, фиг. 7, 8 и 9 представляют соответственно Н-ЯМР, С-ЯМР и масс-спектры соединения 4, то есть, формулы (VI), как определено выше.
Также изучены стабильность и реакционная способность соединений формулы (I), после воздействия на их раствор атмосферного воздуха.
1. МТТ-тест
Введение
МТТ тест является испытанием, используемым для анализа жизнеспособности клеток (Mosmann, 1983). Это колориметрический тест, основанный на использовании соли тетразолия МТТ, который измеряет жизнеспособность клеток, которая затем может быть определена количественно с помощью микропланшет-ридера. МТТ (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолий бромид, тетразол), желтое соединение, восстанавливается до формазана, фиолетового вещества, в митохондриях клеток. Поглощение этого окрашенного раствора может быть определено количественно, его измерением при определенной длине волны (570 нм) с помощью спектрофотометра. Максимальное поглощение будет зависеть от используемого растворителя. Это восстановление происходит только тогда, когда митохондриальные ферменты редуктазы являются активными, и поэтому превращение в формазан может быть непосредственно связано с числом жизнеспособных клеток. Когда количество формазана продуцированного клетками, обработанными веществом, сравнивают с количеством, продуцированным необработанными контрольными клетками, можно сделать вывод об эффективности тестируемого вещества в гибели клеток построением кривой доза-эффект. Растворы МТТ, растворенного в PBS (фосфатно-солевой буферный раствор) или клеточной культуральной среде, без фенолового красного, имеют желтоватый цвет. В жизнеспособных клетках митохондриальные дегидрогеназы раскрывают кольцо тетразолия, давая фиолетовые кристаллы формазана, которые нерастворимы в водных растворах. Кристаллы могут быть растворены в подкисленном изопропаноле или ДМСО. Полученный пурпурный раствор анализируют с помощью спектрофотометрии. Увеличение числа клеток приводит к увеличению полученного формазана и увеличению оптической плотности. Использование МТТ теста имеет ограничения, связанные с: 1) физиологическим состоянием клеток и 2) изменением активности митохондриальных дегидрогеназ в различных типах клеток. Несмотря на это, МТТ тест определения клеток пригоден при измерении роста клеток как реакция на митогены, антигенные стимулы, факторы роста и другие реагенты, которые способствуют росту клеток, исследовании цитотоксичности и построении кривых роста клеток. МТТ тест для определения клеток особенно пригоден, когда культуры готовят в многолуночных планшетах. Для достижения наилучших результатов, количество клеток необходимо определять в ходе экспоненциальной фазы роста.
Материалы
Биологическая модель
Клеточная линия NCTC2544 кератиноцитов человека (Perry V.P. и др., 1957) получена из Национального института по исследованию рака в Генуе, Италия.

Параметры культуры
Клеточную линию выращивают в среде ЕМЕМ (EBSS) с добавлением 10% FBS, 2 мМ L-глутамина, 1% раствора NEAA 1X и 1% смеси пенициллина (10000 ЕД/мл)/стрептомицина (10000 мкг/мл) и выдерживают при температуре 37°С, 5% CO2 в 25 см2 колбе для культуры. Каждые два дня сплошной слой клеток разделяют 1:3-1:6, после промывки PBS IX (без Са2+ и Mg2+), с использованием трипсин/ЭДТА и производят посев 2-5*104 клеток/см2, 37°С, 5% CO2.
Среда для замораживания: культуральная среда с добавлением 20% FBS, 2 мМ L-глутамина, 1% смеси пенициллин/стрептомицин и 10% ДМСО.
Количественное определение клеток: анализ с трипановым синим.
Реагенты и оборудование

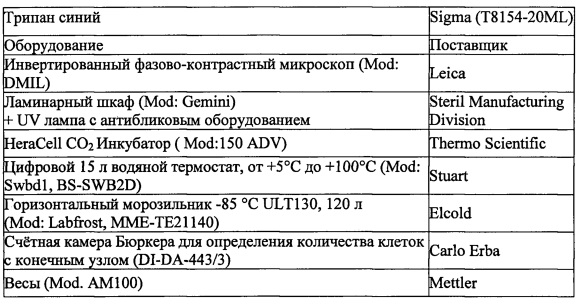
Методы
День 1: посев клеток
Когда NCTC 2544 клетки кератиноцита человека достигают конфлюентность около 80%, их отделяют и собирают с трипсином/ЭДТА, высевают при плотности 5×104 клеток/мл в 96-луночных планшетах и затем инкубируют при 37°С, 5% CO2 (24 ч).
Дни 2-3: воздействие реагентов 24-48 ч
Когда клетки достигают конфлюентность около 80%, они подвергаются воздействию возрастающих концентраций вышеуказанных активных соединений в соответствии с изобретением: N1-метилспермидин, в виде свободного основания и в виде тригидрохлорида (3HCl) и трималеата; а также N1-cycloesilspermidine, N1-этилспермидин, N1-пропилспермидин, N1-изобутилспермидин в виде тригидрохлорида (3HCl) и тригидрохлорида спермидина в качестве эталона для сравнения. Каждое соединение тестируют дважды. Испытывают следующие концентрации всех соединений: 1 нМ, 500 нМ, 1 мкМ, 500 мкМ (конечная концентрация в культуральной среде). SDS используют в качестве внутреннего стандарта.
После приготовления искомых разведений каждого соединения культуральную среду удаляли из планшета и лунки отбирают 100 мкл каждой концентрации. Контроль, содержащий только культуральную среду, включают в каждый планшет.
Клетки инкубируют при 37°С, 5% CO2 в течение различного времени обработки (24-48 ч).
День 4: МТТ-тест
В конце обработки соединениями, представляющими интерес, (24-48 ч) в 96-луночном планшете, среду удаляют и заменяют 100 мкл/лунку раствора МТТ и планшеты инкубируют в течение 3 ч при 37°С, 5% CO2. МТТ соль растворяют в PBS (5 мг/мл) и добавляют к клеткам при разведении 1:10 в среде ЕМЕМ, без фенолового красного, с добавлением 10% FCS, 2 мМ глутамина, 1% раствора NEAA 100Х (жидкая среда) и 1% смеси антибиотиков.
Планшет покрывают алюминиевой фольгой. Затем среду тщательно удаляют. 100 мкл ДМСО добавляют в каждую лунку, чтобы растворить полученный фиолетовый формазан. Планшеты покрывают алюминиевой фольгой и перемешивают в течение 15 мин при комнатной температуре.
Поглощение растворов регистрируют при 570 нм относительно фильтра при 630 нм в ридере для микропланшетов Biotek ELX808, используя предварительно определенную методику, и после правильного определения разметки планшета.
Сбор данных и статистический анализ
Данные оптической плотности регистрируют непосредственно программным обеспечением ридера для микропланшетов Biotek ELX808. Программа автоматически выполняет любые преобразования:
- преобразование 1: Расчет разницы OD 570-630 нм (после автоматической вычета фона),
- преобразование 2: Расчет % жизнеспособных клеток (по отношению к контролю).
Полученные данные затем переносятся в Excel и анализируются статистически и графически, чтобы определить, нецитотоксические концентрации, при которых эти соединения могут быть проверены.
Используемые реагенты и оборудование
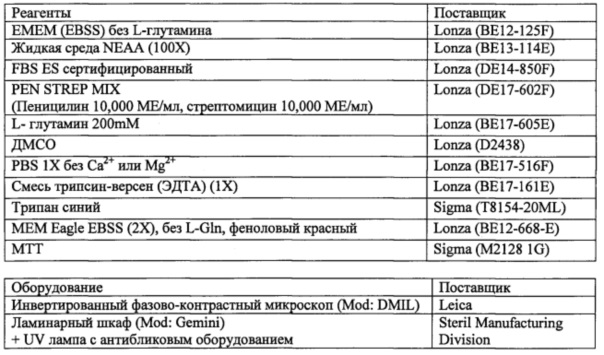

Результаты
Фиг. 1 и 2 суммируют полученные результаты, представленные графиками, соответствующими 24 часам (фиг. 1) и 48 часам (фиг. 2). Восемь колонок приведены для каждой группы равных концентраций, как указано на них, относящиеся соответственно, слева направо, к: спермидину, N1-метилспермидину, N1-циклогексилспермидину, N1-этилспермидину, N1-пропилспермидину, N1-изобутилспермидину, все в виде тригидрохлорида (3HCl); N1-метилспермидин в виде трималеата; N1-метилспермидин в виде свободного основания.
Жизнеспособность клеток выражают в процентах по отношению к контролю, то есть популяции клеток выращенных в стандартных условиях без добавления спермидина или соединений в соответствии с изобретением. При испытанных концентрациях (1 нМ, 500 нМ, 1 мМ, 500 мМ) спермидин не имеет цитотоксического действия через 24 или 48 часов воздействия на клеточную линию кератиноцитов человека (NCTC2544). Аналогичным образом, жизнеспособность клеток после обработки в течение 24 или 48 соединениями по изобретению (при той же концентрации спермидина) по существу не снизилась и в некоторых случаях даже улучшилась, что свидетельствует об отсутствии цитотоксичности соединений. Результаты, полученные для соединений по настоящему изобретению, статистически не отличаются от тех, которые получены для спермидина.
В общем, можно сделать вывод, что МТТ тест не демонстрирует цитотоксичности для соединений в соответствии с изобретением.
2. Испытание окисления - Получение активных форм кислорода (АФК)
Получение активных форм кислорода (АФК) контролируют с помощью спектрофлюориметра с использованием диацетата 2',7'-дихлорфлуоресцеина (DCFH-DA), как описано Tobi и др. (Tobi SE, Paul N, Т MacMillan J.J Photochem Photobiol, В 2000: 57: 102-112).
Вышеуказанные клетки NCTC2544 (конфлюентность ~80%) отделяют с помощью трипсин/ЭДТА и высевают с плотностью 5×104 клеток на лунку, в 96-луночных планшетах. Затем клетки обрабатывают N-метилспермидином в соответствии с изобретением и спермидином. Тестируют следующие концентрации N-метилспермидина и спермидина: 1 нМ, 500 нМ, 1 мкМ, 500 мкМ, 1 мМ (конечная концентрация в культуральной среде).
α-Токоферол (250 мкг/мл) используют в качестве сравнения. Планшеты инкубируют при 37°С в 5% СО2 в течение 1,5 ч. Клетки, выращенные на базальной среде с добавлением 10% FBS используют в качестве контроля.
График фиг. 3 представляет полученные результаты. Результаты, полученные из определения внутриклеточной концентрации активных форм кислорода (АФК), подтвердили антиоксидантную активность спермидина, как сообщалось в литературе. По сравнению с контрольными клетками, обработанными Н2О2, клетки, обработанные 250 мкг/мл α-токоферола, спермидина и N-метилспермидин, свидетельствуют о снижении концентрации продуктов АФК. При сравнении антиоксидантной активности спермидина с N-метилспермидином существенной разницы не обнаруживается.
3. Тест удлинения волосяного стержня
Активность N-метилспермидина тестируют на модели вне организма, что позволяет оценить эффект удлинения волос.
Материалы и методы
Культура органа волосяных фолликулов (HF) в фазе анагена VI получена микродиссекцией HF кожи скальпа человека (височно-лобной области) после информированного согласия пациентов, которые перенесли операцию (лифтинг), в соответствии с Хельсинкской Декларацией и с одобрения Комитета по этике университета Любека. В этой модели фаза роста (анаген) HF продолжается в течение нескольких дней с образованием пигментированного стержня со скоростью, аналогичной скорости в фазе анагена в естественных условиях, дополнительно проявляя циклическую активность роста вне живого организма, самопроизвольно переходящей в фазу регрессии цикла роста волос (катаген).
Для иммуногистохимических исследований, выделенные фолликулы культивируют в течение 6 дней подряд.
Спермидин, N-метилспермидин и растворитель (дистиллированная вода) вводят один раз для каждого изменения культуральной среды (каждые 48 часов), в концентрации 0,5 мкМ.
Замороженные срезы хранят при -80°С до использования.
Измерение роста волос
Измерения удлинения волосяного стержня после обработки растворителем, спермидином и N-метилспермидином регистрировали на 0, 1, 4 и 6 день с использованием Zeiss инвертированного бинокулярного микроскопа с одним окуляром с визирными нитями (Carl Zeiss, Oberkochen, Германия).
Результаты
Результаты удлинения волосяного стержня показаны на графике фиг. 4, на котором представлены результаты на 6 день. И спермидин и N-метилспермидин в соответствии с изобретением значительно улучшают удлинение волосяного стержня по отношению к растворителю. Наблюдаемое различие между спермидином и N-метилспермидином не является статистически значимым и, следовательно, эффект удлинения следует рассматривать близким в обоих случаях при сравнении.
4. Результаты в фазах анагена и катагена
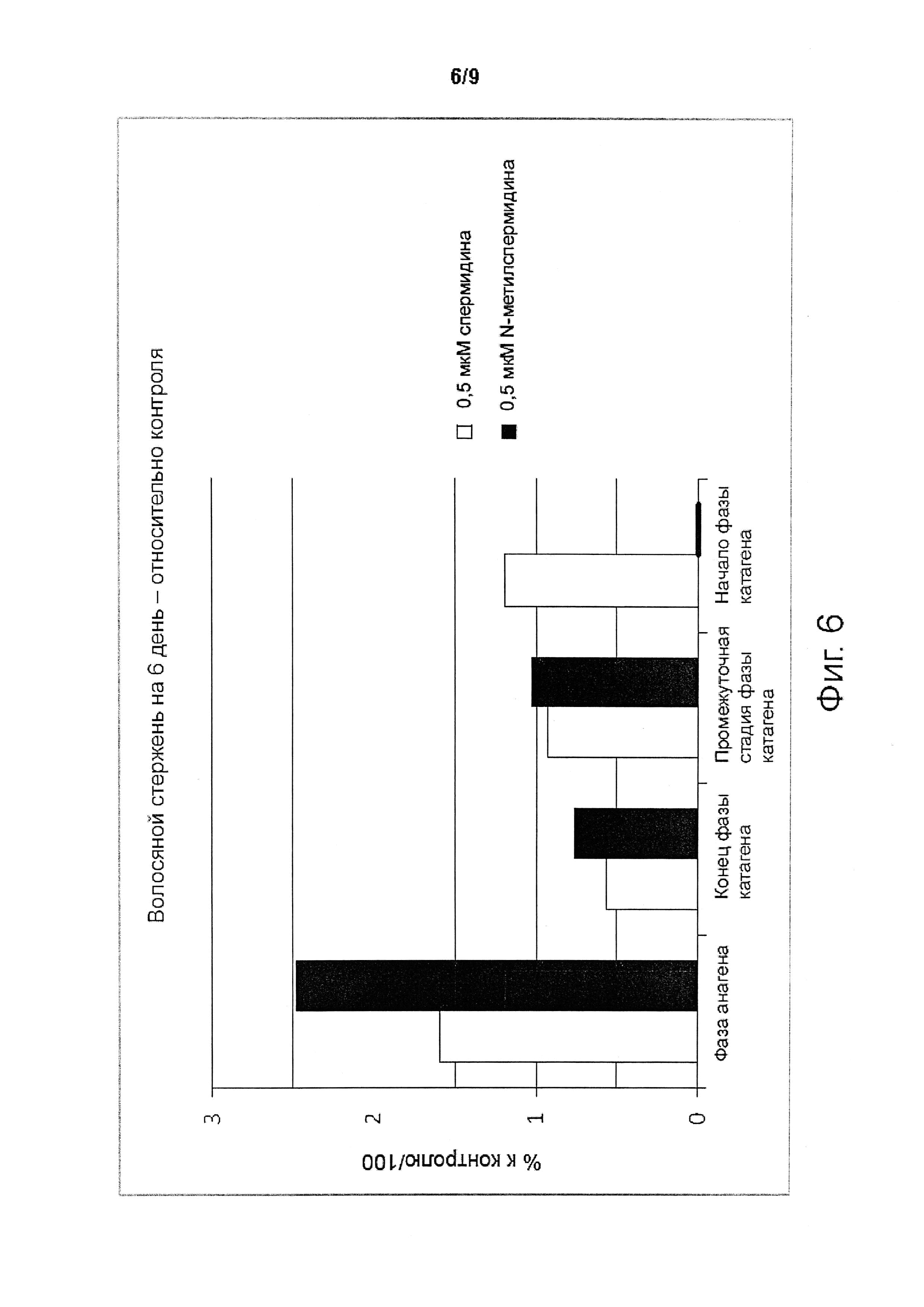
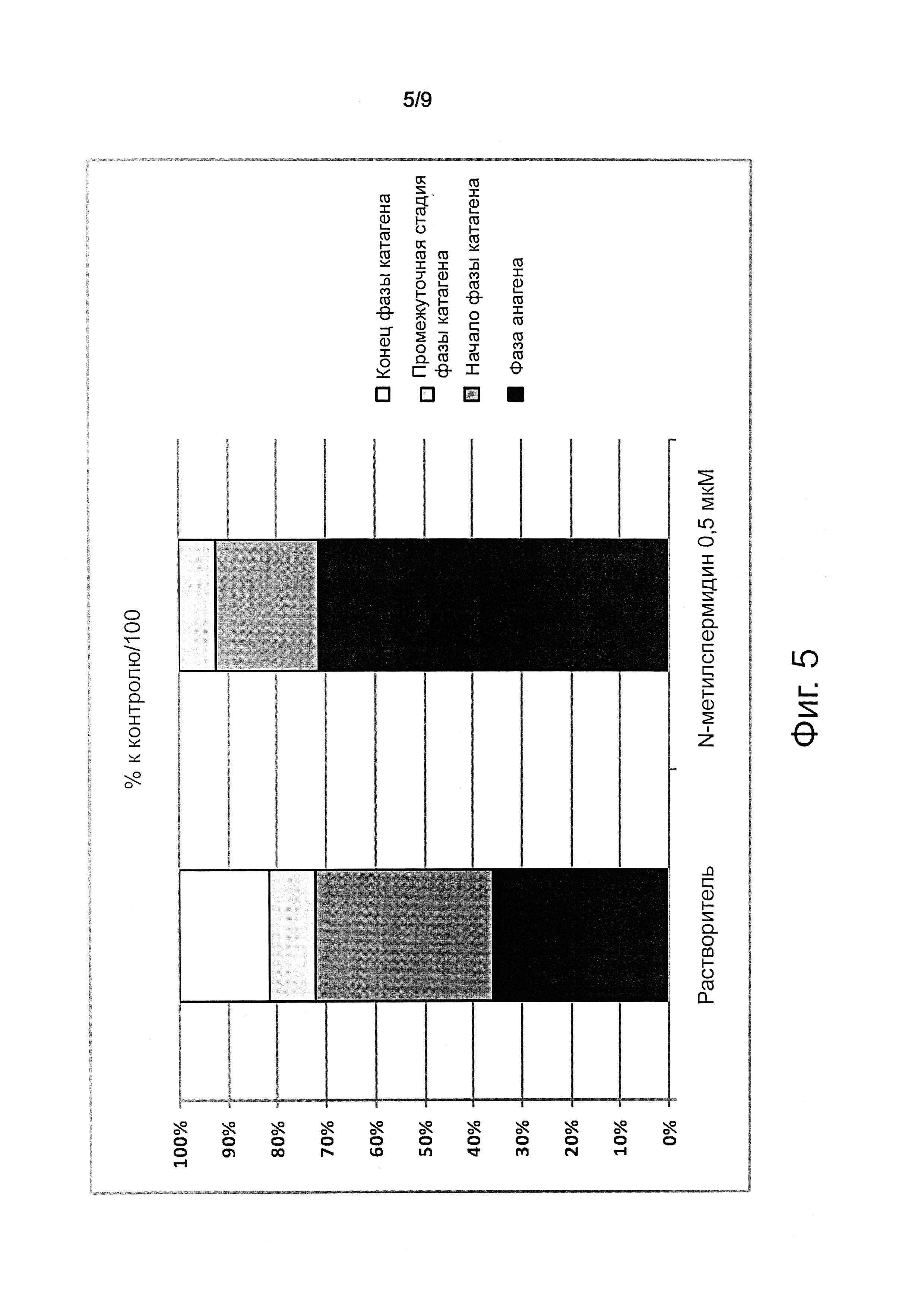
Следующие результаты для фаз анагена и катагена, представленные на графиках фиг.5 и 6, также получены для тое же модели вне организма волосяных фолликулов (HF), описанных в предыдущем тесте удлинения волосяного стержня.
График на фиг. 5 показывает процент фолликулов, обработанных N-метилспермидином на различных этапах цикла роста.
Отсюда можно видеть, что после 6 дней обработка N-метилспермидином значительно увеличивает процент волосяных фолликулов в фазе анагена и уменьшает процент в фазе катагена. В присутствии N-метилспермидина только 30% (около) фолликулов самопроизвольно вступают в фазу катагена, в то время как в присутствии растворителя более 60% фолликулов вступают в фазу катагена.
График на фиг. 6 показывает соответствующие значения в процентах от контроля фаз фолликул, полученные для спермидина (0,5 мкМ) и N-метилспермидина (0,5 мкМ).
Сравнение двух соединений неожиданно демонстрирует более высокий эффект продления фазы анагена в случае N-метилспермидина чем в случае спермидина. Таким образом, количество волос, вступающих в фазу катагена (разделенную на стадии: начальная, промежуточная и конечная), значительно ниже после обработки N-метилспермидином, чем спермидином.
5. Результаты по реакционноспособности
Свойства, N-(3-аминопропил)-N1-метила-1,4-бутандиамина (II) и N(3-аминопропил)-N1-циклогексил-1,4-бутандиамина (III) после воздействия воздуха исследуют по сравнению с соответствующим незамещенным производным, в котором N1 аминогруппа не имеющая R заместителя, становится вторичной аминогруппой, а именно N-(3-аминопропил)-1,4-бутандиамином. Поскольку одним из наиболее распространенных продуктов окисления вторичной аминогруппы являются N-нитрозо производные, которые образуются в результате реакции с окислами азота, присутствующих в воздухе, продукты нитрозирования, которые образовались при выдерживании раствора испытуемых соединений в контакте с окружающим воздухом, определяются в качестве параметра реакционноспособности.
Материалы и методы
Используемые методы состоят в проведении стадии анализа на нитрит-ионы и анализа N-нитрозаминов, последний в условиях сильного денитрозирования. Оксид азота, который образуется в соответствии с количеством нитрит-ионов и который образуется в соответствии с количеством нитрозогрупп, оценивают с помощью хемилюминометрического детектора.
Содержание ионов NO2- анализируют с использованием восстановительной смеси уксусная кислота/йодид калия (5 мл/1 мл 5% р-р Н2О.) При температуре 0-4°С. Нитрозо-группы анализируют с использованием денитрозирующей смеси уксусная кислота/бромистоводородная кислота (5 мл/1 мл) при температуре 70°С.
Реагенты являются коммерчески доступными, например, производства Sigma-Aldrich. Используют газы высокой чистоты газов (Не и NO).
Метод определения окисления соединений воздухом заключается в следующем.
a) 2 мМ раствор испытуемого вещества в очищенной воде дважды отбирают, в количестве, равном 500 мкл, в соответствующие лунки шестилуночных планшетов из инертной пластмассы (полистирол);
b) раствор в каждой лунке разводят 500 мкл смеси очищенной воды и этанола (85/15), свободной от загрязнений. Это способствует дисперсии жидкой пленки на поверхности лунки;
c) планшеты, подготовленные таким образом, подвергают воздействию окружающего воздуха в течение 72 ч;
d) в конце времени воздействия остаток в лунке элюируют 1 мл очищенной воды и затем используют для хемилюминометрического анализа.
Результаты

6. Выводы
С точки зрения отсутствия цитотоксичности, антиоксидантной активности по отношению к АФК и удлинения волосяного стержня, вышеуказанный эксперимент показывает, что соединение в соответствии с изобретением обеспечивает результаты не отличаются от тех, которые получены со спермидином.
Кроме того, N-метилспермидин неожиданно обладает, по-видимому, более высокой активностью, чем спермидин в продлении фазы анагена волос.
Хотя стимулирование удлинения волосяного стержня и продления анагена способствуют физиологическому росту волос, с клинической точки зрения результат расширения фазы анагена можно считать более значимым и актуальным с точки зрения удлинения волосяного стержня, так как удлинение фазы анагена имеет непосредственное положительное влияние на снижение потери волос, что является основной целью настоящего изобретения.
Активность в продлении фазы анагена и относительном ингибировании фазы катагена, как указано выше для N-метилспермидин, пригодна в борьбе со многими различными формами выпадения волос, или алопецией, характеризующимися чрезмерным выпадение из-за нефизиологичного сокращения фазы анагена, например, вызванного андрогенами, перифолликулярным воспалением, дефицитом железа и эстрогенами или введением препаратов, которые вызывают нефизиологическое выпадение в качестве побочного эффекта.
Из вышеприведенного описания в целом можно видеть, что соединения общей формулы (I) активны в соответствии с целями настоящего изобретения, а также в достаточной степени устойчивы, чтобы обеспечить эффективное применение для местного нанесения на кожу головы, без возможного превращения в другие вещества, которые более не являются активными в результате окисления.