Результат интеллектуальной деятельности: НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ
Вид РИД
Изобретение
Настоящее изобретение относится к новым химическим веществам - макроциклическим соединениям, аннелированным с биспидиновым ядром, представляющим значительный интерес в качестве потенциальных физиологически активных веществ, в частности, ингибиторов протеин-протеиновых взаимодействий. Работа выполнена в рамках договора №14.А12.31.005 от 4 июля 2013 г. между Министерством образования и науки Российской Федерации, федеральным государственным автономным образовательным учреждением высшего профессионального образования «Московский физико-технический институт (государственный университет)» (МФТИ) и ведущим ученым Фокиным В.В.
В литературе имеется описание нескольких циклических производных 4-(3,7-диазабицикло[3.3.1]нон-2-ил)масляной кислоты, а именно тетрагидроцитизина и его ацилированных аналогов [Примухамедов, И., Тилляев, К.С. Узбекский Хим. Ж., 1981, 1, 52-55. Примухамедов, И., Тилляев, К.С. Заидова, Р.А. Узбекский Хим. Ж., 1982, 3, 63-64.], представленных следующей формулой А,
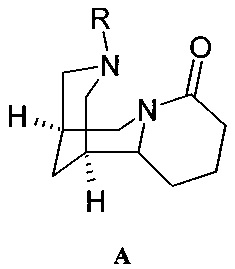
в которых R представляет собой атом водорода, бензил, малеинил, бензоил, 4-толуил, 2-бромбензоил, 2-карбоксибензоил, 3-нитробензоил, 4-нитробензоил и 4-аминобензоил.
Известно, что производные 3,7-диазабицикло[3.3.1]нонана являются эффективными и селективными эффекторами ион-канальных белков и рецептор-канальных комплексов. В качестве примера можно привести антиаритмический модулятор калиевых каналов - Амбазилид (Ambasilide) [Bosch, R.F., Milek, I.V., Popovic, К., Mermi, J., Mewis, C., Kohlkamp, V., Seipel, L. Ambasilide prolongs the action potential and blocks multiple potassium currents in human atrium. J. Cardiovasc. Pharmacol. 1999, 33 (5), 762. Knoll AG. EP 0701442, March 20, 1996. WO 9428899, December 22, 1994.], представленный ниже (Б):
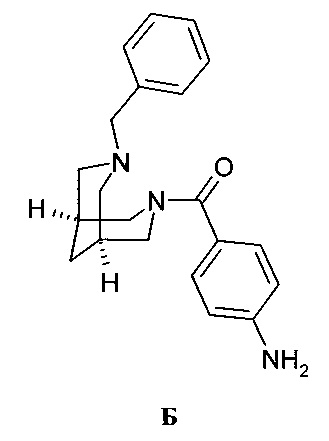
Также, в этом ряду найдены ион-канальные модуляторы, проявляющие антиаритмические свойства - препараты Bisaramil и Tedisamil, проходящие клинические испытания [R.L. Page, D.М. Roden, Natl Rev. Drug Discov., 2005, 4, 899], анальгетические антагонисты тахикининовых рецепторов NK1 [Т.Т. Wager, В.Т. OrNeill, W.М. Welch (Pfizer Inc), WO
Pat. 2004110996; Chem. Abstr., 2004, 142, 93683], антиэпилептические лиганды рецепторов γ-аминомасляной кислоты GABA(B) [P. Malherbe, R. Masciadri, E. Prinssen, W. Spooren, A.W. Thomas (Roche), US Pat. 20050197337; Chem. Abstr., 2005, 143, 266950].
Одно из наиболее известных соединений такого типа - алкалоид(-)цитизин (В),
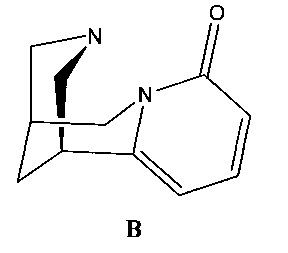
обнаруженный в заметных количествах в растениях видов ракитника (например, Cytisus laburnum L) и термопсиса (Thermopsis lanceolata) [J.W. Daly, Cell Mol. Neurobiol, 2005, 25, 513] семейства бобовых. Цитизин и ряд его производных являются селективными лигандами никотиновых ацетилхолиновых рецепторов (nAChR) [В.Т. OrNeill (Pfizer Inc.), WO Pat. 9818798; Chem. Abstr., 1998, 129, 4774; E. Marriere, J. Rouder, V. Tadino, M.C. Lasne, Org. Lett, 2000, 2, 1121; P. Imming, P. Klaperski, M.T. Stubbs, G. Seitz, D. Gundisch, Eur. J. Med. Chem., 2001, 36, 375], которые в настоящее время рассматриваются как одни из наиболее перспективных биомишеней при разработке новых средств для лечения нейродегенеративных заболеваний и психотических состояний [S.P. Arneric, М. Holladay, М. Williams, Biochem. Pharmacol, 2007, 74, 1092.] и т.д.
Ранее была получена и исследована фокусированная и комбинаторная библиотека соединений на основе 3,7-диазабицикло[3.3.1]нонана общей формулы Г,
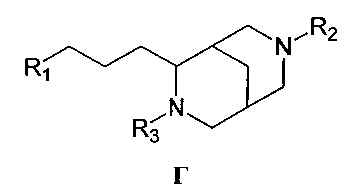
[Ivachtchenko, A.V.; Vvedensky, V.Y.; Sandulenko, Y.B; Khvat, A.V.; Tkachenko, S.E.; Okun, I.M. Substituted 3,7-diazabicyclo-[3.3.1]nonanes, targeted library and combinatorial library. Pat. RU 2228934, 2004]. Также сообщалось о синтезе небольшой тестовой жидкофазной комбинаторной библиотеки на основе 3,7-диазабицикло[3.3.1]нонанового ядра [А.V. Ivachtchenko, S.Е. Tkachenko, Y.В. Sandulenko, V.Y. Vvedensky, А.V. Khvat, J. Comb. Chem., 2004, 6, 828]. В рамках исследований в области высокопроизводительного твердофазного синтеза сходная технология была применена для синтеза более масштабной комбинаторной библиотеки на основе биспидинового ядра [Sandulenko, Yu. В.; Ivashchenko, А.V.; Kravchenko, D.V.; Tkachenko, S.E.; Vvedensky, V. Yu. Parallel solid-phase synthesis of novel 3,7-diazabicyclo[3.3.1]nonane derivatives starting from natural alkaloid cytisine. Russian Chemical Bulletin, 2008, 57 (9), 1999-2004].
В то же время природные макроциклические соединения и их синтетические производные уже долгое время используются в клинической практике, и много внимания уделяется более широкому использованию соединений, содержащих макроциклическое ядро, в медицинской химии в поисках новых лекарств для широкого спектра терапевтических мишеней. Одним из таких видов мишеней, слабо поддающихся воздействию лекарственных средств, являются терапевтически важные протеин-протеиновые взаимодействия (PPI), в которых макроциклические соединения средних и больших размеров, как было доказано, могут быть чрезвычайно применимы [Edward М. Driggers, Stephen P. Hale, Jinbo Lee and Nicholas K. Terrett Nature Reviews Drug Discovery 2008, 7, 608-624].
Несмотря на то что макроциклические структуры широко распространены в природных продуктах, их синтез зачастую чрезвычайно сложен. Таким образом, разработка надежных химических методов получения потенциально биологически активных макроциклов является очень актуальной задачей. В отличие от синтетических низкомолекулярных лекарств, природные циклические структуры обычно включают в себя двенадцатичленные и даже большего размера циклы и часто не удовлетворяют "правилу пяти" Липински. Однако уникальная структурная особенность и конформационная гибкость макроциклического кольца является существенным преимуществом как из-за потенциала связывания с сайтами белков, так и из-за высокой селективности взаимодействия с определенными биологическими мишенями
Для выполнения поставленной задачи авторами данного изобретения были выполнены синтез и широкие исследования новых макроциклов, содержащих биспидиновый (диазабицикло[3.3.1]нонановый) фрагмент как ядро.
Предметом настоящего изобретения является соединение общей формулы 1 или 2, или его фармацевтически приемлемая соль,
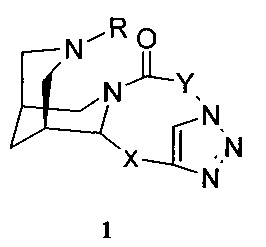
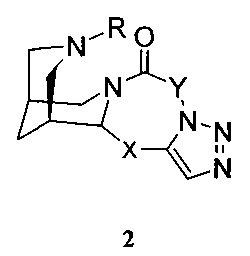
где R представляет собой метил, этил, пропил или бензил;
* -X- * выбран из группы, включающей
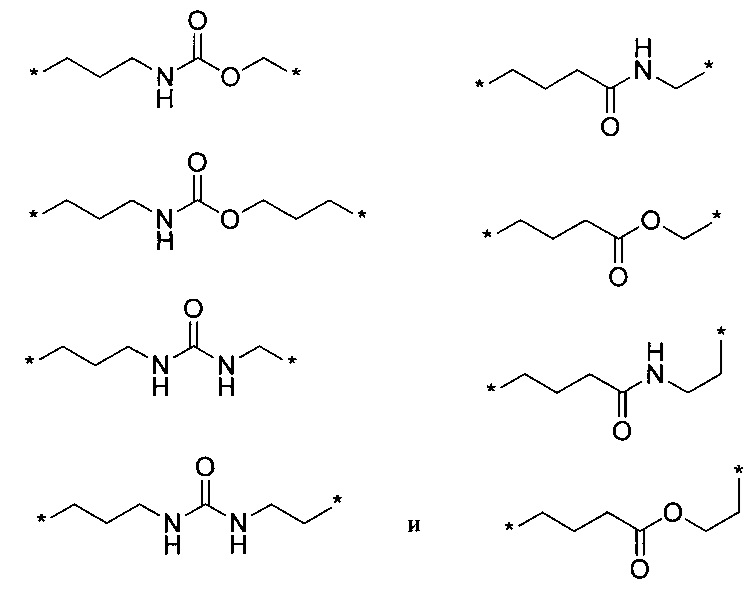
- Y - представляет собой (-CH2-)3 или (-CH2-)4.
Более предпочтительным соединением по настоящему изобретению является соединение, выбранное из группы, включающей:
(1S)-3-бензил-1,3,4,5,6,10,11,19,20,21,22,22а-додекагидро-1,5-метано-12,15-метено[1,5]диазоцино[2,1-g][1,3,8,13,14,15]оксапентаазациклогептадецин-8,18(2H,9H)-дион (1.1.1);
(1S)-3-бензил-1,3,4,5,6,10,11,17,18,21,22,23,24,24а-тетрадекагидро-16Н-1,5-метано-12,15-метено[1,5]диазоцино[2,1-g][1,3,8,13,14,15]оксапентаазациклононадецин-8,20(2H,9H)-дион (1.1.2);
(1S)-3-бензил-1,3,4,5,6,10,11,16,17,19,20,21,22,22а-тетрадекагидро-1,5-метано-12,15-метено[1,5]диазоцино[2,1-l][1,2,3,6,8,13]гексаазациклогептадецин-8,18(2H,9H)-дион (1.1.3);
(1S)-3-бензил-1,3,4,5,6,10,11,17,18,20,21,22,23,23а-тетрадекагидро-2H-1,5-метано-12,15-метено[1,5]диазоцино[2,1-m][1,2,3,7,9,14]гексаазациклооктадецин-8,19(9H,16H)-дион (1.1.4);
(1S)-3-бензил-1,3,4,5,6,10,11,16,17,19,20,21,21а-тридекагидро-2H-1,5-метано-12,15-метено[1,5]диазоцино[2,1-k][1,2,3,6,12]пентаазациклогексадецин-8,18(9H)-дион (1.1.5);
(1S)-3-бензил-1,3,4,5,6,10,11,19,20,21,21а-ундекагидро-2H-1,5-метано-12,15-метено[1,5]диазоцино[1,2-k][1,4,5,6,11]оксатетроазациклогексадецин-8,18(9H)-дион (1-1.6);
(1S)-3-бензил-1,2,3,4,5,6,10,11,17,18,20,21,22,22а-тетрадекагидро-1,5-метано-12,15-метено[1,5] диазоцино[2,1-l] [1,2,3,7,13]пентаазациклогептадецин-8,19(9H,16H)-дион (1.1.7);
(1S)-3-бензил-1,3,4,5,6,10,11,17,18,21,22,23,23а-тридекагидро-2H,16H-1,5-метано-12,15-метено[1,5]диазоцино[1,2-m][1,6,7,8,13]оксатетроазациклооктадецин-8,20(9H)-дион (1.1.8);
(1S)-3-бензил-1,3,4,5,6,9,10,11,12,20,21,22,23,23а-тетрадекагидро-8H-1,5-метано-13,16-метено[1,5]диазоцино[2,1-g][1,3,8,14,15,16]оксапентаазациклооктадецин-8,19(2H)-дион (1.2.1);
(1S)-3-бензил-1,3,4,5,6,9,10,11,12,18,19,22,23,24,25,25а-гексадекагидро-8H,17H-1,5-метано-13,16-метено[1,5]диазоцино[2,1-g][1,3,8,14,15,16]оксапентаазациклоикозин-8,21(2H)-дион (1.2.2);
(1S)-3-бензил-1,3,4,5,6,9,10,11,12,17,18,20,21,22,23,23а-гексадекагидро-8H-1,5-метано-13,16-метено[1,5]диазоцино[2,1-l][1,2,3,6,8,13]гексаазациклооктадецин-8,19(2H)-дион (1.2.3);
(1S)-3-бензил-1,3,4,5,6,9,10,11,12,18,19,21,22,23,24,24а-гексадекагидро-2H,8H-1,5-метано-13,16-метено[1,5]диазоцино[2,1-m][1,2,3,7,9,14]гексаазациклононадецин-8,20(17H)-дион (1.2.4);
(1S)-3-бензил-1,2,3,4,5,6,9,10,11,12,17,18,20,21,22,22а-гексадекагидро-8H,19H-1,5-метано-13,16-метено[1,5]диазоцино[2,1-k][1,2,3,6,12]пентаазациклогептадецин-8,19-дион (1.2.5);
(1S)-3-бензил-1,2,3,4,5,6,9,10,11,12,20,21,22,22а-тетрадекагидро-8H,19H-1,5-метано-13,16-метено[1,5]диазоцино[1,2-l][1,4,5,6,12]оксатетроазациклогептадецин-8,19-дион (1.2.6);
(1S)-3-бензил-1,2,3,4,5,6,9,10,11,12,18,19,21,22,23,23а-гексадекагидро-8H-1,5-метано-13,16-метено[1,5]диазоцино[2,1-l][1,2,3,7,13]пентаазациклооктадецин-8,20(17H)-дион (1.2.7); и
(1S)-3-бензил-1,2,3,4,5,6,9,10,11,12,18,19,22,23,24,24а-гексадекагидро-8H,17H,21H-1,5-метано-13,16-метено[1,5]диазоцино[1,2-n][1,6,7,8,14]оксатетроазациклононадецин-8,21-дион (1.2.8).
Более предпочтительным соединением по настоящему изобретению является соединение, выбранное из группы, включающей:
(11S)-13-бензил-8,9,10,10а,11,12,13,14,15,16,20,21-додекагидро-4H-11,15-метано[1,5]диазоцино[2,1-g][1,2,3]триазоло[1,5-m][1,3,8,13]оксатриазациклопентадецин-6,18(7H,19H)-дион (2.1.1);
(13S)-15-бензил-5,6,10,11,12,12а,13,14,15,16,17,18,22,23-тетрадекагидро-4H-13,17-метано[1,5]диазоцино[2,1-g][1,2,3]триазоло[1,5-m][1,3,8,13]оксатриазациклогептадецин-8,20(9H,21H)-дион (2.1.2);
(11S)-13-бензил-4,5,8,9,10,10а,11,12,13,14,15,16,20,21-тетрадекагидро-11,15-метано[1,5]диазоцино[1,2-k][1,2,3]триазоло[5,1-е][1,3,6,11]тетраазациклопентадецин-6,18(7H,19H)-дион (2.1.3);
(12S)-14-бензил-5,6,9,10,11,11а,12,13,14,15,16,17,21,22-тетрадекагидро-4H-12,16-метано[1,5]диазоцино[1,2-l][1,2,3]триазоло[5,1-f][1,3,7,12]тетраазациклогексадецин-7,19(8H,20H)-дион (2.1.4);
(10S)-12-бензил-5,7,8,9,9а,10,11,12,13,14,15,19,20-тридекагидро-4H-10,14-метано[1,5]диазоцино[1,2-l][1,2,3]триазоло[5,1-с][1,4,9]триазациклотетрадецин-6,17(18H)-дион (2.1.5);
(10S)-12-бензил-7,8,9,9а,10,11,12,13,14,15,19,20-додекагидро-4H,6H-10,14-метано[1,5]диазоцино[1,2-i][1,2,3]триазоло[5,1-с][1,4,9]оксадиазациклотетрадецин-6,17(18H)-дион (2.1.6);
(11S)-13-бензил-5,6,8,9,10,10а,11,12,13,14,15,16,20,21-тетрадекагидро-11,15-метано[1,5]диазоцино[1,2-j][1,2,3]триазоло[5,1-d][1,5,10]триазациклопентадецин-7,18(4H,19H)-дион (2.1.7);
(12S)-14-бензил-5,6,9,10,11,11а,12,13,14,15,16,17,21,22-тетрадекагидро-4H,8H-12,16-метано[1,5]диазоцино[1,2-k][1,2,3]триазоло[5,1-е][1,6,11]оксадиазациклогексадецин-8,19(20H)-дион (2.1.8);
(11S)-13-бензил-8,9,10,10а,11,12,13,14,15,16,19,20,21,22-тетрадекагидро-4H,18H-11,15-метано[1,5]диазоцино[2,1-g][1,2,3]триазоло[1,5-n][1,3,8,14]оксатриазациклогексадецин-6,18(7H)-дион (2.2.1).
(13S)-15-бензил-5,6,10,11,12,12а,13,14,15,16,17,18,21,22,23,24-гексадекагидро-4H,20H-13,17-метано[1,5]диазоцино[2,1-g][1,2,3]триазоло[1,5-n][1,3,8,14]оксатриазациклооктадецин-8,20(9H)-дион (2.2.2);
(11S)-13-бензил-4,5,8,9,10,10а,11,12,13,14,15,16,19,20,21,22-гексадекагидро-18H-11,15-метано[1,5]диазоцино[1,2-l][1,2,3]триазоло[5,1-е][1,3,6,12]тетраазациклогексадецин-6,18(7H)-дион(2.2.3);
(12S)-14-бензил-5,6,9,10,11,11а,12,13,14,15,16,17,20,21,22,23-гексадекагидро-4H,19H-12,16-метано[1,5]диазоцино[1,2-m][1,2,3]триазоло[5,1-f][1,3,7,13]тетраазациклогептадецин-7,19(8H)-дион (2.2.4);
(10S)-12-бензил-4,5,7,8,9,9а,10,11,12,13,14,15,18,19,20,21-гексадекагидро-6H,17H-10,14-метано[1,5]диазоцино[2,1-i][1,2,3]триазоло[1,5-а][1,4,10]триазациклопентадецин-6,17-дион (2.2.5);
(10S)-12-бензил-7,8,9,9а,10,11,12,13,14,15,18,19,20,21-тетрадекагидро-4H,6H,17H-10,14-метано[1,5]диазоцино[1,2-j][1,2,3]триазоло[5,1-с][1,4,10]оксадиазациклопентадецин-6,17-дион (2.2.6);
(11S)-13-бензил-5,6,8,9,10,10а,11,12,13,14,15,16,19,20,21,22-гексадекагидро-18H-11,15-метано[1,5]диазоцино[2,1-γ][1,2,3]триазоло[1,5-а][1,5,11]триазациклогексадецин-7,18(4H)-дион(2.2.7); и
(12S)-14-бензил-5,6,9,10,11,11а,12,13,14,15,16,17,20,21,22,23-гексадекагидро-4H,8H,19H-12,16-метано[1,5]диазоцино[1,2-l][1,2,3]триазоло[5,1-е][1,6,12]оксадиазациклогептадецин-8,19-дион (2.2.8).
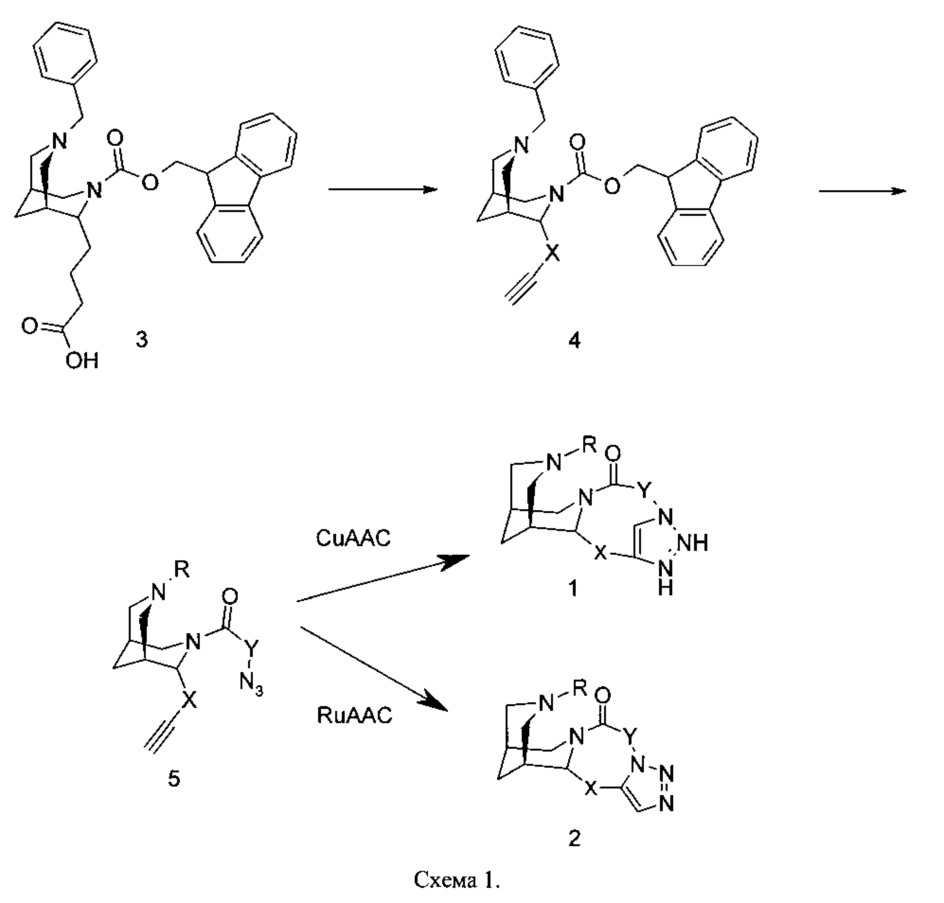
Предметом настоящего изобретения также является способ получения соединения общей формулы 1 или 2, приведенный на Схеме 1.
Ранее описанное в литературе [Sandulenko, Yu. В.; Ivashchenko, А.V.; Kravchenko, D.V.; Tkachenko, S.E.; Vvedensky, V.Yu. Parallel solid-phase synthesis of novel 3,7-diazabicyclo[3.3.1]nonane derivatives starting from natural alkaloid cytisine. Russian Chemical Bulletin, 2008, 57 (9), 1999-2004] соединение 3 с помощью реакции Курциуса в присутствии спирта или амина с концевой тройной связью, либо прямого амидирования или этерификации, превращается в соединение 4, содержащее фрагмент X с концевым алкином. Депротекция соединения 4 с помощью α-хлороэтилхлорформиата с заменой бензила на заместитель R алкилированием, дальнейшая депротекция Fmoc-защиты пирролидином с последующим ацилированием соответствующей ω-азидокарбоновой кислотой приводит к соединению 5 с фрагментом Y, содержащим терминальный азид. Внутримолекулярное азид-алкиновое циклоприсоединение, катализируемое соединениями Cu(I) или Ru(II), приводит, соответственно, к макроциклическим продуктам 1 или 2.
Предметом настоящего изобретения также является фармацевтическая композиция для профилактики или лечения заболевания, опосредованного протеин-протеиновым взаимодействием.
Фармацевтическая композиция может включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с активным компонентом по настоящему изобретению может включать и другие активные ингредиенты, при условии, что они не вызывают нежелательных эффектов, например, аллергических реакций. При необходимости использования фармацевтических композиций по настоящему изобретению в клинической практике они могут смешиваться для изготовления различных форм, при этом они могут включать в свой состав традиционные фармацевтические носители; например, пероральные формы (такие как, таблетки, желатиновые капсулы, пилюли, растворы или суспензии); формы для инъекций (такие как, растворы или суспензии для инъекций, или сухой порошок для инъекций, который требует лишь добавления воды для инъекций перед использованием); местные формы (такие как, мази или растворы).
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в том числе: в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, бесцветные агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Фармацевтическая композиция по настоящему изобретению может быть получена смешением активного компонента, представляющего собой новое соединение общей формулы 1 или 2 с инертным наполнителем, растворителем и/или другими фармацевтически приемлемыми эксципиентами.
Лекарственное средство на основе фармацевтической композиции по настоящему изобретению может вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно, местно или ректально). Клиническая дозировка активного компонента (субстанции) или фармацевтической композиции, включающей фармацевтически эффективное количество активного компонента, у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10~500 мг, предпочтительно - 50~300 мг. Поэтому во время приготовления фармацевтических композиций по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10~500 мг, предпочтительно 50~300 мг. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно - от одного до шести раз).
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
«Активный компонент» (лекарственное вещество, лекарственная субстанция, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «низших алкильных» заместителей. Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей»), включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонил, гетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или RkaRk+1aN-, RkaRk+1aNC(=O)-, RkaRk+1aNC(=S)-, RkaRk+1aNSO2-, где Rka и Rk+1a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например, атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rka и Rk+1a вместе с атомом N, с которым они связаны, образуют через Rka и Rk+1a 4-7 членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензил.
«Аннелированный цикл» (конденсированный цикл) означает би- или полициклическую систему, в которой аннелированный цикл и цикл или полицикл, с которым он «аннелирован», имеют как минимум два общих атома. Аннелированными могут быть ароматические, неароматические системы и гетероциклические системы.
«Лекарственное средство (препарат)» - комбинация нескольких лекарственных веществ для одновременного использования в виде таблеток, капсул, инъекций, мазей, ректальных суспензий и гелей и др. готовых форм, предназначенный для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего. Лекарственные вещества в одном комплекте могут быть представлены в виде различных готовых форм, предназначенных для введения в организм животного или человека различными способами, например перорально и ректально.
«Лиганды» (от латинского ligo - связывать) представляют собой химические вещества (малая молекула, неорганический ион, пептид, белок и прочее), способные взаимодействовать с рецепторами, которые трансформируют это взаимодействие в специфический сигнал.
«Низший алкил» означает линейный или разветвленный алкил с 1-4 атомами углерода.
«Фармацевтическая композиция» обозначает композицию, включающую в себя соединение общей формулы 1 и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как, консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как, парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения. Фармацевтические композиции, как правило, получают с помощью стандартных процедур, предусматривающих смешение активного соединения с жидким или тонко измельченным твердым носителем. Для изготовления суппозиториев помимо активных компонентов используют также масло какао, сплавы его с парафином и гидрогенизированными жирами, растительные и животные гидрогенизированные жиры, твердый жир, ланоль, сплавы гидрогенизированных жиров с воском, твердым парафином и другие основы, разрешенные для медицинского применения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные. (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как, холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
«Фармацевтически приемлемые эксципиенты» под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители.
Представленные ниже примеры иллюстрируют, но не ограничивают изобретение. Структуры полученных соединений подтверждают данными химического, хроматографического и спектрального анализов.
Пример 1. Метод синтеза соединения формулы 1.2.1. Синтез осуществляют в соответствии со Схемой 2.
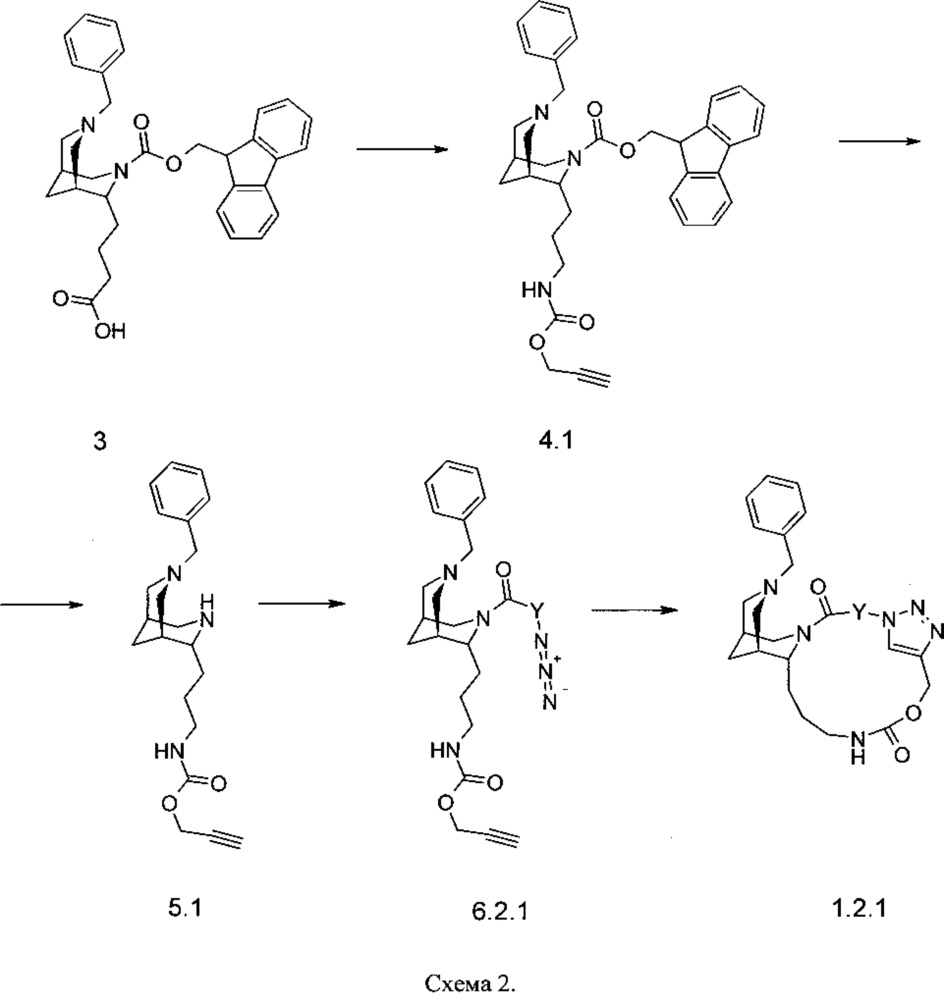
Получение соединения 4.1. К раствору соединения 3 (10 г, 19.06 ммоль) в сухом толуоле (150 мл) при комнатной температуре в инертной атмосфере добавляют dppa (6.4 г, 23.25 ммоль) и триэтиламин (2.31 г, 22.87 ммоль). Смесь нагревают и кипятят 90 мин, после чего добавляют пропаргиловый спирт (2.56 г, 45.74 ммоль). Полученную смесь кипятят при перемешивании 16 ч. После охлаждения до комнатной температуры, смесь разбавляют нас. NaHCO3 (50 мл) и этилацетатом (50 мл). Водную фазу экстрагируют этилацетатом (2×50 мл) Органические фазы объединяют, сушат над Na2SO4, после чего растворитель удаляют под вакуумом. Продукт используют на следующей стадии без дополнительной очистки. Выход принимается количественным. LC-MS: 579 (М+Н).
Получение соединения 5.1. К раствору соединения 4.1 (11 г, 19.04 ммоль) в хлористом метилене (150 мл) при перемешивании при комнатной температуре добавляют пирролидин (4.07 г, 57.12 ммоль). Смесь выдерживают 16 ч, после чего разбавляют водой (50 мл). Водную фазу экстрагируют хлористым метиленом (2×50 мл). Органические фазы объединяют, сушат Na2SO4, после чего растворитель удаляют под вакуумом. Продукт используют на следующей стадии без дополнительной очистки. Выход принимается количественным. LC-MS: 356 (М+Н).
Получение соединения 6.2.1 (Y=(-СН2-)4). К раствору соединения 5.1 (0.247 г, 0.695 ммоль) в хлористом метилене (5 мл) при комнатной температуре добавляют азидовалериановую кислоту (0.109 г, 0.764 ммоль), ДИПЕА (0.269 г, 2.08 ммоль) и TBTU (0.268 мг, 0.834 ммоль). Смесь перемешивают 16 ч, после чего разбавляют водой (5 мл). Водную фазу экстрагируют хлористым метиленом (2×5 мл). Органические фазы объединяют, сушат Na2SO4 и концентрируют под вакуумом. Продукт чистят на силикагеле (5% ТГФ в хлористом метилене). Выход 0.143 г (43%). LC-MS: 482 (М+Н). 1Н NMR (500 MГц, CDCl3: δ - 7.38-7.24 (5Н, m); 4.67 (2Н, s); 3.88-3.04 (7Н, m); 2.65-1.97 (6Н, m); 1.83-1.22 (10Н, m); 0.96-0.85 (4Н, m); 0.15-0.03 (2Н, m).
Получение соединения 1.2.1 (Y=(-СН2-)4). К раствору соединения 6.1 (0.143 г, 0.298 ммоль) в смеси вода: трет-бутанол 1:1 (2 мл) при комнатной температуре добавляют аскорбат натрия (13 мг, 0.06 ммоль, 1М раствор в воде), CuSO4*5H2O (8 мг, 0.03 ммоль). Смесь перемешивают 16 ч, после чего растворитель удаляют под вакуумом. Остаток растворяют в хлористом метилене (5 мл) и чистят на силикагеле (4% МеОН в хлористом метилене). LC-MS: 482 (М+Н). 1Н NMR (500 MГц, DMSO-d6): δ=7.89 (1Н, m); 7.38-7.22 (5H, m); 6.67 (1H, bs); 5.09 (2H, dd, J=23.5, 12.7 Гц); 4.46-4.26 (3H, m); 3.45 (2H, s); 2.80-2.73 (2H, m); 2.61-2.54 (2H, m); 2.38 (1H, m); 2.15-1.96 (5H, m); 1.94-1.78 (2H, m); 1.72-1.14 (10H, m).
Аналогичным образом получают соединения 1.1.1-1.1.8, 1.2.2-1.2.8 (Таблица 1):
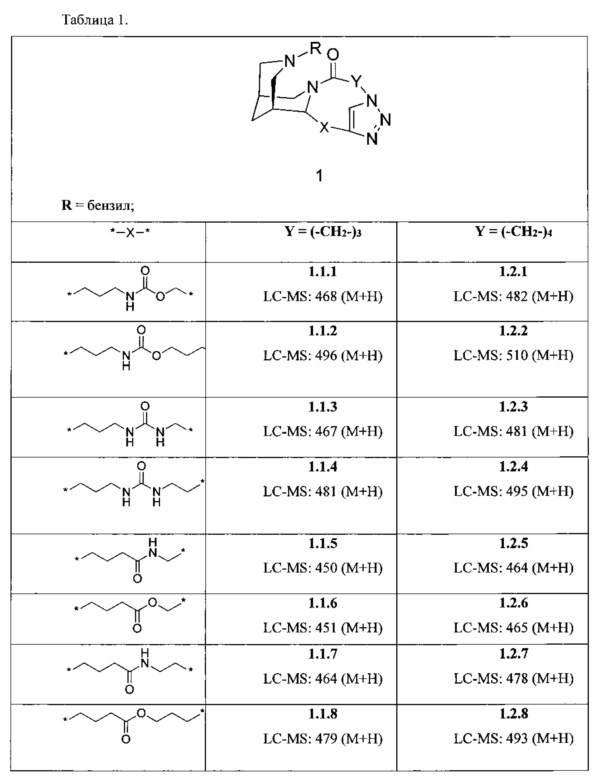
Аналогичным образом получают соединения 2.1.1-2.1.8, 2.2.1-2.2.8 (Таблица 2):
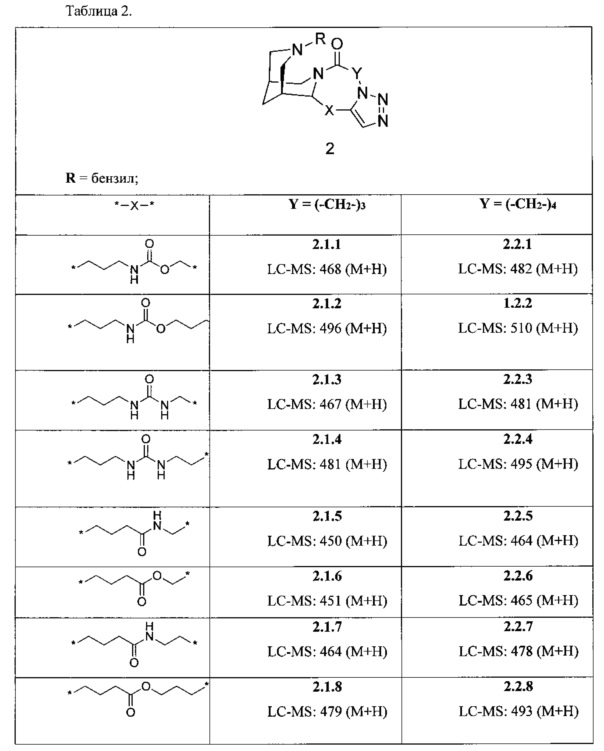
Пример 2. Получение солей (в виде гидрохлоридов). Для получения солей соединения общей формулы 1 или 2 полученные соединения 1.1.1-1.1.8, 1.2.1-1.2.8, 2.1.1-2.1.8, 2.2.1-2.2.8 растворяют в спирте, добавляют к ним насыщенный спиртовой раствор хлороводорода. После окончания реакции выпавший осадок отфильтровывают. Получают кристаллы гидрохлоридов соединения общей формулы 1 или 2.
Пример 3. Получение лекарственного средства по настоящему изобретению в форме таблеток. Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг соединения 1.2.1 и спрессовывают в брусок. Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг каждая.
Получение лекарственного средства по настоящему изобретению в форме капсул. Тщательно смешивают соединение 1.2.1 с порошком лактозы в соотношении 2:1. Полученную порошкообразную смесь упаковывают по 300 мг в желатиновые капсулы подходящего размера.
Получение лекарственного средства по настоящему изобретению в форме инъекционных композиций для внутримышечных, внутрибрюшинных или подкожных инъекций. Смешивают 500 мг соединения 1.2.1 с 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл инъекционной воды. Полученный раствор фильтруют и помещают по 1 мл в ампулы, которые запаивают.
Настоящее изобретение может быть использовано в медицине, ветеринарии, биологии.
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/95527dd775cc0f5224a003a2b7dbd493.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/28fe3e571bd091a1c946277763cb8bcd.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/b8fb4e66759512834ddf592d3984087d.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/2bbb00dbaf4e2c67f40f349da308bbce.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/b02a73ea8f04b28b6ca93de991c07ad8.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/480ab8cf2c4d975d1ad2f7283e549077.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/95c216cf8040b57a395ff4bc47fe58d9.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/c6d7481c77da82a2d10d6cb818789d9f.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/8bb50bc498d43a7f36f443e414621bb4.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/b94087c747cf38a71b282702fd14dc8f.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/fbadc2247269688cb859c2c6aea06d91.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/3aeba40580b789d0231fdd1252c1e492.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/16edece58870afbed8d06ae0b6506a50.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/28cfd536743d4a83713ec2dd25bdb6fa.jpg)
![НОВЫЕ МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ПРИРОДНОЕ 3,7-ДИАЗАБИЦИКЛО[3.3.1]НОНАНОВОЕ ЯДРО И СПОСОБ ИХ ПОЛУЧЕНИЯ](https://fips.edrid.ru/images/rid/43/d3/95/c4c6b31c419c66c52cc5bcbe6a133a97.jpg)

